нано-Лекция 3.ppt
- Количество слайдов: 114
 Методы получения вещества в высокодисперсном состоянии
Методы получения вещества в высокодисперсном состоянии
 Ключевые вопросы ¢ ¢ ¢ ¢ ¢ Классификация методов Обзор наиболее распространенных химических методов синтеза твердофазных материалов Криохимический синтез Химическое восстановление в жидкой фазе Синтез в гетерофазных системах Радиационно-химические методы Золь-гель-метод Принципы получения монодисперсных частиц Управление размерами и формой наночастиц
Ключевые вопросы ¢ ¢ ¢ ¢ ¢ Классификация методов Обзор наиболее распространенных химических методов синтеза твердофазных материалов Криохимический синтез Химическое восстановление в жидкой фазе Синтез в гетерофазных системах Радиационно-химические методы Золь-гель-метод Принципы получения монодисперсных частиц Управление размерами и формой наночастиц
 Две группы методов ¢ Методы, позволяющие получать и изучать наночастицы, но на основе которых трудно создать новые материалы (конденсация при сверхнизких температурах, некоторые варианты химического, фотохимического и радиационного восстановления, лазерное испарение). ¢ Методы, позволяющие на основе наночастиц получать нанокомпозиты и наноматериалы (различные варианты механохимического дробления, конденсация из газовой фазы, плазмохимические методы и некоторые другие).
Две группы методов ¢ Методы, позволяющие получать и изучать наночастицы, но на основе которых трудно создать новые материалы (конденсация при сверхнизких температурах, некоторые варианты химического, фотохимического и радиационного восстановления, лазерное испарение). ¢ Методы, позволяющие на основе наночастиц получать нанокомпозиты и наноматериалы (различные варианты механохимического дробления, конденсация из газовой фазы, плазмохимические методы и некоторые другие).
 Снизу вверх и сверху вниз
Снизу вверх и сверху вниз
 Наиболее распространенные в настоящее время методы синтеза твердофазных материалов
Наиболее распространенные в настоящее время методы синтеза твердофазных материалов
 Прямая реакция ¢ Прекурсоры в растворенном виде смешивают в точном молярном соотношении, чтобы получить желаемый твердый продукт со строгой стехиометрией ¢ Y(NO 3)3 (aq)+ Gd(NO 3)3 (aq) + Fe. Cl 3 (aq) + Na. OH (aq) → →Yx. Gd 3 -x Fe 5 O 12 (s). ¢
Прямая реакция ¢ Прекурсоры в растворенном виде смешивают в точном молярном соотношении, чтобы получить желаемый твердый продукт со строгой стехиометрией ¢ Y(NO 3)3 (aq)+ Gd(NO 3)3 (aq) + Fe. Cl 3 (aq) + Na. OH (aq) → →Yx. Gd 3 -x Fe 5 O 12 (s). ¢
 Реакции одного прекурсора (однопрекурсорные реации, в англоязычной литературе one-pot methods) ¢ Прекурсор содержит все компоненты желаемого продукта в необходимой пропорции и степени окисления, при его разложении получают желаемый продукт ¢ Ba[Ti. O(C 2 O 4)2] (s)→Ba. Ti. O 3 (s) + 2 CO(g)+2 CO 2 (g).
Реакции одного прекурсора (однопрекурсорные реации, в англоязычной литературе one-pot methods) ¢ Прекурсор содержит все компоненты желаемого продукта в необходимой пропорции и степени окисления, при его разложении получают желаемый продукт ¢ Ba[Ti. O(C 2 O 4)2] (s)→Ba. Ti. O 3 (s) + 2 CO(g)+2 CO 2 (g).
 Быстрый твердофазный обмен ¢ ¢ Быстрая экзотермическая реакция между твердыми прекурсорами, движущей силой которой является высокая теплота образования одного из продуктов, инициирует самопроизвольно распространяющийся процесс обмена ионами с образованием желаемого продукта. 2 Mo. Cl (s) +5 Na 2 S (s)→ 2 Mo. S 2+10 Na. Cl (s) + S (s)
Быстрый твердофазный обмен ¢ ¢ Быстрая экзотермическая реакция между твердыми прекурсорами, движущей силой которой является высокая теплота образования одного из продуктов, инициирует самопроизвольно распространяющийся процесс обмена ионами с образованием желаемого продукта. 2 Mo. Cl (s) +5 Na 2 S (s)→ 2 Mo. S 2+10 Na. Cl (s) + S (s)
 Самораспространяющийся высокотемпературный синтез ¢ Заключается в инициировании экзотермической реакции в заранее приготовленной смеси металла с углеродом, кремнием, бором и другими неметаллами. Начавшаяся реакция самопроизвольно поддерживается и распространяется за счет выделения теплоты. Так можно получать порошки тугоплавких карбидов, силицидов, боридов и даже готовые изделия из них (резцы, стержни, кольца), не требующие дополнительной обработки.
Самораспространяющийся высокотемпературный синтез ¢ Заключается в инициировании экзотермической реакции в заранее приготовленной смеси металла с углеродом, кремнием, бором и другими неметаллами. Начавшаяся реакция самопроизвольно поддерживается и распространяется за счет выделения теплоты. Так можно получать порошки тугоплавких карбидов, силицидов, боридов и даже готовые изделия из них (резцы, стержни, кольца), не требующие дополнительной обработки.
 Транспортные реакции в газовой фазе ¢ ¢ ¢ В присутствии транспортного газа малоактивный прекурсор превращается в высоко активное соединение, реакция которого со вторым прекурсором и приводит к образованию желаемого продукта Cr 2 O 3 (s) + 3/2 O 2 (g)→ 2 Cr. O 3(g) +Ni. O (s) + H 2(g)→Ni. Cr 2 O 4 (s) + 3/2 O 2 (g)
Транспортные реакции в газовой фазе ¢ ¢ ¢ В присутствии транспортного газа малоактивный прекурсор превращается в высоко активное соединение, реакция которого со вторым прекурсором и приводит к образованию желаемого продукта Cr 2 O 3 (s) + 3/2 O 2 (g)→ 2 Cr. O 3(g) +Ni. O (s) + H 2(g)→Ni. Cr 2 O 4 (s) + 3/2 O 2 (g)
 Химическое осаждение из паровой фазы ¢ ¢ Пары прекурсоров осаждаются на нагретой подложке и реагируют с образованием желаемого продукта, побочные летучие продукты удаляются за счет связывания с газом-носителем. Me 3 Ga(g) +As. H 3 (g) +H 2 (g)→Ga. As (s) + CH 4(g)
Химическое осаждение из паровой фазы ¢ ¢ Пары прекурсоров осаждаются на нагретой подложке и реагируют с образованием желаемого продукта, побочные летучие продукты удаляются за счет связывания с газом-носителем. Me 3 Ga(g) +As. H 3 (g) +H 2 (g)→Ga. As (s) + CH 4(g)
 Ионный обмен ¢ Na 1+x. Al 11 O 17+x/2 (s) +y. Nd. Cl 3 (l)→Na 1+x-3 y. Ndy. Al 11+x/2 (s) +3 y. Na. Cl (s) ¢ Противоионы натрия, которые покрывают проводящую плоскость дефектной шпинели β-Al 2 O 3, замещаются катионами неодима (три катиона натрия на каждый трехзарядный катион неодима) при погружении шпинели в стехиометрический расплав Nd. Cl 3 в Na. Cl.
Ионный обмен ¢ Na 1+x. Al 11 O 17+x/2 (s) +y. Nd. Cl 3 (l)→Na 1+x-3 y. Ndy. Al 11+x/2 (s) +3 y. Na. Cl (s) ¢ Противоионы натрия, которые покрывают проводящую плоскость дефектной шпинели β-Al 2 O 3, замещаются катионами неодима (три катиона натрия на каждый трехзарядный катион неодима) при погружении шпинели в стехиометрический расплав Nd. Cl 3 в Na. Cl.
 Интеркаляция ¢ Ti. S 2 (s) +x(C 4 H 9)Li (l)→Lix. Ti. S 2 (s) +C 8 H 18 (l) ¢ Стехиометрическая реакция раствора бутил-лития в ТГФ с жидким дисульфидом титана приводит к включению ионов лития в ван-дер. Ваальсовы щели между слоями Ti. S 2 и переходу электронов в зону проводимости дисульфида титана.
Интеркаляция ¢ Ti. S 2 (s) +x(C 4 H 9)Li (l)→Lix. Ti. S 2 (s) +C 8 H 18 (l) ¢ Стехиометрическая реакция раствора бутил-лития в ТГФ с жидким дисульфидом титана приводит к включению ионов лития в ван-дер. Ваальсовы щели между слоями Ti. S 2 и переходу электронов в зону проводимости дисульфида титана.
 Взаимодействие “гостьхозяин” (в англоязычной литературе “host-guest”) ¢ Реакции жидких или твердых прекурсоров в полостях цеолитов с участием групп на поверхности этих полостей с последующей агломерацией продуктов реакции с решеткой цеолита. Si 2 H 6(g) +H 56 Y(s)→( Si 2 H 5)8 Y(s) ¢ ( Si 2 H 5)8 Y(s) →( Si 8)8 Y(s) ¢
Взаимодействие “гостьхозяин” (в англоязычной литературе “host-guest”) ¢ Реакции жидких или твердых прекурсоров в полостях цеолитов с участием групп на поверхности этих полостей с последующей агломерацией продуктов реакции с решеткой цеолита. Si 2 H 6(g) +H 56 Y(s)→( Si 2 H 5)8 Y(s) ¢ ( Si 2 H 5)8 Y(s) →( Si 8)8 Y(s) ¢
 Золь-гель-химия ¢ ¢ ¢ (2 -n)In(OBu)3 (l)+n. Sn(OBu)4 (l)+H 2 O (l)→ Snn In 2 -n O 3 + Bu. OH Гидролитическая поликонденсация в стехиометрической смеси трибутоксииндия(III) и тетрабутоксиолова(IV) в соотношении 1: 10, с последующей термической обработкой образовавшегося геля, дает р-допированный оксид индия-олова (ITO).
Золь-гель-химия ¢ ¢ ¢ (2 -n)In(OBu)3 (l)+n. Sn(OBu)4 (l)+H 2 O (l)→ Snn In 2 -n O 3 + Bu. OH Гидролитическая поликонденсация в стехиометрической смеси трибутоксииндия(III) и тетрабутоксиолова(IV) в соотношении 1: 10, с последующей термической обработкой образовавшегося геля, дает р-допированный оксид индия-олова (ITO).
 Chemie douce ¢ Буквальный перевод этого французского термина – мягкая химия. В основе метода лежит превращение определенных соединений в комплексы сложного строения, которые затем переводятся в гелевую форму и после термического разложения образуют снова исходные соединения, но уже в иной кристаллической форме K 2 O (s) +4 Ti. O 2 (рутил)→K 2 Ti 4 O 9 (s) ¢ K 2 Ti 4 O 9 (s) +HNO 3 (l)→H 2 Ti 4 O 9∙H 2 O (гель) ¢ H 2 Ti 4 O 9∙H 2 O(гель)→ 4 Ti. O 2 (полиморф) +2 H 2 O ¢
Chemie douce ¢ Буквальный перевод этого французского термина – мягкая химия. В основе метода лежит превращение определенных соединений в комплексы сложного строения, которые затем переводятся в гелевую форму и после термического разложения образуют снова исходные соединения, но уже в иной кристаллической форме K 2 O (s) +4 Ti. O 2 (рутил)→K 2 Ti 4 O 9 (s) ¢ K 2 Ti 4 O 9 (s) +HNO 3 (l)→H 2 Ti 4 O 9∙H 2 O (гель) ¢ H 2 Ti 4 O 9∙H 2 O(гель)→ 4 Ti. O 2 (полиморф) +2 H 2 O ¢
 Электрохимический синтез ¢ 2 Al (s) +3 H 3 PO 4 (l) → Al 2 O 3 (s) + 3 H 3 PO 3 (l) ¢ Электрохимическое окисление алюминиевого анода в электролите на основе концентрированной фосфорной кислоты с использованием платинового рабочего электрода включает образование иона Al 3+ с одновременным восстановлением фосфат-ионов до фосфит-ионов и образованием ионов О 2 -. Эти ионы реагируют с ионами алюминия с образованием слоя оксида алюминия на поверхности алюминия.
Электрохимический синтез ¢ 2 Al (s) +3 H 3 PO 4 (l) → Al 2 O 3 (s) + 3 H 3 PO 3 (l) ¢ Электрохимическое окисление алюминиевого анода в электролите на основе концентрированной фосфорной кислоты с использованием платинового рабочего электрода включает образование иона Al 3+ с одновременным восстановлением фосфат-ионов до фосфит-ионов и образованием ионов О 2 -. Эти ионы реагируют с ионами алюминия с образованием слоя оксида алюминия на поверхности алюминия.
 Гидротермальный процесс ¢ ¢ ¢ Na. Al(OH)4 (aq) +Na. Si. O 3 (aq) +x. Na. OH (aq) → Nax(Al. O 2)x(Si. O 2)y∙z. H 2 O (s) Водные растворы прекурсоров подвергаются гидротермальной поликонденсации, в результате чего образуется гель, кристаллизующийся затем в микропористый цеолит, в поры которого включается вода
Гидротермальный процесс ¢ ¢ ¢ Na. Al(OH)4 (aq) +Na. Si. O 3 (aq) +x. Na. OH (aq) → Nax(Al. O 2)x(Si. O 2)y∙z. H 2 O (s) Водные растворы прекурсоров подвергаются гидротермальной поликонденсации, в результате чего образуется гель, кристаллизующийся затем в микропористый цеолит, в поры которого включается вода
 Химия высоких давлений и температур ¢ ¢ С 60 (s)→C(алмаз) Под давлением 20 ГПа в реакторе для синтеза алмазов фуллерен быстро превращается в кристаллический алмаз. Процессу благоприятствует промежуточное между графитом и алмазом sp 2 -3 гибридное состояние углерода в фуллерене.
Химия высоких давлений и температур ¢ ¢ С 60 (s)→C(алмаз) Под давлением 20 ГПа в реакторе для синтеза алмазов фуллерен быстро превращается в кристаллический алмаз. Процессу благоприятствует промежуточное между графитом и алмазом sp 2 -3 гибридное состояние углерода в фуллерене.
 Криохимический синтез ¢ Пары металла (обычно используют лазерное испарение) конденсируют с большим, избытком инертного газа на поверхность, охлаждённую до 4 -12 К. Наиболее широко в качестве матриц используют аргон и ксенон. Сильное разбавление инертным газом и низкие температуры исключают возможность диффузии атомов металлов, и в конденсатах происходит их стабилизация.
Криохимический синтез ¢ Пары металла (обычно используют лазерное испарение) конденсируют с большим, избытком инертного газа на поверхность, охлаждённую до 4 -12 К. Наиболее широко в качестве матриц используют аргон и ксенон. Сильное разбавление инертным газом и низкие температуры исключают возможность диффузии атомов металлов, и в конденсатах происходит их стабилизация.
 Факторы, влияющие на формирование частиц в процессе криоконденсации ¢ скорость достижения атомами охлаждённой поверхности; ¢ скорость потери атомами избыточной энергии через взаимодействие с конденсатом; ¢ скорость удаления кластеров из области повышенной концентрации атомов.
Факторы, влияющие на формирование частиц в процессе криоконденсации ¢ скорость достижения атомами охлаждённой поверхности; ¢ скорость потери атомами избыточной энергии через взаимодействие с конденсатом; ¢ скорость удаления кластеров из области повышенной концентрации атомов.
 Схема химических превращений в низкотемпературных конденсатах ¢ Направление (1) соответствует образованию кластеров металла, направление (2) – продуктов взаимодействия металла и лигандов
Схема химических превращений в низкотемпературных конденсатах ¢ Направление (1) соответствует образованию кластеров металла, направление (2) – продуктов взаимодействия металла и лигандов
 Химические методы получения наночастиц ¢ осаждение ¢ восстановление оксидов и других соединений до металлов ¢ термическое разложение и др.
Химические методы получения наночастиц ¢ осаждение ¢ восстановление оксидов и других соединений до металлов ¢ термическое разложение и др.
 Химические методы получения наночастиц ¢ Основное условие – проведение этих процессов вдали от равновесия и высокая скорость образования зародышей твердой фазы (нуклеации) в сочетании с малой скоростью роста частиц.
Химические методы получения наночастиц ¢ Основное условие – проведение этих процессов вдали от равновесия и высокая скорость образования зародышей твердой фазы (нуклеации) в сочетании с малой скоростью роста частиц.
 Химическое восстановление в жидкой фазе ¢ продукты реакций – ограничено растворимые вещества;
Химическое восстановление в жидкой фазе ¢ продукты реакций – ограничено растворимые вещества;
 Химическое восстановление в жидкой фазе ¢ ключевая роль процесса нуклеации с одновременным образованием большого числа очень малых зародышевых частиц;
Химическое восстановление в жидкой фазе ¢ ключевая роль процесса нуклеации с одновременным образованием большого числа очень малых зародышевых частиц;
 Химическое восстановление в жидкой фазе ¢ заметное влияние вторичных процессов (Оствальдовское созревание) на размер, морфологию и свойства продуктов;
Химическое восстановление в жидкой фазе ¢ заметное влияние вторичных процессов (Оствальдовское созревание) на размер, морфологию и свойства продуктов;
 Химическое восстановление в жидкой фазе ¢ условия пересыщения, необходимые для начала осаждения, являются результатом химической реакции, поэтому все факторы, влияющие на протекание суммарного процесса (скорость добавления реагентов, скорость перемешивания и т. п. ) могут заметно влиять на размер и монодисперсность частиц.
Химическое восстановление в жидкой фазе ¢ условия пересыщения, необходимые для начала осаждения, являются результатом химической реакции, поэтому все факторы, влияющие на протекание суммарного процесса (скорость добавления реагентов, скорость перемешивания и т. п. ) могут заметно влиять на размер и монодисперсность частиц.
 Типичные реагенты в реакциях химического восстановления из растворов ¢ Прекурсоры – соли или комплексные соединения металлов.
Типичные реагенты в реакциях химического восстановления из растворов ¢ Прекурсоры – соли или комплексные соединения металлов.
 Типичные реагенты в реакциях химического восстановления из растворов ¢ Восстановители – водород, борогидриды щелочных металлов, гидразин гидрат или гидразин хлорид, алюмогидриды, гипофосфиты, соли лимонной, щавелевой и винной кислот.
Типичные реагенты в реакциях химического восстановления из растворов ¢ Восстановители – водород, борогидриды щелочных металлов, гидразин гидрат или гидразин хлорид, алюмогидриды, гипофосфиты, соли лимонной, щавелевой и винной кислот.
 Типичные реагенты в реакциях химического восстановления из растворов ¢ Восстановители-стабилизаторы N–S–содержащие ПАВ, тиолы, нитратные соли, органические анионы, полимеры с функциональными группами. –
Типичные реагенты в реакциях химического восстановления из растворов ¢ Восстановители-стабилизаторы N–S–содержащие ПАВ, тиолы, нитратные соли, органические анионы, полимеры с функциональными группами. –
 Типичная реакция восстановления катиона переходного металла Men+ + nē → Me 0, которой соответствует реакция окисления некоторого вещества Х: Xm − nē → Xm-n
Типичная реакция восстановления катиона переходного металла Men+ + nē → Me 0, которой соответствует реакция окисления некоторого вещества Х: Xm − nē → Xm-n
 ∆E = E – E(redox) ¢E – равновесный окислительновосстановительный потенциал частицы, ¢ E redox – соответствующий потенциал раствора ¢ ∆E > 0 –рост частиц, ¢ ∆E < 0 – растворение ¢ ∆E=0 – состояние неустойчивого равновесия
∆E = E – E(redox) ¢E – равновесный окислительновосстановительный потенциал частицы, ¢ E redox – соответствующий потенциал раствора ¢ ∆E > 0 –рост частиц, ¢ ∆E < 0 – растворение ¢ ∆E=0 – состояние неустойчивого равновесия
 Электрохимическая реакция для ионов BH 4− B(OH)3 + 7 H+ + 8ē → BH 4− + 3 H 2 O E= − 0. 48 В
Электрохимическая реакция для ионов BH 4− B(OH)3 + 7 H+ + 8ē → BH 4− + 3 H 2 O E= − 0. 48 В
 Продукты восстановления боргидридом катионов различных металлов ¢ металл (Ag, Hg, Au, Pt, Rh, Os) ¢ борид металла (Co, Ni, Fe) ¢ смесь металла и его гидрида (Cu).
Продукты восстановления боргидридом катионов различных металлов ¢ металл (Ag, Hg, Au, Pt, Rh, Os) ¢ борид металла (Co, Ni, Fe) ¢ смесь металла и его гидрида (Cu).
 Преимущества тетрагидроборатов как восстановителей ¢ высокая скорость восстановления ¢ хорошая растворимость в воде и неводных растворителях ¢ возможность получения большого числа металлов, в том числе всех благородных.
Преимущества тетрагидроборатов как восстановителей ¢ высокая скорость восстановления ¢ хорошая растворимость в воде и неводных растворителях ¢ возможность получения большого числа металлов, в том числе всех благородных.
 Недостаток тетрагидроборатов как восстановителей ¢ Не всегда можно использовать для получения чистых металлов, так как могут образоваться бориды или гидриды металлов.
Недостаток тетрагидроборатов как восстановителей ¢ Не всегда можно использовать для получения чистых металлов, так как могут образоваться бориды или гидриды металлов.
 Электрохимическая реакция для гидразина N 2 + 5 H+ + 4ē → N 2 H 5+ E= − 0. 23 В
Электрохимическая реакция для гидразина N 2 + 5 H+ + 4ē → N 2 H 5+ E= − 0. 23 В
 Наиболее изученная реакция восстановления 2 Au. Cl 4− + 2 H 2→ 2 Au + 6 H+ + 8 Cl− Е=1. 002 В
Наиболее изученная реакция восстановления 2 Au. Cl 4− + 2 H 2→ 2 Au + 6 H+ + 8 Cl− Е=1. 002 В
 Условия проведения реакций восстановления из раствора ¢ максимально возможная концентрация восстановителя ¢ повышенная температура ¢ дезаэрирование растворов инертным газом
Условия проведения реакций восстановления из раствора ¢ максимально возможная концентрация восстановителя ¢ повышенная температура ¢ дезаэрирование растворов инертным газом
 Принципы стабилизации наночастиц ¢ электростатическое отталкивание в результате хемосорбции заряженных частиц (OH−, H+, цитрат-ионов и др. );
Принципы стабилизации наночастиц ¢ электростатическое отталкивание в результате хемосорбции заряженных частиц (OH−, H+, цитрат-ионов и др. );

 Принципы стабилизации наночастиц ¢ стерическое отталкивание между частицами за счет присоединения к их поверхности катионных ПАВ, природных или синтетических полимеров (желатина, крахмала, поливинилового спирта, поливинилпирролидона), высокомолекулярных органических кислот, лигандов π-акцепторного типа (пиридина, фосфинов и др. ).
Принципы стабилизации наночастиц ¢ стерическое отталкивание между частицами за счет присоединения к их поверхности катионных ПАВ, природных или синтетических полимеров (желатина, крахмала, поливинилового спирта, поливинилпирролидона), высокомолекулярных органических кислот, лигандов π-акцепторного типа (пиридина, фосфинов и др. ).
 Функции стабилизаторов увеличивают агрегатную устойчивость системы, ¢ подавляют высокую реакционную способность наночастиц по отношению к кислороду и другим потенциальным окислителям, ¢ снижают высокий восстановительный потенциал наночастиц. ¢
Функции стабилизаторов увеличивают агрегатную устойчивость системы, ¢ подавляют высокую реакционную способность наночастиц по отношению к кислороду и другим потенциальным окислителям, ¢ снижают высокий восстановительный потенциал наночастиц. ¢
 Осаждение оксидов из водных растворов ¢ реакции, в которых оксид осаждается сразу; ¢ реакции, продукты которых являются прекурсорами для получения оксида.
Осаждение оксидов из водных растворов ¢ реакции, в которых оксид осаждается сразу; ¢ реакции, продукты которых являются прекурсорами для получения оксида.
 Общепринятый способ получения кристаллических наноструктурированных оксидов ¢ термическое разложение совместно осажденных гидроксидов, карбонатов, бикарбонатов и оксалатов металлов, которые разлагаются при не очень высоких (<400ºС) температурах, когда тенденция к агломерации менее выражена.
Общепринятый способ получения кристаллических наноструктурированных оксидов ¢ термическое разложение совместно осажденных гидроксидов, карбонатов, бикарбонатов и оксалатов металлов, которые разлагаются при не очень высоких (<400ºС) температурах, когда тенденция к агломерации менее выражена.
 Синтез в гетерофазных системах
Синтез в гетерофазных системах
 Микроэмульсии ¢ термодинамически стабильные изотропные дисперсии двух несмешивающихся жидкостей, состоят из воды, масла ( под этим термином понимается неполярный органический растворитель), ПАВ и спирта или амина. Могут быть прямыми – масло в воде (м/в) или обратными – вода в масле (в/м).
Микроэмульсии ¢ термодинамически стабильные изотропные дисперсии двух несмешивающихся жидкостей, состоят из воды, масла ( под этим термином понимается неполярный органический растворитель), ПАВ и спирта или амина. Могут быть прямыми – масло в воде (м/в) или обратными – вода в масле (в/м).
 Схема упаковки конусообразных единиц в мицеллы с различной кривизной поверхности
Схема упаковки конусообразных единиц в мицеллы с различной кривизной поверхности
 Наиболее широко используемые ПАВ ¢ цетилтриметиламмоний бромид (СТАВ) ¢ диэтилгексилсульфосукцинат натрия (Aerosolе OT или АОТ)
Наиболее широко используемые ПАВ ¢ цетилтриметиламмоний бромид (СТАВ) ¢ диэтилгексилсульфосукцинат натрия (Aerosolе OT или АОТ)
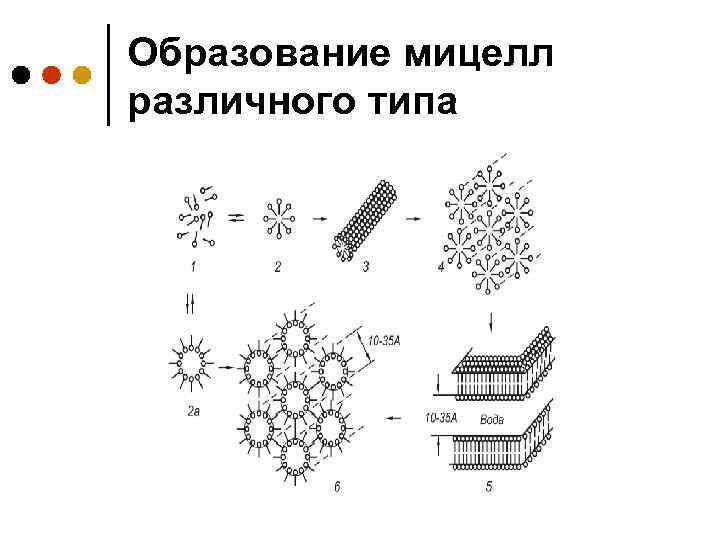 Образование мицелл различного типа
Образование мицелл различного типа
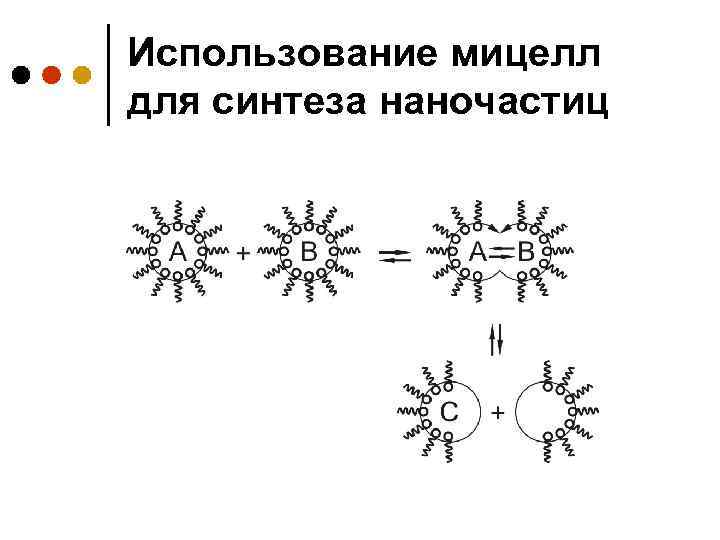 Использование мицелл для синтеза наночастиц
Использование мицелл для синтеза наночастиц
 Межфазный синтез ¢ Сущность – взаимодействие реагентов, растворенных в различных фазах двухфазной системы. В отличие от синтеза в микроэмульсиях, в межфазном синтезе не допускается перемешивание фаз, и реакция начинается, на границе их раздела. Продукты реакции также локализуется на межфазной границе или в одной из несмешивающихся фаз.
Межфазный синтез ¢ Сущность – взаимодействие реагентов, растворенных в различных фазах двухфазной системы. В отличие от синтеза в микроэмульсиях, в межфазном синтезе не допускается перемешивание фаз, и реакция начинается, на границе их раздела. Продукты реакции также локализуется на межфазной границе или в одной из несмешивающихся фаз.
 Дендримеры высокоразветвленные макромолекулы, образованные последовательным присоединением полифункциональных мономеров по периферии заданного ядра; ¢ имеют высокую молекулярную массу и низкую вязкость растворов, объемную форму и пространственную структуру, напоминающую ветвящуюся крону дерева; ¢ размер их составляет от 2 до 15 нм ¢
Дендримеры высокоразветвленные макромолекулы, образованные последовательным присоединением полифункциональных мономеров по периферии заданного ядра; ¢ имеют высокую молекулярную массу и низкую вязкость растворов, объемную форму и пространственную структуру, напоминающую ветвящуюся крону дерева; ¢ размер их составляет от 2 до 15 нм ¢
 Строение дендримеров и их использование в синтезе наночастиц
Строение дендримеров и их использование в синтезе наночастиц
 Типы строения гибридных нанокомпозитов с дендримерами
Типы строения гибридных нанокомпозитов с дендримерами
 Синтез в пористых наноструктурах ¢ прямая адсорбция паров металла в тщательно обезвоженных порах цеолитов; ¢ химическое превращение введенных в поры прекурсоров в виде солей металла, металлокомплексных и металлорганических соединений.
Синтез в пористых наноструктурах ¢ прямая адсорбция паров металла в тщательно обезвоженных порах цеолитов; ¢ химическое превращение введенных в поры прекурсоров в виде солей металла, металлокомплексных и металлорганических соединений.
 Радиационно-химические методы ¢ γ-радиолиз ¢ фотолиз ¢ облучение высокоэнергетическим потоком быстрых электронов
Радиационно-химические методы ¢ γ-радиолиз ¢ фотолиз ¢ облучение высокоэнергетическим потоком быстрых электронов
 Генерация в реакционной среде сильных восстановителей γ-изл. ¢ H 2 O → OH˙, ēaqu, H 2 O 2, H˙, H 2. ¢ сольватированные электроны, атомы водорода, органические и неорганические радикалы ¢
Генерация в реакционной среде сильных восстановителей γ-изл. ¢ H 2 O → OH˙, ēaqu, H 2 O 2, H˙, H 2. ¢ сольватированные электроны, атомы водорода, органические и неорганические радикалы ¢
 Захват радикалов спиртами с короткой цепью OH˙ + СH 3 OH → H 2 O + C˙H 2 OH H˙ + СH 3 OH → H 2 + C˙H 2 OH
Захват радикалов спиртами с короткой цепью OH˙ + СH 3 OH → H 2 O + C˙H 2 OH H˙ + СH 3 OH → H 2 + C˙H 2 OH
 Восстановление иона металла Mn+ + n C˙H 2 OH → M 0 + n. CH 2 O + n. H+
Восстановление иона металла Mn+ + n C˙H 2 OH → M 0 + n. CH 2 O + n. H+
 Достоинства радиационнохимических методов ¢ хорошая воспроизводимость получения наночастиц в широком диапазоне температур и в различных средах, включая твердые (пленки полимеров, объем стекла)
Достоинства радиационнохимических методов ¢ хорошая воспроизводимость получения наночастиц в широком диапазоне температур и в различных средах, включая твердые (пленки полимеров, объем стекла)
 Достоинства радиационнохимических методов ¢ возможность избежать нежелательных примесей (продуктов разложения восстановителей), что характерно для частиц, полученных химическим путем
Достоинства радиационнохимических методов ¢ возможность избежать нежелательных примесей (продуктов разложения восстановителей), что характерно для частиц, полученных химическим путем
 Достоинства радиационнохимических методов ¢ особенно полезны, когда нужно получить достаточно большие частицы или наслоить один металл на другой
Достоинства радиационнохимических методов ¢ особенно полезны, когда нужно получить достаточно большие частицы или наслоить один металл на другой
 Условия проведения радиационно-химических процессов ¢ среда – водная или водно-спиртовая; ¢ прекурсоры – комплексы металлов с различными лигандами; ¢ стабилизаторы – полифосфаты, полиакриловая кислота, поливиниловый спирт, поливинилацетат и др.
Условия проведения радиационно-химических процессов ¢ среда – водная или водно-спиртовая; ¢ прекурсоры – комплексы металлов с различными лигандами; ¢ стабилизаторы – полифосфаты, полиакриловая кислота, поливиниловый спирт, поливинилацетат и др.
 Фотохимический метод (фотолиз) ¢ Суть заключается в возбуждении квантами света одноэлектронных переходов типа металл-лиганд, вызывающих образование нестабильных низковалентных форм (Pt 3+, Pt+, Rh 2+, Rh+, Au 2+, Pd+, Co+) или атомов металла (Ag 0, Au 0).
Фотохимический метод (фотолиз) ¢ Суть заключается в возбуждении квантами света одноэлектронных переходов типа металл-лиганд, вызывающих образование нестабильных низковалентных форм (Pt 3+, Pt+, Rh 2+, Rh+, Au 2+, Pd+, Co+) или атомов металла (Ag 0, Au 0).
 Отличие фотохимического метода ¢ от γ-радиолиза и рентгеновского излучения – не приводит к глубоким структурным изменениям применяемых реагентов и материалов ¢ от химических методов – позволяет лучше контролировать ход процесса во времени и в пространстве, что важно для получения структур с заданной топологией
Отличие фотохимического метода ¢ от γ-радиолиза и рентгеновского излучения – не приводит к глубоким структурным изменениям применяемых реагентов и материалов ¢ от химических методов – позволяет лучше контролировать ход процесса во времени и в пространстве, что важно для получения структур с заданной топологией
 Микроволновая обработка ¢ Приводит к быстрому разогреву реакционной смеси, в частности, содержащей воду, в результате чего происходит быстрое и практически одновременное осаждение наночастиц из растворов.
Микроволновая обработка ¢ Приводит к быстрому разогреву реакционной смеси, в частности, содержащей воду, в результате чего происходит быстрое и практически одновременное осаждение наночастиц из растворов.
 Микроволновая обработка ¢ Преимущества – очень малый размер частиц, узкое распределение по размерам, очень короткое время реакции.
Микроволновая обработка ¢ Преимущества – очень малый размер частиц, узкое распределение по размерам, очень короткое время реакции.
 Микроволновая обработка ¢ Можно получать наночастицы металлов (микроволновой полиолпроцесс) и халькогениды Cd. Se, Pb. Se, Cu 2−x. Se.
Микроволновая обработка ¢ Можно получать наночастицы металлов (микроволновой полиолпроцесс) и халькогениды Cd. Se, Pb. Se, Cu 2−x. Se.
 Ультразвуковая обработка ¢ Происходит кавитация (взрывное схлопывание пузырьков), что создает локализованные “горячие точки” с эффективной температурой в несколько тысяч кельвинов и временем жизни несколько наносекунд.
Ультразвуковая обработка ¢ Происходит кавитация (взрывное схлопывание пузырьков), что создает локализованные “горячие точки” с эффективной температурой в несколько тысяч кельвинов и временем жизни несколько наносекунд.
 Ультразвуковая обработка ¢ Химическая реакция в основном происходит внутри пузырьков. Очень высокая скорость охлаждения способствует образованию аморфных продуктов.
Ультразвуковая обработка ¢ Химическая реакция в основном происходит внутри пузырьков. Очень высокая скорость охлаждения способствует образованию аморфных продуктов.
 Золь-гель (гель-золь) метод ¢ ¢ ¢ получение коллоидных растворов гидроксидов металлов (чаще всего путем гидролиза их солей или алкоксидов): M(OR)n+x. H 2 O→M(OH)x(OR)n-x+ROH (золь) последующая термическая дегидратация или конденсация золя: M(OH)x(OR)n-x→n/2 MO+(2 x-n)/2 H 2 O+(n-x) ROH (гель) (M – металл, R – алкильная группа)
Золь-гель (гель-золь) метод ¢ ¢ ¢ получение коллоидных растворов гидроксидов металлов (чаще всего путем гидролиза их солей или алкоксидов): M(OR)n+x. H 2 O→M(OH)x(OR)n-x+ROH (золь) последующая термическая дегидратация или конденсация золя: M(OH)x(OR)n-x→n/2 MO+(2 x-n)/2 H 2 O+(n-x) ROH (гель) (M – металл, R – алкильная группа)
 Основные стадии зольгель процесса ¢ 1. Формирование стабильных растворов прекурсоров (золей).
Основные стадии зольгель процесса ¢ 1. Формирование стабильных растворов прекурсоров (золей).
 Основные стадии зольгель процесса ¢ 2. Гелеобразование в результате образования сети оловых или оксоловых связей путем поликонденсации или полиэтерификации, что приводит к заметному увеличению вязкости раствора.
Основные стадии зольгель процесса ¢ 2. Гелеобразование в результате образования сети оловых или оксоловых связей путем поликонденсации или полиэтерификации, что приводит к заметному увеличению вязкости раствора.
 Основные стадии зольгель процесса ¢ 3. Старение геля (синерезис), реакции поликонденсации продолжаются до тех пор, пока гель не перейдет в твердую массу, происходит укрепление сетки геля и удаление растворителя из его пор. Процесс старения может длиться около недели.
Основные стадии зольгель процесса ¢ 3. Старение геля (синерезис), реакции поликонденсации продолжаются до тех пор, пока гель не перейдет в твердую массу, происходит укрепление сетки геля и удаление растворителя из его пор. Процесс старения может длиться около недели.
 Основные стадии зольгель процесса ¢ 4. Высушивание, вода и другие летучие жидкости удаляются из сетки геля. Если происходит термическое удаление паров, полученный монолит называют ксерогелем. Если растворитель удаляют при критических или сверхкритических условиях, продукт называют аэрогелем.
Основные стадии зольгель процесса ¢ 4. Высушивание, вода и другие летучие жидкости удаляются из сетки геля. Если происходит термическое удаление паров, полученный монолит называют ксерогелем. Если растворитель удаляют при критических или сверхкритических условиях, продукт называют аэрогелем.
 Основные стадии зольгель процесса ¢ 5. Дегидратация, удаляются поверхностно связанные ОНгруппы. Обычно при температуре до 800ºС.
Основные стадии зольгель процесса ¢ 5. Дегидратация, удаляются поверхностно связанные ОНгруппы. Обычно при температуре до 800ºС.
 Основные стадии зольгель процесса ¢ 6. Уплотнение и разложение геля при температуре выше 800ºС. Поры гелевой сетки закрываются, оставшиеся органические примеси улетают. Используется при получении плотных керамик или стекол.
Основные стадии зольгель процесса ¢ 6. Уплотнение и разложение геля при температуре выше 800ºС. Поры гелевой сетки закрываются, оставшиеся органические примеси улетают. Используется при получении плотных керамик или стекол.
 Гель-золь-метод ¢ ¢ Прекурсор – высоковязкий конденсированный гель, который служит матрицей для образования частиц продукта и одновременно резервуаром ионов металла и гидроксил-ионов. После того, как гель выполнил свою функцию, его удаляют подходящим способом. Если твердый прекурсор сам такой гель не образует, в него вводят лиофильные полимеры и ПАВ.
Гель-золь-метод ¢ ¢ Прекурсор – высоковязкий конденсированный гель, который служит матрицей для образования частиц продукта и одновременно резервуаром ионов металла и гидроксил-ионов. После того, как гель выполнил свою функцию, его удаляют подходящим способом. Если твердый прекурсор сам такой гель не образует, в него вводят лиофильные полимеры и ПАВ.
 Преимущества золь-гель (гель-золь) метода ¢ ¢ ¢ простые и быстрые реакции практически комнатной температуре; относительно чистые продукты, свободные от неорганических анионов; высокая производительность, обусловленная возможностью достижения в исходном материале верхнего предела концентраций для получения монодисперсных частиц.
Преимущества золь-гель (гель-золь) метода ¢ ¢ ¢ простые и быстрые реакции практически комнатной температуре; относительно чистые продукты, свободные от неорганических анионов; высокая производительность, обусловленная возможностью достижения в исходном материале верхнего предела концентраций для получения монодисперсных частиц.
 Метод Печини ¢ Основан на способности щелочных, щелочно-земельных и переходных металлов образовывать хелатные комплексы с би- и тридентатными лигандами (например, лимонной кислотой).
Метод Печини ¢ Основан на способности щелочных, щелочно-земельных и переходных металлов образовывать хелатные комплексы с би- и тридентатными лигандами (например, лимонной кислотой).
 Метод Печини ¢ При добавлении полиалкоголя (например, этиленгликоля) происходит гелеобразование за счет реакции полиэтерификации.
Метод Печини ¢ При добавлении полиалкоголя (например, этиленгликоля) происходит гелеобразование за счет реакции полиэтерификации.
 Метод Печини ¢ После высушивания гель подвергается термической обработке, происходит пиролиз органических компонентов и образуются агрегированные субмикронные частицы оксидов
Метод Печини ¢ После высушивания гель подвергается термической обработке, происходит пиролиз органических компонентов и образуются агрегированные субмикронные частицы оксидов
 Частицы диоксида кремния, полученные по методу Печини
Частицы диоксида кремния, полученные по методу Печини
 Монодисперсные частицы Имеют одинаковый размер, форму, внутреннюю структуру. Распределение по размерам очень узкое (коэффициент вариации не более 10%).
Монодисперсные частицы Имеют одинаковый размер, форму, внутреннюю структуру. Распределение по размерам очень узкое (коэффициент вариации не более 10%).
 Общие принципы синтеза монодисперсных частиц Разделение стадий нуклеации (зародышеобразования) и роста ¢ Ингибирование спонтанной коагуляции растущих частиц ¢ Наличие резервуара мономеров (то есть атомов, ионов или молекул, из которых будут состоять частицы) ¢
Общие принципы синтеза монодисперсных частиц Разделение стадий нуклеации (зародышеобразования) и роста ¢ Ингибирование спонтанной коагуляции растущих частиц ¢ Наличие резервуара мономеров (то есть атомов, ионов или молекул, из которых будут состоять частицы) ¢
 Приемы, способствующие разделению стадий нуклеации и роста ¢ ограничение скорости поступления мономеров. В открытых системах – регулирование скорости подачи реагентов, в закрытых – скорости высвобождения мономеров из данного резервуара (твердого или комплексного прекурсора) путем контроля р. Н и т. п.
Приемы, способствующие разделению стадий нуклеации и роста ¢ ограничение скорости поступления мономеров. В открытых системах – регулирование скорости подачи реагентов, в закрытых – скорости высвобождения мономеров из данного резервуара (твердого или комплексного прекурсора) путем контроля р. Н и т. п.
 Приемы, способствующие разделению стадий нуклеации и роста ¢ добавление растворителя или лиганда для твердой фазы прекурсора ¢ повышение температуры системы
Приемы, способствующие разделению стадий нуклеации и роста ¢ добавление растворителя или лиганда для твердой фазы прекурсора ¢ повышение температуры системы
 Приемы, способствующие разделению стадий нуклеации и роста ¢ подавление пересыщения за счет понижения р. Н, разбавления растворителем, добавления ускорителей роста, быстрого изменения температуры и т. п.
Приемы, способствующие разделению стадий нуклеации и роста ¢ подавление пересыщения за счет понижения р. Н, разбавления растворителем, добавления ускорителей роста, быстрого изменения температуры и т. п.
 Приемы, способствующие разделению стадий нуклеации и роста ¢ введение готовых зародышей в раствор мономера при низком уровне пересыщения (англ. seeding, от seed – семя, зерно)
Приемы, способствующие разделению стадий нуклеации и роста ¢ введение готовых зародышей в раствор мономера при низком уровне пересыщения (англ. seeding, от seed – семя, зерно)
 Приемы, способствующие разделению стадий нуклеации и роста ¢ Впрыскивание прекурсоров в растворитель при высокой температруре
Приемы, способствующие разделению стадий нуклеации и роста ¢ Впрыскивание прекурсоров в растворитель при высокой температруре
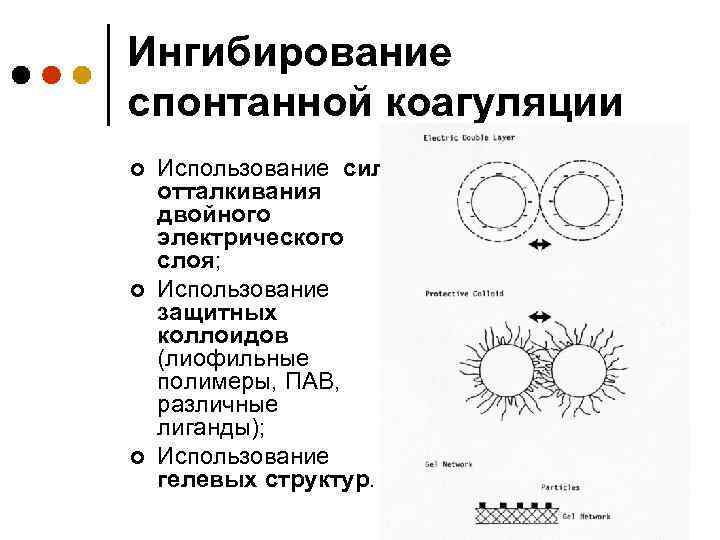 Ингибирование спонтанной коагуляции ¢ ¢ ¢ Использование сил отталкивания двойного электрического слоя; Использование защитных коллоидов (лиофильные полимеры, ПАВ, различные лиганды); Использование гелевых структур.
Ингибирование спонтанной коагуляции ¢ ¢ ¢ Использование сил отталкивания двойного электрического слоя; Использование защитных коллоидов (лиофильные полимеры, ПАВ, различные лиганды); Использование гелевых структур.
 Резервуары мономера ¢ Комплексы металлов с такими лигандами как этилендиаминтетраацетат (ЭДТА), нитрилуксусная кислота (НТА), лимонная кислота. ¢ Твердые прекурсоры
Резервуары мономера ¢ Комплексы металлов с такими лигандами как этилендиаминтетраацетат (ЭДТА), нитрилуксусная кислота (НТА), лимонная кислота. ¢ Твердые прекурсоры
 Другие приемы получения монодисперсных частиц ¢ использование двухструйной контролируемой подачи реагентов (double jet system), когда растворенное вещество поступает извне и его приток легко регулировать во времени
Другие приемы получения монодисперсных частиц ¢ использование двухструйной контролируемой подачи реагентов (double jet system), когда растворенное вещество поступает извне и его приток легко регулировать во времени
 Другие приемы получения монодисперсных частиц ¢ механизм ограниченного роста (Arrested Growth Mechanism), реализуется в микроэмульсионных системах или в золь-гель (гель-золь) системах, где зародыши пространственно локализованы либо в мицеллах, либо в сетке геля
Другие приемы получения монодисперсных частиц ¢ механизм ограниченного роста (Arrested Growth Mechanism), реализуется в микроэмульсионных системах или в золь-гель (гель-золь) системах, где зародыши пространственно локализованы либо в мицеллах, либо в сетке геля
 Улучшение распределения по размерам (фокусировка) ¢ размерноселективное осаждение основано на размерной зависимости растворимости нанокристаллов (при введении нерастворяющей жидкости первой дестабилизируется дисперсия самых крупных частиц)
Улучшение распределения по размерам (фокусировка) ¢ размерноселективное осаждение основано на размерной зависимости растворимости нанокристаллов (при введении нерастворяющей жидкости первой дестабилизируется дисперсия самых крупных частиц)
 Улучшение распределения по размерам (фокусировка) хроматография высокого давления ¢ капиллярный электрофорез (разделение наночастиц достигается благодаря тому, что отношение заряда к радиусу различно для наночастиц разного размера) ¢
Улучшение распределения по размерам (фокусировка) хроматография высокого давления ¢ капиллярный электрофорез (разделение наночастиц достигается благодаря тому, что отношение заряда к радиусу различно для наночастиц разного размера) ¢

 Контроль размера наночастиц ¢ контроль скорости подачи мономера; ¢ контроль скорости роста частиц
Контроль размера наночастиц ¢ контроль скорости подачи мономера; ¢ контроль скорости роста частиц
 Контроль скорости подачи мономера ¢ ¢ в открытых системах за счет регулирования скорости введения в систему реагентов извне, в закрытых – за счет регулирования скорости образования мономерных прекурсоров или высвобождения мономера из резервуара путем изменения температуры, р. Н и/или начальной концентрации растворимой фазы
Контроль скорости подачи мономера ¢ ¢ в открытых системах за счет регулирования скорости введения в систему реагентов извне, в закрытых – за счет регулирования скорости образования мономерных прекурсоров или высвобождения мономера из резервуара путем изменения температуры, р. Н и/или начальной концентрации растворимой фазы
 Контроль скорости роста частиц за счет регулирования растворимости прекурсора ¢ использование веществ, способных адсорбироваться на поверхности растущих частиц ¢
Контроль скорости роста частиц за счет регулирования растворимости прекурсора ¢ использование веществ, способных адсорбироваться на поверхности растущих частиц ¢
 Контроль формы наночастиц адсорбция различных веществ на определенных участках поверхности частицы ¢ наложение внешнего поля ¢ использование микроэмульсионных систем или дендримеров ¢ темплатный синтез ¢
Контроль формы наночастиц адсорбция различных веществ на определенных участках поверхности частицы ¢ наложение внешнего поля ¢ использование микроэмульсионных систем или дендримеров ¢ темплатный синтез ¢
 Эффективные контролеры формы ¢ ¢ многие неорганические анионы (например, галогениды, фосфаты), аммиак, катионы некоторых тяжелых металлов (например, Cd 2+), адсорбируясь на анионных участках поверхности, блокируют их, органические соединения (амины, аминокислоты, органические фосфоновые кислоты, производные гетероциклов, оксалат -, цитрат-, этилендиаминтетраацетат-, нитрилотриацетат-ионы, мочевина, бипиридил, разнообразные ПАВы).
Эффективные контролеры формы ¢ ¢ многие неорганические анионы (например, галогениды, фосфаты), аммиак, катионы некоторых тяжелых металлов (например, Cd 2+), адсорбируясь на анионных участках поверхности, блокируют их, органические соединения (амины, аминокислоты, органические фосфоновые кислоты, производные гетероциклов, оксалат -, цитрат-, этилендиаминтетраацетат-, нитрилотриацетат-ионы, мочевина, бипиридил, разнообразные ПАВы).
 Pd(NO 3)2+(n-C 8 H 17)4 N+(RCO 2)→ Pd-частицы ¢ ¢ ацетат (СH 3 COO-), дихлорацетат (СHСl 2 COO-), пивалят ((СН 3)3 CСOO-) в основном формируются сферические частицы ¢ ¢ гликолят (СH 2 OHCOO-) наряду со сферическими образуются частицы треугольной формы
Pd(NO 3)2+(n-C 8 H 17)4 N+(RCO 2)→ Pd-частицы ¢ ¢ ацетат (СH 3 COO-), дихлорацетат (СHСl 2 COO-), пивалят ((СН 3)3 CСOO-) в основном формируются сферические частицы ¢ ¢ гликолят (СH 2 OHCOO-) наряду со сферическими образуются частицы треугольной формы
 Наностержень, нанопроволока или нанотрубка? Названия наностержни и нанопроволоки достаточно произвольные, но предполагается, что они отличаются по отношению длины к ширине. L D L/D>100 нанопроволока (англ. nanowire) L/D<100 наностержень (англ. nanorod)
Наностержень, нанопроволока или нанотрубка? Названия наностержни и нанопроволоки достаточно произвольные, но предполагается, что они отличаются по отношению длины к ширине. L D L/D>100 нанопроволока (англ. nanowire) L/D<100 наностержень (англ. nanorod)
 Наностержень, нанопроволока или нанотрубка? D L L/D>1 нанотрубка (англ. nanotube) Нанотрубки – полые наностержни с двумя отверстиями и отношением длины к ширине больше единицы.
Наностержень, нанопроволока или нанотрубка? D L L/D>1 нанотрубка (англ. nanotube) Нанотрубки – полые наностержни с двумя отверстиями и отношением длины к ширине больше единицы.
 Синтез на темплатах, имеющих наноразмерные цилиндрические поры
Синтез на темплатах, имеющих наноразмерные цилиндрические поры
 Материалы, используемые в качестве темплатов Синтетические Природные Микропористые цеолиты Пористые алюмосиликаты Анодно окисленные алюминий или кремний Полимерные мембраны Двухслойные липиды, пронизанные поринами
Материалы, используемые в качестве темплатов Синтетические Природные Микропористые цеолиты Пористые алюмосиликаты Анодно окисленные алюминий или кремний Полимерные мембраны Двухслойные липиды, пронизанные поринами
 ПАРО-ЖИДКО-ТВЕРДОФАЗНЫЙ СИНТЕЗ НАНОПРОВОЛОК (VLS GROWTH) Наращивание слоёв Рост Si Образование эвтектики Нанесение / образование зародыша Fe. Si Насыщение / нуклеация Si Si
ПАРО-ЖИДКО-ТВЕРДОФАЗНЫЙ СИНТЕЗ НАНОПРОВОЛОК (VLS GROWTH) Наращивание слоёв Рост Si Образование эвтектики Нанесение / образование зародыша Fe. Si Насыщение / нуклеация Si Si
 Использование соединений с высоко анизотропной кристаллической структурой t-Se
Использование соединений с высоко анизотропной кристаллической структурой t-Se
 Методы создание оболочки на наночастицах Адсорбция органических веществ поверхностью частицы (возможно с предварительным химическим или физическим модифицированием) ¢ Эпитаксиальный рост кристаллов одного вещества на поверхности другого ¢
Методы создание оболочки на наночастицах Адсорбция органических веществ поверхностью частицы (возможно с предварительным химическим или физическим модифицированием) ¢ Эпитаксиальный рост кристаллов одного вещества на поверхности другого ¢
 Схема строения частиц ядрооболочка (core-shell, реже coresheath particles)
Схема строения частиц ядрооболочка (core-shell, реже coresheath particles)
 Синтез полых наночастиц на основе эффекта Киркендалля
Синтез полых наночастиц на основе эффекта Киркендалля


