Методы основанные на взаимодействии электромагнитного излучения с












































Молекулярная спектрометрия.ppt
- Количество слайдов: 46
 Методы основанные на взаимодействии электромагнитного излучения с веществом Молекулярная спектрометрия
Методы основанные на взаимодействии электромагнитного излучения с веществом Молекулярная спектрометрия
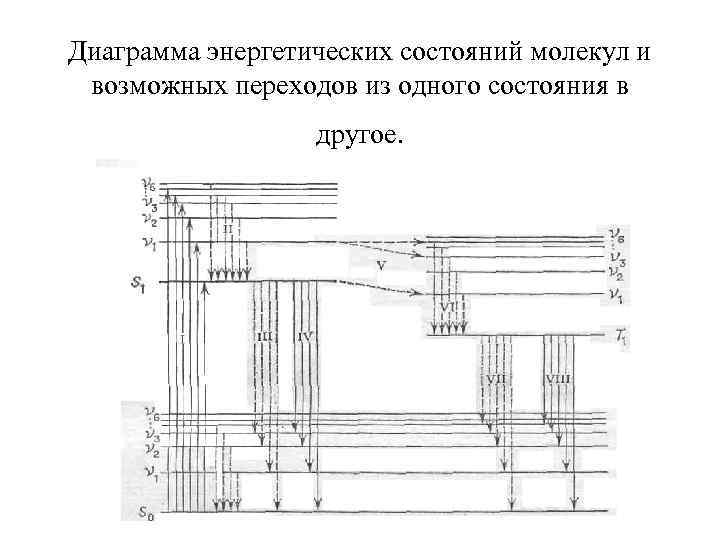
 Диаграмма энергетических состояний молекул и возможных переходов из одного состояния в другое.
Диаграмма энергетических состояний молекул и возможных переходов из одного состояния в другое.
 АБСОРБЦИОННАЯ МОЛЕКУЛЯРНАЯ СПЕКТРОФОТОМЕТРИЯ В УФ- И ВИДИМОЙ ОБЛАСТЯХ СПЕКТРА.
АБСОРБЦИОННАЯ МОЛЕКУЛЯРНАЯ СПЕКТРОФОТОМЕТРИЯ В УФ- И ВИДИМОЙ ОБЛАСТЯХ СПЕКТРА.
 Основной закон светопоглощения (Закон Бугера-Ламберта-Бера)
Основной закон светопоглощения (Закон Бугера-Ламберта-Бера)
 Полуширина ( при ½ макс) полосы пропускания светофильтров: 1 – интерференционный светофильтр; 2 – абсорбционный светофильтр.
Полуширина ( при ½ макс) полосы пропускания светофильтров: 1 – интерференционный светофильтр; 2 – абсорбционный светофильтр.
 Принцип аддитивности (правило аддитивности) оптических плотностей где 1, 2… n – молярные коэффициенты поглощения компонентов смеси; с1, с2…сn – молярные концентрации компонентов смеси.
Принцип аддитивности (правило аддитивности) оптических плотностей где 1, 2… n – молярные коэффициенты поглощения компонентов смеси; с1, с2…сn – молярные концентрации компонентов смеси.
 Фотоколориметрия и спектрофотометрия Фотометрия
Фотоколориметрия и спектрофотометрия Фотометрия
 Два общих случая использования в химическом анализе мокулярной спектрометрии в видимой и УФ областях
Два общих случая использования в химическом анализе мокулярной спектрометрии в видимой и УФ областях
 1. Идентификация и определение в растворах концентрации веществ в тех химических формах, в каких они находятся в растворе.
1. Идентификация и определение в растворах концентрации веществ в тех химических формах, в каких они находятся в растворе.
 Вторым, наиболее часто встречающимся случаем использования молекулярной абсорбционной спектрометрии в анализе является двухстадийная схема анализа, включающая в качестве первой стадии образование в растворе аналитической формы определяемого вещества в результате его взаимодействия со специальным фотометрическим реагентом.
Вторым, наиболее часто встречающимся случаем использования молекулярной абсорбционной спектрометрии в анализе является двухстадийная схема анализа, включающая в качестве первой стадии образование в растворе аналитической формы определяемого вещества в результате его взаимодействия со специальным фотометрическим реагентом.
 Выбор оптимальных условий проведения фотометрических измерений Выбор спектральной области для фотометрических измерений
Выбор оптимальных условий проведения фотометрических измерений Выбор спектральной области для фотометрических измерений
 Оптимальная спектральная область, в которой проводят фотометрические измерения, определяется спектрами поглощения фотометрируемого комплекса и применяемого реагента. При этом существуют два общих случая и промежуточные варианты между ними.
Оптимальная спектральная область, в которой проводят фотометрические измерения, определяется спектрами поглощения фотометрируемого комплекса и применяемого реагента. При этом существуют два общих случая и промежуточные варианты между ними.
 Сравнение погрешности фотометрического определения при разных длинах волн поглощаемого света: а – линия в спектре, по которой определяется фотометрируемое соединение; б – зависимость А от с при макс и мин.
Сравнение погрешности фотометрического определения при разных длинах волн поглощаемого света: а – линия в спектре, по которой определяется фотометрируемое соединение; б – зависимость А от с при макс и мин.
 Спектр поглощения диэтилдитиокарбамината меди в хлороформе (c 5 > c 4 > c 3 > c 2 > c 1)
Спектр поглощения диэтилдитиокарбамината меди в хлороформе (c 5 > c 4 > c 3 > c 2 > c 1)
 Зависимость оптической плотности раствора диэтилдитиокарбамината меди от его концентрации при = 436 нм и = 540 нм.
Зависимость оптической плотности раствора диэтилдитиокарбамината меди от его концентрации при = 436 нм и = 540 нм.
 Второй общий случай, когда спектры поглощения фотометрируемого соединения и применяемого реагента перекрываются
Второй общий случай, когда спектры поглощения фотометрируемого соединения и применяемого реагента перекрываются
 Перекрывание полос поглощения в спектрах определяемого соединения (1) и реагента (2).
Перекрывание полос поглощения в спектрах определяемого соединения (1) и реагента (2).
 Спектры поглощения равновесных форм определяемого элемента: 1 – спектр основного соединения; 2 – спектр конкурентной формы.
Спектры поглощения равновесных форм определяемого элемента: 1 – спектр основного соединения; 2 – спектр конкурентной формы.
 Выбор оптимальных условий проведения фотометрических измерений Выбор оптимального диапазона оптических плотностей.
Выбор оптимальных условий проведения фотометрических измерений Выбор оптимального диапазона оптических плотностей.
 Зависимость относительной погрешности ( , %) определения концентрации от оптической плотности раствора (при sr = 0, 003): 1 – кривая рассчитана по уравнению Шмидта; 2, 3 – кривые рассчитаны для спектрофтометра СФ-4 и фотоколориметра ФЭК-М, соответственно.
Зависимость относительной погрешности ( , %) определения концентрации от оптической плотности раствора (при sr = 0, 003): 1 – кривая рассчитана по уравнению Шмидта; 2, 3 – кривые рассчитаны для спектрофтометра СФ-4 и фотоколориметра ФЭК-М, соответственно.
 Уравнение Шмидта Согласно основному закону светопоглощения: . После дифференцирования и соответствующих преобразований можно получить уравнение Шмидта:
Уравнение Шмидта Согласно основному закону светопоглощения: . После дифференцирования и соответствующих преобразований можно получить уравнение Шмидта:
 Выбор оптимальных условий проведения фотометрических измерений Отклонения от основного закона светопоглощения.
Выбор оптимальных условий проведения фотометрических измерений Отклонения от основного закона светопоглощения.
 инструментальные (физические) и химические Главной физической причиной кажущихся отклонений является немонохроматичность поглощаемого светового потока. Другой физической причиной нарушения закона Б. Л. Б. является рассеяние света. Рассеяние света может возникать в оптической схеме прибора вследствие его отражения от поверхностей линз, зеркал и т. п. , а кроме того, в растворе при возникновении конвективных потоков за счет неравномерного нагрева.
инструментальные (физические) и химические Главной физической причиной кажущихся отклонений является немонохроматичность поглощаемого светового потока. Другой физической причиной нарушения закона Б. Л. Б. является рассеяние света. Рассеяние света может возникать в оптической схеме прибора вследствие его отражения от поверхностей линз, зеркал и т. п. , а кроме того, в растворе при возникновении конвективных потоков за счет неравномерного нагрева.
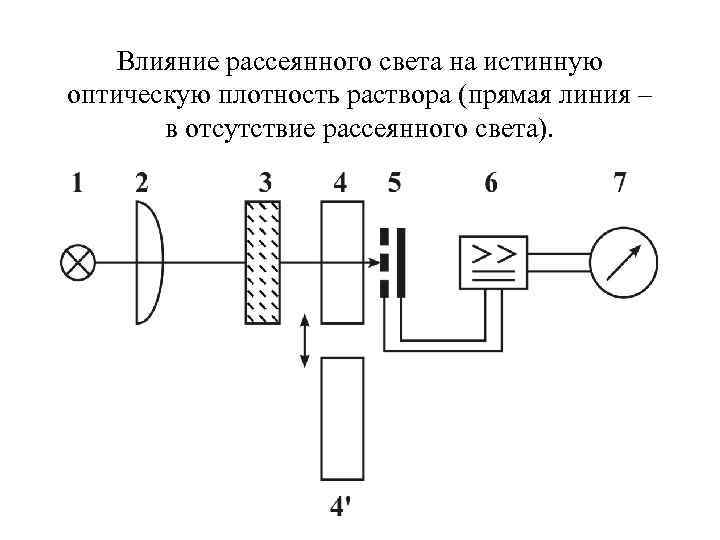
 Влияние рассеянного света на истинную оптическую плотность раствора (прямая линия – в отсутствие рассеянного света).
Влияние рассеянного света на истинную оптическую плотность раствора (прямая линия – в отсутствие рассеянного света).
 Основными «химическими» причинами кажущихся отклонений являются различные побочные реакции, которые приводят к различной (и часто неколичественной) степени связанности аналита в светопоглощающее соединение. Среди этих побочных реакций наиболее важными являются реакции комплексообразования ионов металлов и протонирования фотометрических реагентов.
Основными «химическими» причинами кажущихся отклонений являются различные побочные реакции, которые приводят к различной (и часто неколичественной) степени связанности аналита в светопоглощающее соединение. Среди этих побочных реакций наиболее важными являются реакции комплексообразования ионов металлов и протонирования фотометрических реагентов.
 Выбор условий образования аналитических форм. Существуют две схемы образования аналитических форм для фотометрического анализа. Первая, наиболее общая схема предполагает прямую химическую реакцию между аналитом и фотометрическим реагентом M+R=MR, которая приводит к образованию окрашенного соединения, способного к поглощению света в видимой области спектра.
Выбор условий образования аналитических форм. Существуют две схемы образования аналитических форм для фотометрического анализа. Первая, наиболее общая схема предполагает прямую химическую реакцию между аналитом и фотометрическим реагентом M+R=MR, которая приводит к образованию окрашенного соединения, способного к поглощению света в видимой области спектра.
 Вторая косвенная схема предполагает определение аналита по реакции со вспомогательным окрашенным соединением. В этом случае используют вспомогательное светопоглощающее соединение M 1 R, с которым аналиты М или А взаимодействуют по реакциям катионного или анионного обмена, не образуя при этом светопоглощающих соединений: M 1 R + M ⇄ MR + M 1 M 1 R + A ⇄ M 1 A + R В результате этих реакций концентрация вспомогательного светопоглощающего соединения M 1 R (и соответственно оптическая плотность раствора) уменьшается пропорционально концентрации вступивших в реакцию аналитов M или А.
Вторая косвенная схема предполагает определение аналита по реакции со вспомогательным окрашенным соединением. В этом случае используют вспомогательное светопоглощающее соединение M 1 R, с которым аналиты М или А взаимодействуют по реакциям катионного или анионного обмена, не образуя при этом светопоглощающих соединений: M 1 R + M ⇄ MR + M 1 M 1 R + A ⇄ M 1 A + R В результате этих реакций концентрация вспомогательного светопоглощающего соединения M 1 R (и соответственно оптическая плотность раствора) уменьшается пропорционально концентрации вступивших в реакцию аналитов M или А.
 Выбор условий образования аналитических форм. Аналитические формы аналитов и реакции их образования
Выбор условий образования аналитических форм. Аналитические формы аналитов и реакции их образования
 Способы измерения светопоглощения (оптической плотности) • Фотометрические методы определения концентрации растворов основаны на сравнении поглощения или пропускания света стандартными и анализируемыми растворами. Степень поглощения света фотометрируемыми растворами измеряют с помощью специальных оптических приборов - фотоэлектроколориметров и спектрофотометров, в которых световая энергия, проходящая через фотометрируемый раствор, преобразуется фотоприемником в электрическую с последующим усилением электрического сигнала и его индикацией.
Способы измерения светопоглощения (оптической плотности) • Фотометрические методы определения концентрации растворов основаны на сравнении поглощения или пропускания света стандартными и анализируемыми растворами. Степень поглощения света фотометрируемыми растворами измеряют с помощью специальных оптических приборов - фотоэлектроколориметров и спектрофотометров, в которых световая энергия, проходящая через фотометрируемый раствор, преобразуется фотоприемником в электрическую с последующим усилением электрического сигнала и его индикацией.
 Аналитические формы аналитов и реакции их образования • В фотометрическом анализе применяются различные по природе реагенты, наиболее распространенными продуктами реакций которых с аналитами являются: • 1. Хелатные (внутрикомплексные) соединения металлов с хелатообразующими органическими реагентами. • 2. Соединения металлов с кислотными и основными органическими красителями. • 3. Разнолигандные комплексные соединения и ионные ассоциаты. • 4. Однороднолигандные комплексы металлов с неорганическими лигандами и гетерополисоединения.
Аналитические формы аналитов и реакции их образования • В фотометрическом анализе применяются различные по природе реагенты, наиболее распространенными продуктами реакций которых с аналитами являются: • 1. Хелатные (внутрикомплексные) соединения металлов с хелатообразующими органическими реагентами. • 2. Соединения металлов с кислотными и основными органическими красителями. • 3. Разнолигандные комплексные соединения и ионные ассоциаты. • 4. Однороднолигандные комплексы металлов с неорганическими лигандами и гетерополисоединения.
 Современные приборы позволяют проводить измерения в видимой области спектра (400 -760 нм) и в примыкающих к ней ультрафиолетовой (300 -400 нм) и инфракрасной (760 -1000 нм) областях. Приемниками излучения являются фотоэлементы разных типов, монохроматорами — светофильтры с шириной полосы пропускания 10 -15 нм (интерференционные светофильтры) или 30— 50 нм (абсорбционные светофильтры).
Современные приборы позволяют проводить измерения в видимой области спектра (400 -760 нм) и в примыкающих к ней ультрафиолетовой (300 -400 нм) и инфракрасной (760 -1000 нм) областях. Приемниками излучения являются фотоэлементы разных типов, монохроматорами — светофильтры с шириной полосы пропускания 10 -15 нм (интерференционные светофильтры) или 30— 50 нм (абсорбционные светофильтры).
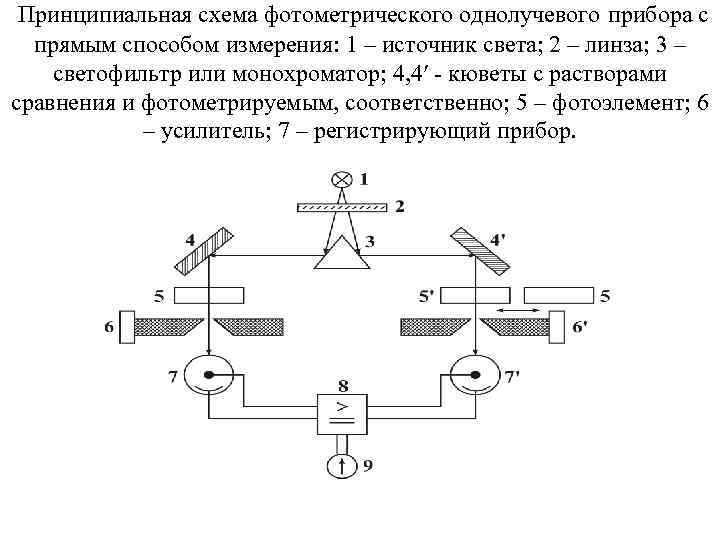
 Принципиальная схема фотометрического однолучевого прибора с прямым способом измерения: 1 – источник света; 2 – линза; 3 – светофильтр или монохроматор; 4, 4 - кюветы с растворами сравнения и фотометрируемым, соответственно; 5 – фотоэлемент; 6 – усилитель; 7 – регистрирующий прибор.
Принципиальная схема фотометрического однолучевого прибора с прямым способом измерения: 1 – источник света; 2 – линза; 3 – светофильтр или монохроматор; 4, 4 - кюветы с растворами сравнения и фотометрируемым, соответственно; 5 – фотоэлемент; 6 – усилитель; 7 – регистрирующий прибор.
 Принципиальная схема фотометрического двухлучевого прибора с компенсационным способом измерения: 1 – источник света; 2 – светофильтр; 3 – линза; 4, 4 - зеркала; 5, 5 - кюветы с раствором сравнения и фотометрируемым, соответственно; 6, 6 - щелевые диафрагмы; 7, 7 - фотоэлементы; 8 – усилитель; 9 – нуль-индикатор.
Принципиальная схема фотометрического двухлучевого прибора с компенсационным способом измерения: 1 – источник света; 2 – светофильтр; 3 – линза; 4, 4 - зеркала; 5, 5 - кюветы с раствором сравнения и фотометрируемым, соответственно; 6, 6 - щелевые диафрагмы; 7, 7 - фотоэлементы; 8 – усилитель; 9 – нуль-индикатор.
 Спектрофотометры • Спектрофотометры также предназначены для измерения коэффициентов пропускания или оптической плотности растворов, но их возможности намного шире по спектральному диапазону (от 190 до 1100 нм), монохроматизации света (до 1 -2 нм), автоматизации и быстродействию всех измерений, сочетанию с ПК, с выдачей спектров и количественных данных на мониторе ПК.
Спектрофотометры • Спектрофотометры также предназначены для измерения коэффициентов пропускания или оптической плотности растворов, но их возможности намного шире по спектральному диапазону (от 190 до 1100 нм), монохроматизации света (до 1 -2 нм), автоматизации и быстродействию всех измерений, сочетанию с ПК, с выдачей спектров и количественных данных на мониторе ПК.
 Концентрацию аналита определяют путем сравнения оптических плотностей анализируемого и стандартных растворов известных концентраций. Для этих целей, как правило, применяют один из следующих вариантов. • 1. Метод сравнения: сх = сст • 2. Метод градуировочного графика А = f ( с ), построенного по стандартным растворам аналита • 3. Метод стандартных добавок
Концентрацию аналита определяют путем сравнения оптических плотностей анализируемого и стандартных растворов известных концентраций. Для этих целей, как правило, применяют один из следующих вариантов. • 1. Метод сравнения: сх = сст • 2. Метод градуировочного графика А = f ( с ), построенного по стандартным растворам аналита • 3. Метод стандартных добавок
 ЛЮМИНЕСЦЕНТНЫЕ МЕТОДЫ АНАЛИЗА
ЛЮМИНЕСЦЕНТНЫЕ МЕТОДЫ АНАЛИЗА
 Зеркальная симметрия спектров поглощения и люминесценции раствора красителя родамина 6 Ж в этаноле: 1 – спектр поглощения возбуждающего излучения ( - молярный коэффициент поглощения); 2 – спектр люминесцентного излучения (Iл – интенсивность люминесценции; - длина волны).
Зеркальная симметрия спектров поглощения и люминесценции раствора красителя родамина 6 Ж в этаноле: 1 – спектр поглощения возбуждающего излучения ( - молярный коэффициент поглощения); 2 – спектр люминесцентного излучения (Iл – интенсивность люминесценции; - длина волны).
 Схематическое изображение спектров поглощения (П) и люминесценции (Л) молекул и областей пропускания оптимальных фильтров (заштрихованные участки): Iл – интенсивность люминесценции; - молярный коэффициент поглощения; - длина волны.
Схематическое изображение спектров поглощения (П) и люминесценции (Л) молекул и областей пропускания оптимальных фильтров (заштрихованные участки): Iл – интенсивность люминесценции; - молярный коэффициент поглощения; - длина волны.
 Приемы сужения полос в спектрах люминесценции • регистрация спектров люминесценции при глубоком охлаждении (метод Шпольского). • метод синхронного сканирования. Синхронные спектры – спектры, получаемые при одновременном изменении длин волн возбуждения и испускания с постоянным сдвигом между ними. С помощью современных спектрофлуориметров можно регистрировать синхронные спектры с шириной полосы излучения 8 -10 нм
Приемы сужения полос в спектрах люминесценции • регистрация спектров люминесценции при глубоком охлаждении (метод Шпольского). • метод синхронного сканирования. Синхронные спектры – спектры, получаемые при одновременном изменении длин волн возбуждения и испускания с постоянным сдвигом между ними. С помощью современных спектрофлуориметров можно регистрировать синхронные спектры с шириной полосы излучения 8 -10 нм
 Интенсивность люминесценции. • Эффективность преобразования энергии возбуждения ( Е погл. ) в энергию излучения ( Е люм ) характеризуют абсолютным энергетическим ( эн) и квантовым ( кв) выходом люминесценции. и , где N л и N n – число излучаемых и поглощенных квантов света, соответственно.
Интенсивность люминесценции. • Эффективность преобразования энергии возбуждения ( Е погл. ) в энергию излучения ( Е люм ) характеризуют абсолютным энергетическим ( эн) и квантовым ( кв) выходом люминесценции. и , где N л и N n – число излучаемых и поглощенных квантов света, соответственно.
 Интенсивность люминесценции Эффективность преобразования энергии возбуждения ( Е погл. ) энергию излучения ( Е люм ) характеризуют абсолютн энергетическим ( эн) и квантовым ( кв) выходом люминесценции.
Интенсивность люминесценции Эффективность преобразования энергии возбуждения ( Е погл. ) энергию излучения ( Е люм ) характеризуют абсолютн энергетическим ( эн) и квантовым ( кв) выходом люминесценции.
 Закон Вавилова • При возбуждении флуоресценции излучением коротковолновой части спектра, величина энергетического выхода до некоторого предела увеличивается пропорционально длине волны возбуждающего излучения.
Закон Вавилова • При возбуждении флуоресценции излучением коротковолновой части спектра, величина энергетического выхода до некоторого предела увеличивается пропорционально длине волны возбуждающего излучения.
 Тушение (гашение) люминесценции. • Под тушением люминесценции понимается любой процесс физической или химической природы, который приводит к уменьшению интенсивности люминесценции. К их числу относят все процессы, сопровождающиеся безызлучательными потерями молекулой избыточной энергии, полученной ею при возбуждении.
Тушение (гашение) люминесценции. • Под тушением люминесценции понимается любой процесс физической или химической природы, который приводит к уменьшению интенсивности люминесценции. К их числу относят все процессы, сопровождающиеся безызлучательными потерями молекулой избыточной энергии, полученной ею при возбуждении.
 Измерение интенсивности люминесценции. 1 - источник возбуждающего излучения; 2, 4 – сфетофильтры; 3 – кювета с анализируемым раствором; 5 – фотоэлемент или фотоумножитель; 6 – электронный усилитель; 7 – регистрирующий прибор.
Измерение интенсивности люминесценции. 1 - источник возбуждающего излучения; 2, 4 – сфетофильтры; 3 – кювета с анализируемым раствором; 5 – фотоэлемент или фотоумножитель; 6 – электронный усилитель; 7 – регистрирующий прибор.
 Полосы в спектре флуоресценции сдвинуты в область больших длин волн по сравнению с полосами в спектрах поглощения тех же молекул. (Закон Стокса и Ломмеля).
Полосы в спектре флуоресценции сдвинуты в область больших длин волн по сравнению с полосами в спектрах поглощения тех же молекул. (Закон Стокса и Ломмеля).
 В то же время форма полос поглощения и флуоресценции определяется одинаковым расположением колебательных подуровней основного S и возбужденного S 1 электронных состояний, являющихся характеристическим признаком молекул каждого типа, и поэтому спектр люминесценции симметричен спектру поглощения (правило зеркальной симметрии Левшина).
В то же время форма полос поглощения и флуоресценции определяется одинаковым расположением колебательных подуровней основного S и возбужденного S 1 электронных состояний, являющихся характеристическим признаком молекул каждого типа, и поэтому спектр люминесценции симметричен спектру поглощения (правило зеркальной симметрии Левшина).

