L5_6 Галогенирование.ppt
- Количество слайдов: 35
 Методы органического синтеза Лекции 5, 6 Галогенирование Повторение – мать учения
Методы органического синтеза Лекции 5, 6 Галогенирование Повторение – мать учения
 Содержание лекции • • • Реакции галогенирования в синтезе лекарственных препаратов Общие сведения о реакциях галогенирования Реагенты, катализаторы, механизмы реакций галогенирования Условия проведения реакций галогенирования Практика проведения хлорирования, бромирования и иодирования ароматических соединений Галогенирование аренов в боковую цепь, галогенирование алканов Механизм реакции свободнорадикального галогенирования Галогенирование непредельных соединений Галогенирование спиртов, карбонильных соединений, карбоновых кислот Синтез фторсодержащих соединений 2
Содержание лекции • • • Реакции галогенирования в синтезе лекарственных препаратов Общие сведения о реакциях галогенирования Реагенты, катализаторы, механизмы реакций галогенирования Условия проведения реакций галогенирования Практика проведения хлорирования, бромирования и иодирования ароматических соединений Галогенирование аренов в боковую цепь, галогенирование алканов Механизм реакции свободнорадикального галогенирования Галогенирование непредельных соединений Галогенирование спиртов, карбонильных соединений, карбоновых кислот Синтез фторсодержащих соединений 2
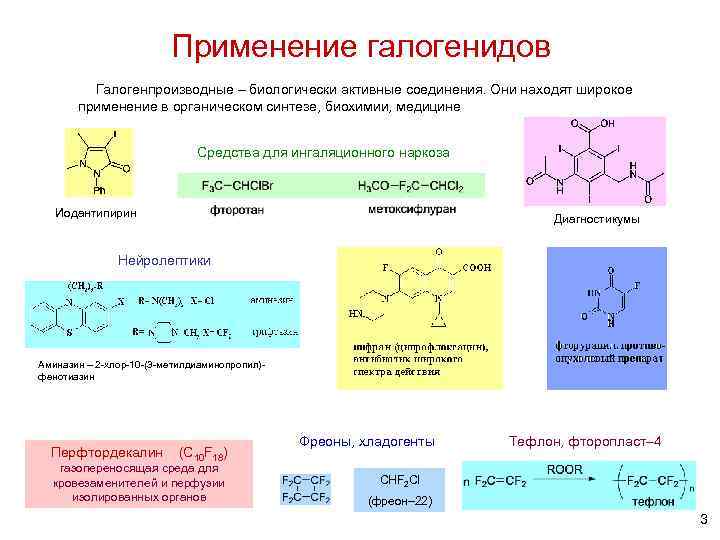 Применение галогенидов Галогенпроизводные – биологически активные соединения. Они находят широкое применение в органическом синтезе, биохимии, медицине Средства для ингаляционного наркоза Иодантипирин Диагностикумы Нейролептики Аминазин – 2 -хлор-10 -(3 -метилдиаминопропил)фенотиазин Перфтордекалин (С 10 F 18) газопереносящая среда для кровезаменителей и перфузии изолированных органов Фреоны, хладогенты Тефлон, фторопласт– 4 CHF 2 Cl (фреон– 22) 3
Применение галогенидов Галогенпроизводные – биологически активные соединения. Они находят широкое применение в органическом синтезе, биохимии, медицине Средства для ингаляционного наркоза Иодантипирин Диагностикумы Нейролептики Аминазин – 2 -хлор-10 -(3 -метилдиаминопропил)фенотиазин Перфтордекалин (С 10 F 18) газопереносящая среда для кровезаменителей и перфузии изолированных органов Фреоны, хладогенты Тефлон, фторопласт– 4 CHF 2 Cl (фреон– 22) 3
 Галогенирование Общие сведения § Галогенированием называют процесс введения атома галогена в органического соединения. § Галогенирование может протекать как реакция замещения атома водорода в органической молекуле или как реакция присоединения галогена. § Галогенирование является одной из наиболее распространенных и важных реакций в тонком органическом синтезе. § В промышленности основным процессом является хлорирование. § Бромирование используется в небольших объемах (стоимость, активность галогенов) § Прямое иодирование осложнено образованием сильного восстановителя HI: § Прямое фторирование используется редко из-за большой активности фтора молекулу 4
Галогенирование Общие сведения § Галогенированием называют процесс введения атома галогена в органического соединения. § Галогенирование может протекать как реакция замещения атома водорода в органической молекуле или как реакция присоединения галогена. § Галогенирование является одной из наиболее распространенных и важных реакций в тонком органическом синтезе. § В промышленности основным процессом является хлорирование. § Бромирование используется в небольших объемах (стоимость, активность галогенов) § Прямое иодирование осложнено образованием сильного восстановителя HI: § Прямое фторирование используется редко из-за большой активности фтора молекулу 4
 Объекты галогенирования: Алифатические и ароматические углеводороды; ароматические амины, спирты, карбонильные соединения, карбоновые кислоты, фенолы; гетероциклические соединения. Ø Ø Ø Галогенирующие агенты: Хлор, бром, иод, фтор HCl c окислителями HCl, HBr, HI Галогениды металлов (соли) Сульфурилхлорид SO 2 Cl 2 Тионилхлорид SOCl 2 PCl 3 PCl 5 POCl 3 N-бромсукцинимид (NBC) Гипогалоидные кислоты HOCl, HOBr Галогенамины RNHCl 5
Объекты галогенирования: Алифатические и ароматические углеводороды; ароматические амины, спирты, карбонильные соединения, карбоновые кислоты, фенолы; гетероциклические соединения. Ø Ø Ø Галогенирующие агенты: Хлор, бром, иод, фтор HCl c окислителями HCl, HBr, HI Галогениды металлов (соли) Сульфурилхлорид SO 2 Cl 2 Тионилхлорид SOCl 2 PCl 3 PCl 5 POCl 3 N-бромсукцинимид (NBC) Гипогалоидные кислоты HOCl, HOBr Галогенамины RNHCl 5
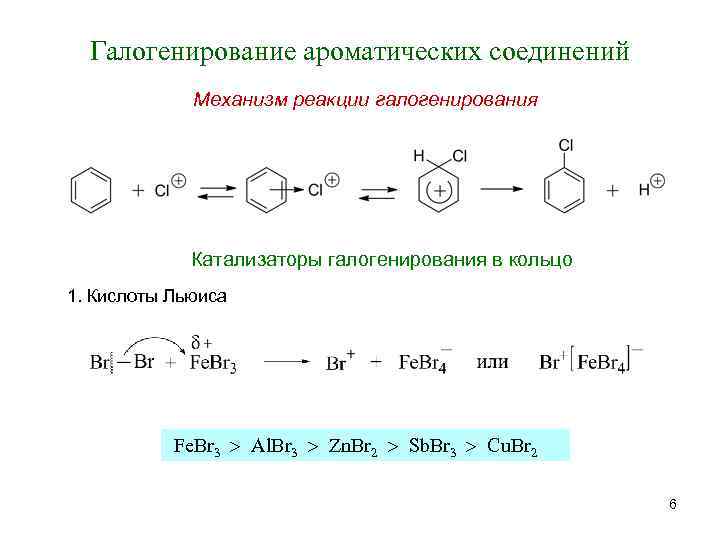 Галогенирование ароматических соединений Механизм реакции галогенирования Катализаторы галогенирования в кольцо 1. Кислоты Льюиса Fe. Br 3 Al. Br 3 Zn. Br 2 Sb. Br 3 Cu. Br 2 6
Галогенирование ароматических соединений Механизм реакции галогенирования Катализаторы галогенирования в кольцо 1. Кислоты Льюиса Fe. Br 3 Al. Br 3 Zn. Br 2 Sb. Br 3 Cu. Br 2 6
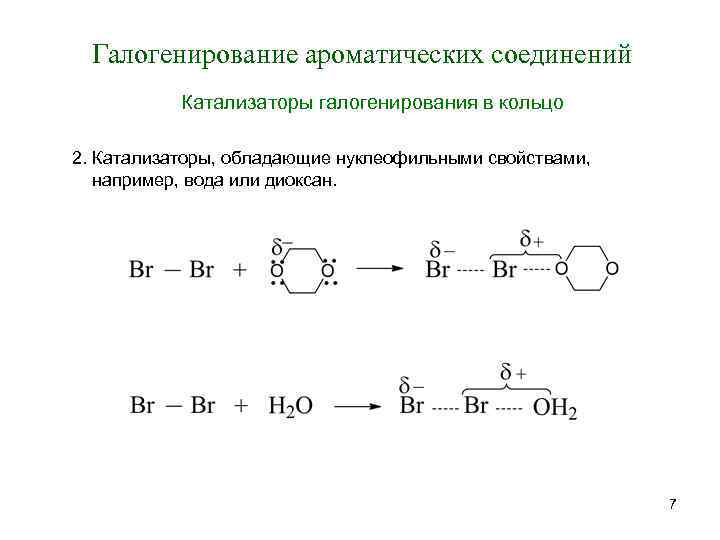 Галогенирование ароматических соединений Катализаторы галогенирования в кольцо 2. Катализаторы, обладающие нуклеофильными свойствами, например, вода или диоксан. 7
Галогенирование ароматических соединений Катализаторы галогенирования в кольцо 2. Катализаторы, обладающие нуклеофильными свойствами, например, вода или диоксан. 7
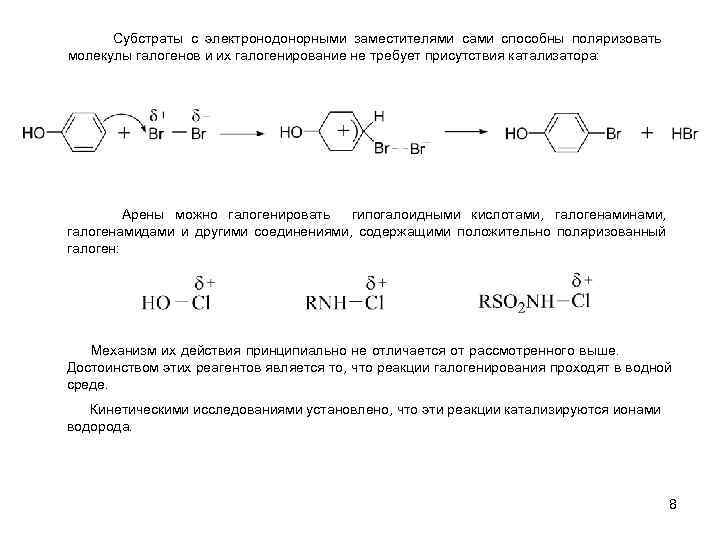 Cубстраты с электронодонорными заместителями сами способны поляризовать молекулы галогенов и их галогенирование не требует присутствия катализатора: Арены можно галогенировать гипогалоидными кислотами, галогенами, галогенамидами и другими соединениями, содержащими положительно поляризованный галоген: Механизм их действия принципиально не отличается от рассмотренного выше. Достоинством этих реагентов является то, что реакции галогенирования проходят в водной среде. Кинетическими исследованиями установлено, что эти реакции катализируются ионами водорода. 8
Cубстраты с электронодонорными заместителями сами способны поляризовать молекулы галогенов и их галогенирование не требует присутствия катализатора: Арены можно галогенировать гипогалоидными кислотами, галогенами, галогенамидами и другими соединениями, содержащими положительно поляризованный галоген: Механизм их действия принципиально не отличается от рассмотренного выше. Достоинством этих реагентов является то, что реакции галогенирования проходят в водной среде. Кинетическими исследованиями установлено, что эти реакции катализируются ионами водорода. 8
 Механизм реакции иодирования аренов Из всех галогенов иод обладает самой низкой электрофильностью. Для его активации применяют окислители или соли серебра (реже соли меди и ртути). В качестве окислителей используют HNO 3, HIO 4, SO 3, H 2 O 2 и ряд других. Роль окислителя заключается в окислении I 2 до 2 I+: I 2 + H 2 O 2 2 HOI или I 2 + HNO 3 2 HOI + 2 NO 2. Для усиления диссоциации HOI необходим протонный катализ, осуществляемый, как правило, добавками H 2 SO 4: Реакция Тронова-Новикова 1) 2) I 2 -Ag. SO 4 -H 2 SO 4 при 1000 C за 2 часа, выход 55% 3) 9 Время 10 минут
Механизм реакции иодирования аренов Из всех галогенов иод обладает самой низкой электрофильностью. Для его активации применяют окислители или соли серебра (реже соли меди и ртути). В качестве окислителей используют HNO 3, HIO 4, SO 3, H 2 O 2 и ряд других. Роль окислителя заключается в окислении I 2 до 2 I+: I 2 + H 2 O 2 2 HOI или I 2 + HNO 3 2 HOI + 2 NO 2. Для усиления диссоциации HOI необходим протонный катализ, осуществляемый, как правило, добавками H 2 SO 4: Реакция Тронова-Новикова 1) 2) I 2 -Ag. SO 4 -H 2 SO 4 при 1000 C за 2 часа, выход 55% 3) 9 Время 10 минут
 Условия проведения процессов галогенирования Характер субстрата Для активных субстратов – более мягкие реагенты Температура Монохлорирование предпочтительно проводить при низкой температуре (20 – 700 С), так как при повышенной температуре образуются полигалогензамещенные арены. Бромирование и иодирование – эндотермические процессы Катализаторы Играют важную роль в процессах галогенирования, так как определяют не только скорость реакции, но и направление процесса. В промышленности для галогенирования в кольцо используют преимущественно железо в виде стружек или опилок в количестве 1% от массы галогенируемого соединения. При использовании хлорида железа количество катализатора уменьшается вдвое. Растворители 1) инертные по отношению к галогену (четыреххлористый углерод); 2) реагирующие с галогеном с более низкой скоростью, чем субстрат (нитробензол, полихлорбензолы); 3) растворители, не вступающие в реакцию с галогеном, но ускоряющие реакцию (серная кислота). Растворитель для конкретной реакции подбирают, учитывая температуру проведения процесса, активность субстрата и другие факторы. 10
Условия проведения процессов галогенирования Характер субстрата Для активных субстратов – более мягкие реагенты Температура Монохлорирование предпочтительно проводить при низкой температуре (20 – 700 С), так как при повышенной температуре образуются полигалогензамещенные арены. Бромирование и иодирование – эндотермические процессы Катализаторы Играют важную роль в процессах галогенирования, так как определяют не только скорость реакции, но и направление процесса. В промышленности для галогенирования в кольцо используют преимущественно железо в виде стружек или опилок в количестве 1% от массы галогенируемого соединения. При использовании хлорида железа количество катализатора уменьшается вдвое. Растворители 1) инертные по отношению к галогену (четыреххлористый углерод); 2) реагирующие с галогеном с более низкой скоростью, чем субстрат (нитробензол, полихлорбензолы); 3) растворители, не вступающие в реакцию с галогеном, но ускоряющие реакцию (серная кислота). Растворитель для конкретной реакции подбирают, учитывая температуру проведения процесса, активность субстрата и другие факторы. 10
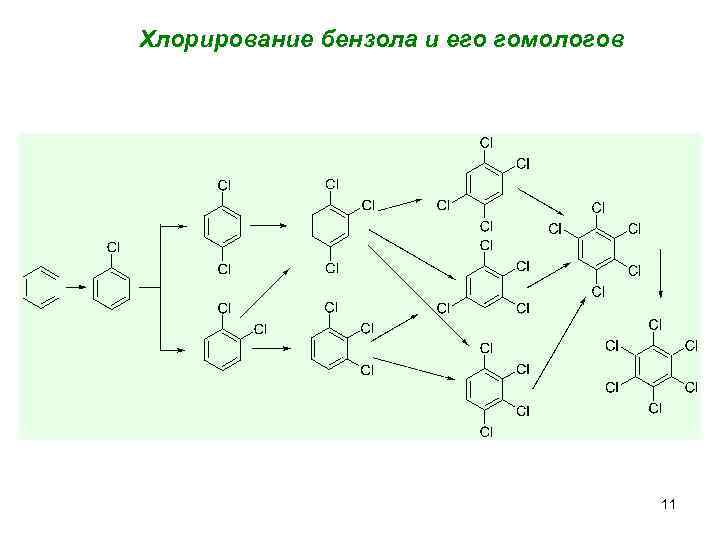 Хлорирование бензола и его гомологов 11
Хлорирование бензола и его гомологов 11
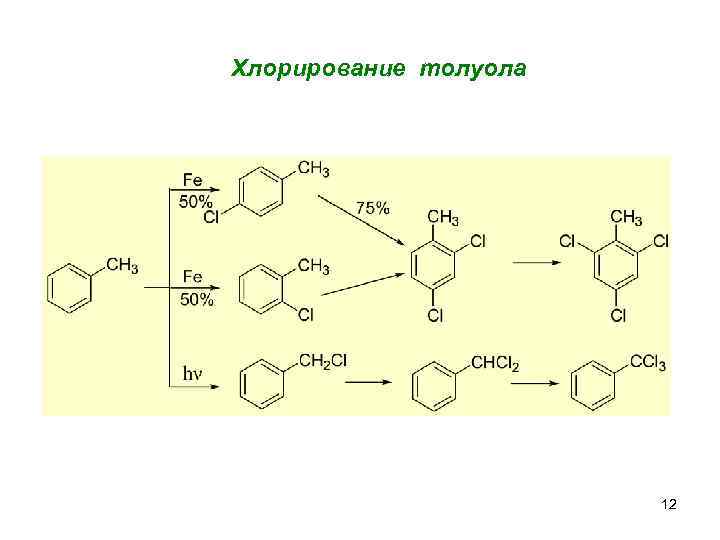 Хлорирование толуола 12
Хлорирование толуола 12
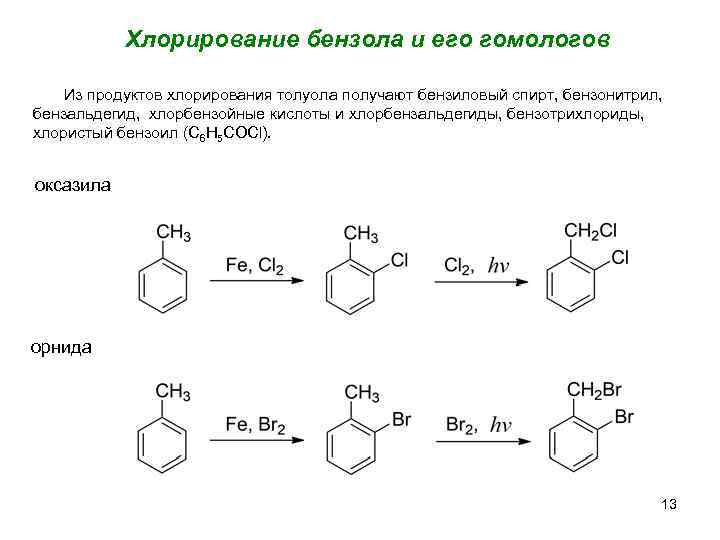 Хлорирование бензола и его гомологов Из продуктов хлорирования толуола получают бензиловый спирт, бензонитрил, бензальдегид, хлорбензойные кислоты и хлорбензальдегиды, бензотрихлориды, хлористый бензоил (C 6 H 5 COCl). оксазила орнида 13
Хлорирование бензола и его гомологов Из продуктов хлорирования толуола получают бензиловый спирт, бензонитрил, бензальдегид, хлорбензойные кислоты и хлорбензальдегиды, бензотрихлориды, хлористый бензоил (C 6 H 5 COCl). оксазила орнида 13
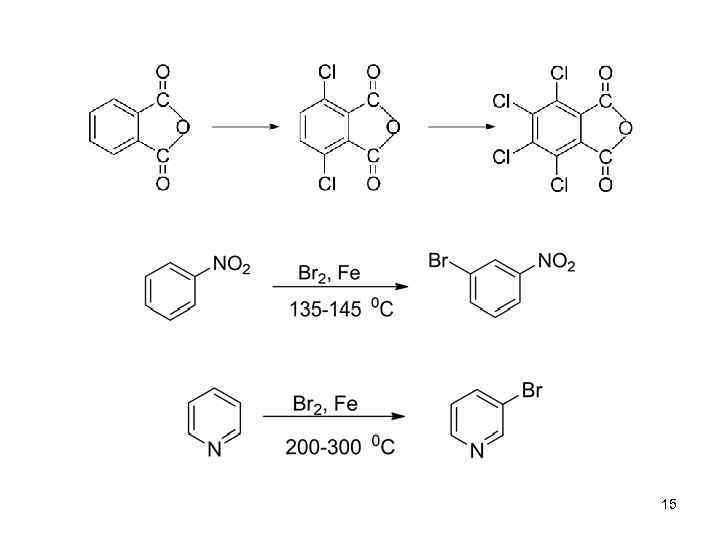
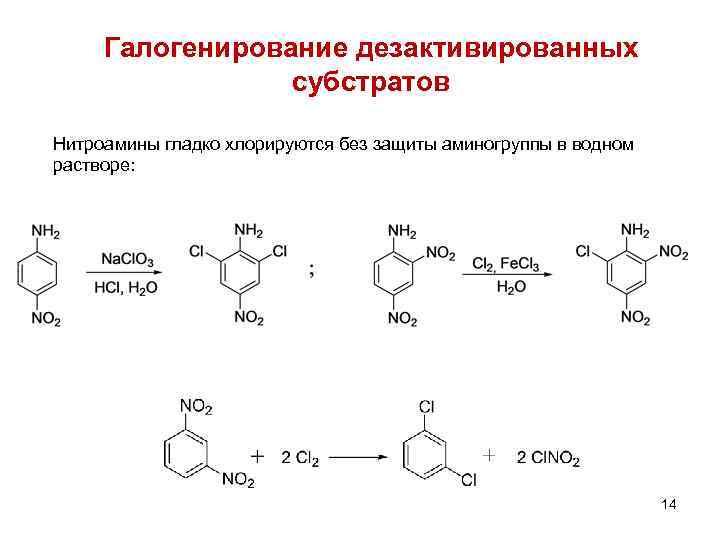 Галогенирование дезактивированных субстратов Нитроамины гладко хлорируются без защиты аминогруппы в водном растворе: 14
Галогенирование дезактивированных субстратов Нитроамины гладко хлорируются без защиты аминогруппы в водном растворе: 14
 15
15
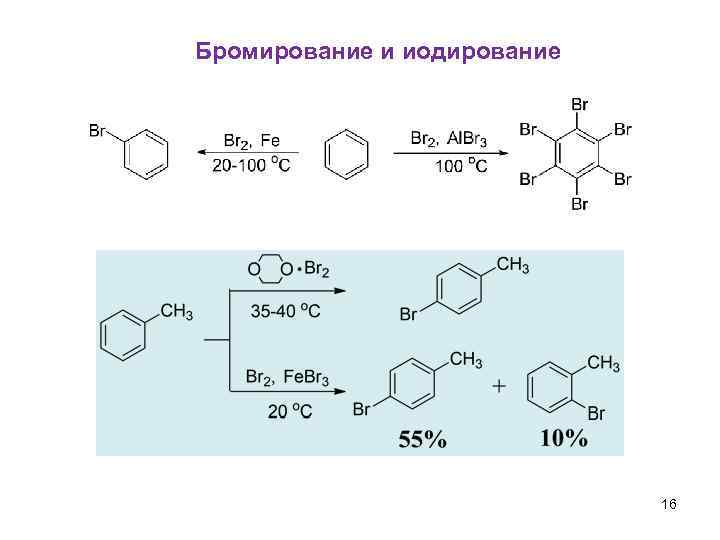 Бромирование и иодирование 16
Бромирование и иодирование 16
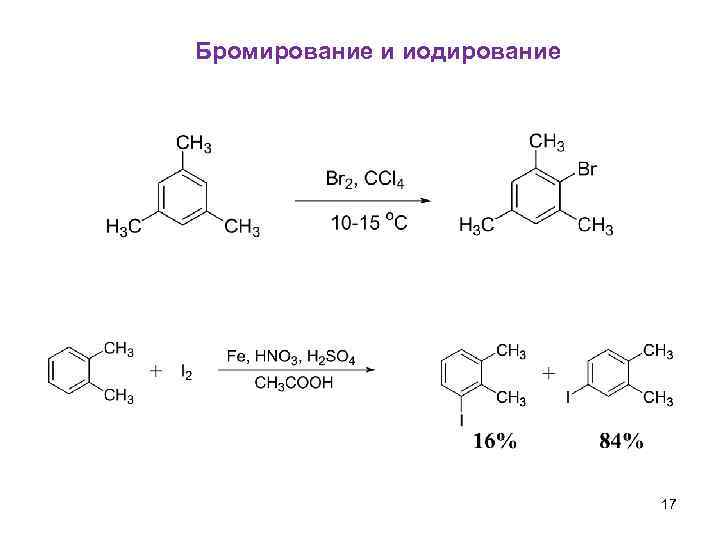 Бромирование и иодирование 17
Бромирование и иодирование 17
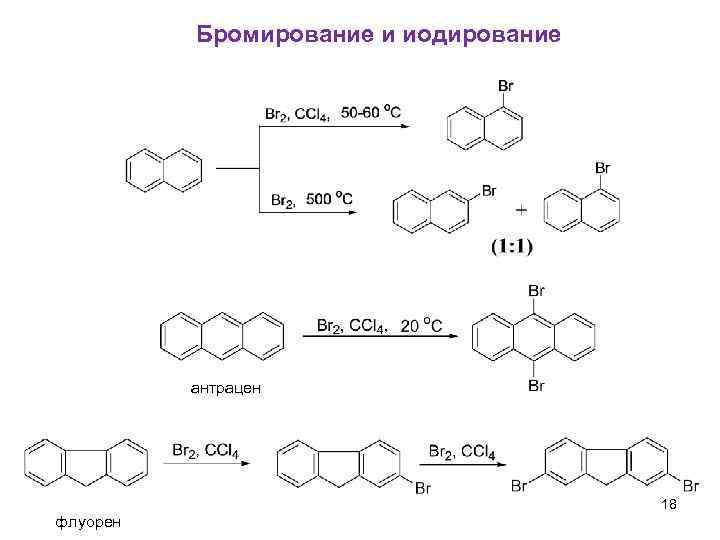 Бромирование и иодирование антрацен 18 флуорен
Бромирование и иодирование антрацен 18 флуорен
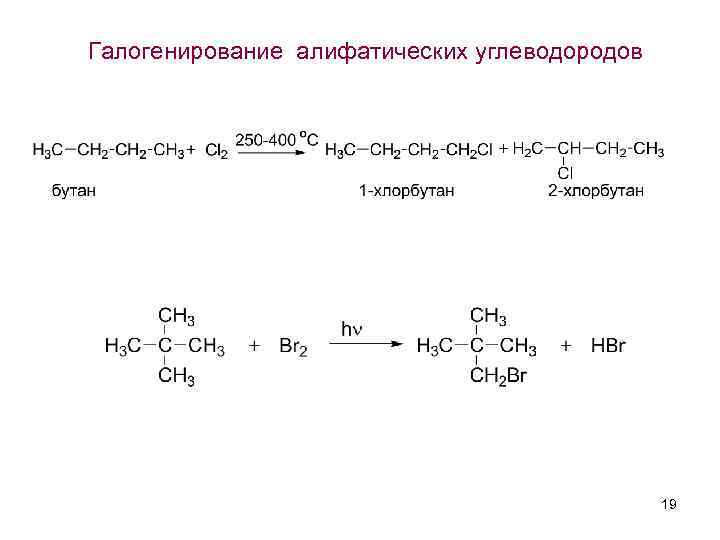 Галогенирование алифатических углеводородов 19
Галогенирование алифатических углеводородов 19
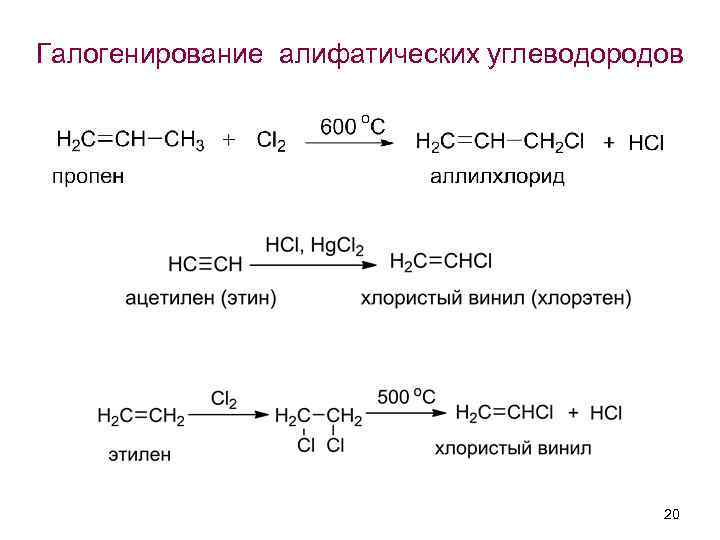 Галогенирование алифатических углеводородов 20
Галогенирование алифатических углеводородов 20
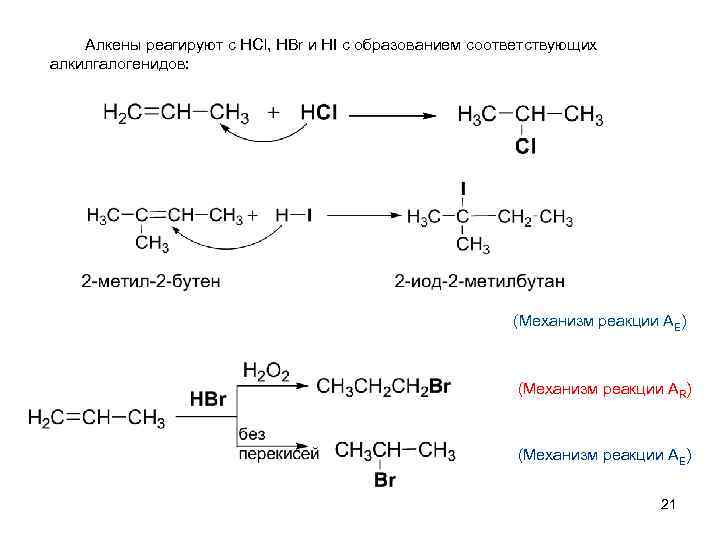 Алкены реагируют с HCl, HBr и HI с образованием соответствующих алкилгалогенидов: (Механизм реакции АЕ) (Механизм реакции АR) (Механизм реакции АЕ) 21
Алкены реагируют с HCl, HBr и HI с образованием соответствующих алкилгалогенидов: (Механизм реакции АЕ) (Механизм реакции АR) (Механизм реакции АЕ) 21
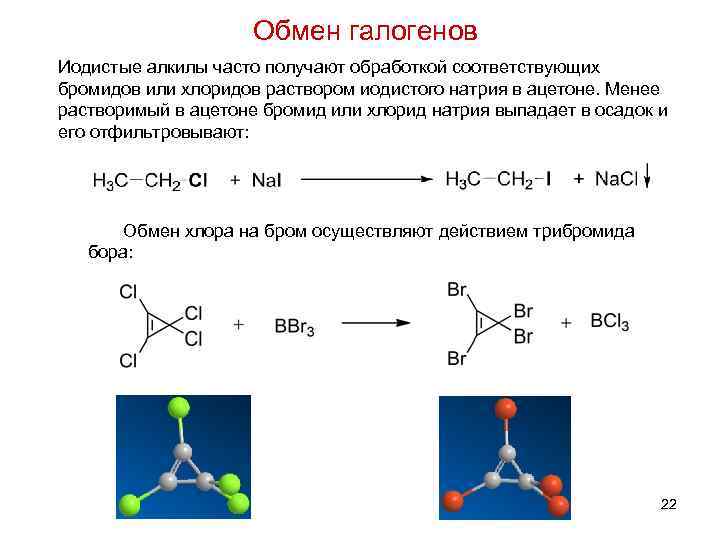 Обмен галогенов Иодистые алкилы часто получают обработкой соответствующих бромидов или хлоридов раствором иодистого натрия в ацетоне. Менее растворимый в ацетоне бромид или хлорид натрия выпадает в осадок и его отфильтровывают: Обмен хлора на бром осуществляют действием трибромида бора: 22
Обмен галогенов Иодистые алкилы часто получают обработкой соответствующих бромидов или хлоридов раствором иодистого натрия в ацетоне. Менее растворимый в ацетоне бромид или хлорид натрия выпадает в осадок и его отфильтровывают: Обмен хлора на бром осуществляют действием трибромида бора: 22
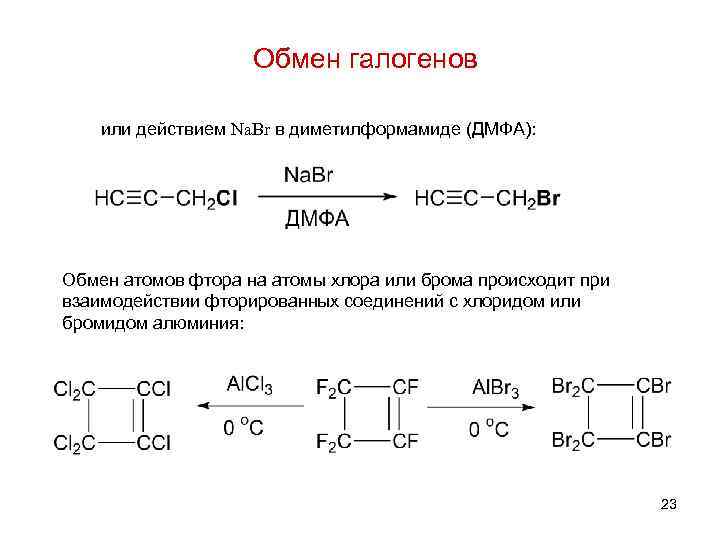 Обмен галогенов или действием Na. Br в диметилформамиде (ДМФА): Обмен атомов фтора на атомы хлора или брома происходит при взаимодействии фторированных соединений с хлоридом или бромидом алюминия: 23
Обмен галогенов или действием Na. Br в диметилформамиде (ДМФА): Обмен атомов фтора на атомы хлора или брома происходит при взаимодействии фторированных соединений с хлоридом или бромидом алюминия: 23
 Синтез фторсодержащих соединений Фторпроизводные невозможно получить прямым фторированием, т. к. в атмосфере фтора углеводороды «сгорают» до CF 4, поэтому их получают замещением хлора на фтор при действии фторидов металлов: 24
Синтез фторсодержащих соединений Фторпроизводные невозможно получить прямым фторированием, т. к. в атмосфере фтора углеводороды «сгорают» до CF 4, поэтому их получают замещением хлора на фтор при действии фторидов металлов: 24
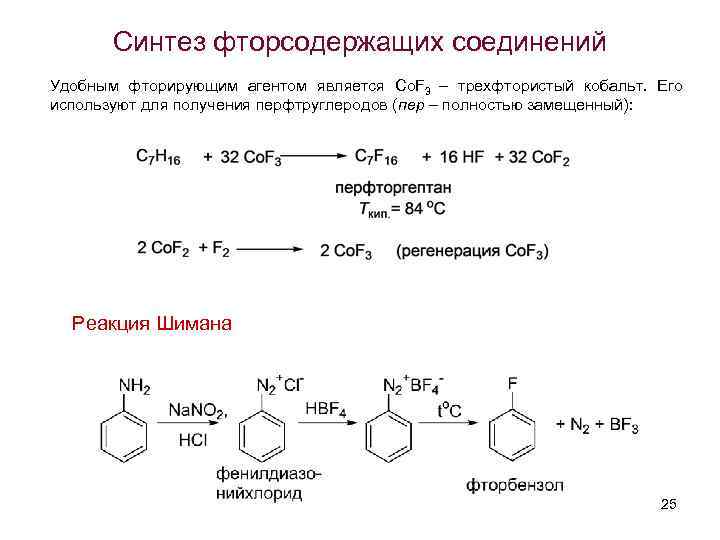 Синтез фторсодержащих соединений Удобным фторирующим агентом является Co. F 3 – трехфтористый кобальт. Его используют для получения перфтруглеродов (пер – полностью замещенный): Реакция Шимана 25
Синтез фторсодержащих соединений Удобным фторирующим агентом является Co. F 3 – трехфтористый кобальт. Его используют для получения перфтруглеродов (пер – полностью замещенный): Реакция Шимана 25
 Галогенирование карбонильных соединений Под действием хлора, брома или йода альдегиды и кетоны галогенируются в -положение по отношению к карбонильной группе: Под действием фтора эта реакция не идет. В качестве галогенирующих агентов применяют также сульфурилхлорид и Nбромсукцинимид. 26
Галогенирование карбонильных соединений Под действием хлора, брома или йода альдегиды и кетоны галогенируются в -положение по отношению к карбонильной группе: Под действием фтора эта реакция не идет. В качестве галогенирующих агентов применяют также сульфурилхлорид и Nбромсукцинимид. 26
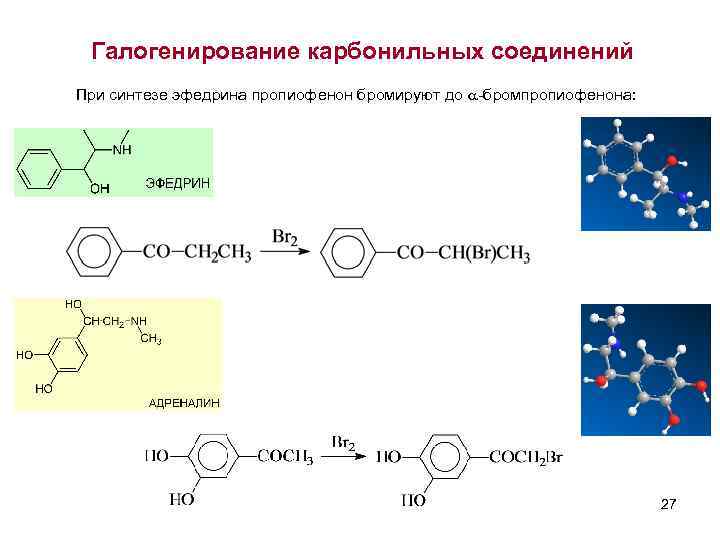 Галогенирование карбонильных соединений При синтезе эфедрина пропиофенон бромируют до -бромпропиофенона: 27
Галогенирование карбонильных соединений При синтезе эфедрина пропиофенон бромируют до -бромпропиофенона: 27
 28
28
 Галогенирование карбоновых кислот Водород -углеродного атома в карбоновых кислотах можно заместить на атом брома или хлора. С иодом и фтором эта реакция не идет. 29
Галогенирование карбоновых кислот Водород -углеродного атома в карбоновых кислотах можно заместить на атом брома или хлора. С иодом и фтором эта реакция не идет. 29
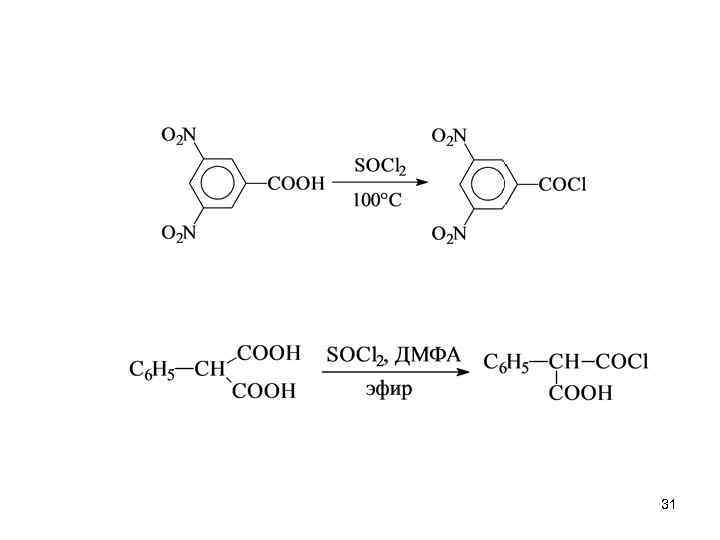
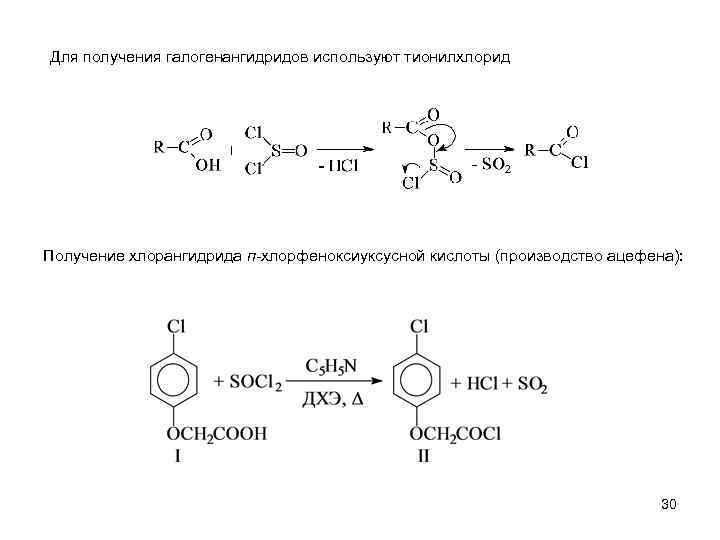 Для получения галогенангидридов используют тионилхлорид Получение хлорангидрида п-хлорфеноксиуксусной кислоты (производство ацефена): 30
Для получения галогенангидридов используют тионилхлорид Получение хлорангидрида п-хлорфеноксиуксусной кислоты (производство ацефена): 30
 31
31
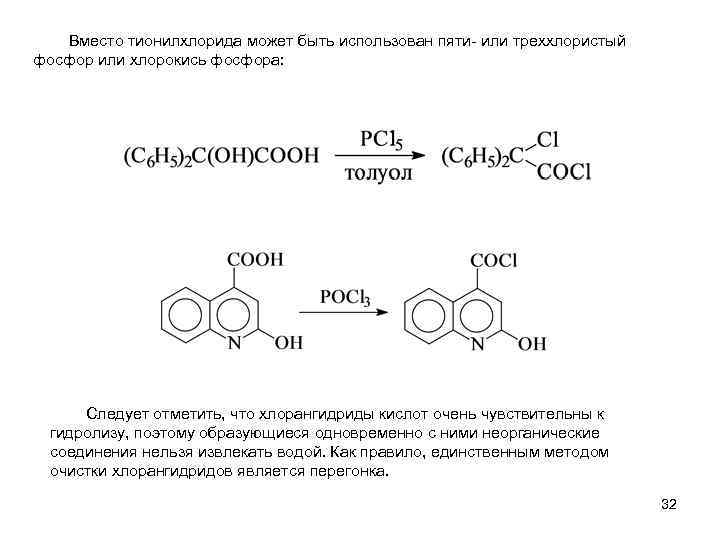 Вместо тионилхлорида может быть использован пяти- или треххлористый фосфор или хлорокись фосфора: Следует отметить, что хлорангидриды кислот очень чувствительны к гидролизу, поэтому образующиеся одновременно с ними неорганические соединения нельзя извлекать водой. Как правило, единственным методом очистки хлорангидридов является перегонка. 32
Вместо тионилхлорида может быть использован пяти- или треххлористый фосфор или хлорокись фосфора: Следует отметить, что хлорангидриды кислот очень чувствительны к гидролизу, поэтому образующиеся одновременно с ними неорганические соединения нельзя извлекать водой. Как правило, единственным методом очистки хлорангидридов является перегонка. 32
 Галогенирование спиртов Образование галогеналканов из спиртов и галогенводородов может протекать по следующим схемам: или: Этот метод пригоден для получения хлор-, бром- и иодалканов. Скорость реакции зависит от природы галогенводорода и строения спирта. Реакционная способность галогенводородов возрастает в ряду HCl < HBr < HI, а спиртов – в ряду Проба Лукаса первичный < вторичный < третичный. 33
Галогенирование спиртов Образование галогеналканов из спиртов и галогенводородов может протекать по следующим схемам: или: Этот метод пригоден для получения хлор-, бром- и иодалканов. Скорость реакции зависит от природы галогенводорода и строения спирта. Реакционная способность галогенводородов возрастает в ряду HCl < HBr < HI, а спиртов – в ряду Проба Лукаса первичный < вторичный < третичный. 33
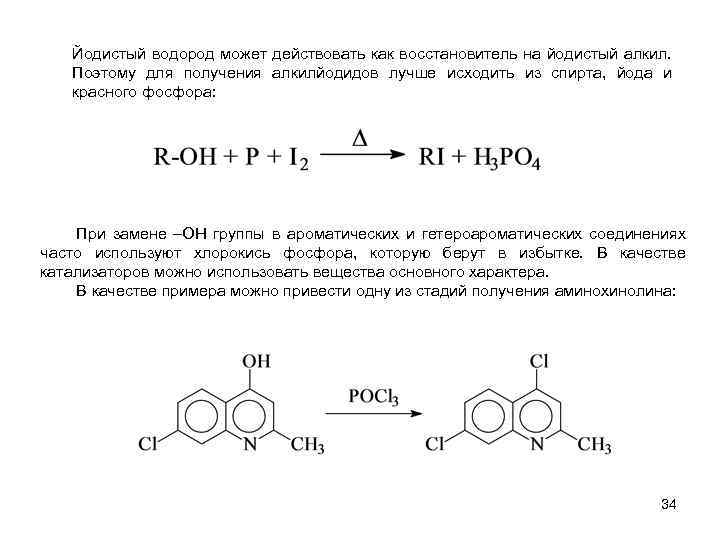 Йодистый водород может действовать как восстановитель на йодистый алкил. Поэтому для получения алкилйодидов лучше исходить из спирта, йода и красного фосфора: При замене –ОН группы в ароматических и гетероароматических соединениях часто используют хлорокись фосфора, которую берут в избытке. В качестве катализаторов можно использовать вещества основного характера. В качестве примера можно привести одну из стадий получения аминохинолина: 34
Йодистый водород может действовать как восстановитель на йодистый алкил. Поэтому для получения алкилйодидов лучше исходить из спирта, йода и красного фосфора: При замене –ОН группы в ароматических и гетероароматических соединениях часто используют хлорокись фосфора, которую берут в избытке. В качестве катализаторов можно использовать вещества основного характера. В качестве примера можно привести одну из стадий получения аминохинолина: 34
 Еще более распространенным в химико-фармацевтической промышленности методом замены ОН-группы на хлор является взаимодействие гидроксилсодержащих соединений с тионилхлоридом, Эта реакция очень часто используется в синтезе лекарственных веществ. 35
Еще более распространенным в химико-фармацевтической промышленности методом замены ОН-группы на хлор является взаимодействие гидроксилсодержащих соединений с тионилхлоридом, Эта реакция очень часто используется в синтезе лекарственных веществ. 35


