Методы определения порядков реакций.ppt
- Количество слайдов: 27
 Методы определения порядков реакций
Методы определения порядков реакций
 Порядок реакции является очень важным кинетическим параметром, т. к. значение его необходимо для установления механизма сложных реакций. Порядок реакции определяют экспериментально. При этом используют два основных метода: 1) Метод изоляции (метод избытка Оствальда), который заключается в выделении частного порядка данной реакции по каждому веществу в отдельности; 2) Метод равных концентраций. Первый метод позволяет определить порядок n 1 по веществу А 1 реакции а 1 А 1 + а 2 А 2 + а 3 А 3 + … продукты, если все вещества, кроме А 1, взяты в избытке и изменением их концентраций в ходе реакции можно пренебречь, т. е. концентрации всех реагентов, кроме А 1, можно ввести в константу скорости. Для исследуемой реакции в этом случае вместо выражения для скорости можно записать: , где Определив, таким образом, порядок ni по каждому из реагентов, общий порядок реакции находится как сумма частных порядков, согласно (1. 9) n = ni
Порядок реакции является очень важным кинетическим параметром, т. к. значение его необходимо для установления механизма сложных реакций. Порядок реакции определяют экспериментально. При этом используют два основных метода: 1) Метод изоляции (метод избытка Оствальда), который заключается в выделении частного порядка данной реакции по каждому веществу в отдельности; 2) Метод равных концентраций. Первый метод позволяет определить порядок n 1 по веществу А 1 реакции а 1 А 1 + а 2 А 2 + а 3 А 3 + … продукты, если все вещества, кроме А 1, взяты в избытке и изменением их концентраций в ходе реакции можно пренебречь, т. е. концентрации всех реагентов, кроме А 1, можно ввести в константу скорости. Для исследуемой реакции в этом случае вместо выражения для скорости можно записать: , где Определив, таким образом, порядок ni по каждому из реагентов, общий порядок реакции находится как сумма частных порядков, согласно (1. 9) n = ni
 Второй метод применяют для нахождения общего порядка реакции. Если реакцию можно провести при условиях равенства концентраций реагентов , то скорость = k. CAn (2. 36) Все известные методы определения общего и частных порядков можно разделить на две группы: интегральные; дифференциальные. Рассмотрим интегральные методы. К ним относятся: а) метод подстановки; б) метод определения порядка реакции по времени полупревращения; в) метод Оствальда – Ноесса.
Второй метод применяют для нахождения общего порядка реакции. Если реакцию можно провести при условиях равенства концентраций реагентов , то скорость = k. CAn (2. 36) Все известные методы определения общего и частных порядков можно разделить на две группы: интегральные; дифференциальные. Рассмотрим интегральные методы. К ним относятся: а) метод подстановки; б) метод определения порядка реакции по времени полупревращения; в) метод Оствальда – Ноесса.
 Интегральные методы расчета порядка реакции основаны на использовании интегральной формы кинетического уравнения данной реакции. Обработку кинетических измерений можно производить аналитическим или графическим способом. а) В методе подстановки используется прием подбора кинетического уравнения. Для этого экспериментально измеренные в разные моменты времени концентрации реагента подставляют в одно из кинетических уравнений первого, второго, третьего порядка. Критерием правильности выбора кинетического уравнения является независимость константы скорости от времени реакции. Если расчет ни по одному из уравнений не дает постоянного значения константы скорости, то это означает, что зависимость скоскорости реакции от концентрации более сложная, чем степенной закон. Аналогично, путем подбора, выполняется графическая обработка результатов. По экспериментальным значениям концентраций и соответствующим им временам строят графики в координатах: ln. C t (реакция первого порядка) 1/С t (реакция второго порядка) 1/С 2 t (реакция третьего порядка) Получение линейной зависимости при этом указывает на порядок изучаемой реакции.
Интегральные методы расчета порядка реакции основаны на использовании интегральной формы кинетического уравнения данной реакции. Обработку кинетических измерений можно производить аналитическим или графическим способом. а) В методе подстановки используется прием подбора кинетического уравнения. Для этого экспериментально измеренные в разные моменты времени концентрации реагента подставляют в одно из кинетических уравнений первого, второго, третьего порядка. Критерием правильности выбора кинетического уравнения является независимость константы скорости от времени реакции. Если расчет ни по одному из уравнений не дает постоянного значения константы скорости, то это означает, что зависимость скоскорости реакции от концентрации более сложная, чем степенной закон. Аналогично, путем подбора, выполняется графическая обработка результатов. По экспериментальным значениям концентраций и соответствующим им временам строят графики в координатах: ln. C t (реакция первого порядка) 1/С t (реакция второго порядка) 1/С 2 t (реакция третьего порядка) Получение линейной зависимости при этом указывает на порядок изучаемой реакции.
 б) Метод периода полупревращения. Этот метод был предложен Раковским. Время полупревращения для реакций различных порядков поразному зависит от начальной концентрации исходных веществ (формулы: (2. 9//), (2. 19), (2. 29), (2. 34)). t 1/2 = ln 2/k 1 (реакция первого порядка) t 1/2 = 1/(k 2. C 0) (реакция второго порядка) t 1/2 = 3/(2 k 3 C 02) (реакция третьего порядка) в) Метод Оствальда – Ноесса – метод определения порядка реакции по времени превращения вещества на долю . В основе метода лежит однозначная связь между t и начальной концентрацией С 0 реагента: для реакций первого порядка, т. е. n = 1 (2. 14) для остальных реакций, т. е. n 1
б) Метод периода полупревращения. Этот метод был предложен Раковским. Время полупревращения для реакций различных порядков поразному зависит от начальной концентрации исходных веществ (формулы: (2. 9//), (2. 19), (2. 29), (2. 34)). t 1/2 = ln 2/k 1 (реакция первого порядка) t 1/2 = 1/(k 2. C 0) (реакция второго порядка) t 1/2 = 3/(2 k 3 C 02) (реакция третьего порядка) в) Метод Оствальда – Ноесса – метод определения порядка реакции по времени превращения вещества на долю . В основе метода лежит однозначная связь между t и начальной концентрацией С 0 реагента: для реакций первого порядка, т. е. n = 1 (2. 14) для остальных реакций, т. е. n 1
 (2. 34/) Порядок реакции рассчитывают по формуле (2. 37/) (аналитический подход), полученной из (2. 34/). Прологарифмируем выражение (2. 34/) lnt = ln(const) – (n – 1)ln. C 0, где (2. 37) для определенного . Измерив t при двух различных С 0, найдем (2. 37/) Для более точного нахождения порядка реакции можно построить график зависимости (2. 37) в логарифмических координатах lnt ln. C 0.
(2. 34/) Порядок реакции рассчитывают по формуле (2. 37/) (аналитический подход), полученной из (2. 34/). Прологарифмируем выражение (2. 34/) lnt = ln(const) – (n – 1)ln. C 0, где (2. 37) для определенного . Измерив t при двух различных С 0, найдем (2. 37/) Для более точного нахождения порядка реакции можно построить график зависимости (2. 37) в логарифмических координатах lnt ln. C 0.
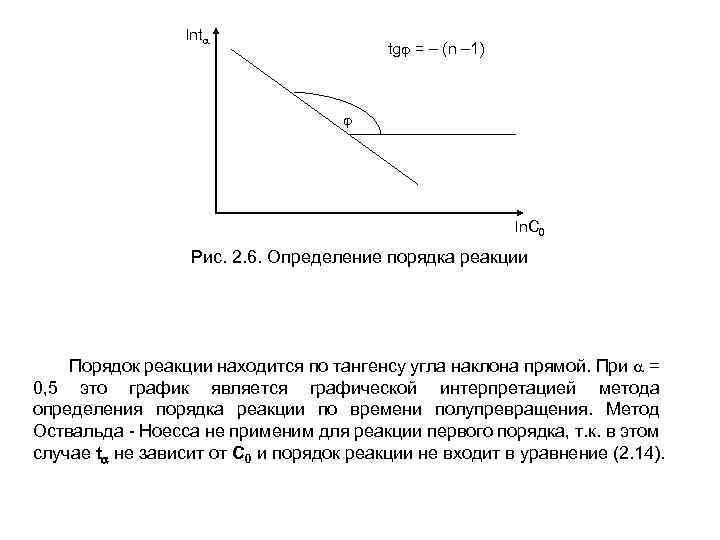 lnt tg = – (n – 1) ln. C 0 Рис. 2. 6. Определение порядка реакции Порядок реакции находится по тангенсу угла наклона прямой. При = 0, 5 это график является графической интерпретацией метода определения порядка реакции по времени полупревращения. Метод Оствальда - Ноесса не применим для реакции первого порядка, т. к. в этом случае t не зависит от С 0 и порядок реакции не входит в уравнение (2. 14).
lnt tg = – (n – 1) ln. C 0 Рис. 2. 6. Определение порядка реакции Порядок реакции находится по тангенсу угла наклона прямой. При = 0, 5 это график является графической интерпретацией метода определения порядка реакции по времени полупревращения. Метод Оствальда - Ноесса не применим для реакции первого порядка, т. к. в этом случае t не зависит от С 0 и порядок реакции не входит в уравнение (2. 14).
 2) Дифференциальные методы расчета основаны на анализе дифференциального кинетического уравнения или в логарифмической форме ln = lnk + nln. C При этом можно использовать зависимости начальной скорости 0 от исходной концентрации реагента ln 0 = lnk + nln. C 0 (2. 38) или изменяющейся в ходе реакции скорости t от концентрации реагента С в момент времени t. ln t = lnk + nln. C (2. 39) Порядок реакции, установленный по зависимости (2. 38), называют концентрационным, или истинным. Порядок, определенный по зависимости (2. 39), называют временным. Для сложных реакций концентрационный и временной порядки могут не совпадать.
2) Дифференциальные методы расчета основаны на анализе дифференциального кинетического уравнения или в логарифмической форме ln = lnk + nln. C При этом можно использовать зависимости начальной скорости 0 от исходной концентрации реагента ln 0 = lnk + nln. C 0 (2. 38) или изменяющейся в ходе реакции скорости t от концентрации реагента С в момент времени t. ln t = lnk + nln. C (2. 39) Порядок реакции, установленный по зависимости (2. 38), называют концентрационным, или истинным. Порядок, определенный по зависимости (2. 39), называют временным. Для сложных реакций концентрационный и временной порядки могут не совпадать.
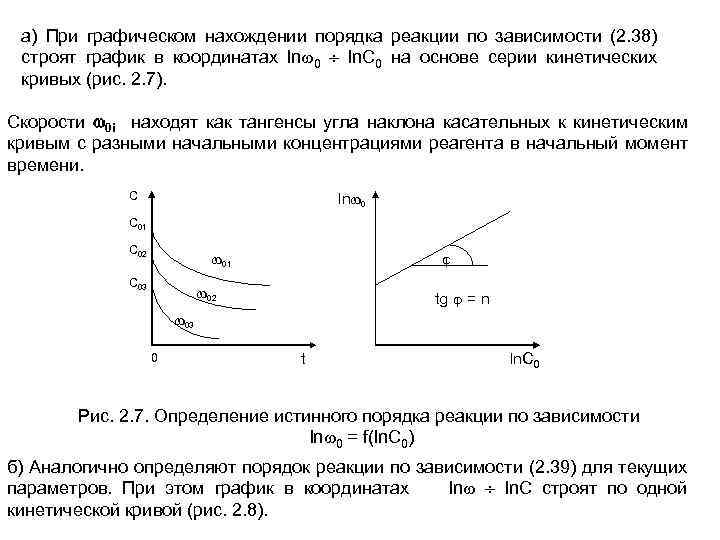 а) При графическом нахождении порядка реакции по зависимости (2. 38) строят график в координатах ln 0 ln. C 0 на основе серии кинетических кривых (рис. 2. 7). Скорости 0 i находят как тангенсы угла наклона касательных к кинетическим кривым с разными начальными концентрациями реагента в начальный момент времени. C ln 0 C 01 C 02 01 C 03 02 tg = n 03 0 t ln. C 0 Рис. 2. 7. Определение истинного порядка реакции по зависимости ln 0 = f(ln. C 0) б) Аналогично определяют порядок реакции по зависимости (2. 39) для текущих параметров. При этом график в координатах ln ln. C строят по одной кинетической кривой (рис. 2. 8).
а) При графическом нахождении порядка реакции по зависимости (2. 38) строят график в координатах ln 0 ln. C 0 на основе серии кинетических кривых (рис. 2. 7). Скорости 0 i находят как тангенсы угла наклона касательных к кинетическим кривым с разными начальными концентрациями реагента в начальный момент времени. C ln 0 C 01 C 02 01 C 03 02 tg = n 03 0 t ln. C 0 Рис. 2. 7. Определение истинного порядка реакции по зависимости ln 0 = f(ln. C 0) б) Аналогично определяют порядок реакции по зависимости (2. 39) для текущих параметров. При этом график в координатах ln ln. C строят по одной кинетической кривой (рис. 2. 8).
 Основной недостаток графического дифференциального метода заключается в том, что трудно с высокой точностью измерить наклон касательной к кинетической кривой в данной точке, т. е. скорость определяется с погрешностью. в) Порядок реакции можно определить аналитически, решив систему уравнений ln 01 = lnk + nln. C 01 ln 02 = lnk + nln. C 02 (2. 40) Этот метод (метод Вант – Гоффа) позволяет находить не только целые, но и дробные порядки. Современные методы вычислительной математики позволяют с помощью ЭВМ по опытным данным найти порядки реакции по отдельным реагентам, а также константу скорости реакции.
Основной недостаток графического дифференциального метода заключается в том, что трудно с высокой точностью измерить наклон касательной к кинетической кривой в данной точке, т. е. скорость определяется с погрешностью. в) Порядок реакции можно определить аналитически, решив систему уравнений ln 01 = lnk + nln. C 01 ln 02 = lnk + nln. C 02 (2. 40) Этот метод (метод Вант – Гоффа) позволяет находить не только целые, но и дробные порядки. Современные методы вычислительной математики позволяют с помощью ЭВМ по опытным данным найти порядки реакции по отдельным реагентам, а также константу скорости реакции.
 Кинетика сложных реакций Большинство химических реакций являются сложными, т. е. состоят из нескольких элементарных стадий. Несмотря на большое разнообразие сложных реакций, их можно свести к комбинации нескольких типов: односторонних, обратимых, параллельных и последовательных реакций. Условие квазистационарности, введенное в кинетику Боденштейном означает, что образующиеся в сложной реакции промежуточные вещества вступают в дальнейшие взаимодействия так быстро, что их концентрации в ходе процесса остаются неизменными, т. е. (2. 41) где Сi – концентрация некоторого промежуточного вещества. Это условие позволяет перейти к рассмотрению алгебраических уравнений вместо дифференциальных, что существенно упрощает решение кинетической задачи.
Кинетика сложных реакций Большинство химических реакций являются сложными, т. е. состоят из нескольких элементарных стадий. Несмотря на большое разнообразие сложных реакций, их можно свести к комбинации нескольких типов: односторонних, обратимых, параллельных и последовательных реакций. Условие квазистационарности, введенное в кинетику Боденштейном означает, что образующиеся в сложной реакции промежуточные вещества вступают в дальнейшие взаимодействия так быстро, что их концентрации в ходе процесса остаются неизменными, т. е. (2. 41) где Сi – концентрация некоторого промежуточного вещества. Это условие позволяет перейти к рассмотрению алгебраических уравнений вместо дифференциальных, что существенно упрощает решение кинетической задачи.
 Двусторонние реакции Двусторонними (обратимыми) в кинетике называют реакции, которые протекаю одновременно в противоположных направлениях. Суммарная скорость процесса находится как разность скоростей прямой ( 1) и обратной ( – 1) реакций. = 1 - – 1 (2. 42) Если скорости прямой и обратной реакций становятся равными 1 = – 1, то наступает химическое равновесие. Понятие двусторонних реакций не соответствует термодинамическому термину "обратимый процесс". Двусторонние химические реакции могут быть названы термодинамически обратимыми только вблизи равновесия. а) Рассмотрим наиболее простую двустороннюю реакцию первого порядка. протекающую в закрытой системе с постоянным объемом. А В
Двусторонние реакции Двусторонними (обратимыми) в кинетике называют реакции, которые протекаю одновременно в противоположных направлениях. Суммарная скорость процесса находится как разность скоростей прямой ( 1) и обратной ( – 1) реакций. = 1 - – 1 (2. 42) Если скорости прямой и обратной реакций становятся равными 1 = – 1, то наступает химическое равновесие. Понятие двусторонних реакций не соответствует термодинамическому термину "обратимый процесс". Двусторонние химические реакции могут быть названы термодинамически обратимыми только вблизи равновесия. а) Рассмотрим наиболее простую двустороннюю реакцию первого порядка. протекающую в закрытой системе с постоянным объемом. А В
 Примером такой реакции является изомеризация, в частности превращение тиоцианата аммония в тиомочевину : NH 4 NCS (NH 2)2 CS С учетом выражений (2. 5) и (2. 42) скорость прямой реакции 1 = k 1 (a – x) скорость обратной реакции – 1 = k – 1 (b + x) суммарная скорость двусторонней реакции = 1 - – 1 = k 1 (a – x) – k – 1 (b + x), (2. 43) где a и b – исходные концентрации веществ А и В, т. е. в начальный момент времени t = 0; х – число моль вещества А, прореагировавшего к моменту времени t в единице объема, т. е. х – степень превращения. Согласно (1. 6) скорость реакции
Примером такой реакции является изомеризация, в частности превращение тиоцианата аммония в тиомочевину : NH 4 NCS (NH 2)2 CS С учетом выражений (2. 5) и (2. 42) скорость прямой реакции 1 = k 1 (a – x) скорость обратной реакции – 1 = k – 1 (b + x) суммарная скорость двусторонней реакции = 1 - – 1 = k 1 (a – x) – k – 1 (b + x), (2. 43) где a и b – исходные концентрации веществ А и В, т. е. в начальный момент времени t = 0; х – число моль вещества А, прореагировавшего к моменту времени t в единице объема, т. е. х – степень превращения. Согласно (1. 6) скорость реакции
 (2. 43) где a и b – исходные концентрации веществ А и В, т. е. в начальный момент времени t = 0; х – число моль вещества А, прореагировавшего к моменту времени t в единице объема, т. е. х – степень превращения. Согласно (1. 6) скорость реакции (2. 43) Объединяя выражения (2. 42) и (2. 43) можно дифференциальное кинетическое уравнение k 1 (a – x) – k – 1 (b + x). Преобразуем его Обозначим через А = k 1 a – k – 1 b – (k 1 + k – 1)x = (k 1 + k – 1) = const, (2. 45) записать (2. 44) следующее
(2. 43) где a и b – исходные концентрации веществ А и В, т. е. в начальный момент времени t = 0; х – число моль вещества А, прореагировавшего к моменту времени t в единице объема, т. е. х – степень превращения. Согласно (1. 6) скорость реакции (2. 43) Объединяя выражения (2. 42) и (2. 43) можно дифференциальное кинетическое уравнение k 1 (a – x) – k – 1 (b + x). Преобразуем его Обозначим через А = k 1 a – k – 1 b – (k 1 + k – 1)x = (k 1 + k – 1) = const, (2. 45) записать (2. 44) следующее
 тогда (k 1 + k – 1)(А - x) (2. 44') Так как А – постоянная величина для данной реакции, то в уравнении (2. 44/) можно разделить переменные и проинтегрировать в пределах от 0 до х и от 0 до t. После интегрирования получаем кинетическое уравнение в интегральном виде k 1 + k – 1 = или = (k 1 + k- – 1)t (2. 46) Уравнение (2. 46) аналогично уравнению односторонней реакции первого порядка (2. 8). Для нахождения суммы констант скоростей прямой и обратной реакций надо знать А.
тогда (k 1 + k – 1)(А - x) (2. 44') Так как А – постоянная величина для данной реакции, то в уравнении (2. 44/) можно разделить переменные и проинтегрировать в пределах от 0 до х и от 0 до t. После интегрирования получаем кинетическое уравнение в интегральном виде k 1 + k – 1 = или = (k 1 + k- – 1)t (2. 46) Уравнение (2. 46) аналогично уравнению односторонней реакции первого порядка (2. 8). Для нахождения суммы констант скоростей прямой и обратной реакций надо знать А.
 Преобразуем выражение (2. 45), разделив и числитель, и знаменатель на k -1 где k 1/k – 1 = Kc (константа равновесия). В момент равновесия = 0, т. е. из (2. 44) получаем k 1 (a – x ) = k – 1 (b + x ). Тогда константу равновесия Кс можно определить из выражения Кс = , (2. 47) зная начальные концентрации веществ а и в и х - количество вещества А, разложившегося к моменту установления равновесия. Найдем из (2. 47)
Преобразуем выражение (2. 45), разделив и числитель, и знаменатель на k -1 где k 1/k – 1 = Kc (константа равновесия). В момент равновесия = 0, т. е. из (2. 44) получаем k 1 (a – x ) = k – 1 (b + x ). Тогда константу равновесия Кс можно определить из выражения Кс = , (2. 47) зная начальные концентрации веществ а и в и х - количество вещества А, разложившегося к моменту установления равновесия. Найдем из (2. 47)
 х = , т. е. х = А Кинетическое уравнение (2. 46) для двусторонней реакции первого порядка теперь можно записать в виде. (2. 46') Таким образом, определив экспериментально Кс и х , можно вычислить отдельно k 1 и k -1. Двусторонние реакции второго порядка CH 3 CHOC 2 H 5 + H 2 O CH 3 COOH + C 2 H 5 OH. В общем виде А+В С+D Скорость такой реакции: = = 1 - -1 = k 1 САСВ – k – 1 СССD (2. 48) где СА, СВ, СС, СD – концентрации реагентов к моменту времени t; х – степень превращения.
х = , т. е. х = А Кинетическое уравнение (2. 46) для двусторонней реакции первого порядка теперь можно записать в виде. (2. 46') Таким образом, определив экспериментально Кс и х , можно вычислить отдельно k 1 и k -1. Двусторонние реакции второго порядка CH 3 CHOC 2 H 5 + H 2 O CH 3 COOH + C 2 H 5 OH. В общем виде А+В С+D Скорость такой реакции: = = 1 - -1 = k 1 САСВ – k – 1 СССD (2. 48) где СА, СВ, СС, СD – концентрации реагентов к моменту времени t; х – степень превращения.
 В простейшем случае, когда при t = 0 СА = СВ = а; С С = СD = 0 (*) = k 1(а - х)2 – k -1 х2 (2. 48') Путем преобразований из (2. 48') получаем = (k 1 – k – 1)(m 1 – x)(m 2 – x) (2. 49) где m 1 и m 2 – корни квадратного уравнения х2 - 2 х+ =0 . Или х2 - 2 Интегрирование дифференциального кинетического уравнения (2. 49) дает выражение k 1 – k – 1 = (2. 50) которое является интегральным кинетическим уравнением двусторонних реакций при условии (*).
В простейшем случае, когда при t = 0 СА = СВ = а; С С = СD = 0 (*) = k 1(а - х)2 – k -1 х2 (2. 48') Путем преобразований из (2. 48') получаем = (k 1 – k – 1)(m 1 – x)(m 2 – x) (2. 49) где m 1 и m 2 – корни квадратного уравнения х2 - 2 х+ =0 . Или х2 - 2 Интегрирование дифференциального кинетического уравнения (2. 49) дает выражение k 1 – k – 1 = (2. 50) которое является интегральным кинетическим уравнением двусторонних реакций при условии (*).
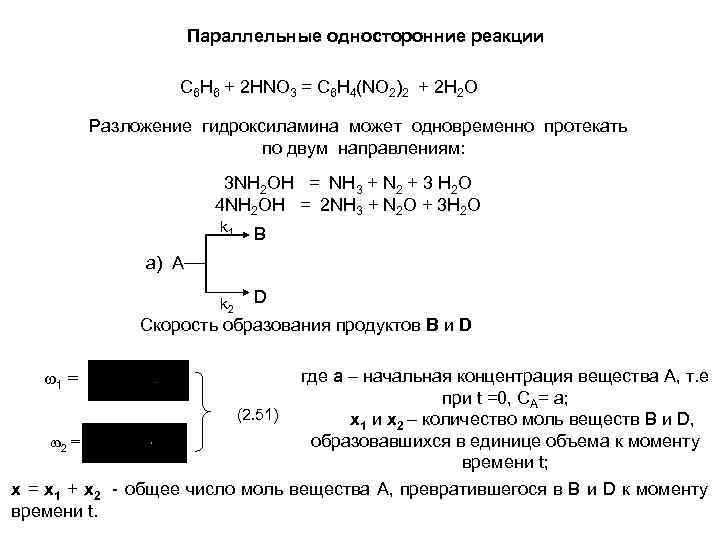 Параллельные односторонние реакции C 6 H 6 + 2 HNO 3 = C 6 H 4(NO 2)2 + 2 H 2 O Разложение гидроксиламина может одновременно протекать по двум направлениям: 3 NH 2 OH = NH 3 + N 2 + 3 H 2 O 4 NH 2 OH = 2 NH 3 + N 2 O + 3 H 2 O k 1 В а) А k 2 D Скорость образования продуктов В и D 1 = 2 = х1 + х2 времени t. где а – начальная концентрация вещества А, т. е при t =0, СА= а; (2. 51) х1 и х2 – количество моль веществ B и D, образовавшихся в единице объема к моменту времени t; - общее число моль вещества А, превратившегося в В и D к моменту
Параллельные односторонние реакции C 6 H 6 + 2 HNO 3 = C 6 H 4(NO 2)2 + 2 H 2 O Разложение гидроксиламина может одновременно протекать по двум направлениям: 3 NH 2 OH = NH 3 + N 2 + 3 H 2 O 4 NH 2 OH = 2 NH 3 + N 2 O + 3 H 2 O k 1 В а) А k 2 D Скорость образования продуктов В и D 1 = 2 = х1 + х2 времени t. где а – начальная концентрация вещества А, т. е при t =0, СА= а; (2. 51) х1 и х2 – количество моль веществ B и D, образовавшихся в единице объема к моменту времени t; - общее число моль вещества А, превратившегося в В и D к моменту
 Общая скорость превращения вещества А по двум направлениям = = k 1(a – x) + k 2(a – x) = (k 1 + k 2)(a - x) (2. 52) После интегрирования в пределах от 0 до а и от 0 до t k 1 + k 2 = (2. 53) Из этого уравнения можно определить сумму констант скоростей (k 1 + k 2). Разделим одно из уравнений (2. 51) на другое , , т. е. k 2 dx 1 = k 1 dx 2 После интегрирования получаем k 2 x 1 = k 1 x 2. Откуда т. е. отношение констант скоростей двух параллельных реакций равно отношению концентраций образующихся продуктов.
Общая скорость превращения вещества А по двум направлениям = = k 1(a – x) + k 2(a – x) = (k 1 + k 2)(a - x) (2. 52) После интегрирования в пределах от 0 до а и от 0 до t k 1 + k 2 = (2. 53) Из этого уравнения можно определить сумму констант скоростей (k 1 + k 2). Разделим одно из уравнений (2. 51) на другое , , т. е. k 2 dx 1 = k 1 dx 2 После интегрирования получаем k 2 x 1 = k 1 x 2. Откуда т. е. отношение констант скоростей двух параллельных реакций равно отношению концентраций образующихся продуктов.
 C B D A 0 t Зависимость концентраций исходного вещества А и продуктов реакции В и Д от времени б) Для двух параллельных односторонних реакций второго порядка получаем уравнение k 1 А+В k 2 С D , (2. 54) где а и в – начальные концентрации исходных веществ А и В. (2. 54/) Полученное выражение аналогично кинетическому уравнению односторонних реакций второго порядка (2. 25).
C B D A 0 t Зависимость концентраций исходного вещества А и продуктов реакции В и Д от времени б) Для двух параллельных односторонних реакций второго порядка получаем уравнение k 1 А+В k 2 С D , (2. 54) где а и в – начальные концентрации исходных веществ А и В. (2. 54/) Полученное выражение аналогично кинетическому уравнению односторонних реакций второго порядка (2. 25).
 Односторонние последовательные (консекутивные) реакции Две реакции называются последовательными, если продукты первой реакции являются исходными веществами для другой. Рассмотрим наиболее простой случай двух последовательных односторонних реакций первого порядка. (k 1 k 2) Пусть в начальный момент времени t = 0 концентрации веществ: СА = а, СВ = СD = 0. Если к моменту времени t в единице объема прореагирует х моль вещества А, причем у моль из них превратится в вещество D, то концентрации веществ к этому моменту t станут: СА = а – х, СВ = х – у, СD = у. Тогда скорость химической реакции по каждому из веществ А, В, D будет равна: (а) б)
Односторонние последовательные (консекутивные) реакции Две реакции называются последовательными, если продукты первой реакции являются исходными веществами для другой. Рассмотрим наиболее простой случай двух последовательных односторонних реакций первого порядка. (k 1 k 2) Пусть в начальный момент времени t = 0 концентрации веществ: СА = а, СВ = СD = 0. Если к моменту времени t в единице объема прореагирует х моль вещества А, причем у моль из них превратится в вещество D, то концентрации веществ к этому моменту t станут: СА = а – х, СВ = х – у, СD = у. Тогда скорость химической реакции по каждому из веществ А, В, D будет равна: (а) б)
 в) Решение уравнения (а) нам известно. Учитывая (2. 8//), получим (2. 55) Уравнение (б) преобразуем к виду Разделим переменные и умножим все слагаемые на (б/) или После интегрирования уравнения (б/) в пределах от 0 до СВ получим Откуда (2. 55/) Ввиду того, что обе стадии мономолекулярные и исчезновение в результате реакции молекул А приводит к образованию такого же количества молекул В и D, выполняется равенство: СА + СВ + СD = а,
в) Решение уравнения (а) нам известно. Учитывая (2. 8//), получим (2. 55) Уравнение (б) преобразуем к виду Разделим переменные и умножим все слагаемые на (б/) или После интегрирования уравнения (б/) в пределах от 0 до СВ получим Откуда (2. 55/) Ввиду того, что обе стадии мономолекулярные и исчезновение в результате реакции молекул А приводит к образованию такого же количества молекул В и D, выполняется равенство: СА + СВ + СD = а,
 (2. 55//) Полученные уравнения (2. 55, 2. 55//) выражают зависимость концентрации исходного (А), промежуточного (В) и конечного (D) веществ от времени Концентрация промежуточного вещества В со временем сначала увеличивается, в момент времени tm достигает максимума, а затем уменьшается. Время tm находят из условия экстремума т. е. Откуда k 2/k 1 = . (2. 56). (СВ)max определяется отношением констант скоростей k 2/k 1. Чем больше = k 2/k 1, тем выше лежит максимум на кривой CB = f(t) и тем ближе он к началу координат.
(2. 55//) Полученные уравнения (2. 55, 2. 55//) выражают зависимость концентрации исходного (А), промежуточного (В) и конечного (D) веществ от времени Концентрация промежуточного вещества В со временем сначала увеличивается, в момент времени tm достигает максимума, а затем уменьшается. Время tm находят из условия экстремума т. е. Откуда k 2/k 1 = . (2. 56). (СВ)max определяется отношением констант скоростей k 2/k 1. Чем больше = k 2/k 1, тем выше лежит максимум на кривой CB = f(t) и тем ближе он к началу координат.
 ХИМИЧЕСКИЕ РЕАКЦИИ В ОТКРЫТЫХ СИСТЕМАХ Имеются две модели реакторов: идеального смешения и идеального вытеснения Пусть в реакторе идеального смешения протекает жидкофазная реакция. А продукты Изменение концентрации исходного вещества А в единицу времени (3. 1) Для мономолекулярных реакций где - скорость подачи вещества А в реактор и вывода продуктов из него; С 0, А, СА – исходная и текущая концентрация вещества А; А – скорость превращения А в продукты; V – объем реактора. Через некоторое время от начала процесса в открытой системе устанавливается стационарный режим, т. е. (3. 2/) где СА, ст – концентрация А, отвечающая стационарному режиму.
ХИМИЧЕСКИЕ РЕАКЦИИ В ОТКРЫТЫХ СИСТЕМАХ Имеются две модели реакторов: идеального смешения и идеального вытеснения Пусть в реакторе идеального смешения протекает жидкофазная реакция. А продукты Изменение концентрации исходного вещества А в единицу времени (3. 1) Для мономолекулярных реакций где - скорость подачи вещества А в реактор и вывода продуктов из него; С 0, А, СА – исходная и текущая концентрация вещества А; А – скорость превращения А в продукты; V – объем реактора. Через некоторое время от начала процесса в открытой системе устанавливается стационарный режим, т. е. (3. 2/) где СА, ст – концентрация А, отвечающая стационарному режиму.
 Для мономолекулярных реакций А 1 А 2 А = k 1 C 1 и выражение (3. 1) запишется в виде (3. 3//) Интегрирование уравнения (3. 3//) при начальных условиях t = 0 и С 1 = С 0, 1 в пределах от t = 0 до t дает (3. 4) Из зависимости концентрации А 1 в реакторе от времени при заданной скорости подачи и объеме реактора V (3. 4) следует, что С 1 нарастает и при t достигает постоянного значения C 1, ст (3. 5) При протекании мономолекулярной двусторонней реакции А 1 A 2 в реакторе идеального смешения устанавливается стационарный режим. Если вещество А 2 не вводится в реактор (С 0, 2 = 0), отношения стационарных концентраций продукта и исходного вещества
Для мономолекулярных реакций А 1 А 2 А = k 1 C 1 и выражение (3. 1) запишется в виде (3. 3//) Интегрирование уравнения (3. 3//) при начальных условиях t = 0 и С 1 = С 0, 1 в пределах от t = 0 до t дает (3. 4) Из зависимости концентрации А 1 в реакторе от времени при заданной скорости подачи и объеме реактора V (3. 4) следует, что С 1 нарастает и при t достигает постоянного значения C 1, ст (3. 5) При протекании мономолекулярной двусторонней реакции А 1 A 2 в реакторе идеального смешения устанавливается стационарный режим. Если вещество А 2 не вводится в реактор (С 0, 2 = 0), отношения стационарных концентраций продукта и исходного вещества
 (3. 6) не зависит от времени. Т. е. при определенных и V (С 2/С 1)ст – величина постоянная, но не равная константе равновесия. В реакторе идеального вытеснения реакционная смесь движется так, что перемешивание вдоль реактора отсутствует. Для жидкофазной мономолекулярной односторонней реакции, протекающей в реакторе идеального вытеснения в стационарном режиме, было получено кинетическое уравнение (3. 7) где – координата вдоль реактора; S – его сечение; – скорость подачи вещества А 1 Интегрирование уравнения (3. 7) в пределах от 0 до L (длина реактора) дает выражение для концентрации А 1 на выходе из реактора. Так как LS – объем реактора V, то (3. 8) Уравнение (3. 8) позволяет рассчитать, например, скорость подачи реагента при заданной концентрации его на выходе из реактора.
(3. 6) не зависит от времени. Т. е. при определенных и V (С 2/С 1)ст – величина постоянная, но не равная константе равновесия. В реакторе идеального вытеснения реакционная смесь движется так, что перемешивание вдоль реактора отсутствует. Для жидкофазной мономолекулярной односторонней реакции, протекающей в реакторе идеального вытеснения в стационарном режиме, было получено кинетическое уравнение (3. 7) где – координата вдоль реактора; S – его сечение; – скорость подачи вещества А 1 Интегрирование уравнения (3. 7) в пределах от 0 до L (длина реактора) дает выражение для концентрации А 1 на выходе из реактора. Так как LS – объем реактора V, то (3. 8) Уравнение (3. 8) позволяет рассчитать, например, скорость подачи реагента при заданной концентрации его на выходе из реактора.


