lek_3.ppt
- Количество слайдов: 12
 Методы определения концентрации растворов 1
Методы определения концентрации растворов 1
 Фотометрические методы определения концентрации веществ В зависимости от способа регистрации поглощения выделяют две группы методов: 1. визуальные, где регистрирующее устройство – глаз; 2. фотоэлектрические – регистрация аналитического сигнала осуществляется с помощью прибора. 2
Фотометрические методы определения концентрации веществ В зависимости от способа регистрации поглощения выделяют две группы методов: 1. визуальные, где регистрирующее устройство – глаз; 2. фотоэлектрические – регистрация аналитического сигнала осуществляется с помощью прибора. 2
 Фотометрические методы определения концентрации веществ Фотоэлектрические методы определения концентрации делятся на две группы: I. Абсолютные – аналитический сигнал (оптическая плотность) фиксируется по сравнению с нулевым раствором, не содержащим определяемый компонент. II. Дифференциальные – в качестве нулевого раствора используют какой-либо стандартный раствор определяемого вещества. I. Абсолютные а) Расчет по ε б) Метод сравнения оптических плотностей стандартного и исследуемого раствора (21) (22) 3
Фотометрические методы определения концентрации веществ Фотоэлектрические методы определения концентрации делятся на две группы: I. Абсолютные – аналитический сигнал (оптическая плотность) фиксируется по сравнению с нулевым раствором, не содержащим определяемый компонент. II. Дифференциальные – в качестве нулевого раствора используют какой-либо стандартный раствор определяемого вещества. I. Абсолютные а) Расчет по ε б) Метод сравнения оптических плотностей стандартного и исследуемого раствора (21) (22) 3
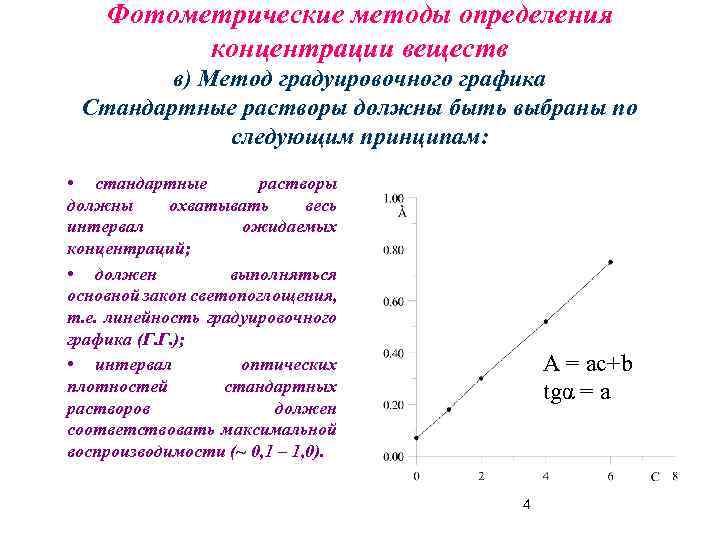 Фотометрические методы определения концентрации веществ в) Метод градуировочного графика Стандартные растворы должны быть выбраны по следующим принципам: • стандартные растворы должны охватывать весь интервал ожидаемых концентраций; • должен выполняться основной закон светопоглощения, т. е. линейность градуировочного графика (Г. Г. ); • интервал оптических плотностей стандартных растворов должен соответствовать максимальной воспроизводимости (~ 0, 1 – 1, 0). А = ас+b tgα = a 4
Фотометрические методы определения концентрации веществ в) Метод градуировочного графика Стандартные растворы должны быть выбраны по следующим принципам: • стандартные растворы должны охватывать весь интервал ожидаемых концентраций; • должен выполняться основной закон светопоглощения, т. е. линейность градуировочного графика (Г. Г. ); • интервал оптических плотностей стандартных растворов должен соответствовать максимальной воспроизводимости (~ 0, 1 – 1, 0). А = ас+b tgα = a 4
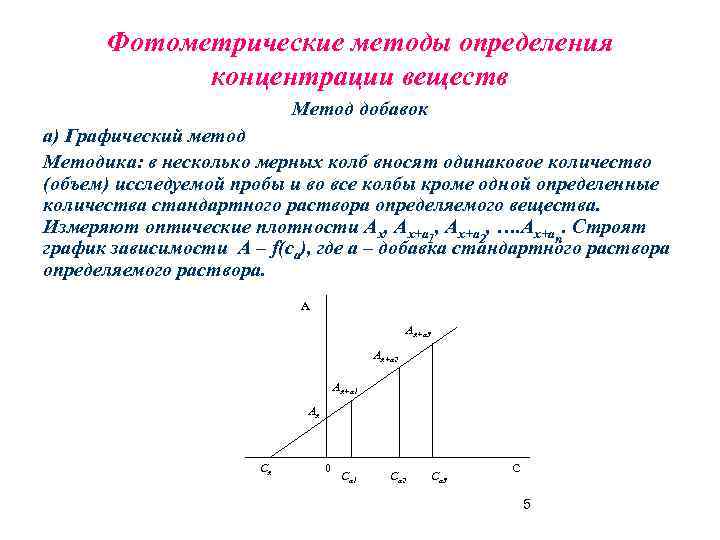 Фотометрические методы определения концентрации веществ Метод добавок а) Графический метод Методика: в несколько мерных колб вносят одинаковое количество (объем) исследуемой пробы и во все колбы кроме одной определенные количества стандартного раствора определяемого вещества. Измеряют оптические плотности Ах, Ах+а 1, Ах+а 2, …. Ах+аn. Строят график зависимости А – f(ca), где а – добавка стандартного раствора определяемого раствора. А Ах+а 3 Ах+а 2 Ах+а 1 Ах Сх 0 Са 1 Са 2 Са 3 С 5
Фотометрические методы определения концентрации веществ Метод добавок а) Графический метод Методика: в несколько мерных колб вносят одинаковое количество (объем) исследуемой пробы и во все колбы кроме одной определенные количества стандартного раствора определяемого вещества. Измеряют оптические плотности Ах, Ах+а 1, Ах+а 2, …. Ах+аn. Строят график зависимости А – f(ca), где а – добавка стандартного раствора определяемого раствора. А Ах+а 3 Ах+а 2 Ах+а 1 Ах Сх 0 Са 1 Са 2 Са 3 С 5
 Фотометрические методы определения концентрации веществ б) расчетный метод (23), (24). 6
Фотометрические методы определения концентрации веществ б) расчетный метод (23), (24). 6
 II. Дифференциальные методы Сущность метода состоит в том, что оптические плотности исследуемого и стандартного растворов измеряются не по отношению к чистому растворителю с нулевым поглощением, а по отношению к окрашенному раствору определяемого элемента с концентрацией Со, близкой к концентрации исследуемого раствора. а) Графический вариант Методика: также как и для ГГ готовят серию стандартных растворов определяемого вещества; в качестве раствора сравнения выбирают стандартный раствор с минимальной концентрацией Со. б)Расчетный вариант (26), (25), (27). 7
II. Дифференциальные методы Сущность метода состоит в том, что оптические плотности исследуемого и стандартного растворов измеряются не по отношению к чистому растворителю с нулевым поглощением, а по отношению к окрашенному раствору определяемого элемента с концентрацией Со, близкой к концентрации исследуемого раствора. а) Графический вариант Методика: также как и для ГГ готовят серию стандартных растворов определяемого вещества; в качестве раствора сравнения выбирают стандартный раствор с минимальной концентрацией Со. б)Расчетный вариант (26), (25), (27). 7
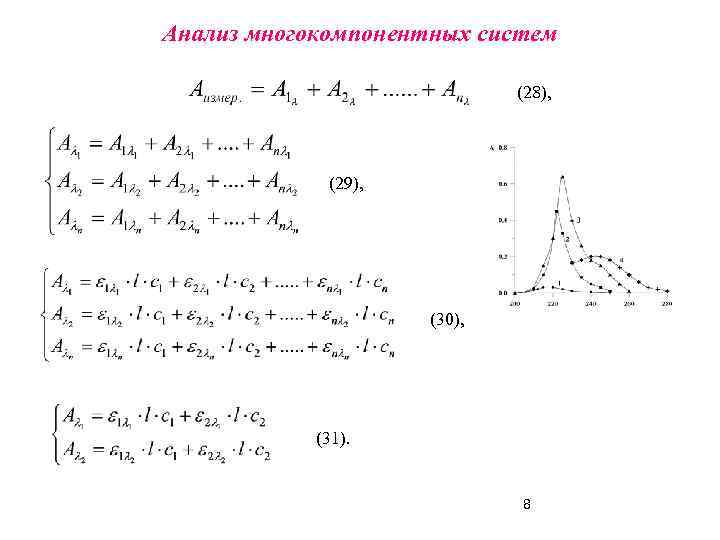 Анализ многокомпонентных систем (28), (29), (30), (31). 8
Анализ многокомпонентных систем (28), (29), (30), (31). 8
 Примеры двухкомпонентных систем 1. Спектры двух компонентов налагаются полностью (32), (33), . 2. Спектры двух компонентов налагаются частично (34) (35) 9
Примеры двухкомпонентных систем 1. Спектры двух компонентов налагаются полностью (32), (33), . 2. Спектры двух компонентов налагаются частично (34) (35) 9
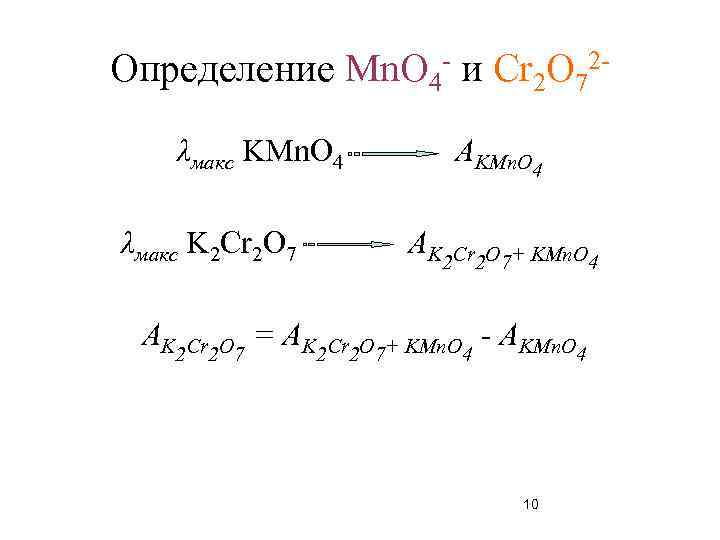 Определение Mn. O 4 - и Cr 2 O 72λмакс KMn. O 4 λмакс K 2 Cr 2 O 7 АKMn. O 4 АK 2 Cr 2 O 7+ KMn. O 4 АK 2 Cr 2 O 7 = АK 2 Cr 2 O 7+ KMn. O 4 - АKMn. O 4 10
Определение Mn. O 4 - и Cr 2 O 72λмакс KMn. O 4 λмакс K 2 Cr 2 O 7 АKMn. O 4 АK 2 Cr 2 O 7+ KMn. O 4 АK 2 Cr 2 O 7 = АK 2 Cr 2 O 7+ KMn. O 4 - АKMn. O 4 10
 Метод изомолярных серий Условия использования метода: 1) компоненты фотометрической реакции и образующееся КС поглощают в разных областях спектра; 2) в системе образуется только одно КС; 3) образуется достаточно устойчивое КС; 4) ионная сила растворов изомолярной серии сохраняется постоянной; 5) химическая реакция между реагирующими веществами не осложняется никакими побочными процессами. А или [Mm. Rn] x = CR/(CM+CR) 11
Метод изомолярных серий Условия использования метода: 1) компоненты фотометрической реакции и образующееся КС поглощают в разных областях спектра; 2) в системе образуется только одно КС; 3) образуется достаточно устойчивое КС; 4) ионная сила растворов изомолярной серии сохраняется постоянной; 5) химическая реакция между реагирующими веществами не осложняется никакими побочными процессами. А или [Mm. Rn] x = CR/(CM+CR) 11
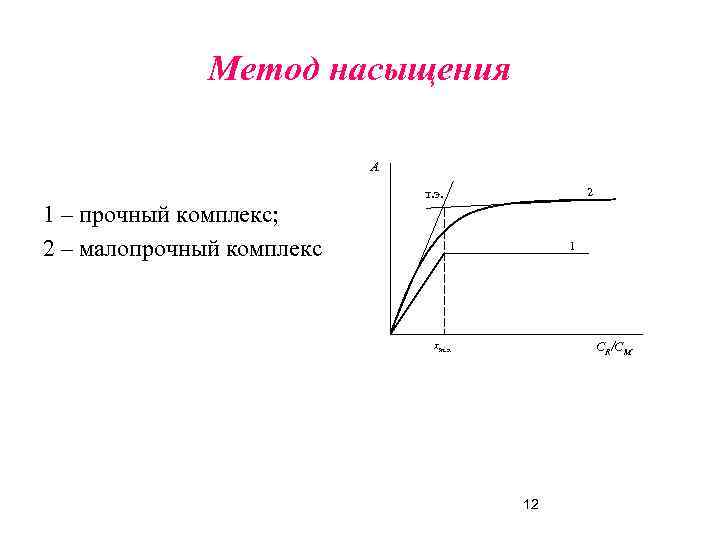 Метод насыщения А 1 – прочный комплекс; 2 – малопрочный комплекс 2 т. э. 1 хт. э. СR/CM 12
Метод насыщения А 1 – прочный комплекс; 2 – малопрочный комплекс 2 т. э. 1 хт. э. СR/CM 12


