Методы определения белка.ppt
- Количество слайдов: 23

Методы определения белка

Цветные реакции на белки и аминокислоты • Белки при взаимодействии с некоторыми химическими веществами дают окрашенные соединения. • Образование этих соединений происходит при участии радикалов аминокислот, их специфических групп или пептидных связей. • Цветные реакции позволяют установить наличие белка в биологическом объекте или растворе и доказать присутствие определенных аминокислот в белковой молекуле. • На основе цветных реакций разработаны некоторые методы количественного определения белков и аминокислот.

• Универсальными считают биуретовую и нингидриновую реакции, так как их дают все белки. • Ксантопротеиновая реакция, реакция Фоля и др. являются специфическими, так как они обусловлены радикальными группами определенных аминокислот в молекуле белка.

БИУРЕТОВАЯ РЕАКЦИЯ • Реакция обусловлена наличием в белках, пептидах, полипептидах пептидных связей, которые в щелочной среде образуют с ионами меди (II) комплексные соединения, окрашенные в фиолетовый (с красным или с синим оттенком) цвет. • Окраска обусловлена наличием в молекуле не менее двух групп -CO-NH-, связанных непосредственно между собой или при участии атома углерода или азота.

Основные методы, используемые для исследования белков • 1. Получение белков в чистом виде. Критерии гомогенности – • одна полоса при проведении ЭФ (желательно двумерного), • одна полоса при центрифугировании. • • 2. Характеристика белка и его идентификация: определение молекулярной массы, выявление небелковых компонентов (ионы металлов, липиды, углеводы), определение N-концевой последовательности, определение аминокислотного состава и аминокислотной последовательности, масс-спектрометрия самого белка и продуктов его протеолиза, кристаллизация белка и рентгеноструктурный анализ.

Денатурация белка • Потеря белком своей вторичной, третичной и четвертичной структуры называется денатурацией • Денатурация бывает полной или частичной, обратимой и необратимой. • Денатурацию может вызвать нагревание, другие физические факторы, изменение ионного состава среды

• Все, что связано с приготовлением мясной пищи, – это необратимая денатурация белков. Приготовление творога – тоже необратимая денатурация, сопровождающаяся склеиванием молекул казеина, – коагуляцией. • Денатурация в некоторых случаях обратима, как в случае осаждения (преципитаци и) водорастворимых белков с помощью солей аммония, и используется как способ их очистки

Денатурация белка • Как правило, белки сохраняют структуру и, следовательно, физико-химические свойства, например, растворимость в условиях, таких как температура и p. H, к которым приспособлен данный организм. • Изменение этих условий, например, нагревание или обработка белка кислотой или щёлочью, приводит к потере четвертичной, третичной и вторичной структур белка.


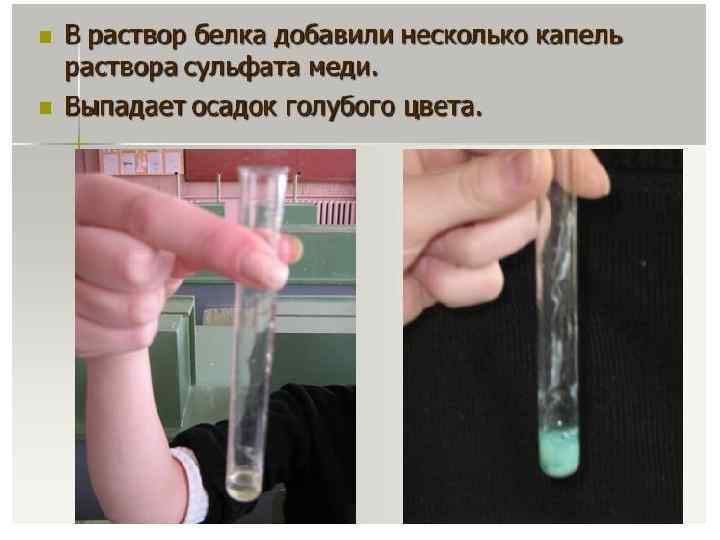

• Первичная структура белка при денатурации сохраняется. • Денатурация может быть обратимой (ренатурация) и необратимой. • Пример необратимой денатурации при тепловом воздействии – свертывание яичного альбумина при варке яиц. • Денатурация может быть полной или частичной, обратимой или необратимой. • Денатурация в некоторых случаях обратима, как в случае осаждения (преципитации) водорастворимых белков с помощью солей аммония, и используется как способ их очистки.

Гидролиз белков • – разрушение первичной структуры белка под действием кислот, щелочей или ферментов, приводящее к образованию a- аминокислот, из которых он был составлен.

Функция качественных реакций Для аминокислот, постоянно встречающихся в составе белков, разработано множество цветных (в том числе именных) реакций. Многие из них высокоспецифичны, что позволяет определять ничтожные количества той или иной аминокислоты. • Надо помнить, что все качественные реакции – это реакции не собственно на белки, а на определенные аминокислоты, входящие в их состав

Качественные реакции на белки • a) Биуретовая реакция – фиолетовое окрашивание при действии солей меди (II) в щелочном растворе. • Такую реакцию дают все соединения, содержащие пептидную связь.

Качественные реакции на белки • Ксантопротеиновая реакция – появление желтого окрашивания при действии концентрированной азотной кислоты на белки, содержащие остатки ароматических и гетероциклических аминокислот (фенилаланина, тирозина, гистидина)

Нингидриновая реакция • Аминокислота с нингидрином образует продукт конденсации типа азометина • 2 -аминоиндандион реагирует с нингидрином и дает краситель. • НИНГИДРИНОВАЯ РЕАКЦИЯ неспецифична, т. к. окрашенный продукт с нингидрином дают также NH 3 и др. соединение, содержащие аминогруппу (в т. ч. белки и пептиды). • Однако реакции с этими соединение осуществляются без выделения СО 2 (с выделением СО 2 специфична только для a-аминокислот). • Реакцию используют для колориметрического количественного определения a-аминокислот, в том числе в автоматических аминокислотных анализаторах.
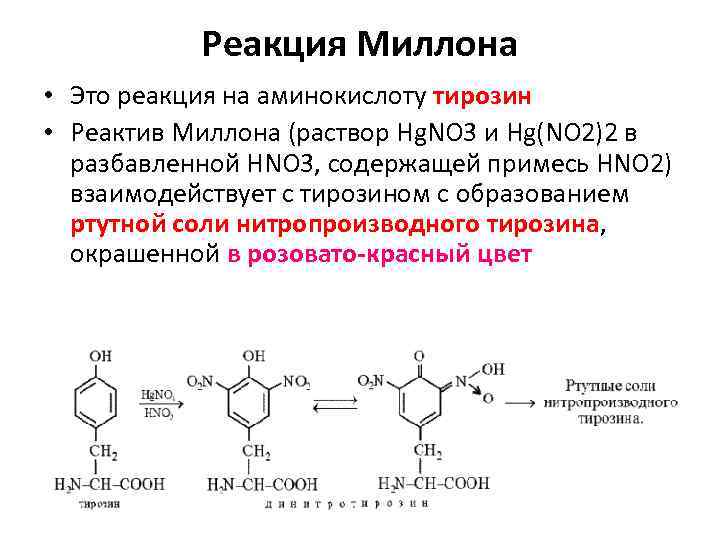
Реакция Миллона • Это реакция на аминокислоту тирозин • Реактив Миллона (раствор Hg. NO 3 и Hg(NO 2)2 в разбавленной HNO 3, содержащей примесь HNO 2) взаимодействует с тирозином с образованием ртутной соли нитропроизводного тирозина, окрашенной в розовато-красный цвет

Реакция Гопкинса–Коле Эта реакция определяет аминокислоту триптофан. • Из глиоксиловой кислоты под действием концентрированной серной кислоты сначала получается формальдегид, который затем конденсируется с триптофаном. Продукт конденсации окисляется до бис-2 триптофанилкарбинола, который в присутствии минеральных кислот образует соли, окрашенные в синефиолетовый цвет: • Наблюдается образование сине-фиолетового окрашивания

По общему типу строения белки можно разбить на три группы: • Фибриллярные белки — образуют полимеры, их структура обычно высокорегулярна и поддерживается, в основном, взаимодействиями между разными цепями. Они образуют микрофиламенты, микротрубочки, фибриллы, поддерживают структуру клеток и тканей. К фибриллярным белкам относятся кератин и коллаген.

• Глобулярные белки — водорастворимы, общая форма молекулы более или менее сферическая. Среди глобулярных и фибриллярных белков выделяют подгруппы.

Третичная структура белка (глобулярные белки) Третичная структура белка – способ пространственной укладки полипептидной цепи в глобулу или фибриллу. Поддерживается за счет ковалентных (S-S), гидрофобных, водородных связей

• Мембранные белки — имеют пересекающие клеточную мембрану домены, но части их выступают из мембраны в межклеточное окружение и цитоплазму клетки. Мембранные белки выполняют функцию рецепторов, то есть осуществляют передачу сигналов, а также обеспечивают трансмембранный транспорт различных веществ.
Методы определения белка.ppt