10-NMR-2011.pptx
- Количество слайдов: 18
 Методы Магнитного Резонанса
Методы Магнитного Резонанса
 Ядерный Магнитный Резонанс
Ядерный Магнитный Резонанс
 Нобелевская премия по физике за 1952 год присуждена Феликсу Блоху и Эдварду Пурселлу за «. . . открытие и разработку нового метода исследования ядерного магнетизма. » Феликс Блох Эдвард Пурселл Стэнфордский университет, Стэнфорд, США Гарвардский университет, Кембридж, США
Нобелевская премия по физике за 1952 год присуждена Феликсу Блоху и Эдварду Пурселлу за «. . . открытие и разработку нового метода исследования ядерного магнетизма. » Феликс Блох Эдвард Пурселл Стэнфордский университет, Стэнфорд, США Гарвардский университет, Кембридж, США
 Принцип метода ЯМР Во многом аналогичен принципу метода ЭПР. Заключается в поглощении электромагнитного излучения ядрами атомов, имеющими ненулевой магнитный момент, при их помещении в магнитное поле. -½g. Nb. NH E E = hn DE = 2 m. H=g. Nb. NH H +½g. Nb. NH = hn
Принцип метода ЯМР Во многом аналогичен принципу метода ЭПР. Заключается в поглощении электромагнитного излучения ядрами атомов, имеющими ненулевой магнитный момент, при их помещении в магнитное поле. -½g. Nb. NH E E = hn DE = 2 m. H=g. Nb. NH H +½g. Nb. NH = hn
 Как определить величину магнитного момента ядра? Число протонов (порядковый номер) четный Массовое число (число протонов + число нейтронов) четное Число нейтронов (массовое число – порядковый номер) четное четный нечетное нечетный четное нечетное Спиновое квантовое число I=0 I = 1/ 2 Пример 12 C 6 16 O 8 13 С 6 I = 1/ 2 1 H 1 15 N 7 I=1 14 N 7 2 D 1 Ядро атома будет иметь ненулевой магнитный момент, в том случае, если число протонов или число нейтронов (или оба), будут нечетные.
Как определить величину магнитного момента ядра? Число протонов (порядковый номер) четный Массовое число (число протонов + число нейтронов) четное Число нейтронов (массовое число – порядковый номер) четное четный нечетное нечетный четное нечетное Спиновое квантовое число I=0 I = 1/ 2 Пример 12 C 6 16 O 8 13 С 6 I = 1/ 2 1 H 1 15 N 7 I=1 14 N 7 2 D 1 Ядро атома будет иметь ненулевой магнитный момент, в том случае, если число протонов или число нейтронов (или оба), будут нечетные.
 Энергия ядра в магнитном поле m. N – магнитный момент ядра PN - механический момент ядра I - спиновое квантовое число ядра e. N - заряд протона m. N – масса протона g - гиромагнитное отношение b. N - ядерный магнетон Бора
Энергия ядра в магнитном поле m. N – магнитный момент ядра PN - механический момент ядра I - спиновое квантовое число ядра e. N - заряд протона m. N – масса протона g - гиромагнитное отношение b. N - ядерный магнетон Бора
 Количественные различия между ЭПР и ЯМР
Количественные различия между ЭПР и ЯМР
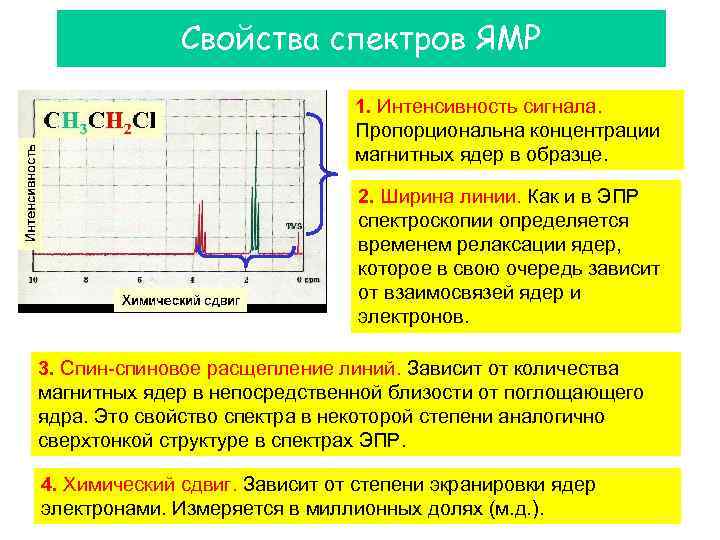 Свойства спектров ЯМР 1. Интенсивность сигнала. Пропорциональна концентрации магнитных ядер в образце. 2. Ширина линии. Как и в ЭПР спектроскопии определяется временем релаксации ядер, которое в свою очередь зависит от взаимосвязей ядер и электронов. 3. Спин-спиновое расщепление линий. Зависит от количества магнитных ядер в непосредственной близости от поглощающего ядра. Это свойство спектра в некоторой степени аналогично сверхтонкой структуре в спектрах ЭПР. 4. Химический сдвиг. Зависит от степени экранировки ядер электронами. Измеряется в миллионных долях (м. д. ).
Свойства спектров ЯМР 1. Интенсивность сигнала. Пропорциональна концентрации магнитных ядер в образце. 2. Ширина линии. Как и в ЭПР спектроскопии определяется временем релаксации ядер, которое в свою очередь зависит от взаимосвязей ядер и электронов. 3. Спин-спиновое расщепление линий. Зависит от количества магнитных ядер в непосредственной близости от поглощающего ядра. Это свойство спектра в некоторой степени аналогично сверхтонкой структуре в спектрах ЭПР. 4. Химический сдвиг. Зависит от степени экранировки ядер электронами. Измеряется в миллионных долях (м. д. ).
 Химический сдвиг CH 3 CH 2 Cl d Электроны, прецессируя вокруг вектора внешнего магнитного поля, создают дополнительное магнитный момент: H'=s*H 0 H' – дополнительный магнитный момент, H 0 – вектор внешнего магнитного поля, s - константа экранирования d Hэфф = H 0 - H' = H 0 – s. H 0 = H 0(1 -s) Химический сдвиг измеряется в относительных единицах, называемых «миллионными долями» (мд или “ppm”) и равен: d = Dn/n 0 *106 = DH/H 0 *106
Химический сдвиг CH 3 CH 2 Cl d Электроны, прецессируя вокруг вектора внешнего магнитного поля, создают дополнительное магнитный момент: H'=s*H 0 H' – дополнительный магнитный момент, H 0 – вектор внешнего магнитного поля, s - константа экранирования d Hэфф = H 0 - H' = H 0 – s. H 0 = H 0(1 -s) Химический сдвиг измеряется в относительных единицах, называемых «миллионными долями» (мд или “ppm”) и равен: d = Dn/n 0 *106 = DH/H 0 *106
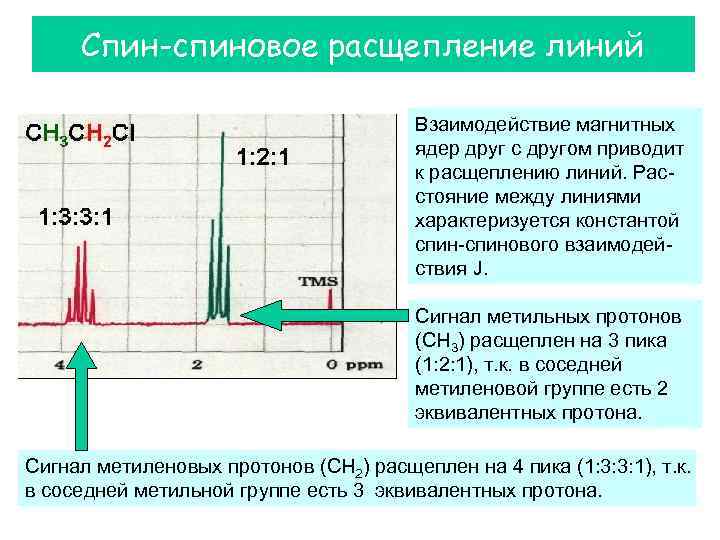 Спин-спиновое расщепление линий Взаимодействие магнитных ядер друг с другом приводит к расщеплению линий. Расстояние между линиями характеризуется константой спин-спинового взаимодействия J. Сигнал метильных протонов (CH 3) расщеплен на 3 пика (1: 2: 1), т. к. в соседней метиленовой группе есть 2 эквивалентных протона. Сигнал метиленовых протонов (CH 2) расщеплен на 4 пика (1: 3: 3: 1), т. к. в соседней метильной группе есть 3 эквивалентных протона.
Спин-спиновое расщепление линий Взаимодействие магнитных ядер друг с другом приводит к расщеплению линий. Расстояние между линиями характеризуется константой спин-спинового взаимодействия J. Сигнал метильных протонов (CH 3) расщеплен на 3 пика (1: 2: 1), т. к. в соседней метиленовой группе есть 2 эквивалентных протона. Сигнал метиленовых протонов (CH 2) расщеплен на 4 пика (1: 3: 3: 1), т. к. в соседней метильной группе есть 3 эквивалентных протона.
 Внешний вид современного ЯМР спектрометра (900 МГц)
Внешний вид современного ЯМР спектрометра (900 МГц)
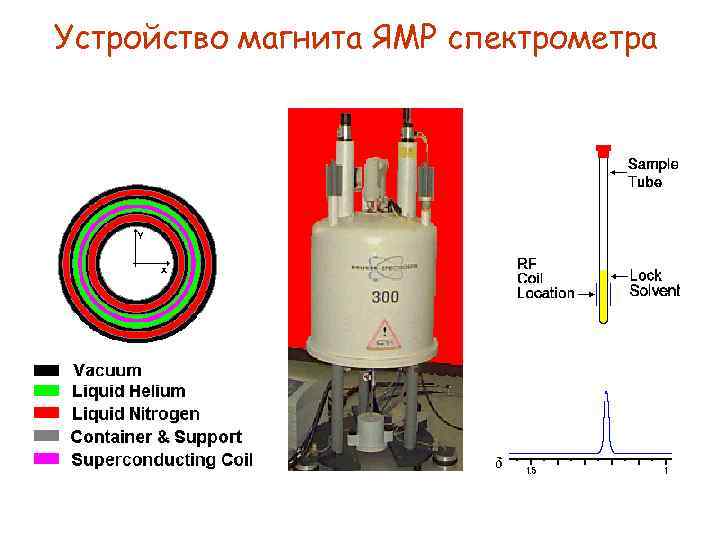 Устройство магнита ЯМР спектрометра
Устройство магнита ЯМР спектрометра
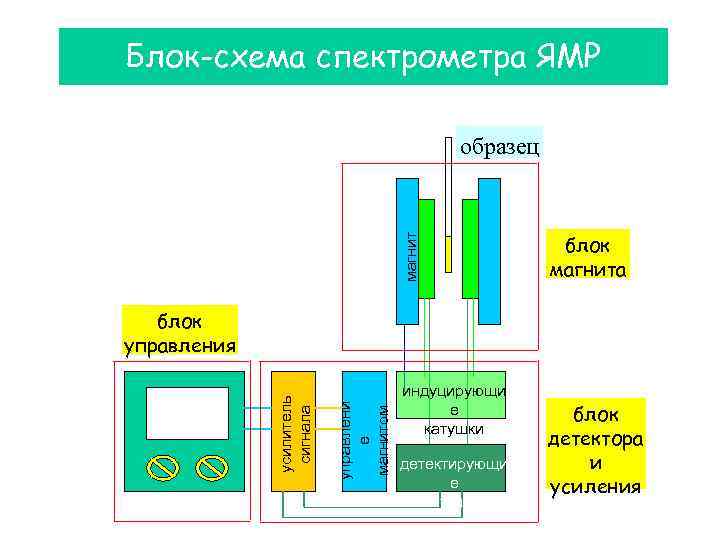 Блок-схема спектрометра ЯМР магнит образец блок магнита управлени е магнитом усилитель сигнала блок управления индуцирующи е катушки детектирующи е катушки блок детектора и усиления
Блок-схема спектрометра ЯМР магнит образец блок магнита управлени е магнитом усилитель сигнала блок управления индуцирующи е катушки детектирующи е катушки блок детектора и усиления
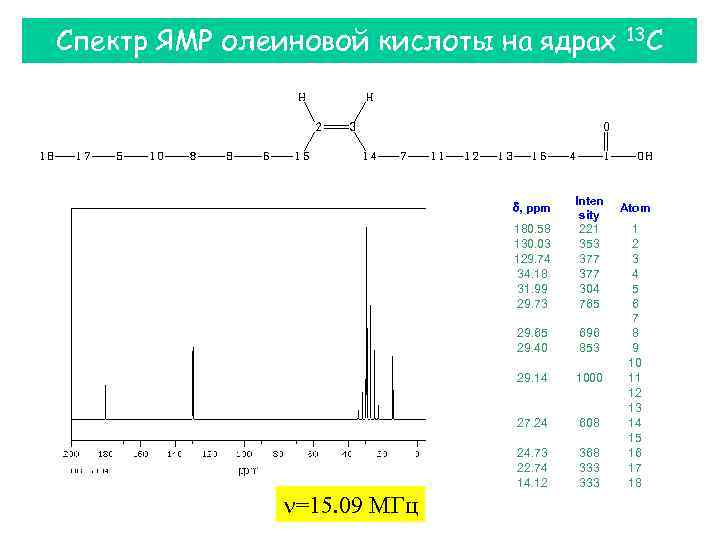 Спектр ЯМР олеиновой кислоты на ядрах 180. 58 130. 03 129. 74 34. 18 31. 99 29. 73 Inten sity 221 353 377 304 765 29. 40 696 853 29. 14 1000 27. 24 608 24. 73 22. 74 14. 12 368 333 d, ppm =15. 09 МГц 13 С Atom 1 2 3 4 5 6 7 8 9 10 11 12 13 14 15 16 17 18
Спектр ЯМР олеиновой кислоты на ядрах 180. 58 130. 03 129. 74 34. 18 31. 99 29. 73 Inten sity 221 353 377 304 765 29. 40 696 853 29. 14 1000 27. 24 608 24. 73 22. 74 14. 12 368 333 d, ppm =15. 09 МГц 13 С Atom 1 2 3 4 5 6 7 8 9 10 11 12 13 14 15 16 17 18
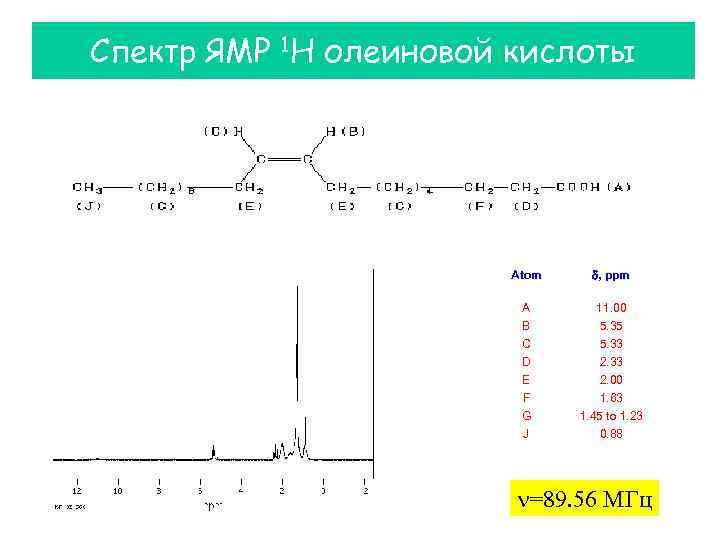 Спектр ЯМР 1 H олеиновой кислоты Atom d, ppm A B 11. 00 5. 35 C D E F G J 5. 33 2. 00 1. 63 1. 45 to 1. 23 0. 88 =89. 56 МГц
Спектр ЯМР 1 H олеиновой кислоты Atom d, ppm A B 11. 00 5. 35 C D E F G J 5. 33 2. 00 1. 63 1. 45 to 1. 23 0. 88 =89. 56 МГц
 Спектр ЯМР 1 H олеиновой кислоты Atom d, ppm A B 5. 34 2. 34 C D E F G J 2. 01 1. 63 1. 35 1. 31 1. 27 0. 88 =399. 65 MHz
Спектр ЯМР 1 H олеиновой кислоты Atom d, ppm A B 5. 34 2. 34 C D E F G J 2. 01 1. 63 1. 35 1. 31 1. 27 0. 88 =399. 65 MHz
 Применение в медико-биологических исследованиях 1. Исследование структуры белков с помощью 1 Н-ЯМР высокого разрешения и Фурье-преобразований. 2. Изучение свойств свободной и связанной воды помощью импульсного 1 Н-ЯМР. 3. 13 С-ЯМР спектроскопия применяется для изучения белков, нуклеиновых кислот и других биологически важных соединений. Обладает большей чувствительностью, чем 1 Н-ЯМР. 4. 31 Р-ЯМР спектроскопия часто применяется для исследования структуры и функций фосфолипидов.
Применение в медико-биологических исследованиях 1. Исследование структуры белков с помощью 1 Н-ЯМР высокого разрешения и Фурье-преобразований. 2. Изучение свойств свободной и связанной воды помощью импульсного 1 Н-ЯМР. 3. 13 С-ЯМР спектроскопия применяется для изучения белков, нуклеиновых кислот и других биологически важных соединений. Обладает большей чувствительностью, чем 1 Н-ЯМР. 4. 31 Р-ЯМР спектроскопия часто применяется для исследования структуры и функций фосфолипидов.
 Рекомендуемая литература: Книги: • Керрингтон Э. и Мак. Лечлан Д. Магнитный резонанс в химии. Издательство «Наука» , 1972 г. • Кантор Л. Р. и Шиммел П. Р. Методы биологической физики. Издательство «Мир» , 1983. Веб-сайт: http: //www. cis. rit. edu/htbooks/nmr
Рекомендуемая литература: Книги: • Керрингтон Э. и Мак. Лечлан Д. Магнитный резонанс в химии. Издательство «Наука» , 1972 г. • Кантор Л. Р. и Шиммел П. Р. Методы биологической физики. Издательство «Мир» , 1983. Веб-сайт: http: //www. cis. rit. edu/htbooks/nmr


