Методы количественного анализа • Количественный


















Методы количественного анализа.ppt
- Количество слайдов: 19
 Методы количественного анализа
Методы количественного анализа
 • Количественный анализ предназначен для определения количественного состава анализируемого вещества.
• Количественный анализ предназначен для определения количественного состава анализируемого вещества.
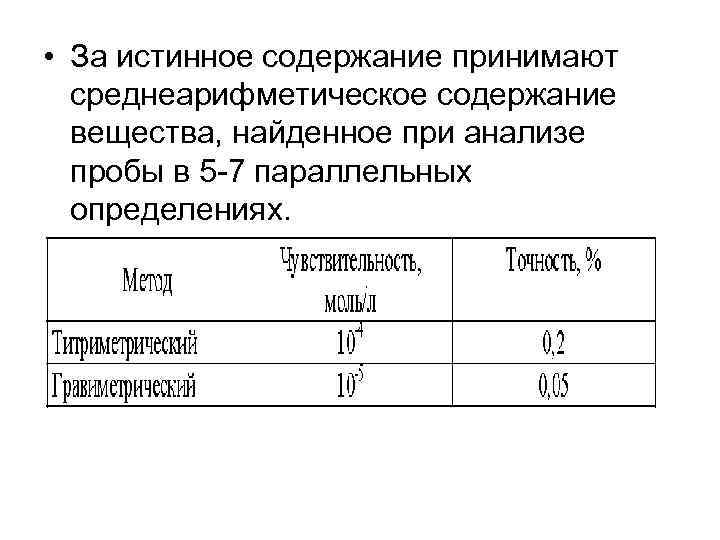
 • Важнейшими характеристиками методов анализа являются их чувствительность и точность. • Чувствительностью метода анализа называют наименьшее количе ство вещества, которое можно достоверно определить данным методом. • Точностью анализа называют относительную ошибку определения, которая представляет собой отношение разности найденного и истинного (х) содержания вещества к истинному содержанию вещества. • Относительную ошибку определения (%) находят по формуле:
• Важнейшими характеристиками методов анализа являются их чувствительность и точность. • Чувствительностью метода анализа называют наименьшее количе ство вещества, которое можно достоверно определить данным методом. • Точностью анализа называют относительную ошибку определения, которая представляет собой отношение разности найденного и истинного (х) содержания вещества к истинному содержанию вещества. • Относительную ошибку определения (%) находят по формуле:
 • За истинное содержание принимают среднеарифметическое содержание вещества, найденное при анализе пробы в 5 7 параллельных определениях.
• За истинное содержание принимают среднеарифметическое содержание вещества, найденное при анализе пробы в 5 7 параллельных определениях.
 Титриметрический анализ • Основан на точном измерении объемов веществ, вступающих в химическую реакцию. • В этом методе используют растворы реактивов точно известной концентрации титранты. • Процесс медленного прибавления титранта к раствору определяемого вещества называется титрованием. • Момент титрования, когда количество прибавленного титранта становится эквивалентным количеству определяемого вещества, называется эквивалентной точкой титрования или точкой эквивалентности. • Ее определяют с помощью индикаторов или по изменению физико химических характеристик титруемого раствора. • Титриметрический анализ отличается быстротой и точностью полученных результатов.
Титриметрический анализ • Основан на точном измерении объемов веществ, вступающих в химическую реакцию. • В этом методе используют растворы реактивов точно известной концентрации титранты. • Процесс медленного прибавления титранта к раствору определяемого вещества называется титрованием. • Момент титрования, когда количество прибавленного титранта становится эквивалентным количеству определяемого вещества, называется эквивалентной точкой титрования или точкой эквивалентности. • Ее определяют с помощью индикаторов или по изменению физико химических характеристик титруемого раствора. • Титриметрический анализ отличается быстротой и точностью полученных результатов.
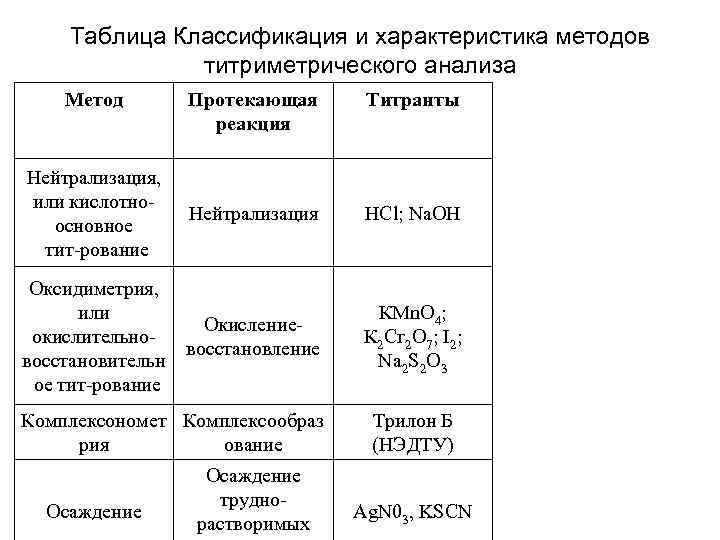
 Таблица Классификация и характеристика методов титриметрического анализа Метод Протекающая Титранты реакция Нейтрализация, или кислотно Нейтрализация НСl; Na. OH основное тит рование Оксидиметрия, или КМn. O 4; Окисление окислительно К 2 Сг 2 О 7; I 2; восстановление восстановительн Na 2 S 2 О 3 ое тит рование Комплексономет Комплексообраз Трилон Б рия ование (НЭДТУ) Осаждение трудно Осаждение Ag. N 03, KSCN растворимых
Таблица Классификация и характеристика методов титриметрического анализа Метод Протекающая Титранты реакция Нейтрализация, или кислотно Нейтрализация НСl; Na. OH основное тит рование Оксидиметрия, или КМn. O 4; Окисление окислительно К 2 Сг 2 О 7; I 2; восстановление восстановительн Na 2 S 2 О 3 ое тит рование Комплексономет Комплексообраз Трилон Б рия ование (НЭДТУ) Осаждение трудно Осаждение Ag. N 03, KSCN растворимых
 Техника выполнения титриметрического анализа 1. Приготовление раствора по точной навеске вещества • Молярные растворы. Для приготовления 1 л 1 М раствора вещества подсчитывают его молекулярную массу и вычисляют массу навески по формуле: где g навеска вещества, г; М молекулярная масса, г; требуемая молярность раствора; V вместимость мерной колбы, мл.
Техника выполнения титриметрического анализа 1. Приготовление раствора по точной навеске вещества • Молярные растворы. Для приготовления 1 л 1 М раствора вещества подсчитывают его молекулярную массу и вычисляют массу навески по формуле: где g навеска вещества, г; М молекулярная масса, г; требуемая молярность раствора; V вместимость мерной колбы, мл.
 • Вычисленную навеску взвешивают на аналитических весах на часовом стекле с точностью до 0, 0001 г и переносят ее в чистую мерную колбу небольшими порциями (обычно для этого используют чистую сухую воронку). Часовое стекло и воронку промывают 3 5 раз дистиллированной водой из промывалки. • Затем колбу заполняют дистиллированной водой на 1/2 ее объема и встряхивают до полного растворения вещества. После этого содержимое колбы доводят до метки водой и тщательно перемешивают. • Пример. Приготовить 0, 5 л 0, 2 М раствора Ag. NO 3. • Вычисляют молекулярную массу нитрата серебра: 169, 875. Подставив это значение в формулу (1), получают массу необходимой навески: •
• Вычисленную навеску взвешивают на аналитических весах на часовом стекле с точностью до 0, 0001 г и переносят ее в чистую мерную колбу небольшими порциями (обычно для этого используют чистую сухую воронку). Часовое стекло и воронку промывают 3 5 раз дистиллированной водой из промывалки. • Затем колбу заполняют дистиллированной водой на 1/2 ее объема и встряхивают до полного растворения вещества. После этого содержимое колбы доводят до метки водой и тщательно перемешивают. • Пример. Приготовить 0, 5 л 0, 2 М раствора Ag. NO 3. • Вычисляют молекулярную массу нитрата серебра: 169, 875. Подставив это значение в формулу (1), получают массу необходимой навески: •
 Нормальные растворы. • Навеску вычисляют по формуле (2) где Э эквивалентная масса вещества, г; N требуемая нормальность раствора; V вместимость мерной колбы, мл.
Нормальные растворы. • Навеску вычисляют по формуле (2) где Э эквивалентная масса вещества, г; N требуемая нормальность раствора; V вместимость мерной колбы, мл.
 • Значение Э находят в табл. В (справочник) • Вычисленную навеску взвешивают и растворяют, как описано выше. • Пример 1. Рассчитать навеску перманганата калия для приготовления 2 л 0, 1 и. раствора. • По табл. В (справочника) находят, что при титровании в кислой среде ЭКМn. О =58, 03/5 = 31, 61 г. Подставив эту величину в формулу (2), получают:
• Значение Э находят в табл. В (справочник) • Вычисленную навеску взвешивают и растворяют, как описано выше. • Пример 1. Рассчитать навеску перманганата калия для приготовления 2 л 0, 1 и. раствора. • По табл. В (справочника) находят, что при титровании в кислой среде ЭКМn. О =58, 03/5 = 31, 61 г. Подставив эту величину в формулу (2), получают:
 • Пример 2. Приготовить 2 л 0, 1 н. раствора соляной кислоты. • По формуле (2) находят массу навески 7, 292 г. • Концентрированную соляную кислоту (плотн. 1, 179 ) взвешивать неудобно, поэтому вычисленную навеску пересчитывают на объем. • Для этого по табл. А (справочник) находят, что такая плотность соответствует соляной кислоте с массовой долей HCI 36%. • Затем устанавливают, в какой массе (х) концентрированного раствора содержится 7, 292 г:
• Пример 2. Приготовить 2 л 0, 1 н. раствора соляной кислоты. • По формуле (2) находят массу навески 7, 292 г. • Концентрированную соляную кислоту (плотн. 1, 179 ) взвешивать неудобно, поэтому вычисленную навеску пересчитывают на объем. • Для этого по табл. А (справочник) находят, что такая плотность соответствует соляной кислоте с массовой долей HCI 36%. • Затем устанавливают, в какой массе (х) концентрированного раствора содержится 7, 292 г:
 • Полученная величина показывает, сколько нужно взять граммов соляной кислоты с массовой долей НСl 36%. Чтобы перевести граммы в миллилитры, используют формулу V = g/p, где р плотность кислоты. • Подставив в нее значения, получим
• Полученная величина показывает, сколько нужно взять граммов соляной кислоты с массовой долей НСl 36%. Чтобы перевести граммы в миллилитры, используют формулу V = g/p, где р плотность кислоты. • Подставив в нее значения, получим
 Установка титра раствора • Для установки титра растворов, приготовленных по точной навеске, применяют два способа: • отдельных навесок • пипетирования. • Наиболее точным, но более продолжительным по выполнению является способ отдельных навесок. • В этом способе предварительно вычисляют навеску установочного вещества по формуле 2 (см. выше). • При этом объем V обычно составляет 25 мл. • Затем на аналитических весах взвешивают три навески (равные вычисленной массе) с точностью до 0, 0001 г. • Эти навески переносят в чистые колбы и растворяют в дистиллированной воде (по 0, 25 мл) или в отдельных случаях в кислоте.
Установка титра раствора • Для установки титра растворов, приготовленных по точной навеске, применяют два способа: • отдельных навесок • пипетирования. • Наиболее точным, но более продолжительным по выполнению является способ отдельных навесок. • В этом способе предварительно вычисляют навеску установочного вещества по формуле 2 (см. выше). • При этом объем V обычно составляет 25 мл. • Затем на аналитических весах взвешивают три навески (равные вычисленной массе) с точностью до 0, 0001 г. • Эти навески переносят в чистые колбы и растворяют в дистиллированной воде (по 0, 25 мл) или в отдельных случаях в кислоте.
 • После полного растворения навески растворы титруют раствором титранта, титр которого необходимо установить. • Расчет титра раствора титранта (Тт) проводят по формуле: • где Эт эквивалентная масса титранта, г; • Эу. в. эквивалентная масса установочного вещества, г; • gу. в. навеска установочного вещества, г; • Кт объем титранта, затраченного на титрование навески, мл. • Необходимо помнить, что титр рассчитывают для каждой навески отдельно.
• После полного растворения навески растворы титруют раствором титранта, титр которого необходимо установить. • Расчет титра раствора титранта (Тт) проводят по формуле: • где Эт эквивалентная масса титранта, г; • Эу. в. эквивалентная масса установочного вещества, г; • gу. в. навеска установочного вещества, г; • Кт объем титранта, затраченного на титрование навески, мл. • Необходимо помнить, что титр рассчитывают для каждой навески отдельно.
 • По найденным трем значениям титра определяют его среднее значение и по полученной величине находят среднее значение нормальности Nпр и коэффициента нормальности К титранта по формулам: • где Nтеор. расчетная нормальность титранта.
• По найденным трем значениям титра определяют его среднее значение и по полученной величине находят среднее значение нормальности Nпр и коэффициента нормальности К титранта по формулам: • где Nтеор. расчетная нормальность титранта.
 • В способе пипетирования предварительно рассчитывают навеску установочного вещества по формуле (2), приняв V равным 250 мл. • Навеску установочного вещества взвешивают на аналитических весах с точностью до 0, 0001 г, переводят в мерную колбу вместимостью 250 мл, растворяют, доводят до метки водой и тщательно перемешивают. • Помещают в колбу для титрования 25 мл раствора, добавляют индикатор и титруют раствором титранта до изменения окраски индикатора. • Нормальность рассчитывают по формуле: • где Nу. в. нормальность раствора установочного вещества; • Кт – объем титранта, мл. • Перечень веществ, применяемых для установки титра важнейших титрантов, и их характеристики приведены в табл. Б(справочники).
• В способе пипетирования предварительно рассчитывают навеску установочного вещества по формуле (2), приняв V равным 250 мл. • Навеску установочного вещества взвешивают на аналитических весах с точностью до 0, 0001 г, переводят в мерную колбу вместимостью 250 мл, растворяют, доводят до метки водой и тщательно перемешивают. • Помещают в колбу для титрования 25 мл раствора, добавляют индикатор и титруют раствором титранта до изменения окраски индикатора. • Нормальность рассчитывают по формуле: • где Nу. в. нормальность раствора установочного вещества; • Кт – объем титранта, мл. • Перечень веществ, применяемых для установки титра важнейших титрантов, и их характеристики приведены в табл. Б(справочники).
 • Установочные вещества необходимо брать в виде препаратов марки «ХЧ» после их перекристаллизации из воды. При установке титра способом пипетирования целесообразно использовать в качестве установочного вещества фиксанал соответствующего реагента.
• Установочные вещества необходимо брать в виде препаратов марки «ХЧ» после их перекристаллизации из воды. При установке титра способом пипетирования целесообразно использовать в качестве установочного вещества фиксанал соответствующего реагента.
 Приемы работы при титровании • Перед началом титрования заполняют бюретку раствором титранта через воронку таким образом, чтобы уровень титранта был на 2 3 см выше нулевого деления бюретки. • Выпускают воздух из носика бюретки для чего у бюретки с резиновым наконечником отгибают наконечник вверх и, отжав пальцами резину от «бусины» , спускают раствор до полного удаления пузырьков воздуха из наконечника. • У бюреток со стеклянным краном надевают на кран кусок резиновой трубки, отгибают его вверх и, открыв кран, выпускают из него воздух. • Вынимают воронку из бюретки и спускают титрант до тех пор, пока нижний мениск раствора не совпадет с нулевым делением бюретки. • В том случае, когда титрант окрашен (растворы I 2 или КМn. О 4), устанавливают нуль по верхнему мениску раствора. • Под бюретку подставляют колбу с титруемым раствором и выполняют титрование со скоростью 1 2 капли раствора в секунду. • В процессе титрования раствор перемешивают круговым вращением колбы и следят за тем, чтобы капли титранта падали в центр колбы, а не на ее стенки.
Приемы работы при титровании • Перед началом титрования заполняют бюретку раствором титранта через воронку таким образом, чтобы уровень титранта был на 2 3 см выше нулевого деления бюретки. • Выпускают воздух из носика бюретки для чего у бюретки с резиновым наконечником отгибают наконечник вверх и, отжав пальцами резину от «бусины» , спускают раствор до полного удаления пузырьков воздуха из наконечника. • У бюреток со стеклянным краном надевают на кран кусок резиновой трубки, отгибают его вверх и, открыв кран, выпускают из него воздух. • Вынимают воронку из бюретки и спускают титрант до тех пор, пока нижний мениск раствора не совпадет с нулевым делением бюретки. • В том случае, когда титрант окрашен (растворы I 2 или КМn. О 4), устанавливают нуль по верхнему мениску раствора. • Под бюретку подставляют колбу с титруемым раствором и выполняют титрование со скоростью 1 2 капли раствора в секунду. • В процессе титрования раствор перемешивают круговым вращением колбы и следят за тем, чтобы капли титранта падали в центр колбы, а не на ее стенки.
 • Для точной фиксации момента изменения окраски раствора под колбу кладут листок чистой белой бумаги и ведут титрование при рассеянном дневном свете. • При титровании в вечернее время колбу с раствором подсвечивают люминесцентной лампой дневного света. • Результаты титрования отсчитывают по нижнему мениску в случае бесцветного титранта или по верхнему мениску, если применяется 0, 1 н. раствор I 2 или КМn. О 4. • Сзади бюретки на время взятия отсчета помещают листок чистой белой бумаги. Если мениск раствора титранта находится между делениями бюретки, объем отсчитывают на глаз с точностью до сотой доли миллилитра. • Перед началом титрования каплю, висящую на кончике бюретки, снимают с помощью кусочка фильтровальной бумаги.
• Для точной фиксации момента изменения окраски раствора под колбу кладут листок чистой белой бумаги и ведут титрование при рассеянном дневном свете. • При титровании в вечернее время колбу с раствором подсвечивают люминесцентной лампой дневного света. • Результаты титрования отсчитывают по нижнему мениску в случае бесцветного титранта или по верхнему мениску, если применяется 0, 1 н. раствор I 2 или КМn. О 4. • Сзади бюретки на время взятия отсчета помещают листок чистой белой бумаги. Если мениск раствора титранта находится между делениями бюретки, объем отсчитывают на глаз с точностью до сотой доли миллилитра. • Перед началом титрования каплю, висящую на кончике бюретки, снимают с помощью кусочка фильтровальной бумаги.

