Методы измерения масс молекул.ppt
- Количество слайдов: 38

Методы измерения масс молекул Калабин Г. А. , Горяинов С. В. Кафедра системной экологии

Что такое молекулярная масса? • Это масса молекулы, выраженная в относительных единицах (а. е. м. или Да) • 1 Да = 1/12 массы атома изотопа углерода-12 (1, 66*10 -27 кг) • Характеристика средней массы молекулы с учетом изотопного состава всех элементов, образующих данное соединение

Методы определения • Газы и пары PV = n. RT/M (уравнение Клапейрона. Менделеева) M = n. RT/PV – формула вычисления молекулярной массы

Методы определения • 1845 г. – метод шприца (предложен А. Реньо) • Принцип Виктора Мейера. Усовершенствовав аппарат В. Мейера, можно было проводить измерения при температурах до 2000° С.

Методы определения Пригодны для исследования: газы, летучие жидкости и твердые вещества

Методы определения • Растворы Измерение осмотического давления (1824 г. , Рене Дютроше) Установлено, что осмотическое давление пропорционально концентрации раствора. P = CRT – 1887 г. , Якоб Вант-Гофф. Означает, что молекулы вещества в р-ре ведут себя так, как будто они находятся в газе, занимающем такой же объем. Высокочувствительный метод.

Методы определения Криоскопия • Криоскопический метод определения молекулярной массы растворенных веществ основан на измерении понижения температуры замерзания раствора с известной моляльной концентрацией относительно температуры замерзания чистого растворителя • М=1000 · К · g · G · ΔTзам, C=ΔTзам · К, i=ΔTзам · К · С

Методы определения

Методы определения Эбулиоскопия • Метод эбулиоскопии заключается в определении характеристик растворенного вещества по его влиянию на температуру кипения растворителя. Эбуллиоскопический метод определения молекулярной массы растворенных веществ обычно используют при анализе только водных растворов, избегая испарения токсичных органических растворителей. При этом концентрация растворенного вещества должна быть относительно невелика для того, чтобы исследуемый раствор мог рассматриваться как близкий к идеальному по своим свойствам • ΔТкип. =0, 00012(760 - Р)·(273 + Т 0)

Методы определения Вискозиметрия • Наиболее простой и доступный метод определения молекулярной массы полимеров в широкой области значений молекулярных масс. Этот метод является косвенным и требует определения констант в уравнении, выражающем зависимость вязкости от молекулярных весов
![Методы определения Вискозиметрия • Уравнение Марка - Хувинка [η] = KMα где К и Методы определения Вискозиметрия • Уравнение Марка - Хувинка [η] = KMα где К и](https://present5.com/presentation/15565596_129476768/image-11.jpg)
Методы определения Вискозиметрия • Уравнение Марка - Хувинка [η] = KMα где К и α — константы для данной системы полимер-растворитель при определенной температуре. Обычно в зависимости от природы растворителя величина α, определяющая степень свернутости макромолекулы, колеблется в пределах 0, 5 -0, 8

Методы определения • Гель-проникающая (эксклюзионная) хроматография Вещества разделяются по размеру за счет их разной способности проникать в поры стационарной фазы

Методы определения • Гель-проникающая (эксклюзионная) хроматография Гель – гетерогенная система, в которой подвижная фаза всегда находится внутри пор стационарной фазы, называемой гелевой матрицей

Методы определения • Гель-проникающая (эксклюзионная) хроматография Сорбенты: - Низкого давления (агароза, декстран, полиакриламид, сефадекс, сефакрил, сефароза, супердекс) - Высокого давления (полиметакрилат, полистирол, силикагель)

Методы определения Масс-спектрометрия - применяется главным образом для двух целей: • 1) определение относительных изотопных масс и изотопного содержания элементов; • 2) определение относительных молекулярных масс и структуры органических соединений.
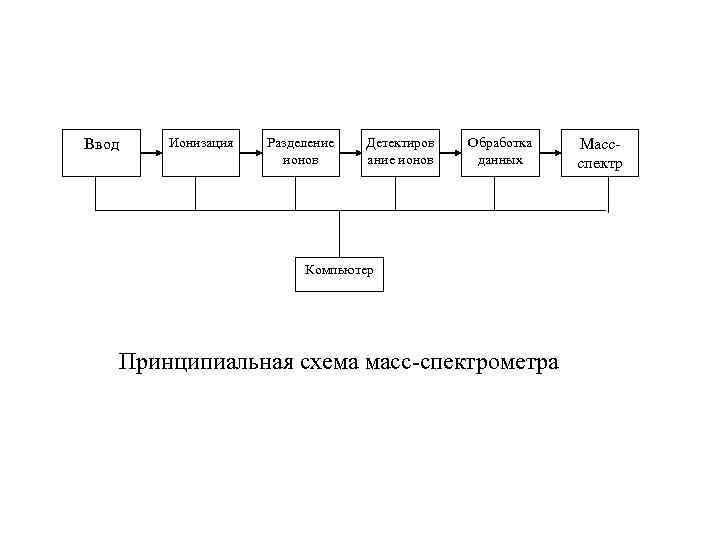
Ввод Ионизация Разделение ионов Детектиров ание ионов Обработка данных Компьютер Принципиальная схема масс-спектрометра Массспектр
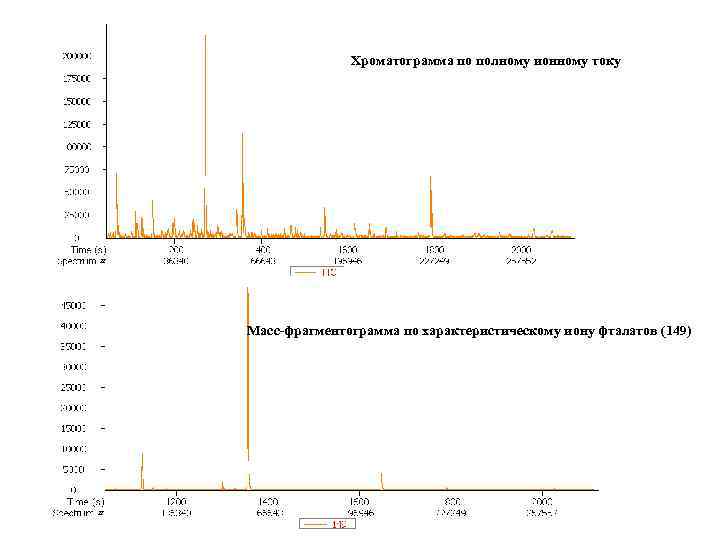
Хроматограмма по полному ионному току Масс-фрагментограмма по характеристическому иону фталатов (149)
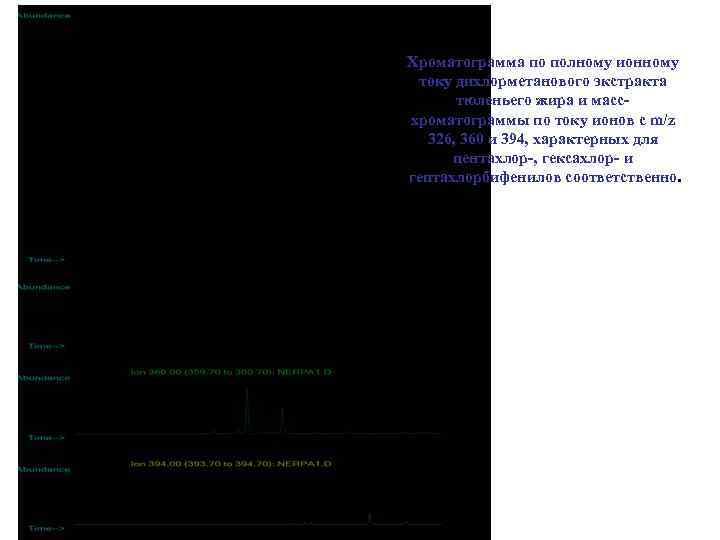
Хроматограмма по полному ионному току дихлорметанового экстракта тюленьего жира и массхроматограммы по току ионов с m/z 326, 360 и 394, характерных для пентахлор-, гексахлор- и гептахлорбифенилов соответственно.
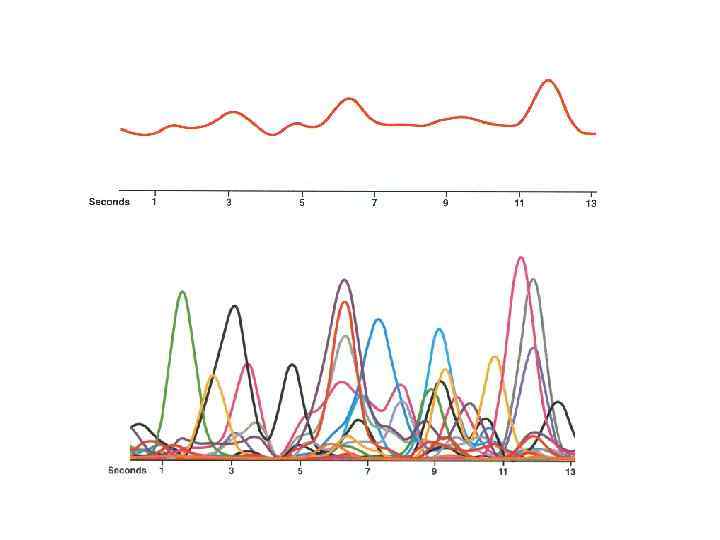
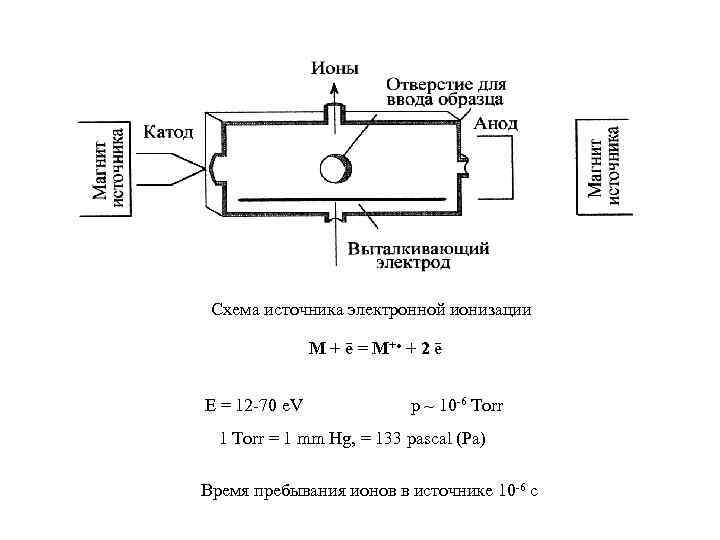
Схема источника электронной ионизации M + ē = M+ + 2 ē E = 12 -70 e. V p ~ 10 -6 Torr 1 Torr = 1 mm Hg, = 133 pascal (Pa) Время пребывания ионов в источнике 10 -6 с

Преимущества и недостатки ионизации электронами • • Воспроизводимость Чувствительность Универсальность Наличие библиотек спектров • Задействованы все пути фрагментации • Высокая избыточная энергия часто приводит к нестабильности молекулярного иона • Необходимость испарения образца • Отсутствие монохроматичности
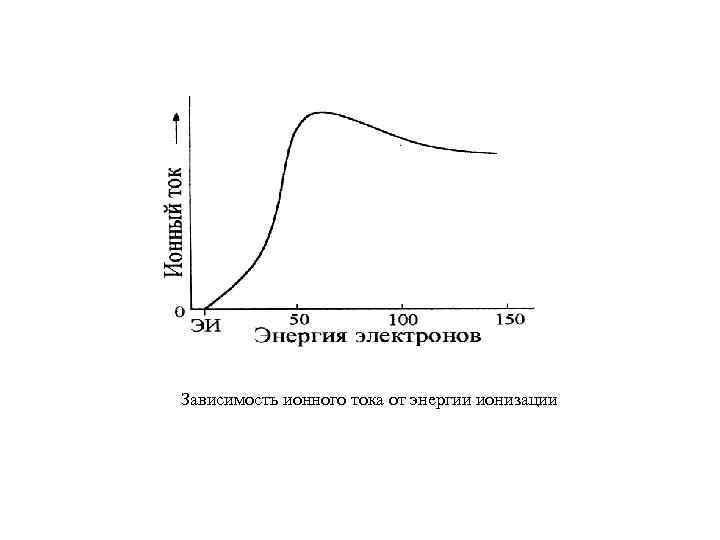
Зависимость ионного тока от энергии ионизации

При уменьшении энергии ионизирующих электронов относительная интенсивность пиков М+ и перегруппировочных ионов увеличивается относительно пиков осколочных ионов. Абсолютная интенсивность всех без исключения пиков становится ниже. Если пик молекулярного иона отсутствует в спектре при энергии электронов 70 e. V, он будет отсутствовать и при более низкой энергии электронов. Спектр ИЭ этилпропионата (молекулярная масса 102 Da) в зависимости от энергии электронов (70, 20 and 14 e. V).

Фрагментация молекулярных ионов M + ē = M+ + 2 ē 10 -16 секунды – потеря электрона Согласно принципа Франка-Кондона геометрия молекулы во время этого процесса не изменяется 10 -13 секунды – атомы начинают осциллировать 10 -8 секунды – электронно возбужденные ионы переходят в невозбужденное состояние или фрагментируют 10 -6 секунды – ионы покидают ионный источник

Виды анализаторов 1. Секторные приборы 2. Квадрупольные приборы 3. Ионные ловушки 4. Времяпролетные приборы 5. Приборы ИЦР (МСПФ) 6. Орбитрап
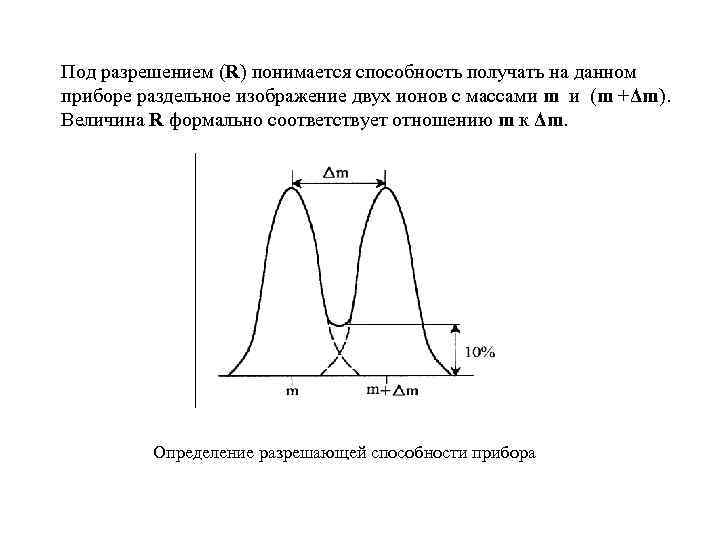
Под разрешением (R) понимается способность получать на данном приборе раздельное изображение двух ионов с массами m и (m +Δm). Величина R формально соответствует отношению m к Δm. Определение разрешающей способности прибора
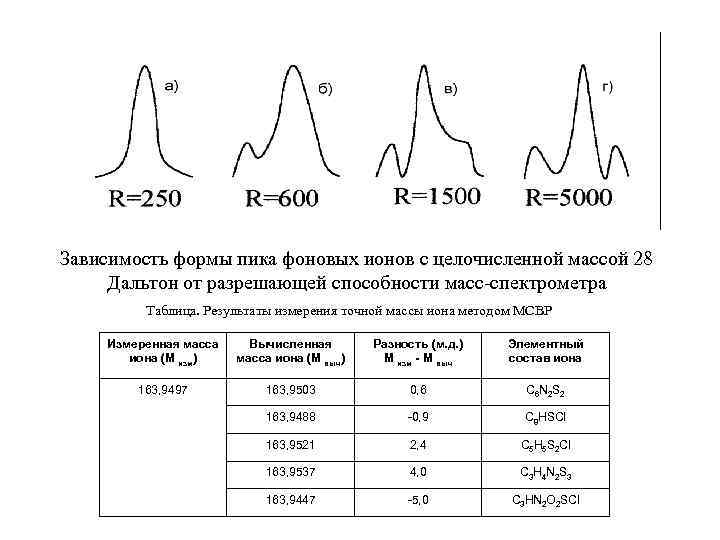
Зависимость формы пика фоновых ионов с целочисленной массой 28 Дальтон от разрешающей способности масс-спектрометра Таблица. Результаты измерения точной массы иона методом МСВР Измеренная масса иона (М изм) Вычисленная масса иона (М выч) Разность (м. д. ) М изм - М выч Элементный состав иона 163, 9497 163, 9503 0, 6 С 6 N 2 S 2 163, 9488 -0, 9 C 8 HSCl 163, 9521 2, 4 C 5 H 5 S 2 Cl 163, 9537 4, 0 C 3 H 4 N 2 S 3 163, 9447 -5, 0 C 3 HN 2 O 2 SCl

- Режим тандемной масс-спектрометрии. Можно получить информацию о нескольких последовательных поколениях фрагментных ионов. Такая техника зачастую обозначается в литературе (MS)n. - Возможность достижения разрешающей способности 25000 - Небольшие размеры - Самая низкая среди масс-спектрометров стоимость прибора - Возможность расширения диапазона регистрируемых масс в режиме резонансного извлечения ионов до десятков тысяч К недостаткам можно отнести протекание в ловушке ионномолекулярных реакций, что приводит к искажениям стандартного масс-спектра.
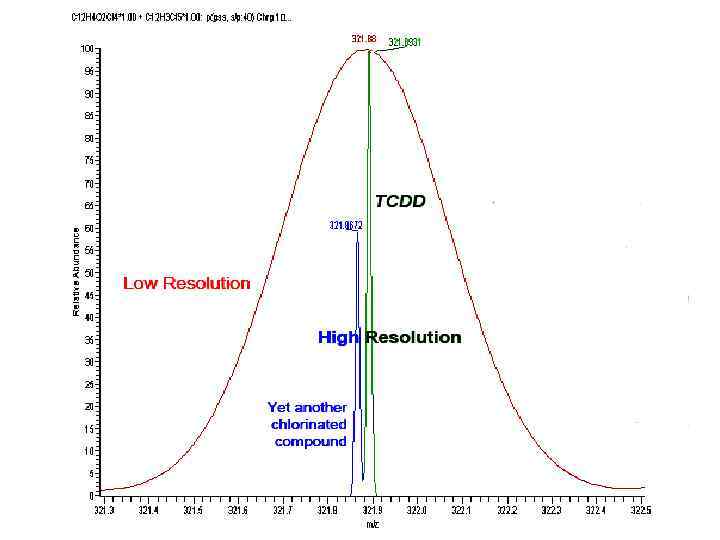
Разрешение в ГХ/МС
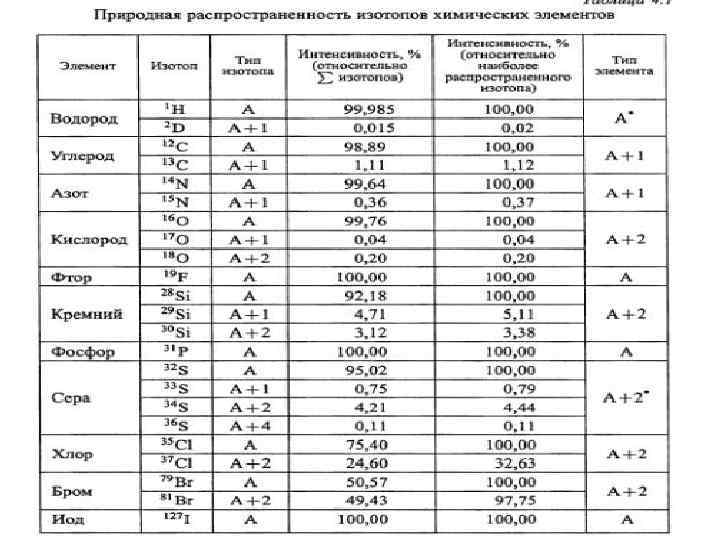
Методы определения
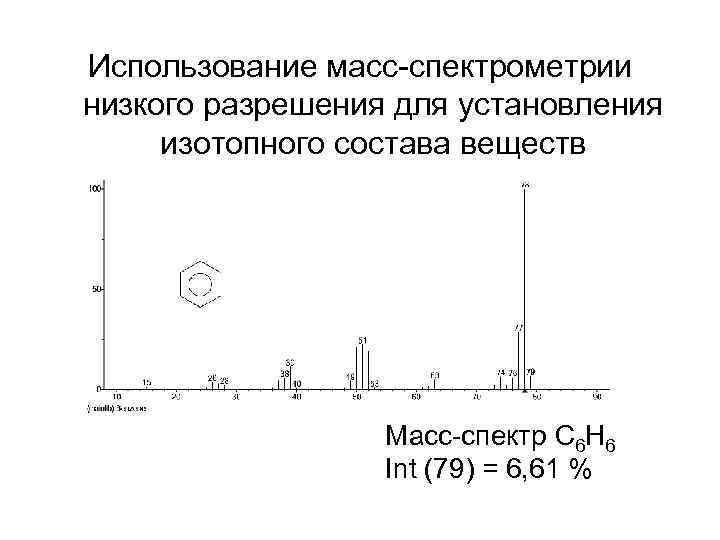
Использование масс-спектрометрии низкого разрешения для установления изотопного состава веществ Масс-спектр C 6 H 6 Int (79) = 6, 61 %

Определение элементного состава c использованием интенсивности изотопных пиков • В случае масс-спектрометрии среднего разрешения заключение об элементном составе исследуемого соединения можно сделать путем анализа интенсивностей группы линий молекулярного иона М+, (М+1)+, (М+2)+ и т. д. , поскольку интенсивности изотопных пиков определяются элементным составом молекул. Возможности этого подхода ограничены. Он позволяет установить молекулярную формулу с достаточной точностью только для соединений, которые включают не более 10 -12 атомов углерода

Определение элементного состава c использованием интенсивности изотопных пиков • Молекулярные ионы состоят только из атомов легких изотопов, которые являются обычно более распространеными. Обозначим массу молекулярного иона через М, и рассчитаем интенсивности изотопных пиков на примере молекулы бензола С 6 Н 6. В ее состав могут входить тяжелые изотопы 13 С и 2 Н. Отношения содержания этих изотопов (распространенности) в природе составляют: 13 С : 12 С ~ 1, 1· 10 -2 и 2 Н : 1 Н ~ 1, 6· 10 -4. Согласно теории вероятностей и комбинаторики, вероятность вхождения в состав молекулы С 6 Н 6 одного атома 13 С или одного атома 2 Н равна, соответственно, 6· 0, 011 = 0, 066 и 6· 0, 00016 = 0, 00096. Интенсивность пика (М+1)+ по отношению к интенсивности пика М+, принимаемой за 100%, представляет сумму интенсивностей изотопных пиков, обусловленных вкладами обоих изотопов: • I(М + 1)/I(М) ~ (0, 066 + 0, 00096)· 100 = 6, 61 %.

Определение элементного состава c использованием интенсивности изотопных пиков • Появление пика (М+2)+ может быть связано с присутствием в молекуле С 6 Н 6 двух атомов 13 С, либо двух атомов 2 Н, либо одновременно одного атома 13 С и одного атома 2 Н. Изотопный вклад в относительную интенсивность пика (М+2)+ от присутствия двух атомов 13 С определяется произведением числа сочетаний из 6 по 2, т. е. (6· 5)/(1· 2) = 15, на квадрат относительной распространенности С, т. е. на (0, 011)2. Аналогично, изотопный вклад от присутствия двух атомов 2 Н равен 15·(0, 00016)2. Вклад от одновременного присутствия атомов 13 С и 2 Н определяется произведением рассчитанных выше вероятностей присутствия их в молекуле бензола поодиночке, т. е. 6· 0, 011· 6· 0, 00016. Суммарная интенсивность пика (М+2)+ по отношению к интенсивности пика М+ (в %) равна: • С = n!/k!(n-k)! – число сочетаний • I(М+2)/I(М) ~ [15·(0, 011)2 + 15·(0, 00016)2 + 6· 0, 011· 6· 0, 00016]· 100 = 0, 19%

Определение элементного состава c использованием интенсивности изотопных пиков • Масс-спектрометрические методы, дающие хороший молекулярный ион – все «мягкие» методы ионизации: • 1) химическая ионизация • 2) матрично-активированная лазерная десорбция/ионизация • 3) химическая ионизация при атмосферном давлении • 4) электроспрей • 5) бомбардировка быстрыми атомами • Эмпирическое правило: если интенсивность иона (М+2)+ меньше 3% относительно М+, то в молекуле не содержится атомов хлора, брома, кремния, серы. • Азотное правило: если соединение содержит четное число атомов азота или не содержит азота вообще, то его молекулярная масса четная; если число атомов азота нечетное, молекулярная масса тоже нечетная
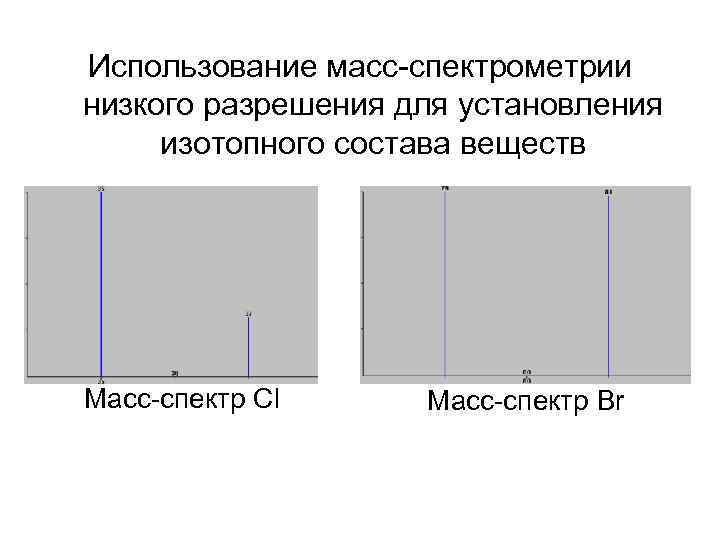
Использование масс-спектрометрии низкого разрешения для установления изотопного состава веществ Масс-спектр Cl Масс-спектр Br

Использование масс-спектрометрии низкого разрешения для установления изотопного состава веществ Масс-спектр C Масс-спектр O
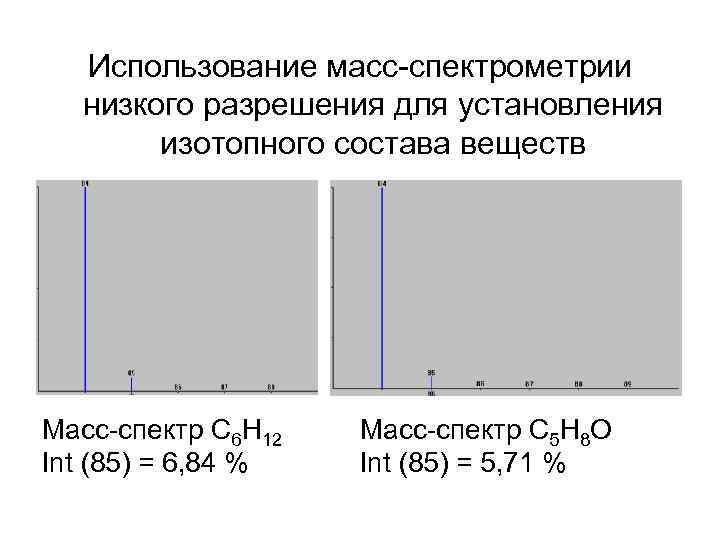
Использование масс-спектрометрии низкого разрешения для установления изотопного состава веществ Масс-спектр C 6 H 12 Int (85) = 6, 84 % Масс-спектр C 5 H 8 O Int (85) = 5, 71 %
Методы измерения масс молекул.ppt