Уравнения Хартри-Фока-Рутаана.ppt
- Количество слайдов: 11

Методы и приближения Приближение Борна-Оппенгеймера Приемы решения уравнения Шредингера: 1. Представление полной волновой функции в виде детерминанта Слэтера. 2. Использование метода МО ЛКАО. 3. Использование гауссовых базисных наборов атомных орбиталей. 1. Приближение самосогласованного поля Хартри. 2. Использование вариационного метода Ритца. Уравнения Хартри-Фока-Рутаана 1 Лекции по квантовой химии
Приближение Борна-Оппенгеймера Ядра движутся значительно медленнее электронов, которые успевают мгновенно подстроиться к любому изменению координат ядер. Поэтому с хорошей степенью точности можно считать положение ядер фиксированным и рассматривать только движение электронов в поле статичных ядер. Зависит только от координат электрона Такой вид оператора Гамильтона позволяет Заменяется на приближенный потециал с превратить многоэлектронное уравнение использованием концепции самосогласованного поля Шредингера в набор одноэлектронных уравнений Хартри-Фока-Рутаана Уравнения Хартри-Фока-Рутаана 2 Лекции по квантовой химии
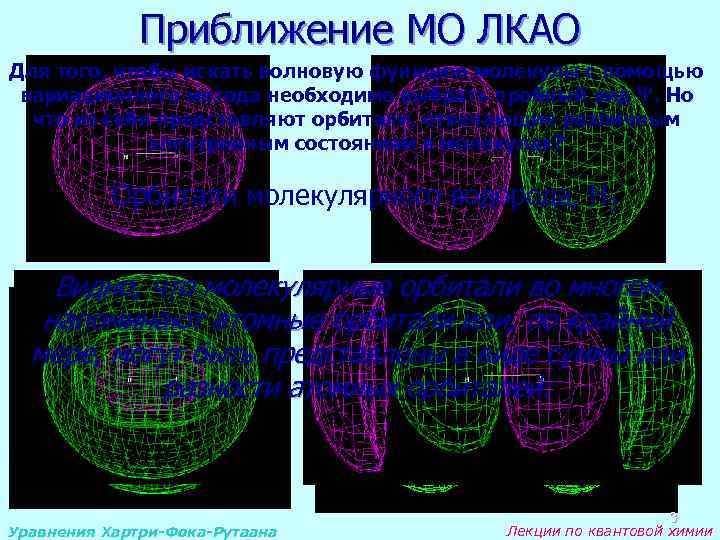
Приближение МО ЛКАО Для того, чтобы искать волновую функцию молекулы с помощью вариационного метода необходимо выбрать пробный вид . Но что из себя представляют орбитали, отвечающие различным электронным состояниям в молекулах? Орбитали молекулярного водорода, H 2 Видно, что молекулярные орбитали во многом напоминают атомные орбитали или, по крайней мере, могут быть представлены в виде суммы или разности атомных орбиталей: Уравнения Хартри-Фока-Рутаана 3 Лекции по квантовой химии
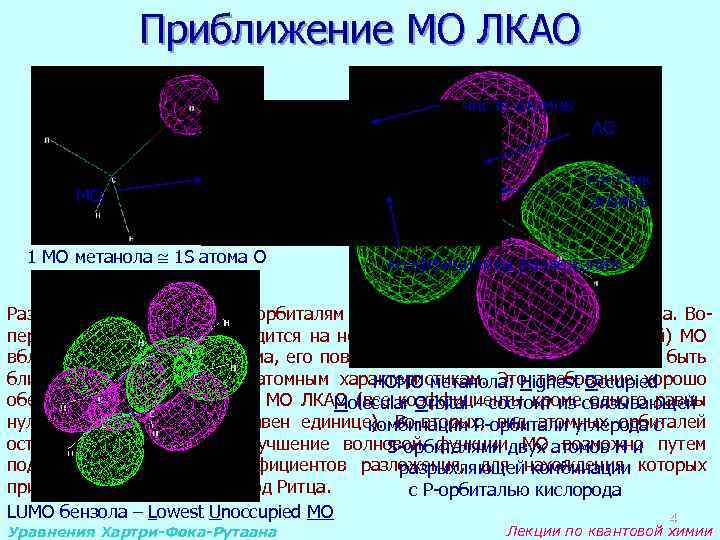
Приближение МО ЛКАО число атомов АО МО 1 МО метанола 1 S атома O счетчик атомов коэффициенты разложения Разложение МО по атомным орбиталям имеет два существенных достоинства. Вопервых, когда электрон находится на некоторой внутренней (низколежащей) МО вблизи ядра какого-либо атома, его поведение и волновая функция должны быть близкими соответствующим атомным характеристикам. Это требование хорошо HOMO метанола: Highest Occupied обеспечивается разложением МО ЛКАО (все коэффициенты кроме одного равны Molecular Orbital – состоит из связывающей нулю, один коэффициент равен единице). Во-вторых, вид атомных орбиталей комбинации P-орбитали углерода с остается неизменным, а улучшение волновой функции МО возможно путем S-орбиталями двух атомов H и подбора оптимальных коэффициентов разложения, для нахождения которых разрыхляющей комбинации применим вариационный метод Ритца. с P-орбиталью кислорода LUMO бензола – Lowest Unoccupied MO 4 Уравнения Хартри-Фока-Рутаана Лекции по квантовой химии

Детерминант Слэтера n электронов находятся в n различных состояниях ( «занимают» n МО). В каком именно порядке распределены электроны? Как это описать? ? ? Li. H 4 электрона на 4 МО: Хартри: = 1(1) 2(2) 3(3) 4(4) 1 2 Слэтер: 1 - 1 (s = +½) 2 - 1 (s = -½) 3 4 Достоинства представления Слэтера: 3 - 2 (s = +½) 1. Удовлетворяет принципу Паули (если 1 = 2, то = 0). 4 - 2 (s = -½) 2. Удовлетворяет 7 постулату (при перестановке двух электронов, т. е. столбцов определителя = - ’). Уравнения Хартри-Фока-Рутаана 5 Лекции по квантовой химии

Детерминант Слэтера Закрытые оболочки Метод RHF Открытые оболочки Метод UHF Restricted Hartree-Fock Unrestricted Hartree-Fock $contrl scftyp=RHF $end $contrl scftyp=UHF $end Метод ROHF Restricted Open-shell Hartree-Fock $contrl scftyp=ROHF $end Уравнения Хартри-Фока-Рутаана 6 Лекции по квантовой химии

Уравнения Хартри-Фока-Рутаана Итак, используя: а) Приближение Борна-Оппенгеймера, позволяющее упростить гамильтониан; б) Пробную волновую функцию в виде детерминанта Слэтера, в котором даны в) МО в виде линейной комбинации АО, получим (в соответствии с постулатом о среднем значении): Применяя приближении Хартри, заменяющее точную энергию межэлектронного отталкивания на эффективный потенциал, найдем электронную энергию в виде: Эффективный потенциал (2 J – K) зависит от коэффициентов разложения МО на АО. Оптимальный набор коэффициентов разложения найдем с помощью вариационного метода Ритца с ключевым условием: Уравнения Хартри-Фока-Рутаана 7 Лекции по квантовой химии

Уравнения Хартри-Фока-Рутаана В результате получим искомые уравнения Хартри-Фока-Рутаана: i – одноэлектронная энергия молекулярной орбитали i, S – элемент N N матрицы, называемой матрицей перекрывания F – элемент другой N N матрицы, называемой матрицей Фока Величины < | > представляют собой двухэлектронные интегралы отталкивания. Они умножены на одноэлектронную матрицу порядков связей или матрицу плотности P : Уравнения Хартри-Фока-Рутаана 8 Лекции по квантовой химии

Уравнения Хартри-Фока-Рутаана Система уравнений имеет нетривиальное решение, если Но!!! Элементы матрицы Фока сами зависят от коэффициентов ci. Такую систему уравнений решают методом последовательных приближений – методом самосогласования: 1. Выбирают из общих соображений начальный набор коэффициентов 2. С этими коэффициентами рассчитывают матрицу Фока 3. Из секулярного уравнения вычисляют набор энергий МО 4. С текущей матрицей Фока и энергиями МО из уравнений Хартри-Фока Рутаана находят новый набор коэффициентов разложения 5. Выполняют снова п. 2 и т. д. до тех пор пока не перестанут изменяться энергии МО и коэффициенты разложения Уравнения Хартри-Фока-Рутаана 9 Лекции по квантовой химии

Уравнения Хартри-Фока-Рутаана ITER EX DEM 1 2 3 4 5 6 7 8 9 0 1 2 3 4 5 6 7 8 TOTAL ENERGY E CHANGE DENSITY CHANGE * * * INITIATING DIIS PROCEDURE * * * 0 -628. 338869710 0. 097519382 0 -628. 383258791 -0. 044389082 0. 020103373 0 -628. 385050379 -0. 001791588 0. 016930226 0 -628. 385843051 -0. 000792672 0. 011641148 0 -628. 385941449 -0. 000098398 0. 003808091 0 -628. 385959093 -0. 000017644 0. 000308872 0 -628. 385959511 -0. 000000418 0. 000129604 0 -628. 385959544 -0. 000000033 0. 000028994 0 -628. 385959546 -0. 00002 0. 000008759 DIIS ERROR 0. 066090424 0. 024685430 0. 012685127 0. 005175559 0. 001230082 0. 000161085 0. 000047380 0. 000011777 0. 000005228 --------DENSITY CONVERGED --------- Уравнения Хартри-Фока-Рутаана 10 Лекции по квантовой химии

Уравнения Хартри-Фока-Рутаана Метод Хартри-Фока-Рутаана ССП МО ЛКАО (SCF MO LCAO) (Self-Consisting Field) Количество собственных значений i и соответствующих им собственных функций i равно числу базисных функций N в разложении ЛКАО. Определитель Слэтера для полной волновой функции молекулы строится из n = N/2 занятых электронами МО. В минимизации полной энергии участвуют только занятые МО и, так как матричные элементы F зависят только от P , а порядок связи рассчитывается из волновых функций только занятых орбиталей, только они могут рассматриваться как физически определенные. Незанятые МО, получаемые из уравнений Хартри-Фока-Рутаана, не участвуют в минимизации полной энергии системы, поэтому их соответствие истинным энергетическим уровням молекулы не вполне определенно. Такие уровни называют виртуальными. Уравнения Хартри-Фока-Рутаана 11 Лекции по квантовой химии
Уравнения Хартри-Фока-Рутаана.ppt