Строение вещества 2л 2016.ppt
- Количество слайдов: 32
 Методы фотоэлектронной спектроскопии Методы анализа и исследования вещества, которые можно условно объединить под общим названием – методы фотоэлектронной спектроскопии, разрабатывались в 50 -х и 60 -х годах ХХ в. параллельно в Швеции, СССР, Англии и США. Их применение в химии началось в конце 60 -х, а соответствующие приборы появились лишь в 70 -х годах минувшего столетия и постоянно совершенствуются.
Методы фотоэлектронной спектроскопии Методы анализа и исследования вещества, которые можно условно объединить под общим названием – методы фотоэлектронной спектроскопии, разрабатывались в 50 -х и 60 -х годах ХХ в. параллельно в Швеции, СССР, Англии и США. Их применение в химии началось в конце 60 -х, а соответствующие приборы появились лишь в 70 -х годах минувшего столетия и постоянно совершенствуются.
 Это методы основанные на явлениях фотоэффекта, получаемого при использовании монохроматического электромагнитного излучения, и вторичной электронной эмиссии. С развитием методов фотоэлектронной спектроскопии химия получила возможность узнавать информацию об электронном строении атомов и молекул, а также экспериментальной проверки теоретических концепций и, прежде всего, тех или иных расчетов в рамках теории молекулярных орбиталей (МО).
Это методы основанные на явлениях фотоэффекта, получаемого при использовании монохроматического электромагнитного излучения, и вторичной электронной эмиссии. С развитием методов фотоэлектронной спектроскопии химия получила возможность узнавать информацию об электронном строении атомов и молекул, а также экспериментальной проверки теоретических концепций и, прежде всего, тех или иных расчетов в рамках теории молекулярных орбиталей (МО).
 Надежное совпадение рассчитанных и измеренных характеристик электронной структуры и, в частности, значений энергий соответствующих МО (в рамках теоремы Купманса) позволяет дать количественное описание тому или иному параметру электронного строения. • Некоторые из методов электронной спектроскопии справедливо рассматривают как «экспериментальные» методы квантовой химии.
Надежное совпадение рассчитанных и измеренных характеристик электронной структуры и, в частности, значений энергий соответствующих МО (в рамках теоремы Купманса) позволяет дать количественное описание тому или иному параметру электронного строения. • Некоторые из методов электронной спектроскопии справедливо рассматривают как «экспериментальные» методы квантовой химии.
 Экспериментальные методы изучения электронной структуры • К таким методам следует отнести, прежде всего метод фотоэлектронной спектроскопии, который оценивает энергии занятых электронных уровней, и метод электронной трансмиссионной спектроскопии, который оценивает энергии вакантных электронных уровней молекул.
Экспериментальные методы изучения электронной структуры • К таким методам следует отнести, прежде всего метод фотоэлектронной спектроскопии, который оценивает энергии занятых электронных уровней, и метод электронной трансмиссионной спектроскопии, который оценивает энергии вакантных электронных уровней молекул.
 Кроме того, информацию о занятых электронных уровнях молекул с развитой электронной структурой дают данные электронной абсорбционной спектроскопии комплексов с переносом заряда. • О граничных занятых и свободных электронных уровнях – данные полярографии и спектроскопии электронного парамагнитного резонанса соответствующих ионрадикальных частиц.
Кроме того, информацию о занятых электронных уровнях молекул с развитой электронной структурой дают данные электронной абсорбционной спектроскопии комплексов с переносом заряда. • О граничных занятых и свободных электронных уровнях – данные полярографии и спектроскопии электронного парамагнитного резонанса соответствующих ионрадикальных частиц.
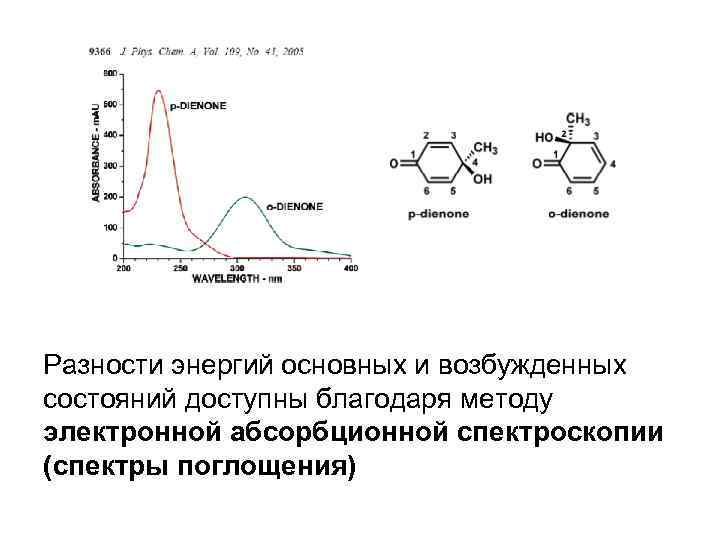 Разности энергий основных и возбужденных состояний доступны благодаря методу электронной абсорбционной спектроскопии (спектры поглощения)
Разности энергий основных и возбужденных состояний доступны благодаря методу электронной абсорбционной спектроскопии (спектры поглощения)
 Метод фотоэлектронной спектроскопии Потенциалы ионизации • Этот метод позволяет определять энергии занятых МО и судить о взаимном расположении занятых МО в системе. • Потенциал ионизации атома является важной характеристикой, определяющей, например, способность элемента проявлять металлические свойства. В равной степени эта характеристика важна и для молекулы, поскольку она служит мерой способности молекулы к переходу в окисленное состояние, сопровождающемуся отрывом от нее электрона.
Метод фотоэлектронной спектроскопии Потенциалы ионизации • Этот метод позволяет определять энергии занятых МО и судить о взаимном расположении занятых МО в системе. • Потенциал ионизации атома является важной характеристикой, определяющей, например, способность элемента проявлять металлические свойства. В равной степени эта характеристика важна и для молекулы, поскольку она служит мерой способности молекулы к переходу в окисленное состояние, сопровождающемуся отрывом от нее электрона.
 Однако атомные и молекулярные ионы, также как и нейтральные атомы и молекулы, имеют много возможных уровней энергии. В результате отрыва электрона от атома или молекулы ион может остаться в низшем, основном состоянии или в одном из своих возбужденных состояний. Термин потенциал ионизации обычно обозначает энергию, необходимую для отрыва электрона от атома или молекулы, находящихся в основном состоянии, с образованием иона в основном состоянии.
Однако атомные и молекулярные ионы, также как и нейтральные атомы и молекулы, имеют много возможных уровней энергии. В результате отрыва электрона от атома или молекулы ион может остаться в низшем, основном состоянии или в одном из своих возбужденных состояний. Термин потенциал ионизации обычно обозначает энергию, необходимую для отрыва электрона от атома или молекулы, находящихся в основном состоянии, с образованием иона в основном состоянии.
 Но можно ввести более общее определение i-того потенциала ионизации, когда ион образуется в своем i-том электронном состоянии • Согласно данному определению, 1 -ый и 2 -ой потенциалы ионизации атома Ne определяются следующими диаграммами: Ne(1 s 22 p 6)→Ne+(1 s 22 p 5)+e; I 1= 21, 6 э. В Ne(1 s 22 p 6)→Ne+(1 s 22 s 12 p 6)+e; I 2= 48, 5 э. В Потенциал ионизации тем больше, чем сильнее связан электрон, а это зависит от типа занимаемой им орбитали и от состояния ионизуемого атома. 1 э. В = 96, 49 к. Дж/моль
Но можно ввести более общее определение i-того потенциала ионизации, когда ион образуется в своем i-том электронном состоянии • Согласно данному определению, 1 -ый и 2 -ой потенциалы ионизации атома Ne определяются следующими диаграммами: Ne(1 s 22 p 6)→Ne+(1 s 22 p 5)+e; I 1= 21, 6 э. В Ne(1 s 22 p 6)→Ne+(1 s 22 s 12 p 6)+e; I 2= 48, 5 э. В Потенциал ионизации тем больше, чем сильнее связан электрон, а это зависит от типа занимаемой им орбитали и от состояния ионизуемого атома. 1 э. В = 96, 49 к. Дж/моль
 Наиболее непосредственной и обладающей широкой областью применимости методикой измерения потенциалов ионизации молекул является фотоэлектронная спектроскопия • Данный метод, предложенный в 1963 г. , широко применяют для изучения электронной структуры молекул. Метод фотоэлектронной спектроскопии (ФЭС) основан на фотоэффекте Эйнштейна.
Наиболее непосредственной и обладающей широкой областью применимости методикой измерения потенциалов ионизации молекул является фотоэлектронная спектроскопия • Данный метод, предложенный в 1963 г. , широко применяют для изучения электронной структуры молекул. Метод фотоэлектронной спектроскопии (ФЭС) основан на фотоэффекте Эйнштейна.
 Фотоэлектрический эффект или фотоэффект M + hν → M·+ + e Суть эффекта заключается в том, что при облучении вещества энергия поглощаемого молекулой фотона расходуется на отрыв электронов от молекулы (эта часть энергии определяет потенциал ионизации Ii) и на передачу ионизируемым электронам соответствующей кинетической энергии: hν = Ii + Eiкин
Фотоэлектрический эффект или фотоэффект M + hν → M·+ + e Суть эффекта заключается в том, что при облучении вещества энергия поглощаемого молекулой фотона расходуется на отрыв электронов от молекулы (эта часть энергии определяет потенциал ионизации Ii) и на передачу ионизируемым электронам соответствующей кинетической энергии: hν = Ii + Eiкин
 • Данное уравнение объясняет почему, увеличивая интенсивность облучения, можно повысить лишь интенсивность потока фотоэлектронов, но не их энергию. Изменение энергии фотоэлектронов может быть достигнуто лишь при изменении частоты облучающих фотонов. • Энергия фотона hν применяемого монохроматического излучения с частотой ν должна превышать измеряемый потенциал ионизации
• Данное уравнение объясняет почему, увеличивая интенсивность облучения, можно повысить лишь интенсивность потока фотоэлектронов, но не их энергию. Изменение энергии фотоэлектронов может быть достигнуто лишь при изменении частоты облучающих фотонов. • Энергия фотона hν применяемого монохроматического излучения с частотой ν должна превышать измеряемый потенциал ионизации
 Величины энергий излучения Энергии коротковолнового УФ излучения (hν < 102 э. В) достаточно для того, чтобы выбить электрон из валентной оболочки атомов или с молекулярных орбиталей, а рентгеновские лучи (и электронный пучок) обладают достаточной энергией (hν >103 э. В) для возбуждении эмиссии электронов с внутренних оболочек. Обычно в качестве монохроматического УФ излучения используется свет, который генерируется в результате электрического разряда в трубке, содержащей гелий.
Величины энергий излучения Энергии коротковолнового УФ излучения (hν < 102 э. В) достаточно для того, чтобы выбить электрон из валентной оболочки атомов или с молекулярных орбиталей, а рентгеновские лучи (и электронный пучок) обладают достаточной энергией (hν >103 э. В) для возбуждении эмиссии электронов с внутренних оболочек. Обычно в качестве монохроматического УФ излучения используется свет, который генерируется в результате электрического разряда в трубке, содержащей гелий.
 Источники УФ излучения для ФЭС • Для потенциалов ионизации, меньших 20 э. В, источником излучения обычно служит линия испускания возбужденного атома гелия He I c длиной волны 58, 4 нм (21, 2 э. В). При изучении валентных оболочек в качестве источников УФ-излучения применяются также линии He II (40, 8 э. В) и Ne I (16, 8 э. В) и др. • Малая ширина атомных линий позволяет определять Ii с точностью до ± 0, 01 э. В. • Измерения более высоких потенциалов ионизации, особенно связанных с отрывом электронов из внутренних оболочек, производят при помощи рентгеновского излучения (РФЭС, шведский ученый Зигбан, 1981 г. - Нобелевская премия).
Источники УФ излучения для ФЭС • Для потенциалов ионизации, меньших 20 э. В, источником излучения обычно служит линия испускания возбужденного атома гелия He I c длиной волны 58, 4 нм (21, 2 э. В). При изучении валентных оболочек в качестве источников УФ-излучения применяются также линии He II (40, 8 э. В) и Ne I (16, 8 э. В) и др. • Малая ширина атомных линий позволяет определять Ii с точностью до ± 0, 01 э. В. • Измерения более высоких потенциалов ионизации, особенно связанных с отрывом электронов из внутренних оболочек, производят при помощи рентгеновского излучения (РФЭС, шведский ученый Зигбан, 1981 г. - Нобелевская премия).
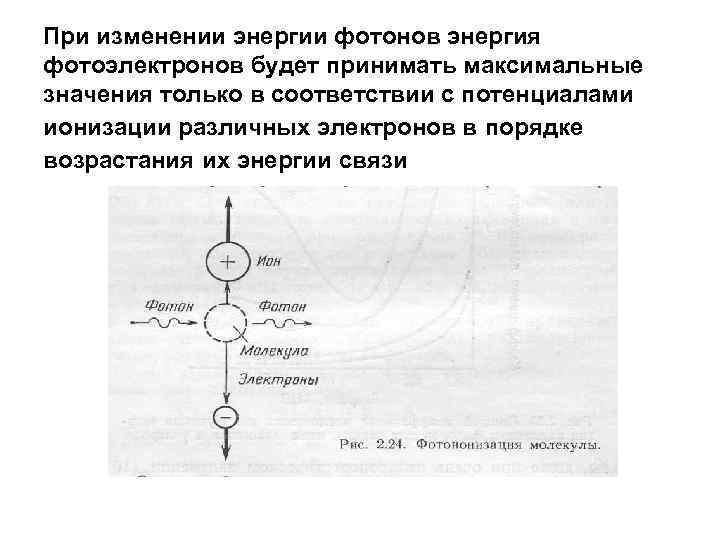 При изменении энергии фотонов энергия фотоэлектронов будет принимать максимальные значения только в соответствии с потенциалами ионизации различных электронов в порядке возрастания их энергии связи
При изменении энергии фотонов энергия фотоэлектронов будет принимать максимальные значения только в соответствии с потенциалами ионизации различных электронов в порядке возрастания их энергии связи
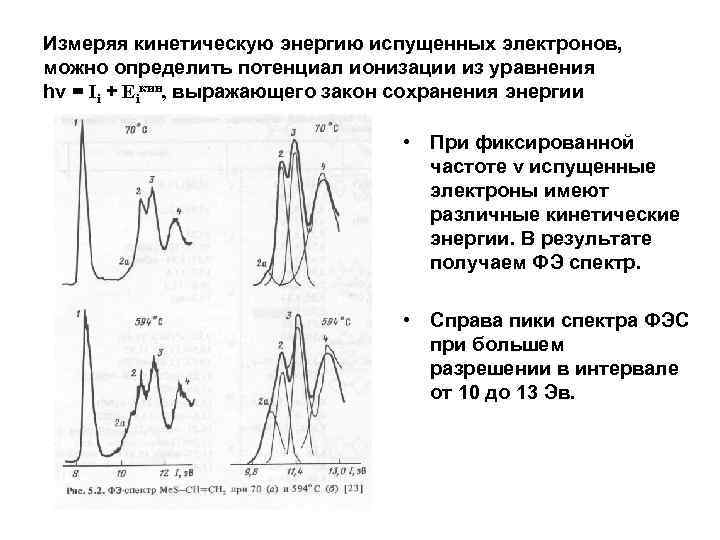 Измеряя кинетическую энергию испущенных электронов, можно определить потенциал ионизации из уравнения hν = Ii + Eiкин, выражающего закон сохранения энергии • При фиксированной частоте ν испущенные электроны имеют различные кинетические энергии. В результате получаем ФЭ спектр. • Справа пики спектра ФЭС при большем разрешении в интервале от 10 до 13 Эв.
Измеряя кинетическую энергию испущенных электронов, можно определить потенциал ионизации из уравнения hν = Ii + Eiкин, выражающего закон сохранения энергии • При фиксированной частоте ν испущенные электроны имеют различные кинетические энергии. В результате получаем ФЭ спектр. • Справа пики спектра ФЭС при большем разрешении в интервале от 10 до 13 Эв.
 • При использовании гелия и других подобных источников излучения этот метод носит название ультрафиолетовой фотоэлектронной спектроскопии (УФЭС), в случае рентгеновских источников – РФЭС. • Часто эти методы можно также встретить под именем ЭСХА – электронная спектроскопия для химического анализа (ESCA – Electron Spectroscopy for Chemical Analysis), т. к. этими методами получают большое количество химической информации.
• При использовании гелия и других подобных источников излучения этот метод носит название ультрафиолетовой фотоэлектронной спектроскопии (УФЭС), в случае рентгеновских источников – РФЭС. • Часто эти методы можно также встретить под именем ЭСХА – электронная спектроскопия для химического анализа (ESCA – Electron Spectroscopy for Chemical Analysis), т. к. этими методами получают большое количество химической информации.
 В отличие от УФ, видимого и ИК излучения, коэффициент поглощения рентгеновских лучей обычно сравнительно мал, чем и объясняется их легкая проницаемость через различные вещества. Методы фотоэлектронной спектроскопии имеют большое преимущество перед рентгеновским поглощением в силу гораздо более высокой чувствительности и разрешающей способности. Пики в ФЭ спектрах относительно более узкие, четкие и интенсивные, их положение, а следовательно, и сдвиги могут быть измерены с высокой точностью.
В отличие от УФ, видимого и ИК излучения, коэффициент поглощения рентгеновских лучей обычно сравнительно мал, чем и объясняется их легкая проницаемость через различные вещества. Методы фотоэлектронной спектроскопии имеют большое преимущество перед рентгеновским поглощением в силу гораздо более высокой чувствительности и разрешающей способности. Пики в ФЭ спектрах относительно более узкие, четкие и интенсивные, их положение, а следовательно, и сдвиги могут быть измерены с высокой точностью.
 • Надо отметить, что метод ФЭС оказался наиболее плодотворным не для атомов, а, именно, для молекул, т. к. он является уникальным средством исследования их электронной структуры, а также проверки применимости метода МО. • ФЭ-данные позволяют не только установить потенциалы ионизации, но и определить такие важные характеристики, как симметрия, преимущественная локализация и связывающий характер многоцентровых МО.
• Надо отметить, что метод ФЭС оказался наиболее плодотворным не для атомов, а, именно, для молекул, т. к. он является уникальным средством исследования их электронной структуры, а также проверки применимости метода МО. • ФЭ-данные позволяют не только установить потенциалы ионизации, но и определить такие важные характеристики, как симметрия, преимущественная локализация и связывающий характер многоцентровых МО.
 Общая характеристика фотоэлектронных спектрометров • Теоретическое объяснение явления фотоэлектронной эмиссии (фотоэффекта) было дано еще в начале ХХ века в работах Эйнштейна и Иоффе, но экспериментальная реализация задержалась почти на 60 лет. Сложность эксперимента объясняется необходимостью соблюдения трех требований.
Общая характеристика фотоэлектронных спектрометров • Теоретическое объяснение явления фотоэлектронной эмиссии (фотоэффекта) было дано еще в начале ХХ века в работах Эйнштейна и Иоффе, но экспериментальная реализация задержалась почти на 60 лет. Сложность эксперимента объясняется необходимостью соблюдения трех требований.
 Три требования для экспериментальной реализации методов фотоэлектронной спектроскопии 1) энергия фотонов должна быть достаточной для ионизации всех или значительной части электронных уровней; 2) разрешение в спектрах должно обеспечивать анализ колебательной структуры полос (ΔЕ ≤ 0, 1 э. В); 3) вакуум в энергоанализаторе электронов. К основным узлам и системам спектрометра можно отнести источник фотонов, ионизационную кювету, детектор электронов и вакуумную систему.
Три требования для экспериментальной реализации методов фотоэлектронной спектроскопии 1) энергия фотонов должна быть достаточной для ионизации всех или значительной части электронных уровней; 2) разрешение в спектрах должно обеспечивать анализ колебательной структуры полос (ΔЕ ≤ 0, 1 э. В); 3) вакуум в энергоанализаторе электронов. К основным узлам и системам спектрометра можно отнести источник фотонов, ионизационную кювету, детектор электронов и вакуумную систему.
 Схема ФЭ спектрометра Для анализа образцы вещества, находящиеся в глубоком вакууме в ионизационной камере ФЭ спектрометра, подвергаются облучению, способному вызвать фотоионизацию отдельных молекул. Ионизационная камера связана с анализатором, в котором фотоэлектроны сортируются по кинетической энергии. Поскольку соотношение между потенциалом ионизации электрона и его кинетической энергией однозначно определяется уравнением hν = Ii + Eiкин, абсцисса ФЭС прямо выражается в значениях Ii. Количество электронов определенной энергии в сек. является мерой интенсивности фотоэлектронного тока и регистрируется по оси ординат.
Схема ФЭ спектрометра Для анализа образцы вещества, находящиеся в глубоком вакууме в ионизационной камере ФЭ спектрометра, подвергаются облучению, способному вызвать фотоионизацию отдельных молекул. Ионизационная камера связана с анализатором, в котором фотоэлектроны сортируются по кинетической энергии. Поскольку соотношение между потенциалом ионизации электрона и его кинетической энергией однозначно определяется уравнением hν = Ii + Eiкин, абсцисса ФЭС прямо выражается в значениях Ii. Количество электронов определенной энергии в сек. является мерой интенсивности фотоэлектронного тока и регистрируется по оси ординат.
 Образцы • Можно получать фотоэлектронные спектры твердых или газообразных (при низких давлениях) образцов. • Жидкости для исследования замораживают или испаряют. • При изучении твердых образцов особенно необходим высокий вакуум для предохранения поверхности от загрязнений адсорбируемыми частицами, иногда необходимо охлаждение. • Детектировать можно все элементы, кроме водорода. ФЭС измеряет, таким образом, энергетические спектры электронов, «вылетающих» из атомов, молекул и твердых тел при облучении их монохроматическим УФ- или рентгеновским излучением.
Образцы • Можно получать фотоэлектронные спектры твердых или газообразных (при низких давлениях) образцов. • Жидкости для исследования замораживают или испаряют. • При изучении твердых образцов особенно необходим высокий вакуум для предохранения поверхности от загрязнений адсорбируемыми частицами, иногда необходимо охлаждение. • Детектировать можно все элементы, кроме водорода. ФЭС измеряет, таким образом, энергетические спектры электронов, «вылетающих» из атомов, молекул и твердых тел при облучении их монохроматическим УФ- или рентгеновским излучением.
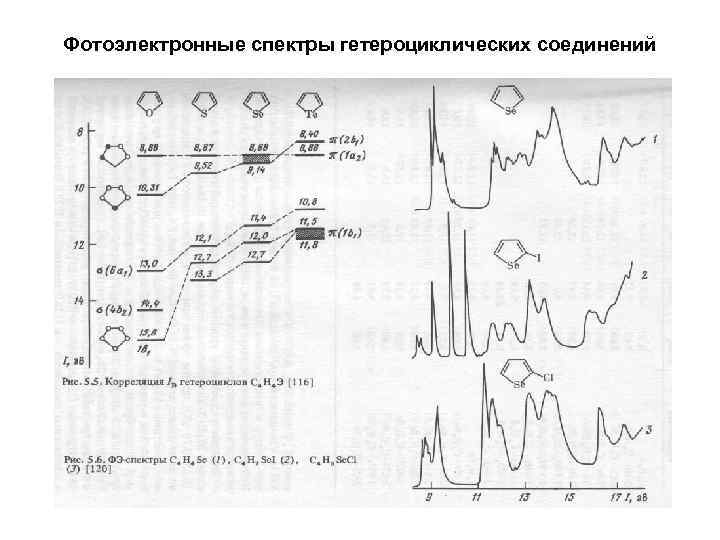 Фотоэлектронные спектры гетероциклических соединений
Фотоэлектронные спектры гетероциклических соединений
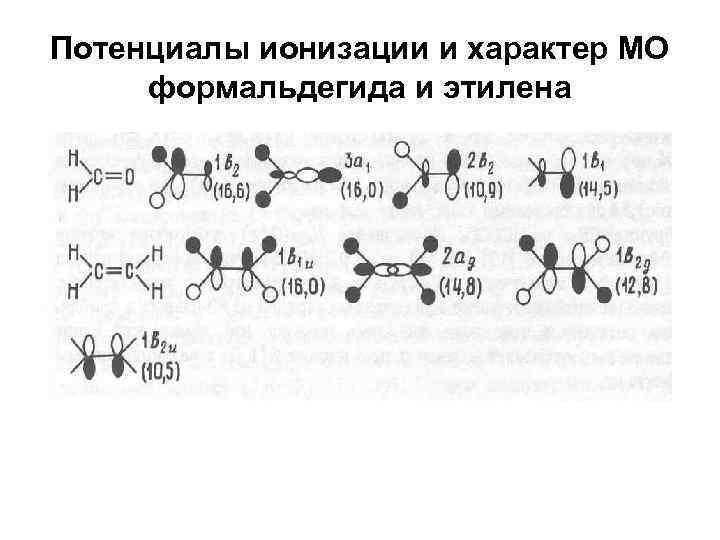 Потенциалы ионизации и характер МО формальдегида и этилена
Потенциалы ионизации и характер МО формальдегида и этилена
 Происхождение структуры фотоионизационных полос В общем случае результирующий ион M·+ может находиться в различных электронных, колебательных, вращательных состояниях. Изменением энергии вращательных состояний при фотоионизации, как правило, пренебрегают. Различные же комбинации электронных и колебательных уровней реализуются при возбуждении и часто наблюдается колебательная структура в ФЭ спектрах. 1 -ый пик полосы в ФЭ спектре оценивает значение адиабатического потенциала Iад и отвечает нулевому колебательному состоянию иона S+i, 0
Происхождение структуры фотоионизационных полос В общем случае результирующий ион M·+ может находиться в различных электронных, колебательных, вращательных состояниях. Изменением энергии вращательных состояний при фотоионизации, как правило, пренебрегают. Различные же комбинации электронных и колебательных уровней реализуются при возбуждении и часто наблюдается колебательная структура в ФЭ спектрах. 1 -ый пик полосы в ФЭ спектре оценивает значение адиабатического потенциала Iад и отвечает нулевому колебательному состоянию иона S+i, 0
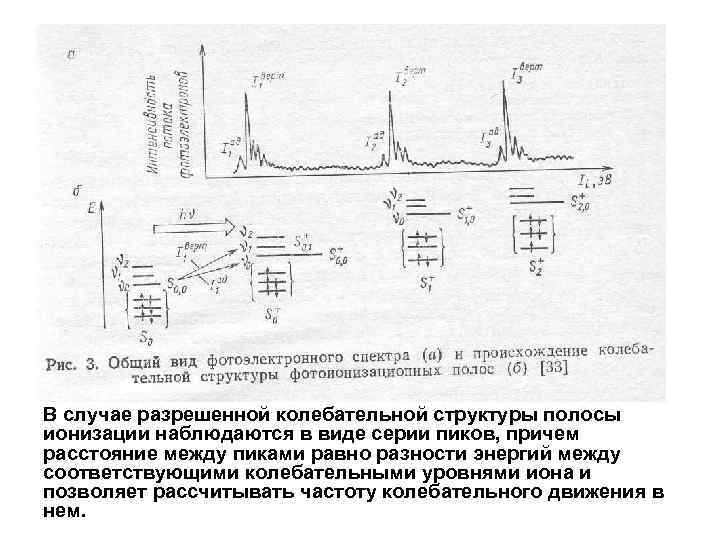 В случае разрешенной колебательной структуры полосы ионизации наблюдаются в виде серии пиков, причем расстояние между пиками равно разности энергий между соответствующими колебательными уровнями иона и позволяет рассчитывать частоту колебательного движения в нем.
В случае разрешенной колебательной структуры полосы ионизации наблюдаются в виде серии пиков, причем расстояние между пиками равно разности энергий между соответствующими колебательными уровнями иона и позволяет рассчитывать частоту колебательного движения в нем.
 Вертикальный потенциал ионизации • Наиболее интенсивным пиком в полосе оказывается, как правило, 2 -ой пик, измеряющий значение вертикального потенциала ионизации Iверт, относящийся к франк-кондоновскому переходу и отвечающий 1 -ому колебательному состоянию иона S+i, 0 Энергия вертикальной ионизации соответствует электронному переходу, при котором геометрическая конфигурация молекулярного иона неизменна по сравнению с исходной молекулой.
Вертикальный потенциал ионизации • Наиболее интенсивным пиком в полосе оказывается, как правило, 2 -ой пик, измеряющий значение вертикального потенциала ионизации Iверт, относящийся к франк-кондоновскому переходу и отвечающий 1 -ому колебательному состоянию иона S+i, 0 Энергия вертикальной ионизации соответствует электронному переходу, при котором геометрическая конфигурация молекулярного иона неизменна по сравнению с исходной молекулой.
 Очевидно, что если исходная молекула находится в основном электронноколебательном состоянии, то энергия вертикальной ионизации может быть равна или превышать энергию адиабатической ионизации, т. е. ΔЕкол равна нулю или положительна. Уравнение для энергии связи электрона в молекуле (на какой-то молекулярной орбитали) можно записать: Есвi = hν - Екинi = Iадi + ΔЕкол, где ΔЕкол – возможное при фотоионизации изменение колебательной энергии.
Очевидно, что если исходная молекула находится в основном электронноколебательном состоянии, то энергия вертикальной ионизации может быть равна или превышать энергию адиабатической ионизации, т. е. ΔЕкол равна нулю или положительна. Уравнение для энергии связи электрона в молекуле (на какой-то молекулярной орбитали) можно записать: Есвi = hν - Екинi = Iадi + ΔЕкол, где ΔЕкол – возможное при фотоионизации изменение колебательной энергии.
 • Колебательная структура полос фотоэлектронных спектров связана со строением молекул и распределением электронной плотности. По ней и по форме полосы можно судить о характере орбитали, с которой удаляется электрон. • При ионизации со связывающей орбитали происходит ослабление связи и понижение частоты валентного колебания в молекулярном ионе.
• Колебательная структура полос фотоэлектронных спектров связана со строением молекул и распределением электронной плотности. По ней и по форме полосы можно судить о характере орбитали, с которой удаляется электрон. • При ионизации со связывающей орбитали происходит ослабление связи и понижение частоты валентного колебания в молекулярном ионе.
 Теорема Купманса • Строгое отнесение полос ФЭС основывается на теореме Купманса, предполагающей применение для этого квантово-химических расчетов. Ii = - ε i Измеренные вертикальные энергии ионизации Ii равны отрицательным величинам рассчитанных орбитальных энергий – εi Именно теорема Купманса определяет возможность применения данных ФЭС для изучения электронной структуры в рамках орбитального подхода.
Теорема Купманса • Строгое отнесение полос ФЭС основывается на теореме Купманса, предполагающей применение для этого квантово-химических расчетов. Ii = - ε i Измеренные вертикальные энергии ионизации Ii равны отрицательным величинам рассчитанных орбитальных энергий – εi Именно теорема Купманса определяет возможность применения данных ФЭС для изучения электронной структуры в рамках орбитального подхода.
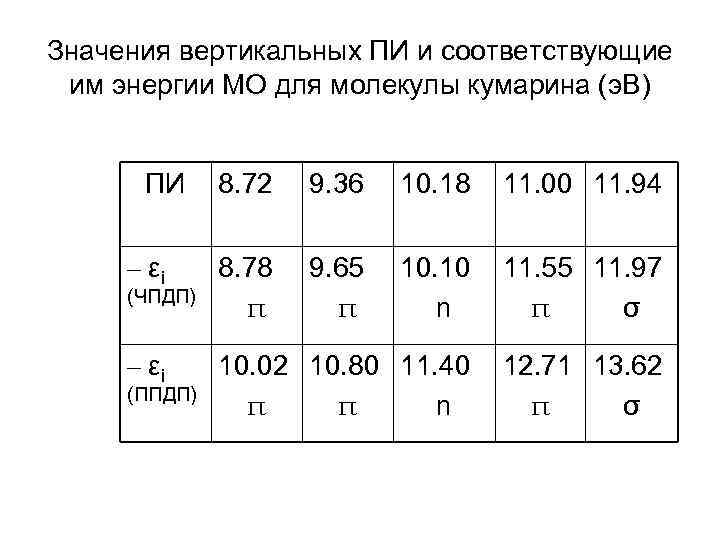 Значения вертикальных ПИ и соответствующие им энергии МО для молекулы кумарина (э. В) ПИ 8. 72 9. 36 10. 18 11. 00 11. 94 – εi 8. 78 π 9. 65 π 10. 10 n 11. 55 11. 97 π σ – εi 10. 02 10. 80 11. 40 π π n 12. 71 13. 62 π σ (ЧПДП) (ППДП)
Значения вертикальных ПИ и соответствующие им энергии МО для молекулы кумарина (э. В) ПИ 8. 72 9. 36 10. 18 11. 00 11. 94 – εi 8. 78 π 9. 65 π 10. 10 n 11. 55 11. 97 π σ – εi 10. 02 10. 80 11. 40 π π n 12. 71 13. 62 π σ (ЧПДП) (ППДП)


