55.pptx
- Количество слайдов: 184
 Методы фармоэкономического анализа Все ующие существ на яшний сегодн етоды день м принято ять на раздел льшие две бо группы. 1
Методы фармоэкономического анализа Все ующие существ на яшний сегодн етоды день м принято ять на раздел льшие две бо группы. 1
 Анализ «минимизация затрат» (cost minimisation analysis CMA) Анализ «минимизация затрат» применяют для сравнения стоимости двух и более вмешательств с равной клинической эффективностью. Идентичность эффективности вмешательств должна быть подтверждена результатами исследований, выполненных в соответствии с принципами медицины, основанной на доказательствах. Для получения корректных результатов этот метод анализа требует оценки всех доступных для учета компонентов лечения, определяющих его затратную сторону. Предпочтение, разумеется, отдают вмешательству с наименьшей стоимостью. 2
Анализ «минимизация затрат» (cost minimisation analysis CMA) Анализ «минимизация затрат» применяют для сравнения стоимости двух и более вмешательств с равной клинической эффективностью. Идентичность эффективности вмешательств должна быть подтверждена результатами исследований, выполненных в соответствии с принципами медицины, основанной на доказательствах. Для получения корректных результатов этот метод анализа требует оценки всех доступных для учета компонентов лечения, определяющих его затратную сторону. Предпочтение, разумеется, отдают вмешательству с наименьшей стоимостью. 2
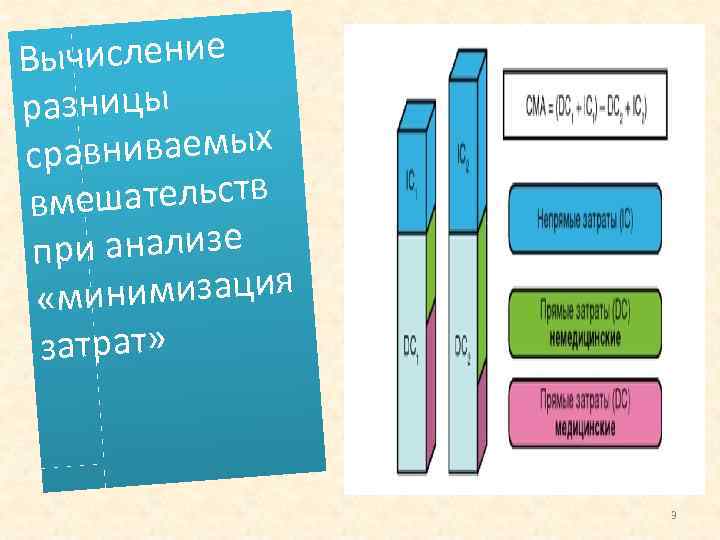 ычисление В разницы вниваемых сра шательств вме анализе при мизация «мини затрат» 3
ычисление В разницы вниваемых сра шательств вме анализе при мизация «мини затрат» 3
 Следует отметить, что в реальной клинической практике вмешательства, имеющие идентичную эффективность и безопасность, встречают крайне редко. Поэтому чаще всего метод «минимизация затрат» используют в следующих случаях: 1) для сравнения эффективности различных схем применения и дозирования одного и того же препарата; 2) при схожих результатах назначения альтернативных схем лечения (например, при лабораторно подтвержденной эрадикации). 4
Следует отметить, что в реальной клинической практике вмешательства, имеющие идентичную эффективность и безопасность, встречают крайне редко. Поэтому чаще всего метод «минимизация затрат» используют в следующих случаях: 1) для сравнения эффективности различных схем применения и дозирования одного и того же препарата; 2) при схожих результатах назначения альтернативных схем лечения (например, при лабораторно подтвержденной эрадикации). 4
 • Обратите внимание, что применение этого метода не рекомендовано для сравнения препаратов генериков. 5
• Обратите внимание, что применение этого метода не рекомендовано для сравнения препаратов генериков. 5
 Анализ «затраты – эффективность» (cost effectiveness analisys – CEA) Анализ «затраты эффективность» применяют для сравнения стоимости двух и более вмешательств, неодинаковых по эффективности и/или безопасности Затраты выражаются в денежных единицах, а эффективность в натуральных единицах тех положительных исходов, которые достигаются с помощью изучаемых вмешательств. 6
Анализ «затраты – эффективность» (cost effectiveness analisys – CEA) Анализ «затраты эффективность» применяют для сравнения стоимости двух и более вмешательств, неодинаковых по эффективности и/или безопасности Затраты выражаются в денежных единицах, а эффективность в натуральных единицах тех положительных исходов, которые достигаются с помощью изучаемых вмешательств. 6
 К единицам таких исходов относятся: количество лет сохраненной жизни; частота эрадикации и т. д. число выздоровевши х пациентов; 7
К единицам таких исходов относятся: количество лет сохраненной жизни; частота эрадикации и т. д. число выздоровевши х пациентов; 7
 В этом случае при анализе используют соответствующие физические единицы мм рт. ст. , ммоль/л и другие. Результаты данного анализа могут быть выражены средним, либо инкрементальным соотношением «затраты эффективность» . При лечении хронических нефатальных заболеваний в качестве промежуточных (суррогатных) критериев эффективности вмешательств используются такие показатели как снижение артериального давления или снижение концентрации холестерина ЛПНП плазмы крови. 8
В этом случае при анализе используют соответствующие физические единицы мм рт. ст. , ммоль/л и другие. Результаты данного анализа могут быть выражены средним, либо инкрементальным соотношением «затраты эффективность» . При лечении хронических нефатальных заболеваний в качестве промежуточных (суррогатных) критериев эффективности вмешательств используются такие показатели как снижение артериального давления или снижение концентрации холестерина ЛПНП плазмы крови. 8
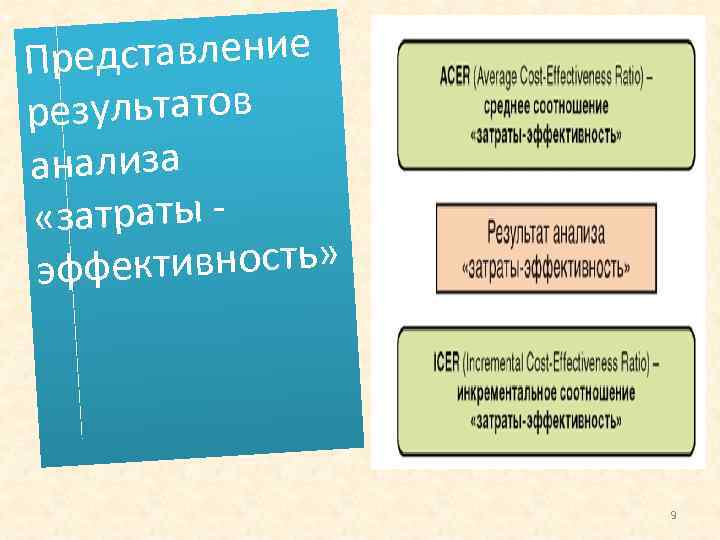 ставление Пред результатов анализа «затраты ективность» эфф 9
ставление Пред результатов анализа «затраты ективность» эфф 9
 • При выражении результата в виде среднего соотношения «затраты эффективность» (ACER) расчет для каждого альтернативного вмешательства проводят отдельно и представляют в виде отношения затрат на единицу эффективности. • На практике более эффективный метод обычно обладает большей стоимостью. 10
• При выражении результата в виде среднего соотношения «затраты эффективность» (ACER) расчет для каждого альтернативного вмешательства проводят отдельно и представляют в виде отношения затрат на единицу эффективности. • На практике более эффективный метод обычно обладает большей стоимостью. 10
 счет среднего Ра соотношения «затраты ффективность» , э где DC прямые затраты, IC непрямые затраты, Ef ффективность э вмешательств 11
счет среднего Ра соотношения «затраты ффективность» , э где DC прямые затраты, IC непрямые затраты, Ef ффективность э вмешательств 11
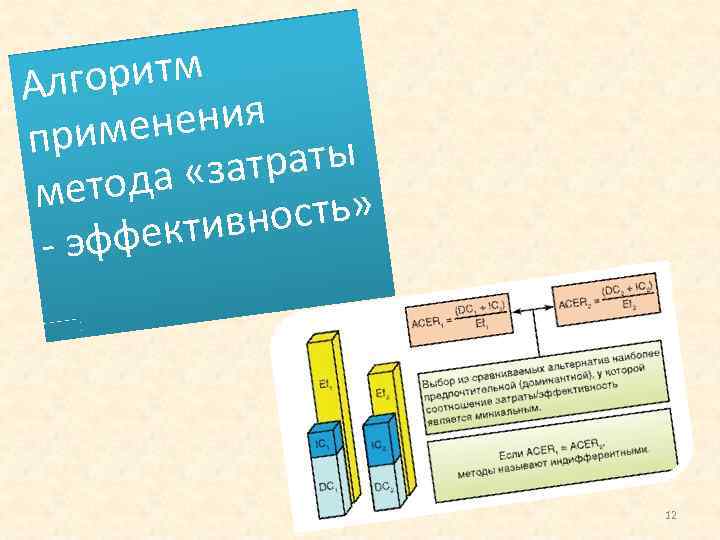 итм Алгор ения римен п траты да «за мето ость» ективн эфф 12
итм Алгор ения римен п траты да «за мето ость» ективн эфф 12
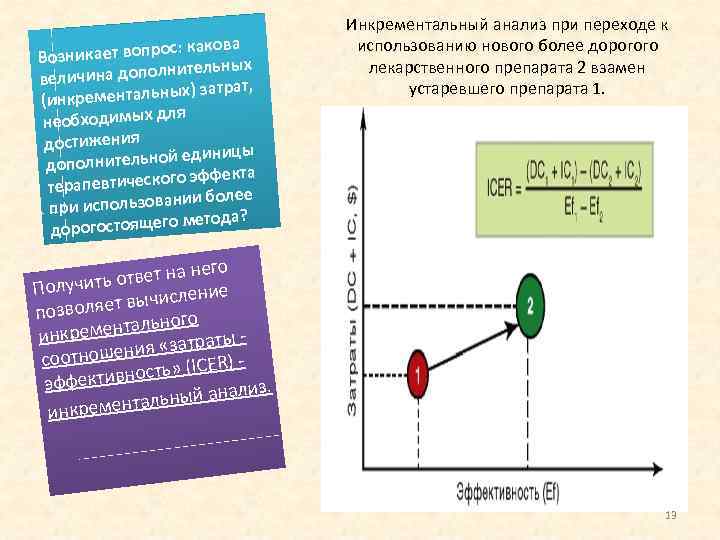 ос: какова Возникает вопр тельных личина дополни ве затрат, рементальных) (инк ля необходимых д достижения ицы нительной един допол эффекта рапевтического те более использовании при метода? дорогостоящего Инкрементальный анализ при переходе к использованию нового более дорогого лекарственного препарата 2 взамен устаревшего препарата 1. го твет на не о Получить е вычислени позволяет о ентальног инкрем ы ия «затрат соотношен ь» (ICER) ост эффективн ализ. альный ан т инкремен 13
ос: какова Возникает вопр тельных личина дополни ве затрат, рементальных) (инк ля необходимых д достижения ицы нительной един допол эффекта рапевтического те более использовании при метода? дорогостоящего Инкрементальный анализ при переходе к использованию нового более дорогого лекарственного препарата 2 взамен устаревшего препарата 1. го твет на не о Получить е вычислени позволяет о ентальног инкрем ы ия «затрат соотношен ь» (ICER) ост эффективн ализ. альный ан т инкремен 13
 Анализ «затраты выгода» (cost benefit + analisys – CBA). Анализ «затраты выгода» применяют для определения финансовой выгоды по отношению к затратам. Особенность данного метода анализа заключается в том, что эффективность сравнимаемых вмешательств выражается не в «натуральных единицах» , А в денежном эквиваленте. Расчет показателя соотношения выгоды и затрат BCR=B/C. Результаты анализа «затраты выгода» представляются в виде показателя соотношения выгоды (B) и затрат (C) BCR (benefit cost ratio). Предпочтение отдают методу, для которого это соотношение является набольшим. 14
Анализ «затраты выгода» (cost benefit + analisys – CBA). Анализ «затраты выгода» применяют для определения финансовой выгоды по отношению к затратам. Особенность данного метода анализа заключается в том, что эффективность сравнимаемых вмешательств выражается не в «натуральных единицах» , А в денежном эквиваленте. Расчет показателя соотношения выгоды и затрат BCR=B/C. Результаты анализа «затраты выгода» представляются в виде показателя соотношения выгоды (B) и затрат (C) BCR (benefit cost ratio). Предпочтение отдают методу, для которого это соотношение является набольшим. 14
 Представление результатов лечения в денежном эквиваленте не всегда выполнимо в силу этических соображений и значительной вариабельности получаемых результатов. По этой причине использование CBA оправдано лишь для сравнения эффективности различных медицинских вмешательств на уровне принятия решений в сфере политики здравоохранения. 15
Представление результатов лечения в денежном эквиваленте не всегда выполнимо в силу этических соображений и значительной вариабельности получаемых результатов. По этой причине использование CBA оправдано лишь для сравнения эффективности различных медицинских вмешательств на уровне принятия решений в сфере политики здравоохранения. 15
 Анализ «затраты полезность» (cost utility analysis CUA) Анализ «затраты полезность» метод, применяемый для определения соотношения стоимости лечения и его полезности, который основан на всестороннем и комплексном изучении качества жизни и его связи со степенью здоровья пациента. Это единственный метод, отражающий предпочтения пациентов, их родственников, а также врачей при выборе методов лечения или возможных исходов заболевания. Расчет полезности затрат осуществляют в несколько этапов. 16
Анализ «затраты полезность» (cost utility analysis CUA) Анализ «затраты полезность» метод, применяемый для определения соотношения стоимости лечения и его полезности, который основан на всестороннем и комплексном изучении качества жизни и его связи со степенью здоровья пациента. Это единственный метод, отражающий предпочтения пациентов, их родственников, а также врачей при выборе методов лечения или возможных исходов заболевания. Расчет полезности затрат осуществляют в несколько этапов. 16
 Визуально аналоговая шкала Этап 1 Количественное определение субъективной прогностической оценки предпочтений, м аемой пациенто дав различным . яниям здоровья состо 17
Визуально аналоговая шкала Этап 1 Количественное определение субъективной прогностической оценки предпочтений, м аемой пациенто дав различным . яниям здоровья состо 17
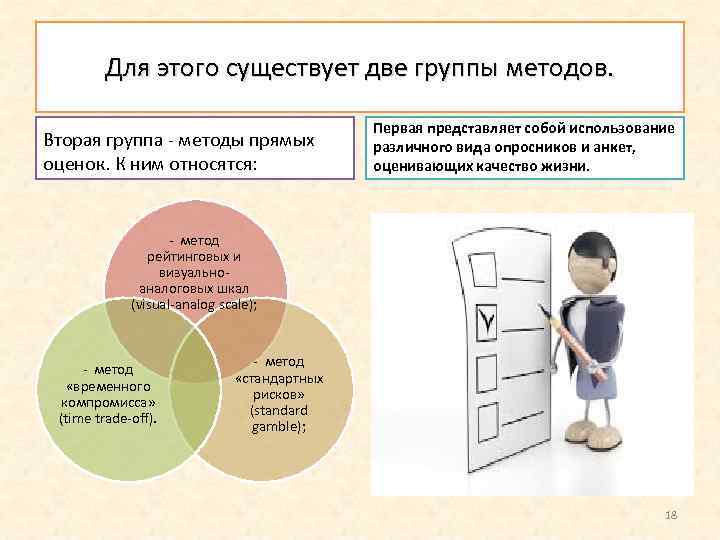 Для этого существует две группы методов. Вторая группа методы прямых оценок. К ним относятся: Первая представляет собой использование различного вида опросников и анкет, оценивающих качество жизни. метод рейтинговых и визуально аналоговых шкал (visual analog scale); метод «временного компромисса» (time trade off). метод «стандартных рисков» (standard gamble); 18
Для этого существует две группы методов. Вторая группа методы прямых оценок. К ним относятся: Первая представляет собой использование различного вида опросников и анкет, оценивающих качество жизни. метод рейтинговых и визуально аналоговых шкал (visual analog scale); метод «временного компромисса» (time trade off). метод «стандартных рисков» (standard gamble); 18
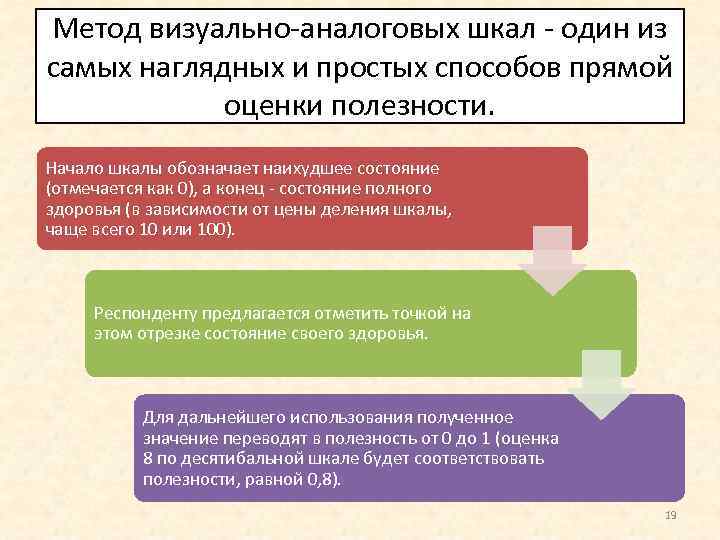 Метод визуально аналоговых шкал один из самых наглядных и простых способов прямой оценки полезности. Начало шкалы обозначает наихудшее состояние (отмечается как 0), а конец состояние полного здоровья (в зависимости от цены деления шкалы, чаще всего 10 или 100). Респонденту предлагается отметить точкой на этом отрезке состояние своего здоровья. Для дальнейшего использования полученное значение переводят в полезность от 0 до 1 (оценка 8 по десятибальной шкале будет соответствовать полезности, равной 0, 8). 19
Метод визуально аналоговых шкал один из самых наглядных и простых способов прямой оценки полезности. Начало шкалы обозначает наихудшее состояние (отмечается как 0), а конец состояние полного здоровья (в зависимости от цены деления шкалы, чаще всего 10 или 100). Респонденту предлагается отметить точкой на этом отрезке состояние своего здоровья. Для дальнейшего использования полученное значение переводят в полезность от 0 до 1 (оценка 8 по десятибальной шкале будет соответствовать полезности, равной 0, 8). 19
 Метод «стандартных рисков» , или «стандартной лотереи» , дусматривает пре выбор между двумя сравниваемыми льтернативами, а исход одной из , которых известен а другой нет. Схема метода «стандартных рисков» 20
Метод «стандартных рисков» , или «стандартной лотереи» , дусматривает пре выбор между двумя сравниваемыми льтернативами, а исход одной из , которых известен а другой нет. Схема метода «стандартных рисков» 20
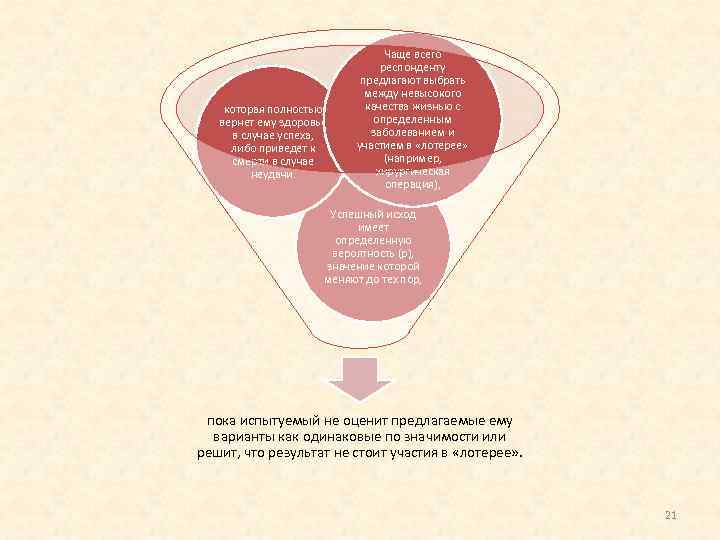 которая полностью вернет ему здоровье в случае успеха, либо приведет к смерти в случае неудачи. Чаще всего респонденту предлагают выбрать между невысокого качества жизнью с определенным заболеванием и участием в «лотерее» (например, хирургическая операция), Успешный исход имеет определенную вероятность (p), значение которой меняют до тех пор, пока испытуемый не оценит предлагаемые ему варианты как одинаковые по значимости или решит, что результат не стоит участия в «лотерее» . 21
которая полностью вернет ему здоровье в случае успеха, либо приведет к смерти в случае неудачи. Чаще всего респонденту предлагают выбрать между невысокого качества жизнью с определенным заболеванием и участием в «лотерее» (например, хирургическая операция), Успешный исход имеет определенную вероятность (p), значение которой меняют до тех пор, пока испытуемый не оценит предлагаемые ему варианты как одинаковые по значимости или решит, что результат не стоит участия в «лотерее» . 21
 Например, если пациент затрудняется сделать выбор между предложенными альтернативами при вероятности здоровья, равной 90%, и вероятностью смерти, равной 10% то в этом случае оценка полезности пребывания в рассматриваемом состоянии равна 0, 9. 22
Например, если пациент затрудняется сделать выбор между предложенными альтернативами при вероятности здоровья, равной 90%, и вероятностью смерти, равной 10% то в этом случае оценка полезности пребывания в рассматриваемом состоянии равна 0, 9. 22
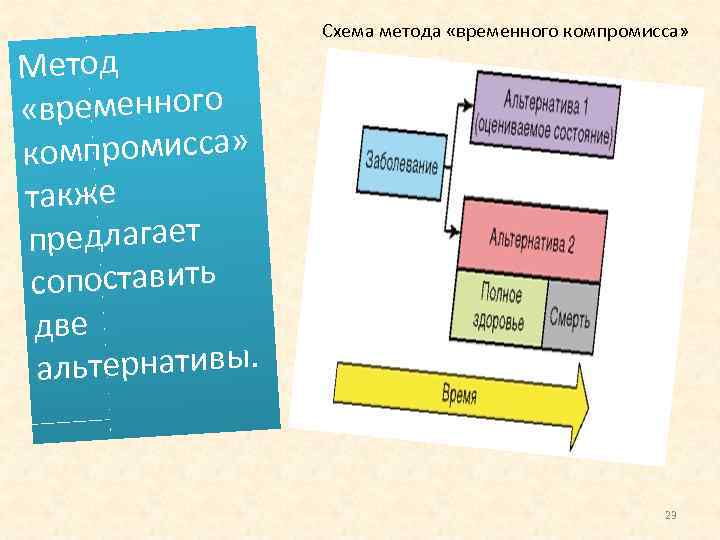 Метод «временного омпромисса» к также предлагает сопоставить две льтернативы. а Схема метода «временного компромисса» 23
Метод «временного омпромисса» к также предлагает сопоставить две льтернативы. а Схема метода «временного компромисса» 23
 Первая альтернатива является жизнью в рассматриваемом состоянии в течение оставшихся лет жизни. Вторая альтернатива представляет жизнь в состоянии полного здоровья, но в течение меньшего срока. 24
Первая альтернатива является жизнью в рассматриваемом состоянии в течение оставшихся лет жизни. Вторая альтернатива представляет жизнь в состоянии полного здоровья, но в течение меньшего срока. 24
 Респонденту предлагают сделать выбор между двумя альтернативами, постепенно изменяя время пребывания в полном здоровье второй альтернативы. Завершается оценка в тот момент, когда пациенту становится затруднительно сделать выбор. Оцениваемой полезностью в этом случае будет отношение продолжительности жизни второй альтернативы к первой. Например, если длительность жизни в оцениваемом состоянии составит 5 лет, а в полном здоровье 3 года, то полезность в этом случае будет равна 0, 6. 25
Респонденту предлагают сделать выбор между двумя альтернативами, постепенно изменяя время пребывания в полном здоровье второй альтернативы. Завершается оценка в тот момент, когда пациенту становится затруднительно сделать выбор. Оцениваемой полезностью в этом случае будет отношение продолжительности жизни второй альтернативы к первой. Например, если длительность жизни в оцениваемом состоянии составит 5 лет, а в полном здоровье 3 года, то полезность в этом случае будет равна 0, 6. 25
 Этап 2 Вычисление интегрированного показателя полезности вмешательства с учетом продолжительности периода времени, для которого он был получен. Чаще всего в расчетах используют показатель QALY (quality adjusted life years годы жизни с поправкой на ее качество) условная величина, отражающая изменения качества жизни, которых можно добиться с помощью данного метода лечения, на определенном промежутке времени. Общее значение QALY представляет собой сумму показателей, рассчитанных для всех изучаемых периодов. 26
Этап 2 Вычисление интегрированного показателя полезности вмешательства с учетом продолжительности периода времени, для которого он был получен. Чаще всего в расчетах используют показатель QALY (quality adjusted life years годы жизни с поправкой на ее качество) условная величина, отражающая изменения качества жизни, которых можно добиться с помощью данного метода лечения, на определенном промежутке времени. Общее значение QALY представляет собой сумму показателей, рассчитанных для всех изучаемых периодов. 26
 Вычисление QALY проводят путем умножения определенного на первом этапе показателя предпочтения для данного состояния здоровья на время, которое пациент предположительно проведет в этом состоянии. 27
Вычисление QALY проводят путем умножения определенного на первом этапе показателя предпочтения для данного состояния здоровья на время, которое пациент предположительно проведет в этом состоянии. 27
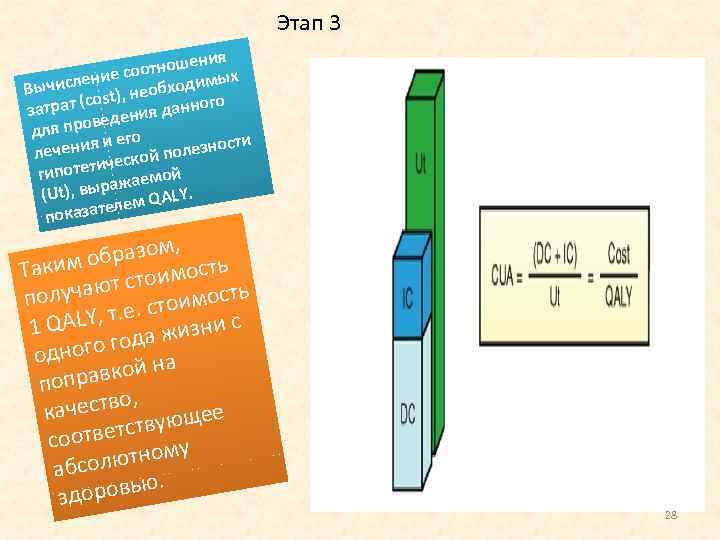 Этап 3 ния отноше ых е со числени необходим Вы ost), ого атрат (c з ия данн еден ля пров го д сти я и е лечени еской полезно ич гипотет жаемой ра (Ut), вы ем QALY. ел показат разом, ь б Таким о стоимост ь лучают по оимост ст LY, т. е. изни с 1 QA ж го года одно кой на поправ ество, кач вующее т оответс му с олютно абс ровью. здо 28
Этап 3 ния отноше ых е со числени необходим Вы ost), ого атрат (c з ия данн еден ля пров го д сти я и е лечени еской полезно ич гипотет жаемой ра (Ut), вы ем QALY. ел показат разом, ь б Таким о стоимост ь лучают по оимост ст LY, т. е. изни с 1 QA ж го года одно кой на поправ ество, кач вующее т оответс му с олютно абс ровью. здо 28
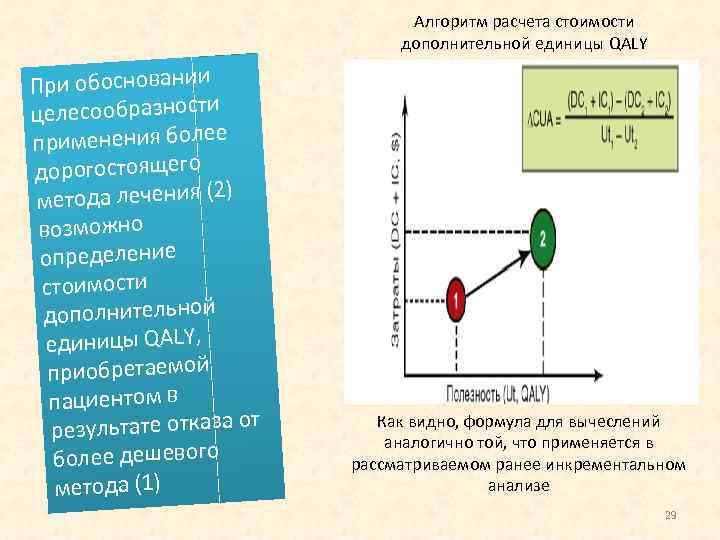 Алгоритм расчета стоимости дополнительной единицы QALY При обосновании целесообразности применения более дорогостоящего метода лечения (2) возможно определение стоимости дополнительной единицы QALY, приобретаемой пациентом в т результате отказа о более дешевого метода (1) Как видно, формула для вычеслений аналогично той, что применяется в рассматриваемом ранее инкрементальном анализе 29
Алгоритм расчета стоимости дополнительной единицы QALY При обосновании целесообразности применения более дорогостоящего метода лечения (2) возможно определение стоимости дополнительной единицы QALY, приобретаемой пациентом в т результате отказа о более дешевого метода (1) Как видно, формула для вычеслений аналогично той, что применяется в рассматриваемом ранее инкрементальном анализе 29
 Этап 4 Оценка ической эконом лемости прием ии при терап а один расчете н изни с год ж лютным абсо еством. кач 30
Этап 4 Оценка ической эконом лемости прием ии при терап а один расчете н изни с год ж лютным абсо еством. кач 30
 Безусловно, представленные стоимостные границы адаптированы для высокоразвитых стран (США и Евросоюза). Они целиком зависят от уровня экономики государства, степени инвестиций в медицину и платежеспособности населения. В нашей стране подобной градации пока не существует, и это приводит к необходимости постоянного сравнения исследуемого медицинского вмешательства с его альтернативами. 31
Безусловно, представленные стоимостные границы адаптированы для высокоразвитых стран (США и Евросоюза). Они целиком зависят от уровня экономики государства, степени инвестиций в медицину и платежеспособности населения. В нашей стране подобной градации пока не существует, и это приводит к необходимости постоянного сравнения исследуемого медицинского вмешательства с его альтернативами. 31
 из VЕМ-анал АВС/ ные типы о Дан а нередк анализ тносят к о ло пидемио э фармако о м, однак гически я тавляетс с нам пред ным ч лее логи бо в ивать их рассматр й вященно теме, пос номике. о армакоэк ф 32
из VЕМ-анал АВС/ ные типы о Дан а нередк анализ тносят к о ло пидемио э фармако о м, однак гически я тавляетс с нам пред ным ч лее логи бо в ивать их рассматр й вященно теме, пос номике. о армакоэк ф 32
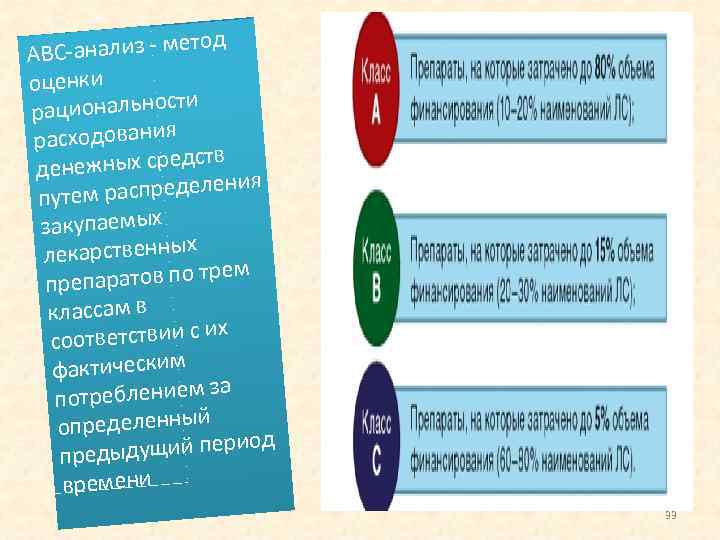 од С анализ мет АВ оценки ти рациональнос расходования ств енежных сред д аспределения путем р закупаемых лекарственных аратов по трем преп классам в х ответствии с и со фактическим реблением за пот определенный д ыдущий перио пред времени 33
од С анализ мет АВ оценки ти рациональнос расходования ств енежных сред д аспределения путем р закупаемых лекарственных аратов по трем преп классам в х ответствии с и со фактическим реблением за пот определенный д ыдущий перио пред времени 33
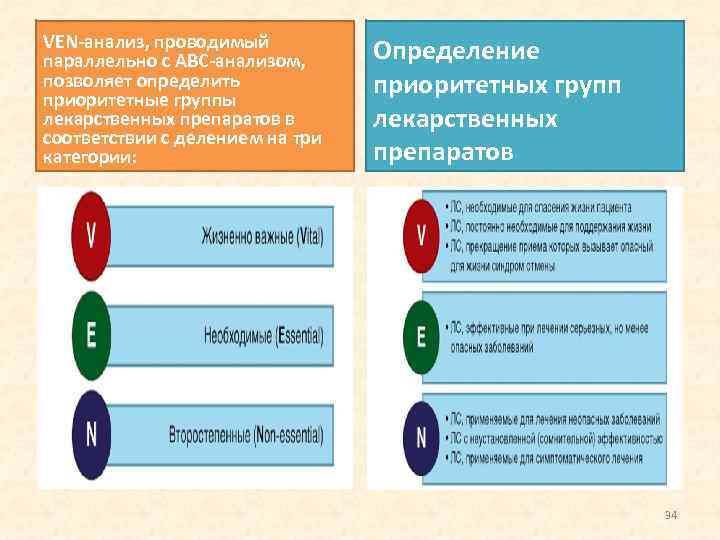 VEN-анализ, проводимый параллельно с АВС-анализом, позволяет определить приоритетные группы лекарственных препаратов в соответствии с делением на три категории: Определение приоритетных групп лекарственных препаратов 34
VEN-анализ, проводимый параллельно с АВС-анализом, позволяет определить приоритетные группы лекарственных препаратов в соответствии с делением на три категории: Определение приоритетных групп лекарственных препаратов 34
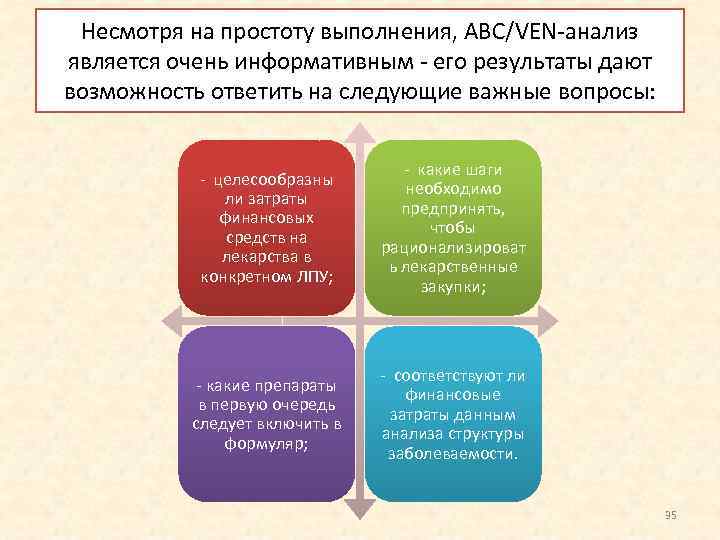 Несмотря на простоту выполнения, АВС/VEN анализ является очень информативным его результаты дают возможность ответить на следующие важные вопросы: целесообразны ли затраты финансовых средств на лекарства в конкретном ЛПУ; какие шаги необходимо предпринять, чтобы рационализироват ь лекарственные закупки; какие препараты в первую очередь следует включить в формуляр; соответствуют ли финансовые затраты данным анализа структуры заболеваемости. 35
Несмотря на простоту выполнения, АВС/VEN анализ является очень информативным его результаты дают возможность ответить на следующие важные вопросы: целесообразны ли затраты финансовых средств на лекарства в конкретном ЛПУ; какие шаги необходимо предпринять, чтобы рационализироват ь лекарственные закупки; какие препараты в первую очередь следует включить в формуляр; соответствуют ли финансовые затраты данным анализа структуры заболеваемости. 35
 • С 2003 г. в связи с изданием приказа Министерства здравоохранения РФ от 22. 10. 03 г. № 494 «О совершенствовании деятельности врачей и клинических фармакологов» этот вид анализа необходимо проводить в ЛПУ не менее одного раза в год. 36
• С 2003 г. в связи с изданием приказа Министерства здравоохранения РФ от 22. 10. 03 г. № 494 «О совершенствовании деятельности врачей и клинических фармакологов» этот вид анализа необходимо проводить в ЛПУ не менее одного раза в год. 36
 ти из стоимос Анал ess - (cost of illn болезни COI) тоимости Анализ с т использую болезни писания и о для учета т дов затра всех ви о какой либ и при енк логии, оц пато ваемого так назы » и болезни «бремен а. я обществ дл 37
ти из стоимос Анал ess - (cost of illn болезни COI) тоимости Анализ с т использую болезни писания и о для учета т дов затра всех ви о какой либ и при енк логии, оц пато ваемого так назы » и болезни «бремен а. я обществ дл 37
 Целевой аудиторией исследований с использованием этого метода являются страховые компании и организаторы здравоохранения, поскольку этот тип анализа позволяет: определить общие стоимостные границы заболевания, выход за пределы которых свидетельствует либо о неполноценности проводимого лечения, либо о его избыточности; более точно оценить целесообразность затрат на проведение профилактических мероприятий по предупреждению заболеваемости. 38
Целевой аудиторией исследований с использованием этого метода являются страховые компании и организаторы здравоохранения, поскольку этот тип анализа позволяет: определить общие стоимостные границы заболевания, выход за пределы которых свидетельствует либо о неполноценности проводимого лечения, либо о его избыточности; более точно оценить целесообразность затрат на проведение профилактических мероприятий по предупреждению заболеваемости. 38
 • Метод не используется для сравнения стоимости альтернативных вмешательств. 39
• Метод не используется для сравнения стоимости альтернативных вмешательств. 39
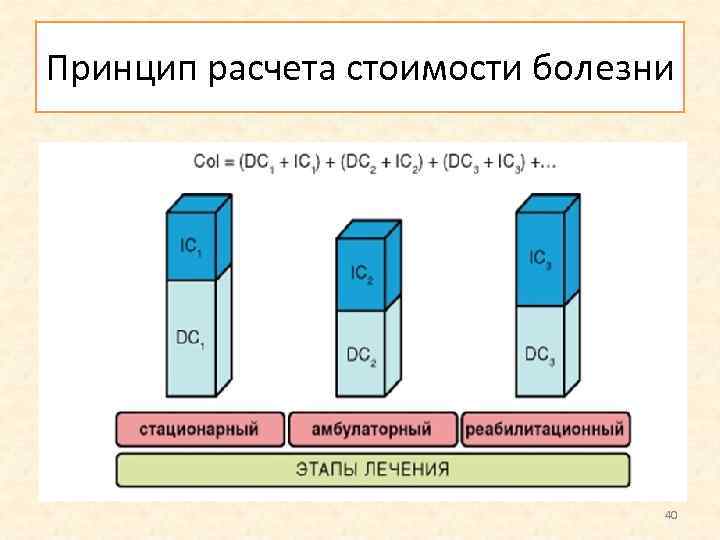 Принцип расчета стоимости болезни 40
Принцип расчета стоимости болезни 40
 Анализ «затраты последствия» (cost consequences analysis CCA) объединяющего затраты на медицинские вмешательства и достигаемые с их помощью исходы. что означает отсутствие какого либо показателя (как, например, ICER при анализе «затраты эффективность» , Анализ «затраты последствия» используется крайне редко, поскольку представляет результаты экономического анализа в дезагрегированной форме, 41
Анализ «затраты последствия» (cost consequences analysis CCA) объединяющего затраты на медицинские вмешательства и достигаемые с их помощью исходы. что означает отсутствие какого либо показателя (как, например, ICER при анализе «затраты эффективность» , Анализ «затраты последствия» используется крайне редко, поскольку представляет результаты экономического анализа в дезагрегированной форме, 41
 Такой подход позволяет организаторам здравоохранения присвоить определенным состояниям здоровья собственную значимость перед сравнением двух различных вмешательств (например, лечение бесплодия по сравнению со снижением уровня холестерина). Различные исходы при этом выражаются в терминах естественных единиц (месяцы выживания; ампутированные конечности; дети, выписанные домой и т. д. ). 42
Такой подход позволяет организаторам здравоохранения присвоить определенным состояниям здоровья собственную значимость перед сравнением двух различных вмешательств (например, лечение бесплодия по сравнению со снижением уровня холестерина). Различные исходы при этом выражаются в терминах естественных единиц (месяцы выживания; ампутированные конечности; дети, выписанные домой и т. д. ). 42
 МЕТОДЫ ФАРМАКОЭКОНОМИЧЕСКОГО МОДЕЛИРОВАНИЯ Моделирование является одним из методов фармакоэкономического анализа, который в последнее время приобретает все большую популярность. В общем случае, моделирование способ изучения различных объектов, процессов и явлений, основанный на использовании математических (логических) моделей, представляющих собой упрощенное описание изучаемого объекта (пациента, заболевания, эпидемиологической ситуации) и его динамику при использовании медицинских вмешательств. 43
МЕТОДЫ ФАРМАКОЭКОНОМИЧЕСКОГО МОДЕЛИРОВАНИЯ Моделирование является одним из методов фармакоэкономического анализа, который в последнее время приобретает все большую популярность. В общем случае, моделирование способ изучения различных объектов, процессов и явлений, основанный на использовании математических (логических) моделей, представляющих собой упрощенное описание изучаемого объекта (пациента, заболевания, эпидемиологической ситуации) и его динамику при использовании медицинских вмешательств. 43
 Наиболее часто применительно к фармакоэкономике используются два типа моделей: модель Маркова. модель «дерево решений» ; 44
Наиболее часто применительно к фармакоэкономике используются два типа моделей: модель Маркова. модель «дерево решений» ; 44
 Модель «дерево решений» обычно используется для описания процесса лечения острого заболевания. Данный вид моделей подразумевает наличие нескольких альтернатив всех прогнозируемых вариантов течения заболевания. При этом вероятность каждого из исходов известна и возможно рассчитать стоимость каждого исхода (разумеется, не вручную, а с привлечением компьютерных программ). Экономическая оценка каждого из них (с учетом вероятности развития) позволяет прогнозироевать вероятные затраты на одного больного и на население в целом (на основании статистических данных). 45
Модель «дерево решений» обычно используется для описания процесса лечения острого заболевания. Данный вид моделей подразумевает наличие нескольких альтернатив всех прогнозируемых вариантов течения заболевания. При этом вероятность каждого из исходов известна и возможно рассчитать стоимость каждого исхода (разумеется, не вручную, а с привлечением компьютерных программ). Экономическая оценка каждого из них (с учетом вероятности развития) позволяет прогнозироевать вероятные затраты на одного больного и на население в целом (на основании статистических данных). 45
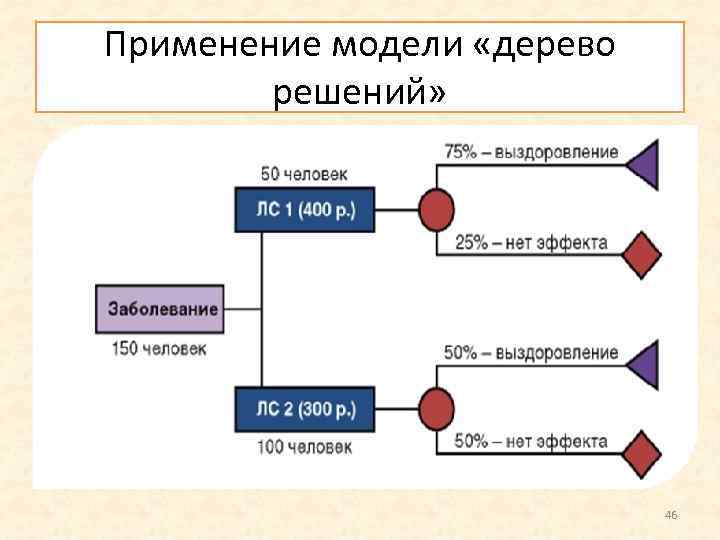 Применение модели «дерево решений» 46
Применение модели «дерево решений» 46
 При анализе лечения хронических заболеваний более удобным считается использование модели Маркова. Модель допускает, что пациент всегда находится в одном из конечных состояний здоровья, называемых состояниями Маркова. В течение определенного временного интервала (цикла Маркова) возможен переход из одного состояния в другое с известной вероятностью, допустимой для отдельной группы пациентов. Длительность циклов зависит от особенностей болезни и предлагаемого лечения, обычно составляя один год. Типичный метод представления марковских моделей древо марковских циклов. Каждое состояние отображается в нем в виде ответвлений от марковского узла. В дальнейшем эта модель обрабатывается с помощью специализированного программого обеспечения и на основании полученных результатов строятся окончательные выводы. 47
При анализе лечения хронических заболеваний более удобным считается использование модели Маркова. Модель допускает, что пациент всегда находится в одном из конечных состояний здоровья, называемых состояниями Маркова. В течение определенного временного интервала (цикла Маркова) возможен переход из одного состояния в другое с известной вероятностью, допустимой для отдельной группы пациентов. Длительность циклов зависит от особенностей болезни и предлагаемого лечения, обычно составляя один год. Типичный метод представления марковских моделей древо марковских циклов. Каждое состояние отображается в нем в виде ответвлений от марковского узла. В дальнейшем эта модель обрабатывается с помощью специализированного программого обеспечения и на основании полученных результатов строятся окончательные выводы. 47
 Марковский анализ рекомендуют использовать в следующих случаях: время наступления эффекта может повлиять на его полезность (например, раннее обнаружение рака по сравнению с поздним); клинические решения влияют на исходы, возникающие на различных этапах жизни пациента. время наступления события точно не определено; 48
Марковский анализ рекомендуют использовать в следующих случаях: время наступления эффекта может повлиять на его полезность (например, раннее обнаружение рака по сравнению с поздним); клинические решения влияют на исходы, возникающие на различных этапах жизни пациента. время наступления события точно не определено; 48
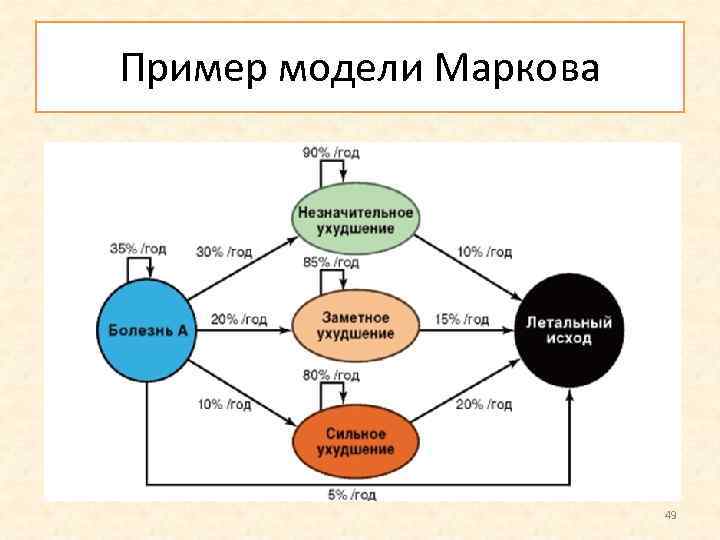 Пример модели Маркова 49
Пример модели Маркова 49
 В настоящее время для оценки эффективности любого изучаемого препарата необходимо использовать принцип трех «Е» , позволяющий сделать выбор в пользу наиболее оптимального. Каждый из этих терминов в переводе с английского означает «эффективность» , однако в каждом случае требования к ней все более строгие. Дадим краткие пояснения, которые не имеют отношения к фармакоэкономике, однако помогут лучше понять суть данной градации. 50
В настоящее время для оценки эффективности любого изучаемого препарата необходимо использовать принцип трех «Е» , позволяющий сделать выбор в пользу наиболее оптимального. Каждый из этих терминов в переводе с английского означает «эффективность» , однако в каждом случае требования к ней все более строгие. Дадим краткие пояснения, которые не имеют отношения к фармакоэкономике, однако помогут лучше понять суть данной градации. 50
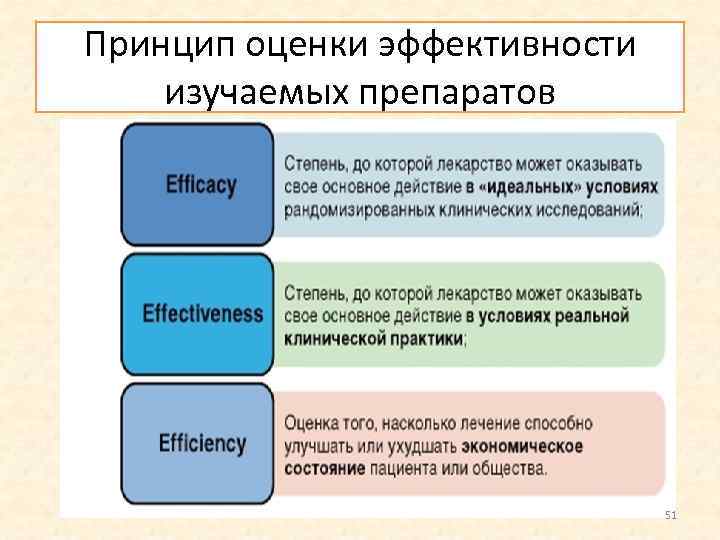 Принцип оценки эффективности изучаемых препаратов 51
Принцип оценки эффективности изучаемых препаратов 51
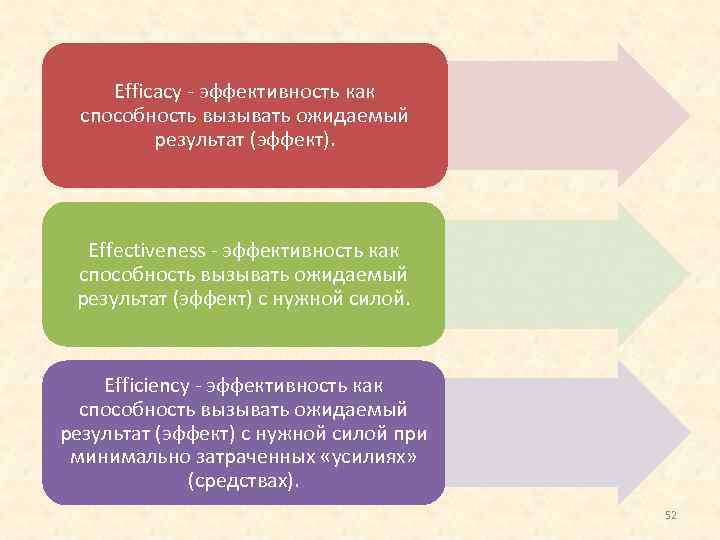 Efficacy эффективность как способность вызывать ожидаемый результат (эффект). Effectiveness эффективность как способность вызывать ожидаемый результат (эффект) с нужной силой. Efficiency эффективность как способность вызывать ожидаемый результат (эффект) с нужной силой при минимально затраченных «усилиях» (средствах). 52
Efficacy эффективность как способность вызывать ожидаемый результат (эффект). Effectiveness эффективность как способность вызывать ожидаемый результат (эффект) с нужной силой. Efficiency эффективность как способность вызывать ожидаемый результат (эффект) с нужной силой при минимально затраченных «усилиях» (средствах). 52
 Фармакоэкономический анализ должен стать неотъемлемой частью принятия решения о необходимости включения любого лекарственного средства в «ограничительные списки» и стандарты лечения. Всем известно, что лечиться дорого, но неправильно лечиться - еще дороже. 53
Фармакоэкономический анализ должен стать неотъемлемой частью принятия решения о необходимости включения любого лекарственного средства в «ограничительные списки» и стандарты лечения. Всем известно, что лечиться дорого, но неправильно лечиться - еще дороже. 53
 Фазы клинического исследования чтобы в ходе исследований, предшествующих регистрации нового ЛС, была получена как можно более точная и полная информация о клинической фармакологии, терапевтической эффективности и безопасности нового ЛС. Производитель и общество заинтересованы в том, 54
Фазы клинического исследования чтобы в ходе исследований, предшествующих регистрации нового ЛС, была получена как можно более точная и полная информация о клинической фармакологии, терапевтической эффективности и безопасности нового ЛС. Производитель и общество заинтересованы в том, 54
 Время, необходимое для разработки и внедрения нового ЛС. Общий цикл исследований нового ЛС обычно превышает 10 лет. В связи с этим неудивительно, что разработка новых ЛС остаётся уделом только крупных фармацевтически х компаний, а общая стоимость исследовательского проекта превышает 500 млн долларов США. 55
Время, необходимое для разработки и внедрения нового ЛС. Общий цикл исследований нового ЛС обычно превышает 10 лет. В связи с этим неудивительно, что разработка новых ЛС остаётся уделом только крупных фармацевтически х компаний, а общая стоимость исследовательского проекта превышает 500 млн долларов США. 55
 Клинические испытания нового ЛС завершающая стадия длительного и трудоёмкого процесса их разработки. Клинические испытания ЛС перед их официальным разрешением к медицинскому применению проводят в 4 этапа, традиционно называемые «фазы клинических исследований» . 56
Клинические испытания нового ЛС завершающая стадия длительного и трудоёмкого процесса их разработки. Клинические испытания ЛС перед их официальным разрешением к медицинскому применению проводят в 4 этапа, традиционно называемые «фазы клинических исследований» . 56
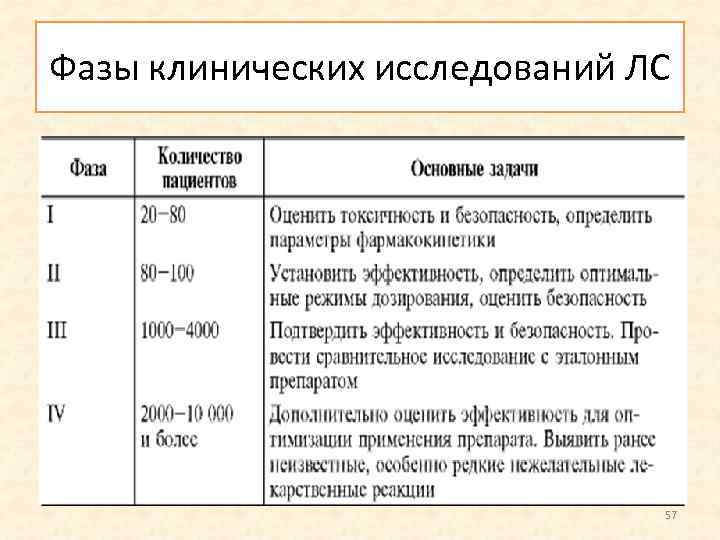 Фазы клинических исследований ЛС 57
Фазы клинических исследований ЛС 57
 Фаза I начальный этап клинических исследований, поисковый и особенно тщательно контролируемый. Обычно клинические испытания I фазы проводят на здоровых добровольцах мужского пола (18 45 лет), однако при изучении препаратов с высокой потенциальной токсичностью (например, противоопухолевые, противоретровирусные препараты) может быть получено разрешение на исследование у пациентов. 58
Фаза I начальный этап клинических исследований, поисковый и особенно тщательно контролируемый. Обычно клинические испытания I фазы проводят на здоровых добровольцах мужского пола (18 45 лет), однако при изучении препаратов с высокой потенциальной токсичностью (например, противоопухолевые, противоретровирусные препараты) может быть получено разрешение на исследование у пациентов. 58
 Исследуемое соединение назначают в низких дозах с постепенным их повышением до появления признаков токсического действия, параллельно определяют концентрацию препарата или его активных метаболитов в плазме крови, тщательно контролируют клинические и лабораторные данные испытуемых для выявления нежелательных лекарственных реакций. Цель I фазы получение информации о максимальной безопасной дозе. 59
Исследуемое соединение назначают в низких дозах с постепенным их повышением до появления признаков токсического действия, параллельно определяют концентрацию препарата или его активных метаболитов в плазме крови, тщательно контролируют клинические и лабораторные данные испытуемых для выявления нежелательных лекарственных реакций. Цель I фазы получение информации о максимальной безопасной дозе. 59
 Начальную токсическую дозу определяют в доклинических исследованиях, у человека она составляет 1/10 экспериментальной. Клинические испытания I фазы проводят в специализированных клиниках, оснащённых оборудованием для оказания экстренной медицинской помощи. 60
Начальную токсическую дозу определяют в доклинических исследованиях, у человека она составляет 1/10 экспериментальной. Клинические испытания I фазы проводят в специализированных клиниках, оснащённых оборудованием для оказания экстренной медицинской помощи. 60
 Фаза II ключевая, так как полученные сведения определяют целесообразность продолжения исследования нового ЛС. Цель доказательство клинической эффективности и безопасности ЛС при испытании на чётко очерченных контингентах больных, установление оптимального режима дозирования. Сравнивают эффективность и безопасность изучаемого препарата с эталонным и плацебо. 61
Фаза II ключевая, так как полученные сведения определяют целесообразность продолжения исследования нового ЛС. Цель доказательство клинической эффективности и безопасности ЛС при испытании на чётко очерченных контингентах больных, установление оптимального режима дозирования. Сравнивают эффективность и безопасность изучаемого препарата с эталонным и плацебо. 61
 я ытани Исп т меваю азу II подр Фаза е наличи ванного ро сплани чётких а, дизайн в е я, ритери я/исключени к и ключен ации, в из рандом ия, процедур. ля ен ослепл щего контро ую послед та фаза о э Обычн ается около 2 ж продол лет. 62
я ытани Исп т меваю азу II подр Фаза е наличи ванного ро сплани чётких а, дизайн в е я, ритери я/исключени к и ключен ации, в из рандом ия, процедур. ля ен ослепл щего контро ую послед та фаза о э Обычн ается около 2 ж продол лет. 62
 Фаза III если препарат оказался эффективен и безопасен во II фазе, его исследуют в фазе III. Клинические испытания III фазы контролируемые, многоцентровые исследования (исследования, проводимые по единому протоколу более чем в одном исследовательском центре), спланированные для определения безопасности и эффективности ЛС в условиях, приближённых к тем, в которых оно будет использовано в случае его разрешения к медицинскому применению. 63
Фаза III если препарат оказался эффективен и безопасен во II фазе, его исследуют в фазе III. Клинические испытания III фазы контролируемые, многоцентровые исследования (исследования, проводимые по единому протоколу более чем в одном исследовательском центре), спланированные для определения безопасности и эффективности ЛС в условиях, приближённых к тем, в которых оно будет использовано в случае его разрешения к медицинскому применению. 63
 Обычно исследования имеют сравнительный дизайн по отношению к существующей стандартной терапии. Полученные сведения уточняют эффективность лекарственного препарата у больных с учётом сопутствующих заболеваний, различных демографических характеристик и режима дозирования. После завершения этой фазы и регистрации фармакологическое средство приобретает статус ЛС (процесса последовательных экспертных и административно правовых действий) с занесением в Государственный реестр РФ и присвоением ему регистрационного номера 64
Обычно исследования имеют сравнительный дизайн по отношению к существующей стандартной терапии. Полученные сведения уточняют эффективность лекарственного препарата у больных с учётом сопутствующих заболеваний, различных демографических характеристик и режима дозирования. После завершения этой фазы и регистрации фармакологическое средство приобретает статус ЛС (процесса последовательных экспертных и административно правовых действий) с занесением в Государственный реестр РФ и присвоением ему регистрационного номера 64
 Дженерики допускают в обращение после истечения срока патентной защиты оригинального препарата на основании оценки регистрационного досье сокращенного объёма и данных по биоэквивалентности. Конкуренция с новыми препаратами заставляет продолжать исследования и после регистрации, для того чтобы подтвердить эффективность препарата и его место в фармакотерапии. 65
Дженерики допускают в обращение после истечения срока патентной защиты оригинального препарата на основании оценки регистрационного досье сокращенного объёма и данных по биоэквивалентности. Конкуренция с новыми препаратами заставляет продолжать исследования и после регистрации, для того чтобы подтвердить эффективность препарата и его место в фармакотерапии. 65
 Фаза IV (постмаркетинговые исследования). Клинические испытания IV фазы проводят после того, как препарат разрешён для клинического применения по определённому показанию. Цель IV фазы уточнение особенностей действия ЛС, дополнительная оценка его эффективности и безопасности у большого количества пациентов. 66
Фаза IV (постмаркетинговые исследования). Клинические испытания IV фазы проводят после того, как препарат разрешён для клинического применения по определённому показанию. Цель IV фазы уточнение особенностей действия ЛС, дополнительная оценка его эффективности и безопасности у большого количества пациентов. 66
 Их назначение выявить ранее неизвестные, особенно редкие побочные эффекты, Расширенные пострегистрационные клинические исследования характеризуются широким применением нового лекарственного препарата в медицинской практике. а также случаи лекарственного взаимодействия на большой и разнородной популяции пациентов, влияние отдаленных эффектов препарата на выживаемость (снижение или повышение уровня смертности). Полученные данные могут послужить основанием для внесения соответствующих изменений в инструкцию по медицинскому применению препарата. 67
Их назначение выявить ранее неизвестные, особенно редкие побочные эффекты, Расширенные пострегистрационные клинические исследования характеризуются широким применением нового лекарственного препарата в медицинской практике. а также случаи лекарственного взаимодействия на большой и разнородной популяции пациентов, влияние отдаленных эффектов препарата на выживаемость (снижение или повышение уровня смертности). Полученные данные могут послужить основанием для внесения соответствующих изменений в инструкцию по медицинскому применению препарата. 67
 Другие 8 новых зарегистрированных ЛС примерно окупают расходы на своё создание, и ещё 1 препарат из 10 причиняет убытки своему производителю и/или снимается с производства. принося производителю значительную прибыль. Несмотря на существенные затраты и строгую оценку эффективности лишь 1 изкаждых 10 новых зарегистрированных препаратов занимает лидирующее положение на рынке ЛС, 68
Другие 8 новых зарегистрированных ЛС примерно окупают расходы на своё создание, и ещё 1 препарат из 10 причиняет убытки своему производителю и/или снимается с производства. принося производителю значительную прибыль. Несмотря на существенные затраты и строгую оценку эффективности лишь 1 изкаждых 10 новых зарегистрированных препаратов занимает лидирующее положение на рынке ЛС, 68
 Цели клинического исследования исследование фармакологического действия препарата на человека, установление терапевтической (лечебной) эффективности или подтверждение терапевтической эффективности в сравнении с другими ЛС, изучение безопасности и переносимости ЛС, а также определение терапевтического применения, то есть той «ниши» , которую может занимать данный препарат в современной фармакотерапии. 69
Цели клинического исследования исследование фармакологического действия препарата на человека, установление терапевтической (лечебной) эффективности или подтверждение терапевтической эффективности в сравнении с другими ЛС, изучение безопасности и переносимости ЛС, а также определение терапевтического применения, то есть той «ниши» , которую может занимать данный препарат в современной фармакотерапии. 69
 Исследование может быть этапом подготовки препарата к регистрации, способствовать продвижению на рынок уже зарегистрированного препарата или служить инструментом решения научных проблем. 70
Исследование может быть этапом подготовки препарата к регистрации, способствовать продвижению на рынок уже зарегистрированного препарата или служить инструментом решения научных проблем. 70
 «Конечные точки» в клинических исследованиях Для оценки и эффективност ового ЛС по н результатам инических кл исследований могут быть использованы первичные, вторичные и третичные . ечные точки» «кон 71
«Конечные точки» в клинических исследованиях Для оценки и эффективност ового ЛС по н результатам инических кл исследований могут быть использованы первичные, вторичные и третичные . ечные точки» «кон 71
 Эти основные показатели оценивают в контролируемых сравнительных исследованиях по результатам лечения по крайней мере в двух группах: и группе сравнения (больные не получают изучаемый препарат или принимают известный препарат сравнения). основной (больные получают новый способ лечения или новый препарат) 72
Эти основные показатели оценивают в контролируемых сравнительных исследованиях по результатам лечения по крайней мере в двух группах: и группе сравнения (больные не получают изучаемый препарат или принимают известный препарат сравнения). основной (больные получают новый способ лечения или новый препарат) 72
 Например, при исследовании эффективности лечения и профилактики ИБС выделяют следующие «конечные точки» . Первичные основные показатели, связанные с возможностью увеличения продолжительности жизни больного. В клинических исследованиях к ним относят снижение общей смертности, смертности от сердечно сосудистых заболеваний, в частности инфаркта миокарда и инсульта. 73
Например, при исследовании эффективности лечения и профилактики ИБС выделяют следующие «конечные точки» . Первичные основные показатели, связанные с возможностью увеличения продолжительности жизни больного. В клинических исследованиях к ним относят снижение общей смертности, смертности от сердечно сосудистых заболеваний, в частности инфаркта миокарда и инсульта. 73
 Вторичные показатели отражают улучшение качества жизни либо вследствие снижения заболеваемости, либо облегчения симптомов заболевания (например, уменьшение частоты приступов стенокардии, увеличение толерантности к физической нагрузке). 74
Вторичные показатели отражают улучшение качества жизни либо вследствие снижения заболеваемости, либо облегчения симптомов заболевания (например, уменьшение частоты приступов стенокардии, увеличение толерантности к физической нагрузке). 74
 Третичные показатели, связанные с возможностью профилактики заболевания (например, у больных с ИБС стабилизация АД, нормализация содержания глюкозы в крови, снижение концентрации общего холестерина, ЛПНП и т. д. ). 75
Третичные показатели, связанные с возможностью профилактики заболевания (например, у больных с ИБС стабилизация АД, нормализация содержания глюкозы в крови, снижение концентрации общего холестерина, ЛПНП и т. д. ). 75
 ета анализ М етод поиска, м оценки и объединения результатов нескольких онтролируем к ых исследований. 76
ета анализ М етод поиска, м оценки и объединения результатов нескольких онтролируем к ых исследований. 76
 которые не могут быть выявлены в отдельных клинических исследованиях. В результате мета анализа можно установить положительные или нежелательные эффекты лечения, Необходимо, чтобы включённые в метаанализ исследования были тщательно рандомизирован ы, их результаты опубликованы с подробным протоколом исследования, указанием критериев отбора и оценки, выбора конечных точек. 77
которые не могут быть выявлены в отдельных клинических исследованиях. В результате мета анализа можно установить положительные или нежелательные эффекты лечения, Необходимо, чтобы включённые в метаанализ исследования были тщательно рандомизирован ы, их результаты опубликованы с подробным протоколом исследования, указанием критериев отбора и оценки, выбора конечных точек. 77
 а в одном увеличение количества смертельных случаев, что является наиболее важным показателем для оценки действия этого препарата. Например, в двух метаанализах установлено благоприятное действие лидокаина при аритмии у больных с инфарктом миокарда, 78
а в одном увеличение количества смертельных случаев, что является наиболее важным показателем для оценки действия этого препарата. Например, в двух метаанализах установлено благоприятное действие лидокаина при аритмии у больных с инфарктом миокарда, 78
 в которые были включены около 60 000 пациентов. была установлена на основании метаанализа 65 рандомизиров анных клинических исследований, Целесообразность назначения низких доз аспирина для снижения смертности и развития сердечно сосудистых осложнений у пациентов высокого риска 79
в которые были включены около 60 000 пациентов. была установлена на основании метаанализа 65 рандомизиров анных клинических исследований, Целесообразность назначения низких доз аспирина для снижения смертности и развития сердечно сосудистых осложнений у пациентов высокого риска 79
 Дизайн исследования в настоящее время практически не используют из за низкой доказательности получаемых результатов. Исследования, в котором все пациенты получают одинаковое лечение, Клиническое исследование может иметь различный дизайн. 80
Дизайн исследования в настоящее время практически не используют из за низкой доказательности получаемых результатов. Исследования, в котором все пациенты получают одинаковое лечение, Клиническое исследование может иметь различный дизайн. 80
 Наиболее распространено сравнительное исследование в параллельных группах (группа «вмешательство» и группа «контроля» ). В качестве контроля может выступать плацебо (плацебоконтролируемое исследование) или другой активный препарат. 81
Наиболее распространено сравнительное исследование в параллельных группах (группа «вмешательство» и группа «контроля» ). В качестве контроля может выступать плацебо (плацебоконтролируемое исследование) или другой активный препарат. 81
 отличить эффект ЛС от спонтанных ремиссий в течение заболевания и влияния внешних факторов, Использование плацебо позволяет разграничить собственно фармакодинамич еские и суггестивные эффекты препарата, избежать получения ложноотрицатель ных заключений (например, равная эффективность исследуемого препарата и плацебо может быть связана с применением недостаточно чувствительного метода оценки эффекта или низкой дозой ЛС). 82
отличить эффект ЛС от спонтанных ремиссий в течение заболевания и влияния внешних факторов, Использование плацебо позволяет разграничить собственно фармакодинамич еские и суггестивные эффекты препарата, избежать получения ложноотрицатель ных заключений (например, равная эффективность исследуемого препарата и плацебо может быть связана с применением недостаточно чувствительного метода оценки эффекта или низкой дозой ЛС). 82
 Исследования со сравнительным дизайном требуют проведения рандомизации распределения испытуемых на опытную и контрольную группы случайным образом, что позволяет создать схожие исходные условия и свести к минимуму систематическую ошибку и предвзятость отбора больных. 83
Исследования со сравнительным дизайном требуют проведения рандомизации распределения испытуемых на опытную и контрольную группы случайным образом, что позволяет создать схожие исходные условия и свести к минимуму систематическую ошибку и предвзятость отбора больных. 83
 Процесс рандомизации, длительность лечения, последовательности периодов лечения и критерии прекращения испытания отражают в дизайне исследования. С проблемой рандомизации тесно связана проблема «слепоты» исследования. 84
Процесс рандомизации, длительность лечения, последовательности периодов лечения и критерии прекращения испытания отражают в дизайне исследования. С проблемой рандомизации тесно связана проблема «слепоты» исследования. 84
 Идеально испытание с использованием двойного слепого метода, когда ни пациент, ни врач не знают, какое лечение получает пациент. Цель слепого метода устранение возможности влияния (осознанного или случайного) врача, исследователя, пациента на полученные результаты. Исследователь может получить доступ к информации о том, какое именно ЛС получает пациент (это может потребоваться при возникновении серьёзных нежелательных реакций), но в этом случае пациент должен быть исключён из исследования. 85
Идеально испытание с использованием двойного слепого метода, когда ни пациент, ни врач не знают, какое лечение получает пациент. Цель слепого метода устранение возможности влияния (осознанного или случайного) врача, исследователя, пациента на полученные результаты. Исследователь может получить доступ к информации о том, какое именно ЛС получает пациент (это может потребоваться при возникновении серьёзных нежелательных реакций), но в этом случае пациент должен быть исключён из исследования. 85
 ия - Протокол исследован основной документ ый исследования, котор «описывает задачи, стические методологию, стати ию аспекты и организац исследования» . На основании ссмотрения ра протокола выдаётся зрешение на ра проведение сследования. и 86
ия - Протокол исследован основной документ ый исследования, котор «описывает задачи, стические методологию, стати ию аспекты и организац исследования» . На основании ссмотрения ра протокола выдаётся зрешение на ра проведение сследования. и 86
 нутренний В иторинг) и (мон ий (аудит) внешн онтроль за к едением пров ледования исс жде всего пре енивает оц тветствие соо действий дователей иссле цедуре, про санной в опи отоколе. пр 87
нутренний В иторинг) и (мон ий (аудит) внешн онтроль за к едением пров ледования исс жде всего пре енивает оц тветствие соо действий дователей иссле цедуре, про санной в опи отоколе. пр 87
 Размер исследования Никаких нормативов, кроме получения необходимой статистической достоверности при определении числа пациентов, участвующих в исследовании, не существует. Небольшое количество пациентов не позволяет добиться однородности сравниваемых групп и статистически достоверного эффекта вмешательства. Размер РКИ зависит от ожидаемого клинически значимого эффекта вмешательства. 88
Размер исследования Никаких нормативов, кроме получения необходимой статистической достоверности при определении числа пациентов, участвующих в исследовании, не существует. Небольшое количество пациентов не позволяет добиться однородности сравниваемых групп и статистически достоверного эффекта вмешательства. Размер РКИ зависит от ожидаемого клинически значимого эффекта вмешательства. 88
 Типичным исходным показателем, необходимым для расчета размера РКИ, является ожидаемый исход заболевания при стандартном общепринятом лечении на момент планирования исследования. Кроме этого, весьма полезными оказываются данные закончившихся РКИ по аналогичной тематике. 89
Типичным исходным показателем, необходимым для расчета размера РКИ, является ожидаемый исход заболевания при стандартном общепринятом лечении на момент планирования исследования. Кроме этого, весьма полезными оказываются данные закончившихся РКИ по аналогичной тематике. 89
 В свою очередь степень достоверности ложноотрицательно го результата обычно устанавливается на уровне 0, 1 ( «b» или «II тип ошибки» ). При этом степень достоверности получения ложноположител ьного обычно устанавливается на уровне 0, 05 ( «а» или «I тип ошибки» ). Принято считать, что снижение относительного риска исхода заболевания на 20% является клинически значимым. 90
В свою очередь степень достоверности ложноотрицательно го результата обычно устанавливается на уровне 0, 1 ( «b» или «II тип ошибки» ). При этом степень достоверности получения ложноположител ьного обычно устанавливается на уровне 0, 05 ( «а» или «I тип ошибки» ). Принято считать, что снижение относительного риска исхода заболевания на 20% является клинически значимым. 90
 Размер РКИ, в котором в качестве критериев эффективности вмешательства используются дискретные показатели исхода заболевания, всегда больше, чем размер такого же РКИ, но в котором критерием эффективности вмешательства являются продолженные показатели исхода заболевания (средние величины показателя или функционального исхода). 91
Размер РКИ, в котором в качестве критериев эффективности вмешательства используются дискретные показатели исхода заболевания, всегда больше, чем размер такого же РКИ, но в котором критерием эффективности вмешательства являются продолженные показатели исхода заболевания (средние величины показателя или функционального исхода). 91
 Достаточность групп наблюдения зависит от степени предполагаемых различий в эффекте вмешательства в опытной и контрольной группах, видом статистического показателя эффекта вмешательства (частоты, средние величины). Естественно, чем больше ожидаемое различие в эффекте между ними, тем меньше окажется необходимое число наблюдений. При одинаковой степени точности необходимое число наблюдений будет значительно меньше, когда для оценки эффекта вмешательства используются средние величины, а не частотные показатели. 92
Достаточность групп наблюдения зависит от степени предполагаемых различий в эффекте вмешательства в опытной и контрольной группах, видом статистического показателя эффекта вмешательства (частоты, средние величины). Естественно, чем больше ожидаемое различие в эффекте между ними, тем меньше окажется необходимое число наблюдений. При одинаковой степени точности необходимое число наблюдений будет значительно меньше, когда для оценки эффекта вмешательства используются средние величины, а не частотные показатели. 92
 При проведении исследования очень важно получить достоверную информацию об эффективности вмешательства в возможно более сжатые сроки. Для этого используют многоцентровые РКИ. В них происходит кооперирование (часто международное) и стандартизация исследовательских центров по единой программе и методам наблюдения, что позволяет получить сопоставимые данные разных учреждений. 93
При проведении исследования очень важно получить достоверную информацию об эффективности вмешательства в возможно более сжатые сроки. Для этого используют многоцентровые РКИ. В них происходит кооперирование (часто международное) и стандартизация исследовательских центров по единой программе и методам наблюдения, что позволяет получить сопоставимые данные разных учреждений. 93
 Выбор больных Вторым по значимости разделом РКИ (после формулирования цели и задач исследования) является определение критериев включения и исключения из исследования. Критерии включения предопределяются целью исследования, более широкие из них облегчают набор пациентов и позволяют экстраполировать полученные результаты на большую популяцию больных. Однако в этом случае существует опасность формирования разнородных исследуемых групп больных как по исходным клинико демографическим показателям, так и по эффективности тестируемого вмешательства. Обычно в РКИ включают пациентов со средней тяжестью заболевания, хотя у пациентов с исходно более высоким риском осложнений можно в более короткие сроки оценить эффект вмешательства на жесткие конечные точки. 94
Выбор больных Вторым по значимости разделом РКИ (после формулирования цели и задач исследования) является определение критериев включения и исключения из исследования. Критерии включения предопределяются целью исследования, более широкие из них облегчают набор пациентов и позволяют экстраполировать полученные результаты на большую популяцию больных. Однако в этом случае существует опасность формирования разнородных исследуемых групп больных как по исходным клинико демографическим показателям, так и по эффективности тестируемого вмешательства. Обычно в РКИ включают пациентов со средней тяжестью заболевания, хотя у пациентов с исходно более высоким риском осложнений можно в более короткие сроки оценить эффект вмешательства на жесткие конечные точки. 94
 Группа пациентов с низким риском и легким течением заболевания требует длительного наблюдения и потенциально опасна в получении статистически достоверного эффекта вмешательства, тогда как на самом деле оно может оказаться эффективным. Критерии исключения должны минимизировать возможность ошибок при проведении исследования (например, исключение из исследования больных с терминальной стадией заболевания, сниженной функцией печени и почек). 95
Группа пациентов с низким риском и легким течением заболевания требует длительного наблюдения и потенциально опасна в получении статистически достоверного эффекта вмешательства, тогда как на самом деле оно может оказаться эффективным. Критерии исключения должны минимизировать возможность ошибок при проведении исследования (например, исключение из исследования больных с терминальной стадией заболевания, сниженной функцией печени и почек). 95
 Если данный контингент пациентов не является предметом РКИ, в него обычно не включают и психических больных. онкологических несовершеннолетних, женщин в период беременности и лактации или не использующих контрацепцию, 96
Если данный контингент пациентов не является предметом РКИ, в него обычно не включают и психических больных. онкологических несовершеннолетних, женщин в период беременности и лактации или не использующих контрацепцию, 96
 а также исключение применения в них во время исследования препаратов, сходных с испытуемым. В целом чем крупнее РКИ и чем быстрее его планируют закончить, шире должны быть критерии включения и тем меньше критериев исключения. Важной задачей критериев исключения является обеспечение одинакового лечения и ведение пациентов в исследуемой и контрольной группах, 97
а также исключение применения в них во время исследования препаратов, сходных с испытуемым. В целом чем крупнее РКИ и чем быстрее его планируют закончить, шире должны быть критерии включения и тем меньше критериев исключения. Важной задачей критериев исключения является обеспечение одинакового лечения и ведение пациентов в исследуемой и контрольной группах, 97
 Этические и правовые нормы клинических исследований Они регламентированы вышеперечисленным и документами, Гарантии прав субъектов исследования и соблюдение этических норм сложная проблема клинических испытаний. гарантом соблюдения прав пациентов служит Независимый этический комитет, одобрение которого необходимо получить до начала клинических испытаний. Основная задача Независимого этического комитета защита прав и здоровья субъектов исследования, а также гарантия их безопасности. 98
Этические и правовые нормы клинических исследований Они регламентированы вышеперечисленным и документами, Гарантии прав субъектов исследования и соблюдение этических норм сложная проблема клинических испытаний. гарантом соблюдения прав пациентов служит Независимый этический комитет, одобрение которого необходимо получить до начала клинических испытаний. Основная задача Независимого этического комитета защита прав и здоровья субъектов исследования, а также гарантия их безопасности. 98
 Независимый ет тический комит э рассматривает информацию о ктуру препарате, стру протокола клинического испытания, содержание ого информированн фии гласия и биогра со с исследователей нкой следующей оце по ожидаемых польза/риск для пациентов. 99
Независимый ет тический комит э рассматривает информацию о ктуру препарате, стру протокола клинического испытания, содержание ого информированн фии гласия и биогра со с исследователей нкой следующей оце по ожидаемых польза/риск для пациентов. 99
 Субъект может участвовать в клинических испытаниях только при полном и сознательном добровольном согласии. Каждый участник исследования должен быть заранее информирован о целях, методах, ожидаемом риске и пользе, обеспечении его необходимой медицинской помощью в случае выявления нежелательных реакций в ходе испытания, страховании на случай причинения ущерба здоровью, связанного с участием в данном исследовании. 100
Субъект может участвовать в клинических испытаниях только при полном и сознательном добровольном согласии. Каждый участник исследования должен быть заранее информирован о целях, методах, ожидаемом риске и пользе, обеспечении его необходимой медицинской помощью в случае выявления нежелательных реакций в ходе испытания, страховании на случай причинения ущерба здоровью, связанного с участием в данном исследовании. 100
 Исследователь должен получить от субъекта подписанное и датированное информированное согласие на участие в исследовании. Каждый участник должен знать, что его участие в исследовании добровольное и что он может в любое время выйти из исследования. Принцип информированного согласия является краеугольным камнем этичности клинических исследований. Важная сторона защиты прав субъектов исследования соблюдение конфиденциальности. 101
Исследователь должен получить от субъекта подписанное и датированное информированное согласие на участие в исследовании. Каждый участник должен знать, что его участие в исследовании добровольное и что он может в любое время выйти из исследования. Принцип информированного согласия является краеугольным камнем этичности клинических исследований. Важная сторона защиты прав субъектов исследования соблюдение конфиденциальности. 101
 Рандомизация ( Randomization ) я Рандомизаци n) - Randomizatio ( процедура, йное ающая случа обеспечив ьных в деление бол распре ную и перименталь экс группы. контрольную м Случайны ем ределени ствие расп отсут стигается до вумя между д м различий м образо и таки группами сть вероятно ки в я снижаетс шиб ической о системат ких вие клиничес х вследст ания им исследов пп по как гру различий кам. зна либо при 102
Рандомизация ( Randomization ) я Рандомизаци n) - Randomizatio ( процедура, йное ающая случа обеспечив ьных в деление бол распре ную и перименталь экс группы. контрольную м Случайны ем ределени ствие расп отсут стигается до вумя между д м различий м образо и таки группами сть вероятно ки в я снижаетс шиб ической о системат ких вие клиничес х вследст ания им исследов пп по как гру различий кам. зна либо при 102
 Надежность данных РКИ прямо зависит от сопоставимости сравниваемых групп. Категорически нельзя сравнивать группы, в одну из которых были включены пациенты с анализируемым вмешательством а в другую отказавшиеся от участия в РКИ и получавшие «традиционную» терапию. 103
Надежность данных РКИ прямо зависит от сопоставимости сравниваемых групп. Категорически нельзя сравнивать группы, в одну из которых были включены пациенты с анализируемым вмешательством а в другую отказавшиеся от участия в РКИ и получавшие «традиционную» терапию. 103
 Также нельзя сопоставлять результаты нового метода лечения в разных клиниках, Аналогичные недостатки имеет и метод «исторического контроля» . если они не проводили его оценку по одному общему протоколу (различий в технической оснащенности, квалификации кадров и принятых стандартах лечения). 104
Также нельзя сопоставлять результаты нового метода лечения в разных клиниках, Аналогичные недостатки имеет и метод «исторического контроля» . если они не проводили его оценку по одному общему протоколу (различий в технической оснащенности, квалификации кадров и принятых стандартах лечения). 104
 Согласие больного подвергнуться лечению новым методом зависит от типа нервной деятельности, степени выраженности заболевания, общего состояния, возраста и прочих факторов, которые могут иметь прогностическое значение. 105
Согласие больного подвергнуться лечению новым методом зависит от типа нервной деятельности, степени выраженности заболевания, общего состояния, возраста и прочих факторов, которые могут иметь прогностическое значение. 105
 Иногда сопоставляются результаты нового метода лечения, проводимого в одной клинике, с эффективностью стандартного способа лечения, используемого в других лечебных учреждениях. В этом случае неоднородность групп еще больше увеличивается за счет различий в технической оснащенности и квалификации кадров, использования разных вспомогательных лечебных методов и прочего. 106
Иногда сопоставляются результаты нового метода лечения, проводимого в одной клинике, с эффективностью стандартного способа лечения, используемого в других лечебных учреждениях. В этом случае неоднородность групп еще больше увеличивается за счет различий в технической оснащенности и квалификации кадров, использования разных вспомогательных лечебных методов и прочего. 106
 Примерно такими же недостатками характеризуется метод так называемого «исторического контроля» , т. е. сравнивают специально подобранную для применения нового метода лечения группу больных с неподобранной группой «прошлого» . когда сопоставляются результаты лечения до внедрения нового метода с эффективностью современного лечения, 107
Примерно такими же недостатками характеризуется метод так называемого «исторического контроля» , т. е. сравнивают специально подобранную для применения нового метода лечения группу больных с неподобранной группой «прошлого» . когда сопоставляются результаты лечения до внедрения нового метода с эффективностью современного лечения, 107
 К рандомизации также не относятся методы, при которых больных распределяют в опытную и контрольную группы в порядке поступления по начальным буквам имен и фамили по нечетным и четным дням включения в исследование дате дня рождения 108
К рандомизации также не относятся методы, при которых больных распределяют в опытную и контрольную группы в порядке поступления по начальным буквам имен и фамили по нечетным и четным дням включения в исследование дате дня рождения 108
 эффектом от вмешательств а в «правильную » группу и наоборот. по его мнению, При таком отборе врач может предвзято включить пациента с хорошим, 109
эффектом от вмешательств а в «правильную » группу и наоборот. по его мнению, При таком отборе врач может предвзято включить пациента с хорошим, 109
 Рандомизация является ключевым моментом при проведении РКИ. Она должна обеспечить случайное распределение больных, не зависящее от желания врача или каких либо других факторов, и сопоставимость сравниваемых групп по клинико демографическим характеристикам пациентов, тяжести основного исследуемого заболевания, сопутствующей патологии и проводимой терапии. 110
Рандомизация является ключевым моментом при проведении РКИ. Она должна обеспечить случайное распределение больных, не зависящее от желания врача или каких либо других факторов, и сопоставимость сравниваемых групп по клинико демографическим характеристикам пациентов, тяжести основного исследуемого заболевания, сопутствующей патологии и проводимой терапии. 110
 При небольшом числе пациентов в группах даже правильно проведенная рандомизация не может обеспечить их однородность. при которой распределение вариантов вмешательства происходит в более однородных группах больных, В этом случае используется предварительная стратификация (stratum слой, пласт), изначально сформированных по одному или нескольким важным признакам. 111
При небольшом числе пациентов в группах даже правильно проведенная рандомизация не может обеспечить их однородность. при которой распределение вариантов вмешательства происходит в более однородных группах больных, В этом случае используется предварительная стратификация (stratum слой, пласт), изначально сформированных по одному или нескольким важным признакам. 111
 Различия пациентов по этим ключевым признакам должны быть минимальными. Такой подход практически гарантирует получение надежных результатов и отсутствие систематической ошибки. 112
Различия пациентов по этим ключевым признакам должны быть минимальными. Такой подход практически гарантирует получение надежных результатов и отсутствие систематической ошибки. 112
 Отсутствие систематической ошибки в РКИ называют обоснованностью (validity). Наиболее частой причиной несопоставимости сравниваемых групп после рандомизации может быть включение в анализ не всех участвовавших в исследовании пациентов. 113
Отсутствие систематической ошибки в РКИ называют обоснованностью (validity). Наиболее частой причиной несопоставимости сравниваемых групп после рандомизации может быть включение в анализ не всех участвовавших в исследовании пациентов. 113
 Существует большое количество методов рандомизации: метод непрозрачных запечатанных и последовательно пронумерованных конвертов, компьютерный метод (процедура рандомизации на основе метода генерации случайных чисел проводится специалистом, непосредственно не участвующим в лечении), метод пронумерованных идентичных контейнеров, подготовленных фармацевтической фирмой (код и истинное содержание контейнеров не известны ни пациентам, ни врачам, участвующим в исследовании), централизованная рандомизация по телефону (IVRS) специалистом фармацевтической фирмы. 114
Существует большое количество методов рандомизации: метод непрозрачных запечатанных и последовательно пронумерованных конвертов, компьютерный метод (процедура рандомизации на основе метода генерации случайных чисел проводится специалистом, непосредственно не участвующим в лечении), метод пронумерованных идентичных контейнеров, подготовленных фармацевтической фирмой (код и истинное содержание контейнеров не известны ни пациентам, ни врачам, участвующим в исследовании), централизованная рандомизация по телефону (IVRS) специалистом фармацевтической фирмы. 114
 Наиболее объективным считается последний из них, а наименее объективным метод конвертов. 115
Наиболее объективным считается последний из них, а наименее объективным метод конвертов. 115
 При рандомизации необходимо соблюсти одно важное условие (нельзя предугадать, в группу вмешательства или контроля попадет пациент). непредсказуемый характер распределения больных на группы 116
При рандомизации необходимо соблюсти одно важное условие (нельзя предугадать, в группу вмешательства или контроля попадет пациент). непредсказуемый характер распределения больных на группы 116
 Ни пациент ни исследователь не должны знать, в какие группы попадают пациенты. 117
Ни пациент ни исследователь не должны знать, в какие группы попадают пациенты. 117
 Это достигается при использовании «слепого» , «двойного слепого» и даже «тройного слепого» отбора. 118
Это достигается при использовании «слепого» , «двойного слепого» и даже «тройного слепого» отбора. 118
 Если о назначаемом вмешательстве известно только врачу, такая организация РКИ называется «простым слепым испытанием» (single blind trial). Если все лица исследовательского центра, общающиеся и работающие с пациентами, не знают, кто из них какое лечение получает, то это «двойное слепое испытание» (double blind trial). 119
Если о назначаемом вмешательстве известно только врачу, такая организация РКИ называется «простым слепым испытанием» (single blind trial). Если все лица исследовательского центра, общающиеся и работающие с пациентами, не знают, кто из них какое лечение получает, то это «двойное слепое испытание» (double blind trial). 119
 Подобная рганизация о И абсолютно РК еобходима в н тех случаях, огда велика к роль ствующего сопут лечения, ример при нап иотико и антиб иотерапии. хим 120
Подобная рганизация о И абсолютно РК еобходима в н тех случаях, огда велика к роль ствующего сопут лечения, ример при нап иотико и антиб иотерапии. хим 120
 Часто процесс «ослепления» достаточно сложен, например традиционная терапия предполагает применение таблетированных форм, а новое вмешательство использует инъекции. В этом случае в первой группе лечение придется дополнить введением физиологического раствора, а во втором приемом плацебо per os. Нелишне отметить, что вид, органолептические свойства и кратность назначения сравниваемых препаратов должны быть одинаковыми. 121
Часто процесс «ослепления» достаточно сложен, например традиционная терапия предполагает применение таблетированных форм, а новое вмешательство использует инъекции. В этом случае в первой группе лечение придется дополнить введением физиологического раствора, а во втором приемом плацебо per os. Нелишне отметить, что вид, органолептические свойства и кратность назначения сравниваемых препаратов должны быть одинаковыми. 121
 В настоящее время существует несколько причин, по которым в научных исследованиях рандомизация не используется: незнание врачами исследователями основ доказательной медицины; слепое следование традиционной практике и боязнь получить результаты, отличные от общепринятых и мнения авторитетов; боязнь применить у пациента менее эффективный метод вмешательства, но именно ради выявления его реальной эффективности проводится РКИ; существующее негативное общественное мнение, отождествляющее РКИ с испытаниями на людях 122
В настоящее время существует несколько причин, по которым в научных исследованиях рандомизация не используется: незнание врачами исследователями основ доказательной медицины; слепое следование традиционной практике и боязнь получить результаты, отличные от общепринятых и мнения авторитетов; боязнь применить у пациента менее эффективный метод вмешательства, но именно ради выявления его реальной эффективности проводится РКИ; существующее негативное общественное мнение, отождествляющее РКИ с испытаниями на людях 122
 В тоже время в последние годы термин «рандомизация» стал использоваться авторами публикаций как «магическое заклинание» , гарантирующее авторам отсутствие критики и повышающее их научный рейтинг самооценки. Истинная рандомизация подменяется ее декларированием, проявляется несопоставимостью сравниваемых групп и «информационным шумом» от выводов по некачественно сделанным исследованиям. Так, K. F. Schultz et al. считают, что только 9 15% статей в медицинских журналах имели истинную рандомизацию. 123
В тоже время в последние годы термин «рандомизация» стал использоваться авторами публикаций как «магическое заклинание» , гарантирующее авторам отсутствие критики и повышающее их научный рейтинг самооценки. Истинная рандомизация подменяется ее декларированием, проявляется несопоставимостью сравниваемых групп и «информационным шумом» от выводов по некачественно сделанным исследованиям. Так, K. F. Schultz et al. считают, что только 9 15% статей в медицинских журналах имели истинную рандомизацию. 123
 ИЯ НТЕРПРЕТАЦ АНАЛИЗ И И В РЕЗУЛЬТАТО Главной задачей статистического ется нализа РКИ явля а установление е ницы и степени е раз о достоверности п ым исходам (конечн точкам) между группой с анализируемым и вмешательством. рольной группой конт 124
ИЯ НТЕРПРЕТАЦ АНАЛИЗ И И В РЕЗУЛЬТАТО Главной задачей статистического ется нализа РКИ явля а установление е ницы и степени е раз о достоверности п ым исходам (конечн точкам) между группой с анализируемым и вмешательством. рольной группой конт 124
 В настоящее время существует много пакетов статических программ для анализа полученных результатов BMDP, Statistica SOLO, и другие 125
В настоящее время существует много пакетов статических программ для анализа полученных результатов BMDP, Statistica SOLO, и другие 125
 Для получения объективной информации об эффективности вмешательства в анализ необходимо включать всех первоначально рандомизированных больных (intention to treat analysis), а не только тех, которым лечение проведено в строгом соответствии с протоколом исследования (on protocol analysis). Это один из основных способов минимизировать возможные ошибки, когда при intention to treat analysis исходят из допущения, что все пациенты получили лечение, предписанное при рандомизации. 126
Для получения объективной информации об эффективности вмешательства в анализ необходимо включать всех первоначально рандомизированных больных (intention to treat analysis), а не только тех, которым лечение проведено в строгом соответствии с протоколом исследования (on protocol analysis). Это один из основных способов минимизировать возможные ошибки, когда при intention to treat analysis исходят из допущения, что все пациенты получили лечение, предписанное при рандомизации. 126
 Если процент выше, результаты исследования некорректны. не должно превышать 15% от исходного числа рандомизиров анных больных. Выбывание пациентов из исследования по разным причинам (отказ от дальнейшего участия, побочные эффекты и плохая переносимость лечения, нарушения протокола пациентами или исследователями) 127
Если процент выше, результаты исследования некорректны. не должно превышать 15% от исходного числа рандомизиров анных больных. Выбывание пациентов из исследования по разным причинам (отказ от дальнейшего участия, побочные эффекты и плохая переносимость лечения, нарушения протокола пациентами или исследователями) 127
 Такой подход существенно снижает вероятность получения ложноположительного результата, когда на самом деле он отсутствует. Считается: если более 80% из включенных больных наблюдались до конца исследования, его результаты могут быть достаточно надежными. Для статистического анализа большого массива дискретных конечных точек вычисляют c квадрат. При малой выборке (число пациентов менее 30 в каждой из групп вмешательства) используют методы непараметрической статистики (тесты Фишера или Йетса). 128
Такой подход существенно снижает вероятность получения ложноположительного результата, когда на самом деле он отсутствует. Считается: если более 80% из включенных больных наблюдались до конца исследования, его результаты могут быть достаточно надежными. Для статистического анализа большого массива дискретных конечных точек вычисляют c квадрат. При малой выборке (число пациентов менее 30 в каждой из групп вмешательства) используют методы непараметрической статистики (тесты Фишера или Йетса). 128
 Результаты исследования представляются с использованием следующих показателей: 129
Результаты исследования представляются с использованием следующих показателей: 129
 Публикация результатов Часто статью с итогами РКИ предваряет опубликование его наиболее значимых результатов и выводов в материалах крупных международных конференций и съездов. Структура статьи имеет обычный характер. Обязательным требованием является максимально широкое представление дизайна и статистических аспектов РКИ. Особый интерес может представлять обсуждение результатов, так как они могут дать дополнительную информацию о спорных моментах при его проведении. 130
Публикация результатов Часто статью с итогами РКИ предваряет опубликование его наиболее значимых результатов и выводов в материалах крупных международных конференций и съездов. Структура статьи имеет обычный характер. Обязательным требованием является максимально широкое представление дизайна и статистических аспектов РКИ. Особый интерес может представлять обсуждение результатов, так как они могут дать дополнительную информацию о спорных моментах при его проведении. 130
 В настоящее время для проведения РКИ разработаны этические и методологическ ие стандарты. Необходимо помнить о том, что плацебо контролируемы е исследования оправданы, эффективность которого не вызывает сомнений. когда не существует альтернативного способа лечения, 131
В настоящее время для проведения РКИ разработаны этические и методологическ ие стандарты. Необходимо помнить о том, что плацебо контролируемы е исследования оправданы, эффективность которого не вызывает сомнений. когда не существует альтернативного способа лечения, 131
 Сегодня врачам, исследователям и организаторам исследований необходимо непрерывно повышать не только профессионализм, но и уровень знаний в области доказательной медицины, правоведения и GCP. 132
Сегодня врачам, исследователям и организаторам исследований необходимо непрерывно повышать не только профессионализм, но и уровень знаний в области доказательной медицины, правоведения и GCP. 132
 что предъявляет еще более высокие этические требования ко всем его участникам. но и особый (и достаточно прибыльный) медицинский бизнес, При этом само проведение РКИ не только наука, 133
что предъявляет еще более высокие этические требования ко всем его участникам. но и особый (и достаточно прибыльный) медицинский бизнес, При этом само проведение РКИ не только наука, 133
 Рандомизированные контролируемые клинические исследования (РКИ) проводятся с середины прошлого века. Их гуманистическая направленность стала ответом научного сообщества на проведение экспериментов на людях во время Второй мировой войны в фашистских концлагерях. 134
Рандомизированные контролируемые клинические исследования (РКИ) проводятся с середины прошлого века. Их гуманистическая направленность стала ответом научного сообщества на проведение экспериментов на людях во время Второй мировой войны в фашистских концлагерях. 134
 Поэтому целесообразно более подробно остановиться на особенностях их планирования и проведения. РКИ предполагают использование тонких и чувствительных операционных и статистических методов во время проспективного исследования, в котором сопоставляемые группы получают различные виды анализируемых вмешательств, лица контрольной группы — стандартное по современным представлениям лечение. 135
Поэтому целесообразно более подробно остановиться на особенностях их планирования и проведения. РКИ предполагают использование тонких и чувствительных операционных и статистических методов во время проспективного исследования, в котором сопоставляемые группы получают различные виды анализируемых вмешательств, лица контрольной группы — стандартное по современным представлениям лечение. 135
 Отличительной особенностью современных РКИ является неукоснительное следование этическим нормам. Перед началом любого РКИ его протокол должен быть одобрен национальным или региональным этическим комитетом {часто и тем, и другим). В дальнейшем этический комитет в обязательном порядке информируется о серьезных побочных эффектах, возникших в ходе РКИ и всех изменениях в протоколе. 136
Отличительной особенностью современных РКИ является неукоснительное следование этическим нормам. Перед началом любого РКИ его протокол должен быть одобрен национальным или региональным этическим комитетом {часто и тем, и другим). В дальнейшем этический комитет в обязательном порядке информируется о серьезных побочных эффектах, возникших в ходе РКИ и всех изменениях в протоколе. 136
 До включения в исследование его потенциальный участник должен на добровольной основе подписать информированное согласие, где в доступной форме должна быть изложена цель исследования, возможные осложнения или неудобства, преимущества, связанные с участием больного в исследовании, и альтернативные методы лечения. 137
До включения в исследование его потенциальный участник должен на добровольной основе подписать информированное согласие, где в доступной форме должна быть изложена цель исследования, возможные осложнения или неудобства, преимущества, связанные с участием больного в исследовании, и альтернативные методы лечения. 137
 Пациент должен быть проинформирован о том, что решение о его участии или неучастии в данном клиническом исследовании на любом этапе выполнения никак не отразится на дальнейшей тактике его ведения, и он в любой момент может прекратить свое участие в РКИ. 138
Пациент должен быть проинформирован о том, что решение о его участии или неучастии в данном клиническом исследовании на любом этапе выполнения никак не отразится на дальнейшей тактике его ведения, и он в любой момент может прекратить свое участие в РКИ. 138
 Только после получения информированного согласия пациент может принимать участие в исследовании. Если РКИ предполагает проведение субисследований, требующих дополнительного обследования, то на них тоже необходимо получить информированное согласие пациента. В ряде случаев, например при проведении РКИ у детей, информированное согласие подписывают родители или опекуны. Для оценки новых методов лечения и диагностики могут применяться два основных вида исследования — контролируемые и неконтролируемые. 139
Только после получения информированного согласия пациент может принимать участие в исследовании. Если РКИ предполагает проведение субисследований, требующих дополнительного обследования, то на них тоже необходимо получить информированное согласие пациента. В ряде случаев, например при проведении РКИ у детей, информированное согласие подписывают родители или опекуны. Для оценки новых методов лечения и диагностики могут применяться два основных вида исследования — контролируемые и неконтролируемые. 139
 Неконтролируемое клиническое испытание (без сравнения с уже применяющимся способом терапии или плацебо) новых методов лечения допустимо только в исключительных случаях, когда новый метод позволяет спасти жизнь или радикально улучшить прогноз у пациентов, страдающих неизлечимым заболеванием (в настоящее время большинство таких исследований связано с ВИЧ инфекцией). Необходимо подчеркнуть, что даже в этом случае предполагаемая польза нового метода должна быть убедительной и сопоставимой, например, с эффектом инсулина при сахарном диабете I типа. Особняком стоят неконтролируемые клинические испытания при изучении новых лекарственных препаратов на этапе фазы I и II их клинического исследования, когда на здоровых добровольцах и ограниченном числе пациентов определяются фармакокинетические и фармакодинамические характеристики нового метода лечения. 140
Неконтролируемое клиническое испытание (без сравнения с уже применяющимся способом терапии или плацебо) новых методов лечения допустимо только в исключительных случаях, когда новый метод позволяет спасти жизнь или радикально улучшить прогноз у пациентов, страдающих неизлечимым заболеванием (в настоящее время большинство таких исследований связано с ВИЧ инфекцией). Необходимо подчеркнуть, что даже в этом случае предполагаемая польза нового метода должна быть убедительной и сопоставимой, например, с эффектом инсулина при сахарном диабете I типа. Особняком стоят неконтролируемые клинические испытания при изучении новых лекарственных препаратов на этапе фазы I и II их клинического исследования, когда на здоровых добровольцах и ограниченном числе пациентов определяются фармакокинетические и фармакодинамические характеристики нового метода лечения. 140
 141
141
 Например, именно "таким исследованием было SYST EUR, результаты которого в значительной степени реабилитировали антагонисты кальция в лечении артериальной гипертензии, когда на них обрушилась волна критики по результатам не совсем корректного мета анализа. Планирование РКИ начинается с формулирования цели и задач исследования, которые отличаются новизной и практической значимостью. Цель исследования должна отличаться как научной новизной, так и практической значимостью. 142
Например, именно "таким исследованием было SYST EUR, результаты которого в значительной степени реабилитировали антагонисты кальция в лечении артериальной гипертензии, когда на них обрушилась волна критики по результатам не совсем корректного мета анализа. Планирование РКИ начинается с формулирования цели и задач исследования, которые отличаются новизной и практической значимостью. Цель исследования должна отличаться как научной новизной, так и практической значимостью. 142
 Поэтому, как правило, крупные многоцентровые РКИ планируют известные в своей области специалисты. Каждое новое РКИ оригинально по дизайну и популяции пациентов, участвующих в нем (определяется критериями включения и исключения), поэтому уже существующие протоколы не могут быть полностью воспроизведены вновь, хотя и могут служить некой базой для адаптации B качестве примера решения сходной задачи можно привести два сильно различающихся как по дизайну, так но итоговым результатам протокола исследований ALLHAT и ASCOT. 143
Поэтому, как правило, крупные многоцентровые РКИ планируют известные в своей области специалисты. Каждое новое РКИ оригинально по дизайну и популяции пациентов, участвующих в нем (определяется критериями включения и исключения), поэтому уже существующие протоколы не могут быть полностью воспроизведены вновь, хотя и могут служить некой базой для адаптации B качестве примера решения сходной задачи можно привести два сильно различающихся как по дизайну, так но итоговым результатам протокола исследований ALLHAT и ASCOT. 143
 Достоверных различий между этими двумя режимами терапии не выявлено, но цель исследования была «доказать преимущества лозартана» , и она не была достигнута. 144
Достоверных различий между этими двумя режимами терапии не выявлено, но цель исследования была «доказать преимущества лозартана» , и она не была достигнута. 144
 Однако новый класс препаратов, оказавшийся не хуже эталонных ингибиторов АПФ, стал важным событием для кардиологов. Если бы целью исследования было доказательство равнозначной эффективности лозартана и каптоприла при хронической сердечной недостаточности, никакой последующей полемики попросту не возникло. Задачи, решаемые в РКИ, не должны быть многочисленными, поскольку это может привести к ложноположительным результатам и затруднить интерпретацию полученных данных для практики. 145
Однако новый класс препаратов, оказавшийся не хуже эталонных ингибиторов АПФ, стал важным событием для кардиологов. Если бы целью исследования было доказательство равнозначной эффективности лозартана и каптоприла при хронической сердечной недостаточности, никакой последующей полемики попросту не возникло. Задачи, решаемые в РКИ, не должны быть многочисленными, поскольку это может привести к ложноположительным результатам и затруднить интерпретацию полученных данных для практики. 145
 Существуют «жесткие» и «мягкие» (суррогатные) конечные точки, оцениваемые в РКИ. К жестким конечным точкам относят, например, общую и сердечно сосудистую смертность, инсульт, инфаркт миокарда. Примерами суррогатных конечных точек являются гипертрофия левого желудочка, фракция выброса, уровень липидов, глюкозы крови тд. R. J. Temple определяет суррогатные конечные точки как «. . . косвенный критерий оценки в клиническом испытании — лабораторный показатель или симптом, который заменяет клинически значимый исход, прямо характеризующий самочувствие больного, его функциональное состояние и выживание. 146
Существуют «жесткие» и «мягкие» (суррогатные) конечные точки, оцениваемые в РКИ. К жестким конечным точкам относят, например, общую и сердечно сосудистую смертность, инсульт, инфаркт миокарда. Примерами суррогатных конечных точек являются гипертрофия левого желудочка, фракция выброса, уровень липидов, глюкозы крови тд. R. J. Temple определяет суррогатные конечные точки как «. . . косвенный критерий оценки в клиническом испытании — лабораторный показатель или симптом, который заменяет клинически значимый исход, прямо характеризующий самочувствие больного, его функциональное состояние и выживание. 146
 Изменения косвенного критерия оценки, вызываемые лечением, должны отражать изменения клинически значимого критерия (исхода)» . Необходимость использования суррогатных конечных точек обусловлена тем, что для получения статистически достоверного влияния вмешательства на жесткие точки необходимо обследовать большое число пациентов и наблюдать их на протяжении длительного времени. Суррогатные конечные точки (типичные для каждой нозологии) позволяют существенно уменьшить длительность исследования и количество больных, участвующих в нем. Однако обязательно нужно помнить: выбранные суррогатные точки должны иметь доказанное влияние на прогноз исследуемого заболевания. Безусловно, выбранным конечным точкам необходимо иметь не только научное, но и клиническое значение. 147
Изменения косвенного критерия оценки, вызываемые лечением, должны отражать изменения клинически значимого критерия (исхода)» . Необходимость использования суррогатных конечных точек обусловлена тем, что для получения статистически достоверного влияния вмешательства на жесткие точки необходимо обследовать большое число пациентов и наблюдать их на протяжении длительного времени. Суррогатные конечные точки (типичные для каждой нозологии) позволяют существенно уменьшить длительность исследования и количество больных, участвующих в нем. Однако обязательно нужно помнить: выбранные суррогатные точки должны иметь доказанное влияние на прогноз исследуемого заболевания. Безусловно, выбранным конечным точкам необходимо иметь не только научное, но и клиническое значение. 147
 Предпочтение отдается объективным (например, развитие инсульта, подтвержденное компьютерной томографией), по которым рассчитывается абсолютный и относительный эффект вмешательства и их легко интерпретировать практическому врачу. стандартизованным критериям (индекс массы миокарда левого желудочка поданным эхо кардиографии) и дискретным показателям эффективности (показатели типа да/нет, жив/умер, госпитализация/отсутств ие госпитализации, улучшение/ухудушение), 148
Предпочтение отдается объективным (например, развитие инсульта, подтвержденное компьютерной томографией), по которым рассчитывается абсолютный и относительный эффект вмешательства и их легко интерпретировать практическому врачу. стандартизованным критериям (индекс массы миокарда левого желудочка поданным эхо кардиографии) и дискретным показателям эффективности (показатели типа да/нет, жив/умер, госпитализация/отсутств ие госпитализации, улучшение/ухудушение), 148
 по которым оценивается эффективность вмешательства, В многих РКИ выделяют основные конечные точки, и второстепенные конечные точки, учитывающие другие аспекты этого вмешательства (например, побочные эффекты, качество жизни, когнитивные нарушения, лабораторные показатели и т. д. ). 149
по которым оценивается эффективность вмешательства, В многих РКИ выделяют основные конечные точки, и второстепенные конечные точки, учитывающие другие аспекты этого вмешательства (например, побочные эффекты, качество жизни, когнитивные нарушения, лабораторные показатели и т. д. ). 149
 Хотя в ряде случаев последние сами могут становиться основной конечной точкой (например, когнитивные изменения в исследовании SCOPE, холестерин — в исследованиях по атеросклерозу, уровень креатинина— в исследованиях по почечной недостаточности, артериальной гипертензин и сахарному диабету). В последнее время в РКИ стали широко использоваться так называемые комбинированные конечные точки, объединяющие сразу несколько показателей. 150
Хотя в ряде случаев последние сами могут становиться основной конечной точкой (например, когнитивные изменения в исследовании SCOPE, холестерин — в исследованиях по атеросклерозу, уровень креатинина— в исследованиях по почечной недостаточности, артериальной гипертензин и сахарному диабету). В последнее время в РКИ стали широко использоваться так называемые комбинированные конечные точки, объединяющие сразу несколько показателей. 150
 Например, в исследовании PREAMI конечной точкой являлся показатель смерть + госпитализация с сердечной недостаточностью + сердечное ремоделирование. Как видно, здесь использованы как жесткие, так и суррогатные конечные точки. Существенно облегчить задачу по выбору оптимальных конечных точек при планировании исследований может использование существующих баз данных о клинических исходах 151
Например, в исследовании PREAMI конечной точкой являлся показатель смерть + госпитализация с сердечной недостаточностью + сердечное ремоделирование. Как видно, здесь использованы как жесткие, так и суррогатные конечные точки. Существенно облегчить задачу по выбору оптимальных конечных точек при планировании исследований может использование существующих баз данных о клинических исходах 151
 Источники информации рекомендуемых для оценки клинических показателей при проведении исследований Название Computerized Needs Oriented Quality Measurement Evaluation System (CONQUEST) National Library of Quality Indicators and ORYX Programme Адрес в Интернете Agency for Healthcare Research and Quality (www. ahcpr. gov) Joint Commission on Accreditation of Healthcare Organization (www. jcaho. Health Plan Employer Data and Information Set (HEDIS) National Commission of Quality Assurance (www. ncqa. org) FACCT Quality Measures Foundation for Accountability (www. facct. org) Quality Indicator Project Acute Health Clinical Indicator Project NHS Performance Indicators Clearing House Databases Zuericher Indicatoren-Set National Quality Measures Clearinghouse , Association of Maryland Hospital & Health Systems (www. qi_project. org) Department of Human Service Victoria, Australia (www. dhs. vic. gov. au/ahs/quality/clinical. htm) National Health Service Executive (www. doh. gov. uk) UK Clearinghouse on Health Outcomes (www. leeds. ac. uk/nuffield/ infoservices/UKCH/home. html) Verein Outcome Zuerich (www. vereinoutcomc. ch) Agency for Healthcare Research and Quality (http: //www. qualitymeasures. ahrq. gov) 152
Источники информации рекомендуемых для оценки клинических показателей при проведении исследований Название Computerized Needs Oriented Quality Measurement Evaluation System (CONQUEST) National Library of Quality Indicators and ORYX Programme Адрес в Интернете Agency for Healthcare Research and Quality (www. ahcpr. gov) Joint Commission on Accreditation of Healthcare Organization (www. jcaho. Health Plan Employer Data and Information Set (HEDIS) National Commission of Quality Assurance (www. ncqa. org) FACCT Quality Measures Foundation for Accountability (www. facct. org) Quality Indicator Project Acute Health Clinical Indicator Project NHS Performance Indicators Clearing House Databases Zuericher Indicatoren-Set National Quality Measures Clearinghouse , Association of Maryland Hospital & Health Systems (www. qi_project. org) Department of Human Service Victoria, Australia (www. dhs. vic. gov. au/ahs/quality/clinical. htm) National Health Service Executive (www. doh. gov. uk) UK Clearinghouse on Health Outcomes (www. leeds. ac. uk/nuffield/ infoservices/UKCH/home. html) Verein Outcome Zuerich (www. vereinoutcomc. ch) Agency for Healthcare Research and Quality (http: //www. qualitymeasures. ahrq. gov) 152
 остававшиеся за рамками основного РКИ. которые используют дополнительные методы обследования и позволяют ответить на дополнительные вопросы, Еще одной особенностью современных РКИ является проведение суб исследований (суб протоколов) в рамках основного РКИ, 153
остававшиеся за рамками основного РКИ. которые используют дополнительные методы обследования и позволяют ответить на дополнительные вопросы, Еще одной особенностью современных РКИ является проведение суб исследований (суб протоколов) в рамках основного РКИ, 153
 Длительность исследования (интервал времени от момента рандомизации больного и осуществления вмешательства до момента оценки конечного исхода заболевания) определяется целью и задачами исследования, зависит от характера патологии, особенностей естественного течения заболевания, риска развития исследуемых осложнений и времени, необходимого вмешательству для оказания потенциального влияния на выбранные конечные точки. 154
Длительность исследования (интервал времени от момента рандомизации больного и осуществления вмешательства до момента оценки конечного исхода заболевания) определяется целью и задачами исследования, зависит от характера патологии, особенностей естественного течения заболевания, риска развития исследуемых осложнений и времени, необходимого вмешательству для оказания потенциального влияния на выбранные конечные точки. 154
 Критерии включения предопределяются целью исследования, более широкие из них облегчают набор пациентов и позволяют экстраполировать полученные результаты на большую популяцию больных. Вторым по значимости разделом РКИ (после формулирования цели и задач исследования) является определение критериев включения и исключения из исследования. 155
Критерии включения предопределяются целью исследования, более широкие из них облегчают набор пациентов и позволяют экстраполировать полученные результаты на большую популяцию больных. Вторым по значимости разделом РКИ (после формулирования цели и задач исследования) является определение критериев включения и исключения из исследования. 155
 Однако в этом случае существует опасность формирования разнородных исследуемых групп больных как по исходным клинико демографическим показателям, хотя у пациентов с исходно более высоким риском осложнений можно в более короткие сроки оценить эффект вмешательства на жесткие конечные точки. так и по эффективности тестируемого вмешательства. Обычно в РКИ вклю¬чают пациентов со средней тяжестью заболевания, 156
Однако в этом случае существует опасность формирования разнородных исследуемых групп больных как по исходным клинико демографическим показателям, хотя у пациентов с исходно более высоким риском осложнений можно в более короткие сроки оценить эффект вмешательства на жесткие конечные точки. так и по эффективности тестируемого вмешательства. Обычно в РКИ вклю¬чают пациентов со средней тяжестью заболевания, 156
 Группа пациентов с низким риском и легким течением заболевания требует длительного наблюдения и потенциально опасна в получении статистически достоверного эффекта вмешательства, тогда как на самом деле оно может оказаться эффективным. 157
Группа пациентов с низким риском и легким течением заболевания требует длительного наблюдения и потенциально опасна в получении статистически достоверного эффекта вмешательства, тогда как на самом деле оно может оказаться эффективным. 157
 Критерии исключения должны минимизировать возможность ошибок при проведении исследования (например, исключение из исследования больных с терминальной стадией заболевания, сниженной функцией печени и почек). Если данный контингент пациентов не является предметом РКИ, в него обычно не включают несовершеннолетних, женщин в период беременности и лактации или не использующих контрацепцию, онкологических и психических больных. Важной задачей критериев исключения является обеспечение одинакового лечения и ведение пациентов в исследуемой и контрольной группах, а также исключение применения в них во время исследования препаратов, сходных с испытуемым. В целом чем крупнее РКИ и чем быстрее его планируют закончить, шире должны быть критерии включения и тем меньше критериев исключения. 158
Критерии исключения должны минимизировать возможность ошибок при проведении исследования (например, исключение из исследования больных с терминальной стадией заболевания, сниженной функцией печени и почек). Если данный контингент пациентов не является предметом РКИ, в него обычно не включают несовершеннолетних, женщин в период беременности и лактации или не использующих контрацепцию, онкологических и психических больных. Важной задачей критериев исключения является обеспечение одинакового лечения и ведение пациентов в исследуемой и контрольной группах, а также исключение применения в них во время исследования препаратов, сходных с испытуемым. В целом чем крупнее РКИ и чем быстрее его планируют закончить, шире должны быть критерии включения и тем меньше критериев исключения. 158
 Никаких нормативов, кроме получения необходимой статистической достоверности при определении числа пациентов, участвующих в исследовании, не сушествует. Небольшое количество пациентов не позволяет добиться однородности сравниваемых групп и статистически достоверного эффекта вмешательства. Размер РКИ зависит от ожидаемого клинически значимого эффекта вмешательства. Кроме этого, весьма полезными оказываются данные закончившихся РКИ по аналогичной тематике. Принято считать, что снижение относительного риска исхода заболевания на 20% является клинически значимым. 159
Никаких нормативов, кроме получения необходимой статистической достоверности при определении числа пациентов, участвующих в исследовании, не сушествует. Небольшое количество пациентов не позволяет добиться однородности сравниваемых групп и статистически достоверного эффекта вмешательства. Размер РКИ зависит от ожидаемого клинически значимого эффекта вмешательства. Кроме этого, весьма полезными оказываются данные закончившихся РКИ по аналогичной тематике. Принято считать, что снижение относительного риска исхода заболевания на 20% является клинически значимым. 159
 При этом степень достоверности получения ложноположительного результата обычно устанавливается на уровне 0, 05 ( «а» ил и «I тип ошибки» ). В свою очередь степень достоверности ложнотрицательного результата обычно устанавливается на уровне 0, 1 ( «Ь» или «II тип ошибки» ). 160
При этом степень достоверности получения ложноположительного результата обычно устанавливается на уровне 0, 05 ( «а» ил и «I тип ошибки» ). В свою очередь степень достоверности ложнотрицательного результата обычно устанавливается на уровне 0, 1 ( «Ь» или «II тип ошибки» ). 160
 Размер РКИ, в котором в качестве критериев эффективности вмешательства используются дискретные показатели исхода заболевания, всегда больше, чем размер такого же РКИ, но в котором критерием эффективности вмешательства являются продолженные показатели исхода заболевания (средние величины показателя или функционального исхода). 161
Размер РКИ, в котором в качестве критериев эффективности вмешательства используются дискретные показатели исхода заболевания, всегда больше, чем размер такого же РКИ, но в котором критерием эффективности вмешательства являются продолженные показатели исхода заболевания (средние величины показателя или функционального исхода). 161
 Естественно, чем больше ожидаемое различие в эффекте между ними, тем меньше окажется необходимое число наблюдений. видом статистического показателя эффекта вмешательства (частоты, средние величины). Достаточность групп наблюдения зависит от степени предполагаемых различий в эффекте вмешательства в опытной и контрольной группах, 162
Естественно, чем больше ожидаемое различие в эффекте между ними, тем меньше окажется необходимое число наблюдений. видом статистического показателя эффекта вмешательства (частоты, средние величины). Достаточность групп наблюдения зависит от степени предполагаемых различий в эффекте вмешательства в опытной и контрольной группах, 162
 При одинаковой степени точности необходимое число наблюдений будет значительно меньше, когда для оценки эффекта вмешательства используются средние величины, а не частотные показатели. При проведении исследования очень важно получить достоверную информацию об эффективности вмешательства в возможно более сжатые сроки. Для этого используют многоцентровые РКИ. В них происходит кооперирование (часто международное) и стандартизация исследовательских центров по единой программе и методам наблюдения, что позволяет получить сопоставимые данные разных учреждений. Надежность данных РКИ прямо зависит от сопоставимости сравниваемых групп. 163
При одинаковой степени точности необходимое число наблюдений будет значительно меньше, когда для оценки эффекта вмешательства используются средние величины, а не частотные показатели. При проведении исследования очень важно получить достоверную информацию об эффективности вмешательства в возможно более сжатые сроки. Для этого используют многоцентровые РКИ. В них происходит кооперирование (часто международное) и стандартизация исследовательских центров по единой программе и методам наблюдения, что позволяет получить сопоставимые данные разных учреждений. Надежность данных РКИ прямо зависит от сопоставимости сравниваемых групп. 163
 Категорически нельзя сравнивать группы, в одну из которых были включены пациенты с анализируемым вмешательством, а в другую — отказавшиеся от участия в РКИ и получавшие «традиционную» терапию. Также нельзя сопоставлять результаты нового метода лечения в разных клиниках, если они не проводили его оценку по одному общему протоколу (различий в технической оснащенности, квалификации кадров и принятых стандартах лечения) Аналогичные недостатки имеет и метод «исторического контроля» 164
Категорически нельзя сравнивать группы, в одну из которых были включены пациенты с анализируемым вмешательством, а в другую — отказавшиеся от участия в РКИ и получавшие «традиционную» терапию. Также нельзя сопоставлять результаты нового метода лечения в разных клиниках, если они не проводили его оценку по одному общему протоколу (различий в технической оснащенности, квалификации кадров и принятых стандартах лечения) Аналогичные недостатки имеет и метод «исторического контроля» 164
 Одно из обязательных условий надежности исследования — сопоставимость сравниваемых групп. Очень часто в публикуемых исследованиях нарушается этот важнейший принцип. Например, группы несопоставимы, если в одну из них включаются больные, лечен¬ные новым методом, а в другую — отказавшиеся от него. Согласие больного подвергнуться лечению новым методом зависит от типа нервной деятельности, степени выраженности заболевания, общего состояния, возраста и прочих факторов, которые могут иметь прогностическое значение. 165
Одно из обязательных условий надежности исследования — сопоставимость сравниваемых групп. Очень часто в публикуемых исследованиях нарушается этот важнейший принцип. Например, группы несопоставимы, если в одну из них включаются больные, лечен¬ные новым методом, а в другую — отказавшиеся от него. Согласие больного подвергнуться лечению новым методом зависит от типа нервной деятельности, степени выраженности заболевания, общего состояния, возраста и прочих факторов, которые могут иметь прогностическое значение. 165
 Иногда сопоставляются результаты нового метода лечения, проводимого в одной клинике, с эффективностью стандартного способа лечения, используемого в других лечебных учреждениях. В этом случае неоднородность групп еще больше увеличивается за счет различий в технической оснащенности и квалификации кадров, использования разных вспомогательных лечебных методов и прочего. 166
Иногда сопоставляются результаты нового метода лечения, проводимого в одной клинике, с эффективностью стандартного способа лечения, используемого в других лечебных учреждениях. В этом случае неоднородность групп еще больше увеличивается за счет различий в технической оснащенности и квалификации кадров, использования разных вспомогательных лечебных методов и прочего. 166
 Примерно такими же недостатками характеризуется метод так называемого «исторического контроля» , когда сопоставляются результаты лечения до внедрения нового метода с эффективностью современного лечения, т. е. сравнивают специально подобранную для применения нового метода лечения группу больных с неподобранной группой «прошлого» . 167
Примерно такими же недостатками характеризуется метод так называемого «исторического контроля» , когда сопоставляются результаты лечения до внедрения нового метода с эффективностью современного лечения, т. е. сравнивают специально подобранную для применения нового метода лечения группу больных с неподобранной группой «прошлого» . 167
 К рандомизации также не относятся методы, при которых больных распределяют в опытную и контрольную группы в порядке поступления, по начальным буквам имен и фамилий, дате дня рождения. по нечетным и четным дням включения в исследовани е, При таком отборе врач может ? ? включить пациента с 168
К рандомизации также не относятся методы, при которых больных распределяют в опытную и контрольную группы в порядке поступления, по начальным буквам имен и фамилий, дате дня рождения. по нечетным и четным дням включения в исследовани е, При таком отборе врач может ? ? включить пациента с 168
 Она должна Рандомизация обеспечить является ключевым случайное моментом при распределение проведении 1 РКИ. больных, не зависящее от желания врача или каких либо других факторов, и сопоставимость сравниваемых групп по клинико демографическим характеристикам пациентов, тяжести основного исследуемого заболевания, сопутствующей патологии и проводимой терапии. 169
Она должна Рандомизация обеспечить является ключевым случайное моментом при распределение проведении 1 РКИ. больных, не зависящее от желания врача или каких либо других факторов, и сопоставимость сравниваемых групп по клинико демографическим характеристикам пациентов, тяжести основного исследуемого заболевания, сопутствующей патологии и проводимой терапии. 169
 При небольшом числе пациентов в группах даже правильно проведенная рандомизаци я не может обеспечить их однородност ь. В этом случае используется предварительная стратификация (stratum — слой, пласт), изначально сформированных по одному или нескольким важным признакам. при которой распределен ие вариантов вмешательс¬ тва происходит в более однородных группах больных, 170
При небольшом числе пациентов в группах даже правильно проведенная рандомизаци я не может обеспечить их однородност ь. В этом случае используется предварительная стратификация (stratum — слой, пласт), изначально сформированных по одному или нескольким важным признакам. при которой распределен ие вариантов вмешательс¬ тва происходит в более однородных группах больных, 170
 Различия пациентов по этим ключевым признакам должны быть минимальными. Такой подход практически гарантирует получение надежных результатов и отсутствие систематической ошибки. Отсутствие систематической ошибки в РКИ называют обоснованностью (validity). Наиболее частой причиной несопоставимости сравниваемых групп после рандомизации может быть включение в анализ не всех участвовавших в исследовании пациентов. 171
Различия пациентов по этим ключевым признакам должны быть минимальными. Такой подход практически гарантирует получение надежных результатов и отсутствие систематической ошибки. Отсутствие систематической ошибки в РКИ называют обоснованностью (validity). Наиболее частой причиной несопоставимости сравниваемых групп после рандомизации может быть включение в анализ не всех участвовавших в исследовании пациентов. 171
 Существует большое количество методов рандомизации: метод непрозрачных запечатанных и последовательно пронумерованных конвертов, компьютерный метод (процедура рандомизации на основе метода генерации случайных чисел проводится специалистом, непосредственно не участвующим в лечении), метод пронумерованных идентичных контейнеров, подготовленных фармацевтической фирмой (код и истинное содержание контейнеров не известны ни пациентам, ни врачам, участвующим в исследовании), централизованная рандомизация по телефону (IVRS) специалистом фармацевтической фирмы. 172
Существует большое количество методов рандомизации: метод непрозрачных запечатанных и последовательно пронумерованных конвертов, компьютерный метод (процедура рандомизации на основе метода генерации случайных чисел проводится специалистом, непосредственно не участвующим в лечении), метод пронумерованных идентичных контейнеров, подготовленных фармацевтической фирмой (код и истинное содержание контейнеров не известны ни пациентам, ни врачам, участвующим в исследовании), централизованная рандомизация по телефону (IVRS) специалистом фармацевтической фирмы. 172
 Наиболее объективным считается последний из них, а наименее объективным — метод конвертов. При рандомизации необходимо соблюсти одно важное условие — непредсказуемый характер распределения больных на группы (нельзя предугадать, в группу вмешательства или контроля попадет пациент). Ни пациент, ни исследователь не должны знать, в какие группы попадают пациенты. Это достигается при использовании «слепого» , «двойного слепого» и даже «тройного слепого» отбора. 173
Наиболее объективным считается последний из них, а наименее объективным — метод конвертов. При рандомизации необходимо соблюсти одно важное условие — непредсказуемый характер распределения больных на группы (нельзя предугадать, в группу вмешательства или контроля попадет пациент). Ни пациент, ни исследователь не должны знать, в какие группы попадают пациенты. Это достигается при использовании «слепого» , «двойного слепого» и даже «тройного слепого» отбора. 173
 Если о назначаемом вмешательстве известно только врачу, такая организация РКИ называется «простым слепым испытанием» (single blind trial). Если все лица исследовательского центра, общаюшиеся и работающие с пациентами, не знают, кто из них какое лечение получает, то это «двойное слепое испытание» (double blind trial). 174
Если о назначаемом вмешательстве известно только врачу, такая организация РКИ называется «простым слепым испытанием» (single blind trial). Если все лица исследовательского центра, общаюшиеся и работающие с пациентами, не знают, кто из них какое лечение получает, то это «двойное слепое испытание» (double blind trial). 174
 Часто процесс «ослепления» достаточно сложен, например традиционная терапия предполагает применение таблетированных форм, а новое вмешательство использует инъекции. первой группе лечение придется дополнить введением физиологического раствора во втором — приемом плацебо per os Нелишне отметить, что вид, органолептические свойств и кратность назначения сравниваемых препаратов должны быть одинаковыми. 175
Часто процесс «ослепления» достаточно сложен, например традиционная терапия предполагает применение таблетированных форм, а новое вмешательство использует инъекции. первой группе лечение придется дополнить введением физиологического раствора во втором — приемом плацебо per os Нелишне отметить, что вид, органолептические свойств и кратность назначения сравниваемых препаратов должны быть одинаковыми. 175
 В настоящее время существует несколько причин, по которым н научных исследованиях рандомизация не используется: • незнание врачами исследователями основ доказательной медицины; • боязнь применить у пациента менее эффективный метол вмешательства, но именно ради выявления его реальной эффективности проводится РКИ; • слепое следование традиционной практике и боязнь получить результаты, отличные от общепринятых и мнения авторитетов; 176
В настоящее время существует несколько причин, по которым н научных исследованиях рандомизация не используется: • незнание врачами исследователями основ доказательной медицины; • боязнь применить у пациента менее эффективный метол вмешательства, но именно ради выявления его реальной эффективности проводится РКИ; • слепое следование традиционной практике и боязнь получить результаты, отличные от общепринятых и мнения авторитетов; 176
 Клинические вопросы и оптимальные типы В тоже время в последние годы термин «рандомизация» стал использоваться авторами публикаций как «магическое заклина¬ние» , гарантирующее авторам отсутствие критики и повышающее и х научный рейтинг самооценки. Истинная рандомизация подменяется ее декларированием, проявляется несопоставимостью сравниваемых групп и «информационным шумом» от выводов по нека¬чественно сделанным исследованиям. Так, K. F. Schultz et аl. считают, что только 9— 15% статей в медицинских журналах имели истинную рандомизацию. Сегодня для решения конкретного клинического вопроса иденти фицированы оптимальные ипы и дизайны иссле дований т. Каждый из видов исследований имеет свои достоинства и недостатки. 177
Клинические вопросы и оптимальные типы В тоже время в последние годы термин «рандомизация» стал использоваться авторами публикаций как «магическое заклина¬ние» , гарантирующее авторам отсутствие критики и повышающее и х научный рейтинг самооценки. Истинная рандомизация подменяется ее декларированием, проявляется несопоставимостью сравниваемых групп и «информационным шумом» от выводов по нека¬чественно сделанным исследованиям. Так, K. F. Schultz et аl. считают, что только 9— 15% статей в медицинских журналах имели истинную рандомизацию. Сегодня для решения конкретного клинического вопроса иденти фицированы оптимальные ипы и дизайны иссле дований т. Каждый из видов исследований имеет свои достоинства и недостатки. 177
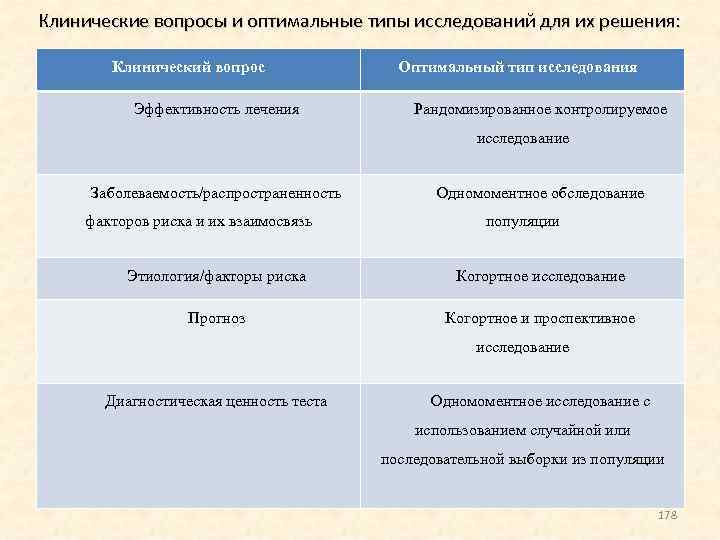 Клинические вопросы и оптимальные типы исследований для их решения: Клинический вопрос Эффективность лечения Оптимальный тип исследования Рандомизированное контролируемое исследование Заболеваемость/распространенность факторов риска и их взаимосвязь Одномоментное обследование популяции Этиология/факторы риска Когортное исследование Прогноз Когортное и проспективное исследование Диагностическая ценность теста Одномоментное исследование с использованием случайной или последовательной выборки из популяции 178
Клинические вопросы и оптимальные типы исследований для их решения: Клинический вопрос Эффективность лечения Оптимальный тип исследования Рандомизированное контролируемое исследование Заболеваемость/распространенность факторов риска и их взаимосвязь Одномоментное обследование популяции Этиология/факторы риска Когортное исследование Прогноз Когортное и проспективное исследование Диагностическая ценность теста Одномоментное исследование с использованием случайной или последовательной выборки из популяции 178
 Важно понять, что структура исследования, в существенной мере предопределяемая поставленным клиническим вопросом, прямо влияет на степень доказательности полученных данных. Главной задачей статистического анализа РКИ является установление разницы и степени ее достоверности по исходам (конечным точкам) между группой с анализируемым вмешательством и контрольной группой. В настоящее время существует много пакетов статистических программ для анализа полученных результатов (BMDP, SOLO, Statistica и другие). 179
Важно понять, что структура исследования, в существенной мере предопределяемая поставленным клиническим вопросом, прямо влияет на степень доказательности полученных данных. Главной задачей статистического анализа РКИ является установление разницы и степени ее достоверности по исходам (конечным точкам) между группой с анализируемым вмешательством и контрольной группой. В настоящее время существует много пакетов статистических программ для анализа полученных результатов (BMDP, SOLO, Statistica и другие). 179
 Для получения объективной информации об эффективности вмешательства в анализ необходимо включать всех первоначально рандомизированных больных, а не только тех, которым лечение проведено в строгом соответствии с протоколом исследования. Это один из основных способов минимизировать возможные ошибки, когда при intention to treat analysis исходят из допущения, что все пациенты получили лечение, предписанное при рандомизации. Выбывание пациентов из исследования по разным причинам (отказ от дальнейшего участия, побочные эффекты и плохая переносимость лечения, нарушения протокола пациентами или исследователями) не должно превышать 15% от исходного числа рандомизированных больных. Если процент выше, результаты исследования некорректны. Такой подход существенно снижает вероятность получения ложноположительного результата, когда на самом деле он отсутствует. 180
Для получения объективной информации об эффективности вмешательства в анализ необходимо включать всех первоначально рандомизированных больных, а не только тех, которым лечение проведено в строгом соответствии с протоколом исследования. Это один из основных способов минимизировать возможные ошибки, когда при intention to treat analysis исходят из допущения, что все пациенты получили лечение, предписанное при рандомизации. Выбывание пациентов из исследования по разным причинам (отказ от дальнейшего участия, побочные эффекты и плохая переносимость лечения, нарушения протокола пациентами или исследователями) не должно превышать 15% от исходного числа рандомизированных больных. Если процент выше, результаты исследования некорректны. Такой подход существенно снижает вероятность получения ложноположительного результата, когда на самом деле он отсутствует. 180
 Считается: если более 80% из включенных больных наблюдались до конца исследования, его результаты могут быть достаточно надежными. При малой выборке (число пациентов менее 30 в каждой из групп вмешательства) используют методы непараметрической статистики (тесты Фишера или Йетса). Для статистического анализа большого массива дискретных конечных точек вычисляют с квадрат. 181
Считается: если более 80% из включенных больных наблюдались до конца исследования, его результаты могут быть достаточно надежными. При малой выборке (число пациентов менее 30 в каждой из групп вмешательства) используют методы непараметрической статистики (тесты Фишера или Йетса). Для статистического анализа большого массива дискретных конечных точек вычисляют с квадрат. 181
 Результаты исследования представляются с использованием следующих показателей: абсолютного/относ ительного риска нежелательного исхода и их снижения с указанием статистической достоверности. которых необходимо пролечить для того, чтобы предотвратить один нежелательный исход заболевания число больных 182
Результаты исследования представляются с использованием следующих показателей: абсолютного/относ ительного риска нежелательного исхода и их снижения с указанием статистической достоверности. которых необходимо пролечить для того, чтобы предотвратить один нежелательный исход заболевания число больных 182
 • Часто статью с итогами РКИ предваряет опубликование его наиболее значимых результатов и выводов в материальных крупных международных конференций и съездов. • Структура статьи имеет обычный характер. • Обязательным требованием является максимально широкое представление дизайна и статистических аспектов РКИ. • Особый интерес может представлять обсуждение результатов, так как они могут дать дополнительную информацию о спорных моментах при его проведении. 183
• Часто статью с итогами РКИ предваряет опубликование его наиболее значимых результатов и выводов в материальных крупных международных конференций и съездов. • Структура статьи имеет обычный характер. • Обязательным требованием является максимально широкое представление дизайна и статистических аспектов РКИ. • Особый интерес может представлять обсуждение результатов, так как они могут дать дополнительную информацию о спорных моментах при его проведении. 183
 • В настоящее время для проведения РКИ разработаны этические и методологические стандарты. Необходимо помнить о том, что плацебо контролируемые исследования оправданы, когда не существует альтернативного способа лечения, эффективность которого не вызывает сомнений. • Сегодня врачам, исследователям и организатором исследований необходимо непрерывно повышать не только профессионализм, но и уровень знаний в области доказательной, правоведения и GCP. • При этом само проведение РКИ – не только наука, но и особый (и достаточно прибыльный) медицинский бизнес, что предъявляет еще более высокие этические требования ко всем его участникам. 184
• В настоящее время для проведения РКИ разработаны этические и методологические стандарты. Необходимо помнить о том, что плацебо контролируемые исследования оправданы, когда не существует альтернативного способа лечения, эффективность которого не вызывает сомнений. • Сегодня врачам, исследователям и организатором исследований необходимо непрерывно повышать не только профессионализм, но и уровень знаний в области доказательной, правоведения и GCP. • При этом само проведение РКИ – не только наука, но и особый (и достаточно прибыльный) медицинский бизнес, что предъявляет еще более высокие этические требования ко всем его участникам. 184


