Молекул. спектр..ppt
- Количество слайдов: 63
 Методы электронной спектроскопии
Методы электронной спектроскопии
 • Спектроскопия — разделы физики и аналитической химии, посвящённые изучению спектров взаимодействия излучения (в том числе, электромагнитного излучения, акустических волн и др. ) с веществом. В физике спектроскопические методы используются для изучения всевозможных свойств этих взаимодействий. В аналитической химии — для обнаружения и определения веществ при помощи измерения их характеристических спектров, то есть методами спектрометрии. К существенным преимуществам спектроскопии можно отнести возможность диагностики in situ, то есть непосредственно в «среде обитания» объекта, бесконтактно, дистанционно, без какой-либо специальной подготовки объекта. Поэтому она получила широкое развитие, например, в астрономии.
• Спектроскопия — разделы физики и аналитической химии, посвящённые изучению спектров взаимодействия излучения (в том числе, электромагнитного излучения, акустических волн и др. ) с веществом. В физике спектроскопические методы используются для изучения всевозможных свойств этих взаимодействий. В аналитической химии — для обнаружения и определения веществ при помощи измерения их характеристических спектров, то есть методами спектрометрии. К существенным преимуществам спектроскопии можно отнести возможность диагностики in situ, то есть непосредственно в «среде обитания» объекта, бесконтактно, дистанционно, без какой-либо специальной подготовки объекта. Поэтому она получила широкое развитие, например, в астрономии.
 • По объектам исследования можно выделить следующие виды спектроскопии: атомная спектроскопия, молекулярная спектроскопия, масс-спектроскопия, ядерная спектроскопия (ЯМР. ЭПР, ОЭС) и другие. • По типу излучения, которое используется в спектроскопии, её можно разделить на оптическую спектроскопию, рентгеновскую спектроскопию, фотоэлектронную спектроскопию, Мёссбауэровскую спектроскопию, масс-спектроскопию, спектроскопию с использованием радиоизлучения (γспектроскопия)и т. д.
• По объектам исследования можно выделить следующие виды спектроскопии: атомная спектроскопия, молекулярная спектроскопия, масс-спектроскопия, ядерная спектроскопия (ЯМР. ЭПР, ОЭС) и другие. • По типу излучения, которое используется в спектроскопии, её можно разделить на оптическую спектроскопию, рентгеновскую спектроскопию, фотоэлектронную спектроскопию, Мёссбауэровскую спектроскопию, масс-спектроскопию, спектроскопию с использованием радиоизлучения (γспектроскопия)и т. д.
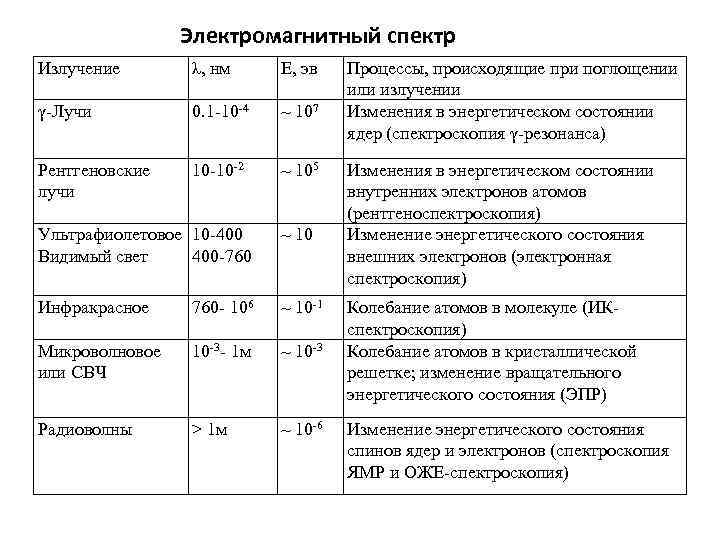 Электромагнитный спектр Излучение λ, нм Е, эв γ-Лучи 0. 1 -10 -4 ~ 107 Рентгеновские лучи 10 -10 -2 ~ 105 Ультрафиолетовое 10 -400 Видимый свет 400 -760 ~ 10 Инфракрасное 760 - 106 ~ 10 -1 Микроволновое или СВЧ 10 -3 - 1 м ~ 10 -3 Радиоволны > 1 м ~ 10 -6 Процессы, происходящие при поглощении или излучении Изменения в энергетическом состоянии ядер (спектроскопия γ-резонанса) Изменения в энергетическом состоянии внутренних электронов атомов (рентгеноспектроскопия) Изменение энергетического состояния внешних электронов (электронная спектроскопия) Колебание атомов в молекуле (ИКспектроскопия) Колебание атомов в кристаллической решетке; изменение вращательного энергетического состояния (ЭПР) Изменение энергетического состояния спинов ядер и электронов (спектроскопия ЯМР и ОЖЕ-спектроскопия)
Электромагнитный спектр Излучение λ, нм Е, эв γ-Лучи 0. 1 -10 -4 ~ 107 Рентгеновские лучи 10 -10 -2 ~ 105 Ультрафиолетовое 10 -400 Видимый свет 400 -760 ~ 10 Инфракрасное 760 - 106 ~ 10 -1 Микроволновое или СВЧ 10 -3 - 1 м ~ 10 -3 Радиоволны > 1 м ~ 10 -6 Процессы, происходящие при поглощении или излучении Изменения в энергетическом состоянии ядер (спектроскопия γ-резонанса) Изменения в энергетическом состоянии внутренних электронов атомов (рентгеноспектроскопия) Изменение энергетического состояния внешних электронов (электронная спектроскопия) Колебание атомов в молекуле (ИКспектроскопия) Колебание атомов в кристаллической решетке; изменение вращательного энергетического состояния (ЭПР) Изменение энергетического состояния спинов ядер и электронов (спектроскопия ЯМР и ОЖЕ-спектроскопия)
 • Прямая задача спектроскопии — предсказание вида спектра вещества исходя из знаний о его строении, составе и прочем. • Обратная задача спектроскопии — определение характеристик вещества (не являющихся непосредственно наблюдаемыми величинами) по свойствам его спектров (которые наблюдаются непосредственно и напрямую зависят как от определяемых характеристик, так и от внешних факторов).
• Прямая задача спектроскопии — предсказание вида спектра вещества исходя из знаний о его строении, составе и прочем. • Обратная задача спектроскопии — определение характеристик вещества (не являющихся непосредственно наблюдаемыми величинами) по свойствам его спектров (которые наблюдаются непосредственно и напрямую зависят как от определяемых характеристик, так и от внешних факторов).
 1. Атомный и молекулярный спектральные анализы позволяют определять элементный и молекулярный состав вещества, соответственно. В эмиссионном и абсорбционном методах состав определяется по спектрам испускания и поглощения. • M* → M + hν (эмиссия) • M + hν → M* (абсорбция)
1. Атомный и молекулярный спектральные анализы позволяют определять элементный и молекулярный состав вещества, соответственно. В эмиссионном и абсорбционном методах состав определяется по спектрам испускания и поглощения. • M* → M + hν (эмиссия) • M + hν → M* (абсорбция)
 • Спектральные методы являются наиболее распространенным видом исследования элементного состава вещества. Они достаточно экспрессные, разнообразны, широко используются для анализа как жидких, так и твердых и газообразных проб. • Под спектральным анализом понимают совокупность приемов, с помощью которых в результате измерения спектров исследуемого образца качественно или количественно определяют содержание в нем интересующих элементов. Обычно наблюдают спектральные линии, лежащие в видимой и ультрафиолетовой областях спектра. При использовании других областей это всегда отмечают в названии соответствующего метода: рентгеноспектральный анализ, инфракрасная спектроскопия, γ-спектроскопия и т. п. Томск, ТПУ, ИГНД, ГЭГХ 7 2/1/2018
• Спектральные методы являются наиболее распространенным видом исследования элементного состава вещества. Они достаточно экспрессные, разнообразны, широко используются для анализа как жидких, так и твердых и газообразных проб. • Под спектральным анализом понимают совокупность приемов, с помощью которых в результате измерения спектров исследуемого образца качественно или количественно определяют содержание в нем интересующих элементов. Обычно наблюдают спектральные линии, лежащие в видимой и ультрафиолетовой областях спектра. При использовании других областей это всегда отмечают в названии соответствующего метода: рентгеноспектральный анализ, инфракрасная спектроскопия, γ-спектроскопия и т. п. Томск, ТПУ, ИГНД, ГЭГХ 7 2/1/2018
 • Молекула, переведенная в возбужденное электронное состояние, может потерять избыток энергии любым из перечисленных ниже путем. • Разрыв связи: обычно приводит к необратимой химической реакции. • Испускание: излучается радиация той же частоты, что и поглощенная. • Флуоресценция: после возбуждения наблюдается излучение с длиной волны больше, чем поглощенная. Флуоресценция происходит быстро, часто за время менее 10 -6 с после поглощения. • Фосфоресценция: после возбуждения излучается более длинноволновая радиация, чем поглощенная. Испускание может продолжаться несколько часов после возбуждения. • Безызлучательные переходы: некоторые молекулы, поглотив энергию УФ-излучения, могут потерять эту энергию в результате процессов, не сопровождающихся излучением. • Способность поглощать электромагнитное излучение является общим свойством всех молекул. Поглощение избирательно, т. е. излучение определенной длины волны данной молекулой сильно поглощается, тогда как излучение других длин волн поглощается слабо или совсем не поглощается.
• Молекула, переведенная в возбужденное электронное состояние, может потерять избыток энергии любым из перечисленных ниже путем. • Разрыв связи: обычно приводит к необратимой химической реакции. • Испускание: излучается радиация той же частоты, что и поглощенная. • Флуоресценция: после возбуждения наблюдается излучение с длиной волны больше, чем поглощенная. Флуоресценция происходит быстро, часто за время менее 10 -6 с после поглощения. • Фосфоресценция: после возбуждения излучается более длинноволновая радиация, чем поглощенная. Испускание может продолжаться несколько часов после возбуждения. • Безызлучательные переходы: некоторые молекулы, поглотив энергию УФ-излучения, могут потерять эту энергию в результате процессов, не сопровождающихся излучением. • Способность поглощать электромагнитное излучение является общим свойством всех молекул. Поглощение избирательно, т. е. излучение определенной длины волны данной молекулой сильно поглощается, тогда как излучение других длин волн поглощается слабо или совсем не поглощается.
 Абсорбционная спектроскопия в видимой и УФ области Молекулярная спектроскопия
Абсорбционная спектроскопия в видимой и УФ области Молекулярная спектроскопия
 Лекция • Электронная, или УФ-спектроскопия – Закон Бера-Бугера-Ламберта – Способы изображения электронных спектров – Взаимосвязь электронных спектров и структуры органических молекул. Хромофоры и ауксохромы. – Классификация полос поглощения – Влияние различных факторов на электронные спектры поглощения
Лекция • Электронная, или УФ-спектроскопия – Закон Бера-Бугера-Ламберта – Способы изображения электронных спектров – Взаимосвязь электронных спектров и структуры органических молекул. Хромофоры и ауксохромы. – Классификация полос поглощения – Влияние различных факторов на электронные спектры поглощения
 • Способность поглощать электромагнитное излучение является общим свойством всех молекул. Поглощение избирательно, т. е. излучение определенной длины волны данной молекулой интенсивно поглощается, тогда как излучение при других длин волн поглощается слабо или совсем не поглощается. Если энергия излученного кванта света с энергией • Е=hν • совпадает с собственной внутренней энергией поглощающей частицы (молекулы, иона и т. д. ) по поглощение произойдет и частица приобретет другую, более высокую энергию • • М + hν = М(+)
• Способность поглощать электромагнитное излучение является общим свойством всех молекул. Поглощение избирательно, т. е. излучение определенной длины волны данной молекулой интенсивно поглощается, тогда как излучение при других длин волн поглощается слабо или совсем не поглощается. Если энергия излученного кванта света с энергией • Е=hν • совпадает с собственной внутренней энергией поглощающей частицы (молекулы, иона и т. д. ) по поглощение произойдет и частица приобретет другую, более высокую энергию • • М + hν = М(+)
 Закон Бера-Бугера-Ламберта Экспериментально открыт П. Бугером (1729), теоретически выведен И. Г. Ламбертом (1760), для растворов исследован А. Бером (1852) lg (I 0/I) = alc А = lc При с [моль/л], l[см] , a = П. Бугер И. Г. Ламберт а - коэффициент поглощения, константа, зависящая от , но не зависящая от концентрации; l - длина оптического пути; c - концентрация - молярный коэффициент поглощения Величина молярного коэффициента поглощения пропорциональна вероятности определенного перехода А = lg (I 0/ I) Т = I/I 0 А = - lg. Т А – погашение (оптическая плотность ) Т - пропускание I=I 0 10 -εlc
Закон Бера-Бугера-Ламберта Экспериментально открыт П. Бугером (1729), теоретически выведен И. Г. Ламбертом (1760), для растворов исследован А. Бером (1852) lg (I 0/I) = alc А = lc При с [моль/л], l[см] , a = П. Бугер И. Г. Ламберт а - коэффициент поглощения, константа, зависящая от , но не зависящая от концентрации; l - длина оптического пути; c - концентрация - молярный коэффициент поглощения Величина молярного коэффициента поглощения пропорциональна вероятности определенного перехода А = lg (I 0/ I) Т = I/I 0 А = - lg. Т А – погашение (оптическая плотность ) Т - пропускание I=I 0 10 -εlc
 • Условия применения закона Бугера- Ламберта. Бера 1. Закон справедлив для монохроматического света не слишком большой интенсивности Аλ=ελ lc 2. Пучек света должен быть параллельным 3. Закон справедлив для не слишком концентрированных растворов ε= f(n) 4. Температура должна быть постоянной в пределах 12 градусов 5. Закон соблюдается для систем, где поглощающими центрами являются частицы одного сорта Cr 2 O 2 -7 + H 2 O = 2 HCr. O-4 = 2 Cr. O 42 - + 2 H+ Различие в εCr O 2 2 - 7 εCr. O 2 - 4
• Условия применения закона Бугера- Ламберта. Бера 1. Закон справедлив для монохроматического света не слишком большой интенсивности Аλ=ελ lc 2. Пучек света должен быть параллельным 3. Закон справедлив для не слишком концентрированных растворов ε= f(n) 4. Температура должна быть постоянной в пределах 12 градусов 5. Закон соблюдается для систем, где поглощающими центрами являются частицы одного сорта Cr 2 O 2 -7 + H 2 O = 2 HCr. O-4 = 2 Cr. O 42 - + 2 H+ Различие в εCr O 2 2 - 7 εCr. O 2 - 4
 • Закон аддитивности • Поглощение света каким либо веществом не зависит от присутствия в растворе других веществ, как поглощающих свет, так и не поглощающих. A=A 1 + A 2 +…An • оптическая плотность смеси веществ равна сумме оптических плотностей каждого из них (при условии подчинения закону Бугера – Ламберта – Бера). Для одной и той же длины волны и толщины слоя для смеси веществ • A = ε 1 ∙l 1 ∙c 1 + ε 2 ∙l 2 ∙c 2 + …εn ∙ln ∙cn
• Закон аддитивности • Поглощение света каким либо веществом не зависит от присутствия в растворе других веществ, как поглощающих свет, так и не поглощающих. A=A 1 + A 2 +…An • оптическая плотность смеси веществ равна сумме оптических плотностей каждого из них (при условии подчинения закону Бугера – Ламберта – Бера). Для одной и той же длины волны и толщины слоя для смеси веществ • A = ε 1 ∙l 1 ∙c 1 + ε 2 ∙l 2 ∙c 2 + …εn ∙ln ∙cn
 Способы изображения электронных спектров Электронные спектры поглощения записываются в виде зависимости поглощения от длины волны (Ǻ , нм) или частоты (см-1) Величина поглощения может быть выражена: процентом поглощения [(I 0 – I)/ I 0 · 100% ], процентом пропускания [(I/I 0) · 100%], оптической плотностью D , коэффициентом молярного поглощения (ε) или его логарифмом (lgε) Область поглощения называется полосой; совокупность полос поглощения-спектр ее поглощения. Спектр – это последовательность квантов энергии электромагнитных колебаний, поглощенных, выделившихся или рассеянных при многочисленных переходах атомов или молекул из одних энергетических состояний в другие.
Способы изображения электронных спектров Электронные спектры поглощения записываются в виде зависимости поглощения от длины волны (Ǻ , нм) или частоты (см-1) Величина поглощения может быть выражена: процентом поглощения [(I 0 – I)/ I 0 · 100% ], процентом пропускания [(I/I 0) · 100%], оптической плотностью D , коэффициентом молярного поглощения (ε) или его логарифмом (lgε) Область поглощения называется полосой; совокупность полос поглощения-спектр ее поглощения. Спектр – это последовательность квантов энергии электромагнитных колебаний, поглощенных, выделившихся или рассеянных при многочисленных переходах атомов или молекул из одних энергетических состояний в другие.
 • Спектры поглощения в ультрафиолетовой (УФспектры) и видимой областях обусловлены энергетическими переходами между электронными состояниями молекулы, в связи с чем их также называют электронными спектрами. • Каждое электронное состояние молекулы характеризуется некоторым интервалом значений энергии, связанным с колебательным движением молекулы. Поэтому любому электронному переходу в спектре соответствует широкая полоса поглощения. При съемке спектра в газовой фазе, как правило, удается выявить колебательную структуру электронного перехода (в таком случае полоса поглощения выглядит как система близко расположенных узких полос)
• Спектры поглощения в ультрафиолетовой (УФспектры) и видимой областях обусловлены энергетическими переходами между электронными состояниями молекулы, в связи с чем их также называют электронными спектрами. • Каждое электронное состояние молекулы характеризуется некоторым интервалом значений энергии, связанным с колебательным движением молекулы. Поэтому любому электронному переходу в спектре соответствует широкая полоса поглощения. При съемке спектра в газовой фазе, как правило, удается выявить колебательную структуру электронного перехода (в таком случае полоса поглощения выглядит как система близко расположенных узких полос)
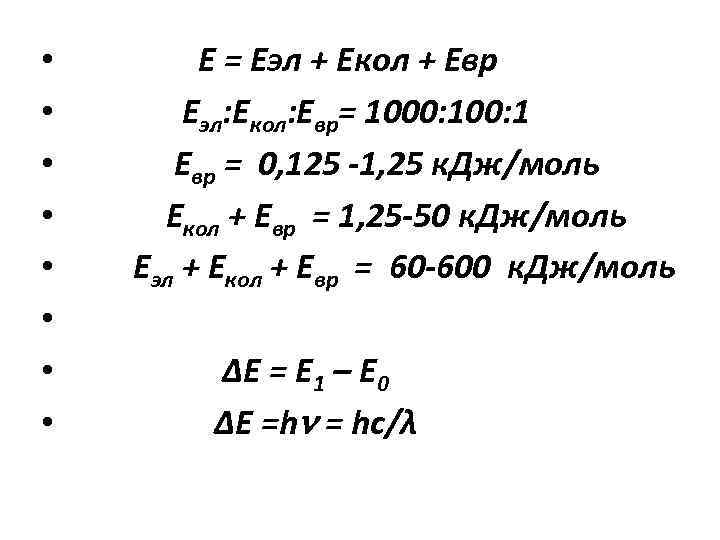 • • Е = Еэл + Екол + Евр Еэл: Екол: Евр= 1000: 1 Евр = 0, 125 -1, 25 к. Дж/моль Екол + Евр = 1, 25 -50 к. Дж/моль Еэл + Екол + Евр = 60 -600 к. Дж/моль ∆Е = Е 1 – Е 0 ∆Е =h = hc/λ
• • Е = Еэл + Екол + Евр Еэл: Екол: Евр= 1000: 1 Евр = 0, 125 -1, 25 к. Дж/моль Екол + Евр = 1, 25 -50 к. Дж/моль Еэл + Екол + Евр = 60 -600 к. Дж/моль ∆Е = Е 1 – Е 0 ∆Е =h = hc/λ
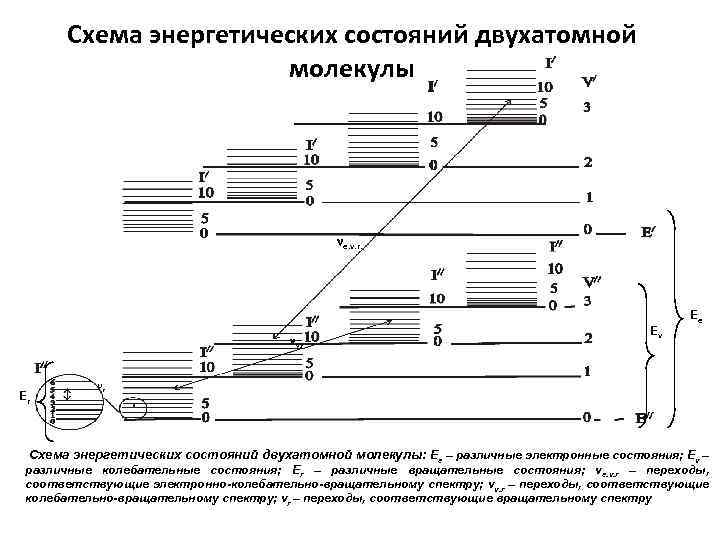 Схема энергетических состояний двухатомной молекулы ne. v. r. nv. r Еr Еv Ее nr Схема энергетических состояний двухатомной молекулы: Ее – различные электронные состояния; Еv – различные колебательные состояния; Еr – различные вращательные состояния; νе. v. r – переходы, соответствующие электронно-колебательно-вращательному спектру; νv. r – переходы, соответствующие колебательно-вращательному спектру; νr – переходы, соответствующие вращательному спектру
Схема энергетических состояний двухатомной молекулы ne. v. r. nv. r Еr Еv Ее nr Схема энергетических состояний двухатомной молекулы: Ее – различные электронные состояния; Еv – различные колебательные состояния; Еr – различные вращательные состояния; νе. v. r – переходы, соответствующие электронно-колебательно-вращательному спектру; νv. r – переходы, соответствующие колебательно-вращательному спектру; νr – переходы, соответствующие вращательному спектру
 • Электронные спектры (ближняя ультрафиолетовая и видимая области) характеризуют только сопряженные системы кратных связей, ароматические структуры, функциональные группы с гетероатомами и - связями (CO, NO 2 и др. ). В пределах этих фрагментов, являющихся "хромофорами", метод дает ценную информацию, включая некоторые данные о конфигурации и степени разветвленности скелета. Однако никаких данных о структуре удаленных от хромофорных частей молекулы, предельных соединений и соединений с изолированными двойными или тройными углерод - углеродными связями электронная спектроскопия не дает.
• Электронные спектры (ближняя ультрафиолетовая и видимая области) характеризуют только сопряженные системы кратных связей, ароматические структуры, функциональные группы с гетероатомами и - связями (CO, NO 2 и др. ). В пределах этих фрагментов, являющихся "хромофорами", метод дает ценную информацию, включая некоторые данные о конфигурации и степени разветвленности скелета. Однако никаких данных о структуре удаленных от хромофорных частей молекулы, предельных соединений и соединений с изолированными двойными или тройными углерод - углеродными связями электронная спектроскопия не дает.
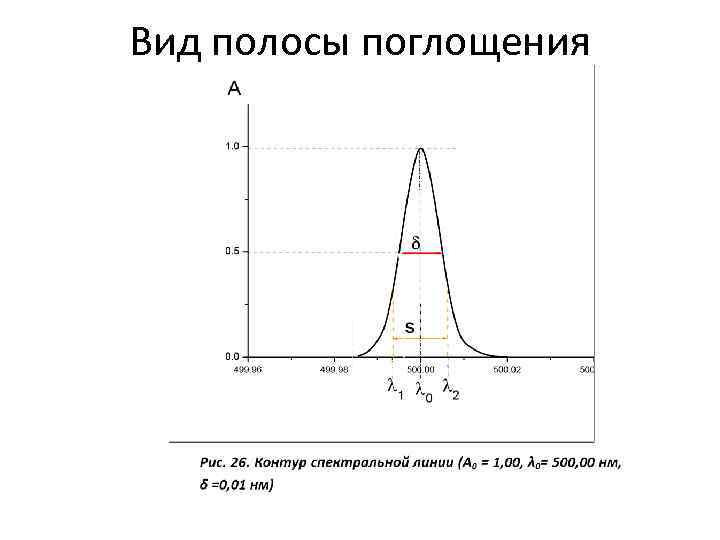 Вид полосы поглощения
Вид полосы поглощения
 Характеристики спектра поглощения Положение максимума по шкале длин волн – характеризуется типом электронных переходов и их энергией. Это качественная характеристика спектра E= hc/ max Высота максимума – соответствует вероятности электронного перехода. Чем больше вероятность перехода, тем выше максимум, тем больше величины А, . Это количественная характеристика спектра. Характер, форма максимума –определяется расстоянием между половинными значениями max. Зависит и определяется глубиной расположения орбиты на которую осуществляются переходы , температурой и окружением молекулами растворителя. Число полос поглощения (число максимумов) в спектре поглощения –определяется числом разрешенных переходов.
Характеристики спектра поглощения Положение максимума по шкале длин волн – характеризуется типом электронных переходов и их энергией. Это качественная характеристика спектра E= hc/ max Высота максимума – соответствует вероятности электронного перехода. Чем больше вероятность перехода, тем выше максимум, тем больше величины А, . Это количественная характеристика спектра. Характер, форма максимума –определяется расстоянием между половинными значениями max. Зависит и определяется глубиной расположения орбиты на которую осуществляются переходы , температурой и окружением молекулами растворителя. Число полос поглощения (число максимумов) в спектре поглощения –определяется числом разрешенных переходов.
 • Электронные переходы в молекуле классифицируют в соответствии с типом содержащихся в ней валентных электронов. Электроны, образующие простую связь, носят название -электронов, образующие двойную (тройную) связь – -электронов. Кроме того, в молекулах, содержащих атомы таких элементов как кислород, азот и т. д. , существуют неспаренные, или n-электроны. • В соответствии с этим различают -, и n-орбитали, которые, как правило, в основном состоянии заняты электронами. При возбуждении молекулы квантом света возможны переходы электронов со связывающей ( ) или несвязывающей (n) орбитали на разрыхляющую орбиталь ( * или *) с более высокой энергией, которая в основном состоянии свободна (вакантна). Эти переходы реализуются только в молекулах, содержащих ненасыщенные группировки.
• Электронные переходы в молекуле классифицируют в соответствии с типом содержащихся в ней валентных электронов. Электроны, образующие простую связь, носят название -электронов, образующие двойную (тройную) связь – -электронов. Кроме того, в молекулах, содержащих атомы таких элементов как кислород, азот и т. д. , существуют неспаренные, или n-электроны. • В соответствии с этим различают -, и n-орбитали, которые, как правило, в основном состоянии заняты электронами. При возбуждении молекулы квантом света возможны переходы электронов со связывающей ( ) или несвязывающей (n) орбитали на разрыхляющую орбиталь ( * или *) с более высокой энергией, которая в основном состоянии свободна (вакантна). Эти переходы реализуются только в молекулах, содержащих ненасыщенные группировки.
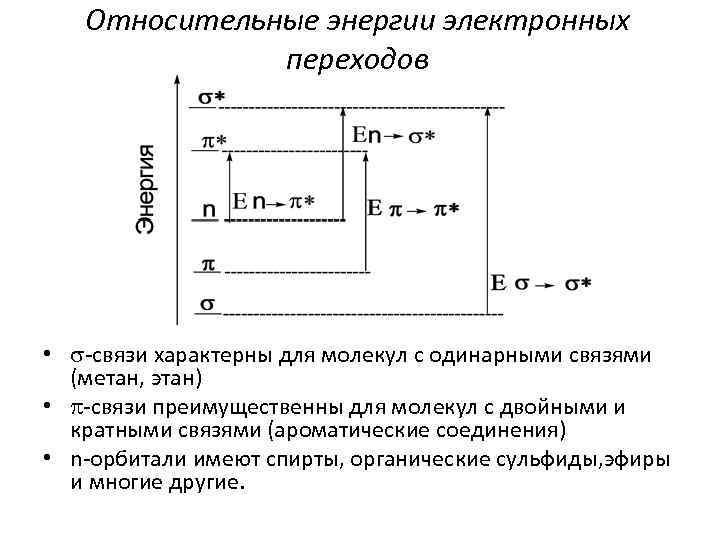 Относительные энергии электронных переходов • -связи характерны для молекул с одинарными связями (метан, этан) • -связи преимущественны для молекул с двойными и кратными связями (ароматические соединения) • n-орбитали имеют спирты, органические сульфиды, эфиры и многие другие.
Относительные энергии электронных переходов • -связи характерны для молекул с одинарными связями (метан, этан) • -связи преимущественны для молекул с двойными и кратными связями (ароматические соединения) • n-орбитали имеют спирты, органические сульфиды, эфиры и многие другие.
 Типы молекулярных орбиталей • пять типов молекулярных орбиталей: -, -, * и n. • переходы - *, n *, • -орбитали-электроны одинарных связей (C–C, C–H, C–O, C–N, C–S, C–Hlg) • -орбитали-электроны кратных связей (С=С, С=N, C=O, и др. ) • n-орбитали -молекулы, содержащие гетероатомы с неподелёнными электронными парами (O: , N: , S: , Hlg: и др. )
Типы молекулярных орбиталей • пять типов молекулярных орбиталей: -, -, * и n. • переходы - *, n *, • -орбитали-электроны одинарных связей (C–C, C–H, C–O, C–N, C–S, C–Hlg) • -орбитали-электроны кратных связей (С=С, С=N, C=O, и др. ) • n-орбитали -молекулы, содержащие гетероатомы с неподелёнными электронными парами (O: , N: , S: , Hlg: и др. )
 Классификация полос поглощения. K-полосы (нем. konjugiert – сопряженный) –полосы высокой интенсивности, характерные для систем, содержащих сопряженные связи. *-переходы 103 R-полосы (нем. radikalartig – радикальный) – полосы средней или низкой интенсивности характерные для систем, содержащих не поделенные электронные пары гетероатомных функциональных групп и радикалов. n *-переходы с 102 При переходе от неполярного растворителя к полярному или введении полярного заместителя K-полосы претерпевают батохромный сдвиг, а R-полосы – гипсохромный сдвиг. Полосы, обусловленные наличием в молекуле кратной (этиленовой) связи называют E-полосами (ethylenic), а бензоидной системы – B-полосами (benzenoid) *переходы ( от 102 до 103 )
Классификация полос поглощения. K-полосы (нем. konjugiert – сопряженный) –полосы высокой интенсивности, характерные для систем, содержащих сопряженные связи. *-переходы 103 R-полосы (нем. radikalartig – радикальный) – полосы средней или низкой интенсивности характерные для систем, содержащих не поделенные электронные пары гетероатомных функциональных групп и радикалов. n *-переходы с 102 При переходе от неполярного растворителя к полярному или введении полярного заместителя K-полосы претерпевают батохромный сдвиг, а R-полосы – гипсохромный сдвиг. Полосы, обусловленные наличием в молекуле кратной (этиленовой) связи называют E-полосами (ethylenic), а бензоидной системы – B-полосами (benzenoid) *переходы ( от 102 до 103 )
 ВЛИЯНИЕ СТРОЕНИЯ И СРЕДЫ НА УФ-СПЕКТРЫ ПОГЛОЩЕНИЯ • На Уф-спектры поглощения многих веществ (хромофоров) оказывает влияние ряд факторов. Проявляться это влияние может изменением интенсивности, формы полос или длины волны, при которой наблюдается поглощения. Наиболее распространенными являются: • смещение полос; • изменение интенсивности полос.
ВЛИЯНИЕ СТРОЕНИЯ И СРЕДЫ НА УФ-СПЕКТРЫ ПОГЛОЩЕНИЯ • На Уф-спектры поглощения многих веществ (хромофоров) оказывает влияние ряд факторов. Проявляться это влияние может изменением интенсивности, формы полос или длины волны, при которой наблюдается поглощения. Наиболее распространенными являются: • смещение полос; • изменение интенсивности полос.
 Взаимосвязь электронных спектров и структуры органических молекул Хромофоры Хромофор -простая функциональная группа, ответственная за поглощение с характеристическими величинами и X - - Y спектр соединения - сумма спектральных характеристик индивидуальных хромофоров X и Y X - Y новый, хромофор с новыми спектральными характеристиками Ауксохром – функциональная группа, которая сама по себе не поглощает в близком ультрафиолете, но может влиять на поведение сопряженного с ней хромофора Типичные ауксохромы: -SH, -NH 2 , -OH
Взаимосвязь электронных спектров и структуры органических молекул Хромофоры Хромофор -простая функциональная группа, ответственная за поглощение с характеристическими величинами и X - - Y спектр соединения - сумма спектральных характеристик индивидуальных хромофоров X и Y X - Y новый, хромофор с новыми спектральными характеристиками Ауксохром – функциональная группа, которая сама по себе не поглощает в близком ультрафиолете, но может влиять на поведение сопряженного с ней хромофора Типичные ауксохромы: -SH, -NH 2 , -OH
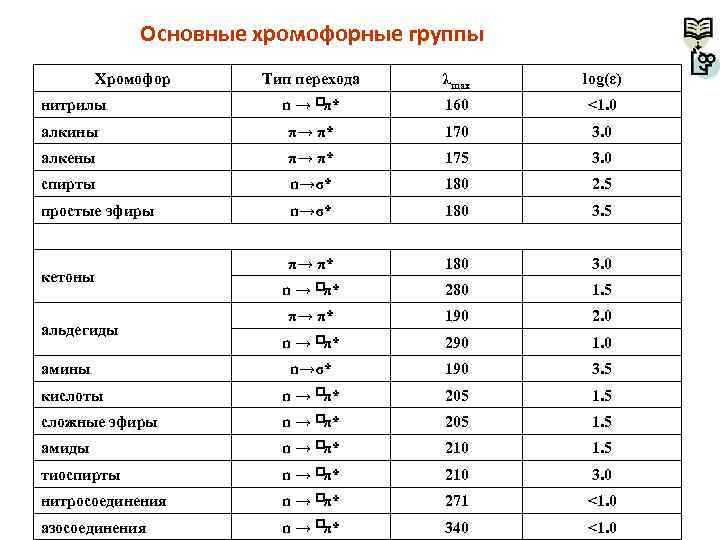 Основные хромофорные группы Хромофор Тип перехода λmax log(ε) нитрилы n → π* 160 <1. 0 алкины π→ π* 170 3. 0 алкены π→ π* 175 3. 0 спирты n→σ* 180 2. 5 простые эфиры n→σ* 180 3. 5 π→ π* 180 3. 0 n → π* 280 1. 5 π→ π* 190 2. 0 n → π* 290 1. 0 n→σ* 190 3. 5 кислоты n → π* 205 1. 5 сложные эфиры n → π* 205 1. 5 амиды n → π* 210 1. 5 тиоспирты n → π* 210 3. 0 нитросоединения n → π* 271 <1. 0 азосоединения n → π* 340 <1. 0 кетоны альдегиды амины
Основные хромофорные группы Хромофор Тип перехода λmax log(ε) нитрилы n → π* 160 <1. 0 алкины π→ π* 170 3. 0 алкены π→ π* 175 3. 0 спирты n→σ* 180 2. 5 простые эфиры n→σ* 180 3. 5 π→ π* 180 3. 0 n → π* 280 1. 5 π→ π* 190 2. 0 n → π* 290 1. 0 n→σ* 190 3. 5 кислоты n → π* 205 1. 5 сложные эфиры n → π* 205 1. 5 амиды n → π* 210 1. 5 тиоспирты n → π* 210 3. 0 нитросоединения n → π* 271 <1. 0 азосоединения n → π* 340 <1. 0 кетоны альдегиды амины
 • Атомную группировку, которая придает соединению способность и избирательному поглощению в ближнем ультрафиолете или видимой области, называют хромофором. • Хромофоры подразделяются на изолированные и сопряженные. К первым относят группировки с одной кратной связью, такие как С = С, С = О, N = N и т. п. , а ко вторым – структурные элементы, представляющие собой системы сопряженных кратных связей. Соединение, содержащее сопряженный хромофор, поглощает в более длинноволновой области и с большей интенсивностью, чем соединение, включающее те же, но изолированные хромофоры. В последнем случае спектр полифункционального соединения можно трактовать просто как результат суммирования поглощения соответствующих изолированных кратных связей. Некоторые из хромофоров (например, сопряженный хромофор С = С – С = С), обеспечивают поглощение в ближнем ультрафиолете за счет только *-перехода, другие (как изолированный хромофор С = О) – за счет *перехода, а третьи (например, сопряженный хромофор С = С – С = О) – вследствие реализации как *-, так и n *-переходов.
• Атомную группировку, которая придает соединению способность и избирательному поглощению в ближнем ультрафиолете или видимой области, называют хромофором. • Хромофоры подразделяются на изолированные и сопряженные. К первым относят группировки с одной кратной связью, такие как С = С, С = О, N = N и т. п. , а ко вторым – структурные элементы, представляющие собой системы сопряженных кратных связей. Соединение, содержащее сопряженный хромофор, поглощает в более длинноволновой области и с большей интенсивностью, чем соединение, включающее те же, но изолированные хромофоры. В последнем случае спектр полифункционального соединения можно трактовать просто как результат суммирования поглощения соответствующих изолированных кратных связей. Некоторые из хромофоров (например, сопряженный хромофор С = С – С = С), обеспечивают поглощение в ближнем ультрафиолете за счет только *-перехода, другие (как изолированный хромофор С = О) – за счет *перехода, а третьи (например, сопряженный хромофор С = С – С = О) – вследствие реализации как *-, так и n *-переходов.
 • Атомную группировку, не содержащую кратных связей, которая не имеет максимума поглощения в ближнем ультрафиолете, но включение которой в систему хромофора приводит к увеличению длины волны *перехода и увеличению интенсивности поглощения, называют ауксохромом. • Типичными ауксохромами являются ОН, NH 2, SH, т. е. группы, содержащие гетероатом со свободной электронной парой.
• Атомную группировку, не содержащую кратных связей, которая не имеет максимума поглощения в ближнем ультрафиолете, но включение которой в систему хромофора приводит к увеличению длины волны *перехода и увеличению интенсивности поглощения, называют ауксохромом. • Типичными ауксохромами являются ОН, NH 2, SH, т. е. группы, содержащие гетероатом со свободной электронной парой.
 • При выявлении взаимосвязи спектра со структурой молекулы бывает целесообразным наблюдение за изменениями в положении и интенсивности полос поглощения при переходе от некоторого родоначального хромофора, ответственного за поглощение, к модифицированному. Для этого в систему вводят дополнительную хромофорную или ауксохромную группу. Для характеристики спектральных изменений, вызванных модификацией структуры, используется специальная терминология:
• При выявлении взаимосвязи спектра со структурой молекулы бывает целесообразным наблюдение за изменениями в положении и интенсивности полос поглощения при переходе от некоторого родоначального хромофора, ответственного за поглощение, к модифицированному. Для этого в систему вводят дополнительную хромофорную или ауксохромную группу. Для характеристики спектральных изменений, вызванных модификацией структуры, используется специальная терминология:
 Взаимосвязь электронных спектров и структуры органических молекул Для характеристики спектральных изменений, вызванных модификацией структуры, введены специальные термины: гипсохромный сдвиг (синий сдвиг) – для смещения полос поглощения в коротковолновую область спектра; батохромный сдвиг (красный сдвиг) – для смещения полос поглощения в область длинных волн; гиперхромный эффект – увеличение интенсивности поглощения; гипохромный эффект – уменьшение интенсивности поглощения.
Взаимосвязь электронных спектров и структуры органических молекул Для характеристики спектральных изменений, вызванных модификацией структуры, введены специальные термины: гипсохромный сдвиг (синий сдвиг) – для смещения полос поглощения в коротковолновую область спектра; батохромный сдвиг (красный сдвиг) – для смещения полос поглощения в область длинных волн; гиперхромный эффект – увеличение интенсивности поглощения; гипохромный эффект – уменьшение интенсивности поглощения.
 • Смещение в сторону меньших длин волн (больших частот и энергий) называется гипсохромных сдвигом или синим смещением. Смещение в сторону больших длин волн (меньших частот и энергий) называется батохромным сдвигом или красным смещением. • Увеличение интенсивности полосы – называется гиперхромным эффектом, уменьшение – гипохромным эффектом
• Смещение в сторону меньших длин волн (больших частот и энергий) называется гипсохромных сдвигом или синим смещением. Смещение в сторону больших длин волн (меньших частот и энергий) называется батохромным сдвигом или красным смещением. • Увеличение интенсивности полосы – называется гиперхромным эффектом, уменьшение – гипохромным эффектом
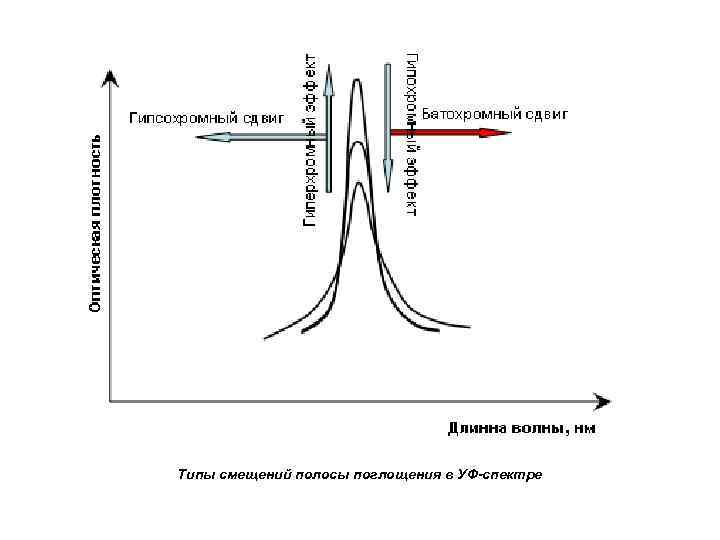 Типы смещений полосы поглощения в УФ-спектре
Типы смещений полосы поглощения в УФ-спектре
 • Наиболее чувствительны к различным факторам строения и среды являются n → π* и π → π* переходы. Здесь отчетливо проявляются эффекты сопряжения двойных связей в молекулах, полярность заместителей и среды. Рассмотрим последовательно эти три случая. • Сопряжение проявляется батохромным смещением полос поглощения для n → π* и π → π* переходов. • Увеличение полярности заместителя в α-положении такого хромофора как карбонильная группа сопровождается гипсохромным сдвигом n → π* полосы (см рис. ).
• Наиболее чувствительны к различным факторам строения и среды являются n → π* и π → π* переходы. Здесь отчетливо проявляются эффекты сопряжения двойных связей в молекулах, полярность заместителей и среды. Рассмотрим последовательно эти три случая. • Сопряжение проявляется батохромным смещением полос поглощения для n → π* и π → π* переходов. • Увеличение полярности заместителя в α-положении такого хромофора как карбонильная группа сопровождается гипсохромным сдвигом n → π* полосы (см рис. ).
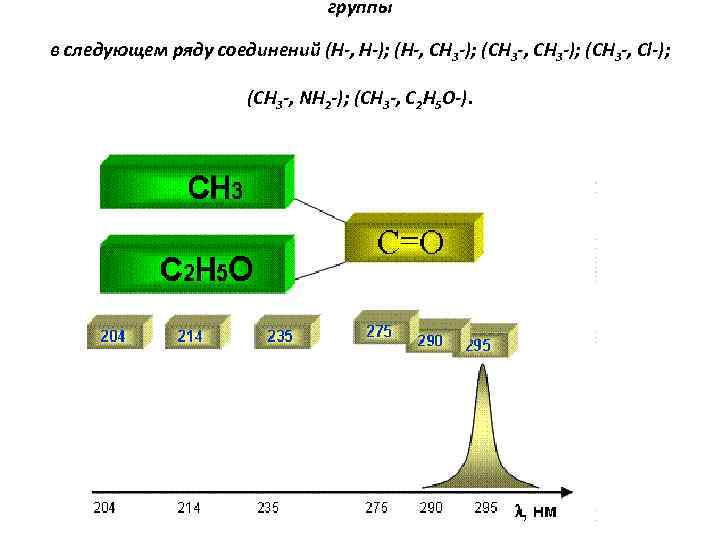 группы в следующем ряду соединений (H-, H-); (H-, CH 3 -); (CH 3 -, Cl-); (CH 3 -, NH 2 -); (CH 3 -, C 2 H 5 O-).
группы в следующем ряду соединений (H-, H-); (H-, CH 3 -); (CH 3 -, Cl-); (CH 3 -, NH 2 -); (CH 3 -, C 2 H 5 O-).
 • При переходе из газовой фазы в жидкую, или изменении полярности растворителя, энергия основного и возбужденного электронных состояний молекулы изменяется. Это также приводит к гипсо- или батохромным сдвигам полос поглощения для n → π* и π → π* переходов, т. е. оказывают влияние на разность энергий между электронными состояниями(см. рис. ). В общем случае влияние растворителя должно проявляться в понижении средней энергии как основного так и возбужденного состояний. И чем больше полярность растворителя, тем сильнее должны быть такие взаимодействия.
• При переходе из газовой фазы в жидкую, или изменении полярности растворителя, энергия основного и возбужденного электронных состояний молекулы изменяется. Это также приводит к гипсо- или батохромным сдвигам полос поглощения для n → π* и π → π* переходов, т. е. оказывают влияние на разность энергий между электронными состояниями(см. рис. ). В общем случае влияние растворителя должно проявляться в понижении средней энергии как основного так и возбужденного состояний. И чем больше полярность растворителя, тем сильнее должны быть такие взаимодействия.
 Механизм возникновения гипсо- и батохромных сдвигов в электронных спектрах поглощения под влиянием растворителя.
Механизм возникновения гипсо- и батохромных сдвигов в электронных спектрах поглощения под влиянием растворителя.
 • В общем случае влияние растворителя должно проявляться в понижении средней энергии как основного так и возбужденного состояний. И чем больше полярность растворителя, тем сильнее должны быть такие взаимодействия. Однако для того, чтобы произошел сдвиг частоты поглощения, необходимо изменить относительную энергию двух состояний.
• В общем случае влияние растворителя должно проявляться в понижении средней энергии как основного так и возбужденного состояний. И чем больше полярность растворителя, тем сильнее должны быть такие взаимодействия. Однако для того, чтобы произошел сдвиг частоты поглощения, необходимо изменить относительную энергию двух состояний.
 • В эксперименте для π → π* - переходов в полярных растворителях спектр поглощения сдвигается (батохромно) в сторону больших длин волн, а для n → π* - переходов гипсохромно. • В качестве примера на рис. приведены данные по влиянию растворителя на n → π* и π → π* переходы в карбонильной группе. • При n → π* - переходах взаимодействие молекул вещества с растворителем понижает энергию nорбитали в основном электронном состоянии изза сольватации или, в частности, при образовании водородной связи.
• В эксперименте для π → π* - переходов в полярных растворителях спектр поглощения сдвигается (батохромно) в сторону больших длин волн, а для n → π* - переходов гипсохромно. • В качестве примера на рис. приведены данные по влиянию растворителя на n → π* и π → π* переходы в карбонильной группе. • При n → π* - переходах взаимодействие молекул вещества с растворителем понижает энергию nорбитали в основном электронном состоянии изза сольватации или, в частности, при образовании водородной связи.
 Гипсохромный и батохромный сдвиги для n → π* и π → π* переходов (карбонильная группа) в ряду растворителей: гексан, диэтиловый эфир, этанол, метанол, вода.
Гипсохромный и батохромный сдвиги для n → π* и π → π* переходов (карбонильная группа) в ряду растворителей: гексан, диэтиловый эфир, этанол, метанол, вода.
 • Важным экспериментальным критерием отнесения полосы к *- или n *-переходам является направление смещения максимума поглощения (правило Мак – Конелла) при переходе от неполярных растворителей к полярным. Для n *-переходов в этом случае наблюдается "синий" или гипсохромный (в сторону более коротких волн), а для *-переходов чаще "красный" или батохромный (длинноволновый) сдвиг. • Самым надежным критерием отнесения полосы к переходу с участием несвязывающих электронов (n *) является ее исчезновение в кислых средах. Это объясняется протонированием n‑электронов неподеленной пары, в результате чего они теряют свой несвязывающий характер, и поэтому переход вообще не наблюдается.
• Важным экспериментальным критерием отнесения полосы к *- или n *-переходам является направление смещения максимума поглощения (правило Мак – Конелла) при переходе от неполярных растворителей к полярным. Для n *-переходов в этом случае наблюдается "синий" или гипсохромный (в сторону более коротких волн), а для *-переходов чаще "красный" или батохромный (длинноволновый) сдвиг. • Самым надежным критерием отнесения полосы к переходу с участием несвязывающих электронов (n *) является ее исчезновение в кислых средах. Это объясняется протонированием n‑электронов неподеленной пары, в результате чего они теряют свой несвязывающий характер, и поэтому переход вообще не наблюдается.
 • ЭЛЕКТРОННЫЕ СПЕКТРЫ ПОГЛОЩЕНИЯ ОСНОВНЫХ КЛАССОВ ОРГАНИЧЕСКИХ СОЕДИНЕНИЙ. • Предельные углеводороды. В этих соединениях содержатся только σ-связи, поэтому в их молекулах возможны только σ → σ* переходы. Соответствующие им полосы поглощения лежат в далеком ультрафиолете: • метан – 122 нм • этан – 135 нм • алканы - < 150 нм. • Для исследования этих соединений методом УФспектроскопии требуется специальная техника для работы в области вакуумного ультрафиолета.
• ЭЛЕКТРОННЫЕ СПЕКТРЫ ПОГЛОЩЕНИЯ ОСНОВНЫХ КЛАССОВ ОРГАНИЧЕСКИХ СОЕДИНЕНИЙ. • Предельные углеводороды. В этих соединениях содержатся только σ-связи, поэтому в их молекулах возможны только σ → σ* переходы. Соответствующие им полосы поглощения лежат в далеком ультрафиолете: • метан – 122 нм • этан – 135 нм • алканы - < 150 нм. • Для исследования этих соединений методом УФспектроскопии требуется специальная техника для работы в области вакуумного ультрафиолета.
 • Насыщенные углеводороды с гетероатомами. Таковыми являются алканы, содержащие в своем составе атомы О, S, N, галогенов. Они имеют неподеленные пары электронов на несвязывающих n-орбиталях. Для них, наряду с σ → σ* переходами могут наблюдаться и n → σ* переходы. В области 200 – 800 нм большинство углеводородов и их производных «прозрачны» , что позволяет использовать их в качестве растворителей. Для функциональных производных эта область чуть уже: 250 – 800 нм.
• Насыщенные углеводороды с гетероатомами. Таковыми являются алканы, содержащие в своем составе атомы О, S, N, галогенов. Они имеют неподеленные пары электронов на несвязывающих n-орбиталях. Для них, наряду с σ → σ* переходами могут наблюдаться и n → σ* переходы. В области 200 – 800 нм большинство углеводородов и их производных «прозрачны» , что позволяет использовать их в качестве растворителей. Для функциональных производных эта область чуть уже: 250 – 800 нм.
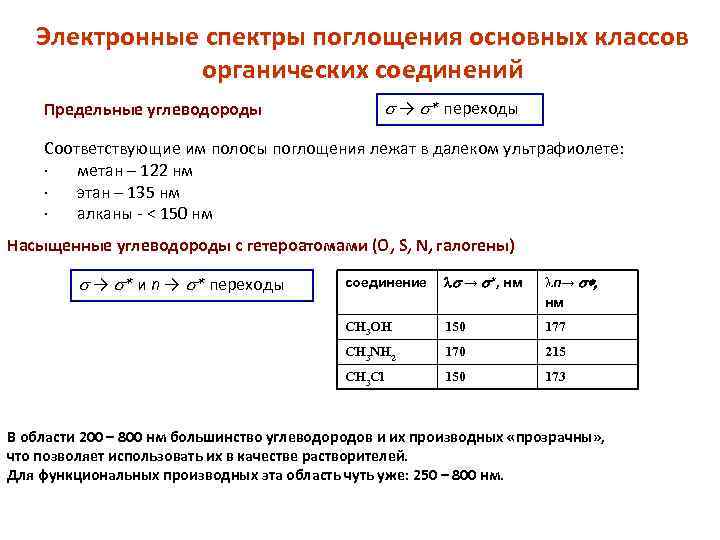 Электронные спектры поглощения основных классов органических соединений s → s* переходы Предельные углеводороды Соответствующие им полосы поглощения лежат в далеком ультрафиолете: · метан – 122 нм · этан – 135 нм · алканы - < 150 нм Насыщенные углеводороды с гетероатомами (О, S, N, галогены) s → s* и n → s* переходы соединение → *, нм n→ *, нм CH 3 OH 150 177 CH 3 NH 2 170 215 CH 3 Cl 150 173 В области 200 – 800 нм большинство углеводородов и их производных «прозрачны» , что позволяет использовать их в качестве растворителей. Для функциональных производных эта область чуть уже: 250 – 800 нм.
Электронные спектры поглощения основных классов органических соединений s → s* переходы Предельные углеводороды Соответствующие им полосы поглощения лежат в далеком ультрафиолете: · метан – 122 нм · этан – 135 нм · алканы - < 150 нм Насыщенные углеводороды с гетероатомами (О, S, N, галогены) s → s* и n → s* переходы соединение → *, нм n→ *, нм CH 3 OH 150 177 CH 3 NH 2 170 215 CH 3 Cl 150 173 В области 200 – 800 нм большинство углеводородов и их производных «прозрачны» , что позволяет использовать их в качестве растворителей. Для функциональных производных эта область чуть уже: 250 – 800 нм.
 Электронные спектры поглощения основных классов органических соединений Этилены s → s* → p* (lmax =165 нм, emax > 104) переходы Алкильные заместители в этилене смещают → * полосу поглощения в красную область, и с ростом числа алкильных заместителей величина батохромного сдвига увеличивается. Соединения с сопряженными двойными связями Сопряжение проявляется в УФ-спектрах батохромным сдвигом для полосы → * перехода Структура Фрагмента Величина инкремента, нм Диеновая система в одном кольце 36 Дополнительное сопряжение, двойная связь 30 Экзоциклическая двойная связь (двойная связь вне цикла) 5 Заместители: · алкил · -OR · -OCOR · SR · -NR 2 · -Cl, -Br 5 6 0 30 60 5
Электронные спектры поглощения основных классов органических соединений Этилены s → s* → p* (lmax =165 нм, emax > 104) переходы Алкильные заместители в этилене смещают → * полосу поглощения в красную область, и с ростом числа алкильных заместителей величина батохромного сдвига увеличивается. Соединения с сопряженными двойными связями Сопряжение проявляется в УФ-спектрах батохромным сдвигом для полосы → * перехода Структура Фрагмента Величина инкремента, нм Диеновая система в одном кольце 36 Дополнительное сопряжение, двойная связь 30 Экзоциклическая двойная связь (двойная связь вне цикла) 5 Заместители: · алкил · -OR · -OCOR · SR · -NR 2 · -Cl, -Br 5 6 0 30 60 5
 Электронные спектры поглощения основных классов органических соединений Карбонилсодержащие соединения n → * переходы Обнаруживается в УФ-спектре по полосе n → * перехода. Положение чувствительно к полярности растворителя и характеру заместителей X, Y. В полярных растворителях (особенно склонных к образованию водородных связей) эта полоса смещается гипсохромно. Замена Н-атома другими заместителями X, Y также приводит к гипсохромному сдвигу.
Электронные спектры поглощения основных классов органических соединений Карбонилсодержащие соединения n → * переходы Обнаруживается в УФ-спектре по полосе n → * перехода. Положение чувствительно к полярности растворителя и характеру заместителей X, Y. В полярных растворителях (особенно склонных к образованию водородных связей) эта полоса смещается гипсохромно. Замена Н-атома другими заместителями X, Y также приводит к гипсохромному сдвигу.
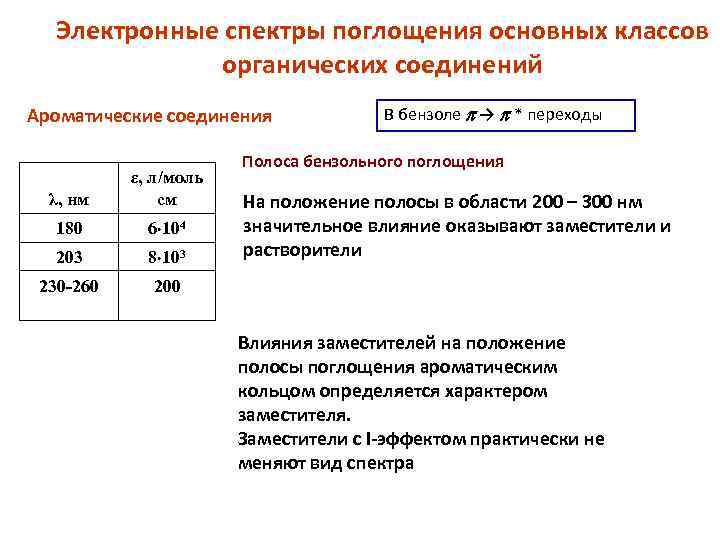 Электронные спектры поглощения основных классов органических соединений Ароматические соединения λ, нм ε, л/моль см 180 6 104 203 8 103 230 -260 В бензоле → * переходы Полоса бензольного поглощения 200 На положение полосы в области 200 – 300 нм значительное влияние оказывают заместители и растворители Влияния заместителей на положение полосы поглощения ароматическим кольцом определяется характером заместителя. Заместители с I-эффектом практически не меняют вид спектра
Электронные спектры поглощения основных классов органических соединений Ароматические соединения λ, нм ε, л/моль см 180 6 104 203 8 103 230 -260 В бензоле → * переходы Полоса бензольного поглощения 200 На положение полосы в области 200 – 300 нм значительное влияние оказывают заместители и растворители Влияния заместителей на положение полосы поглощения ароматическим кольцом определяется характером заместителя. Заместители с I-эффектом практически не меняют вид спектра
 • В УФ-спектре бензола наблюдается три полосы различной интенсивности • На положение полосы в области 200 – 300 нм значительное влияние оказывают заместители и растворители. Она имеет, как правило, отчетливо выраженную колебательную структуру. На рис. в качестве примера приведены спектры поглощения бензола, толуола и бензальдегида соответственно.
• В УФ-спектре бензола наблюдается три полосы различной интенсивности • На положение полосы в области 200 – 300 нм значительное влияние оказывают заместители и растворители. Она имеет, как правило, отчетливо выраженную колебательную структуру. На рис. в качестве примера приведены спектры поглощения бензола, толуола и бензальдегида соответственно.
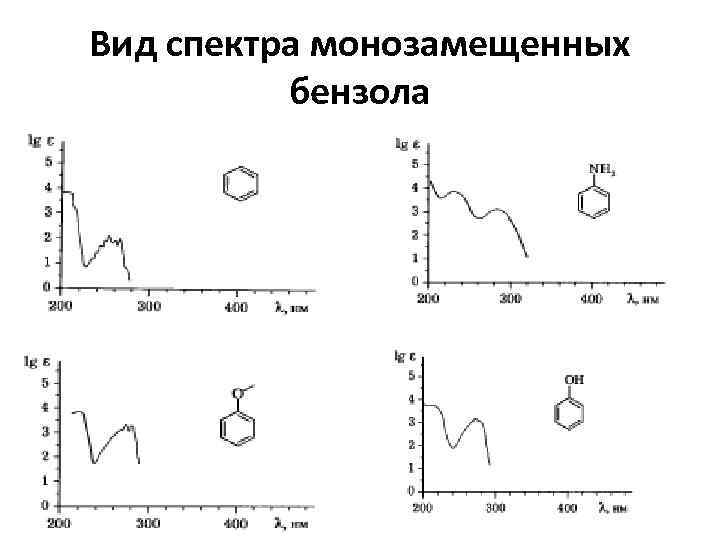 Вид спектра монозамещенных бензола
Вид спектра монозамещенных бензола

 • Соединения с сопряженными двойными связями. Сопряжение проявляется в УФспектрах батохромным сдвигом для полосы π → π* перехода. Объяснение этому эффекту находят в π - π сопряжении, т. е. перекрывании π орбиталей. В результате такого сопряжения образуются две новые связующие и две разрыхляющие МО, что уменьшает разность энергий между ними, т. е. существенно облегчает электронные переходы типа n → π* и π → π* (см. рис. ).
• Соединения с сопряженными двойными связями. Сопряжение проявляется в УФспектрах батохромным сдвигом для полосы π → π* перехода. Объяснение этому эффекту находят в π - π сопряжении, т. е. перекрывании π орбиталей. В результате такого сопряжения образуются две новые связующие и две разрыхляющие МО, что уменьшает разность энергий между ними, т. е. существенно облегчает электронные переходы типа n → π* и π → π* (см. рис. ).
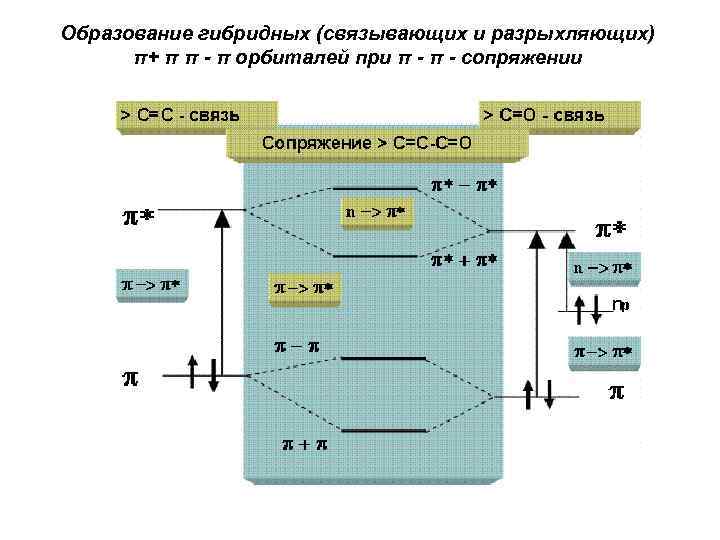 Образование гибридных (связывающих и разрыхляющих) π+ π π - π орбиталей при π - сопряжении
Образование гибридных (связывающих и разрыхляющих) π+ π π - π орбиталей при π - сопряжении
 • Полоса π → π* перехода для изолированной двойной связи (этилене, например) имеет максимум при λ = 165 нм, а за счет π - π сопряжения (в бутадиене) - λ = 217 нм. Если цепь сопряжения в молекуле разорвать (разъединить, например –С=С- связи метиленовой группой -СН 2 -), то батохромный сдвиг исчезает и наблюдается поглощение характерное для изолированного π → π* перехода в этилене.
• Полоса π → π* перехода для изолированной двойной связи (этилене, например) имеет максимум при λ = 165 нм, а за счет π - π сопряжения (в бутадиене) - λ = 217 нм. Если цепь сопряжения в молекуле разорвать (разъединить, например –С=С- связи метиленовой группой -СН 2 -), то батохромный сдвиг исчезает и наблюдается поглощение характерное для изолированного π → π* перехода в этилене.
 Изменение спектральных характеристик систем с сопряженными связями • Наличие системы сопряженных кратных связей вносит принципиальные изменения в спектры: в этих случаях наблюдается изменение и максимума и интенсивности поглощения. В этих системах полосы поглощения невозможно приписать отдельным структурным элементам , ответственной за поглощение становится вся система сопряженных связей. • в сопряженных системах полосы поглощения обладают гораздо большей интенсивностью (К-полосы, lgε > 4), чем в несопряженных, причем коэффициент экстинкции возрастает с увеличением цепи сопряжения. CH 2=CH–CH=CH 2 λмакс. , нм = 218 ; ε (л/моль • см)=23000 • CH 3 CH=CH–CH=CH 2 λмакс. , нм =223 ε(л /моль • см) = 25000 • (CH 3)2 C=CH–CH=C(CH 3)2 λмакс. , нм = 242 ε (л/моль • см)= 26000 • Сопряжение ненасыщенных хромофоров приводит к батохромному смещению соответствующих полос поглощения. • смещение полосы поглощения закономерно зависит от протяженности системы сопряженных связей. • для сопряженных систем характерно увеличение интенсивности поглощения.
Изменение спектральных характеристик систем с сопряженными связями • Наличие системы сопряженных кратных связей вносит принципиальные изменения в спектры: в этих случаях наблюдается изменение и максимума и интенсивности поглощения. В этих системах полосы поглощения невозможно приписать отдельным структурным элементам , ответственной за поглощение становится вся система сопряженных связей. • в сопряженных системах полосы поглощения обладают гораздо большей интенсивностью (К-полосы, lgε > 4), чем в несопряженных, причем коэффициент экстинкции возрастает с увеличением цепи сопряжения. CH 2=CH–CH=CH 2 λмакс. , нм = 218 ; ε (л/моль • см)=23000 • CH 3 CH=CH–CH=CH 2 λмакс. , нм =223 ε(л /моль • см) = 25000 • (CH 3)2 C=CH–CH=C(CH 3)2 λмакс. , нм = 242 ε (л/моль • см)= 26000 • Сопряжение ненасыщенных хромофоров приводит к батохромному смещению соответствующих полос поглощения. • смещение полосы поглощения закономерно зависит от протяженности системы сопряженных связей. • для сопряженных систем характерно увеличение интенсивности поглощения.
 • Имеются эмпирические уравнения и правила, которые позволяют рассчитывать длину волны максимума поглощения для соединений с сопряженными двойными связями (правила Вудворда-Физера для оценки положения полосы π- π*-перехода, расширенное правило Вудворда для оценки положения полосы π- π*-перехода, правило Скотта для оценки К-полосы. . • За основу берут бутадиеновый остов. Для этой структуры максимум полосы поглощения принимают равным λmax = 217 нм. Далее к этой величине добавляют значения инкрементов для отдельных фрагментов молекулы, т. е. ведут расчет по формуле: • λх max = 217 +Σ инкрементов •
• Имеются эмпирические уравнения и правила, которые позволяют рассчитывать длину волны максимума поглощения для соединений с сопряженными двойными связями (правила Вудворда-Физера для оценки положения полосы π- π*-перехода, расширенное правило Вудворда для оценки положения полосы π- π*-перехода, правило Скотта для оценки К-полосы. . • За основу берут бутадиеновый остов. Для этой структуры максимум полосы поглощения принимают равным λmax = 217 нм. Далее к этой величине добавляют значения инкрементов для отдельных фрагментов молекулы, т. е. ведут расчет по формуле: • λх max = 217 +Σ инкрементов •
 • Количественный спектральный анализ 1. Метод градуировочного (калибровочного) графика 2. Метод молярного коэффициента погашения: ε=Aст/l. Cст Cx =Ax/εl 3. Метод добавок: Ах = εl. Cx Ах+ст = εl(Сх + Сст) Сх = Сст Ах/ Ах+ст - Ах
• Количественный спектральный анализ 1. Метод градуировочного (калибровочного) графика 2. Метод молярного коэффициента погашения: ε=Aст/l. Cст Cx =Ax/εl 3. Метод добавок: Ах = εl. Cx Ах+ст = εl(Сх + Сст) Сх = Сст Ах/ Ах+ст - Ах
 → 4. Метод дифференциальной фотометрии Применяется для фотометрирования интенсивно окрашенных растворов Тх= Ix /I 0 Т/х= Ix /I ср Тср= Iср/I 0 Ix / I ср= Т/х= Тх / Тср / А x =Ax – Aср / А x =εl. Cx -Aср
→ 4. Метод дифференциальной фотометрии Применяется для фотометрирования интенсивно окрашенных растворов Тх= Ix /I 0 Т/х= Ix /I ср Тср= Iср/I 0 Ix / I ср= Т/х= Тх / Тср / А x =Ax – Aср / А x =εl. Cx -Aср
 Нефелометрический и турбидиметрический анализ
Нефелометрический и турбидиметрический анализ
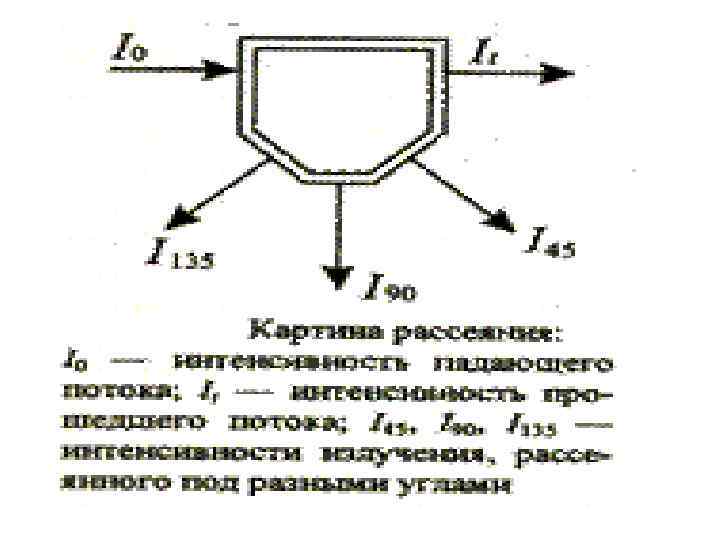
 В нефелометрическом и турбидиметрическом анализе используется явление рассеяния света твердыми частицами, находящимися в растворе во взвешенном состоянии. Метод, в котором используют интенсивность прошедшего света It, называют турбидиметрией • S = lg (I 0/ It) = k b N • S – мутность; k – коэффициент мутности; b – длина пути; N – число рассеивающих частиц в единице объема. А=εlc Для турбидиметрических измерений используют фотометр или спектрофотометр. Для нефелометрических измерений используют нефелометр или флуориметр. максимальная чувствительность достигается при использовании излучения голубой (400 нм) или ближней ультрафиолетовой области.
В нефелометрическом и турбидиметрическом анализе используется явление рассеяния света твердыми частицами, находящимися в растворе во взвешенном состоянии. Метод, в котором используют интенсивность прошедшего света It, называют турбидиметрией • S = lg (I 0/ It) = k b N • S – мутность; k – коэффициент мутности; b – длина пути; N – число рассеивающих частиц в единице объема. А=εlc Для турбидиметрических измерений используют фотометр или спектрофотометр. Для нефелометрических измерений используют нефелометр или флуориметр. максимальная чувствительность достигается при использовании излучения голубой (400 нм) или ближней ультрафиолетовой области.
 • Метод с измерением интенсивности рассеянного света под углом 90 о (или какимлибо другим) называют нефелометрией. Зависимость интенсивности рассеянного света от концентрации передается уравнением Релея • Ip=I 0 [ n 21 – n 22 / n 22 Nv 2/λ 4 r 2 (1 + cos 2β ) ] • Ip=I 0 k Nv 2/λ 4 C=N/NAV • Ip=I 0 k NACV v 2/λ 4 • При V, v, λ=const Ip=I 0 k/C Ip / I 0. =k/C • Aкаж=-lg Ip / I 0 Aкаж= -lg. C -lg k/
• Метод с измерением интенсивности рассеянного света под углом 90 о (или какимлибо другим) называют нефелометрией. Зависимость интенсивности рассеянного света от концентрации передается уравнением Релея • Ip=I 0 [ n 21 – n 22 / n 22 Nv 2/λ 4 r 2 (1 + cos 2β ) ] • Ip=I 0 k Nv 2/λ 4 C=N/NAV • Ip=I 0 k NACV v 2/λ 4 • При V, v, λ=const Ip=I 0 k/C Ip / I 0. =k/C • Aкаж=-lg Ip / I 0 Aкаж= -lg. C -lg k/
 Применение методов, основанных на измерении рассеяния света, достаточно ограничено, прежде всего потому, что на измеряемый сигнал сильно влияет размер частиц. Поэтому необходимо строгое соблюдение идентичности условий построения градуировочного графика и анализа исследуемого раствора. Нефелометрия, и турбидиметрия могут быть полезными для селективных аналитических реакций, в результате которых образуется твердое соединение. Описаны методики определения аммиака иодидом ртути (реактив Несслера), фосфата в виде малорастворимого соединения с молибденом и стрихнином, сульфата бария с пределами обнаружения десятые-сотые доли микрограмма в миллилитре и др. Практическое использования таких методов – это применение лазеров для дистанционного определения частиц, содержащихся в воздушном пространстве, определение средней молекулярной массы полимеров в растворах.
Применение методов, основанных на измерении рассеяния света, достаточно ограничено, прежде всего потому, что на измеряемый сигнал сильно влияет размер частиц. Поэтому необходимо строгое соблюдение идентичности условий построения градуировочного графика и анализа исследуемого раствора. Нефелометрия, и турбидиметрия могут быть полезными для селективных аналитических реакций, в результате которых образуется твердое соединение. Описаны методики определения аммиака иодидом ртути (реактив Несслера), фосфата в виде малорастворимого соединения с молибденом и стрихнином, сульфата бария с пределами обнаружения десятые-сотые доли микрограмма в миллилитре и др. Практическое использования таких методов – это применение лазеров для дистанционного определения частиц, содержащихся в воздушном пространстве, определение средней молекулярной массы полимеров в растворах.


