Методы экстракции и анализа НК1.ppt
- Количество слайдов: 21

Методы экстракции и анализа нуклеиновых кислот ЦКП ВНИИСБ «Биотехнология»

Общие сведения о НК Нуклеиновые кислоты – это макромолекулы, обеспечивающие хранение, наследование и реализацию генетической информации. ДНК • у эукариот находится в ядре в составе хромосом, в митохондриях и пластидах, • у прокариот кольцевая молекула прикреплена к внутренней мембране, имеются автономные плазмидные ДНК Размер генома мыши 2. 8 x 109 п. н. , человека 3. 3 х109 п. н. , пшеницы 17 х109 п. н. РНК р-РНК находятся в составе рибосом (80 -90% тотальной РНК), и-РНК информационные РНК (2%), т-РНК (6%) микро-РНК (1%) Размеры РНК 10 -10 000 п. н.

ДНК человека Общая длина всех молекул ДНК гаплоидного набора человека составляет 3. 3 х109 н. п. (1 м). Полная запись генома человека с использованием однобуквенных символов (AGCAAT. . . ) заняла бы около 1000 томов по 1000 страниц каждый и 3000 знаков на странице. В каждой хромосоме содержится одна молекула ДНК. В хромосоме 21 (самая маленькая хромосома в геноме человека) молекула ДНК содержит 50 000 н. п. , длина ее равна 1, 5 см. Длина молекулы ДНК в хромосоме среднего размера равна примерно 130 000 н. п. , или 4 см (в записи однобуквенными символами — 45 томов). В геноме человека содержится 22 -25 тыс. генов, что составляет 1. 5 – 2 % от общего количества ДНК. Остальная часть генома – некодирующая.

Материал для выделения ДНК можно выделить практически из любого материала. Биологический материал (кровь, слюна , моча, волосы, кости, ткань, экскременты, растительный материал, клеточные культуры ) Пищевые продукты, кроме прошедших глубокую переработку Неорганические материалы, содержащие биоту (почва, вода, смывы и соскобы с поверхностей

Для чего выделять НК 1. Анализ присутствия патогенов (вирусов, бактерий, паразитов) в организме. 2. Анализ онкомаркеров 3. Выявление мутаций 4. Поиск генов 5. Идентификация организмов (видов, сортов, индивидуумов) 6. Поиск специфических маркеров 7. Филогения 8. Секвенирование генов и геномов Метод выделения ДНК зависит от типа образца, поставленной задачи, времени и стоимости анализа.

Пробоподготовка • Отбор проб (представительная проба) • Исключение контаминации пробы • Соблюдение режимов хранения и доставки пробы • Измельчение пробы • Концентрация пробы • Предварительный лизис образца
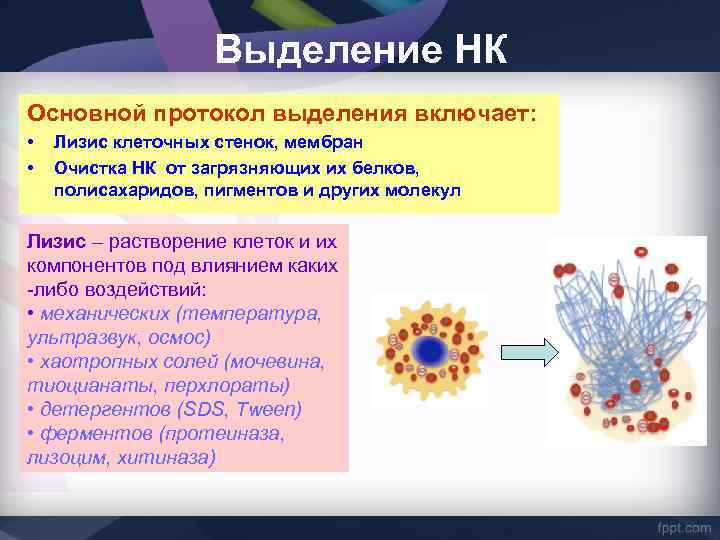
Выделение НК Основной протокол выделения включает: • • Лизис клеточных стенок, мембран Очистка НК от загрязняющих их белков, полисахаридов, пигментов и других молекул Лизис – растворение клеток и их компонентов под влиянием каких -либо воздействий: • механических (температура, ультразвук, осмос) • хаотропных солей (мочевина, тиоцианаты, перхлораты) • детергентов (SDS, Tween) • ферментов (протеиназа, лизоцим, хитиназа)

Выделение НК Очистка НК Удаление загрязнителей Удаление ДНК • органическими растворителями • на сорбенте (силика, магнитные (фенол, хлороформ) – фенольный метод выделения • осаждением солевыми растворами – солевой метод выделения • ионнообменными смолами и сорбентами (Сheleх, декстраны) – экспресс-методы выделения частицы) – сорбентный метод выделения, выделение на магнитных частицах, выделение на колонках • прямое осаждение спиртом • СТАВ – СТАВ-метод

Ph/Сl метод выделения ДНК 1. Механическое или энзиматическое разрушение клеток в присутствии детергентов 2. Удаление клеточного дебриса центрифугированием 3. Смешивание с фенолом или фенол/хлороформом 1: 1, центрифугирование 4. Осаждение ДНК спиртом 5. Промывка 70% спиртом 6. Высушивание ДНК 7. Растворение ДНК

Ph/Сl метод выделения ДНК Преимущества: получение ДНК высокой степени очистки, незначительные механические повреждения ДНК, получение ДНК в высокой концентрации, подходит для различных объектов выделения (листьев, семян, коры, животных тканей) Недостатки: токсичность реагентов, большой расход одноразового пластика, длительность процедуры, невозможность автоматизации, наборы реагентов редко выпускаются производителями из-за токсичности производства и специальных условий транспортировки, высокая стоимость набора

Сорбентный метод выделения ДНК 1. Лизис клеток хаотропными солями 2. Осаждение ДНК на сорбент 3. Отмывка сорбента от ингибиторов (2 -3 раза в зависимости от загрязнения) 4. Элюция ДНК с сорбента Преимущества: высокая степень очистки ДНК, подходит для различных объектов выделения (биологических жидкостей, бактериальных культур, очистки после энзиматического лизиса), низкая стоимость и доступность растворов реагентов Недостатки: большие потери при выделении, невозможность выделения малого количества материала, фрагментация ДНК, большой расход одноразового пластика, длительность процедуры, невозможность автоматизации

Выделение на магнитных частицах Преимущества: возможность автоматизации, высокая степень очистки ДНК, подходит для различных объектов выделения (биологических жидкостей, бактериальных культур, очистки после энзиматического лизиса), низкая стоимость и доступность растворов реагентов Недостатки: большие потери при выделении, ухудшение качества выделения при нестандартных образцах

Выделение на колонках Готовая к использованию ДНК Лизис Сорбция Отмывка 1 Отмывка 2 Элюция Преимущества: возможность автоматизации, высокая степень очистки ДНК, низкая фрагментация, возможность концентрации ДНК, разработаны наборы для разных типов образцов Недостатки: высокая стоимость наборов, ухудшение качества выделения при нестандартных образцах

Выделение на колонках Готовая к использованию ДНК Лизис Сорбция Отмывка 1 Отмывка 2 Элюция Преимущества: возможность автоматизации, высокая степень очистки ДНК, низкая фрагментация, возможность концентрации ДНК, разработаны наборы для разных типов образцов Недостатки: высокая стоимость наборов, ухудшение качества выделения при нестандартных образцах
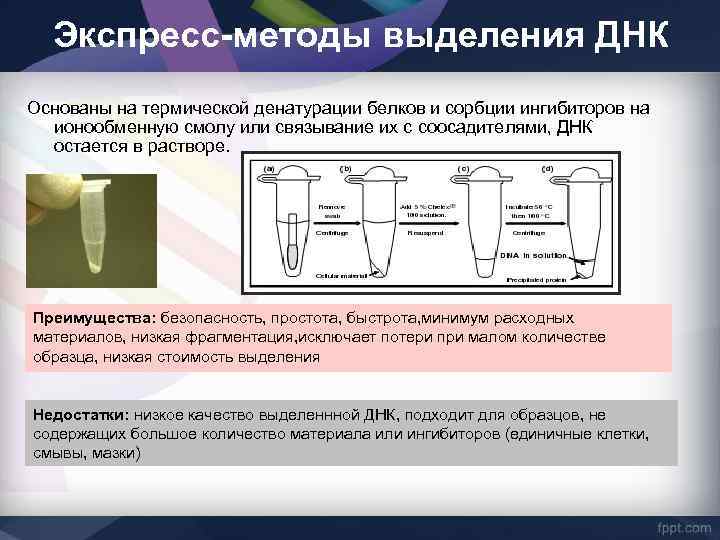
Экспресс-методы выделения ДНК Основаны на термической денатурации белков и сорбции ингибиторов на ионообменную смолу или связывание их с соосадителями, ДНК остается в растворе. Преимущества: безопасность, простота, быстрота, минимум расходных материалов, низкая фрагментация, исключает потери при малом количестве образца, низкая стоимость выделения Недостатки: низкое качество выделеннной ДНК, подходит для образцов, не содержащих большое количество материала или ингибиторов (единичные клетки, смывы, мазки)

СTAB-метод выделения ДНК 1. Лизис клеток 2. Связывание ДНК с цетилтриметиламмонием Br 3. Осаждение комплекса с ДНК центрифугированием 4. Растворение ДНК комплекса при повышении концентрации солей 5. Осаждение ДНК спиртом или на сорбент 6. Промывка ДНК 7. Высушивание 8. Элюция ДНК Преимущества: хорошо подходит для выделения ДНК из растительного материала, содержащего большое количество полисахаридов и полифенольных соединений Недостатки: длительность процедуры, большой расход одноразового пластика, , невозможность автоматизации
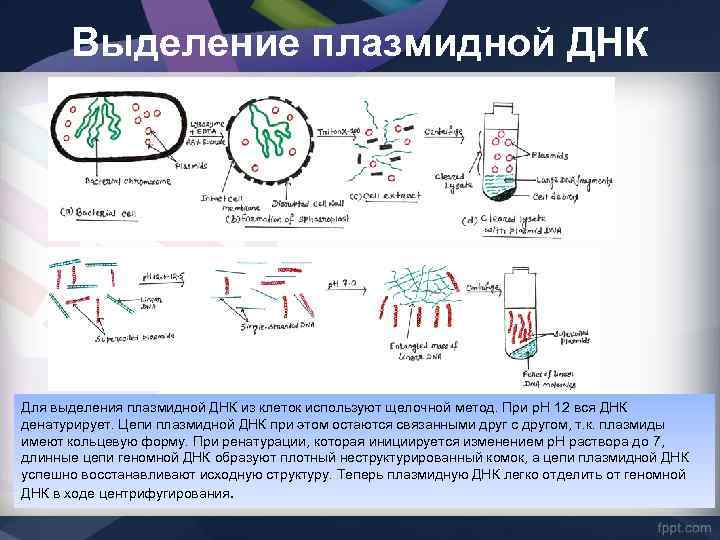
Выделение плазмидной ДНК Для выделения плазмидной ДНК из клеток используют щелочной метод. При p. H 12 вся ДНК денатурирует. Цепи плазмидной ДНК при этом остаются связанными друг с другом, т. к. плазмиды имеют кольцевую форму. При ренатурации, которая инициируется изменением p. H раствора до 7, длинные цепи геномной ДНК образуют плотный неструктурированный комок, а цепи плазмидной ДНК успешно восстанавливают исходную структуру. Теперь плазмидную ДНК легко отделить от геномной ДНК в ходе центрифугирования.

Выделение РНК Важно помнить, что РНК менее стабильна и легко подвергается воздействию РНКаз, поэтому при выделении РНК необходимо соблюдать следущие требования: • Выделение проводят в одноразовых перчатках • Необходимо иметь одноразовый пластик с маркировкой “RNAse Free” • Вода и посуда должна быть проавтоклавирована • Крайне желательно меть оборудование (стеклянную и пластиковую посуду, автоматические пипетки, камеры для электрофореза и т. д. ), предназначенное исключительно для работы с РНК, и выделить в лаборатории место, где не проводится никаких работ с РНКазами • Желательно использовать белковые ингибиторы РНКаз или VO(IV)рибонуклеозидные комплексы
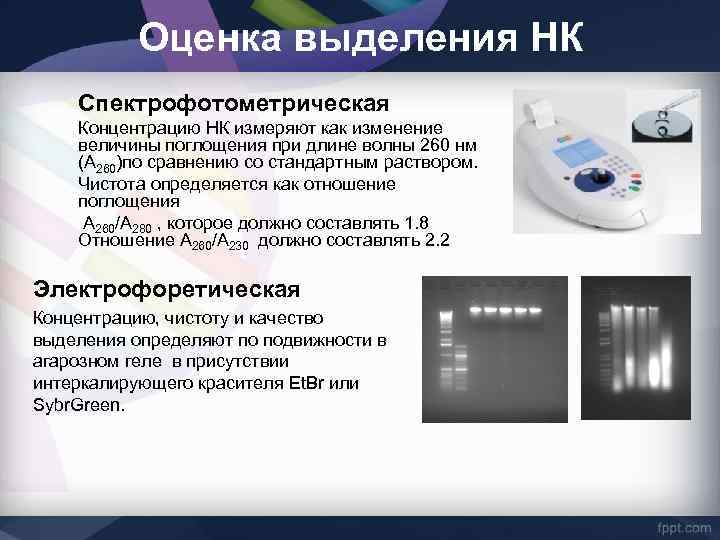
Оценка выделения НК Спектрофотометрическая Концентрацию НК измеряют как изменение величины поглощения при длине волны 260 нм (А 260)по сравнению со стандартным раствором. Чистота определяется как отношение поглощения А 260/А 280 , которое должно составлять 1. 8 Отношение А 260/А 230 должно составлять 2. 2 Электрофоретическая Концентрацию, чистоту и качество выделения определяют по подвижности в агарозном геле в присутствии интеркалирующего красителя Et. Br или Sybr. Green.
Методы анализа ДНК 1. 2. 3. 4. 5. Рестрикционный анализ ПЦР-анализ Гибридизация Секвенирование Фрагментный анализ

Требования к лаборатории Выделение нуклеиновых кислот проводят в специально оборудованной лаборатории на столе, в боксах и ламинарах различного класса безопасности, который зависит от биологического материала и объекта выделения. В лаборатории должны соблюдаться требования биологической безопасности, продумана утилизация биологических и химических отходов. Должны соблюдаться меры против перекрестной контаминации образцов и контаминации продуктами ПЦР-реакции. Лаборатория должна быть оснащена необходимым оборудованием: дозаторы переменного объема, вортекс, центрифуга, термостат, шейкер, вакуумный отсасыватель, холодильник, штативы, одноразовый пластик. Следует соблюдать требования к чистоте помещения и рабочего места.
Методы экстракции и анализа НК1.ppt