Методика химии-продолжение.ppt
- Количество слайдов: 35
 Методика преподавания химии Лекция 2. Искусство подготовки и чтения лекций и проведения семинаров
Методика преподавания химии Лекция 2. Искусство подготовки и чтения лекций и проведения семинаров
 Мастерство лектора
Мастерство лектора
 Основные определения Лекция – это: • последовательное изложение учебного материала • метод и средство формирования научного мышления • активный ввод студента в основные проблемы науки • установка на обращение к учебнику, пособиям, другим источникам Требования к лекции: • научность • доступность • посильная трудность • эмоциональность • наличие обратной связи • связь с другими организационными формами обучения (содержание, сроки проведения, формы)
Основные определения Лекция – это: • последовательное изложение учебного материала • метод и средство формирования научного мышления • активный ввод студента в основные проблемы науки • установка на обращение к учебнику, пособиям, другим источникам Требования к лекции: • научность • доступность • посильная трудность • эмоциональность • наличие обратной связи • связь с другими организационными формами обучения (содержание, сроки проведения, формы)
 Структура и формат лекции Характер изложения материала: объяснительно-описательный проблемно-дискуссионный систематический и системный опережающее изучение материала (связь с будущим учебным материалом) учет подготовленности аудитории к восприятию лекции Оптимизации соотношения материала • информационного ( «готовые знания» ) • стимулирующего познавательную активность (проблемы, задачи) Лекция – способ передачи студенту типа мышления преподавателя!
Структура и формат лекции Характер изложения материала: объяснительно-описательный проблемно-дискуссионный систематический и системный опережающее изучение материала (связь с будущим учебным материалом) учет подготовленности аудитории к восприятию лекции Оптимизации соотношения материала • информационного ( «готовые знания» ) • стимулирующего познавательную активность (проблемы, задачи) Лекция – способ передачи студенту типа мышления преподавателя!
 Техника чтения лекции Внутренняя организация лекции Приветствие Актуализация опорных знаний (в формате «вопрос – ответ» ) Поддержание интереса (иллюстративный материал, постановка проблем, демонстрация «парадоксов» , исторические сведения и т. п. ) Варианты завершающего этапа очередной лекции Оптимальный темп речи лектора: 60 -80 слов в минуту Слишком быстрая (100 -110 слов в мин) и слишком медленная (40 -50 слов в мин) речь лектора затрудняют работу студентов Не диктовать!
Техника чтения лекции Внутренняя организация лекции Приветствие Актуализация опорных знаний (в формате «вопрос – ответ» ) Поддержание интереса (иллюстративный материал, постановка проблем, демонстрация «парадоксов» , исторические сведения и т. п. ) Варианты завершающего этапа очередной лекции Оптимальный темп речи лектора: 60 -80 слов в минуту Слишком быстрая (100 -110 слов в мин) и слишком медленная (40 -50 слов в мин) речь лектора затрудняют работу студентов Не диктовать!
 Оценка качества лекции Критерии оценки отсутствуют Свободное посещение лекций Посещение лекций по выбору Уровень обратной связи «студент – лектор» Количество и качество задаваемых на лекции вопросов
Оценка качества лекции Критерии оценки отсутствуют Свободное посещение лекций Посещение лекций по выбору Уровень обратной связи «студент – лектор» Количество и качество задаваемых на лекции вопросов
 Лекция: технические средства Традиционные ТСО: плакаты, таблицы, портреты лекционные демонстрации (вещества, минералы, изделия) химический демонстрационный эксперимент Новые ТСО: • слайдопроектор и кодоскоп • компьютерный проектор, экран и анимированные презентации • интерактивная доска • компьютерный класс, оборудованный ПК
Лекция: технические средства Традиционные ТСО: плакаты, таблицы, портреты лекционные демонстрации (вещества, минералы, изделия) химический демонстрационный эксперимент Новые ТСО: • слайдопроектор и кодоскоп • компьютерный проектор, экран и анимированные презентации • интерактивная доска • компьютерный класс, оборудованный ПК
 Анимированные презентации Оптимальное сочетание: информативность + наглядность Иллюстрации Видео Анимированные объяснения Далее: примеры анимированных презентаций к лекциям по общей и неорганической химии
Анимированные презентации Оптимальное сочетание: информативность + наглядность Иллюстрации Видео Анимированные объяснения Далее: примеры анимированных презентаций к лекциям по общей и неорганической химии
 Открытие фтора Фтор впервые получен в 1886 г. (А. Муассан, электролиз смеси HF и KF) Анри Муассан (1852 - 1907) Установки для получения фтора
Открытие фтора Фтор впервые получен в 1886 г. (А. Муассан, электролиз смеси HF и KF) Анри Муассан (1852 - 1907) Установки для получения фтора
 Простые вещества: F 2, Cl 2, Br 2, I 2, At 2 Фтор Бром Хлор Иод
Простые вещества: F 2, Cl 2, Br 2, I 2, At 2 Фтор Бром Хлор Иод
 Фтор: распространение в природе Кларк 0, 03% Флюорит (плавиковый шпат) Ca. F 2 Криолит Na 3[Al. F 6] Фторапатит 3 Ca 3(PO 4)2 · Ca. F 2 Криолит Флюорит Фторапатит
Фтор: распространение в природе Кларк 0, 03% Флюорит (плавиковый шпат) Ca. F 2 Криолит Na 3[Al. F 6] Фторапатит 3 Ca 3(PO 4)2 · Ca. F 2 Криолит Флюорит Фторапатит
 Обнаружение соединений бора Na 2 B 4 O 7 + 12 C 2 H 5 OH + 2 H 2 SO 4 = = 4 B(OC 2 H 5)3 + 7 H 2 O + 2 Na. HSO 4 2 B(OC 2 H 5)3 + 18 O 2 = B 2 O 3 + 15 H 2 O + 2 CO 2 Получение и горение борноэтилового эфира. Видео
Обнаружение соединений бора Na 2 B 4 O 7 + 12 C 2 H 5 OH + 2 H 2 SO 4 = = 4 B(OC 2 H 5)3 + 7 H 2 O + 2 Na. HSO 4 2 B(OC 2 H 5)3 + 18 O 2 = B 2 O 3 + 15 H 2 O + 2 CO 2 Получение и горение борноэтилового эфира. Видео
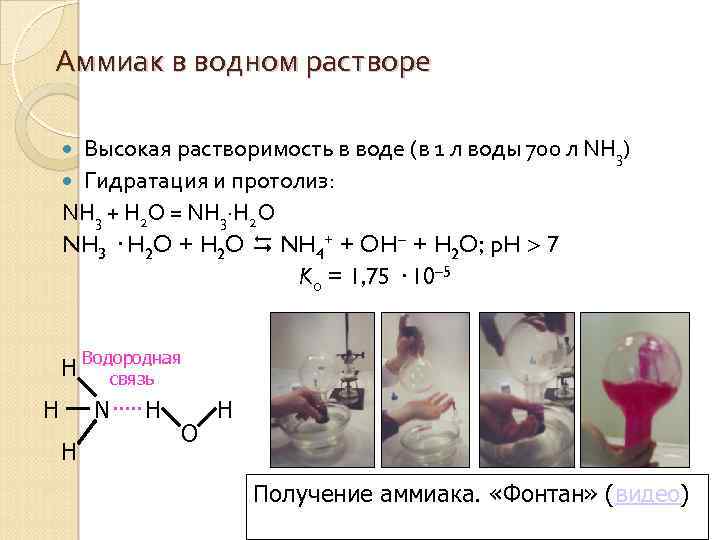 Аммиак в водном растворе Высокая растворимость в воде (в 1 л воды 700 л NH 3) Гидратация и протолиз: NH 3 + H 2 O = NH 3·H 2 O NH 3 · H 2 O + H 2 O NH 4+ + OH + H 2 O; p. H 7 Kо = 1, 75 · 10– 5 H Водородная связь H N H H O H Получение аммиака. «Фонтан» (видео)
Аммиак в водном растворе Высокая растворимость в воде (в 1 л воды 700 л NH 3) Гидратация и протолиз: NH 3 + H 2 O = NH 3·H 2 O NH 3 · H 2 O + H 2 O NH 4+ + OH + H 2 O; p. H 7 Kо = 1, 75 · 10– 5 H Водородная связь H N H H O H Получение аммиака. «Фонтан» (видео)
 2 NO 2(г) N 2 O 4 (г); ΔH° 298 = − 57 к. Дж При повышении температуры (горячая вода) газ внутри правого сосуда приобретает интенсивную бурую окраску (NO 2) – смещение равновесия влево • При охлаждении левого сосуда (стакан с льдом) окраска становится светлее (образование бесцветного N 2 O 4, димеризация) – смещение равновесия вправо •
2 NO 2(г) N 2 O 4 (г); ΔH° 298 = − 57 к. Дж При повышении температуры (горячая вода) газ внутри правого сосуда приобретает интенсивную бурую окраску (NO 2) – смещение равновесия влево • При охлаждении левого сосуда (стакан с льдом) окраска становится светлее (образование бесцветного N 2 O 4, димеризация) – смещение равновесия вправо •
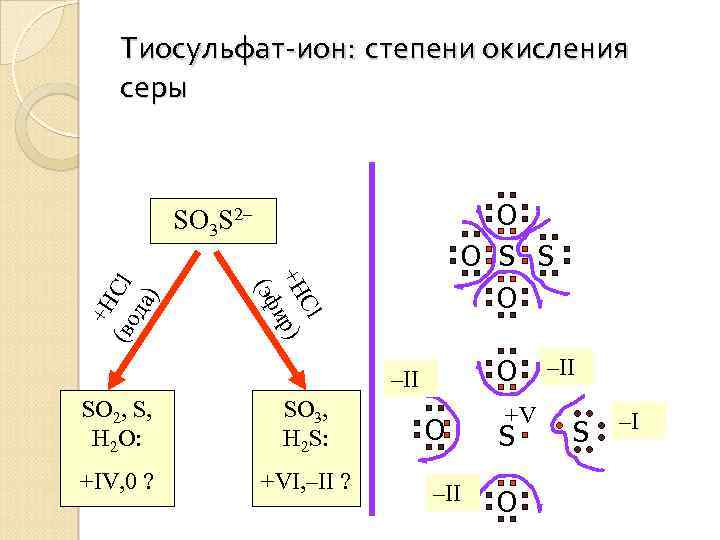 Тиосульфат-ион: степени окисления серы O O S S O Cl +H ир) (эф +H (во Cl да ) SO 3 S 2– O –II SO 2, S, H 2 O: SO 3, H 2 S: +IV, 0 ? +VI, –II ? O –II +V S O –II S –I
Тиосульфат-ион: степени окисления серы O O S S O Cl +H ир) (эф +H (во Cl да ) SO 3 S 2– O –II SO 2, S, H 2 O: SO 3, H 2 S: +IV, 0 ? +VI, –II ? O –II +V S O –II S –I
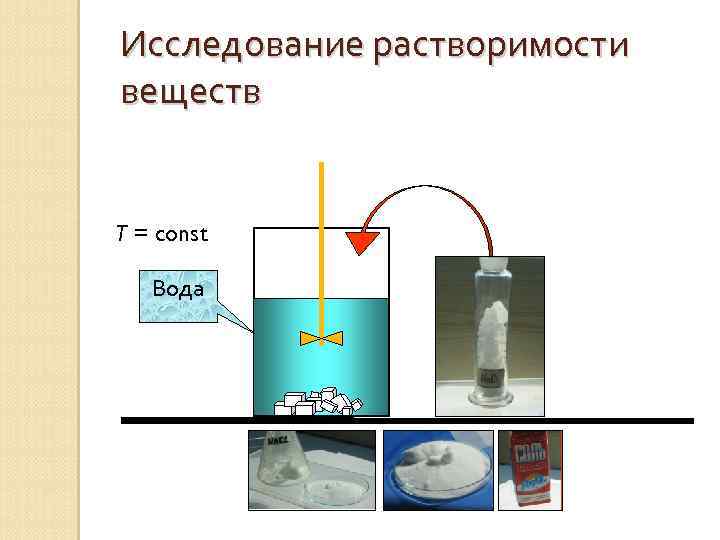 Исследование растворимости веществ T = const Вода
Исследование растворимости веществ T = const Вода
 Диаграмма растворимости График зависимости растворимости от температуры – диаграмма (политерма) растворимости
Диаграмма растворимости График зависимости растворимости от температуры – диаграмма (политерма) растворимости
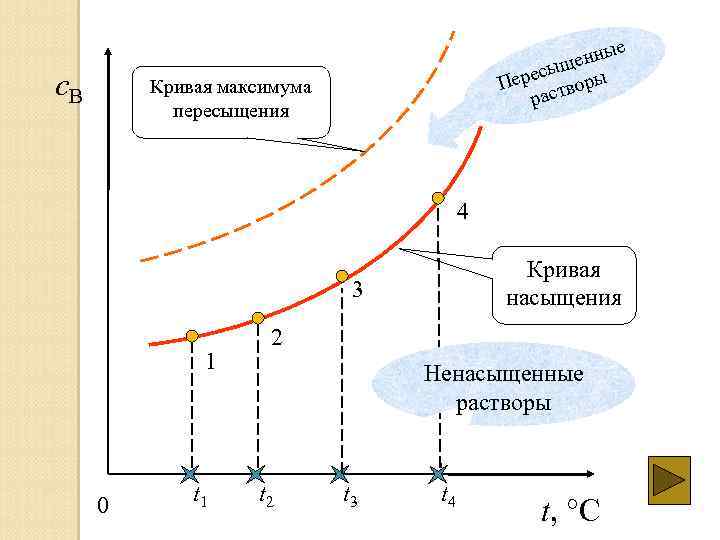 c. B е енны щ ресы оры Пе ств ра Кривая максимума пересыщения 4 Кривая насыщения 3 1 0 t 1 2 Ненасыщенные растворы t 2 t 3 t 4 t, °C
c. B е енны щ ресы оры Пе ств ра Кривая максимума пересыщения 4 Кривая насыщения 3 1 0 t 1 2 Ненасыщенные растворы t 2 t 3 t 4 t, °C
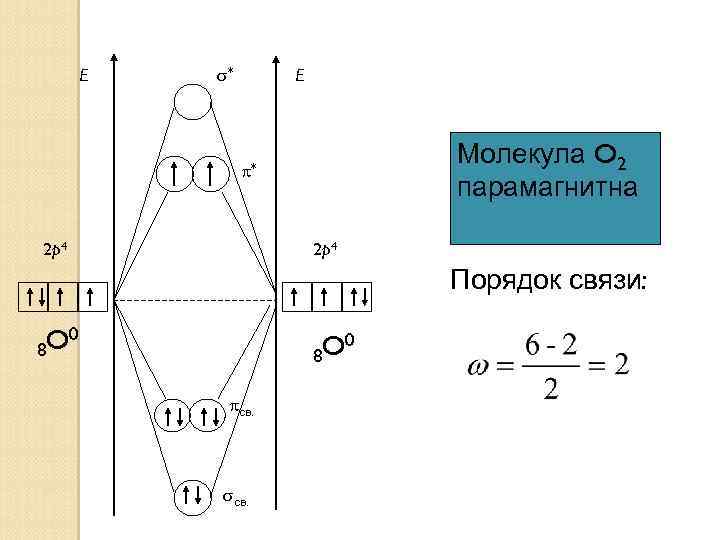 E * E Молекула O 2 парамагнитна * 2 p 4 Порядок связи: 8 O 0 8 св.
E * E Молекула O 2 парамагнитна * 2 p 4 Порядок связи: 8 O 0 8 св.
![Решение задач. 3. Разрушение комплекса [Cu(NH 3)4]2+ + 4 H 3 O+ [Cu(H 2 Решение задач. 3. Разрушение комплекса [Cu(NH 3)4]2+ + 4 H 3 O+ [Cu(H 2](https://present5.com/presentation/3/131736652_437384197.pdf-img/131736652_437384197.pdf-20.jpg) Решение задач. 3. Разрушение комплекса [Cu(NH 3)4]2+ + 4 H 3 O+ [Cu(H 2 O)4]2+ + 4 NH 4+ ; Kc = ? Cu 2+ + 4 NH 3 [Cu(NH 3)4]2+ ; обр = 7, 9· 1012 NH 4+ + 2 H 2 O NH 3·H 2 O + H 3 O+ ; Kк = 5, 75· 10– 10 Kc = [Cu 2+] [NH 4+]4 [NH 3]4 [Cu(NH 3)4 2+] [H 3 O +] 4 [NH 3 ]4 = 1 обр Kк 4 Kc = 1 / (7, 9· 1012· 5, 754· 10– 40 ) = 1, 16· 1020 >> 1 Наблюдается разрушение аммиачного комплекса в кислотной среде (смещение равновесия вправо )
Решение задач. 3. Разрушение комплекса [Cu(NH 3)4]2+ + 4 H 3 O+ [Cu(H 2 O)4]2+ + 4 NH 4+ ; Kc = ? Cu 2+ + 4 NH 3 [Cu(NH 3)4]2+ ; обр = 7, 9· 1012 NH 4+ + 2 H 2 O NH 3·H 2 O + H 3 O+ ; Kк = 5, 75· 10– 10 Kc = [Cu 2+] [NH 4+]4 [NH 3]4 [Cu(NH 3)4 2+] [H 3 O +] 4 [NH 3 ]4 = 1 обр Kк 4 Kc = 1 / (7, 9· 1012· 5, 754· 10– 40 ) = 1, 16· 1020 >> 1 Наблюдается разрушение аммиачного комплекса в кислотной среде (смещение равновесия вправо )
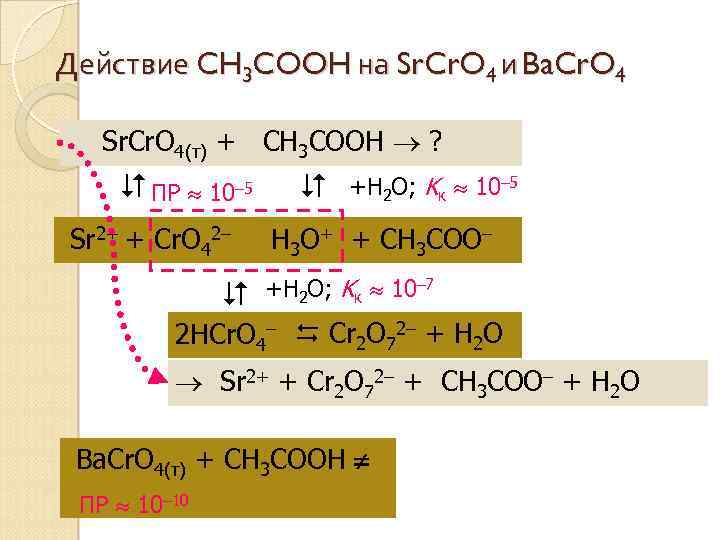 Действие CH 3 COOH на Sr. Cr. O 4 и Ba. Cr. O 4 Sr. Cr. O 4(т) + CH 3 COOH ? ПР 10– 5 Sr 2+ + Cr. O 42– +H 2 O; Kк 10– 5 H 3 O+ + CH 3 COO– +H 2 O; Kк 10– 7 2 HCr. O 4– Cr 2 O 72– + H 2 O Sr 2+ + Cr 2 O 72– + CH 3 COO– + H 2 O Ba. Cr. O 4(т) + CH 3 COOH ПР 10– 10
Действие CH 3 COOH на Sr. Cr. O 4 и Ba. Cr. O 4 Sr. Cr. O 4(т) + CH 3 COOH ? ПР 10– 5 Sr 2+ + Cr. O 42– +H 2 O; Kк 10– 5 H 3 O+ + CH 3 COO– +H 2 O; Kк 10– 7 2 HCr. O 4– Cr 2 O 72– + H 2 O Sr 2+ + Cr 2 O 72– + CH 3 COO– + H 2 O Ba. Cr. O 4(т) + CH 3 COOH ПР 10– 10
 Федеральный центр информационно-образовательных ресурсов (http: //fcior. edu. ru/about. page) Каталог сайта ФЦИОР объединяет более 12 000 электронных учебных модулей, созданных для общего образования, и более 5 000 – ориентированных на профессиональное образование. Для удобства загрузки ресурсов ФЦИОР – региональные представительства (Краснодарский край, Саратовская, Томская, Кемеровская обл. , республика Башкортостан). Технологическая площадка ФЦИОР – программноаппаратный комплекс для надежного хранения образовательных ресурсов, безотказного функционирования сервисов и приложений, рекомендованных к использованию образовательными учреждениями. Открытые образовательные модульные мультимедиа системы (ОМС), объединяющие электронные учебные модули трех типов: информационные, практические и контрольные.
Федеральный центр информационно-образовательных ресурсов (http: //fcior. edu. ru/about. page) Каталог сайта ФЦИОР объединяет более 12 000 электронных учебных модулей, созданных для общего образования, и более 5 000 – ориентированных на профессиональное образование. Для удобства загрузки ресурсов ФЦИОР – региональные представительства (Краснодарский край, Саратовская, Томская, Кемеровская обл. , республика Башкортостан). Технологическая площадка ФЦИОР – программноаппаратный комплекс для надежного хранения образовательных ресурсов, безотказного функционирования сервисов и приложений, рекомендованных к использованию образовательными учреждениями. Открытые образовательные модульные мультимедиа системы (ОМС), объединяющие электронные учебные модули трех типов: информационные, практические и контрольные.
 Портал ФЦИОР
Портал ФЦИОР
 Пример модуля ФЦИОР
Пример модуля ФЦИОР
 Единая коллекция цифровых образовательных ресурсов (http: //school-collection. edu. ru/)
Единая коллекция цифровых образовательных ресурсов (http: //school-collection. edu. ru/)
 Из коллекции «Химия»
Из коллекции «Химия»
 Видеоопыт «Взаимодействие алюминия с бромом» Демонстрация видеоопыта
Видеоопыт «Взаимодействие алюминия с бромом» Демонстрация видеоопыта
 Дополнительно… Обобщение и систематизация лекционного материала (как задания для внеаудиторной СРС) Организация деловых игр и поточных консультаций Понятие о текущем контроле на лекциях Проработка лекций
Дополнительно… Обобщение и систематизация лекционного материала (как задания для внеаудиторной СРС) Организация деловых игр и поточных консультаций Понятие о текущем контроле на лекциях Проработка лекций
 Семинарские занятия Семинар – этап громкой внешней речи Разъяснение правил, формулировок, законов Решение расчетных задач Опробование применения алгоритмических предписаний (примеры) Включение проблемных элементов (примеры)
Семинарские занятия Семинар – этап громкой внешней речи Разъяснение правил, формулировок, законов Решение расчетных задач Опробование применения алгоритмических предписаний (примеры) Включение проблемных элементов (примеры)
 Семинарские занятия • • • Активная форма проведения семинара (примеры) Включение элементов текущего персонального контроля (примеры) Подготовка преподавателя к проведению семинаров
Семинарские занятия • • • Активная форма проведения семинара (примеры) Включение элементов текущего персонального контроля (примеры) Подготовка преподавателя к проведению семинаров
 Структура и формат семинара • Организационный момент: проверка присутствия студентов на семинаре. • Краткое вступительное слово преподавателя (связь с предшествующей темой, целевая установка; практическая значимость выносимых на обсуждение вопросов) • Обсуждение вопросов семинара: 1. выступления по основному вопросу; 2. вопросы выступающим; 3. дискуссия (анализ достоинств и недостатков выступления, дополнения и замечания); 4. заключительное слово основного выступающего в связи с замечаниями и дополнениями; • Заключительное слово преподавателя.
Структура и формат семинара • Организационный момент: проверка присутствия студентов на семинаре. • Краткое вступительное слово преподавателя (связь с предшествующей темой, целевая установка; практическая значимость выносимых на обсуждение вопросов) • Обсуждение вопросов семинара: 1. выступления по основному вопросу; 2. вопросы выступающим; 3. дискуссия (анализ достоинств и недостатков выступления, дополнения и замечания); 4. заключительное слово основного выступающего в связи с замечаниями и дополнениями; • Заключительное слово преподавателя.
 Алгоритм предсказания типа гибридизации и формы частицы • находят центральный атом и определяют число -связей (по числу концевых атомов); • определяют степени окисления атомов в частице; • составляют электронную конфигурацию центрального атома в нужной степени окисления; • изображают схему распределения валентных электронов центрального атома по орбиталям, при этом, вопреки правилу Гунда, максимально «спаривают» электроны; • отмечают орбитали, участвующие в образовании связей с концевыми атомами; • если валентных орбиталей недостаточно, используют орбитали последующих энергетических уровней; • определяют тип гибридизации, учитывая все орбитали, участвующие в образовании связи, а также неподеленные электронные пары; • по типу гибридизации определяют геометрическую конфигурацию химической частицы
Алгоритм предсказания типа гибридизации и формы частицы • находят центральный атом и определяют число -связей (по числу концевых атомов); • определяют степени окисления атомов в частице; • составляют электронную конфигурацию центрального атома в нужной степени окисления; • изображают схему распределения валентных электронов центрального атома по орбиталям, при этом, вопреки правилу Гунда, максимально «спаривают» электроны; • отмечают орбитали, участвующие в образовании связей с концевыми атомами; • если валентных орбиталей недостаточно, используют орбитали последующих энергетических уровней; • определяют тип гибридизации, учитывая все орбитали, участвующие в образовании связи, а также неподеленные электронные пары; • по типу гибридизации определяют геометрическую конфигурацию химической частицы
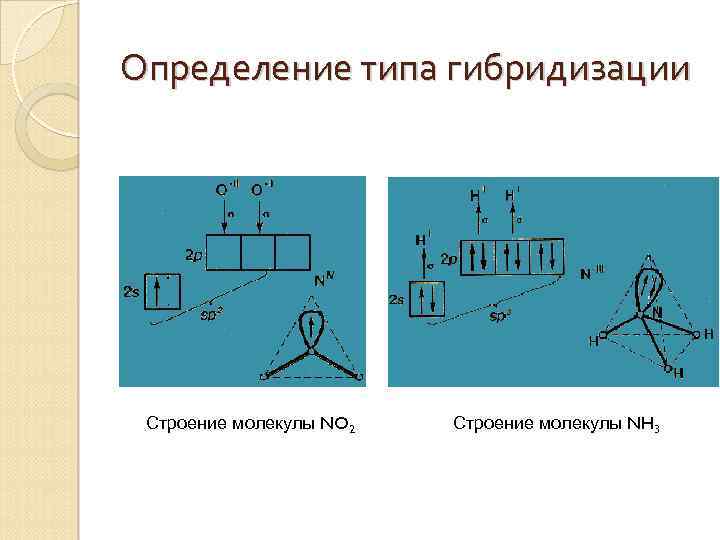 Определение типа гибридизации Строение молекулы NO 2 Строение молекулы NH 3
Определение типа гибридизации Строение молекулы NO 2 Строение молекулы NH 3
 Семинарские занятия Преодоление психологических трудностей В группах, неоднородных по возрасту или уровню подготовки студентов, применяются сочетания • письменной и устной формы работы • коллективного и персонального выступлений
Семинарские занятия Преодоление психологических трудностей В группах, неоднородных по возрасту или уровню подготовки студентов, применяются сочетания • письменной и устной формы работы • коллективного и персонального выступлений
 Основатели Российского химического общества
Основатели Российского химического общества


