8_9Providni_teor_pon.ppt
- Количество слайдов: 30
 МЕТОДИКА ФОРМУВАННЯ ПРОВІДНИХ ТЕОРЕТИЧНИХ УЯВЛЕНЬ В КУРСІ ХІМІЇ СЕРЕДНІХ НАВЧАЛЬНИХ ЗАКЛАДІВ План 1. Формування понять про основні класи неорганічних сполук. 2. Методика формування теоретичної концепції періодичного закону та періодичної системи. 3. Вивчення будови речовини в курсі середньої школи. 4. Теорія дисоціації в шкільному курсі хімії. 5. Основи вчення про напрямок та швидкість хімічного процесу. 6. Окисно-відновні реакції, електроліз.
МЕТОДИКА ФОРМУВАННЯ ПРОВІДНИХ ТЕОРЕТИЧНИХ УЯВЛЕНЬ В КУРСІ ХІМІЇ СЕРЕДНІХ НАВЧАЛЬНИХ ЗАКЛАДІВ План 1. Формування понять про основні класи неорганічних сполук. 2. Методика формування теоретичної концепції періодичного закону та періодичної системи. 3. Вивчення будови речовини в курсі середньої школи. 4. Теорія дисоціації в шкільному курсі хімії. 5. Основи вчення про напрямок та швидкість хімічного процесу. 6. Окисно-відновні реакції, електроліз.
 1. Формування понять про основні класи неорганічних сполук Утворення деяких понять 7 клас Тема “Початкові хімічні поняття” (17 год. ) • Речовина в залежності від кількості сортів атомів, що входять до їх складу поділяються на прості та складні. • Прості речовини на основі фізичних властивостей класифікують на метали на неметали. • Перша поява Періодичної системи як зручний спосіб систематизації елементів. Лінія Цинтля (діагональ B-At) Тема “Прості речовини метали та неметали” (10 год). • Кисень взаємодіє з простими речовинами з утворенням складних речовин: Е + O 2 → Ex. Oy • Утворені сполуки можна класифікувати на оксиди металів та оксиди неметалів.
1. Формування понять про основні класи неорганічних сполук Утворення деяких понять 7 клас Тема “Початкові хімічні поняття” (17 год. ) • Речовина в залежності від кількості сортів атомів, що входять до їх складу поділяються на прості та складні. • Прості речовини на основі фізичних властивостей класифікують на метали на неметали. • Перша поява Періодичної системи як зручний спосіб систематизації елементів. Лінія Цинтля (діагональ B-At) Тема “Прості речовини метали та неметали” (10 год). • Кисень взаємодіє з простими речовинами з утворенням складних речовин: Е + O 2 → Ex. Oy • Утворені сполуки можна класифікувати на оксиди металів та оксиди неметалів.
 1. Формування понять про основні класи неорганічних сполук Розвиток понять 8 клас Тема “Основні класи неорганічних речовин” (25 год) разом з цим продовжується утворенням нових: • Оксиди (розвиток) + номенклатура + класифікація Основні – кислотні – амфотерні – несолетвірні • Кислоти (розвиток) класифікація ОВР) + (без + номенклатура Оксигенвмісні-безоксигенові одноосновнібагатоосновні + поняття “Ряд активності металів” • Солі (розвиток) + номенклатура + класифікація Основні-Середні-кислі + поняття “Реакції обміну” • Основи (розвиток) + номенклатура + класифікація Однокислотні-багатокислотні розчинні-нерозчинні • Амфотерні гідроксиди (утворення) + номенклатура + класифікація
1. Формування понять про основні класи неорганічних сполук Розвиток понять 8 клас Тема “Основні класи неорганічних речовин” (25 год) разом з цим продовжується утворенням нових: • Оксиди (розвиток) + номенклатура + класифікація Основні – кислотні – амфотерні – несолетвірні • Кислоти (розвиток) класифікація ОВР) + (без + номенклатура Оксигенвмісні-безоксигенові одноосновнібагатоосновні + поняття “Ряд активності металів” • Солі (розвиток) + номенклатура + класифікація Основні-Середні-кислі + поняття “Реакції обміну” • Основи (розвиток) + номенклатура + класифікація Однокислотні-багатокислотні розчинні-нерозчинні • Амфотерні гідроксиди (утворення) + номенклатура + класифікація
 1. Формування понять про основні класи неорганічних сполук 8 клас Тема “Основні класи неорганічних речовин” підсумовується розглядом генетичних зв'язки між окремими класами неорганічних речовин. На відповідних уроках: 1. Відбувається узагальнення та систематизація знань про кожний із класів неорганічних сполук. 2. Є можливість закріпити знання про групи речовин у межах кожного класу неорганічних сполук на основі їх складу та властивостей 3. Показується практичне значення про взаємозв'язок речовин для добування сполук та матеріалів Основні “інструменти” – хімічні перетворення, можливе використання експериментальних задач
1. Формування понять про основні класи неорганічних сполук 8 клас Тема “Основні класи неорганічних речовин” підсумовується розглядом генетичних зв'язки між окремими класами неорганічних речовин. На відповідних уроках: 1. Відбувається узагальнення та систематизація знань про кожний із класів неорганічних сполук. 2. Є можливість закріпити знання про групи речовин у межах кожного класу неорганічних сполук на основі їх складу та властивостей 3. Показується практичне значення про взаємозв'язок речовин для добування сполук та матеріалів Основні “інструменти” – хімічні перетворення, можливе використання експериментальних задач
 2. Методика формування теоретичної концепції періодичного закону та періодичної системи. Передумови 7 клас Перша поява періодичної системи як зручний спосіб систематизації елементів. Лінія Цинтля (діагональ B-At) Кілька підходів до формування концепції ПЗ та ПС: • На первинному етапі догматично на основі атомної маси з поверненням після теми “Будова атома”. • Спочатку будова атома, а потім вивчення ПЗ та ПС. + Первинне наступним ознайомлення з інтегрованим вивченням разом із будовою атома
2. Методика формування теоретичної концепції періодичного закону та періодичної системи. Передумови 7 клас Перша поява періодичної системи як зручний спосіб систематизації елементів. Лінія Цинтля (діагональ B-At) Кілька підходів до формування концепції ПЗ та ПС: • На первинному етапі догматично на основі атомної маси з поверненням після теми “Будова атома”. • Спочатку будова атома, а потім вивчення ПЗ та ПС. + Первинне наступним ознайомлення з інтегрованим вивченням разом із будовою атома
 2. Методика формування теоретичної концепції періодичного закону та періодичної системи. Основний матеріал теми складається з двох взаємопов'язаних блоків: • відомостей про періодичну зміну властивостей хімічних елементів (а також їх сполук) від величини заряду ядра(атомної маси); • інформації про будову атомів елементів, структуру їх електронних оболонок. Освітне завдання - виявлення причинно-наслідкових зв'язків між блоками інформації та набуття учнями навиків узагальнення й прогнозування. Виховне завдання - відображення наполегливої праці по пошуку взаємозв'язку між елементами. Наголошення на пріоритеті Д. І. Менделєєва у формулюванні періодичного закону на основі історичних відомостей про інші спроби класифікації (А. Шанкуртуа, Д. Ньюлендс, Ю. Мейер). Розвиваюче завдання - розвиток мислення через проблемні ситуації, підвищенню пізнавального інтересу школярів.
2. Методика формування теоретичної концепції періодичного закону та періодичної системи. Основний матеріал теми складається з двох взаємопов'язаних блоків: • відомостей про періодичну зміну властивостей хімічних елементів (а також їх сполук) від величини заряду ядра(атомної маси); • інформації про будову атомів елементів, структуру їх електронних оболонок. Освітне завдання - виявлення причинно-наслідкових зв'язків між блоками інформації та набуття учнями навиків узагальнення й прогнозування. Виховне завдання - відображення наполегливої праці по пошуку взаємозв'язку між елементами. Наголошення на пріоритеті Д. І. Менделєєва у формулюванні періодичного закону на основі історичних відомостей про інші спроби класифікації (А. Шанкуртуа, Д. Ньюлендс, Ю. Мейер). Розвиваюче завдання - розвиток мислення через проблемні ситуації, підвищенню пізнавального інтересу школярів.
 2. Методика формування теоретичної концепції періодичного закону та періодичної системи. Історичні відомості про спроби класифікації хімічних елементів. Можливо побудувати у вигляді діалогу “питання-відповідь” • Що таке наука? • Як розвивається наука? • Які ознаки лежать в основі класифікації об'єктів суміжних наук (напр. біології)? • Чи відразу у суміжних науках (біологія) була сформована класифікація об'єктів? Після відповіді, вчитель наводить інформацію про спроби класифікації (метали та неметали; тріади Деберейнера (1816 р. ); спіраль Шанкуртуа (1862 р. ); закон октав Ньюлендса (1863 р. ); таблиці Л. Майера (1864 р. )). • Чому спроби до Менделєєва були невдалими? не було враховано важливі властивості сполук елементів та їх взаємозв'язки.
2. Методика формування теоретичної концепції періодичного закону та періодичної системи. Історичні відомості про спроби класифікації хімічних елементів. Можливо побудувати у вигляді діалогу “питання-відповідь” • Що таке наука? • Як розвивається наука? • Які ознаки лежать в основі класифікації об'єктів суміжних наук (напр. біології)? • Чи відразу у суміжних науках (біологія) була сформована класифікація об'єктів? Після відповіді, вчитель наводить інформацію про спроби класифікації (метали та неметали; тріади Деберейнера (1816 р. ); спіраль Шанкуртуа (1862 р. ); закон октав Ньюлендса (1863 р. ); таблиці Л. Майера (1864 р. )). • Чому спроби до Менделєєва були невдалими? не було враховано важливі властивості сполук елементів та їх взаємозв'язки.
 2. Методика формування теоретичної концепції періодичного закону та періодичної системи. Поняття про лужні, інертні елементи, галогени. Періодичний закон та періодична система хімічних елементів Д. І. Менделєєва. Орієнтовний алгоритм Показати подібність хімічних властивостей деяких елементів, що об'єднані у “групи”. Показати однаковий характер зміни хімічних властивостей елементів в межах рядків періодичної системи. Сформулювати періодичний закон на основі періодичної системи. Будова атома: ядро і електронна оболонка. Склад атомних ядер (протони і нейтрони). Протонне число. Нуклонне число. Ізотопи (стабільні та радіоактивні). Будова електронних оболонок атомів хiмічних елементів. Поняття про радіус атома. Стан електронів у атомі. Енергетичні рівні та підрівні. Допустимим є використання “застарілої” планетарної моделі як такої що спирається на вже відомі факти про будову Сонячної системи. Проте можливим є використання альтернативних “описів” – багатоквартирного будинку та ін.
2. Методика формування теоретичної концепції періодичного закону та періодичної системи. Поняття про лужні, інертні елементи, галогени. Періодичний закон та періодична система хімічних елементів Д. І. Менделєєва. Орієнтовний алгоритм Показати подібність хімічних властивостей деяких елементів, що об'єднані у “групи”. Показати однаковий характер зміни хімічних властивостей елементів в межах рядків періодичної системи. Сформулювати періодичний закон на основі періодичної системи. Будова атома: ядро і електронна оболонка. Склад атомних ядер (протони і нейтрони). Протонне число. Нуклонне число. Ізотопи (стабільні та радіоактивні). Будова електронних оболонок атомів хiмічних елементів. Поняття про радіус атома. Стан електронів у атомі. Енергетичні рівні та підрівні. Допустимим є використання “застарілої” планетарної моделі як такої що спирається на вже відомі факти про будову Сонячної системи. Проте можливим є використання альтернативних “описів” – багатоквартирного будинку та ін.
 2. Методика формування теоретичної концепції періодичного закону та періодичної системи. При висвітлені відповідних питань обов'язковим є наголошення на рівності заряду ядра та порядкового номеру. Поняття ізотопів слід відобразити на прикладі елементів з нецілочисельними атомними масами. (Cl, Mg, уникайте O, Al, P (в природі моноізтопні, із дефектом маси) !!!). Поняття підрівнів лише оглядово, без будови орбіталей.
2. Методика формування теоретичної концепції періодичного закону та періодичної системи. При висвітлені відповідних питань обов'язковим є наголошення на рівності заряду ядра та порядкового номеру. Поняття ізотопів слід відобразити на прикладі елементів з нецілочисельними атомними масами. (Cl, Mg, уникайте O, Al, P (в природі моноізтопні, із дефектом маси) !!!). Поняття підрівнів лише оглядово, без будови орбіталей.
 2. Методика формування теоретичної концепції періодичного закону та періодичної системи. Сучасне формулювання періодичного закону. Структура періодичної системи. Взаємозв’язок між розмiщенням елементів у перiодичній системі та властивостями хімічних елементів, простих речовин, сполук елементів з Гідрогеном та Оксигеном. Характеристика хiмічних елементів малих періодів за їх місцем у періодичній системі та будовою атома. На основі залежності: “заряд ядра = порядковому номеру елементу” (Закон Мозлі, історичні відомості), пояснюємо існування “перестановок” в ПС, потім подаємо сучасне формулювання ПЗ. Опис структури проводимо паралельно з написанням електронної конфігурації деяких елементів – формулюємо визначення група та період з точки зору електронної конфігурації. Можливе ознайомлення з іншими способами зображення ПС (розгорнута або довга (18 груп), наддовга (кожен період-1 рядок). Формули оксидів і “гідридів” виводимо на основі електронної будови атомів
2. Методика формування теоретичної концепції періодичного закону та періодичної системи. Сучасне формулювання періодичного закону. Структура періодичної системи. Взаємозв’язок між розмiщенням елементів у перiодичній системі та властивостями хімічних елементів, простих речовин, сполук елементів з Гідрогеном та Оксигеном. Характеристика хiмічних елементів малих періодів за їх місцем у періодичній системі та будовою атома. На основі залежності: “заряд ядра = порядковому номеру елементу” (Закон Мозлі, історичні відомості), пояснюємо існування “перестановок” в ПС, потім подаємо сучасне формулювання ПЗ. Опис структури проводимо паралельно з написанням електронної конфігурації деяких елементів – формулюємо визначення група та період з точки зору електронної конфігурації. Можливе ознайомлення з іншими способами зображення ПС (розгорнута або довга (18 груп), наддовга (кожен період-1 рядок). Формули оксидів і “гідридів” виводимо на основі електронної будови атомів
 2. Методика формування теоретичної концепції періодичного закону та періодичної системи. Значення періодичного закону. Життя і наукова діяльність Д. І. Менделєєва. Наукове значення ― ПЗ є надійним засобом для пояснення явищ, у яких беруть участь хімічні елементи, і для передбачення нових фактів. Світоглядне значення ― всі елементи як подібні, так і відмінні за властивостями, містяться в єдиній системі, де їх властивості змінюються закономірно, шляхом переходу кількісних змін (заряд ядра) у якісні (властивості елементів). 1834 – 1907 р. р. Відкриття періодичного закону Фізикохімічні дослідження (теорія розчинів, критична температура) Рецепт бездимного пороху Міф про рецепт 40º горілки Робота в “Палате мер и весов” Дослідження в галузі нафтопереробки Мінералогічні колекції Н. А. Ярошенко. Д. І. Менделєєв. 1886 р. Летопись жизни и деятельности Д. И. Менделеева. / Ред. О. В. Сторонкин. Ленинград: «Наука» . ― 1984. Максимов І. Таблиця хімічних елементів Д. І. Менделєєва: оптимізація елементів/І. Максимов // Біологія і хімія в школі, 2006, № 2. -С. 22 -24 Максимов О. С. Внесок Д. І. Менделєєва в розвиток молекулярно-кінетичної теорії газів /О. С. Максимов, К. Ф. Янків // Біологія і хімія в школі, 2007, № 1. -С. 49 -51
2. Методика формування теоретичної концепції періодичного закону та періодичної системи. Значення періодичного закону. Життя і наукова діяльність Д. І. Менделєєва. Наукове значення ― ПЗ є надійним засобом для пояснення явищ, у яких беруть участь хімічні елементи, і для передбачення нових фактів. Світоглядне значення ― всі елементи як подібні, так і відмінні за властивостями, містяться в єдиній системі, де їх властивості змінюються закономірно, шляхом переходу кількісних змін (заряд ядра) у якісні (властивості елементів). 1834 – 1907 р. р. Відкриття періодичного закону Фізикохімічні дослідження (теорія розчинів, критична температура) Рецепт бездимного пороху Міф про рецепт 40º горілки Робота в “Палате мер и весов” Дослідження в галузі нафтопереробки Мінералогічні колекції Н. А. Ярошенко. Д. І. Менделєєв. 1886 р. Летопись жизни и деятельности Д. И. Менделеева. / Ред. О. В. Сторонкин. Ленинград: «Наука» . ― 1984. Максимов І. Таблиця хімічних елементів Д. І. Менделєєва: оптимізація елементів/І. Максимов // Біологія і хімія в школі, 2006, № 2. -С. 22 -24 Максимов О. С. Внесок Д. І. Менделєєва в розвиток молекулярно-кінетичної теорії газів /О. С. Максимов, К. Ф. Янків // Біологія і хімія в школі, 2007, № 1. -С. 49 -51
 3. Вивчення будови речовини в курсі середньої школи. Вивчення будови речовини в шкільному найбільших змін впродовж останніх років. курсі зазнало 8 клас Тема 4. Хімічний зв’язок і будова речовини. (10 год) Освітня мета - засвоєння понять про електронну природу та види хімічного зв'язку, типи кристалічної ґратки. Виховна мета – формування уявлень про матеріальну природу речовин. Вивчення будови речовини допомагає пояснити учням суперечливість внутрішньої будови атомів та молекул, показати як вивчення будови речовини стимулювало розвиток науки. Розвиваюча мета – розвиток мислення учнів, розширення навичок співставлення та порівняння.
3. Вивчення будови речовини в курсі середньої школи. Вивчення будови речовини в шкільному найбільших змін впродовж останніх років. курсі зазнало 8 клас Тема 4. Хімічний зв’язок і будова речовини. (10 год) Освітня мета - засвоєння понять про електронну природу та види хімічного зв'язку, типи кристалічної ґратки. Виховна мета – формування уявлень про матеріальну природу речовин. Вивчення будови речовини допомагає пояснити учням суперечливість внутрішньої будови атомів та молекул, показати як вивчення будови речовини стимулювало розвиток науки. Розвиваюча мета – розвиток мислення учнів, розширення навичок співставлення та порівняння.
 3. Вивчення будови речовини в курсі середньої школи. Опорні поняття для вивчення теми є Будова атома: склад атомних ядер, ізотопи, стан електронних оболонок атомів, порядок заповнення орбіталей. Формуються поняття Хімічний зв’язок: зона перекривання орбіталей, електронегативність, ковалентний (полярний, неполярний), іонний, металічний, водневий, сили міжмолекулярної взаємодії. Умови засвоєння: • виконання принципу систематичності; • широке використання наочностей; • проблемний підхід.
3. Вивчення будови речовини в курсі середньої школи. Опорні поняття для вивчення теми є Будова атома: склад атомних ядер, ізотопи, стан електронних оболонок атомів, порядок заповнення орбіталей. Формуються поняття Хімічний зв’язок: зона перекривання орбіталей, електронегативність, ковалентний (полярний, неполярний), іонний, металічний, водневий, сили міжмолекулярної взаємодії. Умови засвоєння: • виконання принципу систематичності; • широке використання наочностей; • проблемний підхід.
 4. Теорія дисоціації в шкільному курсі хімії Окремої теми немає у рівні стандарту, реалізується впродовж кількох уроків як підтема 9 клас Тема “Розчини” 15 год. Освітня мета: сформувати поняття про сутність, механізми, умови процесу дисоціації, речовини електроліти, поведінку іонів в розчинах та реакції між ними. Виховна мета: розвиток уявлень про навколишній світ, підтвердження на конкретних прикладах найважливіших філософських категорій. Розвиваюча мета: поглиблення понять про речовину та хімічну реакцію, створення теоретичної бази для подальшого вивчення хімії
4. Теорія дисоціації в шкільному курсі хімії Окремої теми немає у рівні стандарту, реалізується впродовж кількох уроків як підтема 9 клас Тема “Розчини” 15 год. Освітня мета: сформувати поняття про сутність, механізми, умови процесу дисоціації, речовини електроліти, поведінку іонів в розчинах та реакції між ними. Виховна мета: розвиток уявлень про навколишній світ, підтвердження на конкретних прикладах найважливіших філософських категорій. Розвиваюча мета: поглиблення понять про речовину та хімічну реакцію, створення теоретичної бази для подальшого вивчення хімії
 4. Теорія дисоціації в шкільному курсі хімії Профільний рівень 9 клас 4 год. на тиждень Тема 2. Електролітична дисоціація (20 год. ) Електролітична дисоціація кислот, лугів, солей. Електроліти і неелектроліти. Механізм дисоціації речовин з йонним і полярним ковалентними зв’язками. Поняття про ступінчасту дисоціацію. Ступінь дисоціації. Сильні й слабкі електроліти. Дисоціація електролітів у водних розчинах. Хімічні властивості кислот, основ, амфотерних гідроксидів, солей у світлі уявлень про електролітичну дисоціацію та окисно-відновні процеси. Реакції обміну між розчинами електролітів. Йонні рівняння. Дисоціація води. Поняття про водневий показник — р. Н реакції середовища. Гідроліз солей.
4. Теорія дисоціації в шкільному курсі хімії Профільний рівень 9 клас 4 год. на тиждень Тема 2. Електролітична дисоціація (20 год. ) Електролітична дисоціація кислот, лугів, солей. Електроліти і неелектроліти. Механізм дисоціації речовин з йонним і полярним ковалентними зв’язками. Поняття про ступінчасту дисоціацію. Ступінь дисоціації. Сильні й слабкі електроліти. Дисоціація електролітів у водних розчинах. Хімічні властивості кислот, основ, амфотерних гідроксидів, солей у світлі уявлень про електролітичну дисоціацію та окисно-відновні процеси. Реакції обміну між розчинами електролітів. Йонні рівняння. Дисоціація води. Поняття про водневий показник — р. Н реакції середовища. Гідроліз солей.
 4. Теорія дисоціації в шкільному курсі хімії Основні поняття “теми” Об'єкти: будова електролітів, класифікація електролітів, особливості дисоціації, іони в розчині, властивості іонів; Процеси: сутність процесу дисоціації, умови дисоціації, механізм дисоціації, реакції іонів в розчинах (обмін, гідроліз, ОВР). Послідовність вивчення: • від практики до теорії електролітів; • стан іонів у розчинах (розширення уявлень про речовину); • розвиток поняття хімічна реакція: реакція обміну проходить в напрямку зв'язування іонів; гідроліз як частинний випадок реакції обміну; введення поняття окисно-відновна реакція.
4. Теорія дисоціації в шкільному курсі хімії Основні поняття “теми” Об'єкти: будова електролітів, класифікація електролітів, особливості дисоціації, іони в розчині, властивості іонів; Процеси: сутність процесу дисоціації, умови дисоціації, механізм дисоціації, реакції іонів в розчинах (обмін, гідроліз, ОВР). Послідовність вивчення: • від практики до теорії електролітів; • стан іонів у розчинах (розширення уявлень про речовину); • розвиток поняття хімічна реакція: реакція обміну проходить в напрямку зв'язування іонів; гідроліз як частинний випадок реакції обміну; введення поняття окисно-відновна реакція.
 4. Теорія дисоціації в шкільному курсі хімії Основні проблеми для розв'язання; • Чому електроліти проводять ел. струм, а неелектроліти – ні (міжпредметні зв'язки з фізикою); • Чому іонні та полярні сполуки дисоціюють на іони, а неполярні ні (внутрішньокурсові зв'язки з теорією будови); • Що впливає на дисоціацію – розчинник чи струм; • Чи є відмінності між атомом чи іоном; Важливо Розділення понять валентність – ступінь окиснення – заряд іона Широке використання засобів наочності, лабораторного експерименту
4. Теорія дисоціації в шкільному курсі хімії Основні проблеми для розв'язання; • Чому електроліти проводять ел. струм, а неелектроліти – ні (міжпредметні зв'язки з фізикою); • Чому іонні та полярні сполуки дисоціюють на іони, а неполярні ні (внутрішньокурсові зв'язки з теорією будови); • Що впливає на дисоціацію – розчинник чи струм; • Чи є відмінності між атомом чи іоном; Важливо Розділення понять валентність – ступінь окиснення – заряд іона Широке використання засобів наочності, лабораторного експерименту
 4. Теорія дисоціації в шкільному курсі хімії Гідроліз Поняття вилучене з вимог рівня стандарту проте є в програмах профільних та спеціалізованих класів. Опорними поняттями для вивчення є реакція іонного обміну, оборотність реакції, хімічна рівновага та способи її зміщення, сильні та слабкі електроліти. Велика кількість опорних понять та їх складність і є причиною для вилучення поняття гідроліз із рівня стандарту. • На початку актуалізуємо знання учнів про дію кислот та лугів на індикатори. • Проблемне вивчення через експеримент: дія розчинів солей на індикатори Пояснення вчителя Солі при розчинені дисоціюють: Na 2 CO 3 ↔ 2 Na+ + CO 32– Також самочинно дисоціює вода: H 2 O ↔ H+ + OH– Потім відбувається реакція: CO 32– + H 2 O ↔ HCO 3– + OH– БО Взаємодія іонів натрію з водою неможлива… • Наступна проблемна ситуація: чи можливий повний гідроліз і за яких умов… Важливим є звернути увагу на оборотність реакції та обговорити способи змішення рівноваги
4. Теорія дисоціації в шкільному курсі хімії Гідроліз Поняття вилучене з вимог рівня стандарту проте є в програмах профільних та спеціалізованих класів. Опорними поняттями для вивчення є реакція іонного обміну, оборотність реакції, хімічна рівновага та способи її зміщення, сильні та слабкі електроліти. Велика кількість опорних понять та їх складність і є причиною для вилучення поняття гідроліз із рівня стандарту. • На початку актуалізуємо знання учнів про дію кислот та лугів на індикатори. • Проблемне вивчення через експеримент: дія розчинів солей на індикатори Пояснення вчителя Солі при розчинені дисоціюють: Na 2 CO 3 ↔ 2 Na+ + CO 32– Також самочинно дисоціює вода: H 2 O ↔ H+ + OH– Потім відбувається реакція: CO 32– + H 2 O ↔ HCO 3– + OH– БО Взаємодія іонів натрію з водою неможлива… • Наступна проблемна ситуація: чи можливий повний гідроліз і за яких умов… Важливим є звернути увагу на оборотність реакції та обговорити способи змішення рівноваги
 5. Основи вчення про напрямок та швидкість хімічного процесу. Стандартний рівень 9 клас 2 год. на тиждень Тема 2. Хімічні реакції (9 год) Класифікація хімічних реакцій за різними ознаками. Реакції сполучення, розкладу, заміщення, обміну. Оборотні й необоротні реакції. Окисно-відновні реакції, їхнє значення. Процеси окиснення, відновлення, окисники, відновники. Складання рівнянь найпростіших окисно-відновних реакцій, добір коефіцієнтів. Тепловий ефект реакції. Екзотермічні та ендотермічні реакції. Термохімічне рівняння. Швидкість хімічної реакції, залежність швидкості реакції від різних чинників. Демонстрації: 5. Залежність швидкості реакції металів (цинк, магній, залізо) з хлоридною кислотою від природи металу та концентрації кислоти. Лабораторні досліди: 5. Вплив площі поверхні контакту реагентів, концентрації й температури на швидкість реакції цинку з хлоридною кислотою. Складність теми та обсяг матеріалу вимагають особливого підходу до викладання. Зокрема необхідні засоби концентрування інформації: демонстрації опорні схеми О. О. Шишкіна. Використання нових педагогічних технологій у процесі підготовки вчителів хімії http: //www. intellect-invest. org. ua/pedagog_editions_e-magazine_pedagogical_science_arhiv_pn_n 1_2008_st_22 /
5. Основи вчення про напрямок та швидкість хімічного процесу. Стандартний рівень 9 клас 2 год. на тиждень Тема 2. Хімічні реакції (9 год) Класифікація хімічних реакцій за різними ознаками. Реакції сполучення, розкладу, заміщення, обміну. Оборотні й необоротні реакції. Окисно-відновні реакції, їхнє значення. Процеси окиснення, відновлення, окисники, відновники. Складання рівнянь найпростіших окисно-відновних реакцій, добір коефіцієнтів. Тепловий ефект реакції. Екзотермічні та ендотермічні реакції. Термохімічне рівняння. Швидкість хімічної реакції, залежність швидкості реакції від різних чинників. Демонстрації: 5. Залежність швидкості реакції металів (цинк, магній, залізо) з хлоридною кислотою від природи металу та концентрації кислоти. Лабораторні досліди: 5. Вплив площі поверхні контакту реагентів, концентрації й температури на швидкість реакції цинку з хлоридною кислотою. Складність теми та обсяг матеріалу вимагають особливого підходу до викладання. Зокрема необхідні засоби концентрування інформації: демонстрації опорні схеми О. О. Шишкіна. Використання нових педагогічних технологій у процесі підготовки вчителів хімії http: //www. intellect-invest. org. ua/pedagog_editions_e-magazine_pedagogical_science_arhiv_pn_n 1_2008_st_22 /
 5. Основи вчення про напрямок та швидкість хімічного процесу. Профільний рівень 9 клас 4 год. на тиждень Тема 4. Хімічні реакції та закономірності їх перебігу (20 год. ) Узагальнення знань про основні типи хімічних реакцій. Окисно-відновні реакції. Найважливіші окисники і відновники. Поняття про енергетику хімічних реакцій. Закон збереження енергії, його значення для хімічних процесів. Перетворення енергії під час хімічних реакцій. Внутрішня енергія і тепловий ефект, поняття про ентальпію. Екзо- та ендотермічні реакції. Термохімічні рівняння. Закон Гесса. Розрахунки за термохімічними рівняннями. Поняття про хімічну кінетику. Швидкість хімічної реакції. Залежність швидкості реакції від концентрації реагуючих речовин. Закон діючих мас. Залежність швидкості реакції від температури і природи реагуючих речовин. Поняття про енергетичний бар’єр, активований комплекс, енергію активації. Залежність швидкості реакції від наявності каталізатора і від площі поверхні зіткнення реагуючих речовин. Поняття про ланцюгові реакції. Каталізатори та інгібітори. Теорія проміжних сполук. Загальні відомості про гомогенний і гетерогенний каталіз. Хімічна рівновага. Оборотні та необоротні реакції. Константа хімічної рівноваги. Порушення рівноваги внаслідок зміни концентрації будь-якої з речовин, що беруть участь в реакції, тиску і температури. Принцип Ле Шательє.
5. Основи вчення про напрямок та швидкість хімічного процесу. Профільний рівень 9 клас 4 год. на тиждень Тема 4. Хімічні реакції та закономірності їх перебігу (20 год. ) Узагальнення знань про основні типи хімічних реакцій. Окисно-відновні реакції. Найважливіші окисники і відновники. Поняття про енергетику хімічних реакцій. Закон збереження енергії, його значення для хімічних процесів. Перетворення енергії під час хімічних реакцій. Внутрішня енергія і тепловий ефект, поняття про ентальпію. Екзо- та ендотермічні реакції. Термохімічні рівняння. Закон Гесса. Розрахунки за термохімічними рівняннями. Поняття про хімічну кінетику. Швидкість хімічної реакції. Залежність швидкості реакції від концентрації реагуючих речовин. Закон діючих мас. Залежність швидкості реакції від температури і природи реагуючих речовин. Поняття про енергетичний бар’єр, активований комплекс, енергію активації. Залежність швидкості реакції від наявності каталізатора і від площі поверхні зіткнення реагуючих речовин. Поняття про ланцюгові реакції. Каталізатори та інгібітори. Теорія проміжних сполук. Загальні відомості про гомогенний і гетерогенний каталіз. Хімічна рівновага. Оборотні та необоротні реакції. Константа хімічної рівноваги. Порушення рівноваги внаслідок зміни концентрації будь-якої з речовин, що беруть участь в реакції, тиску і температури. Принцип Ле Шательє.
 5. Основи вчення про напрямок та швидкість хімічного процесу. Демонстрації: 9. Приклади екзо- та ендотермічних реакцій. 10. Проведення реакцій з різним тепловим ефектом (горіння магнію, утворення купрум(ІІ) оксиду тощо). 11. Досліди, що демонструють залежність швидкості хімічних реакцій: від природи реагуючих речовин (взаємодія цинку з хлоридною та оцтовою кислотами); 12. … від розмірів поверхні зіткнення (взаємодія однакової маси шматочків і порошку мармуру з однаковим об’ємом хлоридної кислоти з однаковою масовою часткою НCl); 13. … від концентрації і температури (взаємодія купрум(ІІ) оксиду із сульфатною кислотою різної концентрації і за різних температур). 14. Взаємодія алюмінієвого (цинкового) пилу з йодом під дією води. 15. Вивчення оборотності хімічних реакцій (Fe. Cl 3 i KSCN). Лабораторні досліди: 8. Дослідження впливу різних факторів на швидкість хімічних реакцій. 9. Оборотні та необоротні реакції. ? ? клас ? год. на тиждень Узагальнювальне повторення найважливіших питань курсу хімії Тема 4. Хімічні реакції (12 год. )
5. Основи вчення про напрямок та швидкість хімічного процесу. Демонстрації: 9. Приклади екзо- та ендотермічних реакцій. 10. Проведення реакцій з різним тепловим ефектом (горіння магнію, утворення купрум(ІІ) оксиду тощо). 11. Досліди, що демонструють залежність швидкості хімічних реакцій: від природи реагуючих речовин (взаємодія цинку з хлоридною та оцтовою кислотами); 12. … від розмірів поверхні зіткнення (взаємодія однакової маси шматочків і порошку мармуру з однаковим об’ємом хлоридної кислоти з однаковою масовою часткою НCl); 13. … від концентрації і температури (взаємодія купрум(ІІ) оксиду із сульфатною кислотою різної концентрації і за різних температур). 14. Взаємодія алюмінієвого (цинкового) пилу з йодом під дією води. 15. Вивчення оборотності хімічних реакцій (Fe. Cl 3 i KSCN). Лабораторні досліди: 8. Дослідження впливу різних факторів на швидкість хімічних реакцій. 9. Оборотні та необоротні реакції. ? ? клас ? год. на тиждень Узагальнювальне повторення найважливіших питань курсу хімії Тема 4. Хімічні реакції (12 год. )
 5. Основи вчення про напрямок та швидкість хімічного процесу. Поглиблений рівень 11 клас 6 год. на тиждень Органічна хімія (65 год. ) + Загальна хімія (190 год) + 20 год. резерв Загальна хімія Тема 3. Хімічні реакції (12 год. ) Суть хімічних реакцій. Енергетика хімічних реакцій: поняття про внутрішню енергію речовин, енергію активізації, екзо- й ендотермічні процеси, тепловий ефект реакції, ентальпію. Обчислення за термохімічними рівняннями реакцій. Механізми хімічних реакцій: радикального заміщення (ланцюгові реакції) та електрофільного приєднання (йонні реакції). Швидкість хімічної реакції, обчислення середньої швидкості. Гомогенні та гетерогенні системи. Чинники, що впливають на швидкість реакції: природа реагентів, стан і величина поверхні твердого реагенту, концентрація реагуючих речовин, температура, каталізатор Закон діючих мас. Механізм каталітичної дії. Каталізатори й інгібітори. Каталіз у живих організмах і в хімічній промисловості. Оборотні та необоротні реакції. Хімічна рівновага. Константа рівноваги. Умови зміщення хімічної рівноваги: тиск, температура, концентрація реагуючих речовин. Принцип Ле Шательє. Його значення в керуванні хімічними процесами. Класифікація хімічних реакцій у неорганічній та органічній хімії, її критерії. Окисно -відновні реакції. Електроліз водних розчинів солей. Електроліз як один із способів добування активних металів. Значення хімічних реакцій у хімічній промисловості, живих організмах, довкіллі.
5. Основи вчення про напрямок та швидкість хімічного процесу. Поглиблений рівень 11 клас 6 год. на тиждень Органічна хімія (65 год. ) + Загальна хімія (190 год) + 20 год. резерв Загальна хімія Тема 3. Хімічні реакції (12 год. ) Суть хімічних реакцій. Енергетика хімічних реакцій: поняття про внутрішню енергію речовин, енергію активізації, екзо- й ендотермічні процеси, тепловий ефект реакції, ентальпію. Обчислення за термохімічними рівняннями реакцій. Механізми хімічних реакцій: радикального заміщення (ланцюгові реакції) та електрофільного приєднання (йонні реакції). Швидкість хімічної реакції, обчислення середньої швидкості. Гомогенні та гетерогенні системи. Чинники, що впливають на швидкість реакції: природа реагентів, стан і величина поверхні твердого реагенту, концентрація реагуючих речовин, температура, каталізатор Закон діючих мас. Механізм каталітичної дії. Каталізатори й інгібітори. Каталіз у живих організмах і в хімічній промисловості. Оборотні та необоротні реакції. Хімічна рівновага. Константа рівноваги. Умови зміщення хімічної рівноваги: тиск, температура, концентрація реагуючих речовин. Принцип Ле Шательє. Його значення в керуванні хімічними процесами. Класифікація хімічних реакцій у неорганічній та органічній хімії, її критерії. Окисно -відновні реакції. Електроліз водних розчинів солей. Електроліз як один із способів добування активних металів. Значення хімічних реакцій у хімічній промисловості, живих організмах, довкіллі.
 5. Основи вчення про напрямок та швидкість хімічного процесу. Демонстрації. 6. Приклади екзо- та ендотермічних реакцій. 7. Досліди, що підтверджують залежність швидкості реакції від концентрації реагуючих речовин і температури. 8. Розкладання гідроген пероксиду за участю каталізатора манган(ІV) оксиду або взаємодія алюмінію (алюмінієвий пил) з йодом (дрібнокристалічним) за участю води як каталізатора. 9. Уповільнення швидкості реакції між залізом (залізні ошурки) та хлоридною кислотою інгібітором (формалін). 10. Зміщення рівноваги у розчині амоніаку при нагріванні або в системі нітроген(ІІ) оксид – нітроген(ІV) оксид. 11. Приклади окисно-відновних реакцій розкладу солей (калій перманганату, амоній дихромату). 12. Електроліз розчину купрум(ІІ) хлориду та купрум(ІІ) сульфату. Практичні роботи. 1. Швидкість хімічної реакції. 2. Окисно-відновні реакції. 3. Вправи на генетичний зв’язок між неорганічними та органічними сполуками. 4. Якісні реакції на неорганічні речовини. 5. Якісні реакції на органічні речовини.
5. Основи вчення про напрямок та швидкість хімічного процесу. Демонстрації. 6. Приклади екзо- та ендотермічних реакцій. 7. Досліди, що підтверджують залежність швидкості реакції від концентрації реагуючих речовин і температури. 8. Розкладання гідроген пероксиду за участю каталізатора манган(ІV) оксиду або взаємодія алюмінію (алюмінієвий пил) з йодом (дрібнокристалічним) за участю води як каталізатора. 9. Уповільнення швидкості реакції між залізом (залізні ошурки) та хлоридною кислотою інгібітором (формалін). 10. Зміщення рівноваги у розчині амоніаку при нагріванні або в системі нітроген(ІІ) оксид – нітроген(ІV) оксид. 11. Приклади окисно-відновних реакцій розкладу солей (калій перманганату, амоній дихромату). 12. Електроліз розчину купрум(ІІ) хлориду та купрум(ІІ) сульфату. Практичні роботи. 1. Швидкість хімічної реакції. 2. Окисно-відновні реакції. 3. Вправи на генетичний зв’язок між неорганічними та органічними сполуками. 4. Якісні реакції на неорганічні речовини. 5. Якісні реакції на органічні речовини.
 5. Основи вчення про напрямок та швидкість хімічного процесу. На усіх рівнях важливим етапом вивчення тем є введення поняття швидкості хімічної реакції: Труднощі викликані різницею між поняттям швидкості тіла та швидкості х. р. Можливо запропонувати учням аналогію з фізикою “Фізична” швидкість – відношення довжини шляху до часу руху (зазвичай в с. ) “Хімічна” швидкість - ? Відношення кількості частинок що прореагували до часу реакції (“―” бо швидкість буде змінною в залежності від кількості речовини два окремих вогнища мають згоріти швидше ніж одне). Відношення кількість частинок в одиниці об'єму, до часу реакції (“ +”). Наступним кроком є встановлення факторів які впливають на швидкість х. р. • Природа • Концентрація • Температура (потребує уявлення про х. р. як результат зіткнень частинок) • Каталізатор (проміжна реакція або активний стан) • Величини поверхні розділу (подібно до концентрації, в твердій фізі частина речовини схована в середині шматочків))
5. Основи вчення про напрямок та швидкість хімічного процесу. На усіх рівнях важливим етапом вивчення тем є введення поняття швидкості хімічної реакції: Труднощі викликані різницею між поняттям швидкості тіла та швидкості х. р. Можливо запропонувати учням аналогію з фізикою “Фізична” швидкість – відношення довжини шляху до часу руху (зазвичай в с. ) “Хімічна” швидкість - ? Відношення кількості частинок що прореагували до часу реакції (“―” бо швидкість буде змінною в залежності від кількості речовини два окремих вогнища мають згоріти швидше ніж одне). Відношення кількість частинок в одиниці об'єму, до часу реакції (“ +”). Наступним кроком є встановлення факторів які впливають на швидкість х. р. • Природа • Концентрація • Температура (потребує уявлення про х. р. як результат зіткнень частинок) • Каталізатор (проміжна реакція або активний стан) • Величини поверхні розділу (подібно до концентрації, в твердій фізі частина речовини схована в середині шматочків))
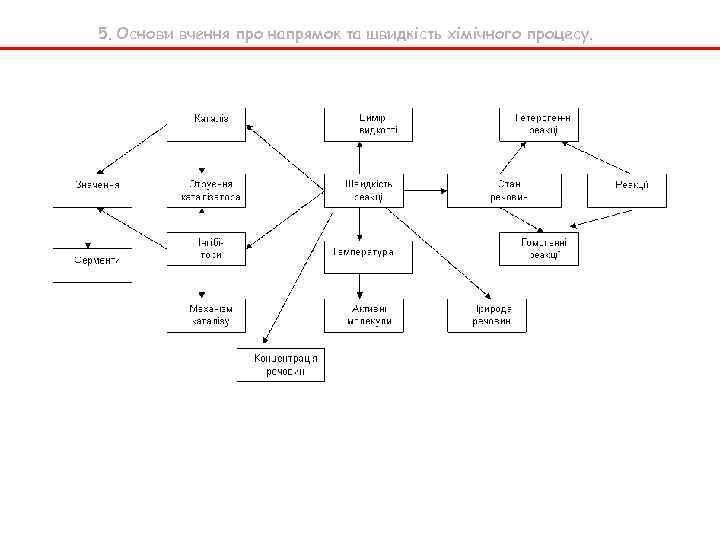
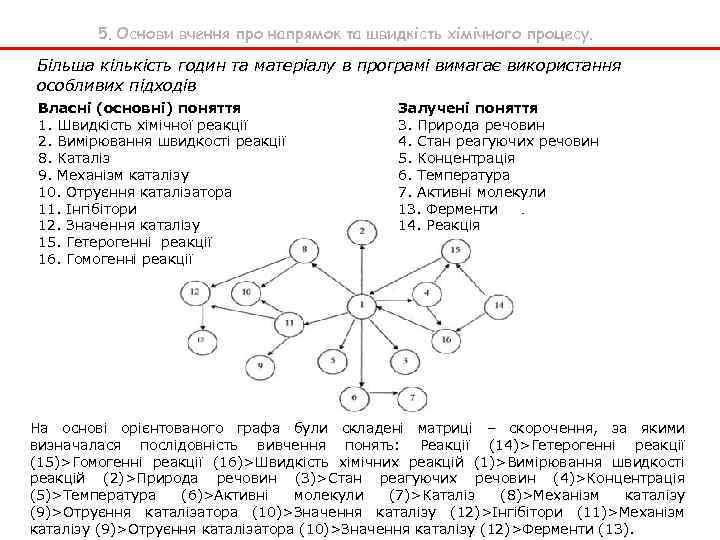 5. Основи вчення про напрямок та швидкість хімічного процесу. Більша кількість годин та матеріалу в програмі вимагає використання особливих підходів Власні (основні) поняття 1. Швидкість хімічної реакції 2. Вимірювання швидкості реакції 8. Каталіз 9. Механізм каталізу 10. Отруєння каталізатора 11. Інгібітори 12. Значення каталізу 15. Гетерогенні реакції 16. Гомогенні реакції Залучені поняття 3. Природа речовин 4. Стан реагуючих речовин 5. Концентрація 6. Температура 7. Активні молекули 13. Ферменти 14. Реакція На основі орієнтованого графа були складені матриці – скорочення, за якими визначалася послідовність вивчення понять: Реакції (14)>Гетерогенні реакції (15)>Гомогенні реакції (16)>Швидкість хімічних реакцій (1)>Вимірювання швидкості реакцій (2)>Природа речовин (3)>Стан реагуючих речовин (4)>Концентрація (5)>Температура (6)>Активні молекули (7)>Каталіз (8)>Механізм каталізу (9)>Отруєння каталізатора (10)>Значення каталізу (12)>Інгібітори (11)>Механізм каталізу (9)>Отруєння каталізатора (10)>Значення каталізу (12)>Ферменти (13).
5. Основи вчення про напрямок та швидкість хімічного процесу. Більша кількість годин та матеріалу в програмі вимагає використання особливих підходів Власні (основні) поняття 1. Швидкість хімічної реакції 2. Вимірювання швидкості реакції 8. Каталіз 9. Механізм каталізу 10. Отруєння каталізатора 11. Інгібітори 12. Значення каталізу 15. Гетерогенні реакції 16. Гомогенні реакції Залучені поняття 3. Природа речовин 4. Стан реагуючих речовин 5. Концентрація 6. Температура 7. Активні молекули 13. Ферменти 14. Реакція На основі орієнтованого графа були складені матриці – скорочення, за якими визначалася послідовність вивчення понять: Реакції (14)>Гетерогенні реакції (15)>Гомогенні реакції (16)>Швидкість хімічних реакцій (1)>Вимірювання швидкості реакцій (2)>Природа речовин (3)>Стан реагуючих речовин (4)>Концентрація (5)>Температура (6)>Активні молекули (7)>Каталіз (8)>Механізм каталізу (9)>Отруєння каталізатора (10)>Значення каталізу (12)>Інгібітори (11)>Механізм каталізу (9)>Отруєння каталізатора (10)>Значення каталізу (12)>Ферменти (13).
 5. Основи вчення про напрямок та швидкість хімічного процесу.
5. Основи вчення про напрямок та швидкість хімічного процесу.
 6. Окисно-відновні реакції, електроліз. Стандартний рівень 9 клас 2 год. на тиждень Тема 2. Хімічні реакції (9 год) Класифікація хімічних реакцій за різними ознаками. Реакції сполучення, розкладу, заміщення, обміну. Окисно-відновні реакції, їхнє значення. Процеси окиснення, відновлення, окисники, відновники. Складання рівнянь найпростіших окисно-відновних реакцій, добір коефіцієнтів. Тепловий ефект Оборотні й необоротні реакції. Екзотермічні та ендотермічні реакції. Термохімічне Швидкість хімічної реакції, залежність швидкості реакції від різних чинників. Демонстрації: – Лабораторні досліди: – рівняння.
6. Окисно-відновні реакції, електроліз. Стандартний рівень 9 клас 2 год. на тиждень Тема 2. Хімічні реакції (9 год) Класифікація хімічних реакцій за різними ознаками. Реакції сполучення, розкладу, заміщення, обміну. Окисно-відновні реакції, їхнє значення. Процеси окиснення, відновлення, окисники, відновники. Складання рівнянь найпростіших окисно-відновних реакцій, добір коефіцієнтів. Тепловий ефект Оборотні й необоротні реакції. Екзотермічні та ендотермічні реакції. Термохімічне Швидкість хімічної реакції, залежність швидкості реакції від різних чинників. Демонстрації: – Лабораторні досліди: – рівняння.
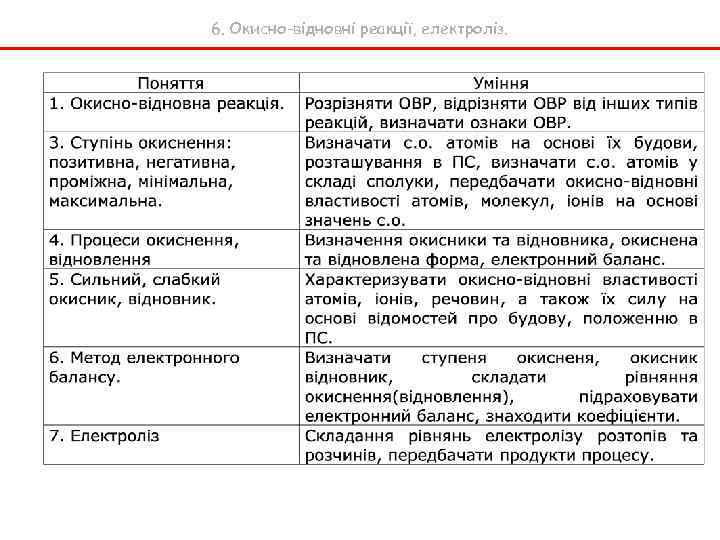
 6. Окисно-відновні реакції, електроліз. Профільний рівень 9 клас 4 год. на тиждень Тема 3. Окисно-відновні та електрохімічні процеси (15 год. ) Ступінь окиснення. Визначення ступеня окиснення атома елемента за хімічною формулою сполуки. Складання формули сполуки за відомими ступенями окиснення атомів елементів. Процеси окиснення і відновлення, відновники та окисники. Окисно-відновні реакції. Складання рівнянь окисно-відновних реакцій за методом електронного балансу. Роль окисно-відновних процесів. Електрохімічні процеси. Закони Фарадея. Поняття про електродний потенціал. Гальванічний елемент, його робота. Електроліз, послідовність електродних процесів, застосування електролізу. Демонстрації: 7. Окисно-відновні реакції (взаємодія Fe i Cu. SO 4, розчину калій йодиду з хлорною водою).
6. Окисно-відновні реакції, електроліз. Профільний рівень 9 клас 4 год. на тиждень Тема 3. Окисно-відновні та електрохімічні процеси (15 год. ) Ступінь окиснення. Визначення ступеня окиснення атома елемента за хімічною формулою сполуки. Складання формули сполуки за відомими ступенями окиснення атомів елементів. Процеси окиснення і відновлення, відновники та окисники. Окисно-відновні реакції. Складання рівнянь окисно-відновних реакцій за методом електронного балансу. Роль окисно-відновних процесів. Електрохімічні процеси. Закони Фарадея. Поняття про електродний потенціал. Гальванічний елемент, його робота. Електроліз, послідовність електродних процесів, застосування електролізу. Демонстрації: 7. Окисно-відновні реакції (взаємодія Fe i Cu. SO 4, розчину калій йодиду з хлорною водою).
 6. Окисно-відновні реакції, електроліз. Профільний рівень 10 клас 4 год. на тиждень Розділ ІІІ. Металічні елементи та їхні сполуки Тема 1. Загальні відомості про металічні елементи та метали Положення металічних елементів у періодичній системі. Особливості будови їх атомів. Поширеність у природі. Метали. Металічний зв’язок. Характерні фізичні та хімічні властивості металів: взаємодія з неметалами, водою, лугами, кислотами, розчинами солей. Обчислення за рівняннями реакцій між розчином солі та металом. Корозія металів. Види корозії: хімічна та електрохімічна. Захист від корозії. Поняття про сплави. Загальні способи добування металів із руд. Поняття про металургію. Пірометалургія, гідрометалургія, електрометалургія, мікробіометалургія. Електроліз водних розчинів та розплавів безоксигенових солей. ? ? клас ? год. на тиждень Узагальнювальне повторення найважливіших питань курсу хімії Тема 4. Хімічні реакції (12 год. ) Сучасні уявлення про природу хімічного зв’язку; Ковалентний зв’язок, способи його утворення. Гібридизація електронних орбіта лей атомів. Просторова будова молекул. Йонний зв'язок. Йонні кристали. Металічний зв'язок. Водневий зв'язок. Міжмолекулярна взаємодія. Валентність елементів у світлі електронної теорії хімічного зв’язку. Валентність і ступінь окиснення. Окисно-відновіні реакції.
6. Окисно-відновні реакції, електроліз. Профільний рівень 10 клас 4 год. на тиждень Розділ ІІІ. Металічні елементи та їхні сполуки Тема 1. Загальні відомості про металічні елементи та метали Положення металічних елементів у періодичній системі. Особливості будови їх атомів. Поширеність у природі. Метали. Металічний зв’язок. Характерні фізичні та хімічні властивості металів: взаємодія з неметалами, водою, лугами, кислотами, розчинами солей. Обчислення за рівняннями реакцій між розчином солі та металом. Корозія металів. Види корозії: хімічна та електрохімічна. Захист від корозії. Поняття про сплави. Загальні способи добування металів із руд. Поняття про металургію. Пірометалургія, гідрометалургія, електрометалургія, мікробіометалургія. Електроліз водних розчинів та розплавів безоксигенових солей. ? ? клас ? год. на тиждень Узагальнювальне повторення найважливіших питань курсу хімії Тема 4. Хімічні реакції (12 год. ) Сучасні уявлення про природу хімічного зв’язку; Ковалентний зв’язок, способи його утворення. Гібридизація електронних орбіта лей атомів. Просторова будова молекул. Йонний зв'язок. Йонні кристали. Металічний зв'язок. Водневий зв'язок. Міжмолекулярна взаємодія. Валентність елементів у світлі електронної теорії хімічного зв’язку. Валентність і ступінь окиснення. Окисно-відновіні реакції.
 6. Окисно-відновні реакції, електроліз.
6. Окисно-відновні реакції, електроліз.


