392b77b47552f7ddd9a764a0e9038f68.ppt
- Количество слайдов: 27

Методическая разработка к уроку химии СЕРА И СОЕДИНЕНИЯ СЕРЫ Ялышева И. А. Учитель химии ГБОУ СОШ № 305 Санкт-Петербурга

Цели урока: n Актуализация опорных предметных и межпредметных знаний n Сформировать понятие о валентных возможностях серы на основании положения в П. С. и строении атома n Сформировать понятие об аллотропии серы, ее физических и химических свойствах, применении
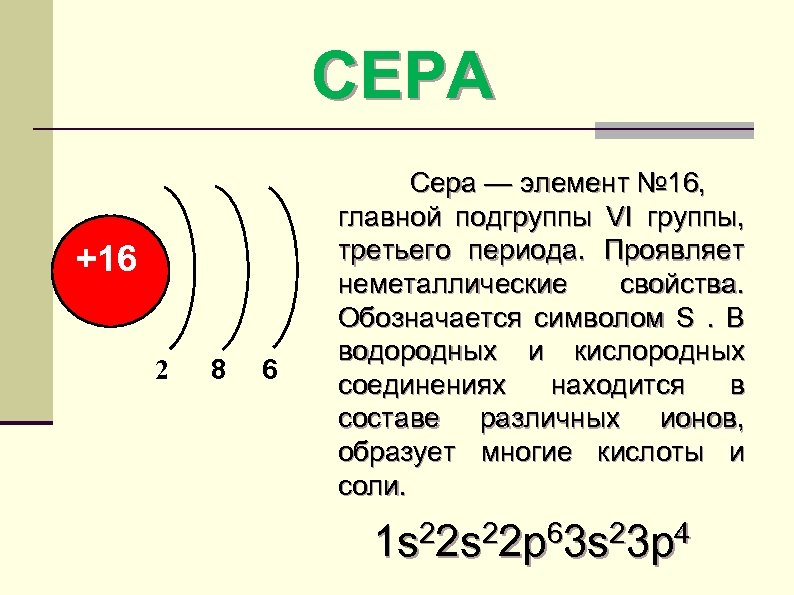
СЕРА +16 2 8 6 Сера — элемент № 16, главной подгруппы VI группы, третьего периода. Проявляет неметаллические свойства. Обозначается символом S. В водородных и кислородных соединениях находится в составе различных ионов, образует многие кислоты и соли. 22 s 22 p 63 s 23 p 4 1 s

Строение атома серы Электронное строение Степень окисления +2, -2 +4 +6

Получение серы 1. Неполное окисление сероводорода: 2 H 2 S + O 2 = 2 S↓ + 2 H 2 O (недостаток O 2). 2. Реакция Валенродера: 2 H 2 S + SO 2 = 3 S↓ + 2 H 2 O

Химические свойства серы Реагирует с металлами (искл. золото, платина и рутений): 2 Na + S = Na 2 S; 2 Al + 3 S = Al 2 S 3; Нg + S = Hg. S (демеркуризация)
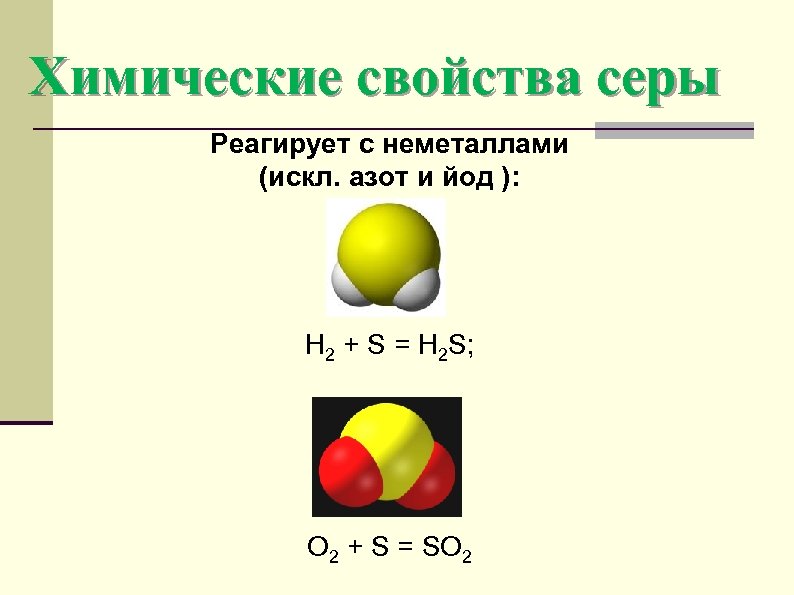
Химические свойства серы Реагирует с неметаллами (искл. азот и йод ): H 2 + S = H 2 S; O 2 + S = SO 2

Химические свойства серы Реагирует со сложными веществами: 3 S + 2 KCl. O 3 = 2 KCl + 3 SO 2; S + 2 H 2 SO 4(конц. ) = 3 SO 2 + 2 H 2 O; 3 S + 6 KOH = K 2 SO 3 + 2 K 2 S + 3 H 2 O

Сера (англ. Sulfur, фр. Soufre, нем. Schwefel) в самородном состоянии, а также в виде сернистых соединений известна с древнейших времён. Из-за своих свойств сера использовалась жрецами в составе священных курений при религиозных обрядах. Сера считалась произведением сверхчеловеческих существ из мира духов или подземных богов. Очень давно сера стала применяться в составе различных горючих смесей для военных целей.

Сера, вероятно, входила в состав «греческого огня» , наводившего ужас на противников. Около китайцы стали использовать её в пиротехнических смесях, в частности, в смеси типа пороха. Горючесть серы, лёгкость, с которой она соединяется с металлами с образованием сульфидов.
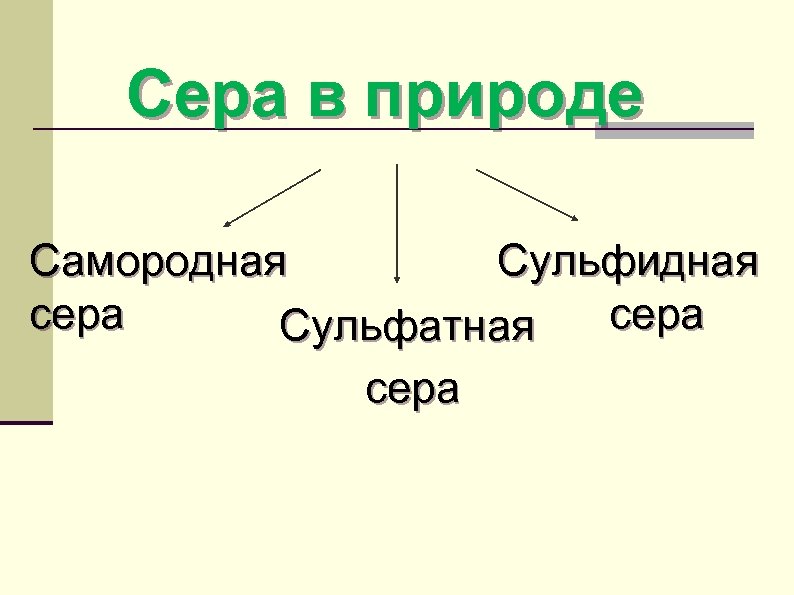
Сера в природе Самородная Сульфидная сера Сульфатная сера

Самородная сера

Самородная сера Химическая формула: S Сингония: ромбическая Цвет: Жёлто-оранжевый, серовато-жёлтый, серовато-бурый. Блеск: жирный Прозрачность: мутный, просвечивает Легко плавится (при 119°С) и сгорает синим пламенем, превращаясь в SO 3. Поведение в кислотах: Не растворяется в воде, но растворима в CS 2.


Сульфидная сера Пирит-Fe. S 2 Fe 46, 6%; S 53, 4% Киноварь-Hg. S Hg 86, 2%; S 13, 8%

Сульфатная сера Гипс – Ca. SO 4*2 H 2 O Барит – Ba. SO 4

Сера в природе халькопирит Cu. Fe. S 2 киноварь Hg. S пирит Fe. S 2 галенит Pb. S самородная сера S гипс Са. SO 4. 2 H 2 O
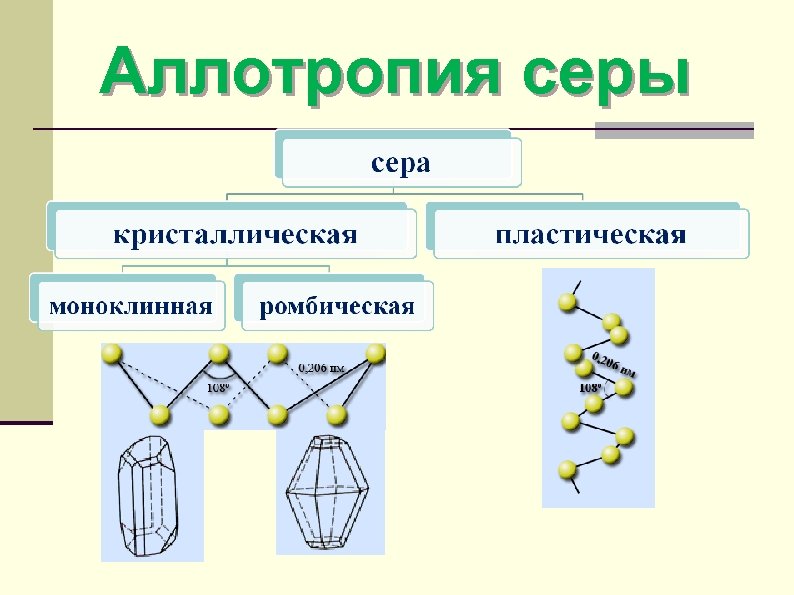
Аллотропия серы
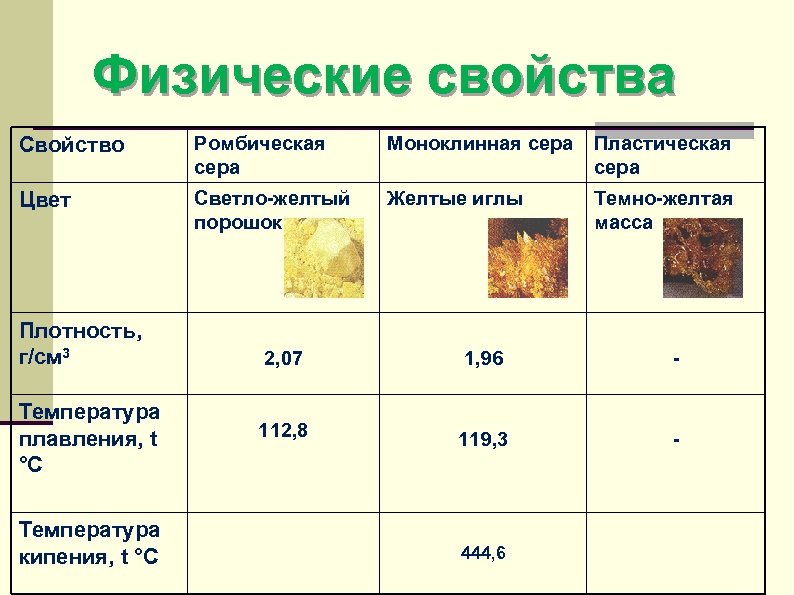
Физические свойства Свойство Ромбическая сера Моноклинная сера Пластическая сера Цвет Светло-желтый порошок Желтые иглы Темно-желтая масса Плотность, г/см 3 Температура плавления, t °C Температура кипения, t °C 2, 07 1, 96 - 112, 8 119, 3 - 444, 6

Применение серы » » » » Производство серной кислоты Получение резины Получение гидросульфата кальция (для производства бумаги) Производство пороха, пиротехники Получение «сусального золота» – Sn. S 2 В медицине для лечения кожных заболеваний В сельском хозяйстве для борьбы с вредителями

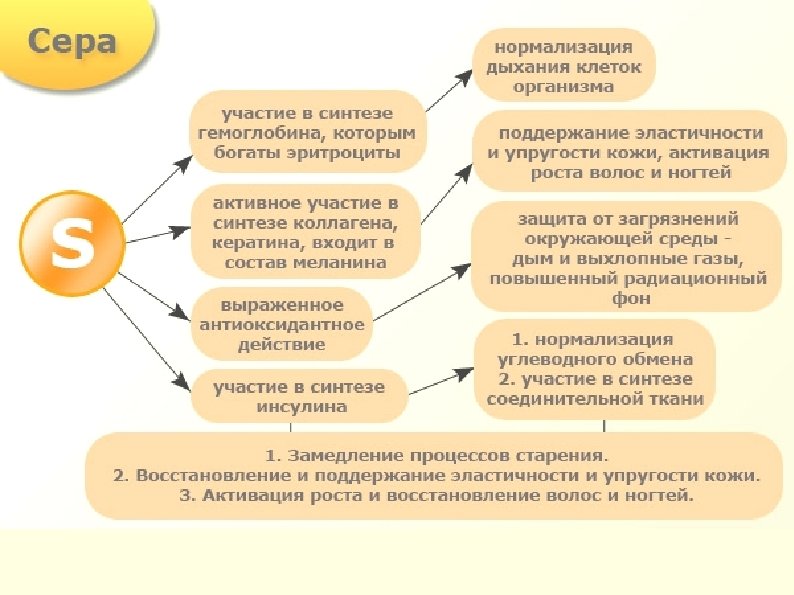
Роль серы в организме

Биологическая роль серы » Сера участвует в ОВР в организмах растений и животных » Сера входит в состав белков и аминокислот » Особенно много серы в волосах, шерсти, рогах, копытах » Соединения серы обнаружены в хрящах, костях, в желчи

Оксид серы (IV) SO 2 токсичен. Симптомы при отравлении сернистым газом — насморк, кашель, охриплость, першение в горле. При вдыхании сернистого газа более высокой концентрации — удушье, расстройство речи, затруднение глотания, рвота, возможен острый отёк лёгких. ПДК(предельно допустимая концентрация): - в атмосферном воздухе максимальноразовая — 0, 5 мг/м³, среднесуточная — 0, 05 мг/м³; - в помещении (рабочая зона) — 10 мг/м³

Повторение n Строение атома серы на основе положения ее в П. С. n Физические свойства серы n Окислительно-восстановительные свойства серы; n Природные соединения серы; n Применение серы

Литература n О. С. Габриелян, Химия 9 класс

Благодарю за внимание!!!
392b77b47552f7ddd9a764a0e9038f68.ppt