методи очистки води 2.ppt
- Количество слайдов: 30
 Методи очистки води
Методи очистки води
 Метод нейтралізації стічних вод Стічні води, які містять мінеральні кислоти, або луги, перед їх скиданням у природні водойми або перед використанням у технологічних процесах піддають нейтралізації. Практично нейтральними вважають води, які мають р. Н 6, 5 -8, 5. Для нейтралізації кислотних вод сполуки основного характеру, а лужних – кислотного. p. H нейтрализация призначена для доведення рівня р. Н стічних вод до нейтрального стану.
Метод нейтралізації стічних вод Стічні води, які містять мінеральні кислоти, або луги, перед їх скиданням у природні водойми або перед використанням у технологічних процесах піддають нейтралізації. Практично нейтральними вважають води, які мають р. Н 6, 5 -8, 5. Для нейтралізації кислотних вод сполуки основного характеру, а лужних – кислотного. p. H нейтрализация призначена для доведення рівня р. Н стічних вод до нейтрального стану.
 Для нейтралізації кислих вод можуть бути використані луги (Na. OH, КОН), сода (Nа 2 СО 3), аміачна вода (NH 4 OH), карбонати кальцію і магнію (Са. СО 3, Mg. CO 3), доломіт (Ca. CО 3*Mg. CO 3), цемент. Однак найбільш дешевим реагентом є вапняне молоко зі вмістом активного вапна Са(ОН)2 5 - 10%. Соду і їдкий натр варто використовувати, якщо вони є відходами виробництва. Іноді для нейтралізації застосовують різні відходи виробництва. Наприклад, шлаки сталеплавильного, феррохромового і доменного виробництв використовують для нейтралізації вод, що містять сірчану кислоту. Реагенти вибирають у залежності від складу і концентрації кислої стічної води. При цьому враховують, чи буде в процесі утворюватися осад чи ні. Розрізняють три види кислотовмісних стічних вод: 1) води, що містять слабкі кислоти (Н 2 СО 3, СН 3 СООН); 2) води, що містять сильні кислоти (НС 1, HNO 3). Для їхньої нейтралізації може бути використаний будь-який названий вище реагент. Солі цих кислот добре розчинні у воді; 3) води, що містять сірчану і сірчисту кислоту. Кальцієві солі цих кислот погано розчинні у воді і випадають в осад. Вапно для нейтралізації вводиться у стічну воду у вигляді вапняного молока ("мокре" дозування) або у вигляді сухого порошку ("сухе" дозування).
Для нейтралізації кислих вод можуть бути використані луги (Na. OH, КОН), сода (Nа 2 СО 3), аміачна вода (NH 4 OH), карбонати кальцію і магнію (Са. СО 3, Mg. CO 3), доломіт (Ca. CО 3*Mg. CO 3), цемент. Однак найбільш дешевим реагентом є вапняне молоко зі вмістом активного вапна Са(ОН)2 5 - 10%. Соду і їдкий натр варто використовувати, якщо вони є відходами виробництва. Іноді для нейтралізації застосовують різні відходи виробництва. Наприклад, шлаки сталеплавильного, феррохромового і доменного виробництв використовують для нейтралізації вод, що містять сірчану кислоту. Реагенти вибирають у залежності від складу і концентрації кислої стічної води. При цьому враховують, чи буде в процесі утворюватися осад чи ні. Розрізняють три види кислотовмісних стічних вод: 1) води, що містять слабкі кислоти (Н 2 СО 3, СН 3 СООН); 2) води, що містять сильні кислоти (НС 1, HNO 3). Для їхньої нейтралізації може бути використаний будь-який названий вище реагент. Солі цих кислот добре розчинні у воді; 3) води, що містять сірчану і сірчисту кислоту. Кальцієві солі цих кислот погано розчинні у воді і випадають в осад. Вапно для нейтралізації вводиться у стічну воду у вигляді вапняного молока ("мокре" дозування) або у вигляді сухого порошку ("сухе" дозування).
 При нейтралізації стічних вод, що містять сірчану кислоту, вапняним молоком - в осад виділяється гіпс Ca. SO 4*H 2 О. Розчинність гіпсу мало змінюється з температурою. При переміщенні таких розчинів, відбувається відкладання гіпсу на стінках трубопроводів і їх забивання. Для усунення забивання трубопроводу необхідно промивати їх чистой водою або додавати в стічні води спеціальні пом`якшувачі, наприклад гексаметафосфат. Збільшення швидкості руху нейтралізованих вод сприяє зменшенню відкладень гіпсу на стінках трубопроводу. Для нейтралізації лужних стічних вод використовують різні кислоти або кислі гази. Хімічне очищення стічних вод проводиться з метою вилучення розчинених речовин та завислих часток. Її проводять перед подачею стічних вод на біологічне очищення.
При нейтралізації стічних вод, що містять сірчану кислоту, вапняним молоком - в осад виділяється гіпс Ca. SO 4*H 2 О. Розчинність гіпсу мало змінюється з температурою. При переміщенні таких розчинів, відбувається відкладання гіпсу на стінках трубопроводів і їх забивання. Для усунення забивання трубопроводу необхідно промивати їх чистой водою або додавати в стічні води спеціальні пом`якшувачі, наприклад гексаметафосфат. Збільшення швидкості руху нейтралізованих вод сприяє зменшенню відкладень гіпсу на стінках трубопроводу. Для нейтралізації лужних стічних вод використовують різні кислоти або кислі гази. Хімічне очищення стічних вод проводиться з метою вилучення розчинених речовин та завислих часток. Її проводять перед подачею стічних вод на біологічне очищення.
 Нейтралізація кислими газами Для нейтралізації лужних стічних вод останнім часом починають використовувати гази, які містять СО 2, SO 2, N 2 O 3 і ін. Застосування кислих газів дозволяє не тільки нейтралізувати стічні води, але й одночасно робити високоефективне очищення самих цих газів від шкідливих компонентів. Використання для нейтралізації лужних стічних вод діоксиду вуглецю має ряд переваг у порівнянні із сірчаною або соляною кислотами. Застосування СО 2 димових газів дозволяє різко знизити вартість процесу нейтралізації. Унаслідок поганої розчинності СО 2, зменшується небезпека переокисления нейтралізованих розчинів. Карбонати, що утворюються, знаходять більше застосування в порівнянні із сульфатами або хлоридами, крім того, корозійні і токсичні дії СО 32 - -іонів у воді менше, ніж для іонів SO 42 - і Сl-.
Нейтралізація кислими газами Для нейтралізації лужних стічних вод останнім часом починають використовувати гази, які містять СО 2, SO 2, N 2 O 3 і ін. Застосування кислих газів дозволяє не тільки нейтралізувати стічні води, але й одночасно робити високоефективне очищення самих цих газів від шкідливих компонентів. Використання для нейтралізації лужних стічних вод діоксиду вуглецю має ряд переваг у порівнянні із сірчаною або соляною кислотами. Застосування СО 2 димових газів дозволяє різко знизити вартість процесу нейтралізації. Унаслідок поганої розчинності СО 2, зменшується небезпека переокисления нейтралізованих розчинів. Карбонати, що утворюються, знаходять більше застосування в порівнянні із сульфатами або хлоридами, крім того, корозійні і токсичні дії СО 32 - -іонів у воді менше, ніж для іонів SO 42 - і Сl-.
 «Суха» нейтралізація Нейтралізацію кислих вод можна проводити шляхом фільтрування їх через нейтралізуючі матеріали. У цьому випадку для нейтралізації кислих вод проводять фільтрування їх через шар магнезиту, доломіту, вапняку, твердих відходів (шлак, зола). Процес ведуть у фільтрах-нейтралізаторах, що можуть бути горизонтальными або вертикальними. Для вертикальних фільтрів використовують шматки вапняку або доломіту розміром 30 - 80 мм. При висоті шару матеріалу 0, 85 - 1, 2 м швидкість повинна бути не більш 5 м/год, а тривалість контакту не менш 10 хв. У горизонтальних фільтрів швидкість руху стічних вод 1 - 3 м/с.
«Суха» нейтралізація Нейтралізацію кислих вод можна проводити шляхом фільтрування їх через нейтралізуючі матеріали. У цьому випадку для нейтралізації кислих вод проводять фільтрування їх через шар магнезиту, доломіту, вапняку, твердих відходів (шлак, зола). Процес ведуть у фільтрах-нейтралізаторах, що можуть бути горизонтальными або вертикальними. Для вертикальних фільтрів використовують шматки вапняку або доломіту розміром 30 - 80 мм. При висоті шару матеріалу 0, 85 - 1, 2 м швидкість повинна бути не більш 5 м/год, а тривалість контакту не менш 10 хв. У горизонтальних фільтрів швидкість руху стічних вод 1 - 3 м/с.
 Метод коагуляції Коагуляція – це процес укрупнення диспергованих частинок внаслідок їх взаємодії і об’єднання в агрегати. При очистці стічних вод її використовують для прискорення осадження тонкодиспергованих домішок і емульсованих речовин. Коагуляція може проходити самовільно під впливом хімічних і фізичних процесів і це явище має велике значення для самоочищення водних джерел. Проте в процесах очистки стічних вод очистка проходить під впливом коагулянтів.
Метод коагуляції Коагуляція – це процес укрупнення диспергованих частинок внаслідок їх взаємодії і об’єднання в агрегати. При очистці стічних вод її використовують для прискорення осадження тонкодиспергованих домішок і емульсованих речовин. Коагуляція може проходити самовільно під впливом хімічних і фізичних процесів і це явище має велике значення для самоочищення водних джерел. Проте в процесах очистки стічних вод очистка проходить під впливом коагулянтів.
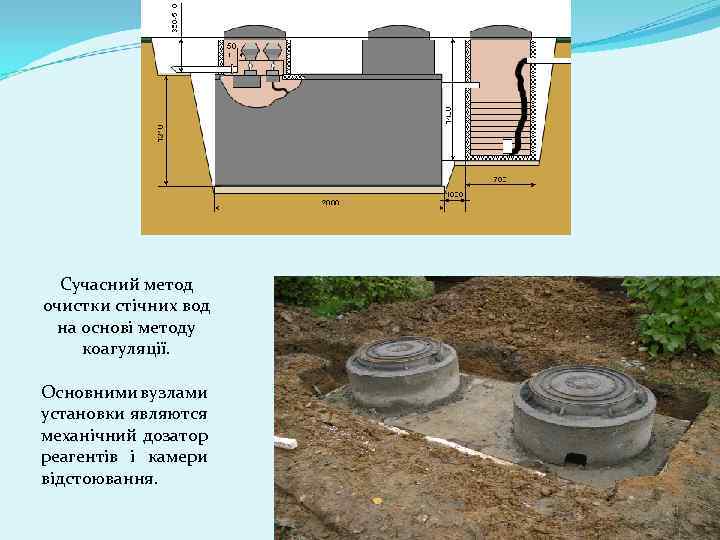 Сучасний метод очистки стічних вод на основі методу коагуляції. Основними вузлами установки являются механічний дозатор реагентів і камери відстоювання.
Сучасний метод очистки стічних вод на основі методу коагуляції. Основними вузлами установки являются механічний дозатор реагентів і камери відстоювання.
 Коагулянти у воді утворюють пластівці гідратів окисів металів, що швидко осідають під дією сили тяжіння. Пластівці володіють здатністю уловлювати колоїдні і зважені частки й агрегувати їх. Тому що колоїдні часточки мають слабкий негативний заряд, а пластівці коагулянтів слабкий позитивний заряд, то між ними виникає взаємне тяжіння. Процес гідролізу коагулянтів і утворення пластівців відбувається на наступних стадіях: Ме 3+ + НОН = Ме(ОН)2+ + Н+ Ме(ОН)2++ НОН = Me(OH)22+ + H+ Me(OH)2+ + НОН = Ме(ОН)3 + Н+ Ме 3+ + НОН = Ме(ОН)3 v + 3 Н+ (2. 5) Як коагулянти звичайно використовують солі алюмінію, заліза або їх суміші. Вибір коагулянту залежить від його складу, фізико-хімічних властивостей і вартості. Як коагулянти використовуються наступні солі алюмінію: сульфат алюмінію Al 2(SО 4)3*18 H 2 O; алюмінат натрію Na. Al. О 2, оксихлорид алюмінію А 13(ОН)5 С 1; квасці - алюмокалієві KAl(SO 4)2*12 H 2 О і аміачні NH 4 Al(SO 4)2*12 H 2 О. З цих сполук найбільш розповсюджений сульфат алюмінію, що ефективний в інтервалі значень р. Н 5 - 7, 5. Він добре розчиняється у воді і має відносно низьку вартість. Його застосовують у сухому вигляді або в вигляді 50% -ного розчину. Алюмінат натрію застосовують у сухому вигляді або у ввигляді 45% розчину. Він є лужним реагентом, при р. Н 9, 3 - 9, 8 утворюються швидкоосаджувані пластівці.
Коагулянти у воді утворюють пластівці гідратів окисів металів, що швидко осідають під дією сили тяжіння. Пластівці володіють здатністю уловлювати колоїдні і зважені частки й агрегувати їх. Тому що колоїдні часточки мають слабкий негативний заряд, а пластівці коагулянтів слабкий позитивний заряд, то між ними виникає взаємне тяжіння. Процес гідролізу коагулянтів і утворення пластівців відбувається на наступних стадіях: Ме 3+ + НОН = Ме(ОН)2+ + Н+ Ме(ОН)2++ НОН = Me(OH)22+ + H+ Me(OH)2+ + НОН = Ме(ОН)3 + Н+ Ме 3+ + НОН = Ме(ОН)3 v + 3 Н+ (2. 5) Як коагулянти звичайно використовують солі алюмінію, заліза або їх суміші. Вибір коагулянту залежить від його складу, фізико-хімічних властивостей і вартості. Як коагулянти використовуються наступні солі алюмінію: сульфат алюмінію Al 2(SО 4)3*18 H 2 O; алюмінат натрію Na. Al. О 2, оксихлорид алюмінію А 13(ОН)5 С 1; квасці - алюмокалієві KAl(SO 4)2*12 H 2 О і аміачні NH 4 Al(SO 4)2*12 H 2 О. З цих сполук найбільш розповсюджений сульфат алюмінію, що ефективний в інтервалі значень р. Н 5 - 7, 5. Він добре розчиняється у воді і має відносно низьку вартість. Його застосовують у сухому вигляді або в вигляді 50% -ного розчину. Алюмінат натрію застосовують у сухому вигляді або у ввигляді 45% розчину. Він є лужним реагентом, при р. Н 9, 3 - 9, 8 утворюються швидкоосаджувані пластівці.
 Із солей заліза як коагулянти використовують сульфати заліза Fe 2(SO 4)3*2 H 2 O, Fe 2(SO 4)3*3 H 2 O і Fe. SO 4 * 7 H 2 О, а також хлорне залізо Fe. Cl 3. Найбільше освітлення відбувається при використанні солей тривалентного заліза. Хлорне залізо застосовують у сухому вигляді або у вигляді 10 -15%них розчинів. Сульфати використовують у вигляді порошків. Для підлужнення стічних вод використовують Na. OH і Ca(OH)2. Солі заліза, як коагулянти, мають ряд переваг перед солями алюмінію: кращу дію виявляють при низьких температурах води; більш широка область оптимальних значень р. Н середовища; велика міцність і гідравлічна крупність пластівців; можливість використовувати для вод з більш широким діапазоном сольового складу; здатність усувати шкідливі запахи і присмаки, обумовлені присутністю сірководню. Однак є і недоліки: утворення при реакції катіонів заліза з деякими органічними сполуками сильно забарвлених розчинних комплексів; сильні кислотні властивості підсилюють корозію апаратури; менш розвинена поверхня пластівців. У полідисперсних системах коагуляція відбувається швидше, ніж у монодиоперсних, тому що великі частки при осіданні захоплюють за собою більш дрібні. Міцність пластівців залежить від гранулометричного складу часточок, що утворюються, і пластичності. Агломерати часточок неоднорідних за розміром міцніші, ніж однорідні. Унаслідок виділення газів з води, а також у результаті аерації і флотації відбувається газонасичення пластівців, що супроводжується зменшенням об'ємної маси пластівців і зменшенням швидкості осадження.
Із солей заліза як коагулянти використовують сульфати заліза Fe 2(SO 4)3*2 H 2 O, Fe 2(SO 4)3*3 H 2 O і Fe. SO 4 * 7 H 2 О, а також хлорне залізо Fe. Cl 3. Найбільше освітлення відбувається при використанні солей тривалентного заліза. Хлорне залізо застосовують у сухому вигляді або у вигляді 10 -15%них розчинів. Сульфати використовують у вигляді порошків. Для підлужнення стічних вод використовують Na. OH і Ca(OH)2. Солі заліза, як коагулянти, мають ряд переваг перед солями алюмінію: кращу дію виявляють при низьких температурах води; більш широка область оптимальних значень р. Н середовища; велика міцність і гідравлічна крупність пластівців; можливість використовувати для вод з більш широким діапазоном сольового складу; здатність усувати шкідливі запахи і присмаки, обумовлені присутністю сірководню. Однак є і недоліки: утворення при реакції катіонів заліза з деякими органічними сполуками сильно забарвлених розчинних комплексів; сильні кислотні властивості підсилюють корозію апаратури; менш розвинена поверхня пластівців. У полідисперсних системах коагуляція відбувається швидше, ніж у монодиоперсних, тому що великі частки при осіданні захоплюють за собою більш дрібні. Міцність пластівців залежить від гранулометричного складу часточок, що утворюються, і пластичності. Агломерати часточок неоднорідних за розміром міцніші, ніж однорідні. Унаслідок виділення газів з води, а також у результаті аерації і флотації відбувається газонасичення пластівців, що супроводжується зменшенням об'ємної маси пластівців і зменшенням швидкості осадження.
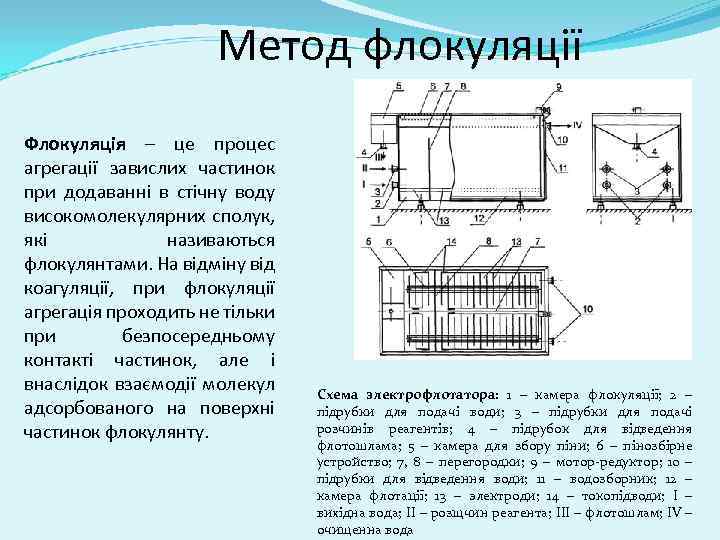 Метод флокуляції Флокуляція – це процес агрегації завислих частинок при додаванні в стічну воду високомолекулярних сполук, які називаються флокулянтами. На відміну від коагуляції, при флокуляції агрегація проходить не тільки при безпосередньому контакті частинок, але і внаслідок взаємодії молекул адсорбованого на поверхні частинок флокулянту. Схема электрофлотатора: 1 – камера флокуляції; 2 – підрубки для подачі води; 3 – підрубки для подачі розчинів реагентів; 4 – підрубок для відведення флотошлама; 5 – камера для збору піни; 6 – пінозбірне устройство; 7, 8 – перегородки; 9 – мотор-редуктор; 10 – підрубки для відведення води; 11 – водозборник; 12 – камера флотації; 13 – электроди; 14 – токопідводи; I – вихідна вода; II – розщчин реагента; III – флотошлам; IV – очищенна вода
Метод флокуляції Флокуляція – це процес агрегації завислих частинок при додаванні в стічну воду високомолекулярних сполук, які називаються флокулянтами. На відміну від коагуляції, при флокуляції агрегація проходить не тільки при безпосередньому контакті частинок, але і внаслідок взаємодії молекул адсорбованого на поверхні частинок флокулянту. Схема электрофлотатора: 1 – камера флокуляції; 2 – підрубки для подачі води; 3 – підрубки для подачі розчинів реагентів; 4 – підрубок для відведення флотошлама; 5 – камера для збору піни; 6 – пінозбірне устройство; 7, 8 – перегородки; 9 – мотор-редуктор; 10 – підрубки для відведення води; 11 – водозборник; 12 – камера флотації; 13 – электроди; 14 – токопідводи; I – вихідна вода; II – розщчин реагента; III – флотошлам; IV – очищенна вода
 для очищення стічних вод використовують природні і синтетичні флокулянти. До природних флокулянтів відносяться крохмаль, декстрин, ефіри, целюлози, ін. Із синтетичних органічних флокулянтів найбільше застосування в нашій країні одержав поліакриламід технічний (ПАА) і гідролізований (ГПАА). Технічний ПАА одержують при взаємодії акрилонітрилу із сірчаною кислотою з наступною полімеризацією акриламіду. Гідралізований поліакриламід одержують омиленням технічного ПАА лугом. При виборі складу і дози флокулянта, враховують властивості його макромолекул і природу диспергированих часточок. Оптимальна доза ПАА для очищення промислових стічних вод коливається в межах 0, 4 - 1 г/м 3. ПАА діє в широкому діапазоні р. Н середовища. Однак швидкість осадження сфлокульованих пластівців при р. Н 9 зменшується. Механізм дії флокулянтів оснований на наступних явищах: адсорбції молекул флокулянта на поверхні колоїдних частоток; ретикуляції (утворення сітчастої структури) молекул флокулята; злипанні колоїдних часточок за рахунок сил Ван-дер-Ваальса. Процес очищення стічних вод коагуляцією і флокуляцією складається з наступних стадій: дозування і змішування реагентів зі стічною водою; утворення пластівців та їх осадження.
для очищення стічних вод використовують природні і синтетичні флокулянти. До природних флокулянтів відносяться крохмаль, декстрин, ефіри, целюлози, ін. Із синтетичних органічних флокулянтів найбільше застосування в нашій країні одержав поліакриламід технічний (ПАА) і гідролізований (ГПАА). Технічний ПАА одержують при взаємодії акрилонітрилу із сірчаною кислотою з наступною полімеризацією акриламіду. Гідралізований поліакриламід одержують омиленням технічного ПАА лугом. При виборі складу і дози флокулянта, враховують властивості його макромолекул і природу диспергированих часточок. Оптимальна доза ПАА для очищення промислових стічних вод коливається в межах 0, 4 - 1 г/м 3. ПАА діє в широкому діапазоні р. Н середовища. Однак швидкість осадження сфлокульованих пластівців при р. Н 9 зменшується. Механізм дії флокулянтів оснований на наступних явищах: адсорбції молекул флокулянта на поверхні колоїдних частоток; ретикуляції (утворення сітчастої структури) молекул флокулята; злипанні колоїдних часточок за рахунок сил Ван-дер-Ваальса. Процес очищення стічних вод коагуляцією і флокуляцією складається з наступних стадій: дозування і змішування реагентів зі стічною водою; утворення пластівців та їх осадження.
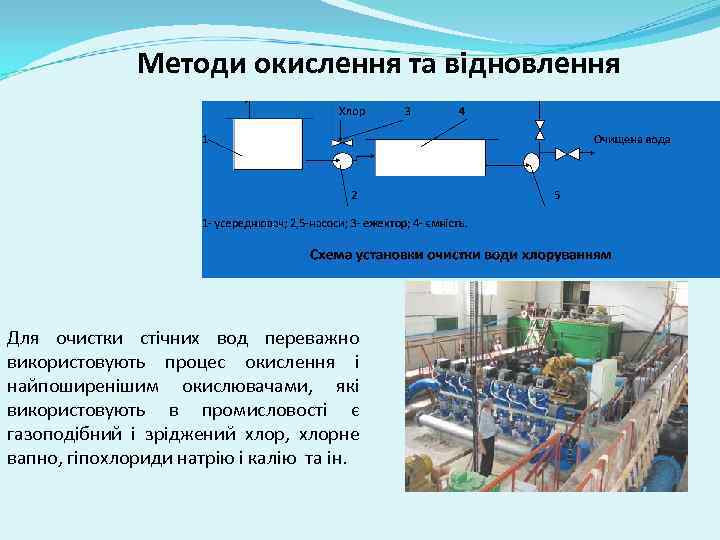 Методи окислення та відновлення Для очистки стічних вод переважно використовують процес окислення і найпоширенішим окислювачами, які використовують в промисловості є газоподібний і зріджений хлор, хлорне вапно, гіпохлориди натрію і калію та ін.
Методи окислення та відновлення Для очистки стічних вод переважно використовують процес окислення і найпоширенішим окислювачами, які використовують в промисловості є газоподібний і зріджений хлор, хлорне вапно, гіпохлориди натрію і калію та ін.
 Навіщо хлорують воду Це найбільш поширений спосіб знезараження питної води; Хлор пригноблює ферментні системи мікробів, що каталізують окислювально-відновні процеси; Хлорування застосовується і для знезараження води в системах централізованого водопостачання при епідеміологічних свідченнях, а також для знезараження стічних вод, води плавальних басейнів, знебарвлення, знезалізнення виробничих вод і ін.
Навіщо хлорують воду Це найбільш поширений спосіб знезараження питної води; Хлор пригноблює ферментні системи мікробів, що каталізують окислювально-відновні процеси; Хлорування застосовується і для знезараження води в системах централізованого водопостачання при епідеміологічних свідченнях, а також для знезараження стічних вод, води плавальних басейнів, знебарвлення, знезалізнення виробничих вод і ін.
 Озонування води Озон є природним засобом дезинфекції, який широко використовується в технічних і медичних цілях. Він являє собою сполуку, що діє як активний окислювач. Зустрічаючи у воді забруднення і органічні сполуки, він їх тут же нейтралізує, утворюючи оксиди, які негайно затримуються фільтрами.
Озонування води Озон є природним засобом дезинфекції, який широко використовується в технічних і медичних цілях. Він являє собою сполуку, що діє як активний окислювач. Зустрічаючи у воді забруднення і органічні сполуки, він їх тут же нейтралізує, утворюючи оксиди, які негайно затримуються фільтрами.
 атмосфери. При температурі -111, 9°С озон перетворюється в нестійку рідину темно-синього кольору. Чистий озон вибухонебезпечний, тому що при його розкладанні вивільняється значна кількість тепла; дуже токсичний. Максимальна припустима концентрація в повітрі робочої зони дорівнює 0, 0001 мг/м 3. Знезаражуюча дія озону основана на високій окисній здатності, обумовлене легкістю віддачі ним активного атома кисню (О 3 = О 2+О). Озон окислює всі метали, крім золота, перетворюючи їх в окисли. У водному розчині озон дисоціює швидше, ніж у повітрі; дуже швидко дисоціює у слаболужних розчинах. У кислотних розчинах озон виявляє велику стійкість. У чистому сухому повітрі він розкладається дуже повільно. При обробці води озоном відбувається розкладання органічних речовин і знезараження води; бактерії гинуть у кілька тисяч разів швидше, ніж при обробці води хлором. Розчинність озону у воді залежить від р. Н і вмісту у воді розчинених речовин. Невеликий вміст кислот та нейтральних солей збільшує розчинність озону у воді. Присутність лугів знижує розчинність О 3. Дія озону в процесах окислення може відбуватися в трьох різних напрямках: безпосереднє окислення за участю одного атома кисню; приєднання цілої молекули озону до речовини, що окислюється, з утворенням озонідів; каталітичне посилення впливу кисню, присутнього в озонованому повітрі. Озон подають у стічну воду у вигляді озоно-повітряної або озоно-кисневої суміші. Концентрація озону у суміші - близько 3%. Для посилення процесу окислення суміш диспергують у стічній воді на дрібні пухирці газу. Озонування являє собою процес абсорбції, супроводжуваний хімічною реакцією в рідкій фазі.
атмосфери. При температурі -111, 9°С озон перетворюється в нестійку рідину темно-синього кольору. Чистий озон вибухонебезпечний, тому що при його розкладанні вивільняється значна кількість тепла; дуже токсичний. Максимальна припустима концентрація в повітрі робочої зони дорівнює 0, 0001 мг/м 3. Знезаражуюча дія озону основана на високій окисній здатності, обумовлене легкістю віддачі ним активного атома кисню (О 3 = О 2+О). Озон окислює всі метали, крім золота, перетворюючи їх в окисли. У водному розчині озон дисоціює швидше, ніж у повітрі; дуже швидко дисоціює у слаболужних розчинах. У кислотних розчинах озон виявляє велику стійкість. У чистому сухому повітрі він розкладається дуже повільно. При обробці води озоном відбувається розкладання органічних речовин і знезараження води; бактерії гинуть у кілька тисяч разів швидше, ніж при обробці води хлором. Розчинність озону у воді залежить від р. Н і вмісту у воді розчинених речовин. Невеликий вміст кислот та нейтральних солей збільшує розчинність озону у воді. Присутність лугів знижує розчинність О 3. Дія озону в процесах окислення може відбуватися в трьох різних напрямках: безпосереднє окислення за участю одного атома кисню; приєднання цілої молекули озону до речовини, що окислюється, з утворенням озонідів; каталітичне посилення впливу кисню, присутнього в озонованому повітрі. Озон подають у стічну воду у вигляді озоно-повітряної або озоно-кисневої суміші. Концентрація озону у суміші - близько 3%. Для посилення процесу окислення суміш диспергують у стічній воді на дрібні пухирці газу. Озонування являє собою процес абсорбції, супроводжуваний хімічною реакцією в рідкій фазі.
 Як окислювач при очищенні стічних вод може бути використаний перекис водню, що є безбарвною рідиною й у будь-яких співвідношеннях змішується з водою. Процес окислювання варто проводити в ємності при інтенсивному перемішуванні або в барботажному апараті. Перекисом водню легко розкладаються нітрити, альдегіди, феноли, сульфати. Знебарвлення стічних вод, що містять активні барвники, при р. Н 7 - 10 протікає з високою ефективністю. Присутність каталізаторів (солей Fe. SO 4і Cu. SO 4) прискорює процес знебарвлення в 8 - 10 разів. Перспективним є окислювання забруднень пероксосірчаними кислотами: пероксомоносірчаної H 2 SO 5 і пероксодисірчаної Н 2 S 2 О 8. Наприклад, фенол окислюється пероксомоносірчаною кислотою (кислота Каро) при р. Н 10. Цим методом можливо знизити вміст фенолу до 5*10 -6 %. Швидкість окислювання залежить від співвідношення H 2 SO 5/C 6 H 5 OH і підвищується з ростом температури. Руйнування ціанідів під дією пероксосірчаних кислот протікає також дуже швидко. При цьому, у випадку невеликих концентрацій ціанідів (0, 01 - 0, 05%) у стічній воді, використовують H 2 SO 5, а при високих концентраціях - Н 2 S 2 О 8. Оптимальним умовам відповідає р. Н 9. У нейтральному середовищі реакція окислювання різко сповільнюється під дією іонів заліза, які утворюють ферроціани, що не піддаються окисленню.
Як окислювач при очищенні стічних вод може бути використаний перекис водню, що є безбарвною рідиною й у будь-яких співвідношеннях змішується з водою. Процес окислювання варто проводити в ємності при інтенсивному перемішуванні або в барботажному апараті. Перекисом водню легко розкладаються нітрити, альдегіди, феноли, сульфати. Знебарвлення стічних вод, що містять активні барвники, при р. Н 7 - 10 протікає з високою ефективністю. Присутність каталізаторів (солей Fe. SO 4і Cu. SO 4) прискорює процес знебарвлення в 8 - 10 разів. Перспективним є окислювання забруднень пероксосірчаними кислотами: пероксомоносірчаної H 2 SO 5 і пероксодисірчаної Н 2 S 2 О 8. Наприклад, фенол окислюється пероксомоносірчаною кислотою (кислота Каро) при р. Н 10. Цим методом можливо знизити вміст фенолу до 5*10 -6 %. Швидкість окислювання залежить від співвідношення H 2 SO 5/C 6 H 5 OH і підвищується з ростом температури. Руйнування ціанідів під дією пероксосірчаних кислот протікає також дуже швидко. При цьому, у випадку невеликих концентрацій ціанідів (0, 01 - 0, 05%) у стічній воді, використовують H 2 SO 5, а при високих концентраціях - Н 2 S 2 О 8. Оптимальним умовам відповідає р. Н 9. У нейтральному середовищі реакція окислювання різко сповільнюється під дією іонів заліза, які утворюють ферроціани, що не піддаються окисленню.
 Кисень повітря використовують при очищенні води від заліза для окислення сполук двовалентного заліза в тривалентне з наступним відділенням від води гідроокису заліза. Реакція окислення у водному розчині протікає за схемою: 4 Fe 2+ + О 2 + 2 Н 2 О = 4 Fe 3+ + 4 OHFe 3++ + 3 H 2 O = Fe(OH)3 + 3 H+ Окислювання піролюзитом проводять фільтрацією стічної води через цей матеріал або в апаратах з мішалкою. Піролюзит є природним матеріалом, що складається в основному з двоокису марганцю. Він широко використовується для окислювання тривалентного миш'яку в пятивалентний: Н 3 Аs. О 3 + Мn. О 2 + Н 2 SО 4 = Н 3 Аs. О 4 + Мn. SО 4 + Н 2 О (2. 3)
Кисень повітря використовують при очищенні води від заліза для окислення сполук двовалентного заліза в тривалентне з наступним відділенням від води гідроокису заліза. Реакція окислення у водному розчині протікає за схемою: 4 Fe 2+ + О 2 + 2 Н 2 О = 4 Fe 3+ + 4 OHFe 3++ + 3 H 2 O = Fe(OH)3 + 3 H+ Окислювання піролюзитом проводять фільтрацією стічної води через цей матеріал або в апаратах з мішалкою. Піролюзит є природним матеріалом, що складається в основному з двоокису марганцю. Він широко використовується для окислювання тривалентного миш'яку в пятивалентний: Н 3 Аs. О 3 + Мn. О 2 + Н 2 SО 4 = Н 3 Аs. О 4 + Мn. SО 4 + Н 2 О (2. 3)
 Методи відновного очищення стічних вод застосовують у тих випадках, коли вони містять легко відновлювані речовини. Ці методи широко використовуються для видалення зі стічних вод сполук ртуті, хрому, миш'яку. Метод очищення стічних вод від речовин, що містять шестивалентний хром, заснований на відновленні його до тривалентного з наступним осадженням у вигляді гідроокису в лужному середовищі. У якості відновників можуть бути використані активне вугілля, сульфат закисного заліза, бісульфат натрію, водень, двоокис сірки, відходи органічних речовин (наприклад, газетний папір). На практиці для відновлення найбільше часто використовують розчини бісульфіту натрію: 4 Н 2 Сr. О 4 + 6 Na. HSO 3 + 3 Н 2 О > 2 Cr 2(SO 4)3 + 3 Na 2 SO 4 + 10 Н 2 О Реакція протікає швидко при р. Н 3 - 4 і надлишку сірчаної кислоти. Відновлення двоокисом сірки відбувається за реакціями SО 2 + H 2 О > H 2 SO 3 2 Сr. O 3 + H 2 SO 4 > Cr 2 (SO 4)3 + 3 H 2 O Найбільше швидко вони протікають при р. Н 2 - 2, 5. Цей процес є перспективним, тому що для відновлення можна використовувати гази, що містять SO 2. Відновлення можна провести в колонному апараті. Це дозволяє забезпечити очищення не тільки стічних вод від токсичних сполук хрому, але і газів, що утворюються, від SO 2.
Методи відновного очищення стічних вод застосовують у тих випадках, коли вони містять легко відновлювані речовини. Ці методи широко використовуються для видалення зі стічних вод сполук ртуті, хрому, миш'яку. Метод очищення стічних вод від речовин, що містять шестивалентний хром, заснований на відновленні його до тривалентного з наступним осадженням у вигляді гідроокису в лужному середовищі. У якості відновників можуть бути використані активне вугілля, сульфат закисного заліза, бісульфат натрію, водень, двоокис сірки, відходи органічних речовин (наприклад, газетний папір). На практиці для відновлення найбільше часто використовують розчини бісульфіту натрію: 4 Н 2 Сr. О 4 + 6 Na. HSO 3 + 3 Н 2 О > 2 Cr 2(SO 4)3 + 3 Na 2 SO 4 + 10 Н 2 О Реакція протікає швидко при р. Н 3 - 4 і надлишку сірчаної кислоти. Відновлення двоокисом сірки відбувається за реакціями SО 2 + H 2 О > H 2 SO 3 2 Сr. O 3 + H 2 SO 4 > Cr 2 (SO 4)3 + 3 H 2 O Найбільше швидко вони протікають при р. Н 2 - 2, 5. Цей процес є перспективним, тому що для відновлення можна використовувати гази, що містять SO 2. Відновлення можна провести в колонному апараті. Це дозволяє забезпечити очищення не тільки стічних вод від токсичних сполук хрому, але і газів, що утворюються, від SO 2.
 Електрохімічні методи Для очистки стічних вод від різноманітних розчинних і диспергованих речовин використовують процеси анодного окислення і катодного відновлення, електрокоагуляції, електрофлотації і електродіалізу. Всі ці процеси проходять при пропусканні через стічну воду постійного струму. Електрохімічні методи дозволяють вилучити із стічних вод цінні продукти при відносно простій автоматизації без використання хімічних реагентів. Основним недоліком цих методів є великі витрати електрики.
Електрохімічні методи Для очистки стічних вод від різноманітних розчинних і диспергованих речовин використовують процеси анодного окислення і катодного відновлення, електрокоагуляції, електрофлотації і електродіалізу. Всі ці процеси проходять при пропусканні через стічну воду постійного струму. Електрохімічні методи дозволяють вилучити із стічних вод цінні продукти при відносно простій автоматизації без використання хімічних реагентів. Основним недоліком цих методів є великі витрати електрики.
 Цей метод використовують для видалення з стічних вод розчинних домішок( ціанідів, амінів, спиртів, альдегдів, нітросполук, азосполук, сульфідів). У процесах електрохімічного окислення речовин, які містяться у стічних водах, вони повністю розкладаються з утворенням вуглекислого газу, аміаку і води. В якості анодів використовують різноманітні електролітично нерозчинні матеріали: графіт, магнетит, діоксид свинцю. Катоди виготовляють з молібдену, сплаву вольфраму з ферумом та нікелем, із графіту. Процес проводять в електролізерах з діафрагмою, в яких, крім основного процесів елуктрохімічного оккислення і відновлення, одночасно можуть протікати електрофлотація, електрофорез і електрокоагуляція.
Цей метод використовують для видалення з стічних вод розчинних домішок( ціанідів, амінів, спиртів, альдегдів, нітросполук, азосполук, сульфідів). У процесах електрохімічного окислення речовин, які містяться у стічних водах, вони повністю розкладаються з утворенням вуглекислого газу, аміаку і води. В якості анодів використовують різноманітні електролітично нерозчинні матеріали: графіт, магнетит, діоксид свинцю. Катоди виготовляють з молібдену, сплаву вольфраму з ферумом та нікелем, із графіту. Процес проводять в електролізерах з діафрагмою, в яких, крім основного процесів елуктрохімічного оккислення і відновлення, одночасно можуть протікати електрофлотація, електрофорез і електрокоагуляція.
 Біохімічні методи Ці методи використовують для очистки господарськопобутових і промислових стічних вод від розчинів органічних і неорганічних (сірководень, сульфіди, нітрити тощо) речовин. Процес очистки базується на здатності мікроорганізмів використовувати речовинизабруднювачі для харчування в процесі своєї життєдіяльності – органічні речовини для мікроорганізмів є джерелом карбону.
Біохімічні методи Ці методи використовують для очистки господарськопобутових і промислових стічних вод від розчинів органічних і неорганічних (сірководень, сульфіди, нітрити тощо) речовин. Процес очистки базується на здатності мікроорганізмів використовувати речовинизабруднювачі для харчування в процесі своєї життєдіяльності – органічні речовини для мікроорганізмів є джерелом карбону.
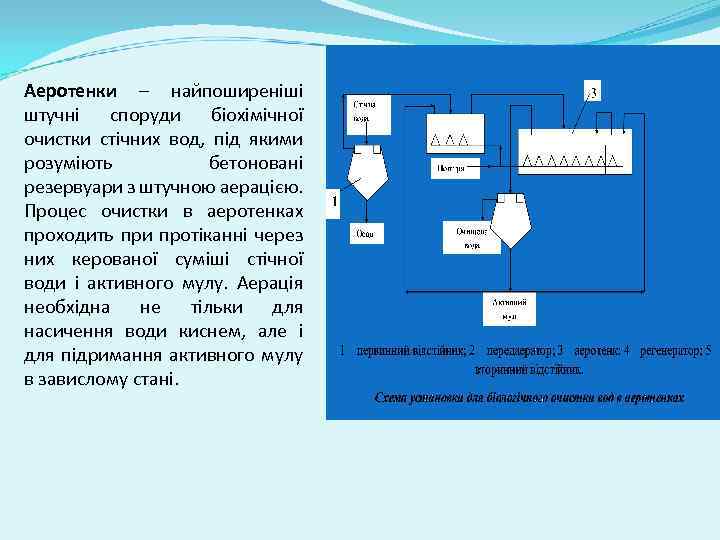 Аеротенки – найпоширеніші штучні споруди біохімічної очистки стічних вод, під якими розуміють бетоновані резервуари з штучною аерацією. Процес очистки в аеротенках проходить при протіканні через них керованої суміші стічної води і активного мулу. Аерація необхідна не тільки для насичення води киснем, але і для підримання активного мулу в завислому стані.
Аеротенки – найпоширеніші штучні споруди біохімічної очистки стічних вод, під якими розуміють бетоновані резервуари з штучною аерацією. Процес очистки в аеротенках проходить при протіканні через них керованої суміші стічної води і активного мулу. Аерація необхідна не тільки для насичення води киснем, але і для підримання активного мулу в завислому стані.

 Біофільтри – це споруди, в корпусі яких розташована кускована насадка (загрузка) і перебачені розподільчі пристрої для стічної води і повітря. У біофільтрах стічна вода фільтрується через шар завантаження, який вкритий плівкою (біоплівкою) мікроорганізмів, Які окислюють органічні речовини, використовують їх як джерело живлення та енергії. Як загрузка використовуються різні матеріали з високою пористістю, малою густиною і великою питомою поверхнею (щебінь, гравій, керамзит та ін. )
Біофільтри – це споруди, в корпусі яких розташована кускована насадка (загрузка) і перебачені розподільчі пристрої для стічної води і повітря. У біофільтрах стічна вода фільтрується через шар завантаження, який вкритий плівкою (біоплівкою) мікроорганізмів, Які окислюють органічні речовини, використовують їх як джерело живлення та енергії. Як загрузка використовуються різні матеріали з високою пористістю, малою густиною і великою питомою поверхнею (щебінь, гравій, керамзит та ін. )

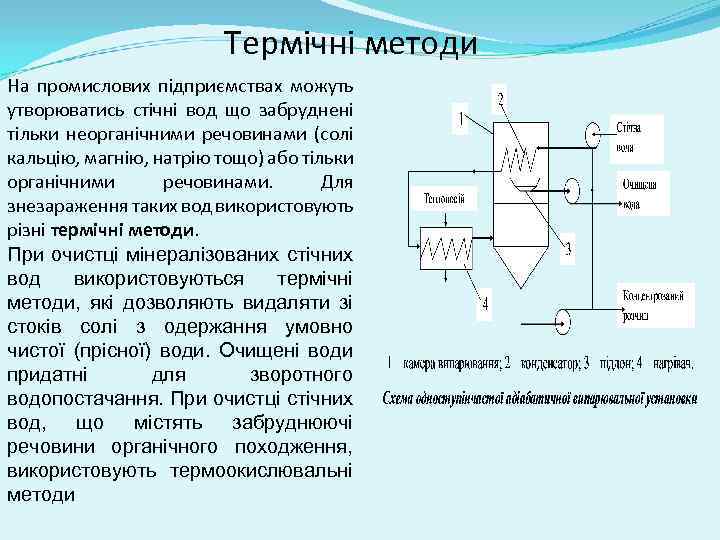 Термічні методи На промислових підприємствах можуть утворюватись стічні вод що забруднені тільки неорганічними речовинами (солі кальцію, магнію, натрію тощо) або тільки органічними речовинами. Для знезараження таких вод використовують різні термічні методи. При очистці мінералізованих стічних вод використовуються термічні методи, які дозволяють видаляти зі стоків солі з одержання умовно чистої (прісної) води. Очищені води придатні для зворотного водопостачання. При очистці стічних вод, що містять забруднюючі речовини органічного походження, використовують термоокислювальні методи
Термічні методи На промислових підприємствах можуть утворюватись стічні вод що забруднені тільки неорганічними речовинами (солі кальцію, магнію, натрію тощо) або тільки органічними речовинами. Для знезараження таких вод використовують різні термічні методи. При очистці мінералізованих стічних вод використовуються термічні методи, які дозволяють видаляти зі стоків солі з одержання умовно чистої (прісної) води. Очищені води придатні для зворотного водопостачання. При очистці стічних вод, що містять забруднюючі речовини органічного походження, використовують термоокислювальні методи
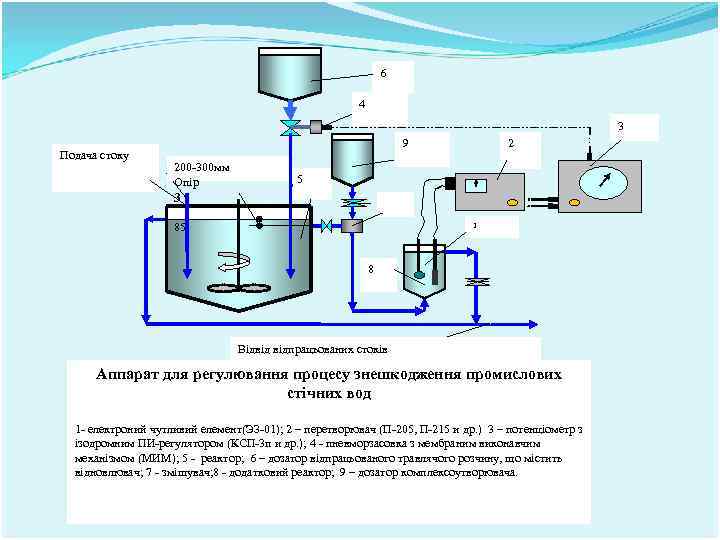 6 4 3 Подача стоку 9 200 -300 мм Опір 2 5 3 1 85 8 Відвід відпрацьованих стоків Аппарат для регулювання процесу знешкодження промислових стічних вод 1 - електроний чутливий елемент(ЭЗ-01); 2 – перетворювач (П-205, П-215 и др. ) 3 – потенціометр з ізодромним ПИ-регулятором (КСП-3 п и др. ); 4 - пневморзасовка з мембраним виконавчим механізмом (МИМ); 5 - реактор; 6 – дозатор відпрацьованого травлячого розчину, що містить відновлювач; 7 - змішувач; 8 - додатковий реактор; 9 – дозатор комплексоутворювача.
6 4 3 Подача стоку 9 200 -300 мм Опір 2 5 3 1 85 8 Відвід відпрацьованих стоків Аппарат для регулювання процесу знешкодження промислових стічних вод 1 - електроний чутливий елемент(ЭЗ-01); 2 – перетворювач (П-205, П-215 и др. ) 3 – потенціометр з ізодромним ПИ-регулятором (КСП-3 п и др. ); 4 - пневморзасовка з мембраним виконавчим механізмом (МИМ); 5 - реактор; 6 – дозатор відпрацьованого травлячого розчину, що містить відновлювач; 7 - змішувач; 8 - додатковий реактор; 9 – дозатор комплексоутворювача.
 Сьогодні на Землі практично не залишилось місць, де б можна було знайти чисту природну воду, придатну для вживання. Гірські людовики, деякі підземні озера, джерела, Байкал, Антарктида і Арктика - ось, і все можливе. Що із цього доступне сучасному міскому жителю? Великі ріки зіпсовані промисловими стоками, дощова вода містить розтворені газоподібні викиди, вода із лісового озера чи річки містить велику кількість органіки. Вчені вважають, що питтєва вода хорошої якості збільшила б середню тривалість життя сучасної людини на 20 -25 років! Все більше людей в Україні розуміють це і тому не вживають в їжу воду з крану, а купляють фільтри для води, або користуються купленою водою.
Сьогодні на Землі практично не залишилось місць, де б можна було знайти чисту природну воду, придатну для вживання. Гірські людовики, деякі підземні озера, джерела, Байкал, Антарктида і Арктика - ось, і все можливе. Що із цього доступне сучасному міскому жителю? Великі ріки зіпсовані промисловими стоками, дощова вода містить розтворені газоподібні викиди, вода із лісового озера чи річки містить велику кількість органіки. Вчені вважають, що питтєва вода хорошої якості збільшила б середню тривалість життя сучасної людини на 20 -25 років! Все більше людей в Україні розуміють це і тому не вживають в їжу воду з крану, а купляють фільтри для води, або користуються купленою водою.



