Lektsia_65.ppt
- Количество слайдов: 34
 МЕТОД КВАЗИСТАЦИОНАРНЫХ КОНЦЕНТРАЦИЙ. ВЛИЯНИЕ ТЕМПЕРАТУРЫ НА СКОРОСТЬ ХИМИЧЕСКОЙ РЕАКЦИИ Лекция 5
МЕТОД КВАЗИСТАЦИОНАРНЫХ КОНЦЕНТРАЦИЙ. ВЛИЯНИЕ ТЕМПЕРАТУРЫ НА СКОРОСТЬ ХИМИЧЕСКОЙ РЕАКЦИИ Лекция 5
 Стационарное и квазистационарное состояние n n n Стационарность - постоянство концентрации промежуточного вещества во времени В стационарном состоянии скорости образования и расходования промежуточного вещества равны Строго это означает равенство нулю производной концентрации промежуточного соединения по времени. d. B/dt≈0 При этом сама по себе концентрация промежуточного вещества, как и исходного, может меняться. Такое состояние принято называть квазистационарным Это условие выполняется только в точке максимума
Стационарное и квазистационарное состояние n n n Стационарность - постоянство концентрации промежуточного вещества во времени В стационарном состоянии скорости образования и расходования промежуточного вещества равны Строго это означает равенство нулю производной концентрации промежуточного соединения по времени. d. B/dt≈0 При этом сама по себе концентрация промежуточного вещества, как и исходного, может меняться. Такое состояние принято называть квазистационарным Это условие выполняется только в точке максимума
 Скорость получения продукта в условиях стационарности n Рассмотрим поведение концентрации промежуточного вещества в процессе n При этом из условия следует, что скорость получения продукта
Скорость получения продукта в условиях стационарности n Рассмотрим поведение концентрации промежуточного вещества в процессе n При этом из условия следует, что скорость получения продукта
 Отношение скоростей превращения и образования промежуточного вещества В n введем параметр D, равный отношению скоростей превращения и образования вещества В. При равенстве скоростей первой и второй реакций он равен 1.
Отношение скоростей превращения и образования промежуточного вещества В n введем параметр D, равный отношению скоростей превращения и образования вещества В. При равенстве скоростей первой и второй реакций он равен 1.
 Выполнение условия D = 1 n для того, чтобы величина D стремилась к единице, значение k 2 должно быть больше k 1. При таком условии и достаточно больших значениях t экспонента стремится к нулю и
Выполнение условия D = 1 n для того, чтобы величина D стремилась к единице, значение k 2 должно быть больше k 1. При таком условии и достаточно больших значениях t экспонента стремится к нулю и
 Идеальные случаи применения метода квазистационарности Рассмотрим последовательные химические реакции A В Z. n Пусть промежуточное вещество В обладает высокой химической активностью. n Тогда, как только вещество В образуется в реакции A В, оно сразу же будет вступать в реакцию В Z и расходоваться. При этом скорость реакции образования вещества В будет равна скорости расходования n
Идеальные случаи применения метода квазистационарности Рассмотрим последовательные химические реакции A В Z. n Пусть промежуточное вещество В обладает высокой химической активностью. n Тогда, как только вещество В образуется в реакции A В, оно сразу же будет вступать в реакцию В Z и расходоваться. При этом скорость реакции образования вещества В будет равна скорости расходования n
 Упрощение решения уравнений n n n n При этом скорость реакции образования вещества В будет равна скорости расходования, k 1[A] = k 2[B]. [B] = k 1/k 2[A] d[B]/dt = 0 Если концентрация А известна, выражение (2) позволяет вычислить концентрацию В без решения дифференциальных уравнений, что значительно упрощает расчеты. Необходимо помнить, что вышеприведенные рассуждения являются нестрогими и требуют количественной проверки Высокая химическая активность вещества В означает, что константы скорости реакций с его участием велики, т. е. k 2 >> k 1
Упрощение решения уравнений n n n n При этом скорость реакции образования вещества В будет равна скорости расходования, k 1[A] = k 2[B]. [B] = k 1/k 2[A] d[B]/dt = 0 Если концентрация А известна, выражение (2) позволяет вычислить концентрацию В без решения дифференциальных уравнений, что значительно упрощает расчеты. Необходимо помнить, что вышеприведенные рассуждения являются нестрогими и требуют количественной проверки Высокая химическая активность вещества В означает, что константы скорости реакций с его участием велики, т. е. k 2 >> k 1
![Зависимость концентрации промежуточного вещества от времени. [A]0 = 1 М, [B]0 = 0, [Z]0 Зависимость концентрации промежуточного вещества от времени. [A]0 = 1 М, [B]0 = 0, [Z]0](https://present5.com/presentation/116048518_223139583/image-8.jpg) Зависимость концентрации промежуточного вещества от времени. [A]0 = 1 М, [B]0 = 0, [Z]0 = 0.
Зависимость концентрации промежуточного вещества от времени. [A]0 = 1 М, [B]0 = 0, [Z]0 = 0.
 Влияние точности анализа на соотношение констант n n При точности анализа в 5% должно выполняться отношение k 2 /k 1 = 20, При точности 1% - 100. При таком соотношении после достижения максимума концентрация В будет меняться, но, в максимуме она не превышает точности анализа, и практически мы не будем отмечать ее изменения. При больших значениях k 2 показатель степени примерно равен (– 1) и относительная концентрация промежуточного продукта равна отношению k 1/ k 2.
Влияние точности анализа на соотношение констант n n При точности анализа в 5% должно выполняться отношение k 2 /k 1 = 20, При точности 1% - 100. При таком соотношении после достижения максимума концентрация В будет меняться, но, в максимуме она не превышает точности анализа, и практически мы не будем отмечать ее изменения. При больших значениях k 2 показатель степени примерно равен (– 1) и относительная концентрация промежуточного продукта равна отношению k 1/ k 2.
![Условие квазистационарности при [B] ≠ 0. n n При больших значениях времени экспонента стремится Условие квазистационарности при [B] ≠ 0. n n При больших значениях времени экспонента стремится](https://present5.com/presentation/116048518_223139583/image-10.jpg) Условие квазистационарности при [B] ≠ 0. n n При больших значениях времени экспонента стремится к нулю, и квазистационарность будет наблюдаться при k 2 >> k 1. При малых значениях времени значение экспоненты близко к единице.
Условие квазистационарности при [B] ≠ 0. n n При больших значениях времени экспонента стремится к нулю, и квазистационарность будет наблюдаться при k 2 >> k 1. При малых значениях времени значение экспоненты близко к единице.
 ЗАПИСЬ ДИФФЕРЕНЦИАЛЬНЫХ УРАВНЕНИЙ ХИМИЧЕСКОЙ КИНЕТИКИ Предлагается следующий механизм термического распада озона. n O 3 + M → O + O 2 + M (1) n O + O 2 + M → O 3 + M (2) n O + O 3 → 2 O 2 (3) n
ЗАПИСЬ ДИФФЕРЕНЦИАЛЬНЫХ УРАВНЕНИЙ ХИМИЧЕСКОЙ КИНЕТИКИ Предлагается следующий механизм термического распада озона. n O 3 + M → O + O 2 + M (1) n O + O 2 + M → O 3 + M (2) n O + O 3 → 2 O 2 (3) n
 Применение закона действующих масс Запишем выражения для скорости всех стадий реакций, согласно основному постулату химической кинетики n w 1 = k 1[O 3][M], n w 2 = k 2[O][O 2][M], n w 3 = k 3[O][O 3]. n
Применение закона действующих масс Запишем выражения для скорости всех стадий реакций, согласно основному постулату химической кинетики n w 1 = k 1[O 3][M], n w 2 = k 2[O][O 2][M], n w 3 = k 3[O][O 3]. n
 Скорости образования и расходования участников реакции n n n Затем составим дифференциальные уравнения. Озон расходуется в первой и третьей реакции и образуется во второй d[O 3]/dt = – w 1 + w 2 – w 3 Атом кислорода образуется в первой реакции и расходуется во второй и третьей d[O]/dt = w 1 – w 2 –w 3 Молекулярный кислород образуется в первой и третьей реакциях и расходуется во второй, d[О 2]/dt = w 1 – w 2 + 2 w 3
Скорости образования и расходования участников реакции n n n Затем составим дифференциальные уравнения. Озон расходуется в первой и третьей реакции и образуется во второй d[O 3]/dt = – w 1 + w 2 – w 3 Атом кислорода образуется в первой реакции и расходуется во второй и третьей d[O]/dt = w 1 – w 2 –w 3 Молекулярный кислород образуется в первой и третьей реакциях и расходуется во второй, d[О 2]/dt = w 1 – w 2 + 2 w 3
 Конечные уравнения скоростей превращения n Подставляя выражения скорости реакций через концентрации реагентов согласно закону действующих масс, получаем n d[O 3]/dt = – k 1[O 3][M] + k 2[O][O 2][M] – k 3[O][O 3], d[O]/dt = k 1[O 3][M] – k 2[O][O 2][M] – k 3[O][O 3], d[О 2]/dt = k 1[O 3][M] – k 2[O][O 2][M] + 2 k 3[O][O 3]. n n
Конечные уравнения скоростей превращения n Подставляя выражения скорости реакций через концентрации реагентов согласно закону действующих масс, получаем n d[O 3]/dt = – k 1[O 3][M] + k 2[O][O 2][M] – k 3[O][O 3], d[O]/dt = k 1[O 3][M] – k 2[O][O 2][M] – k 3[O][O 3], d[О 2]/dt = k 1[O 3][M] – k 2[O][O 2][M] + 2 k 3[O][O 3]. n n
![Нахождение концентрации промежуточного вещества n d[O]/dt = k 1[O 3][M] – k 2[O][O 2][M] Нахождение концентрации промежуточного вещества n d[O]/dt = k 1[O 3][M] – k 2[O][O 2][M]](https://present5.com/presentation/116048518_223139583/image-15.jpg) Нахождение концентрации промежуточного вещества n d[O]/dt = k 1[O 3][M] – k 2[O][O 2][M] – k 3[O][O 3] ≈0 n [O] = k 1[O 3][M] / (k 2[O 2][M] + k 3[O 3] ) n [M] – постоянная n [ O] = k 1[O 3] / (k 2[O 2] + k 3[O 3] )
Нахождение концентрации промежуточного вещества n d[O]/dt = k 1[O 3][M] – k 2[O][O 2][M] – k 3[O][O 3] ≈0 n [O] = k 1[O 3][M] / (k 2[O 2][M] + k 3[O 3] ) n [M] – постоянная n [ O] = k 1[O 3] / (k 2[O 2] + k 3[O 3] )
 Правило Вант - Гоффа n n n скорость ( константа скорости) увеличивается с ростом температуры не линейно. при увеличении температуры на 10 о. С скорость (константа скорости) увеличивается в 2 4 раза правило выполнимо лишь для небольшого числа реакций и в интервале температур вблизи комнатной
Правило Вант - Гоффа n n n скорость ( константа скорости) увеличивается с ростом температуры не линейно. при увеличении температуры на 10 о. С скорость (константа скорости) увеличивается в 2 4 раза правило выполнимо лишь для небольшого числа реакций и в интервале температур вблизи комнатной
 Температурный коэффициент n γ - температурный коэффициент скорости реакции
Температурный коэффициент n γ - температурный коэффициент скорости реакции
 Температурная активация химическое взаимодействие происходит при соударениях частиц, n рост константы может быть связан с увеличением числа соударений с ростом температуры за счет увеличения скорости движения частиц. Экспериментально установлено, что скорость увеличивается пропорционально T 1/2 n
Температурная активация химическое взаимодействие происходит при соударениях частиц, n рост константы может быть связан с увеличением числа соударений с ростом температуры за счет увеличения скорости движения частиц. Экспериментально установлено, что скорость увеличивается пропорционально T 1/2 n
 Уравнение Аррениуса где А – предэкспоненциальный множитель (его размерность совпадает с размерностью константы скорости), Еа – энергия активации (Дж/моль), R –универсальная газовая постоянная (R = 8, 31441 Дж/моль⋅К), Т – абсолютная температура (К). Чтобы полностью определить температурную зависимость константы скорости по формуле Аррениуса, требуются две величины – А и Еа.
Уравнение Аррениуса где А – предэкспоненциальный множитель (его размерность совпадает с размерностью константы скорости), Еа – энергия активации (Дж/моль), R –универсальная газовая постоянная (R = 8, 31441 Дж/моль⋅К), Т – абсолютная температура (К). Чтобы полностью определить температурную зависимость константы скорости по формуле Аррениуса, требуются две величины – А и Еа.
 Логарифмическая форма уравнения Аррениуса • откуда следует, что логарифм константы скорости является линейной функцией обратной температуры 1/Т
Логарифмическая форма уравнения Аррениуса • откуда следует, что логарифм константы скорости является линейной функцией обратной температуры 1/Т
 Дифференциальная форма уравнения Аррениуса • или
Дифференциальная форма уравнения Аррениуса • или
 Условия активации и определение энергии активации n n При сближении молекул на расстояния меньшие, чем равновесное (это требуется для их перестройки), будут действовать силы отталкивания. Само химическое превращение требует разрыва связей в молекуле. Для этого энергия реагирующей молекулы должна быть больше средней равновесной при заданной температуре. Энергией активации называют избыток энергии по сравнению со средней энергией молекул при данной температуре, необходимый для того, чтобы химическая реакция произошла. Величина ее определяется свойствами реагирующих частиц, их энергетическим состоянием.
Условия активации и определение энергии активации n n При сближении молекул на расстояния меньшие, чем равновесное (это требуется для их перестройки), будут действовать силы отталкивания. Само химическое превращение требует разрыва связей в молекуле. Для этого энергия реагирующей молекулы должна быть больше средней равновесной при заданной температуре. Энергией активации называют избыток энергии по сравнению со средней энергией молекул при данной температуре, необходимый для того, чтобы химическая реакция произошла. Величина ее определяется свойствами реагирующих частиц, их энергетическим состоянием.
 Промежуточное состояние n n A + B ↔ AB* →ΣP. АВ* означает промежуточное состояние, обладающее энергией равной или большей, чем необходимо для превращения. на первой стадии устанавливается равновесие, концентрация активных частиц полагается малой, (частиц с энергией большей, чем статистически равновесной, должно быть мало, и поэтому их превращение не влияет на равновесие), скорость распада активных частиц (т. е. и константа скорости) не зависит от температуры.
Промежуточное состояние n n A + B ↔ AB* →ΣP. АВ* означает промежуточное состояние, обладающее энергией равной или большей, чем необходимо для превращения. на первой стадии устанавливается равновесие, концентрация активных частиц полагается малой, (частиц с энергией большей, чем статистически равновесной, должно быть мало, и поэтому их превращение не влияет на равновесие), скорость распада активных частиц (т. е. и константа скорости) не зависит от температуры.
 Скорость реакции в условиях термической активации скорость реакции можно выразить как , n W = k′[AB∗], n где k' – константа скорости распада активных частиц. n Концентрацию AB∗ можно выразить через константу равновесия, Kc: [AB∗ ]= Kc[A][B]. Обозначим величину k′Kc как k. Тогда W =k[A][B].
Скорость реакции в условиях термической активации скорость реакции можно выразить как , n W = k′[AB∗], n где k' – константа скорости распада активных частиц. n Концентрацию AB∗ можно выразить через константу равновесия, Kc: [AB∗ ]= Kc[A][B]. Обозначим величину k′Kc как k. Тогда W =k[A][B].
 Термическая активация n n Термическая активация включает не только увеличение энергии столкновения молекул, но и возрастание их вращательной и колебательной (а при высоких температурах и электронной) энергии. Протекание некоторых реакций (реакции распада) можно упрощенно представить как увеличение амплитуды колебаний одной из связей, приводящее к её разрыву
Термическая активация n n Термическая активация включает не только увеличение энергии столкновения молекул, но и возрастание их вращательной и колебательной (а при высоких температурах и электронной) энергии. Протекание некоторых реакций (реакции распада) можно упрощенно представить как увеличение амплитуды колебаний одной из связей, приводящее к её разрыву
 Изменение внутренней энергии. Теплота активации n Т. к. k‘ (скорость распада активных частиц) не зависит от температуры, то : ΔU соответствует изменению внутренней энергии при образовании активной частицы, т. е. E имеет смысл энергии активации (иногда ее называют теплотой активации, т. к. это термодинамическая величина при определенной температуре)
Изменение внутренней энергии. Теплота активации n Т. к. k‘ (скорость распада активных частиц) не зависит от температуры, то : ΔU соответствует изменению внутренней энергии при образовании активной частицы, т. е. E имеет смысл энергии активации (иногда ее называют теплотой активации, т. к. это термодинамическая величина при определенной температуре)
 Ограничения действия уравнения Аррениуса n n уравнение справедливо для значительных величин энергии активации, поскольку активных частиц должно быть мало. это выполнимо для частиц с большой энергией. увеличение в 2 - 4 раза константы скорости при увеличении температуры на 10 o. C возможно лишь в определенном интервале значений энергии активации и небольшом изменении температуры. Например, начальная температура 298 K и Е = 51 – 90 к. Дж/моль.
Ограничения действия уравнения Аррениуса n n уравнение справедливо для значительных величин энергии активации, поскольку активных частиц должно быть мало. это выполнимо для частиц с большой энергией. увеличение в 2 - 4 раза константы скорости при увеличении температуры на 10 o. C возможно лишь в определенном интервале значений энергии активации и небольшом изменении температуры. Например, начальная температура 298 K и Е = 51 – 90 к. Дж/моль.
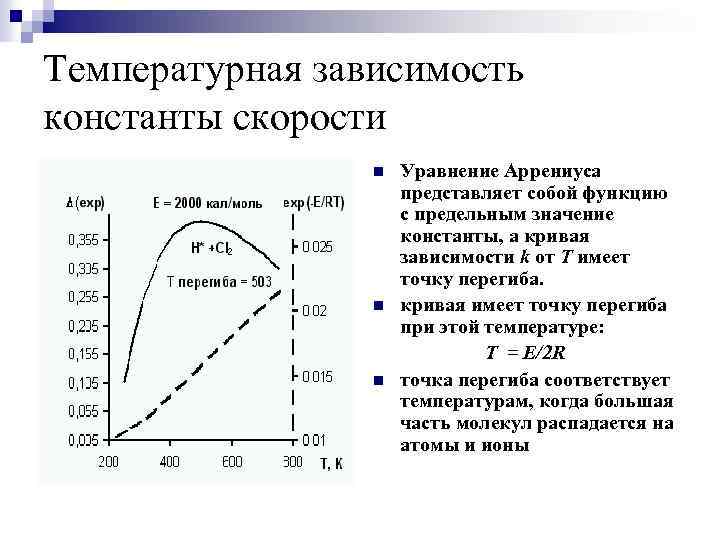 Температурная зависимость константы скорости n n n Уравнение Аррениуса представляет собой функцию с предельным значение константы, а кривая зависимости k от Т имеет точку перегиба. кривая имеет точку перегиба при этой температуре: T = E/2 R точка перегиба соответствует температурам, когда большая часть молекул распадается на атомы и ионы
Температурная зависимость константы скорости n n n Уравнение Аррениуса представляет собой функцию с предельным значение константы, а кривая зависимости k от Т имеет точку перегиба. кривая имеет точку перегиба при этой температуре: T = E/2 R точка перегиба соответствует температурам, когда большая часть молекул распадается на атомы и ионы
 Расчет энергии активации n Пусть нам известны значения констант скорости k 1 и k 2 при минимум двух температурах Т 1 и Т 2. Для обеих температур выполняется формула Аррениуса, т. е Константы скорости реакций с участием ионов в растворах зависят ещё от ионной силы раствора
Расчет энергии активации n Пусть нам известны значения констант скорости k 1 и k 2 при минимум двух температурах Т 1 и Т 2. Для обеих температур выполняется формула Аррениуса, т. е Константы скорости реакций с участием ионов в растворах зависят ещё от ионной силы раствора
 Вычисление предэкспонициального множителя n Предэкспоненциальный множитель вычисляем из формулы подставив в неё соответствующие значения константы и температуры (например, k 1 и Т 1), и рассчитанную энергию активации
Вычисление предэкспонициального множителя n Предэкспоненциальный множитель вычисляем из формулы подставив в неё соответствующие значения константы и температуры (например, k 1 и Т 1), и рассчитанную энергию активации
 Графическое определение энергии активации n n n Если нам известны значения константы скорости при более чем двух температурах, для определения энергии активации и предэкспоненциального множителя можно нанести значения (k, Т) на график в координатах lnk – 1/T, и провести через них прямую линию тангенс угла наклона этой линии будет равен – Ea/R, а точка пересечения прямой линии с осью ординат даст значение ln. A.
Графическое определение энергии активации n n n Если нам известны значения константы скорости при более чем двух температурах, для определения энергии активации и предэкспоненциального множителя можно нанести значения (k, Т) на график в координатах lnk – 1/T, и провести через них прямую линию тангенс угла наклона этой линии будет равен – Ea/R, а точка пересечения прямой линии с осью ординат даст значение ln. A.
 РСЧЕТ ПАРАМЕТРОВ ТЕМПЕРАТУРНОЙ ЗАВИСИМОСТИ КОНСТАНТЫ СКОРОСТИ ХИМИЧЕСКОЙ РЕАКЦИИ
РСЧЕТ ПАРАМЕТРОВ ТЕМПЕРАТУРНОЙ ЗАВИСИМОСТИ КОНСТАНТЫ СКОРОСТИ ХИМИЧЕСКОЙ РЕАКЦИИ
 Решение. Нахождение эффективной энергии активации по 2 температурам
Решение. Нахождение эффективной энергии активации по 2 температурам
 Контрольные вопросы Какие реакции относятся к сложным? n В чем заключается принцип независимости n Записать кинетическое уравнение для обратимых реакций 1 -го порядка n Что такое порядок реакции n Как графически определить 1/К 1 по кинетическим кривым? n
Контрольные вопросы Какие реакции относятся к сложным? n В чем заключается принцип независимости n Записать кинетическое уравнение для обратимых реакций 1 -го порядка n Что такое порядок реакции n Как графически определить 1/К 1 по кинетическим кривым? n


