гель-электрофорез.ppt
- Количество слайдов: 33
 Метод гель-электрофореза
Метод гель-электрофореза
 Назначение метода и принцип его действия. Гель-электрофорез – аналитический метод для разделения и анализа макромолекул (нуклеиновых кислот и белков) размером от 20 до 2000 к. Да. Гель-электрофорез – стандартный метод, используемый для разделения, идентификации и очистки фрагментов ДНК.
Назначение метода и принцип его действия. Гель-электрофорез – аналитический метод для разделения и анализа макромолекул (нуклеиновых кислот и белков) размером от 20 до 2000 к. Да. Гель-электрофорез – стандартный метод, используемый для разделения, идентификации и очистки фрагментов ДНК.
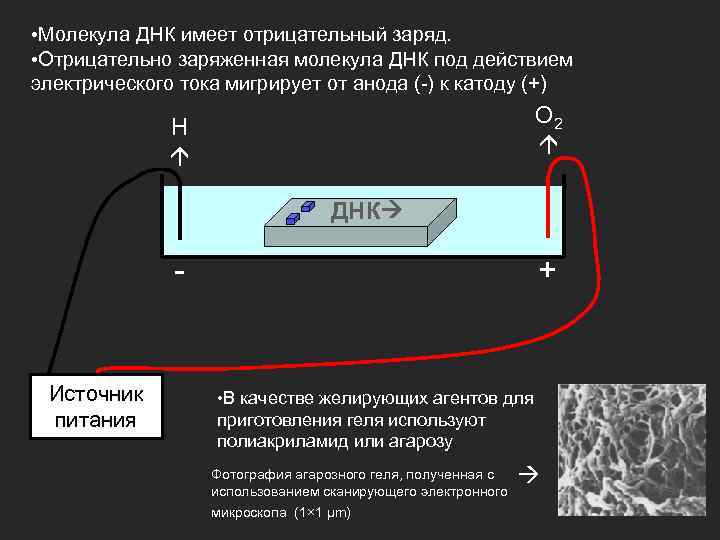 • Молекула ДНК имеет отрицательный заряд. • Отрицательно заряженная молекула ДНК под действием электрического тока мигрирует от анода (-) к катоду (+) O 2 H ДНК - Источник питания + • В качестве желирующих агентов для приготовления геля используют полиакриламид или агарозу Фотография агарозного геля, полученная с использованием сканирующего электронного микроскопа (1× 1 µm)
• Молекула ДНК имеет отрицательный заряд. • Отрицательно заряженная молекула ДНК под действием электрического тока мигрирует от анода (-) к катоду (+) O 2 H ДНК - Источник питания + • В качестве желирующих агентов для приготовления геля используют полиакриламид или агарозу Фотография агарозного геля, полученная с использованием сканирующего электронного микроскопа (1× 1 µm)
 Выбор желирующего агента До 500 pb – полиакриламид (ПАА) позволяет разделить фрагменты ДНК, размер которых различается даже на один нуклеотид. > 500 pb – агароза
Выбор желирующего агента До 500 pb – полиакриламид (ПАА) позволяет разделить фрагменты ДНК, размер которых различается даже на один нуклеотид. > 500 pb – агароза
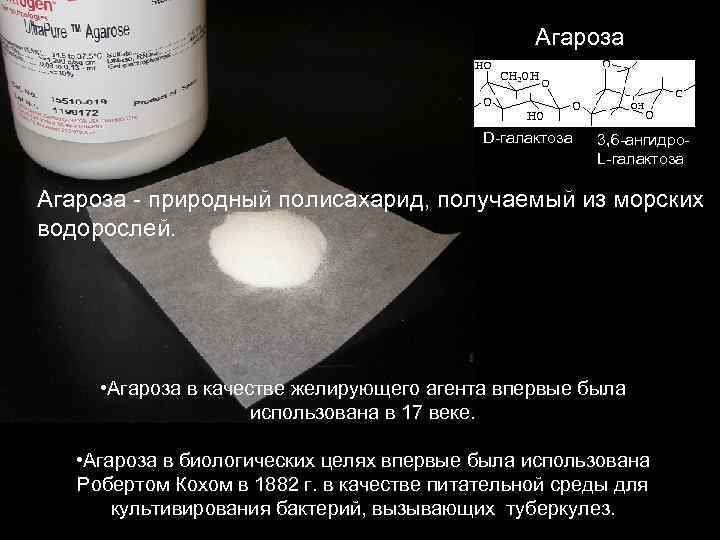 Aгароза D-галактоза 3, 6 -ангидро. L-галактоза Агароза - природный полисахарид, получаемый из морских водорослей. • Агароза в качестве желирующего агента впервые была использована в 17 веке. • Aгароза в биологических целях впервые была использована Робертом Кохом в 1882 г. в качестве питательной среды для культивирования бактерий, вызывающих туберкулез.
Aгароза D-галактоза 3, 6 -ангидро. L-галактоза Агароза - природный полисахарид, получаемый из морских водорослей. • Агароза в качестве желирующего агента впервые была использована в 17 веке. • Aгароза в биологических целях впервые была использована Робертом Кохом в 1882 г. в качестве питательной среды для культивирования бактерий, вызывающих туберкулез.
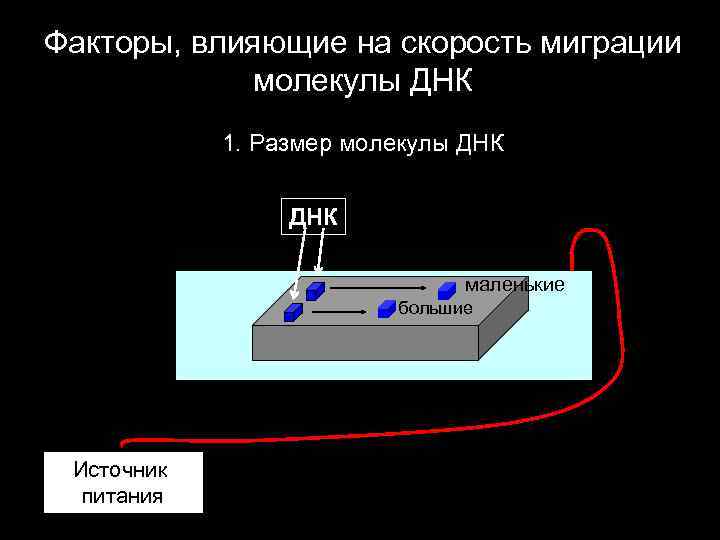 Факторы, влияющие на скорость миграции молекулы ДНК 1. Размер молекулы ДНК маленькие большие - Источник питания +
Факторы, влияющие на скорость миграции молекулы ДНК 1. Размер молекулы ДНК маленькие большие - Источник питания +
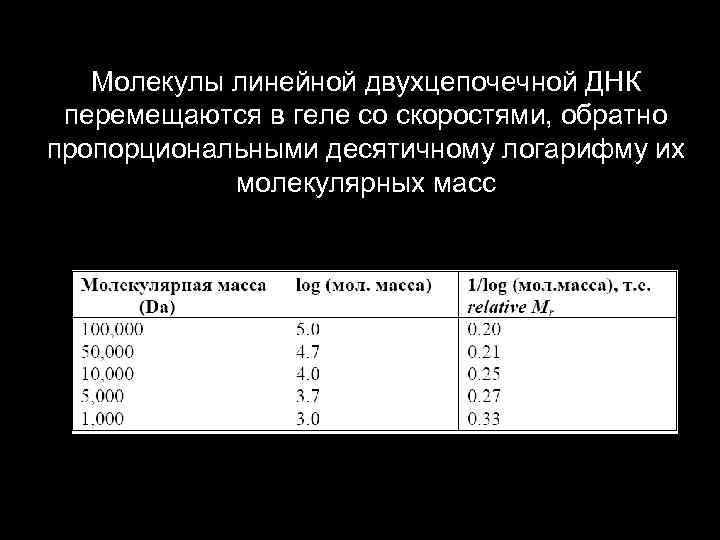 Молекулы линейной двухцепочечной ДНК перемещаются в геле со скоростями, обратно пропорциональными десятичному логарифму их молекулярных масс
Молекулы линейной двухцепочечной ДНК перемещаются в геле со скоростями, обратно пропорциональными десятичному логарифму их молекулярных масс
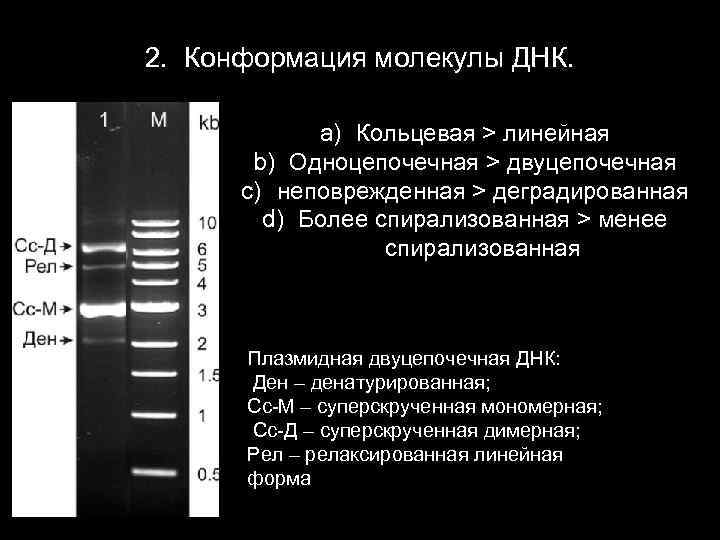 2. Конформация молекулы ДНК. a) Кольцевая > линейная b) Одноцепочечная > двуцепочечная c) неповрежденная > деградированная d) Более спирализованная > менее спирализованная Плазмидная двуцепочечная ДНК: Ден – денатурированная; Сс-М – суперскрученная мономерная; Сс-Д – суперскрученная димерная; Рел – релаксированная линейная форма
2. Конформация молекулы ДНК. a) Кольцевая > линейная b) Одноцепочечная > двуцепочечная c) неповрежденная > деградированная d) Более спирализованная > менее спирализованная Плазмидная двуцепочечная ДНК: Ден – денатурированная; Сс-М – суперскрученная мономерная; Сс-Д – суперскрученная димерная; Рел – релаксированная линейная форма
 3. Концентрация агарозы. ЗАВИСИМОСТЬ КОНЦЕНТРАЦИИ АГАРОЗНОГО ГЕЛЯ ОТ РАЗМЕРА МОЛЕКУЛЫ ДНК 4. Напряженность электрического поля.
3. Концентрация агарозы. ЗАВИСИМОСТЬ КОНЦЕНТРАЦИИ АГАРОЗНОГО ГЕЛЯ ОТ РАЗМЕРА МОЛЕКУЛЫ ДНК 4. Напряженность электрического поля.
 Приготовление агарозного геля
Приготовление агарозного геля
 Буфер Для приготовления агарозного геля требуется желирующий агент (агароза) и буферный раствор. Колба Агароза
Буфер Для приготовления агарозного геля требуется желирующий агент (агароза) и буферный раствор. Колба Агароза
 Оборудования для проведения Гель-электрофореза Источник питания Камера для электрофореза Крышка Электрические провода Подложка Гребенки
Оборудования для проведения Гель-электрофореза Источник питания Камера для электрофореза Крышка Электрические провода Подложка Гребенки
 Подложка для геля и гребенки
Подложка для геля и гребенки
 Подготовка приборов для заливки геля
Подготовка приборов для заливки геля
 Aгароза Буферный раствор Смешайте агарозу и буферный раствор. Используйте термостабильную колбу, которая в несколько раз превышает объем приливаемого буфера.
Aгароза Буферный раствор Смешайте агарозу и буферный раствор. Используйте термостабильную колбу, которая в несколько раз превышает объем приливаемого буфера.
 Приготовление агарозы Агароза нерастворима при комнатной температуре (слева). Раствор агарозы после кипячения (справа). Аккуратно перемешивайте раствор агарозы при нагревании, чтобы она полностью растворилась. *** Будьте осторожны приготовлении раствора агарозы!!!- при высокой температуре раствор сильно кипит.
Приготовление агарозы Агароза нерастворима при комнатной температуре (слева). Раствор агарозы после кипячения (справа). Аккуратно перемешивайте раствор агарозы при нагревании, чтобы она полностью растворилась. *** Будьте осторожны приготовлении раствора агарозы!!!- при высокой температуре раствор сильно кипит.
 Заливка геля Растворенную агарозу необходимо охладить (~60ºC), после чего перенести в заливочную камеру. !!! Избегайте образования пузырьков воздуха !!!
Заливка геля Растворенную агарозу необходимо охладить (~60ºC), после чего перенести в заливочную камеру. !!! Избегайте образования пузырьков воздуха !!!
 Гребенка должна быть погружена в раствор агарозы.
Гребенка должна быть погружена в раствор агарозы.
 Расплавленная агароза при остывании полимеризуется, образуя гель (30 -45 минут). Об образовании геля можно судить по его внешнему виду. После застывания геля осторожно снимите гребенки из заливочной камеры.
Расплавленная агароза при остывании полимеризуется, образуя гель (30 -45 минут). Об образовании геля можно судить по его внешнему виду. После застывания геля осторожно снимите гребенки из заливочной камеры.
 Поместите подложку с агарозным гелем в камеру для электрофореза.
Поместите подложку с агарозным гелем в камеру для электрофореза.
 ДНК Буфер для электрофореза лунки катод (-) Anode (+) Добавить в камеру для проведения электрофореза буферный раствор, который был использован приготовлении агарозного геля. При этом буферный раствор должен покрывать гель не менее 1 см.
ДНК Буфер для электрофореза лунки катод (-) Anode (+) Добавить в камеру для проведения электрофореза буферный раствор, который был использован приготовлении агарозного геля. При этом буферный раствор должен покрывать гель не менее 1 см.
 Использование буфера для внесения проб Смешать буфер для внесения проб (6 X loading buffer ) с препаратами ДНК. Буфер для внесения проб представляют собой Буфер для внесения проб - раствор высокой плотности, которые позволяют легко вводить пробы в лунки геля. Они содержат также красители, что позволяет легко визуально следить за электрофорезом. 6 X буфер для внесения проб: Бромфеноловый синий (для цвета) Глицерин (для веса)
Использование буфера для внесения проб Смешать буфер для внесения проб (6 X loading buffer ) с препаратами ДНК. Буфер для внесения проб представляют собой Буфер для внесения проб - раствор высокой плотности, которые позволяют легко вводить пробы в лунки геля. Они содержат также красители, что позволяет легко визуально следить за электрофорезом. 6 X буфер для внесения проб: Бромфеноловый синий (для цвета) Глицерин (для веса)
 Приготовление буфера для нанесения проб на основе бромфенолового синего и ксилолцианола.
Приготовление буфера для нанесения проб на основе бромфенолового синего и ксилолцианола.
 Красители, входящие в состав буфера для внесения проб. Выбор красителя: · Бромфеноловый синий и ксилолцианол Рабочая концентрация в 1 х буфере ~0. 005 -0. 02%. Могут заметно мешать наблюдению фрагментов под УФ. · Крезоловый красный Рабочая концентрация в 1 х буфере ~0. 1 m. M. Совместим с ферментативными реакциями, практически не мешает наблюдению под УФ. · Orange. G Рабочая концентрация в 1 х буфере составляет 0. 01 -0. 05%. Наиболее подвижный краситель, практически всегда находится вне «рабочей зоны» . Заметен под УФ.
Красители, входящие в состав буфера для внесения проб. Выбор красителя: · Бромфеноловый синий и ксилолцианол Рабочая концентрация в 1 х буфере ~0. 005 -0. 02%. Могут заметно мешать наблюдению фрагментов под УФ. · Крезоловый красный Рабочая концентрация в 1 х буфере ~0. 1 m. M. Совместим с ферментативными реакциями, практически не мешает наблюдению под УФ. · Orange. G Рабочая концентрация в 1 х буфере составляет 0. 01 -0. 05%. Наиболее подвижный краситель, практически всегда находится вне «рабочей зоны» . Заметен под УФ.
 Внесение проб в лунку геля Аккуратно помесите наконечник пипетки в лунку геля (так, чтобы не повредить карман и дно геля) и медленно внесите пробу
Внесение проб в лунку геля Аккуратно помесите наконечник пипетки в лунку геля (так, чтобы не повредить карман и дно геля) и медленно внесите пробу
 Включение блока питания Закрыть крышкой камеру для проведения электрофореза, после чего подсоединить электрические провода к источнику питания. Убедитесь, что провода присоединены правильно - ДНК мигрирует к аноду (красный). При включении питания, пузыри должны формироваться на электродах, расположенных в электрофорезной камере.
Включение блока питания Закрыть крышкой камеру для проведения электрофореза, после чего подсоединить электрические провода к источнику питания. Убедитесь, что провода присоединены правильно - ДНК мигрирует к аноду (красный). При включении питания, пузыри должны формироваться на электродах, расположенных в электрофорезной камере.
 Катод (-) лунка Бромфеноловый синий ДНК (-) Gel Анод (+) После включения источника питания убедитесь, что движение ДНК в геле происходит в правильном направлении. Визуализация разделения осуществляется за счет бромфенолового синего.
Катод (-) лунка Бромфеноловый синий ДНК (-) Gel Анод (+) После включения источника питания убедитесь, что движение ДНК в геле происходит в правильном направлении. Визуализация разделения осуществляется за счет бромфенолового синего.
 Маркер молекулярной массы 12, 000 bp 5, 000 Примечание: бромфеноловый синий мигрирует на расстояние, равное размеру фрагмента ДНК примерно в 300 п. о. бромфеноловый синий Миграция ДНК 2, 000 1, 650 1, 000 850 650 500 400 300 200 100 + Использование молекулярного маркера позволяет определить примерный размер ДНК
Маркер молекулярной массы 12, 000 bp 5, 000 Примечание: бромфеноловый синий мигрирует на расстояние, равное размеру фрагмента ДНК примерно в 300 п. о. бромфеноловый синий Миграция ДНК 2, 000 1, 650 1, 000 850 650 500 400 300 200 100 + Использование молекулярного маркера позволяет определить примерный размер ДНК
 Интеркалирующие красители • Бромистый этидий. Молекула этого вещества содержит плоскую группу, которая встраивается между соседними основаниями ДНК и интеркалирует в УФ свете. • Для окрашивания бромистый этидий добавляют непосредственно в гель (0, 5 мкг/мл) или после разделения. ***Предостережение! Бромистый этидий – сильный мутаген. Все манипуляции с гелями и растворами, содержащими краситель, необходимо проводить в перчатках.
Интеркалирующие красители • Бромистый этидий. Молекула этого вещества содержит плоскую группу, которая встраивается между соседними основаниями ДНК и интеркалирует в УФ свете. • Для окрашивания бромистый этидий добавляют непосредственно в гель (0, 5 мкг/мл) или после разделения. ***Предостережение! Бромистый этидий – сильный мутаген. Все манипуляции с гелями и растворами, содержащими краситель, необходимо проводить в перчатках.
 Альтернативные красители Метиленовый синий Bio. RAD - Bio-Safe DNA Stain Ward’s - QUIKView DNA Stain Carolina BLU Stain …другие Преимущества Менее токсичные Не требеют УФ света Не требуют специальной утилизации (нет опасных отходов) Недостатки Дорогие Менее чувствительны Требуют большие количества ДНК Длительный период окрашивания
Альтернативные красители Метиленовый синий Bio. RAD - Bio-Safe DNA Stain Ward’s - QUIKView DNA Stain Carolina BLU Stain …другие Преимущества Менее токсичные Не требеют УФ света Не требуют специальной утилизации (нет опасных отходов) Недостатки Дорогие Менее чувствительны Требуют большие количества ДНК Длительный период окрашивания
 Окрашивание геля • Поместить гель в лоток с дистиллированной водой и бромистым этидием и выдерживать около 25 -30 минут. • После окрашивания несколько раз промыть гель в дистиллированной воде.
Окрашивание геля • Поместить гель в лоток с дистиллированной водой и бромистым этидием и выдерживать около 25 -30 минут. • После окрашивания несколько раз промыть гель в дистиллированной воде.
 Визуализация в проходящем УФ-свете трансиллюминатора. !!!Предостерижение!!! Работая с УФ-излучением необходимо предохранять глаза и кожу от ожогов. Одевайте очки!
Визуализация в проходящем УФ-свете трансиллюминатора. !!!Предостерижение!!! Работая с УФ-излучением необходимо предохранять глаза и кожу от ожогов. Одевайте очки!
 Электрофореграмма препаратов ДНК, выделенных из трансгенных растений томата (этидиум бромид)
Электрофореграмма препаратов ДНК, выделенных из трансгенных растений томата (этидиум бромид)


