Метастазы злокачественных новообразований в ЦНС


Метастазы злокачественных новообразований в ЦНС

По определению ВОЗ метастазирование в структуры ЦНС происходит гематогенным или ликворным путём. Новообразования, врастающие путём прямой инвазии, метастазами не являются.

При жизни метастазы в структуры ЦНС выявляются у 20 -40% онкологических больных, а на аутопсии среди умерших от рака встречаются в 65% случаев.

Наиболее часто метастазирование в ЦНС наблюдается при следующих злокачественных новообразованиях: - мелкоклеточный рак и аденокарцинома лёгкого 50 -60% - рак молочной железы 10 -20% - почечно-клеточный рак 5 -10% - меланома 5 -16% - колоректальный рак 5 -8% - неизвестная локализация первичной опухоли 11%

Мацко Д. Е. , Коршунов А. Г. (1998) классификация метастатического поражения структур центральной нервной системы: 1)Метастазы в кости черепа и твёрдую мозговую оболочку (2 -9%). ( рак почки, рак предстательной железы и меланомы). 2)Метастазы в позвонки и эпидуральное пространство спинного мозга (5 -10%). рак молочной железы, рак лёгкого, лимфомы, миеломная болезнь. 3)Метастазы в мягкую мозговую оболочку (канцероматозный менингит)(4 -15%). Имплантационное метастазирование медуллобластом, аденокарцинома желудка, рак молочной железы. 4)Метастазирование в вещество головного и спинного мозга. Наиболее частый вариант метастазирования большинства злокачественных новообразований

Наиболее частая локализация церебральных метастазов: - лобная доля 25 -40% - теменная доля 15 -20% - височная доля 10 -17% - затылочная доля до 5% - подкорковые образования 5 -7% - ствол мозга до 5% - мозолистое тело 2 -4% - желудочки мозга 1 -2%

Особенности патоморфологии метастазов в головной мозг: 1. Локализуются на границе серого и белого вещества головного мозга вследствие сужения в данном месте мелких артериальных сосудов ( «ловушка эмболов» )(Barth A et al. , 1995). 2. Наличие выраженного инфильтративного роста, распространение опухолевых клеток по интраадевентициальным щелям мозговых сосудов 3. в 70% случаев в центре метастаза наблюдается зона некроза, либо зона асептического или микробного воспаления 4. Наличие перитуморального отёка или токсического энцефалита

Морфологическая верификация показана в следующих ситуациях (степень В): - сомнительность при лучевом исследовании - нетипичность метастазирования - солитарный характер - отсутствие экстракраниальных симптомов и очагов поражения - техническая доступность

Цели иммуногистохимической верификации метастазов: - минимизации ошибок световой микроскопии - определении первичной опухоли (если неизвестна) - определения антигенной структуры опухолевых клеток с целью оценки прогноза и назначения таргетной терапии

Более чем в 80% случаев метастазирование в головной мозг носит множественный характер. В случае солитарного поражения (на данный момент), если у пациента есть онкологический анамнез, в 70% случаев речь идёт о метастатической природе поражения. Наличие множественных очагов поражения значительно повышает вероятность метастатического поражения.
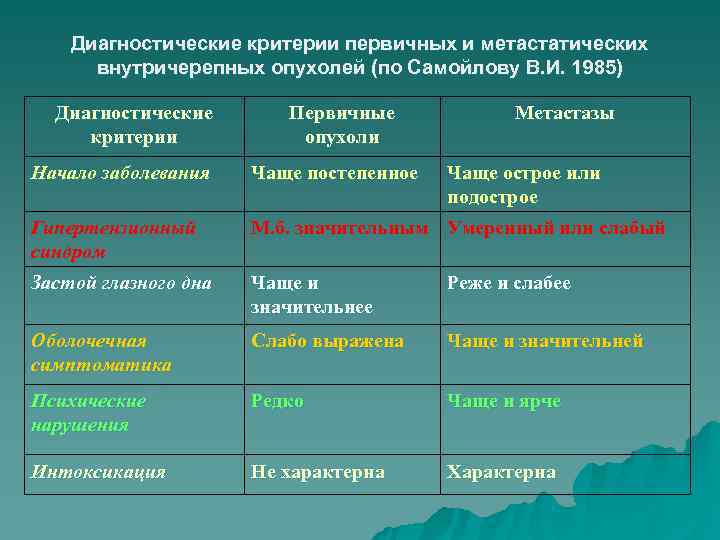
Диагностические критерии первичных и метастатических внутричерепных опухолей (по Самойлову В. И. 1985) Диагностические Первичные Метастазы критерии опухоли Начало заболевания Чаще постепенное Чаще острое или подострое Гипертензионный М. б. значительным Умеренный или слабый синдром Застой глазного дна Чаще и Реже и слабее значительнее Оболочечная Слабо выражена Чаще и значительней симптоматика Психические Редко Чаще и ярче нарушения Интоксикация Не характерна Характерна

Симптом Частота Головная боль 84% Интеллектуально-мнестические 52% расстройства Выпадения полей зрения 44% Застой глазного дна 39% Двигательные и чувствительные 38% расстройства Мозжечковая симптоматика 33, 6% Эписиндром 22, 1% Речевые нарушения 20, 3% Менингеальная симптоматика 16% Тазовые расстройства 6, 2%

Клинические варианты дебюта метастатического поражения головного мозга: 1. Бластоматозный. (40%) Подострое нарастание гипертензионного синдрома 2. Сосудистый. (54, 6% случаев). Острое инсульто-подобное начало 3. Воспалительный (5, 7%). Острое или подострое начало, синдром интоксикации с гипертермией, часто оболочечная симптоматика.

Кровоизлияния в церебральные метастазы встречаются от 25 до 50% случаев. Наиболее часто наблюдается при следующих первичных опухолях: - меланобластома - почечно-клеточный рак - рак щитовидной железы

Факторы патогенеза геморрагических осложнений метастазов в головной мозг: 1. Ускоренный и неполноценный ангиогенез в метастазах 2. Некрозы опухолевой ткани 3. Расстройства местного и системного гемостаза 4. Стереотаксическая радиохирургия

МРТ – «золотой» стандарт диагностики метастазов в головной мозг, а так же при симптомах сдавления спинного мозга (степень рекомендации А). Возможно использование КТ головного мозга с контрастированием.

Достоинства МРТ: 1. неинвазивность 2. отсутствие лучевой нагрузки 3. трёхмерность изображения 4. отсутствие артефактов от костных структур 5. высокая дифференциация мягких тканей

Недостатки МРТ: 1. длительность исследования 2. низкая точность для костной патологии 3. высокая стоимость 4. невозможность использования при наличии водителей ритма и при наличии металлических имплантов

Позитронно-эмиссионная томография (ПЭТ) позволяет изучать на только топику или размер патологического объёма, но и метаболизм, жизнеспособность, транспорт веществ, экспрессию генов и т. д.

Наиболее частые патологические процессы для дифференциальной лучевой и морфологической диагностики: - Ишемические и геморрагические инсульты - Абсцессы головного мозга - Злокачественные глиомы - Рассеянный склероз - Аутоиммунные васкулиты - Первичные лимфомы головного мозга - Вирусный энцефалит - Туберкулома - Диспластические и опухолевые поражения костей черепа

Прогностические факторы при метастазах в головной мозг: - общесоматический статус пациента - состояние основного заболевания (наличие экстракраниального поражения, прогрессирование или ремиссия) - количество метастазов в головном мозге - возраст

Основные принципы лечения (Российский научно-исследовательский нейрохирургический институт им. проф. А. Л. Поленова) 1. Хирургическое лечение, особенно при возможности тотального удаления метастатического очага, эффективнее облучения всего головного мозга (ОВМ). 2. Послеоперационная лучевая терапия не увеличивает выживаемость пациентов, однако снижает частоту рецидивов и появления новых метастазов.

3. Сочетание радиохирургии (СРХ) с облучением всего головного мозга (ОВМ) значительно улучшает выживаемость пациентов. 4. Радиохирургия как самостоятельный метод уступает по результатам комбинации его с хирургией иили с облучением всего головного мозга (ОВМ).

5. Сочетание СРХ и ОВМ по эффективности может рассматриваться как альтернатива хирургическому лечению. 6. Химиотерапия может рассматриваться только в сочетании с другими местными методами лечения (хирургия, СРХ, ОВМ). 7. Выбор комбинации методов лечения должен проводиться индивидуально с учётом прогностических факторов.

Показания к первичному оперативному вмешательству при метастазировании в головной мозг (степень В): 1. необходимость морфологической верификации в сомнительных случаях 2. солитарный метастаз 3. циторедуктивное вмешательство при больших симптомных метастазах При множественных метастазах (более 3) хирургия рутинно не рекомендована. Целесообразность удаления более чем одного метастаза в мозг неизвестна.

Ситуация № 1. - удовлетворительное общее состояние - солитарный очаг в мозге - отсутствие экстракраниального поражения -Резектабельность Рекомендовано: удаление метастаза сбез ОВМ. Возможные варианты: - Хирургия + СРХ на ложе метастаза -самостоятельная СРХ при метастазах менее 3, 5 см в диаметре Если метастаз нерезектабелен: СРХ + ОВМ.

При сравнении самостоятельного ОВМ и сочетания хирургия + ОВМ при одиночном метастазе обнаружено, что медиана выживаемости составила 15 и 40 недель соответственно (Patchell et al. 1990) (уровень 2). Проведено сравнение самостоятельной хирургии с сочетанием хирургия + ОВМ. Местные рецидивы 46% против 10%, генерализация в головном мозге 37% против 14% (уровень 2)(Patchell et al. 1998).

Локальный контроль при различных вариантах лечения солитарных метастазов в мозг по данным Rogers et al. 2006 Локальный контроль Самостоятельная 54% радикальная резекция Резекция + СРХ 79% Резекция + ОВМ 80 -90%

Ситуация № 2. - удовлетворительное общее состояние - 1 -3 метастаза -отсутствие экстракраниального поражения Варианты лечения: - ОВМ + СРХ - самостоятельная СРХ - Возможна тактика как при солитарном метастазе

Сравнение результатов лечения в группах больных с 1 -3 метастазами в головной мозг, при размере метастазов менее 2, 5 см (степень А, уровень 2). Kondziolka et al. 1999. ОВМ (30 Гр за ОВМ+СРХ 12 фракций) Период до 6 мес 36 мес локальной неудачи Медиана 7, 5 мес 11 мес выживаемости

При количестве метастазов до 4 -х, может быть рекомендована самостоятельная СРХ (степень В). Хотя большинство авторов логично обнаружили улучшение локального контроля при СРХ в сравнении с ОВМ, но имелся худший интракраниальный контроль над метастатической болезнью при отсутствии отличий в выживаемости (уровень 1)(Sneed et al. 2002).

СРХ рекомендована в сочетании с ОВМ при 1 -3 метастазах в головной мозг (степень рекомендации А). Исследования показали, что при использовании сочетания ОВМ + СРХ при 1 -3 метастазах в головной мозг, значительно улучшается интракраниальный контроль, но не обнаружено значимого улучшения выживаемости. Выгода не обнаружена при большем чем 3 количестве метастазов (уровень 1)(Mehta et al. 2005).

Режимы облучения при СРХ: - менее 20 мм в диаметре – 24 Гр, - 21 -30 мм – 18 Гр -31 -40 мм – 15 Гр Побочные эффекты – радионекроз тканей головного мозга, поздние геморрагические осложнения.

Пациент в стереотаксической раме Gamma-knife

Пациент в стереотаксической раме Cyber-knife

Cyber-knife

Ситуация № 3. - удовлетворительное общее состояние - 4 и более метастазов -отсутствие экстракраниального поражения Доказанным вариантом лечения является ОВМ. При масс-эффекте возможна циторедуктивная хирургия. При очагах менее 3 см в диаметре, возможна СРХ. Возможно сочетание СРХ и ОВМ.

Ситуация № 4. - плохое общее состояние - прогрессирование первичной опухоли -множественное экстракраниальное поражение Возможна попытка СРХ с симптоматическо- психологической целью

Эффективность самостоятельного лекарственного лечения больных с метастазами злокачественных новообразований в структуры центральной нервной системы не превышает 30%. Факторы низкой эффективности химиотерапии: 1. тяжесть состояния пациентов 2. лекарственная устойчивость опухолевых клеток 3. гетерогенностью опухолевой клеточной популяции 4. гемато-энцефалический барьер

Принципы назначения химиотерапии у больных с метастазами в головной мозг: 1. химиотерапия не должна проводиться, если не известна гистологическая структура опухоли 2. подбор лекарств проводится с учётом чувствительности первичной опухоли и проходимости через ГЭБ

3. соблюдать принцип – минимум побочных эффектов (в связи с паллиативностью лечения) 4. не следует проводить лечение, если в стационаре отсутствуют условия для диагностики и лечения возможных осложнений.

Наиболее часто используемые цитостатики при лечении больных с метастазами в головной мозг: - темозоломид - ломустин (CCNU) - кармустин - прокарбазин - фторпиримидины - цисплатин, карбоплатин - капецитабин - циклофосфамид - этопозид - винкристин

Метастазы в спинной мозг и оболочки. Облучение без хирургии рекомендовано при (степень В): - болевой синдром без эпидурально- спинальной компрессии - эпидурально-спинальная компрессия при радиочувствительных опухолях - неоперабельный пациент - значительная генерализация болезни

Показания для декомпрессивной хирургии с последующей лучевой терапией (степень А): - радиорезистентная первичная опухоль - продолжительность пареза и паралича менее 48 часов - предполагаемая продолжительность жизни более 3 месяцев - операбельность пациента

При условно-благоприятном прогнозе рекомендовано (степень А): СОД 30 -40 Гр за 10 -20 фракций. При ожидаемой ограниченной выживаемости (3 мес и менее)– единственная фракция 8 Гр.

Рекомендованной тактикой при наличии спинальной компрессии является сочетание декомпрессивной хирургии и облучения (степень А) Sundaresan et al. 1995 (уровень 1) Хирургия+ДЛТ Восстановлен 84% 57% ие движения Возможность 62% 19% ходить

Стереотаксическая радиохирургия при метастазировании в спинной мозг и оболочки только дополнительная опция лечения. Типичное дозирование: 16 -30 Гр за 1 -4 фракции. Контроль боли и локальный контроль лучше, чем при однократной дозе 8 Гр. СРХ можно использовать у пациентов уже проходивших курс облучения с неудачей (степень В). Результаты СРХ: контроль боли 84%- 97%, локальный контроль 84%-92%.
метастазы в цнс.ppt
- Количество слайдов: 47

