Метастатический РМЖ.ppt
- Количество слайдов: 56
 Метастатический рак молочной железы д. м. н. Устинова Елена Юрьевна
Метастатический рак молочной железы д. м. н. Устинова Елена Юрьевна
 n В настоящее время сформирована активная позиция в паллиативном лечении больных РМЖ с метастазами в кости, печень, легкие, головной мозг. n Больные раком молочной железы с метастазами в кости, печень, легкие, головной мозг, проявившимися в различные сроки после радикального лечения первичной опухоли, не могут быть отнесены в группу инкурабельных и нуждаются в специальном противоопухолевом лечении.
n В настоящее время сформирована активная позиция в паллиативном лечении больных РМЖ с метастазами в кости, печень, легкие, головной мозг. n Больные раком молочной железы с метастазами в кости, печень, легкие, головной мозг, проявившимися в различные сроки после радикального лечения первичной опухоли, не могут быть отнесены в группу инкурабельных и нуждаются в специальном противоопухолевом лечении.
 n Лечение метастазов мало влияет на выживаемость, однако при правильном применении терапия даже с относительно сильно выраженными побочными эффектами (в частности, химиотерапия) временно ослабляет симптомы и облегчает жизнь больного. На выбор схемы лечения больной РМЖ могут влиять следующие факторы: n наличие рецепторов эстрогенов и/или прогестерона в первичной опухоли или в биоптатах метастазов; n временной интервал между постановкой диагноза и появлением метастазов; n число метастазов и пораженных ими органов; n физиологическое состояние женщины (до или после менопаузы).
n Лечение метастазов мало влияет на выживаемость, однако при правильном применении терапия даже с относительно сильно выраженными побочными эффектами (в частности, химиотерапия) временно ослабляет симптомы и облегчает жизнь больного. На выбор схемы лечения больной РМЖ могут влиять следующие факторы: n наличие рецепторов эстрогенов и/или прогестерона в первичной опухоли или в биоптатах метастазов; n временной интервал между постановкой диагноза и появлением метастазов; n число метастазов и пораженных ими органов; n физиологическое состояние женщины (до или после менопаузы).
 Метастазы рака молочной железы в кости (Диагностика, лечение)
Метастазы рака молочной железы в кости (Диагностика, лечение)
 Вопросы для обсуждения: n Диагностика костных метастазов РМЖ, n Состояние проблемы: стандарты лечения, n Принципы комплексного лечения.
Вопросы для обсуждения: n Диагностика костных метастазов РМЖ, n Состояние проблемы: стандарты лечения, n Принципы комплексного лечения.
 Что нам известно? n Рак молочной железы обладает очень высокой потенцией к метастазированию. n В числе мишеней для этого процесса на одном из первых мест стоит костная система. n Частота метастазирования рака молочной железы в кости по данным различных авторов колеблется в очень широких пределах - от 5% до 85%. n Медиана общей выживаемости больных после развития метастазов в кости составляет 2 -3 года.
Что нам известно? n Рак молочной железы обладает очень высокой потенцией к метастазированию. n В числе мишеней для этого процесса на одном из первых мест стоит костная система. n Частота метастазирования рака молочной железы в кости по данным различных авторов колеблется в очень широких пределах - от 5% до 85%. n Медиана общей выживаемости больных после развития метастазов в кости составляет 2 -3 года.
 Что нам известно? n Метастазы локализуются преимущественно в плоских костях, при этом чаще всего поражается позвоночник, n среди других участков скелета это - тазовая кость, бедренная и плечевая, ребра и череп. Тип опухолевого Частота развития Медиана заболевания метастазов в кости у выживаемости с больных с момента выявления распространенной формой метастазов в кости, рака % месяцы Рак молочной железы 65 -75 19 -25
Что нам известно? n Метастазы локализуются преимущественно в плоских костях, при этом чаще всего поражается позвоночник, n среди других участков скелета это - тазовая кость, бедренная и плечевая, ребра и череп. Тип опухолевого Частота развития Медиана заболевания метастазов в кости у выживаемости с больных с момента выявления распространенной формой метастазов в кости, рака % месяцы Рак молочной железы 65 -75 19 -25
 Симптомы метастазов в кости: n Боли в позвоночнике и костях - первый клинический симптом метастазов в кости (в 71 % случаев), при этом более половины пациентов трактуют ее как непереносимую. Сначала они носят непостоянный характер, затем становятся постоянными и сильными, значительно ухудшающими качество жизни. n Ограничение подвижности (из-за болей). n Патологические переломы (выявляются у 46% пациентов).
Симптомы метастазов в кости: n Боли в позвоночнике и костях - первый клинический симптом метастазов в кости (в 71 % случаев), при этом более половины пациентов трактуют ее как непереносимую. Сначала они носят непостоянный характер, затем становятся постоянными и сильными, значительно ухудшающими качество жизни. n Ограничение подвижности (из-за болей). n Патологические переломы (выявляются у 46% пациентов).
 Осложнения метастазов в кости: Другие симптомы могут появляться в связи с компрессией спинного мозга: n прогрессирующая мышечная слабость (76%), n нарушение функции органов малого таза, проблемы с мочеиспусканием (57%), n нарушение чувствительности, онемение в области живота и конечностей (51%). Длительное сдавление или деформация нервных тканей приводит к необратимому параличу !!! n Серьезное и опасное для жизни осложнение метастатического поражения костей – гиперкальциемия (30 -40% больных), угрожающее жизни осложнение, которое проявляется сухостью во рту, жаждой, запорами, тошнотой, рвотой, полиурией. Затем наступает заторможенность, сонливость, нарушение ориентации и кома. В крови, как правило, повышается уровень креатинина и мочевины. n Развитие гиперкальциемии обусловлено усиленной костной резорбцией вследствие стимуляции остеокластов клетками опухоли, а также непосредственным их воздействием на костную ткань.
Осложнения метастазов в кости: Другие симптомы могут появляться в связи с компрессией спинного мозга: n прогрессирующая мышечная слабость (76%), n нарушение функции органов малого таза, проблемы с мочеиспусканием (57%), n нарушение чувствительности, онемение в области живота и конечностей (51%). Длительное сдавление или деформация нервных тканей приводит к необратимому параличу !!! n Серьезное и опасное для жизни осложнение метастатического поражения костей – гиперкальциемия (30 -40% больных), угрожающее жизни осложнение, которое проявляется сухостью во рту, жаждой, запорами, тошнотой, рвотой, полиурией. Затем наступает заторможенность, сонливость, нарушение ориентации и кома. В крови, как правило, повышается уровень креатинина и мочевины. n Развитие гиперкальциемии обусловлено усиленной костной резорбцией вследствие стимуляции остеокластов клетками опухоли, а также непосредственным их воздействием на костную ткань.
 Диагностика В комплексе лучевого исследования для выявления костных MTS рака молочной железы каждый из перечисленных методов имеет свою "нишу", выполняя, по ходу обследования пациента, определенную роль в дополнении предшествующих данных. § Остеосцинтиграфия, визуализируя одномоментно весь скелет, отвечает на вопрос - одиночный у пациента МТС или они имеют множественный характер. Магнитно-резонансная томография: n регистрация костных метастазов (с контрастным усилением и без внутривенного введения препарата) позволяет определить инвазию разрастающейся метастатической опухоли за пределы кости в мягкие ткани. Компьютерная томография: n может использоваться для проведения СТ-биопсии; n используется только для нахождения остеолитических очагов. Лабораторные тесты: n определение маркеров костной резорбции в моче (соотношение мочевого N- концевого телопептида и креатинина); n определение уровня кальция и щелочной фосфатазы в сыворотке крови; n костные маркеры используются как дополнительные факторы оценки эффективности терапии (примерно у 50% больных с костными метастазами они не определяются).
Диагностика В комплексе лучевого исследования для выявления костных MTS рака молочной железы каждый из перечисленных методов имеет свою "нишу", выполняя, по ходу обследования пациента, определенную роль в дополнении предшествующих данных. § Остеосцинтиграфия, визуализируя одномоментно весь скелет, отвечает на вопрос - одиночный у пациента МТС или они имеют множественный характер. Магнитно-резонансная томография: n регистрация костных метастазов (с контрастным усилением и без внутривенного введения препарата) позволяет определить инвазию разрастающейся метастатической опухоли за пределы кости в мягкие ткани. Компьютерная томография: n может использоваться для проведения СТ-биопсии; n используется только для нахождения остеолитических очагов. Лабораторные тесты: n определение маркеров костной резорбции в моче (соотношение мочевого N- концевого телопептида и креатинина); n определение уровня кальция и щелочной фосфатазы в сыворотке крови; n костные маркеры используются как дополнительные факторы оценки эффективности терапии (примерно у 50% больных с костными метастазами они не определяются).
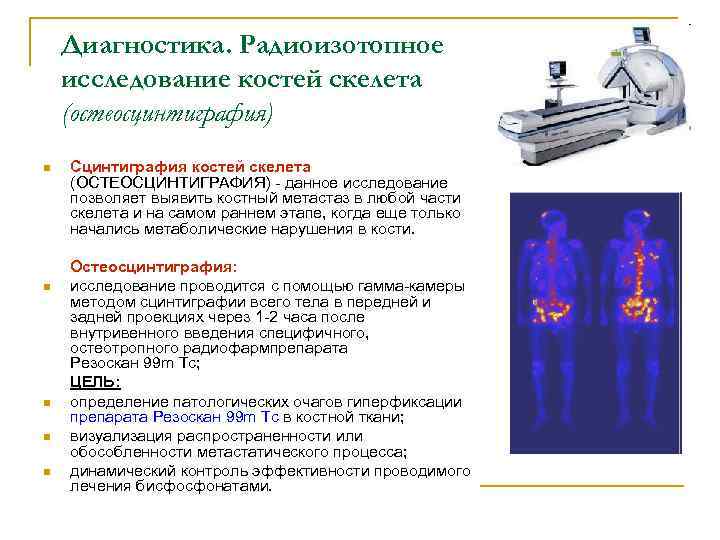 Диагностика. Радиоизотопное исследование костей скелета (остеосцинтиграфия) n Сцинтиграфия костей скелета (ОСТЕОСЦИНТИГРАФИЯ) - данное исследование позволяет выявить костный метастаз в любой части скелета и на самом раннем этапе, когда еще только начались метаболические нарушения в кости. Остеосцинтиграфия: n исследование проводится с помощью гамма-камеры методом сцинтиграфии всего тела в передней и задней проекциях через 1 -2 часа после внутривенного введения специфичного, остеотропного радиофармпрепарата Резоскан 99 m Тс; ЦЕЛЬ: n определение патологических очагов гиперфиксации препарата Резоскан 99 m Тс в костной ткани; n визуализация распространенности или обособленности метастатического процесса; n динамический контроль эффективности проводимого лечения бисфосфонатами.
Диагностика. Радиоизотопное исследование костей скелета (остеосцинтиграфия) n Сцинтиграфия костей скелета (ОСТЕОСЦИНТИГРАФИЯ) - данное исследование позволяет выявить костный метастаз в любой части скелета и на самом раннем этапе, когда еще только начались метаболические нарушения в кости. Остеосцинтиграфия: n исследование проводится с помощью гамма-камеры методом сцинтиграфии всего тела в передней и задней проекциях через 1 -2 часа после внутривенного введения специфичного, остеотропного радиофармпрепарата Резоскан 99 m Тс; ЦЕЛЬ: n определение патологических очагов гиперфиксации препарата Резоскан 99 m Тс в костной ткани; n визуализация распространенности или обособленности метастатического процесса; n динамический контроль эффективности проводимого лечения бисфосфонатами.
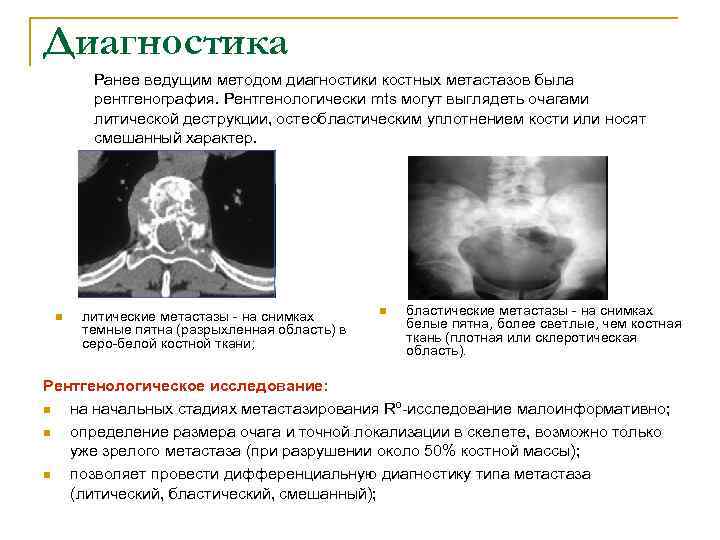 Диагностика Ранее ведущим методом диагностики костных метастазов была рентгенография. Рентгенологически mts могут выглядеть очагами литической деструкции, остеобластическим уплотнением кости или носят смешанный характер. n литические метастазы - на снимках n бластические метастазы - на снимках темные пятна (разрыхленная область) в белые пятна, более светлые, чем костная серо-белой костной ткани; ткань (плотная или склеротическая область). Рентгенологическое исследование: n на начальных стадиях метастазирования Rº-исследование малоинформативно; n определение размера очага и точной локализации в скелете, возможно только уже зрелого метастаза (при разрушении около 50% костной массы); n позволяет провести дифференциальную диагностику типа метастаза (литический, бластический, смешанный);
Диагностика Ранее ведущим методом диагностики костных метастазов была рентгенография. Рентгенологически mts могут выглядеть очагами литической деструкции, остеобластическим уплотнением кости или носят смешанный характер. n литические метастазы - на снимках n бластические метастазы - на снимках темные пятна (разрыхленная область) в белые пятна, более светлые, чем костная серо-белой костной ткани; ткань (плотная или склеротическая область). Рентгенологическое исследование: n на начальных стадиях метастазирования Rº-исследование малоинформативно; n определение размера очага и точной локализации в скелете, возможно только уже зрелого метастаза (при разрушении около 50% костной массы); n позволяет провести дифференциальную диагностику типа метастаза (литический, бластический, смешанный);
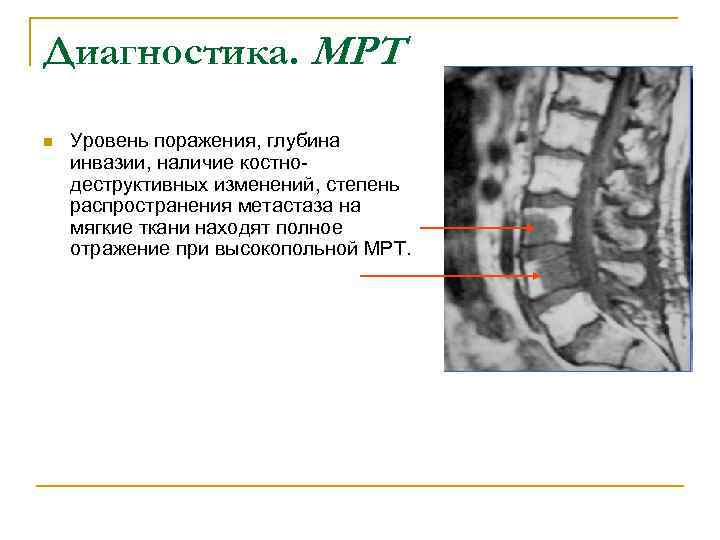 Диагностика. МРТ n Уровень поражения, глубина инвазии, наличие костно- деструктивных изменений, степень распространения метастаза на мягкие ткани находят полное отражение при высокопольной МРТ.
Диагностика. МРТ n Уровень поражения, глубина инвазии, наличие костно- деструктивных изменений, степень распространения метастаза на мягкие ткани находят полное отражение при высокопольной МРТ.
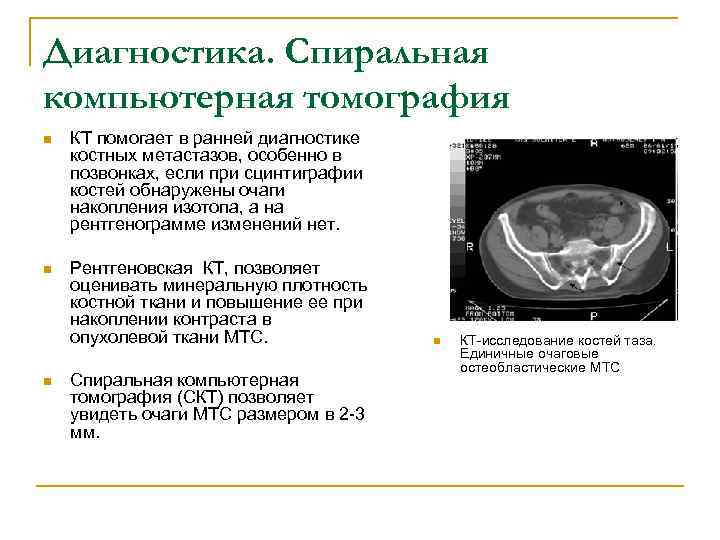 Диагностика. Спиральная компьютерная томография n КТ помогает в ранней диагностике костных метастазов, особенно в позвонках, если при сцинтиграфии костей обнаружены очаги накопления изотопа, а на рентгенограмме изменений нет. n Рентгеновская КТ, позволяет оценивать минеральную плотность костной ткани и повышение ее при накоплении контраста в опухолевой ткани МТС. n КТ-исследование костей таза. Единичные очаговые остеобластические МТС n Спиральная компьютерная томография (СКТ) позволяет увидеть очаги МТС размером в 2 -3 мм.
Диагностика. Спиральная компьютерная томография n КТ помогает в ранней диагностике костных метастазов, особенно в позвонках, если при сцинтиграфии костей обнаружены очаги накопления изотопа, а на рентгенограмме изменений нет. n Рентгеновская КТ, позволяет оценивать минеральную плотность костной ткани и повышение ее при накоплении контраста в опухолевой ткани МТС. n КТ-исследование костей таза. Единичные очаговые остеобластические МТС n Спиральная компьютерная томография (СКТ) позволяет увидеть очаги МТС размером в 2 -3 мм.
 Лечение костных метастазов – носит комплексный характер и включает в себя: 1. СИСТЕМНОЕ (медикаментозное) лечение : n противоопухолевую терапию (химиотерапию, гормонотерапию, иммунотерапию); n поддерживающую терапию, основанную на действии бисфосфонатов и анальгетиков. n Своевременное лечение костных 2. Местное лечение: метастазов, снижает частоту возникновения новых очагов n лучевую терапию; костного метастазирования, увеличивает выживаемость n хирургическое вмешательство; больных, существенно улучшает качество жизни этих больных за n радиациочастотную абляцию; счет снижения частоты скелетных осложнений – болевого синдрома, n цементопластику. патологических переломов, компрессии спинного мозга, гиперкальциемии.
Лечение костных метастазов – носит комплексный характер и включает в себя: 1. СИСТЕМНОЕ (медикаментозное) лечение : n противоопухолевую терапию (химиотерапию, гормонотерапию, иммунотерапию); n поддерживающую терапию, основанную на действии бисфосфонатов и анальгетиков. n Своевременное лечение костных 2. Местное лечение: метастазов, снижает частоту возникновения новых очагов n лучевую терапию; костного метастазирования, увеличивает выживаемость n хирургическое вмешательство; больных, существенно улучшает качество жизни этих больных за n радиациочастотную абляцию; счет снижения частоты скелетных осложнений – болевого синдрома, n цементопластику. патологических переломов, компрессии спинного мозга, гиперкальциемии.
 Лечение. Что нам известно? n Больные раком молочной железы, находящиеся в менопаузе (на момент лечения первичной опухоли) имеют лучшие результаты лечения костных метастазов, по сравнению с пациентками, имевшими сохраненную менструальную функцию. n Лучевая терапия в большей степени обеспечивает противоболевой эффект, как субъективный так и объективный (вследствие частичной или полной репарации костного очага), в то время как системная терапия в большей мере влияет на продолжительность этого эффекта. n Чем раньше проявляются метастатические поражения костей после окончания лечения рака молочной железы, тем агрессивнее течение заболевания.
Лечение. Что нам известно? n Больные раком молочной железы, находящиеся в менопаузе (на момент лечения первичной опухоли) имеют лучшие результаты лечения костных метастазов, по сравнению с пациентками, имевшими сохраненную менструальную функцию. n Лучевая терапия в большей степени обеспечивает противоболевой эффект, как субъективный так и объективный (вследствие частичной или полной репарации костного очага), в то время как системная терапия в большей мере влияет на продолжительность этого эффекта. n Чем раньше проявляются метастатические поражения костей после окончания лечения рака молочной железы, тем агрессивнее течение заболевания.
 Системное лечение. Химиотерапия. n Эффективность эндокринотерапии костных метастазов РМЖ составляет в среднем 31 %, а эффективность химиотерапии не превышает 50%. n Для лечения больных с костными метастазами разработан режим химиотерапии, содержащий три синергичные комбинации: Ø доксорубицин + метотрексат; Ø доксорубицин + 5 -ФУ; Ø доксорубицин + циклофосфан. n Введение цитостатиков прекращают при достижении общей курсовой дозы доксорубицина 400— 450 мг/м 2 или признаках прогрессирования опухолевого процесса.
Системное лечение. Химиотерапия. n Эффективность эндокринотерапии костных метастазов РМЖ составляет в среднем 31 %, а эффективность химиотерапии не превышает 50%. n Для лечения больных с костными метастазами разработан режим химиотерапии, содержащий три синергичные комбинации: Ø доксорубицин + метотрексат; Ø доксорубицин + 5 -ФУ; Ø доксорубицин + циклофосфан. n Введение цитостатиков прекращают при достижении общей курсовой дозы доксорубицина 400— 450 мг/м 2 или признаках прогрессирования опухолевого процесса.
 Лечение гиперкальциемии (ОСЛОЖНЕНИЕ КОСТНЫХ МЕТАСТАЗОВ) 1) Регидратация – введение солевых растворов (0, 9% натрия хлорида), 250– 500 мл/ч – для больных с выраженной гиповолемией, компенсированной сердечной деятельностью и удовлетворительными функциями почек, либо в варианте 3000 мл/24 ч. Желательно поддержание центрального венозного давления на уровне 10 см; 2) Мочегонные – исключаются тиазидные диуретики, которые могут приводить к повышению уровня Са++ в крови. Предпочтение отдается « петлевым диуретикам» – фуросемид 20– 40 мг внутривенно каждые 2– 4 ч, на фоне осуществляемой активно регидратации (!), при удовлетворительных гемодинамических показателях, с поддержанием уровня диуреза 150– 200 мл/ч; 3) Кортикостероиды – преднизолон 40– 100 мг (или эквивалентные дозы гидрокортизона, дексаметазона) внутривенно каждые 8 ч, с последующим поддерживающим применением препарата внутрь 10– 30 мг/сут; 4) Бисфосфонаты – внутривенно капельно после первых этапов регидратации. Продолжительность инфузий от 2 ч для ибандраната и до 4 – 6 ч для клодроната и памидроната. 5) Кальцитонин – для достижения быстрого лечебного эффекта: 4– 8 МЕ/кг внутримышечно или подкожно каждые 6– 12 ч в течение 2 дней.
Лечение гиперкальциемии (ОСЛОЖНЕНИЕ КОСТНЫХ МЕТАСТАЗОВ) 1) Регидратация – введение солевых растворов (0, 9% натрия хлорида), 250– 500 мл/ч – для больных с выраженной гиповолемией, компенсированной сердечной деятельностью и удовлетворительными функциями почек, либо в варианте 3000 мл/24 ч. Желательно поддержание центрального венозного давления на уровне 10 см; 2) Мочегонные – исключаются тиазидные диуретики, которые могут приводить к повышению уровня Са++ в крови. Предпочтение отдается « петлевым диуретикам» – фуросемид 20– 40 мг внутривенно каждые 2– 4 ч, на фоне осуществляемой активно регидратации (!), при удовлетворительных гемодинамических показателях, с поддержанием уровня диуреза 150– 200 мл/ч; 3) Кортикостероиды – преднизолон 40– 100 мг (или эквивалентные дозы гидрокортизона, дексаметазона) внутривенно каждые 8 ч, с последующим поддерживающим применением препарата внутрь 10– 30 мг/сут; 4) Бисфосфонаты – внутривенно капельно после первых этапов регидратации. Продолжительность инфузий от 2 ч для ибандраната и до 4 – 6 ч для клодроната и памидроната. 5) Кальцитонин – для достижения быстрого лечебного эффекта: 4– 8 МЕ/кг внутримышечно или подкожно каждые 6– 12 ч в течение 2 дней.
 Применение бисфосфонатов n Имеющиеся в настоящее время рекомендации предусматривают использование бисфосфонатов у всех больных РМЖ с метастазами в кости, подтвержденными рентгенологически (назначение на основании только данных сцинтиграфии не рекомендовано). n Лечение должно начинаться с момента первичного выявления метастазов в кости и продолжаться непрерывно. ДОСТОИНСТВА НЕДОСТАТКИ n Однако, применение бисфосфонатов n В исследованиях было показано, что сопряжено с развитием таких использование внутривенных форм нежелательных явлений, как почечная бисфосфонатов (золедроновой токсичность, некроз челюсти, кислоты, памидроната, ибандроната и гриппоподобный синдром. клодроната) позволило снизить риск развития ОКМ на 16– 40 % и увеличить время до развития первого скелетного n Несмотря на использование бисфосфонатов до 38– 43 % больных все осложнения до 12– 13 месяцев. же имеют осложнения костных метастазов.
Применение бисфосфонатов n Имеющиеся в настоящее время рекомендации предусматривают использование бисфосфонатов у всех больных РМЖ с метастазами в кости, подтвержденными рентгенологически (назначение на основании только данных сцинтиграфии не рекомендовано). n Лечение должно начинаться с момента первичного выявления метастазов в кости и продолжаться непрерывно. ДОСТОИНСТВА НЕДОСТАТКИ n Однако, применение бисфосфонатов n В исследованиях было показано, что сопряжено с развитием таких использование внутривенных форм нежелательных явлений, как почечная бисфосфонатов (золедроновой токсичность, некроз челюсти, кислоты, памидроната, ибандроната и гриппоподобный синдром. клодроната) позволило снизить риск развития ОКМ на 16– 40 % и увеличить время до развития первого скелетного n Несмотря на использование бисфосфонатов до 38– 43 % больных все осложнения до 12– 13 месяцев. же имеют осложнения костных метастазов.
 ДЕНОСУМАБ. Результаты, достигнутые благодаря внедрению бисфосфонатов, могут быть улучшены. Использование ДЕНОСУМАБА позволяет значимо снизить риск развития осложнений или отодвинуть сроки их возникновения: n снизить риск развития гиперкальциемии и существенно увеличить время до ее развития (снижает уровень кальция в крови), n снизить риск развития почечной токсичности и реакций острой фазы, n позволяет использовать более комфортный путь введения препарата в виде подкожной инъекции.
ДЕНОСУМАБ. Результаты, достигнутые благодаря внедрению бисфосфонатов, могут быть улучшены. Использование ДЕНОСУМАБА позволяет значимо снизить риск развития осложнений или отодвинуть сроки их возникновения: n снизить риск развития гиперкальциемии и существенно увеличить время до ее развития (снижает уровень кальция в крови), n снизить риск развития почечной токсичности и реакций острой фазы, n позволяет использовать более комфортный путь введения препарата в виде подкожной инъекции.
 Местное лечение. Сдавление спинного мозга. n Для устранения боли, связанной с костными осложнениями, наряду с наркотическими анальгетиками как минимум у 40 % пациентов требуется хирургическое вмешательство и/или лучевая терапия. n Ортопедическая хирургия чаще всего используется в связи с патологическими переломами или сдавлением спинного мозга. n При своевременном адекватном лечении (ЛТ или ламинэктомия) у многих больных можно рассчитывать на купирование симптомов заболевания. У больных с параличами только в 10% случаев наблюдается желаемое восстановление двигательных функций (возможность передвигаться). Цели терапии этого синдрома включают в себя восстановление и поддержание в нормальном состоянии нарушенных двигательных и других функций, локальный контроль опухоли, фиксацию позвоночника и купирование болей. К неотложным лечебным мероприятиям относится назначение: n высоких доз дексаметазона 100 мг внутривенно, с переходом на режим 4 мг каждые 6 ч, n сосудистых препаратов (кавинтон), n препаратов, улучшающих метаболизм нервной ткани (ноотропил).
Местное лечение. Сдавление спинного мозга. n Для устранения боли, связанной с костными осложнениями, наряду с наркотическими анальгетиками как минимум у 40 % пациентов требуется хирургическое вмешательство и/или лучевая терапия. n Ортопедическая хирургия чаще всего используется в связи с патологическими переломами или сдавлением спинного мозга. n При своевременном адекватном лечении (ЛТ или ламинэктомия) у многих больных можно рассчитывать на купирование симптомов заболевания. У больных с параличами только в 10% случаев наблюдается желаемое восстановление двигательных функций (возможность передвигаться). Цели терапии этого синдрома включают в себя восстановление и поддержание в нормальном состоянии нарушенных двигательных и других функций, локальный контроль опухоли, фиксацию позвоночника и купирование болей. К неотложным лечебным мероприятиям относится назначение: n высоких доз дексаметазона 100 мг внутривенно, с переходом на режим 4 мг каждые 6 ч, n сосудистых препаратов (кавинтон), n препаратов, улучшающих метаболизм нервной ткани (ноотропил).
 Местное лечение. Лучевая терапия. n Дистанционная лучевая терапия является эффективным методом лечения костных метастазов, n эффективность локальной лучевой терапии отдельных очагов достигает 85%, n Метод весьма результативен при единичных метастазах, однако, при диссеминированных поражениях его возможности снижаются пропорционально количеству и распространенности метастатических очагов, в основном, в связи с увеличением побочных эффектов.
Местное лечение. Лучевая терапия. n Дистанционная лучевая терапия является эффективным методом лечения костных метастазов, n эффективность локальной лучевой терапии отдельных очагов достигает 85%, n Метод весьма результативен при единичных метастазах, однако, при диссеминированных поражениях его возможности снижаются пропорционально количеству и распространенности метастатических очагов, в основном, в связи с увеличением побочных эффектов.
 Метастатическое поражение печени при раке молочной железы (Диагностика, лечение)
Метастатическое поражение печени при раке молочной железы (Диагностика, лечение)
 Метастатическое поражение печени. n Метастатическое поражение печени у больных РМЖ отмечается в 13% случаев. Классификация метастазов в печень (по количеству): n Одиночные (солитарные), n Единичные (2 -3), n Множественные. Классификация метастазов в печень (по расположению): n Унилобарные (поражают одну долю печени), n Билобарные (поражают обе доли печени).
Метастатическое поражение печени. n Метастатическое поражение печени у больных РМЖ отмечается в 13% случаев. Классификация метастазов в печень (по количеству): n Одиночные (солитарные), n Единичные (2 -3), n Множественные. Классификация метастазов в печень (по расположению): n Унилобарные (поражают одну долю печени), n Билобарные (поражают обе доли печени).
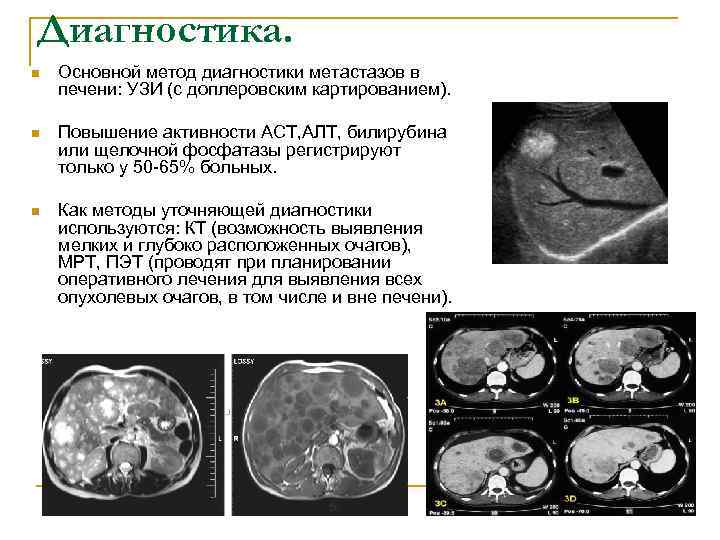 Диагностика. n Основной метод диагностики метастазов в печени: УЗИ (с доплеровским картированием). n Повышение активности АСТ, АЛТ, билирубина или щелочной фосфатазы регистрируют только у 50 -65% больных. n Как методы уточняющей диагностики используются: КТ (возможность выявления мелких и глубоко расположенных очагов), МРТ, ПЭТ (проводят при планировании оперативного лечения для выявления всех опухолевых очагов, в том числе и вне печени).
Диагностика. n Основной метод диагностики метастазов в печени: УЗИ (с доплеровским картированием). n Повышение активности АСТ, АЛТ, билирубина или щелочной фосфатазы регистрируют только у 50 -65% больных. n Как методы уточняющей диагностики используются: КТ (возможность выявления мелких и глубоко расположенных очагов), МРТ, ПЭТ (проводят при планировании оперативного лечения для выявления всех опухолевых очагов, в том числе и вне печени).
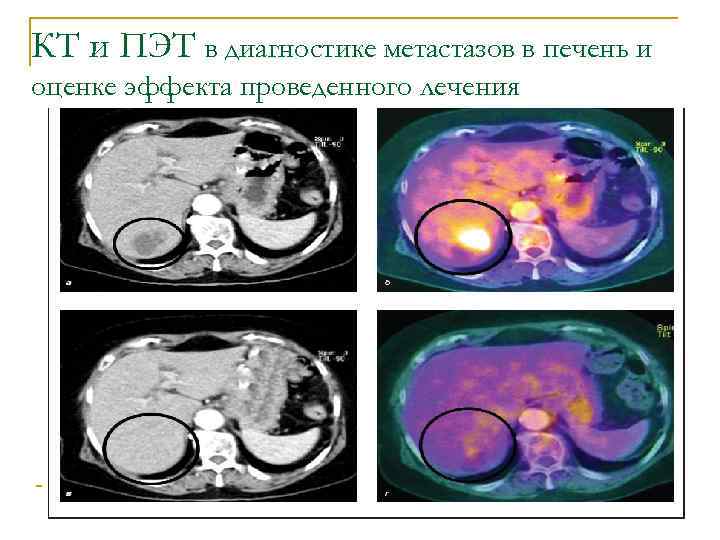 КТ и ПЭТ в диагностике метастазов в печень и оценке эффекта проведенного лечения
КТ и ПЭТ в диагностике метастазов в печень и оценке эффекта проведенного лечения
 Метастатическое поражение печени. Лечение. n Диссеминированный рак молочной железы рассматривается в первую очередь как показание к системному лекарственному лечению, но среди пациентов выделяется группа больных с солитарным (1 очаг) и изолированным единичным (до 4 очагов) метастатическим поражением печени. В этих случаях возможно проведение локального вмешательства на печени, в первую очередь оперативного удаления метастазов (резекция печени, термоабляция). n Пятилетняя выживаемость при метастатическом поражении печени составляет от 25– 28 % до 35– 40 % (Scaife C. I. et al. , 2006). n Но операбельность при данной патологии не превышает 15 – 20% (Steele G. et al. , 2002).
Метастатическое поражение печени. Лечение. n Диссеминированный рак молочной железы рассматривается в первую очередь как показание к системному лекарственному лечению, но среди пациентов выделяется группа больных с солитарным (1 очаг) и изолированным единичным (до 4 очагов) метастатическим поражением печени. В этих случаях возможно проведение локального вмешательства на печени, в первую очередь оперативного удаления метастазов (резекция печени, термоабляция). n Пятилетняя выживаемость при метастатическом поражении печени составляет от 25– 28 % до 35– 40 % (Scaife C. I. et al. , 2006). n Но операбельность при данной патологии не превышает 15 – 20% (Steele G. et al. , 2002).
 Метастатическое поражение печени. Лечение. n При метастатическом поражении печени сначала используется: противоопухолевая терапия (системная или регионарная) для уменьшения размеров метастазов, затем хирургическое лечение (резекция печени). n При нерезектабельных метастазах, противопоказанных к оперативному лечению используют методы локальной деструкции очагов, проводимые чрезкожным, оперативным или лапароскопическим способом под контролем УЗИ или КТ (алкогольная аблация, криодеструкция, лазер-индуцированная аблация, РЧА, микроволновая деструкция). n РЧА – относительно безопасный метод лечения больных раком молочной железы с солитарным и изолированным метастатическим поражением печени, является составной частью комплексного подхода и может стать методом выбора при лечении данного контингента больных.
Метастатическое поражение печени. Лечение. n При метастатическом поражении печени сначала используется: противоопухолевая терапия (системная или регионарная) для уменьшения размеров метастазов, затем хирургическое лечение (резекция печени). n При нерезектабельных метастазах, противопоказанных к оперативному лечению используют методы локальной деструкции очагов, проводимые чрезкожным, оперативным или лапароскопическим способом под контролем УЗИ или КТ (алкогольная аблация, криодеструкция, лазер-индуцированная аблация, РЧА, микроволновая деструкция). n РЧА – относительно безопасный метод лечения больных раком молочной железы с солитарным и изолированным метастатическим поражением печени, является составной частью комплексного подхода и может стать методом выбора при лечении данного контингента больных.
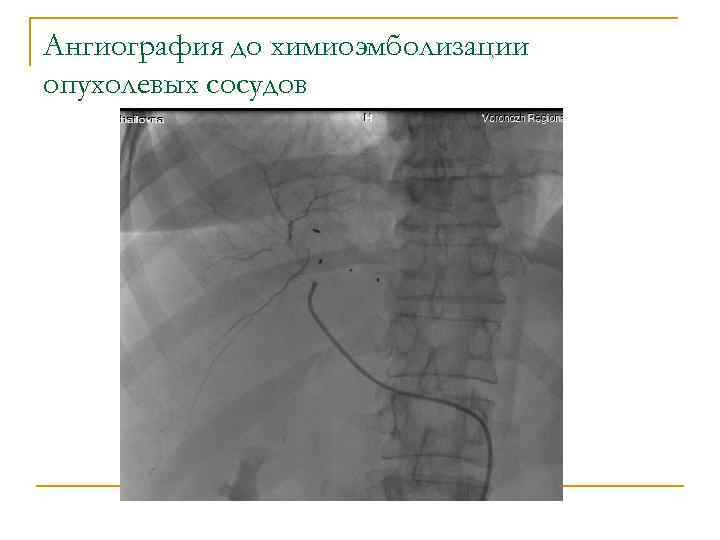 Ангиография до химиоэмболизации опухолевых сосудов
Ангиография до химиоэмболизации опухолевых сосудов
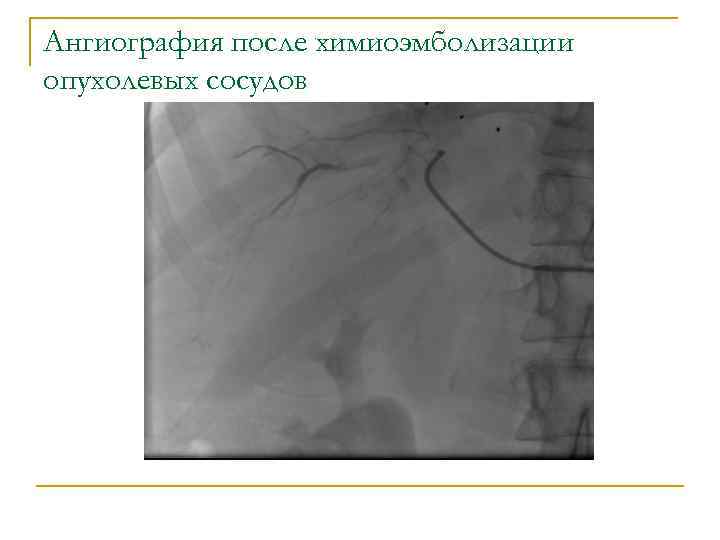 Ангиография после химиоэмболизации опухолевых сосудов
Ангиография после химиоэмболизации опухолевых сосудов
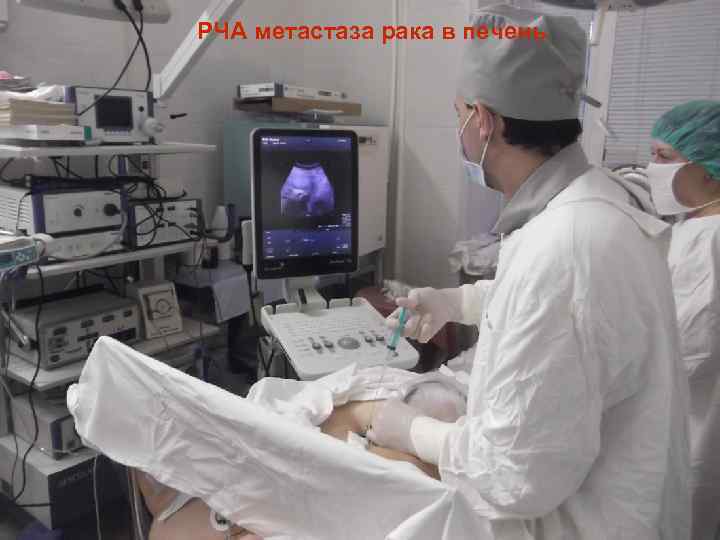 РЧА метастаза рака в печень
РЧА метастаза рака в печень
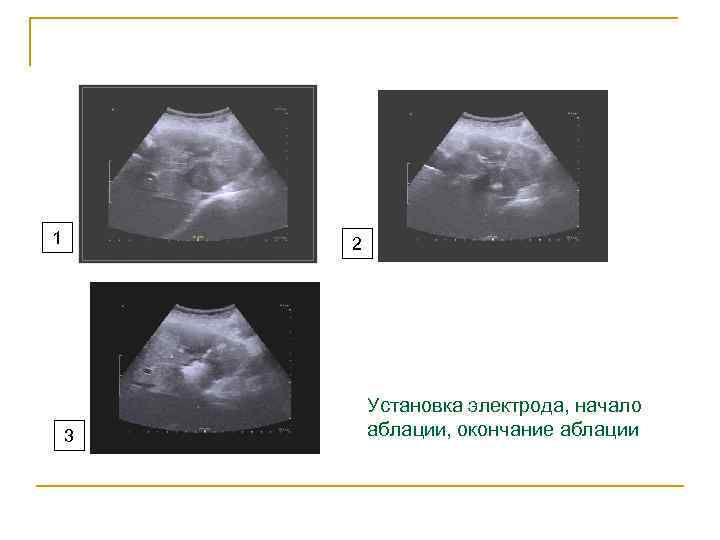 1 2 Установка электрода, начало 3 аблации, окончание аблации
1 2 Установка электрода, начало 3 аблации, окончание аблации
 Метастатическое поражение легких при раке молочной железы (Диагностика, лечение)
Метастатическое поражение легких при раке молочной железы (Диагностика, лечение)
 n Частота метастазирования РМЖ в легкие составляет 21%. n В клинической практике различают: солитарные (1 узел), единичные (2 -3 узла) и множественные (более 3 узлов) легочные метастазы. n По локализации различают: односторонние и двусторонние. n Основной путь метастазирования РМЖ в легкие – гематогенный. n Метастазы расположены в периферических отделах паренхимы легкого, часто – СУБПЛЕВРАЛЬНО.
n Частота метастазирования РМЖ в легкие составляет 21%. n В клинической практике различают: солитарные (1 узел), единичные (2 -3 узла) и множественные (более 3 узлов) легочные метастазы. n По локализации различают: односторонние и двусторонние. n Основной путь метастазирования РМЖ в легкие – гематогенный. n Метастазы расположены в периферических отделах паренхимы легкого, часто – СУБПЛЕВРАЛЬНО.
 Клинические проявления. n Так как метастазы расположены в плащевой зоне легких, то клинические проявления незначительны. У 70% больных заболевание протекает бессимптомно. n При прорастании висцеральной плевры появляются: кашель, боли в грудной клетке, кровохарканье, одышка, повышение температуры). n В 2 -10% наблюдений РМЖ метастазирует непосредственно в стенку бронха и проявляется симптоматикой, характерной для центральной первичной опухоли легкого с нарушением вентиляции соответствующей доли или сегмента. n Осложнения метастазов: перифокальная пневмония, распад в опухолевом узле, спонтанный пневмоторакс, кровотечение, гиповентиляция сегмента либо доли легкого, пневмония с абсцедированием, плеврит и эмпиема плевры.
Клинические проявления. n Так как метастазы расположены в плащевой зоне легких, то клинические проявления незначительны. У 70% больных заболевание протекает бессимптомно. n При прорастании висцеральной плевры появляются: кашель, боли в грудной клетке, кровохарканье, одышка, повышение температуры). n В 2 -10% наблюдений РМЖ метастазирует непосредственно в стенку бронха и проявляется симптоматикой, характерной для центральной первичной опухоли легкого с нарушением вентиляции соответствующей доли или сегмента. n Осложнения метастазов: перифокальная пневмония, распад в опухолевом узле, спонтанный пневмоторакс, кровотечение, гиповентиляция сегмента либо доли легкого, пневмония с абсцедированием, плеврит и эмпиема плевры.
 Диагностика. n Основной метод диагностики метастатической опухоли легкого – рентгенологический. n КТ – обязательный метод в алгоритме обследования больных с метастазами в легких, позволяющий выявить на 50 -70% больше образований по сравнению с рутинным рентгенологическим исследованием. n ПЭТ – специфичность и диагностическая точность метода составляет 85 -92%. n Торакоскопия с биопсией образования в легких. n Морфологическое исследование.
Диагностика. n Основной метод диагностики метастатической опухоли легкого – рентгенологический. n КТ – обязательный метод в алгоритме обследования больных с метастазами в легких, позволяющий выявить на 50 -70% больше образований по сравнению с рутинным рентгенологическим исследованием. n ПЭТ – специфичность и диагностическая точность метода составляет 85 -92%. n Торакоскопия с биопсией образования в легких. n Морфологическое исследование.
 Лечение. n Для лечения легочных метастазов используются все виды противоопухолевого воздействия: хирургическое, лучевое, химиотерапия и их комбинации. n Большинству больных показано проведение системного противоопухолевого лечения, т. к. метастазы в легких редко бывают изолированными и потому, что РМЖ чувствителен к лекарственной терапии. n При изолированном поражении легочной ткани используют оперативное лечение. Принят щадящий подход (ээкономная сублобарная резекция: краевая, клиновидная, прецизионная; сегментарная резекция). Реже выполняют классические оперативные вмешательства: лобэктомию, пневмонэктомию. Предложена прецизионная резекция неодимовым ИАГ лазером).
Лечение. n Для лечения легочных метастазов используются все виды противоопухолевого воздействия: хирургическое, лучевое, химиотерапия и их комбинации. n Большинству больных показано проведение системного противоопухолевого лечения, т. к. метастазы в легких редко бывают изолированными и потому, что РМЖ чувствителен к лекарственной терапии. n При изолированном поражении легочной ткани используют оперативное лечение. Принят щадящий подход (ээкономная сублобарная резекция: краевая, клиновидная, прецизионная; сегментарная резекция). Реже выполняют классические оперативные вмешательства: лобэктомию, пневмонэктомию. Предложена прецизионная резекция неодимовым ИАГ лазером).
 Лечение. Хирургическое лечение возможно не более, чем у 5 -10% больных. Критерии отбора для оперативного лечения: n Отсутствие рецидива первичной опухоли по данным комплексного обследования, n Солитарное или изолированное поражение легких, n Техническая возможность удаления метастаза, n Функциональная операбельность больного, В настоящее время общепринятым доступом при хирургическом лечении легочных метастазов являются: n односторонних метастазов – торакотомия, n двусторонних – стернотомия или двусторонняя торакотомия, n Для удаления солитарного метастаза в легком широко используют видеоторакоскопию.
Лечение. Хирургическое лечение возможно не более, чем у 5 -10% больных. Критерии отбора для оперативного лечения: n Отсутствие рецидива первичной опухоли по данным комплексного обследования, n Солитарное или изолированное поражение легких, n Техническая возможность удаления метастаза, n Функциональная операбельность больного, В настоящее время общепринятым доступом при хирургическом лечении легочных метастазов являются: n односторонних метастазов – торакотомия, n двусторонних – стернотомия или двусторонняя торакотомия, n Для удаления солитарного метастаза в легком широко используют видеоторакоскопию.
 Результаты хирургического лечения n Частота осложнений составляет 10 -15% (пневмоторакс, ателектазы, нарушение дренажной функции бронхов), n Летальность варьирует от 1, 2 до 6%, возрастая с объемом оперативного вмешательства и достигая максимума при пневмонэктомии, n 5 -летняя выживаемость после хирургического лечения легочных метастазов достигает 30 -42%; 10 -летняя – 15, 8 -20%.
Результаты хирургического лечения n Частота осложнений составляет 10 -15% (пневмоторакс, ателектазы, нарушение дренажной функции бронхов), n Летальность варьирует от 1, 2 до 6%, возрастая с объемом оперативного вмешательства и достигая максимума при пневмонэктомии, n 5 -летняя выживаемость после хирургического лечения легочных метастазов достигает 30 -42%; 10 -летняя – 15, 8 -20%.
 Альтернативные методы лечения n Изолированная нормотермическая (37º) перфузия легкого с химиопрепаратами в сочетании с полным хирургическим удалением метастатических очагов из легкого для лечения пациентов с изолированным метастатическим поражением легких Это - хирургическая процедура, в процессе которой происходит временное выключение легкого из кровообращения и перфузия его модифицированным физиологическим раствором, содержащим высокие концентрации противоопухолевого препарата, что позволяет осуществить доставку высоких доз цитостатика в легкое, избегая при этом системного воздействия препарата. (проводится в НИИ онкологии им. Н. Н. Петрова, Санкт -Петербург). Использовался химиопрепарат: цисплатин. n РЧА метастазов в легкие (у функционально неоперабельных больных или при отказе от операции). Выполняют под контролем КТ в условиях раздельной вентиляции легких. Размер опухолевого очага не более 4 см
Альтернативные методы лечения n Изолированная нормотермическая (37º) перфузия легкого с химиопрепаратами в сочетании с полным хирургическим удалением метастатических очагов из легкого для лечения пациентов с изолированным метастатическим поражением легких Это - хирургическая процедура, в процессе которой происходит временное выключение легкого из кровообращения и перфузия его модифицированным физиологическим раствором, содержащим высокие концентрации противоопухолевого препарата, что позволяет осуществить доставку высоких доз цитостатика в легкое, избегая при этом системного воздействия препарата. (проводится в НИИ онкологии им. Н. Н. Петрова, Санкт -Петербург). Использовался химиопрепарат: цисплатин. n РЧА метастазов в легкие (у функционально неоперабельных больных или при отказе от операции). Выполняют под контролем КТ в условиях раздельной вентиляции легких. Размер опухолевого очага не более 4 см
 Факторы благоприятного прогноза n Солитарный метастаз, n Временной интервал между излечением первичной опухоли и появлением метастаза > 36 месяцев, n Одностороннее поражение легкого при единичных и множественных метастазах, n Интактность внутригрудных лимфоузлов, n Радикальный характер операции. данные МНИОИ им. П. А. Герцена
Факторы благоприятного прогноза n Солитарный метастаз, n Временной интервал между излечением первичной опухоли и появлением метастаза > 36 месяцев, n Одностороннее поражение легкого при единичных и множественных метастазах, n Интактность внутригрудных лимфоузлов, n Радикальный характер операции. данные МНИОИ им. П. А. Герцена
 Метастатическое поражение головного мозга при раке молочной железы (Диагностика, лечение)
Метастатическое поражение головного мозга при раке молочной железы (Диагностика, лечение)
 Вопросы для обсуждения Цель: улучшение непосредственных и отдаленных результатов лечения больных с метастазами РМЖ в головной мозг с использованием новых технологий нейрохирургического лечения, современных режимов химиотерапии и химиолучевой терапии
Вопросы для обсуждения Цель: улучшение непосредственных и отдаленных результатов лечения больных с метастазами РМЖ в головной мозг с использованием новых технологий нейрохирургического лечения, современных режимов химиотерапии и химиолучевой терапии
 Что нам известно? n Метастазы в головной мозг выявляются у 10 -20% пациенток РМЖ. n При аутопсии метастазы в головной мозг диагностируются у 30% пациентов. n Метастазы в мозг редко проявляются до выявления первичной опухоли молочной железы (менее 1% больных). n Интервал от момента постановки диагноза РМЖ до выявления метастазов в головной мозг составляет в среднем 34 месяца. n 80% метастазов локализуются в больших полушариях головного мозга, 20% - в мозжечке и стволе головного мозга. n Продолжительность жизни этих больных составляет в среднем около 1 года.
Что нам известно? n Метастазы в головной мозг выявляются у 10 -20% пациенток РМЖ. n При аутопсии метастазы в головной мозг диагностируются у 30% пациентов. n Метастазы в мозг редко проявляются до выявления первичной опухоли молочной железы (менее 1% больных). n Интервал от момента постановки диагноза РМЖ до выявления метастазов в головной мозг составляет в среднем 34 месяца. n 80% метастазов локализуются в больших полушариях головного мозга, 20% - в мозжечке и стволе головного мозга. n Продолжительность жизни этих больных составляет в среднем около 1 года.
 Что нам известно? n В 50% случаев метастазы в головной мозг бывают единичными. n Наиболее часто встречающемся гистологическим вариантом церебральных метастазов РМЖ является инфильтративный протоковый рак. n Метастатические очаги чаще расположены субкортикально, четко структурно отграничены от окружающей мозговой ткани. n Отмечена тенденция РМЖ к метастазированию в твердую мозговую оболочку с последующим распространением метастаза в ткань мозга.
Что нам известно? n В 50% случаев метастазы в головной мозг бывают единичными. n Наиболее часто встречающемся гистологическим вариантом церебральных метастазов РМЖ является инфильтративный протоковый рак. n Метастатические очаги чаще расположены субкортикально, четко структурно отграничены от окружающей мозговой ткани. n Отмечена тенденция РМЖ к метастазированию в твердую мозговую оболочку с последующим распространением метастаза в ткань мозга.
 Клиническая картина n Клиническая картина зависит от локализации метастазов и может проявляться в виде: церебральных судорог, очаговой симптоматики (гемипарезы, афазия), атаксии (при поражении мозжечка, изменений психики, повышения внутричерепного давления (головные боли, рвота). n Продолжительность жизни напрямую зависит от ранней диагностики метастаза. n Появление у больной тех или иных неврологических симптомов – основание для проведения диагностических мероприятий.
Клиническая картина n Клиническая картина зависит от локализации метастазов и может проявляться в виде: церебральных судорог, очаговой симптоматики (гемипарезы, афазия), атаксии (при поражении мозжечка, изменений психики, повышения внутричерепного давления (головные боли, рвота). n Продолжительность жизни напрямую зависит от ранней диагностики метастаза. n Появление у больной тех или иных неврологических симптомов – основание для проведения диагностических мероприятий.
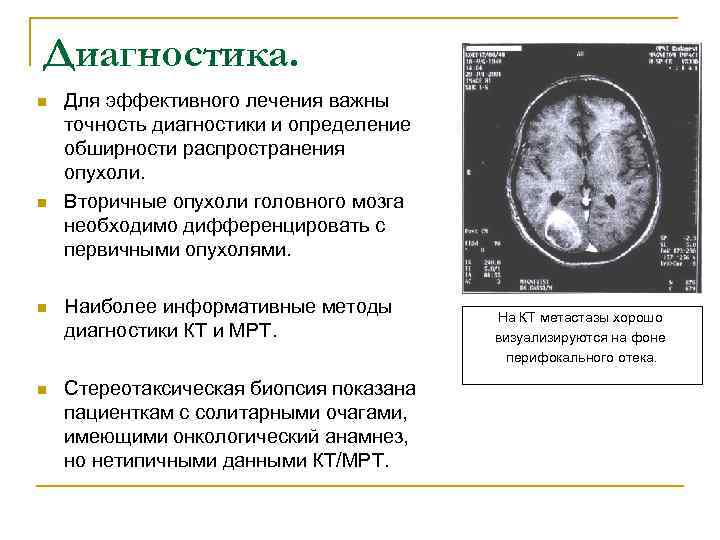 Диагностика. n Для эффективного лечения важны точность диагностики и определение обширности распространения опухоли. n Вторичные опухоли головного мозга необходимо дифференцировать с первичными опухолями. n Наиболее информативные методы На КТ метастазы хорошо диагностики КТ и МРТ. визуализируются на фоне перифокального отека. n Стереотаксическая биопсия показана пациенткам с солитарными очагами, имеющими онкологический анамнез, но нетипичными данными КТ/МРТ.
Диагностика. n Для эффективного лечения важны точность диагностики и определение обширности распространения опухоли. n Вторичные опухоли головного мозга необходимо дифференцировать с первичными опухолями. n Наиболее информативные методы На КТ метастазы хорошо диагностики КТ и МРТ. визуализируются на фоне перифокального отека. n Стереотаксическая биопсия показана пациенткам с солитарными очагами, имеющими онкологический анамнез, но нетипичными данными КТ/МРТ.
 Диагностика для принятия решения о тактике лечения больной. Для принятия решения о тактике лечения больной с метастазом в головной мозг необходимо: n уточнение степени распространения опухолевого процесса в организме (сцинтиграфия костей скелета; КТ органов брюшной и грудной полости, малого таза; ПЭТ), n оценка тяжести состояния больной и наличия возможности дальнейшего лечения.
Диагностика для принятия решения о тактике лечения больной. Для принятия решения о тактике лечения больной с метастазом в головной мозг необходимо: n уточнение степени распространения опухолевого процесса в организме (сцинтиграфия костей скелета; КТ органов брюшной и грудной полости, малого таза; ПЭТ), n оценка тяжести состояния больной и наличия возможности дальнейшего лечения.
 Лечение. ü Лечение больных с солитарным метастазом в головной мозг комплексное: n хирургическое удаление образования, n облучение всего мозга и дополнительно «ложа опухоли» для увеличения абластичности операции (снижает вероятность рецидива), n по показания с последующей химиотерапией (с учетом проникновения химиопрепарата через гематоэнцифалический барьер). ü При выявлении 2 -х или 3 -х метастазов, расположенных в поверхностных отделах полушарий мозга также возможно аналогичное лечение. ü При множественных метастазах или расположенных в области жизненно важных структур - оптимальный метод лечения – радиохирургия, часто комбинируемая с облучением всего головного мозга.
Лечение. ü Лечение больных с солитарным метастазом в головной мозг комплексное: n хирургическое удаление образования, n облучение всего мозга и дополнительно «ложа опухоли» для увеличения абластичности операции (снижает вероятность рецидива), n по показания с последующей химиотерапией (с учетом проникновения химиопрепарата через гематоэнцифалический барьер). ü При выявлении 2 -х или 3 -х метастазов, расположенных в поверхностных отделах полушарий мозга также возможно аналогичное лечение. ü При множественных метастазах или расположенных в области жизненно важных структур - оптимальный метод лечения – радиохирургия, часто комбинируемая с облучением всего головного мозга.
 Лечение. n Появление таких методов лечения как гамма-нож, векторная лучевая терапия, нейтронзахватная терапия существенно улучшает прогноз лечения этих больных.
Лечение. n Появление таких методов лечения как гамма-нож, векторная лучевая терапия, нейтронзахватная терапия существенно улучшает прогноз лечения этих больных.
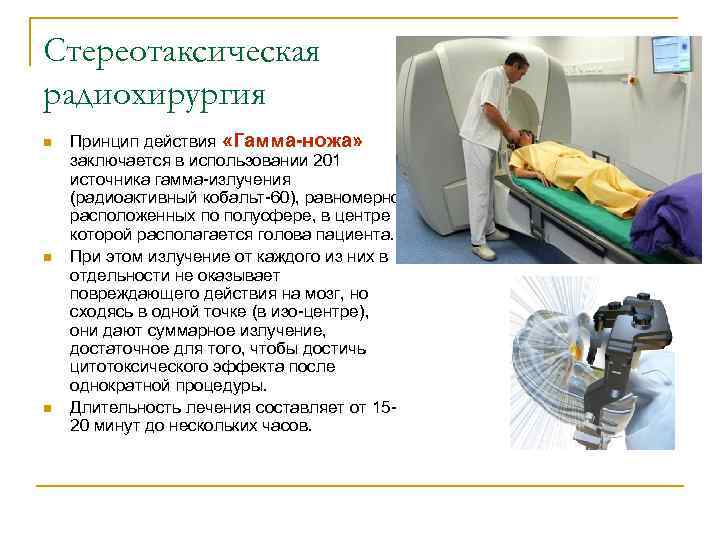 Стереотаксическая радиохирургия n Принцип действия «Гамма-ножа» заключается в использовании 201 источника гамма-излучения (радиоактивный кобальт-60), равномерно расположенных по полусфере, в центре которой располагается голова пациента. n При этом излучение от каждого из них в отдельности не оказывает повреждающего действия на мозг, но сходясь в одной точке (в изо-центре), они дают суммарное излучение, достаточное для того, чтобы достичь цитотоксического эффекта после однократной процедуры. n Длительность лечения составляет от 15 - 20 минут до нескольких часов.
Стереотаксическая радиохирургия n Принцип действия «Гамма-ножа» заключается в использовании 201 источника гамма-излучения (радиоактивный кобальт-60), равномерно расположенных по полусфере, в центре которой располагается голова пациента. n При этом излучение от каждого из них в отдельности не оказывает повреждающего действия на мозг, но сходясь в одной точке (в изо-центре), они дают суммарное излучение, достаточное для того, чтобы достичь цитотоксического эффекта после однократной процедуры. n Длительность лечения составляет от 15 - 20 минут до нескольких часов.
 Стереотаксическая радиохирургия n Кибер-нож -данный метод лечения позволяет воздействовать на опухоли мозга, которые недоступны для скальпеля хирурга. n Опухоль облучается с разных сторон тонким пучком радиации. При этом пациенту не требуется такой жесткой фиксации, как при традиционной лучевой терапии или использовании гамма-ножа. n Главные преимущества Кибер-Ножа, помимо его неинвазивности, являются, практическое отсутствие осложнений этого метода, сравнимых с оперативным лечением, химиотерапией или традиционным облучением радиацией. n Лечение кибер-ножом можно проводить в амбулаторном режиме, n К применению кибер-ножа нет каких-либо практических противопоказаний. Метод может применяться в случае, когда пациент неоперабелен из-за тяжелого состояния или сопутствующих заболеваний.
Стереотаксическая радиохирургия n Кибер-нож -данный метод лечения позволяет воздействовать на опухоли мозга, которые недоступны для скальпеля хирурга. n Опухоль облучается с разных сторон тонким пучком радиации. При этом пациенту не требуется такой жесткой фиксации, как при традиционной лучевой терапии или использовании гамма-ножа. n Главные преимущества Кибер-Ножа, помимо его неинвазивности, являются, практическое отсутствие осложнений этого метода, сравнимых с оперативным лечением, химиотерапией или традиционным облучением радиацией. n Лечение кибер-ножом можно проводить в амбулаторном режиме, n К применению кибер-ножа нет каких-либо практических противопоказаний. Метод может применяться в случае, когда пациент неоперабелен из-за тяжелого состояния или сопутствующих заболеваний.
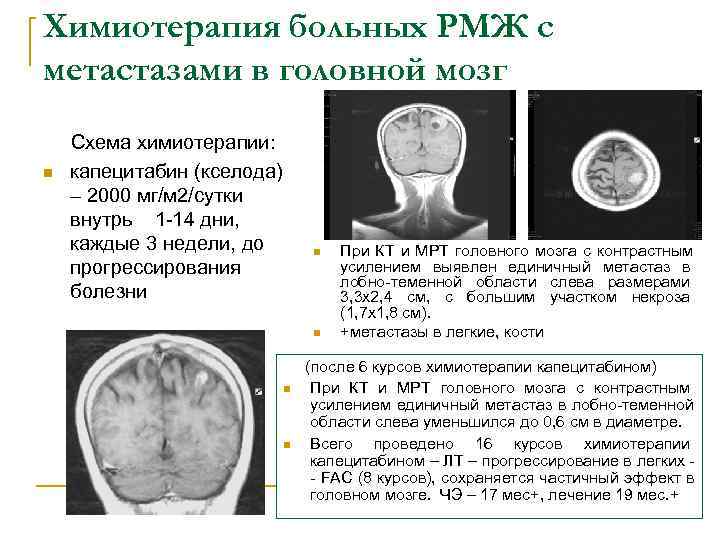 Химиотерапия больных РМЖ с метастазами в головной мозг Схема химиотерапии: n капецитабин (кселода) – 2000 мг/м 2/сутки внутрь 1 -14 дни, каждые 3 недели, до n При КТ и МРТ головного мозга с контрастным прогрессирования усилением выявлен единичный метастаз в лобно-теменной области слева размерами болезни 3, 3 х2, 4 см, с большим участком некроза (1, 7 х1, 8 см). n +метастазы в легкие, кости (после 6 курсов химиотерапии капецитабином) n При КТ и МРТ головного мозга с контрастным усилением единичный метастаз в лобно-теменной области слева уменьшился до 0, 6 см в диаметре. n Всего проведено 16 курсов химиотерапии капецитабином – ЛТ – прогрессирование в легких - - FAC (8 курсов), cохраняется частичный эффект в головном мозге. ЧЭ – 17 мес+, лечение 19 мес. +
Химиотерапия больных РМЖ с метастазами в головной мозг Схема химиотерапии: n капецитабин (кселода) – 2000 мг/м 2/сутки внутрь 1 -14 дни, каждые 3 недели, до n При КТ и МРТ головного мозга с контрастным прогрессирования усилением выявлен единичный метастаз в лобно-теменной области слева размерами болезни 3, 3 х2, 4 см, с большим участком некроза (1, 7 х1, 8 см). n +метастазы в легкие, кости (после 6 курсов химиотерапии капецитабином) n При КТ и МРТ головного мозга с контрастным усилением единичный метастаз в лобно-теменной области слева уменьшился до 0, 6 см в диаметре. n Всего проведено 16 курсов химиотерапии капецитабином – ЛТ – прогрессирование в легких - - FAC (8 курсов), cохраняется частичный эффект в головном мозге. ЧЭ – 17 мес+, лечение 19 мес. +
 Симптоматическое лечение. ЦЕЛЬ: n Стабилизация острой неврологической симптоматики, вызванной повышением внутричерепного давления и/или судорожным синдромом. ЛЕЧЕНИЕ: n Стероидные препараты (дексаметазон не менее 8 мг/сутки) – противоотечный эффект. Препараты способствуют обратному развитию гипертензионной и неврологической симптоматики. n Назначение осмотических диуретиков при выраженной внутричерепной гипертензии. n Назначение противосудорожных препаратов ведет к уменьшению выраженности пароксизмальной симптоматики (барбитураты или карбамазепин, или вальпроаты в зависимости от структуры приступа),
Симптоматическое лечение. ЦЕЛЬ: n Стабилизация острой неврологической симптоматики, вызванной повышением внутричерепного давления и/или судорожным синдромом. ЛЕЧЕНИЕ: n Стероидные препараты (дексаметазон не менее 8 мг/сутки) – противоотечный эффект. Препараты способствуют обратному развитию гипертензионной и неврологической симптоматики. n Назначение осмотических диуретиков при выраженной внутричерепной гипертензии. n Назначение противосудорожных препаратов ведет к уменьшению выраженности пароксизмальной симптоматики (барбитураты или карбамазепин, или вальпроаты в зависимости от структуры приступа),
 Прогноз. Медиана продолжительности жизни у больных с диагностированными метастазами в головной мозг составляет: n без лечения - 3 месяца, n при использовании лучевой терапии без операции - около 4 месяцев, n при условии комплексного лечения (операция+лучевая терапия) - превышает 2 года.
Прогноз. Медиана продолжительности жизни у больных с диагностированными метастазами в головной мозг составляет: n без лечения - 3 месяца, n при использовании лучевой терапии без операции - около 4 месяцев, n при условии комплексного лечения (операция+лучевая терапия) - превышает 2 года.
 Спасибо за внимание!
Спасибо за внимание!


