МЕТАНОЛ, ПРОПАНОЛ, БУТАНОЛ, 2 ЭТИЛГЕКСАНОЛ. СВОЙСТВА СПИРТОВ


МЕТАНОЛ, ПРОПАНОЛ, БУТАНОЛ, 2 ЭТИЛГЕКСАНОЛ. СВОЙСТВА СПИРТОВ Свойства спиртов обусловлены их функциональной группой. Эти свойства вызваны в основном наличием в молекулах спиртов полярных связей Сδ+– Оδ – Нδ+. Связи углерод– кислород и кислород – водород поляризованы. Реакции могут протекать по разрыву связи Оδ- – Нδ+ и менее полярной связи Сδ+– Оδ- 1. Спирты взаимодействуют со щелочными и щелочно-земельными металлами 2. Превращение спиртов в эфиры неорганических кислот С Нитратной кислотой образует нитратнометиловий эфир, или метилнитрат: 1
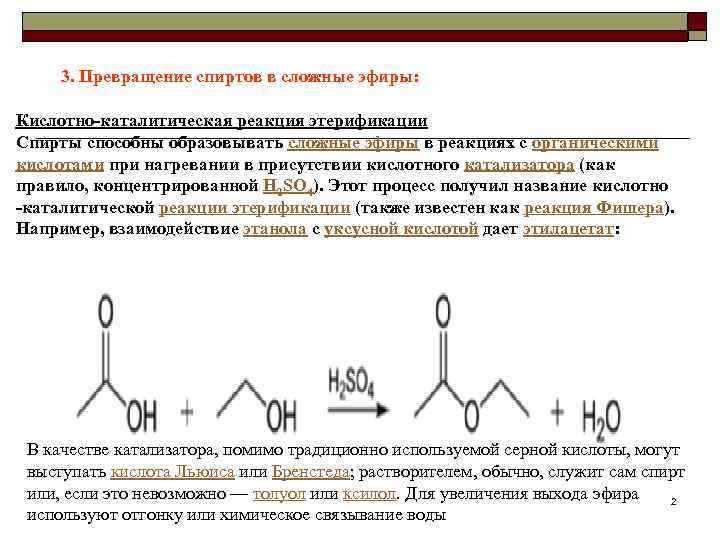
3. Превращение спиртов в сложные эфиры: Кислотно-каталитическая реакция этерификации Спирты способны образовывать сложные эфиры в реакциях с органическими кислотами при нагревании в присутствии кислотного катализатора (как правило, концентрированной H 2 SO 4). Этот процесс получил название кислотно -каталитической реакции этерификации (также известен как реакция Фишера). Например, взаимодействие этанола с уксусной кислотой дает этилацетат: В качестве катализатора, помимо традиционно используемой серной кислоты, могут выступать кислота Льюиса или Бренстеда; растворителем, обычно, служит сам спирт или, если это невозможно — толуол или ксилол. Для увеличения выхода эфира 2 используют отгонку или химическое связывание воды
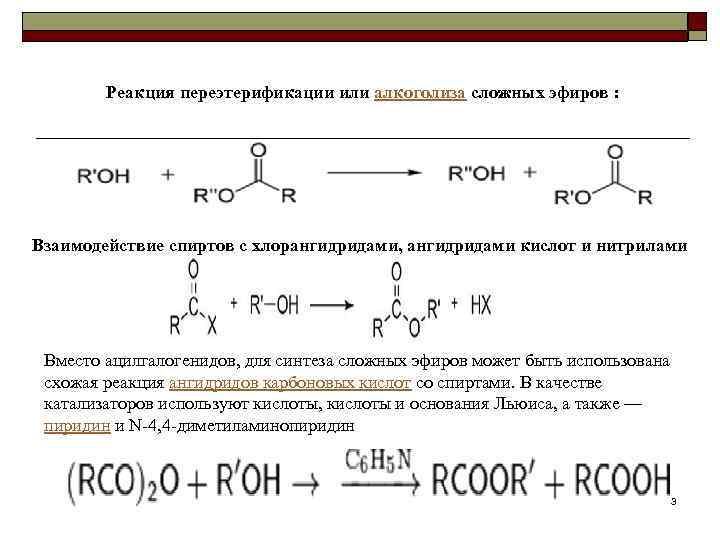
Реакция переэтерификации или алкоголиза сложных эфиров : Взаимодействие спиртов с хлорангидридами, ангидридами кислот и нитрилами Вместо ацилгалогенидов, для синтеза сложных эфиров может быть использована схожая реакция ангидридов карбоновых кислот со спиртами. В качестве катализаторов используют кислоты, кислоты и основания Льюиса, а также — пиридин и N 4, 4 диметиламинопиридин 3

Превращение спиртов в галогеналканы Гидроксильная группа в спиртах может быть замещена на атом галогена несколькими способами: взаимодействием с галогенводородами (HCl, HBr, HI); реакцией с тионилхлоридом; действием галогенидов фосфора (III) и (V) (РВr 3, РСl 5, РОСl 3 или РI 3) ; реакцией с квазифосфониевыми солями; превращением в алкилсульфонат с последующей реакцией замещения. 4

Превращение спиртов в простые эфиры При осторожном нагревании в присутствии серной кислоты происходит межмолекулярная дегидратация спиртов с образованием простых эфиров: Существуют и методы термокаталитической дегидратации спиртов. Например, первичные спирты в присутствии смешанного Ni−Al 2 O 3−Si. O 2 катализатора и водорода при нагревании превращаются в простые эфиры[37]: 5
Общие химические методы получения спиртов Существует множество методов получения спиртов, наиболее общие: • реакции окисления --окислении углеводородов (реже — галогенпроизводных углеводородов), содержащих кратные или активированные C−H связи; Окислительные агенты для алканов и циклоалканов используются сильные неорганические окислители: озон, перманганат калия, оксид хрома (VI), хромовая кислота, диоксид селена, а также пероксид водорода и некоторые пероксикислоты. Из-за возможности более глубокого окисления, метод имеет значение, как правило, только для получения третичных спиртов 6

• реакции восстановления — восстановление карбонильных соединений: альдегидов, кетонов, карбоновых кислот и сложных эфиров; Для восстановления альдегидов или кетонов, обычно, пользуются борогидридом натрия или калия, а также алюмогидридом лития в протонном растворителе: • реакции гидратации — кислотно-катализируемое присоединение воды к алкенам (гидратация); 7

• реакции присоединения: синтез газа, формальдегида, оксирана по кратным углеводородным связям; • Простейший пример такой реакции — промышленный синтез метанола: • реакции замещения (гидролиза) — реакции нуклеофильного замещения, при которых имеющиеся функциональные группы замещаются на гидроксильную группу; 8

МЕТАНОЛ, СВОЙСТВА Метано л (метиловый спирт, карбинол, гидроксид метила) — CH 3 OH, простейший одноатомный спирт, бесцветная ядовитая жидкость. Метанол — это первый представитель гомологического ряда Метиловый спирт подвижная жидкость со слабым запахом похожим на запах обычного спирта. Плотность его 0, 792 г / см 3. Температура кипения 64, 5 0 С, С водой смешивается в любых соотношениях. Хороший растворитель для многих органических веществ. Метиловый спирт ядовитое вещество, действующее на нервную и сосудистую системы человека. При попадании в организм человека 10 мл метанола может привести к тяжелому отравлению, до слепоты; попадания 25 -30 мл метанола 9 приводит к смертельному случаю

Применение метанола для производства продукции основного органического синтеза 1. Для производство формальдегида : Двумя методами А) дегидрированием, совмещенным с частичным окислением Т= 500— 600°С, временя контакта 0, 01— 0, 03 с. Выход формальдегида на пропущенное сырье 80— 85 %, степень конверсии метанола 85— 90 % • Катализаторы: металлическая медь (в виде сетки или стружек) или серебро, осажденное на А 1203. Последний катализатор оказался более эффективным и широко применяется в промышленности Б)окислением в избытке воздуха. CH 3 OH + O 2 → 2 HCHO + 2 H 2 O 2 Формальдегид применяют для производства ряда полимеров (феноло , карбамидо и меламиноформальдегидные полимеры, полиформальдегид) и в качестве 10 промежуточного вещества для синтеза изопрена, пентаэритрита, гексаметилентетрамина (уротропин) и других ценных веществ.

2. Для производства уксусной кислоты CH 3 OH + CO → CH 3 COOH Жидкофазное карбонилирование при 220— 250 °С и давлении 30 МПа в присутствии сложного родиевого катализатора и небольших количеств иодметана. Уксусная кислота широко применяется в пищевых целях, в качестве растворителя, промежуточного продукта для синтеза монохлоруксусной кислоты, растворителей — сложных эфиров уксусной кислоты (этилацетат, бутилацетат и др. ), мономеров (винилацетат) и других ценных веществ. 11
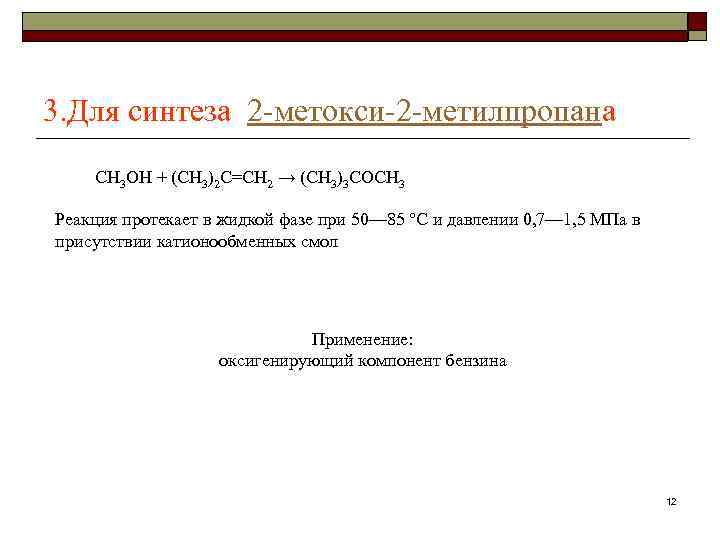
3. Для синтеза 2 метокси 2 метилпропана CH 3 OH + (CH 3)2 C=CH 2 → (CH 3)3 COCH 3 Реакция протекает в жидкой фазе при 50— 85 °С и давлении 0, 7— 1, 5 МПа в присутствии катионообменных смол Применение: оксигенирующий компонент бензина 12

4. Для производства. N диметиланилина C 6 H 5 NH 2 + 2 CH 3 OH → C 6 H 5 N(CH 3)2 + 2 H 2 O Жидкофазное алкилирование анилина при 200 °С и давлении 3, 7 МПа в присутствии каталитических количеств серной кислоты Диметиланилнн является важным полупродуктом в производ стве красителей, а также используется для получения тетрила — тринитрофенилметилнитрамина сильного взрывчатого вещества. 13

5. Для производства метиламинов CH 3 OH + NH 3 → CH 3 NH 2 + H 2 O CH 3 OH + 2 NH 3 → (CH 3)2 NH + 2 H 2 O CH 3 OH + 3 NH 3 → (CH 3)3 N + 3 H 2 O Условия процесса: Гетерогенные катализаторы кислотного типа Процесс в газовой фазе при 350— 450°С. Чаще всего применяют оксид алюминия, алюмосиликаты, фосфаты алюминия, фосфат аммония. Применение метиламинов: для производства инсектицидов, фунгицидов, ускорителей вулканизации, ПАВ, дубильных веществ, лекарственных средств, красителей, ракетных топлив, растворителей. 14

6. Для производства хлорметана Реакция протекает в газовой фазе при 200— 350 °С в присутствии Zn. Cl 2 на твёрдом носителе CH 3 OH + HCl → CH 3 Cl + H 2 O Хлорметан применяется в органических синтезах ( метилирующее средство) , для получения низких температур ( хладоагент) и других целей. CH 3 OH + HCl → CH 3 Cl + H 2 O 7. Прямое использование в качестве топлива. 8. Метанол применяется в производстве метил третбутилового эфира – МТБЭ, являющегося одной из широко применяемых октано повышающих присадок к бензинам. 15

Сырьевые источники получения метанола. Перспективы использования различных видов сырья. Раньше метанол получали сухой перегонкой древесины (древесный спирт), но этот метод полностью вытеснен синтезом из окиси углерода и водорода, который осуществлен в крупных масштабах во всех передовых странах. Твердое топливо сохраняет в качестве сырья определенное значение. Разработка процесса газификации угля с целью получения синтез газа, содержащего Н 2, СО 2, СО, может изменить структуру сырьевой базы производства метанола и таким образом неудобный для транспортирования уголь будет превращен в удобный для хранения, транспортирования и использования метанол. Перспективным способом получения метанола является неполное окисления метана и его гомологов. 16

Современные промышленные способы получения метанола. 1. ОКИСЛЕНИЕ МЕТАНА 1. Давление 106 атм. и температура реакции 3400 С. 2. Соотношении метан : кислород = 9 : 1 3. Степень окисления метана составляет 22 %, причем 17 % прореагировавшего метана превращается в спирт, 4. 0, 75 % в формальдегид, а остальное количество полностью окисляется до двуокиси углерода и воды. 17

Радикально-цепной механизм получения кислородсодержащих соединений. Активация кислорода Зарождение цепи Образование перекиси Обрыв цепи Разложение перекиси 18

2. Способ получения метанола из окиси углерода и водорода (синтез газа). Наиболее удобный и экономичный В связи с экзотермичностью процесса константа равновесия падает с повышением температуры, составляя 2, 316 10 4 при 300°С и всего 1, 091 10 5 при 400°С. Приходится поэтому повышать давление, что способствует росту равновесной степени конверсии ввиду уменьшения объема газовой смеси в результате реакции. Синтез метанола из СО и Н 2 был впервые разработан Патаром в 1924 г. , применившим в качестве катализатора Zn. O. Затем оксид цинка стали активировать оксидом хрома (8 масс. ч. Zn. O на 1 масс. ч. Сг 203). Более активны, но требуют тонкой очистки реагентов оксидные медьхромовые и цинкмедьхромовые катализаторы. 19

Механизм образования метанола: Побочно образуются: диметиловый эфир (за счет дегидратации метанола), метан (как продукт гидрирования метанола и СО), диоксид углерода и вода: Получаются также: другие спирты, альдегиды, ацетона. Селективность реакции по метанолу в присутствии указанных катализаторов является высокой, превышая 95%. 20

Выбор параметров процесса ■ Температура зависит от активности катализаторов и может изменяться в пределах 250— 420 °С. ■ В зависимости от этого выбирают давление, которое, в соответствии с термодинамическими характеристиками, должно быть тем больше, чем выше температура, и может изменяться от 5 до 20— 35 МПа. ■ Снижение давления благоприятно для уменьшения энергетических затрат на сжатие газа. Этому же способствует снижение рециркуляции непревращенного газа, т. е. увеличение фактической степени конверсии реагентов. ■ Приближение к равновесной степени конверсии невыгодно из за падения производительности и селективности. Поэтому фактическую степень конверсии синтез газа ограничивают величиной 15— 20%, что достигается при времени контакта 10— 40 с. ■ Долгое время процесс проводили при высоких давлении и температуре (20— 35 МПа и 370— 420 °С) с оксидным цинк хромовым катализатором. ■ В настоящее время благодаря тонкой очистке синтез газа стали применять более активные катализаторы на основе Си. О Сг 203 и Zn. O Cu. O Cr 20 с добавками 3 промоторов, что позволило снизить температуру до 250— 300°С и давление до 5 — 10 МПА. 21

Реакционный узел при синтезе метанола зависит от способа отвода тепла и проведения реакции. Трубчатые реакторы : (рис. 151, а), в трубах находится катализатор и движется реакционная масса, охлаждаемая кипящим в межтрубном пространстве водным конденсатом. Тепло реакционных газов используют для подогрева исходной смеси. Достигается наиболее высокий эксергетический к. п. д. и генерируется да 1 т пара высокого давления на 1 т метанола, но высока металлоемкость аппарата. Адиабатические реакторы с несколькими (обычно с четырьмя) слоями катализатора: Теплоплообменные устройства отсутствуют, для съема тепла и регулирования температуры подают холодный синтез газ между слоями катализатора через специальные ромбические распределители, обеспечивающие эффективное смешение горячего и холодного газа. Профиль температуры в таком реакторе ступенчатый, постепенное повышение в слоях катализатора сменяется резким падением при смешении с холодным газом. Предварительно подогревают лишь часть исходного синтез газа, а остальное реакционное тепло утилизируют для получения пара высокого давления. С точки зрения эксергетического к. п. д. , более выгодна несколько измененная схема, когда для подогрева исходного газа используют только необходимую часть реакционных газов, а основная их масса идет в котел утилизатор. 22

Синтез метанола в трехфазной системе (рис. 151, в). В жидкой фазе инертного углеводорода с суспендированным в жидкости гетерогенным катализатором и барботированием синтез газа через эту суспензию. Тепло реакции отводят за счет циркуляции жидкости через парогенератор или при помощи внутренних теплообменников с кипящим водным конденсатом. Метанол (и часть углеводорода) уносятся непревращенным синтез газом; их тепло используют для подогрева исходного газа. Преимущество этого способа состоит в более благоприятном для синтеза состоянии равновесия при жидкофазной реакции, что позволяет достигнуть концентрации метанола в реакционном газе 15 % (об. ) вместо 5 % (об. ) при обычном синтезе, доведя степень конверсии синтез газа до 35 вместо 15 %. Этим снижаются рециркуляция газа и энергетические затраты. 23
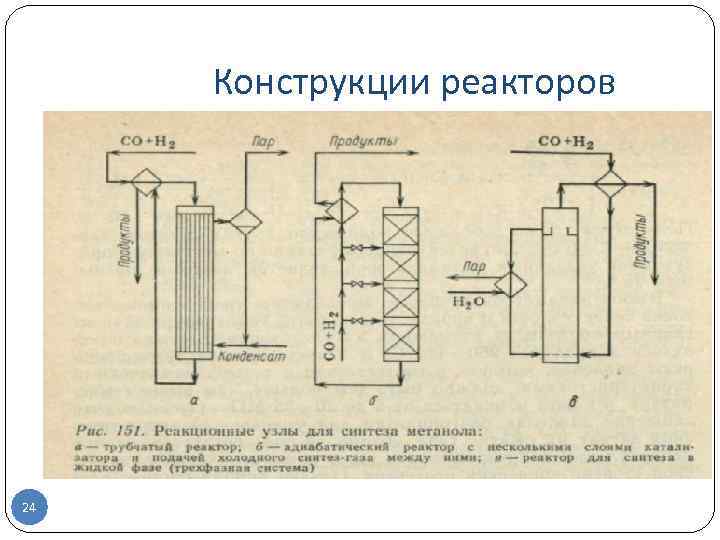
Конструкции реакторов 24
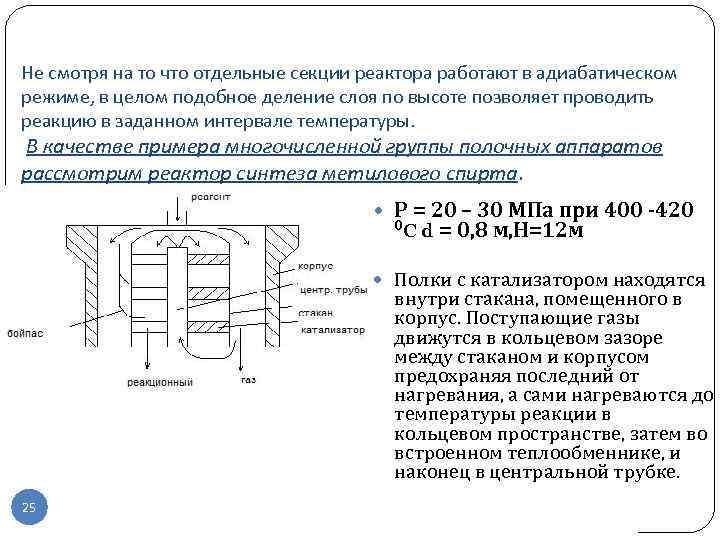
Не смотря на то что отдельные секции реактора работают в адиабатическом режиме, в целом подобное деление слоя по высоте позволяет проводить реакцию в заданном интервале температуры. В качестве примера многочисленной группы полочных аппаратов рассмотрим реактор синтеза метилового спирта. Р = 20 – 30 МПа при 400 -420 0 C d = 0, 8 м, Н=12 м Полки с катализатором находятся внутри стакана, помещенного в корпус. Поступающие газы движутся в кольцевом зазоре между стаканом и корпусом предохраняя последний от нагревания, а сами нагреваются до температуры реакции в кольцевом пространстве, затем во встроенном теплообменнике, и наконец в центральной трубке. 25

Промышленный синтез метилового спирта включает три основные стадии: 1) получение смеси окиси углерода и водорода (синтез газ); 2) получение метилового спирта сырца; 3) выделение и очистка метилового спирта. 26
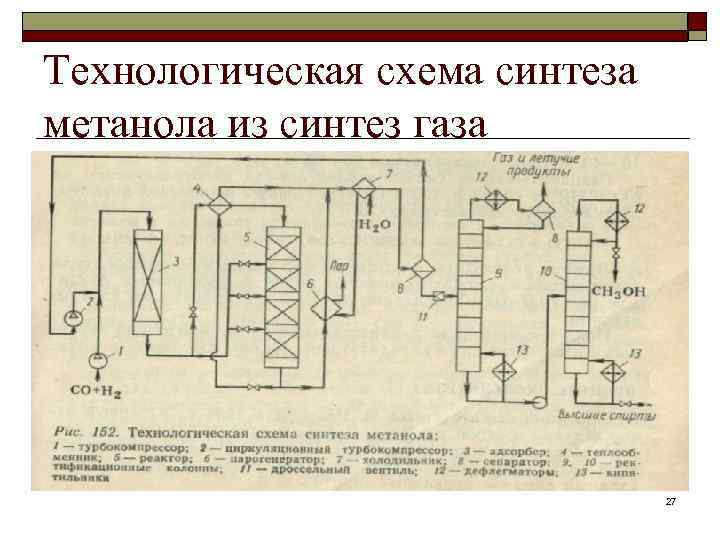
Технологическая схема синтеза метанола из синтез газа 27

ОПИСАНИЕ СХЕМЫ Очищенный синтез газ сжимают турбокомпрессором 1 до 5— 10 МПа и смешивают с циркулирующим газом, который дожимают до рабочего давления циркуляционным турбокомпрес сором . Смесь проходит адсорбер 3, предназначенный для очистки газа от 2 пентакарбонила железа. Это вещество обра зуется при взаимодействии СО с железом аппаратуры и разла гается в реакторе с образованием мелкодисперсного железа, катализирующего нежелательные реакции получения СН 4 и С 02. По этой причине, а также из за водородной коррозии реактор выполняют из легированной стали. Газ после адсорбера разделяют на два потока: один подо гревают в теплообменнике и подают на синтез в верхнюю 4 часть реактора 5, а другой вводят в реактор 5 между слоями катализатора в холодном виде для регулирования температуры и отвода тепла. Газ проходит сверху вниз через все слои катализатора и выходит из реактора при « 300°С. Этот газ тоже разделяют на два потока: один проходит теп лообменник и служит для подогрева 4 части исходной смеси до температуры синтеза, а другой направляют в парогенератор 6, где его тепло используют для получения пара высокого давле ния. Потоки газа после этого объединяют и охлаждают в холо дильнике 7, где метанол конденсируется и отделяется от газа в сепараторе 8 высокого давления. Газ с верха сепаратора до жимают циркуляционным компрессором и 2 возвращают на синтез. Конденсат с низа сепаратора дросселируют до давления, близкого к атмосферному, и в ректификационной колонне 9 отделяют метанол от растворенных газов 28

и летучих продуктов (диметиловый эфир), которые идут на сжигание. В следующей ректификационной колонне 10 отгоняют метанол от небольшого количества тяжелых примесей (высшие спирты), которые также направляют на сжигание. Полученный товарный метанол имеет высокую степень чистоты (до 99, 95 % основного вещества) и получается с общим выходом до 95 % при учете всех потерь. 29

Изопропанол СН 3 СНОНСН 3 жидкость (т. кип. 82, 5°С), смешивающаяся с водой. Его пары дают с воздухом взрывоопасные смеси в пределах концентраций 2— 12% (об. ). Образует с водой азеотропную смесь, содержащую 88 % спирта и кипящую при 80, 3°С. Изопропанол нашел применение в качестве растворителя, заменяющего во многих случаях этанол. Кроме того, из него получают сложные эфиры, ацетон и т. д. Получают исключительно синтетическим путем, а именно гидратацией пропилена. 30
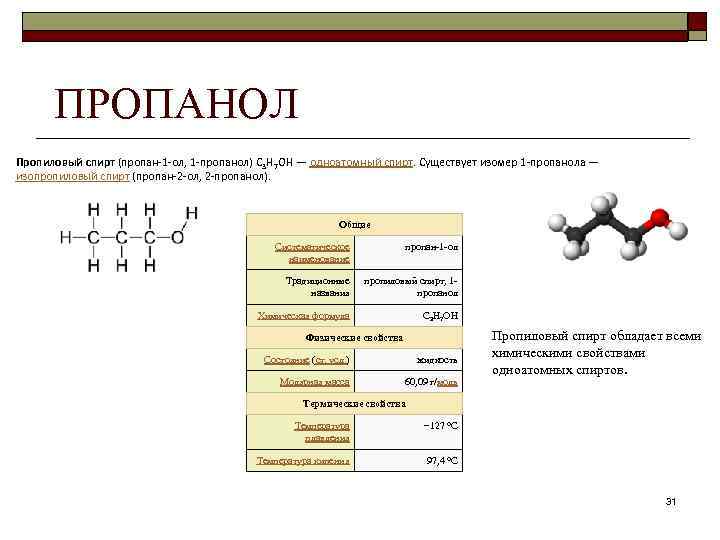
ПРОПАНОЛ Пропиловый спирт (пропан-1 -ол, 1 -пропанол) C 3 H 7 OH — одноатомный спирт. Существует изомер 1 -пропанола — изопропиловый спирт (пропан-2 -ол, 2 -пропанол). Общие Систематическое пропан 1 ол наименование Традиционные пропиловый спирт, 1 названия пропанол Химическая формула C 3 H 7 OH Физические свойства Пропиловый спирт обладает всеми Состояние (ст. усл. ) жидкость химическими свойствами одноатомных спиртов. Молярная масса 60, 09 г/моль Термические свойства Температура − 127 °C плавления Температура кипения 97, 4 °C 31

Промышленные способы получения н- пропанола, и изобутанола • Гидроформилирование ( оксосинтез) этилена с последующим гидрированием CH 2=CH 2 + CO + 2 H 2 → C 3 H 7 OH Первый этап: T 80— 120 °С, давление 2 МПа, катализатор: карбонил родия. Второй этап: Восстановление альдегидов в мягких условиях — при 50— 150°С (на никелевых и медьхромоксидных катализаторах) или при 200— 250°С (с сульфидами металлов) Гидрирование завершающая стадия превращения в спирты альдегидов, получаемых оксосинтезом из олефинов, СО и Н 2: 32
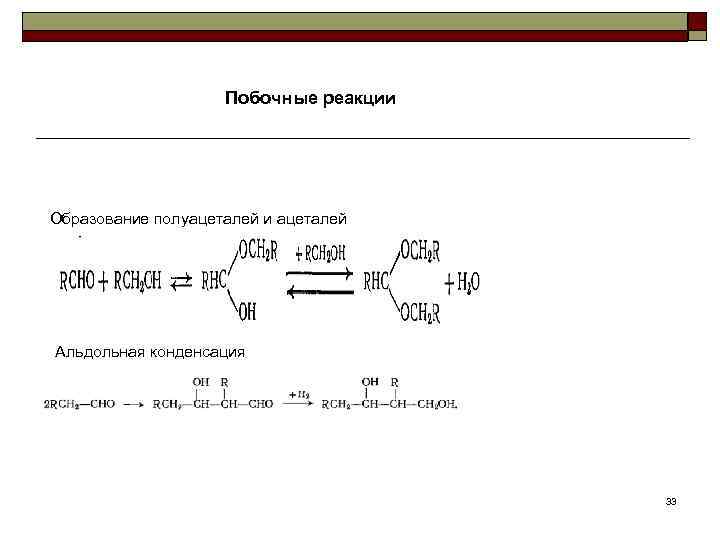
Побочные реакции Образование полуацеталей и ацеталей Альдольная конденсация 33

Гидроформилирование( оксосинтез) в гетерофазной среде, барботируя смесь СО и Н 2 через жидкую реакционную массу. Эти газы плохо растворимы в органических жидкостях, и для преодоления диффузионных сопротивлений очень важно достаточное перемешивание смеси. (применение избытка смеси СО + Н 2; коэффициент циркуляции (отношение рециркулята к свежему синтез газу) составляет (2/3): 1. ) Смесь СО + Н 2 обычно берут в стехиометрическом отношении (1: 1), требуемом для оксосинтеза. Селективность реакции растет при понижении температуры. большинство побочных реакций являются последовательными по отношению к образованию альдегидов. Чтобы снизить их роль, важно создать условия, при которых скорость гидроформилирования была бы высокой, а скорость конденсации альдегидов небольшой. Это достигается за счет неполной конверсии олефинов и применения растворителей — побочных продуктов реакции (кубовые остатки от перегонки, содержащие тримеры альдегидов, спирты и др. ), а также различных углеводородов (толуол и пентан гексановые фракции). 34
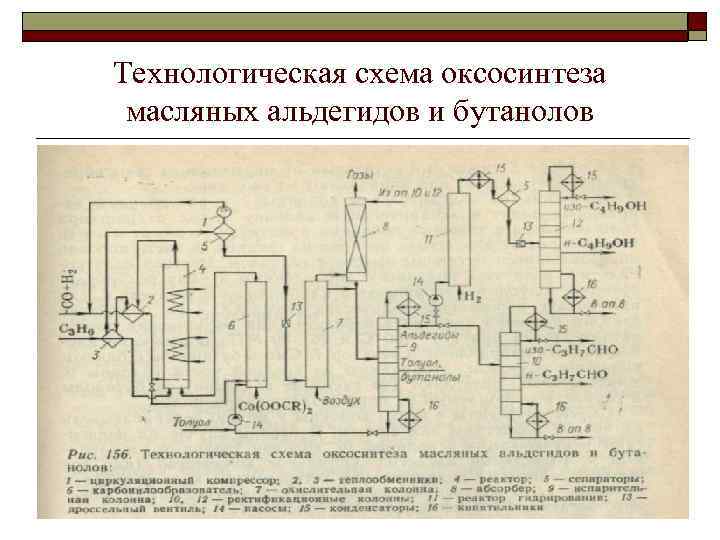
Технологическая схема оксосинтеза масляных альдегидов и бутанолов 35

Жидкая пропиленовая фракция, а также свежий синтез газ под давлением 25— 30 МПа и рециркулирующий синтез газ, сжатый до этого же давления циркуляционным компрессором /, подо гревают соответственно в теплообменниках и 3 за счет тепла 2 горячей реакционной массы. Затем они поступают в реактор 4, куда из карбонилообразователя 6 подают раствор карбонилов кобальта в толуоле и тяжелых остатках от перегонки продук тов. В реакторе при Т— 160°С происходит 4 образование альдегидов и побочных веществ, причем выделяющееся тепло отводят водой или кипящим водным конденсатом (в зависимости от температуры) с получением пара низкого давления. Тепло реакционной массы используют в теплообменниках 2 и 3, а в сепараторе 5 отделяют жидкость от синтез газа, который вместе с частью непревращенного пропилена возвращают на реакцию компрессором /. Жидкость из сепаратора дроссели руют до 0, 2— 0, 4 МПа и при 40— 70 °С окисляют небольшим количеством воздуха в окислительной колонне 7 (декобальти зёр). Вместе с воздухом, обедненным кислородом, в газовую фазу в этой колонне переходят СО, Нг и пропилен, находив шиеся в растворенном состоянии при высоком давлении, а так же пары альдегидов, унесенные газом. Последние поглощают в абсорбере 8 тяжелыми остатками от перегонки, а газы сбрасывают в атмосферу или направляют на сжигание 36

Жидкость из окислительной колонны 7 и абсорбера 8 направляют далее в испарительную колонну 9, где от раствора соли кобальта в тяжелых побочных продуктах отгоняют с верха колонны сырые альдегиды, отбирая из средней ее части побочно образовавшиеся бутанолы вместе с толуолом. Раствор соли ко бальта с низа этой колонны с добавленным к нему рециркулирующим толуолом направляют в карбонилообразователь 6, где при подаче небольшого количества смеси СО + Н 2 и добавке свежего раствора нафтената кобальта (для восполнения потерь катализатора) при 170— 180°С и 25— 30 МПа образуются карбонилы. Их направляют в реактор 4. Смесь бутанолов с близко кипящим толуолом, отбираемую из средней части колонны 9, дополнительно разделяют (на схеме не показано) на бутанолы и толуол, возвращаемый на приготовление карбонилов. Сырые альдегиды с верха колонны 9 можно перерабатывать на чистые альдегиды или спирты. В первом случае их подвер гают ректификации в колонне 10, получая товарные изомасляный и масляный альдегид. Остальное количество (или все сырые альдегиды) гидрируют на гетерогенном катализаторе в реакторе 11, а полученные изо- и м бутанол отделяют от тяжелого остатка в ректификационной колонне 12. 37

ПРОИЗВОДСТВО ИЗОПРОПАНОЛА 1. Газофазная гидратация с фосфорнокислотным катализатором. CH 3 CH=CH 2 + H 2 O → CH 3 CH(OH)CH 3 2. Ввиду более высокой реакционной способности пропилена температура реакции 200°С, когда равновесие более благоприятно для гидратации. Поэтому давление при синтезе можно снизить до 2— 3 МПа. 3. При этом, чтобы предотвратить чрезмерное образование диизопропилового эфира, приходится ограничивать степень конверсии водяных паров уровнем 4— 5%, что позволяет после конденсации получать 15— 20 %-й спирт. 4. степень конверсии пропилена достигается регулированием состава исходной смеси: при синтезе изопропанола, в отличие от гидратации этилена, используют избыток водяного пара и доводят степень конверсии пропилена до 10— 12 %. Все это существенно улучшает технико экономические показатели производства по сравнению с прямой гидратацией этилена и тем более с сернокислотным методом. 38

2. При жидкофазной гидратации пропилена ----катализатор сульфокатионит (сульфированный сопо лимер стирола с дивинилбензолом; размер частиц 0, 2— 0, 9 мм). Он активен для гидратации пропилена уже при 130— 150°С. При Р— 10 МПа и мольном отношении Н 20 : С 3 Н 6 = (12, 5— 15) : 1 степень конверсии пропилена достигает 75— 80% Реактор с четырьмя слоями катализатора (рис. 63) при прямоточном движении (сверху вниз) газообразного пропилена и воды, омывающей зерна катализатора. Для регулирования температуры снимают выделяющееся тепло за счет подачи части воды в недостаточно подогретом состоянии между слоями катализатора. Одновременно это позволяет создать близкий к оптимальному для обратимой экзотермической реакции профиль температуры, понижающейся по мере протекания реакции. Другой жидкофазный процесс основан на применении в качестве катализатора поли -вольфрамовой кислоты при 240— 270 СС и 15— 20 МПа, когда степень конверсии пропилена составляет 60— 70%, а селективность по изопропанолу доходит до 98 % Рис. 63. Реакционный узел для гидратации пропилена на сульфокатионите 39

Аналогичным образом прямой гидратацией н бутенов можно получать втор- бутанол. Существует и способ прямой гидратации изобутена на сульфокатионите, являющийся составной частью переработки С 4 фракций и служащий для извлечения изобутена. 40

Синтез н бутанола из ацетальдегида. При альдольной конденсации ацетальдегида образуется гидроксимасляный альдегид, называемый просто альдолем: Его используют как промежуточный продукт для получения бутандиола 1, 3, кротонового альдегида и н бутанола. Предлагался также метод синтеза бутадиена через альдоль (метод Остромысленского), сейчас, потерявший значение: 41

Практическое значение имеет только синтез н бутанола. Его экономичнее получать оксосинтезом из пропилена, СО и Н 2 Конденсацию ацетальдегида проводят при 20— 300 С в присутствии 0, 05 % щелочи. Чтобы избежать образования высших продуктов конденсации, степень конверсии ацетальдегида ограничивают 40— 60% При этом в реакционной массе находится не сам альдоль, а его циклический ацеталь с исходным ацетальдегидом (производное 1, 3 диоксана Ацеталь разлагается при перегонке на альдоль и ацетальдегид Для синтеза кротонового альдегида и далее н бутанола, подкисляют реакционную массу уксусной или фосфорной кислотой; тогда при перегонке не только разлагается ацеталь, но и происходит дегидратация альдоля в кротоновый альдегид. После отгонки ацетальдегида кротоновый альдегид перегоняют в виде азеотропной смеси с 10 % воды. Выход альдегида достигает 90 %. Спирты применяют как растворители, в том числе в виде сложных эфиров уксусной кислоты (особенно н бутилацетат). н Бутанол, кроме того, используют для получения трибутилфталата (пластификатор), трибутилфосфата (экстрагент). 42

Производство 2 -этилгексанола Сложные эфиры которого широко применяют как пластификаторы полимеров, как смазочные масла и присадки. Получают альдольной конденсацией н-масляного альдегида с последующей дегидратацией в 2 -этилгексеналь и гидрированием последнего в 2 - этилгексанола 43
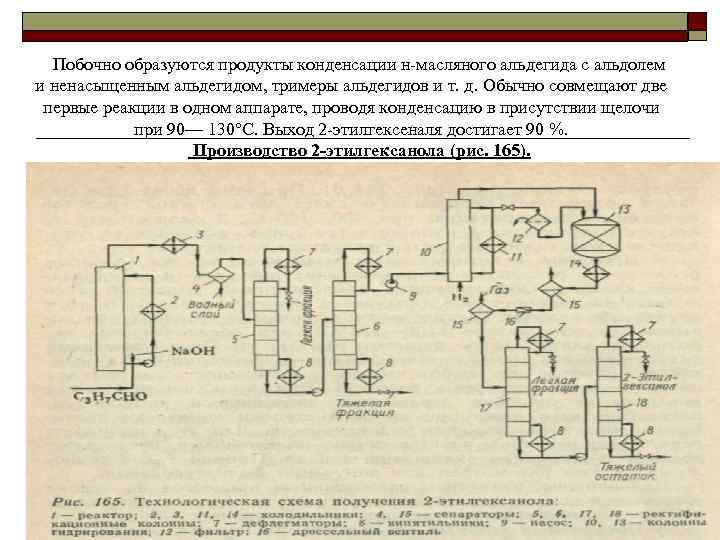
Побочно образуются продукты конденсации н масляного альдегида с альдолем и ненасыщенным альдегидом, тримеры альдегидов и т. д. Обычно совмещают две первые реакции в одном аппарате, проводя конденсацию в присутствии щелочи при 90— 130°С. Выход 2 этилгексеналя достигает 90 %. Производство 2 -этилгексанола (рис. 165). 44

Описание технологической схемы производства 2 -этилгексанола К н масляному альдегиду, поступающему в реактор1, непосредственно перед введением в реактор дозируют 40% й Na. OH (0, 05%). Тем пературный режим в реакторе (100— 130°С) поддерживают за счет выделяющегося тепла, избыток которого снимают путем циркуляции реакционной массы через выносной холодильник 2. В реакторе происходят альдолизация и дегидратация альдоля с образованием 2 этилгексеналя. Продукты реакции охлаждают в холодильнике 3, после чего они расслаиваются в сепараторе 4 на нижний (водный) и верхний (органический) слой. Воду на правляют на отпаривание органических веществ и затем на очистку. Органический слой подвергают ректификации в колон нах 5 и 6, отгоняя вначале легкий погон (непревращенныймасляный альдегид, остатки воды и др. ), а затем (в вакууме) 2 этилгексеналь, выводя из куба колонны 6 тяжелые побочные продукты. 2 Этнлгексеналь подвергают затем гидрированию. Чтобы избежать в дальнейшем потемнения эфиров 2 этилгексанола и полимерных материалов (к которым эти эфиры добавляют как пластификаторы), гидрирование нужно вести до высокой степени насыщения как двойных связей, так и альдегидных групп. По этой причине гидрирование проводят в две стадии в жидкой фазе под давлением 2— 3 МПа. 45

Первую ступень гидрирования проводят в колонне 10 с суспендированным в жидкости смешанным металлоксидным катализатором. Тепло реакции отводится за счет нагревания водо рода, частичного испарения и циркуляции смеси через выносной холодильник 11. Вторая стадия (дегидрирование) ведется в адиабатических условиях в аппарате 13 со стационарным слоем катализатора Ni • Cr 2 0 3 , причем жидкость из реактора 10 предварительно освобождается от взвешенного катализатора в фильтре 12. После охлаждения газожидкостную смесь из ре актора 3 разделяют в сепараторе 15, после которого водород дожимают 1 до рабочего давления и возвращают в реактор пер вой тадии, а жидкость с дросселируют и направляют на рек тификацию Ректификация проводится под вакуумом в колоннах 17 и /5. Вначале отгоняют легкий погон и затем отделяют технически чистый 2 этилгексанол от тяжелого остатка, направляемого на сжигание. Выход продукта составляет 85— 90 % 46

Более новые способы синтеза 2 - этилгексанола состоят в совмещении оксосинтеза масляных альдегидов с альдольной конденсацией и дегидратацией (альдокс процесс), когда к карбонилам кобальта добавляют щелочь, катализирующую две последние реакции. Предложен и другой процесс, совмещающий гидроформилирование, альдольную конденсацию, дегидратацию и гидрирование. Это удается осуществить в присутствии щелочи и при катализе карбонилами кобальта, модифицированными трибутилфосфином. 47

Применение спиртов в качестве топлива Для топливных целей в настоящий момент используются в промышленных объёмах три спирта: метанол, этанол и бутанол, что связано, прежде всего, с их коммерческой доступностью и возможностью массового производства из растительного сырья (кроме метанола. При этом возможно использование спиртов в виде горючего в чистом виде, в виде различных смесей с бензином или дизельным топливом а также в качестве оксигенирующих добавок (до 10 %) с целью повышения октанового числа и снижения токсичности отработанных газов Также отдельным направлением является использование метанола для переэтерификации жиров в производстве биодизеля Основные причины, послужившие активному изучению спиртов в качестве альтернативного горючего, это: рост цен на нефть и газ, исчерпаемость этих ресурсов в ближайшем будущем; спирты обладают высокими эксплуатационными характеристиками, а продукты сгорания содержат меньше вредных веществ; спирты могут изготавливаться биохимическим методом из отходов пищевой, деревообрабатывающей и целлюлозно бумажной промышленности, тем самым попутно решая проблему утилизации. 48

Массовое использование вышеуказанных спиртов в качестве моторного топлива, помимо чисто экономических причин, имеет ряд недостатков: метанол и этанол обладают по сравнению с бензином меньшей энергоэффективностью и, соответственно, обеспечивают больший расход; низкие температуры кипения спиртов могут служить причиной образования паровых пробок, что может существенно усложнить работу двигателя; гигроскопичность спиртов, а также их растворимость в воде может привести к резкому снижению мощности при попадании влаги в топливную систему; спирты обладают существенно более высокими коррозионными характеристиками по сравнению с углеводородами; относительно высокая скрытая теплота сгорания метанола и этанола может служить причиной проблемы при смешении этих спиртов с воздухом и дальнейшей транспортировки через впускной коллектор двигателя. 49
Тема4 метанол и др. спирты.ppt
- Количество слайдов: 49

