Металлы..pptx
- Количество слайдов: 30
 Металлы Выполнила: Полещук Наталья, 27 гр
Металлы Выполнила: Полещук Наталья, 27 гр
 Определение Металлы – это химические элементы, атом которых отдают электроны внешн (а иногда и предвнешнего) электронного слоя, превращаясь положительные ионы. Из 114 элементов, 92 - металлы.
Определение Металлы – это химические элементы, атом которых отдают электроны внешн (а иногда и предвнешнего) электронного слоя, превращаясь положительные ионы. Из 114 элементов, 92 - металлы.
 Изменение свойств металлов относительно их положения в таблице Менделеева В главной подгруппе - число электронов на внешнем слое не изменяется - радиус атома увеличивается - электроотрицательность уменьшает - восстановительные свойства усилив - металлические свойства усиливают
Изменение свойств металлов относительно их положения в таблице Менделеева В главной подгруппе - число электронов на внешнем слое не изменяется - радиус атома увеличивается - электроотрицательность уменьшает - восстановительные свойства усилив - металлические свойства усиливают
 Изменение свойств металлов относительно их положения в таблице Менделеева В периоде - число электронов на внешнем слое увеличивается - радиус атома уменьшается - электроотрицательность увеличива - восстановительные свойства умень - металлические свойства ослабеваю - заряды ядер атомов увеличиваются
Изменение свойств металлов относительно их положения в таблице Менделеева В периоде - число электронов на внешнем слое увеличивается - радиус атома уменьшается - электроотрицательность увеличива - восстановительные свойства умень - металлические свойства ослабеваю - заряды ядер атомов увеличиваются
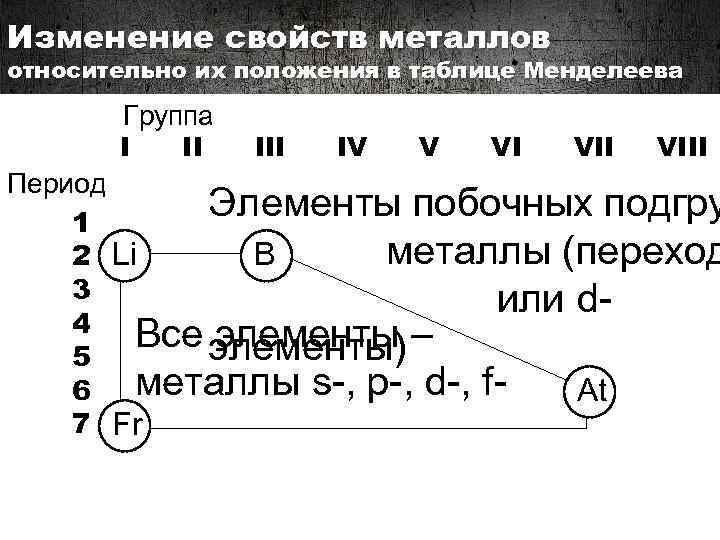 Изменение свойств металлов относительно их положения в таблице Менделеева Группа I II IV V VI VIII Период Элементы побочных подгру 1 металлы (переход B 2 Li 3 или d 4 Все элементы) – элементы 5 металлы s-, p-, d-, f 6 At 7 Fr
Изменение свойств металлов относительно их положения в таблице Менделеева Группа I II IV V VI VIII Период Элементы побочных подгру 1 металлы (переход B 2 Li 3 или d 4 Все элементы) – элементы 5 металлы s-, p-, d-, f 6 At 7 Fr
 Металлический вид химической связи Металлическая связь это связь в металлах и сплавах между том-ионами металлов, расположенным в узлах кристаллической решётки - мало валентных электронов - много пустых валентных орбиталей - орбитали перекрываются, и электроны становятся общими
Металлический вид химической связи Металлическая связь это связь в металлах и сплавах между том-ионами металлов, расположенным в узлах кристаллической решётки - мало валентных электронов - много пустых валентных орбиталей - орбитали перекрываются, и электроны становятся общими
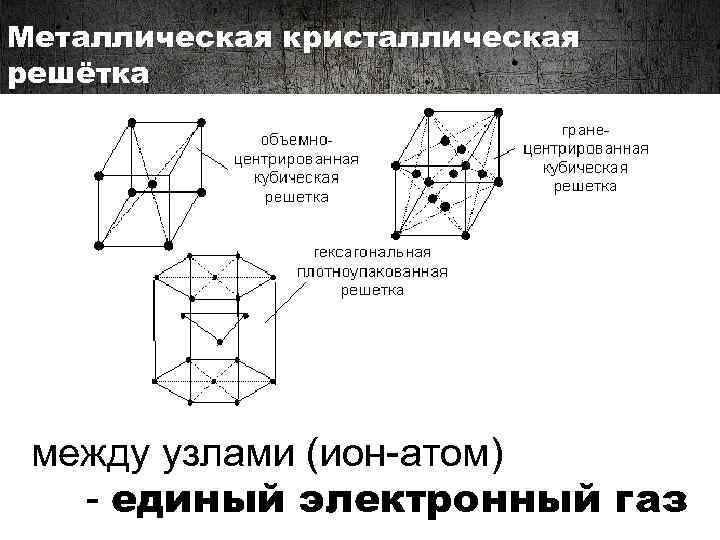 Металлическая кристаллическая решётка между узлами (ион-атом) - единый электронный газ
Металлическая кристаллическая решётка между узлами (ион-атом) - единый электронный газ
 Универсальные физические свойства - ковкость и пластичность - металлический блеск и непрозра - электропроводимость - теплопроводность - плотность, прочность, t° плавлен
Универсальные физические свойства - ковкость и пластичность - металлический блеск и непрозра - электропроводимость - теплопроводность - плотность, прочность, t° плавлен
 Аллотропия - полиморфизм Аллотропия - это полиморфизм (свойство существовать в нескольких кристаллических модификациях) у простых веществ. Причина полиморфизма - перестройка кристаллической решётки, под оздействием температуры или давлени
Аллотропия - полиморфизм Аллотропия - это полиморфизм (свойство существовать в нескольких кристаллических модификациях) у простых веществ. Причина полиморфизма - перестройка кристаллической решётки, под оздействием температуры или давлени
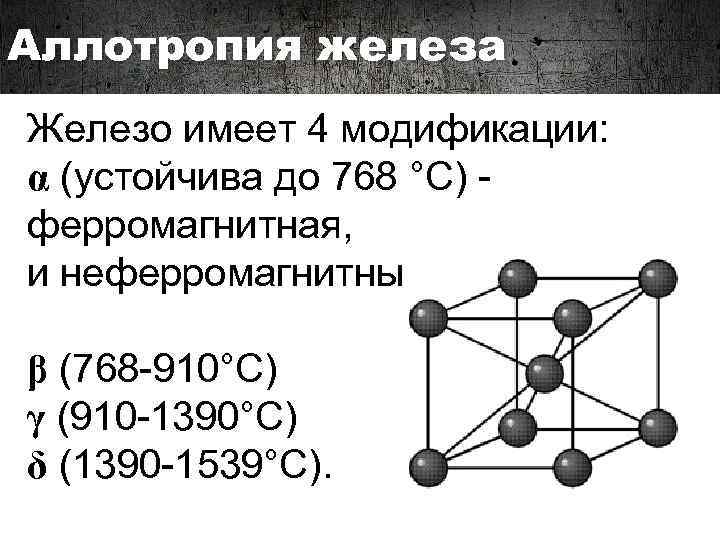 Аллотропия железа Железо имеет 4 модификации: α (устойчива до 768 °C) ферромагнитная, и неферромагнитные: β (768 -910°C) γ (910 -1390°C) δ (1390 -1539°C).
Аллотропия железа Железо имеет 4 модификации: α (устойчива до 768 °C) ферромагнитная, и неферромагнитные: β (768 -910°C) γ (910 -1390°C) δ (1390 -1539°C).
 Ряд активности металлов В 1865 году Николай Николаевич Бекетов составил ряд электроотрицательн ости металлов (электрохимический ряд активности, ряд напряжений).
Ряд активности металлов В 1865 году Николай Николаевич Бекетов составил ряд электроотрицательн ости металлов (электрохимический ряд активности, ряд напряжений).
 Ряд активности металлов Справа налево от водорода у элементов усиливаются восстановительные свойства, а слева направо окислительные.
Ряд активности металлов Справа налево от водорода у элементов усиливаются восстановительные свойства, а слева направо окислительные.
 Получение металлов Пирометаллургия - это восстановление металлов из руд при высоких температурах. Sn. O 2 + 2 C → Sn + 2 CO ↑ Cu 2 O + C → 2 Cu + CO ↑
Получение металлов Пирометаллургия - это восстановление металлов из руд при высоких температурах. Sn. O 2 + 2 C → Sn + 2 CO ↑ Cu 2 O + C → 2 Cu + CO ↑
 Получение металлов Гидрометаллургия - это восстановление металлов из солей в растворе. Cu. O + H 2 SO 4 → Cu. SO 4 + H 2 O ↓ Cu. SO 4 + Fe → Cu + Fe. SO 4
Получение металлов Гидрометаллургия - это восстановление металлов из солей в растворе. Cu. O + H 2 SO 4 → Cu. SO 4 + H 2 O ↓ Cu. SO 4 + Fe → Cu + Fe. SO 4
 Получение металлов Электрометаллургия - это восстановление металлов в процессе электролиза растворов или расплавов их соединений.
Получение металлов Электрометаллургия - это восстановление металлов в процессе электролиза растворов или расплавов их соединений.
 Электролиз - это окислительновосстановительный процесс, протекающий на электродах при прохождении электрического тока через расплав или раствор электролита. + + ē → Na 0 Na -― 2 Cl 2ē → Cl 2 ↑ + + 2 Cl- = 2 Na 0 + Cl 0 ↑ 2 Na 2 0
Электролиз - это окислительновосстановительный процесс, протекающий на электродах при прохождении электрического тока через расплав или раствор электролита. + + ē → Na 0 Na -― 2 Cl 2ē → Cl 2 ↑ + + 2 Cl- = 2 Na 0 + Cl 0 ↑ 2 Na 2 0
 Химические свойства взаимодействие с простыми веществами: кислород - образуются оксиды, пероксиды и надпероксиды 4 Li + O 2 = 2 Li 2 O оксид лития 2 Na + O 2 = Na 2 O 2 пероксид натрия K + O 2 = KO 2 надпероксид калия
Химические свойства взаимодействие с простыми веществами: кислород - образуются оксиды, пероксиды и надпероксиды 4 Li + O 2 = 2 Li 2 O оксид лития 2 Na + O 2 = Na 2 O 2 пероксид натрия K + O 2 = KO 2 надпероксид калия
 Химические свойства взаимодействие с простыми веществами: галогены - образуются соли галогеноводородных кислот Mg + Cl 2 = Mg. Cl 2 хлорид магния 2 Fe + 3 Cl 2 = 2 Fe. Cl 3 железа(III) хлорид
Химические свойства взаимодействие с простыми веществами: галогены - образуются соли галогеноводородных кислот Mg + Cl 2 = Mg. Cl 2 хлорид магния 2 Fe + 3 Cl 2 = 2 Fe. Cl 3 железа(III) хлорид
 Химические свойства взаимодействие с простыми веществами: водород - самые активные металлы образуют гидриды Ca 0 + H 20 → Ca+2 H 2 -1 гидрид кальция взаимодействие с простыми веществами: сера - образуются соли-сульфиды 0 + S 0 → Fe+2 S-2 сульфид Fe железа (ii)
Химические свойства взаимодействие с простыми веществами: водород - самые активные металлы образуют гидриды Ca 0 + H 20 → Ca+2 H 2 -1 гидрид кальция взаимодействие с простыми веществами: сера - образуются соли-сульфиды 0 + S 0 → Fe+2 S-2 сульфид Fe железа (ii)
 Химические свойства взаимодействие с простыми веществами: азот - образуются нитриды 6 Li 0 + N 20 = 2 Li 3+1 N-3 нитрид лития взаимодействие с кислотами - при взаимодействии кислот с металлами, стоящими в ряду активности металлов до H, образуется соль и H 2 0 + 6 H+1 Cl → 2 Al
Химические свойства взаимодействие с простыми веществами: азот - образуются нитриды 6 Li 0 + N 20 = 2 Li 3+1 N-3 нитрид лития взаимодействие с кислотами - при взаимодействии кислот с металлами, стоящими в ряду активности металлов до H, образуется соль и H 2 0 + 6 H+1 Cl → 2 Al
 Химические свойства взаимодействие с концентрированной серной кислотой Na + H 2 SO 4→ Na. SO 4 + -H 2 O+SO 2 кислота взаимодействует по разбавленная обычной схеме, при увеличении концентрации, помимо соли и воды образуются кислоты и простые элементы.
Химические свойства взаимодействие с концентрированной серной кислотой Na + H 2 SO 4→ Na. SO 4 + -H 2 O+SO 2 кислота взаимодействует по разбавленная обычной схеме, при увеличении концентрации, помимо соли и воды образуются кислоты и простые элементы.
 Химические свойства взаимодействие с азотной кислотой Cu+4 HNO 3(60%)=Cu(NO 3)2 +2 NO 2 +2 H 2 O Zn+4 HNO 3(60%)=Zn(NO 3)2 +2 NO 2 +2 H 2 O Концентрированные HNO 3 и H 2 SO 4 пассивируют металл(Fe, Cr, Al).
Химические свойства взаимодействие с азотной кислотой Cu+4 HNO 3(60%)=Cu(NO 3)2 +2 NO 2 +2 H 2 O Zn+4 HNO 3(60%)=Zn(NO 3)2 +2 NO 2 +2 H 2 O Концентрированные HNO 3 и H 2 SO 4 пассивируют металл(Fe, Cr, Al).
 Химические свойства взаимодействие с водой - щелочные металлы вытесняют водород из воды и образуют растворимые основания - щелочи. 2 Na + 2 H 2 O = 2 Na. OH + H 2 -↑ другие металлы, стоящие в ряду напряжений до водорода, вытесняют воду при кипячении(Mg), удалении оксидной плёнки(Al) или в раскалённом виде(Fe) с образованием железной окалины (Fe+2 Fe 2+3). t 3 Fe + 4 H 2 O → (Fe. Fe 2)O 4 +
Химические свойства взаимодействие с водой - щелочные металлы вытесняют водород из воды и образуют растворимые основания - щелочи. 2 Na + 2 H 2 O = 2 Na. OH + H 2 -↑ другие металлы, стоящие в ряду напряжений до водорода, вытесняют воду при кипячении(Mg), удалении оксидной плёнки(Al) или в раскалённом виде(Fe) с образованием железной окалины (Fe+2 Fe 2+3). t 3 Fe + 4 H 2 O → (Fe. Fe 2)O 4 +
 Коррозия металлов Коррозия - это самопроизвольное разрушение металлов и сплавов под воздействием окружающей среды.
Коррозия металлов Коррозия - это самопроизвольное разрушение металлов и сплавов под воздействием окружающей среды.
 Коррозия металлов Химическая коррозия - в среде, не проводящей электрический ток, при взаимодействии металлов с сухими газами и жидкостяминеэлектролитами. 4 Fe + 3 O 2 → 2 Fe 2 O 3 t 2 Fe + 3 SO 2 + 3 O 2 →
Коррозия металлов Химическая коррозия - в среде, не проводящей электрический ток, при взаимодействии металлов с сухими газами и жидкостяминеэлектролитами. 4 Fe + 3 O 2 → 2 Fe 2 O 3 t 2 Fe + 3 SO 2 + 3 O 2 →
 Коррозия металлов Электрохимическая коррозия - в токопроводящей среде, с возникновением внутри системы электрического тока. 0 Fe + 2 e → 2+(анод) Fe - окисление металла при соприкосновении с электролитом, переход его катионов в электролит
Коррозия металлов Электрохимическая коррозия - в токопроводящей среде, с возникновением внутри системы электрического тока. 0 Fe + 2 e → 2+(анод) Fe - окисление металла при соприкосновении с электролитом, переход его катионов в электролит
 Коррозия металлов Способы борьбы с коррозией:
Коррозия металлов Способы борьбы с коррозией:
 Коррозия металлов Способы борьбы с коррозией: Также используется шлифование поверхности, сплавы с хромом, никелем и деаэрация
Коррозия металлов Способы борьбы с коррозией: Также используется шлифование поверхности, сплавы с хромом, никелем и деаэрация
 Коррозия металлов Способы борьбы с коррозией: Оцинкованное ведро — изделие Процесс покрытия защитны из стали, защищённое цинковым составом конструкций мост покрытием от коррозии.
Коррозия металлов Способы борьбы с коррозией: Оцинкованное ведро — изделие Процесс покрытия защитны из стали, защищённое цинковым составом конструкций мост покрытием от коррозии.



