Металлы_34слайда.ppt
- Количество слайдов: 34

 Металлы С давних пор простые вещества разделяли на металлы и неметаллы. В средние века было известно всего 7 металлов: Au, Ag, Cu, Sn, Pb, Fe, Hg. К металлам относили вещества с характерным «металлическим» блеском, ковкие. По мере развития химии было обнаружено много других отличительных свойств, присущих металлам.
Металлы С давних пор простые вещества разделяли на металлы и неметаллы. В средние века было известно всего 7 металлов: Au, Ag, Cu, Sn, Pb, Fe, Hg. К металлам относили вещества с характерным «металлическим» блеском, ковкие. По мере развития химии было обнаружено много других отличительных свойств, присущих металлам.
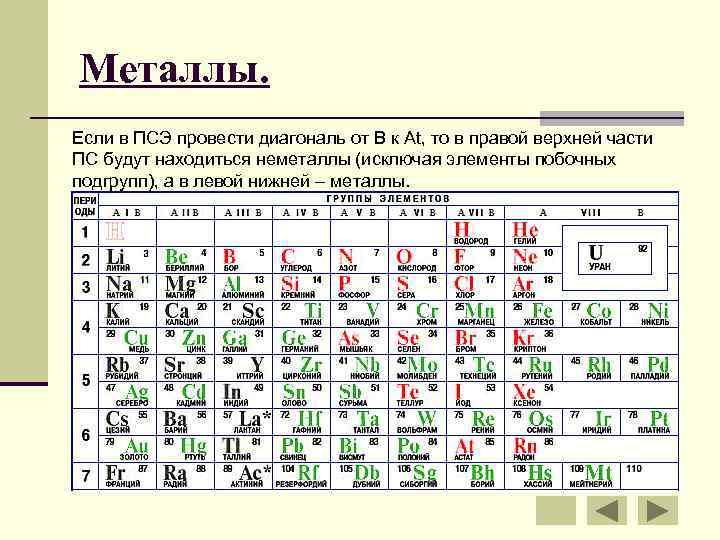 Металлы. Если в ПСЭ провести диагональ от B к At, то в правой верхней части ПС будут находиться неметаллы (исключая элементы побочных подгрупп), а в левой нижней – металлы.
Металлы. Если в ПСЭ провести диагональ от B к At, то в правой верхней части ПС будут находиться неметаллы (исключая элементы побочных подгрупп), а в левой нижней – металлы.
 Металлы. Элементы, расположенные вблизи диагонали (Al, Ti, Ga, Nb, Sb и другие), обладают двойственным характером (промежуточными свойствами). То есть к металлам относятся: все s - элементы (I и II гр. ), все d- и f- элементы, а также p-элементы главных подгрупп: III (кроме B), IV (Sn, Pb), V (Sb, Bi) и VI (Po). Т. о. из 118 элементов 96 являются металлами.
Металлы. Элементы, расположенные вблизи диагонали (Al, Ti, Ga, Nb, Sb и другие), обладают двойственным характером (промежуточными свойствами). То есть к металлам относятся: все s - элементы (I и II гр. ), все d- и f- элементы, а также p-элементы главных подгрупп: III (кроме B), IV (Sn, Pb), V (Sb, Bi) и VI (Po). Т. о. из 118 элементов 96 являются металлами.
 Металлы. Нахождение в природе Самыми распространёнными металлами в земной коре являются: 7% - Al 5% - Fe 4% - Ca по 2% - Na, K, Mg Ag-1∙ 10 -5% Au- 5∙ 10 -7% Pt- 5∙ 10 -8% Содержание остальных металлов незначительно: 0, 3 % - Cr 0, 2 % - Ni 0, 01 % - Cu
Металлы. Нахождение в природе Самыми распространёнными металлами в земной коре являются: 7% - Al 5% - Fe 4% - Ca по 2% - Na, K, Mg Ag-1∙ 10 -5% Au- 5∙ 10 -7% Pt- 5∙ 10 -8% Содержание остальных металлов незначительно: 0, 3 % - Cr 0, 2 % - Ni 0, 01 % - Cu
 Металлы. Нахождение в природе Металлы встречаются в природе как в свободном виде, так и в соединениях: Щелочные, щелочно-земельные (до Ni) – в виде солей, металлы средней активности – в виде оксидов. Ag, Pt, Au - в свободном виде
Металлы. Нахождение в природе Металлы встречаются в природе как в свободном виде, так и в соединениях: Щелочные, щелочно-земельные (до Ni) – в виде солей, металлы средней активности – в виде оксидов. Ag, Pt, Au - в свободном виде
 Металлы. Физические свойства 1) Все металлы ( за исключением Hg, Cs и Ga ) в обычных условиях являются твёрдыми веществами. Натрий – мягкий металл, его можно резать ножом
Металлы. Физические свойства 1) Все металлы ( за исключением Hg, Cs и Ga ) в обычных условиях являются твёрдыми веществами. Натрий – мягкий металл, его можно резать ножом
 Металлы. Физические свойства 2) Высокая электро- и теплопроводность Это обусловлено наличием в металлических решётках свободно перемещающихся электронов, которые в электрическом поле легко приобретают направленное движение. Лучшими проводниками являются: Ag, Cu и Al. При повышении tº электропроводность и теплопроводность металлов понижается, т. к. усиливаются колебания атомов, что затрудняет направленное движение электронов. Hо при понижении tº электропроводность растёт и вблизи абсолютного 0 переходит в сверхпроводимость.
Металлы. Физические свойства 2) Высокая электро- и теплопроводность Это обусловлено наличием в металлических решётках свободно перемещающихся электронов, которые в электрическом поле легко приобретают направленное движение. Лучшими проводниками являются: Ag, Cu и Al. При повышении tº электропроводность и теплопроводность металлов понижается, т. к. усиливаются колебания атомов, что затрудняет направленное движение электронов. Hо при понижении tº электропроводность растёт и вблизи абсолютного 0 переходит в сверхпроводимость.
 Металлы. Физические свойства 3) Ковкость и пластичность. Многие металлы пластичны и обладают хорошей ковкостью, что объясняется особенностью металлической связи; т. к. атомы в металлической решётке непосредственно не связаны друг с другом, отдельные слои могут перемещаться один относительно другого. Это свойство металлов используется при их механической обработке. Ковкие: щелочные металлы, Au, Ag, Cu. Хрупкие: Cr, Mn, Sb…- т. к. у атомов этих элементов по 5 -7 свободных электронов, которые препятствуют свободному перемещению слоёв атомов.
Металлы. Физические свойства 3) Ковкость и пластичность. Многие металлы пластичны и обладают хорошей ковкостью, что объясняется особенностью металлической связи; т. к. атомы в металлической решётке непосредственно не связаны друг с другом, отдельные слои могут перемещаться один относительно другого. Это свойство металлов используется при их механической обработке. Ковкие: щелочные металлы, Au, Ag, Cu. Хрупкие: Cr, Mn, Sb…- т. к. у атомов этих элементов по 5 -7 свободных электронов, которые препятствуют свободному перемещению слоёв атомов.
 Металлы. Физические свойства 4) Плотность различна. Она тем меньше, чем меньше атомная масса элемента – металла и чем больше радиус атома. Самый лёгкий: Li = 0, 53 г/см 3 Самый тяжёлый: Os = 22, 6 г/см 3 < 5 г/см 3 - лёгкие металлы > 5 г/см 3 - тяжёлые металлы. Металлический рубидий в ампуле
Металлы. Физические свойства 4) Плотность различна. Она тем меньше, чем меньше атомная масса элемента – металла и чем больше радиус атома. Самый лёгкий: Li = 0, 53 г/см 3 Самый тяжёлый: Os = 22, 6 г/см 3 < 5 г/см 3 - лёгкие металлы > 5 г/см 3 - тяжёлые металлы. Металлический рубидий в ампуле
 Металлы. Физические свойства 5) tº плавления. Самые легкоплавкие: Hg t плавления = -38, 9 º C Cs t плавления = 29 º С Ga t плавления = 29, 8 º C Самый тугоплавкий: W t плавления = 3390 º C он применяется для изготовления нитей накаливания электроламп t плавления ‹ 1000 º C - легкоплавкие металлы. t плавления › 1000 º C - тугоплавкие. Металлический цезий в ампуле
Металлы. Физические свойства 5) tº плавления. Самые легкоплавкие: Hg t плавления = -38, 9 º C Cs t плавления = 29 º С Ga t плавления = 29, 8 º C Самый тугоплавкий: W t плавления = 3390 º C он применяется для изготовления нитей накаливания электроламп t плавления ‹ 1000 º C - легкоплавкие металлы. t плавления › 1000 º C - тугоплавкие. Металлический цезий в ампуле
 Металлы. Физические свойства 6) Отношение к магнитным полям а) Ферромагнитные – способные намагничиваться при действии слабых магнитных полей (Fe, Co, Ni…) б) Парамагнитные – проявляют слабую способность к намагничиванию (Al, Cr, Ti…) в) Диамагнитные – не притягивающиеся к магниту (Bi, Sn, Cu) и даже слегка отталкивающиеся от него.
Металлы. Физические свойства 6) Отношение к магнитным полям а) Ферромагнитные – способные намагничиваться при действии слабых магнитных полей (Fe, Co, Ni…) б) Парамагнитные – проявляют слабую способность к намагничиванию (Al, Cr, Ti…) в) Диамагнитные – не притягивающиеся к магниту (Bi, Sn, Cu) и даже слегка отталкивающиеся от него.
 Способы получения металлов Au, Pt – встречаются в виде самородных металлов. Ag, Cu, Hg, Sn – металлы, находящиеся в природе как в самородном состоянии, так и виде соединений. Остальные металлы, стоящие в ряду напряжений до Sn – только в виде соединений. Металлы получают из минералов или горных пород, содержащих металлы или их соединения – из руд. Минералы алюминия: Боксит Креолит Кристаллы хлорида натрия – минерал галит
Способы получения металлов Au, Pt – встречаются в виде самородных металлов. Ag, Cu, Hg, Sn – металлы, находящиеся в природе как в самородном состоянии, так и виде соединений. Остальные металлы, стоящие в ряду напряжений до Sn – только в виде соединений. Металлы получают из минералов или горных пород, содержащих металлы или их соединения – из руд. Минералы алюминия: Боксит Креолит Кристаллы хлорида натрия – минерал галит
 Ученые, занимающиеся получением металлов. Николай Николаевич Бекетов (1827 -1911) Русский химик и физик. Способствовал развитию физической химии как самостоятельной области науки. Открыл химический процесс вытеснения металлов из растворов их солей под действием других металлов и водорода.
Ученые, занимающиеся получением металлов. Николай Николаевич Бекетов (1827 -1911) Русский химик и физик. Способствовал развитию физической химии как самостоятельной области науки. Открыл химический процесс вытеснения металлов из растворов их солей под действием других металлов и водорода.
 Ученые, занимающиеся получением металлов. Гемфри Дэви (1778 -1829) Английский химик и физик. Один из основателей электрохимии. Путем электролиза солей и щелочей получил калий, натрий, барий, кальций, амальгаму (раствор металла в ртути) стронция и магния.
Ученые, занимающиеся получением металлов. Гемфри Дэви (1778 -1829) Английский химик и физик. Один из основателей электрохимии. Путем электролиза солей и щелочей получил калий, натрий, барий, кальций, амальгаму (раствор металла в ртути) стронция и магния.
 Металлы. Способы получения металлов Металлургия – наука о промышленных способах получения металлов из природного сырья. Металлургией также называют металлургическую промышленность. Современная металлургия получает более 75 металлов и сплавов на их основе В зависимости от способов получение металлов различают: -пирометаллургию -гидрометаллургию -электрометаллургию
Металлы. Способы получения металлов Металлургия – наука о промышленных способах получения металлов из природного сырья. Металлургией также называют металлургическую промышленность. Современная металлургия получает более 75 металлов и сплавов на их основе В зависимости от способов получение металлов различают: -пирометаллургию -гидрометаллургию -электрометаллургию
 Металлы. Способы получения металлов 1. Пирометаллургия - занимает ведущее место в металлургии. Она основана на реакциях восстановления при высокой tº. В качестве восстановителей применяют: уголь, активные металлы, CO, H 2, CH 4. Cu 2 O + C = 2 Cu + CO Cu 2 O + CO = 2 Cu + CO 2 Если руда – это сульфид металла, её предварительно переводят в оксид путём окислительного обжига: 2 Zn. S + 3 O 2 = 2 Zn. O + 2 SO 2 Zn. O + C = Zn + CO
Металлы. Способы получения металлов 1. Пирометаллургия - занимает ведущее место в металлургии. Она основана на реакциях восстановления при высокой tº. В качестве восстановителей применяют: уголь, активные металлы, CO, H 2, CH 4. Cu 2 O + C = 2 Cu + CO Cu 2 O + CO = 2 Cu + CO 2 Если руда – это сульфид металла, её предварительно переводят в оксид путём окислительного обжига: 2 Zn. S + 3 O 2 = 2 Zn. O + 2 SO 2 Zn. O + C = Zn + CO
 Пирометаллургия Если восстановитель металлотермия: - металл, процесс называется Cr 2 O 3 + 2 Al = 2 Cr + Al 2 O 3 Ti. Cl 4+ 2 Mg = Ti + 2 Mg. Cl 2 Этим способом получают металлы, которые с углеродом образуют карбиды – Mn, Cr, Ti, Mo, W и другие. Если восстановитель – H 2, процесс называют водородотермия. В этом случае получают металлы большой чистоты: Mo. O 3 + 3 H 2 = Mo + 3 H 2 O WO 3 + 3 H 2 = W + 3 H 2 O
Пирометаллургия Если восстановитель металлотермия: - металл, процесс называется Cr 2 O 3 + 2 Al = 2 Cr + Al 2 O 3 Ti. Cl 4+ 2 Mg = Ti + 2 Mg. Cl 2 Этим способом получают металлы, которые с углеродом образуют карбиды – Mn, Cr, Ti, Mo, W и другие. Если восстановитель – H 2, процесс называют водородотермия. В этом случае получают металлы большой чистоты: Mo. O 3 + 3 H 2 = Mo + 3 H 2 O WO 3 + 3 H 2 = W + 3 H 2 O
 Металлы. Способы получения металлов 2. Гидрометаллургия – способы получения металлов из растворов их солей. Металл, входящий в состав руды, сначала переводят в раствор, затем извлекают из раствора. Cu. O + H 2 SO 4= Cu. SO 4 + H 2 O Cu. SO 4 + Fe = Cu + Fe. SO 4 Этот метод позволяет получать металлы, не извлекая руду на поверхность: добывают: Au, Ag, Zn, Cd, U и другие. Например, Au (метод цианирования, из бедных руд) Руду, содержащую самородное золото обрабатывают KCN. Всё KCN золото переходит в раствор в виде растворимых комплексных соединений. Из раствора его извлекают вытеснением металлическим Zn, Al или электролизом.
Металлы. Способы получения металлов 2. Гидрометаллургия – способы получения металлов из растворов их солей. Металл, входящий в состав руды, сначала переводят в раствор, затем извлекают из раствора. Cu. O + H 2 SO 4= Cu. SO 4 + H 2 O Cu. SO 4 + Fe = Cu + Fe. SO 4 Этот метод позволяет получать металлы, не извлекая руду на поверхность: добывают: Au, Ag, Zn, Cd, U и другие. Например, Au (метод цианирования, из бедных руд) Руду, содержащую самородное золото обрабатывают KCN. Всё KCN золото переходит в раствор в виде растворимых комплексных соединений. Из раствора его извлекают вытеснением металлическим Zn, Al или электролизом.
 Металлы. Способы получения металлов 3. Электрометаллургия – способы получения металлов с помощью электролиза Т. о. получают лёгкие металлы - Al, Na и другие из их расплавленных оксидов или хлоридов. Электролиз также используют для очистки некоторых металлов. Из очищаемого металла изготавливают анод. При электролизе анод растворяется, ионы металла переходят в раствор, а на катоде они осаждаются. Примеси переходят в раствор. Так получаются электролитические чистые металлы: Cu, Ag, Fe, Ni, Pb и многие другие.
Металлы. Способы получения металлов 3. Электрометаллургия – способы получения металлов с помощью электролиза Т. о. получают лёгкие металлы - Al, Na и другие из их расплавленных оксидов или хлоридов. Электролиз также используют для очистки некоторых металлов. Из очищаемого металла изготавливают анод. При электролизе анод растворяется, ионы металла переходят в раствор, а на катоде они осаждаются. Примеси переходят в раствор. Так получаются электролитические чистые металлы: Cu, Ag, Fe, Ni, Pb и многие другие.
 Металлы. Способы получения металлов Электролиз расплава Mg. Cl 2: (-) катод: Mg 2+ + 2 е- = Mg (+) анод: 2 Cl- = 2 Cl + 2 е 2 Cl = 2 Cl 2 Mg 2++2 Cl= Mg + Cl 2 Электролиз – совокупность процессов, происходящих при прохождении электрического тока через электрохимическую систему. Электрохимическая система состоит из двух электродов (проводников 1 рода), раствора или расплава электролита (проводника 2 рода) и внешней цепи, соединяющей электроды.
Металлы. Способы получения металлов Электролиз расплава Mg. Cl 2: (-) катод: Mg 2+ + 2 е- = Mg (+) анод: 2 Cl- = 2 Cl + 2 е 2 Cl = 2 Cl 2 Mg 2++2 Cl= Mg + Cl 2 Электролиз – совокупность процессов, происходящих при прохождении электрического тока через электрохимическую систему. Электрохимическая система состоит из двух электродов (проводников 1 рода), раствора или расплава электролита (проводника 2 рода) и внешней цепи, соединяющей электроды.
 Способы получения металлов Доменная печь
Способы получения металлов Доменная печь
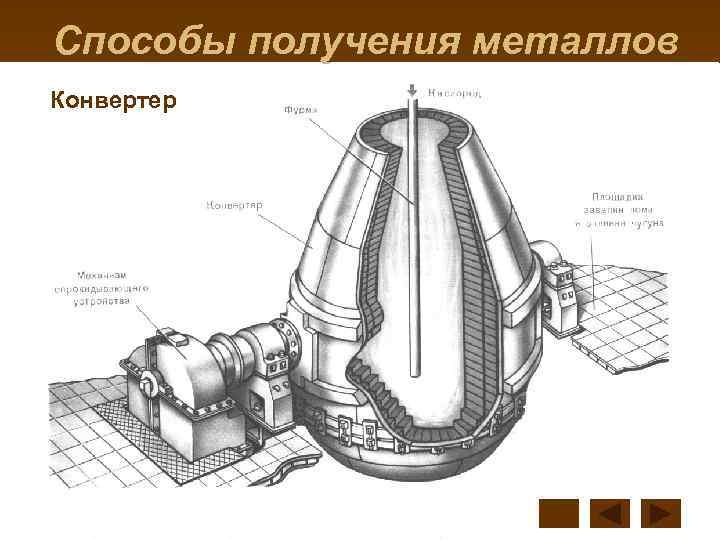 Способы получения металлов Конвертер
Способы получения металлов Конвертер
 Металлы. Химические свойства металлов Атомы металлов сравнительно легко отдают валентные электроны, поэтому металлы являются восстановителями. Вступают в реакции с различными веществами, среди которых могут быть - простые вещества, - кислоты, - соли менее активных металлов и другие.
Металлы. Химические свойства металлов Атомы металлов сравнительно легко отдают валентные электроны, поэтому металлы являются восстановителями. Вступают в реакции с различными веществами, среди которых могут быть - простые вещества, - кислоты, - соли менее активных металлов и другие.
 I. Реакции с простыми веществами. Атом водорода восстанавливается до степени окисления – 1.
I. Реакции с простыми веществами. Атом водорода восстанавливается до степени окисления – 1.
 Металлы. Химические свойства металлов II. Реакции со сложными веществами. 1) Взаимодействие с кислотами. Металлы, стоящие в ряду напряжений левее водорода, вытесняют его из кислот: (Исключение составляют концентрированная серная кислота и азотная кислота). 2) Взаимодействие с солями. Более активные металлы вытесняют менее активные из растворов их солей:
Металлы. Химические свойства металлов II. Реакции со сложными веществами. 1) Взаимодействие с кислотами. Металлы, стоящие в ряду напряжений левее водорода, вытесняют его из кислот: (Исключение составляют концентрированная серная кислота и азотная кислота). 2) Взаимодействие с солями. Более активные металлы вытесняют менее активные из растворов их солей:
 Металлы. Химические свойства металлов 3) Самые активные металлы взаимодействуют с H 2 O с образованием щёлочи: Менее активные – с образованием оксида: Кусочек металлического натрия реагирует с водой в присутствии фенолфталеина 4) Металлы могут образовывать соединения между собой интерметаллиды В этих веществах химическая связь преимущественно металлическая. По внешнему виду они похожи на металлы. Твёрдость – выше, пластичность – ниже, чем у образующих их металлов. Применение – полупроводники.
Металлы. Химические свойства металлов 3) Самые активные металлы взаимодействуют с H 2 O с образованием щёлочи: Менее активные – с образованием оксида: Кусочек металлического натрия реагирует с водой в присутствии фенолфталеина 4) Металлы могут образовывать соединения между собой интерметаллиды В этих веществах химическая связь преимущественно металлическая. По внешнему виду они похожи на металлы. Твёрдость – выше, пластичность – ниже, чем у образующих их металлов. Применение – полупроводники.
 Окраска пламени ионами щелочных металлов Li+ Cs+ Na+ Cs+
Окраска пламени ионами щелочных металлов Li+ Cs+ Na+ Cs+
 Сплавы – это материалы, состоящие из 2 -х и более компонентов, из которых хотя бы один - металл. Свойства сплавов весьма разнообразные и отличаются от исходных компонентов. (Например; сплав Ag и Au характеризуются большой твёрдостью). При взаимодействии металлов возможны следующие варианты. 1) Расплавленные металлы смешиваются в любых соотношениях, однако при охлаждении твёрдый раствор не образуется, получаются мелкие образуется кристаллики (т. е. механическая смесь). Pb - Sn, Bi - Cd, Ag - Pb.
Сплавы – это материалы, состоящие из 2 -х и более компонентов, из которых хотя бы один - металл. Свойства сплавов весьма разнообразные и отличаются от исходных компонентов. (Например; сплав Ag и Au характеризуются большой твёрдостью). При взаимодействии металлов возможны следующие варианты. 1) Расплавленные металлы смешиваются в любых соотношениях, однако при охлаждении твёрдый раствор не образуется, получаются мелкие образуется кристаллики (т. е. механическая смесь). Pb - Sn, Bi - Cd, Ag - Pb.
 Сплавы 2) Расплавленные металлы смешиваются в любых соотношениях, неограниченно растворяясь друг в друге. При охлаждении получаются твёрдые растворы (Ag-Cu, Cu-Ni, Ag. Au, Mg-Fe, Pt-Au), т. е. металлы, кристаллизующиеся в однотипных решётках и имеющие близкие по размерам атомы. По сравнению с чистыми металлами твёрдые растворы характеризуются более высокой прочностью, твёрдостью, химической стойкостью, они пластичны и хорошо проводят электрический ток. 3) Расплавленные металлы при смешивании взаимодействуют друг с другом, образуя химические соединения – интерметаллиды. Cu. Zn, Cu. Zn 3, Cu 2 Zn 3 Ca 3 Sb 3 , Na 2 Pb 5, Na 4 Pb, Zn 3 Hq, Aq 2 Zn 5, Cu 3 Zn.
Сплавы 2) Расплавленные металлы смешиваются в любых соотношениях, неограниченно растворяясь друг в друге. При охлаждении получаются твёрдые растворы (Ag-Cu, Cu-Ni, Ag. Au, Mg-Fe, Pt-Au), т. е. металлы, кристаллизующиеся в однотипных решётках и имеющие близкие по размерам атомы. По сравнению с чистыми металлами твёрдые растворы характеризуются более высокой прочностью, твёрдостью, химической стойкостью, они пластичны и хорошо проводят электрический ток. 3) Расплавленные металлы при смешивании взаимодействуют друг с другом, образуя химические соединения – интерметаллиды. Cu. Zn, Cu. Zn 3, Cu 2 Zn 3 Ca 3 Sb 3 , Na 2 Pb 5, Na 4 Pb, Zn 3 Hq, Aq 2 Zn 5, Cu 3 Zn.
 Применение сплавов
Применение сплавов
 Оборудование для получения сплавов
Оборудование для получения сплавов
 Примеры сплавов Бронза – 90% Cu, 10% Sn 20% Латунь – 60% Cu, 40% Zn – детали механизмов Мельхиор – 80% Cu, 20% Zn Нихром - 80% Ni, 20% Cr Нейзильбер – 65% Cu, 20% Zn, 15% Zn –монеты Дюралюмин – 94% Al, 4% Cu, 0, 5% Mg 0, 5% Mn 0, 5% Fe 0, 5% Si Чугун – Fe ≥ 1, 7% C, Si, Mg, S, P. Сталь – Fe 0, 1 -2% C, , Si, Mn, S, P.
Примеры сплавов Бронза – 90% Cu, 10% Sn 20% Латунь – 60% Cu, 40% Zn – детали механизмов Мельхиор – 80% Cu, 20% Zn Нихром - 80% Ni, 20% Cr Нейзильбер – 65% Cu, 20% Zn, 15% Zn –монеты Дюралюмин – 94% Al, 4% Cu, 0, 5% Mg 0, 5% Mn 0, 5% Fe 0, 5% Si Чугун – Fe ≥ 1, 7% C, Si, Mg, S, P. Сталь – Fe 0, 1 -2% C, , Si, Mn, S, P.
 Примеры сплавов Сплав: 10% Tl, 20% Sn, 70% Pb – не разъедается даже смесью H 2 SO 4 + HCl + HNO 3. Нержавеющая сталь ≥ 12% Cr Победит – 80 -85% W, 7 -13% Co, 5 -7% C. Константан – 40% Ni, 60% Cu – измерительные приборы. Никелин – 31% Ni, 56% Cu, 13% Zn – электрические нагреватели.
Примеры сплавов Сплав: 10% Tl, 20% Sn, 70% Pb – не разъедается даже смесью H 2 SO 4 + HCl + HNO 3. Нержавеющая сталь ≥ 12% Cr Победит – 80 -85% W, 7 -13% Co, 5 -7% C. Константан – 40% Ni, 60% Cu – измерительные приборы. Никелин – 31% Ni, 56% Cu, 13% Zn – электрические нагреватели.


