Металлы подгруппы платины Название благородные


Металлы подгруппы платины Название благородные металлы они получили благодаря высокой химической стойкости (практически не окисляются на воздухе) и блеску в изделиях. Золото, серебро и чистая платина обладают высокой пластичностью, а металлы платиновой группы, к тому же — очень высокой тугоплавкостью. По числу валентных электронов и аналогии химических свойств платиновые металлы можно разделить на три группы: Ru – Os Rh – Ir Pd – Pt
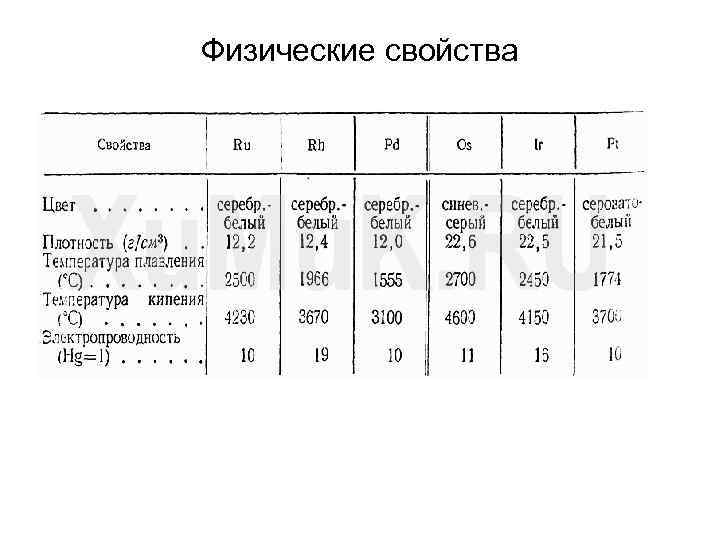
Физические свойства

Открытие платины • В 1 - й половине XVI века испанские колонизаторы обратили внимание на неплавкий тяжелый белый металл, встречающийся попутно с золотом в россыпях Новой Гранады. По внешнему сходству с серебром (исп. plata) они дали ему уменьшительное название «платина» (исп. platina), в переводе на русский - серебришко. Платина была известна ещё в древности, самородки этого металла находили вместе с золотом и называли их «белым золотом» (Древний Египет, Испания, Абиссиния), «лягушачьим золотом» (остров Борнео) и т. д. Первоначально испанцы считали её вредной примесью, поэтому был издан правительственный декрет, предписывающий выбрасывать платину в море. Первое научное описание платины сделал Уотсон в 1741 в связи с началом её добычи в промышленных масштабах в Колумбии (1735).

Открытие палладия, родия, иридия, осмия и рутения • В 1803 английский учёный У. Х. Волластон открыл палладий и родий , а в 1804 английский учёный С. Теннант открыл иридий и осмий. Палладий был назван в честь маленькой планеты(астероида) Pallas, открытой в 1802 г. другом Волластона Олберсом. • В 1808 русский учёный А. Снядицкий , исследуя платиновую руду, привезенную из Южной Америки, извлек новый химический элемент , названный им вестием. В 1844 профессор Казанского университета К. Клаус всесторонне изучил этот элемент и назвал его в честь России рутением.

Распространение в природе и добыча • Металлы платиновой группы встречаются в природе чаще всего в полиметаллических (медно-никелевых) рудах, а также в месторождениях золота и платины. • Первое письменное упоминание о добыче золота из россыпей Урала относится к 1669 (летопись Долматовского монастыря). Одно из первых месторождений золота в России было открыто в Карелии в 1737; его разработка относится к 1745. Началом золотого промысла на Урале принято считать 1745, когда Е. Марков открыл Берёзовское рудное месторождение. • В 1819 в россыпных месторождениях золота на Урале был обнаружен «новый сибирский металл» (платина). В 1824 на восточном склоне Уральских гор найдена богатая россыпь платины с золотом и заложен первый в России и Европе платиновый прииск. Позднее К. П. Голляховским и др. открыта Исовская система золото-платиновых россыпей, получившая мировую известность. В 1828 русский учёный В. Любарский опубликовал работы о первом в мире коренном месторождении платины, обнаруженном у Главного Уральского хребта. 95 % платины до 1915 года в основном добывали из россыпей, остальное количество получали при электролитическом рафинировании меди и золота.

Выделение платины • Очистка и обработка платины затруднялась высокой температурой её плавления (1773, 5° С). В 1 -й половине XIX века А. А. Мусин-Пушкин получил ковкую платину прокаливанием её амальгамы. В 1827 русские учёные П. Г. Соболевский и В. В. Любарский предложили новый способ очистки сырой платины, положивший начало порошковой металлургии. В течение года этим способом было очищено впервые в мире около 800 кг платины, то есть осуществлена переработка платины в больших масштабах. В 1859 французские учёные А. Э. Сент- Клер Девиль и А. Дебре впервые выплавили платину в печи в кислородно-водородном пламени. Первые работы по электролизу золота относятся к 1863, в производство этот метод введён в 80 -х гг. XIX века.

При обработке хлоридом аммония раствора, полученного действием царской водки на сырую платину или концентраты платиновых руд, образуется желтый осадок (NH 4)2[Pt. Cl 6], который при термическом разложении дает металлическую платину 99%-ной чистоты (1% - платиновые металлы)

Химические свойства Платиновые металлы обнаруживают большое сходство в свойствах: • все они относятся к тугоплавким металлам, • Проявляют высокую устойчивость к действию многих химических реагентов, • Характеризуются переменной валентностью и • Способностью к образованию многочисленных координационных соединений
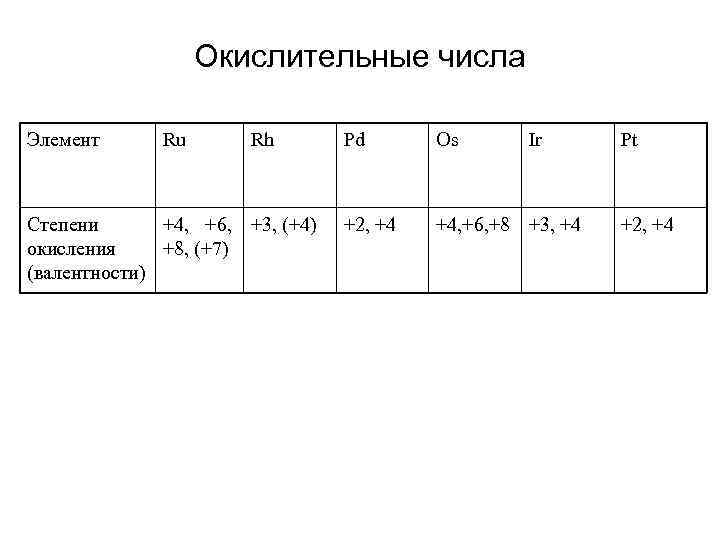
Окислительные числа Элемент Ru Rh Pd Os Ir Pt Степени +4, +6, +3, (+4) +2, +4 +4, +6, +8 +3, +4 +2, +4 окисления +8, (+7) (валентности)

Свойства Ru и Os • При действии кислорода на металлические Ru и Os образуются летучие четырехокиси Ru. O 4 и Os. O 4 • Ru, Os + Hal 2 = Ru. F 5, Ru. Cl 2, Ru. Cl 3, Os. F 4, Os. F 6, Os. F 8 • Царская водка на Ru и Os не действует • Под действием окислительно-щелочных расплавов Ru и Os переходят в рутенаты M 2 Ru. O 4 и осматы M 2 Os. O 4: Ru + KOH + KNO 3 = K 2 Ru. O 4 + KNO 2 + H 2 O Ru + KOH + KCl. O 3 = K 2 Ru. O 4 + KCl + H 2 O • Перрутенат калия KRu. O 4 и Ru. O 4 получают окислением рутената газообразным хлором: K 2 Ru. O 4 + Cl 2 = KRu. O 4 + KCl KRu. O 4 + Cl 2 = Ru. O 4 + KCl • Под действием щелочей KRu. O 4 и Ru. O 4 превращаются в рутенаты: KRu. O 4 + KOH = K 2 Ru. O 4 + O 2 + H 2 O Ru. O 4 + KOH = K 2 Ru. O 4 + O 2 + H 2 O • Под действием кислот K 2 Ru. O 4 и Ru. O 4 превращаются в соединения Ru(IV): K 2 Ru. O 4 + H 2 SO 4 = Ru. O 2 + K 2 SO 4 + H 2 O Ru. O 4 + HCl = Ru. Cl 4 + Cl + H 2 O

Свойства Rh и Ir • При действии кислорода на металлические Rh и Ir (при нагревании до высоких температур), а также окислительно- щелочных расплавов образуются оксиды Rh 2 O 3, Rh. O 2, Ir. O 2 • При нагревании с галогенами образуются: Rh, Ir + Hal 2 = Rh. F 3, Rh. Cl 3, Rh. F 4, Ir. F 6, Ir. Cl 4, Ir. Cl 3 • Ir не взаимодействует с царской водкой и кислотами, а Rh (в виде порошка) постепенно растворяется в царской водке и кислотах в присутствии кислорода: Rh + HNO 3 + HCl = H 3[Rh. Cl 6] + NO + H 2 O • При сплавлении металлических Rh и Ir с Na. Cl в атмосфере хлора получают комплексные хлориды: Rh + Cl 2 + Na. Cl = Na 3[Rh. Cl 6] Ir + Cl 2 + KCl = K 2[Ir. Cl 6] • При сильном нагревании металлических Rh и Ir с K 2 S 2 O 7 или KHSO 4 образуются Rh 2(SO 4)3 и Ir 2(SO 4)3

Свойства Pd и Pt • Металлический палладий ( в виде порошка, губчатом или коллоидном состоянии) обладает большой абсорбционной способностью по отношению к водороду (CO и др. ). При комнатной t один объем металлич. Pd поглощает 2800 объемов водорода. При этом образуются гидриды включения Pd 2 H, Pd. H 0, 8 • Pd и Pt растворяются в царской водке: Pt + HNO 3 + HCl = H 2[Pt. Cl 6] + NO + H 2 O Pd + HNO 3 + HCl = H 2[Pd. Cl 4] + NO + H 2 O • При обработке хлоридом аммония раствора, полученного действием царской водки на сырую платину или концентраты платиновых руд, образуется желтый осадок NH 4[Pt. Cl 6], который при термическом разложении дает металлическую платину 99%-ной чистоты (1% - платиновые металлы): NH 4[Pt. Cl 6] → Pt + Cl 2 + HCl • При нагревании с галогенами образуются: Pd, Pt + Hal 2 = Pd. F 2, Pd. Cl 2, Pd. F 3, Pd. I 2, Pt. Cl 4, Pt. F 4, Pt. Cl 2, Pt. I 4 • Металлический Pd растворяется в конц. HNO 3 и горячей конц. H 2 SO 4 кислотах • Цианиды щелочных металлов действуют на Pt в присутствии паров воды выше 500º: Pt + 4 KCN + 2 H 2 O = K 2[Pt. CN 4] + 2 KOH + H 2

Применение

Химическая посуда

Ювелирное дело
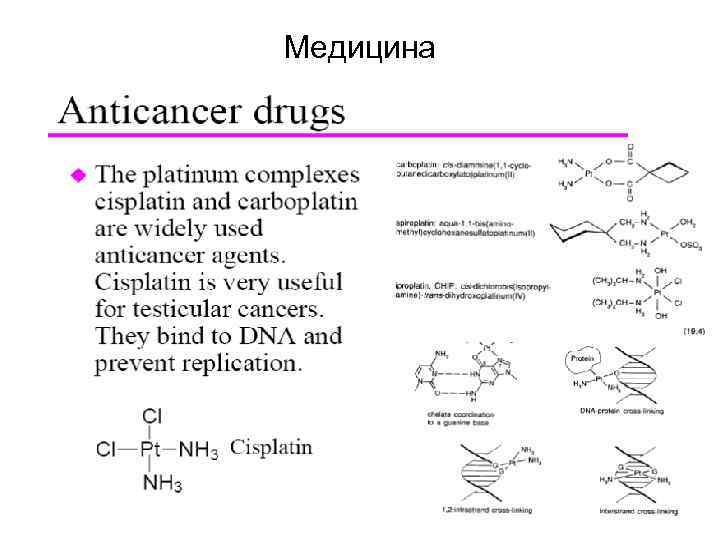
Медицина
Металлы подгруппы платины.ppt
- Количество слайдов: 16

