МЕТАЛЛЫ Металловедение — наука, изучающая связь

















3 металлы.ppt
- Количество слайдов: 25
 МЕТАЛЛЫ
МЕТАЛЛЫ
 Металловедение — наука, изучающая связь между составом, строением и свойствами металлов и сплавов, а также их изменение при различных внешних воздействиях (тепловом, механическом, химическом). Основное практическое значение металловедения — изыскание оптимального состава и способа обработки сплавов для получения заданных свойств.
Металловедение — наука, изучающая связь между составом, строением и свойствами металлов и сплавов, а также их изменение при различных внешних воздействиях (тепловом, механическом, химическом). Основное практическое значение металловедения — изыскание оптимального состава и способа обработки сплавов для получения заданных свойств.
 Под металлами понимают вещества, обладающие комплексом механических свойств: характерным металлическим блеском, высокой электропроводимость, хорошей теплопроводностью, высокой пластичностью.
Под металлами понимают вещества, обладающие комплексом механических свойств: характерным металлическим блеском, высокой электропроводимость, хорошей теплопроводностью, высокой пластичностью.
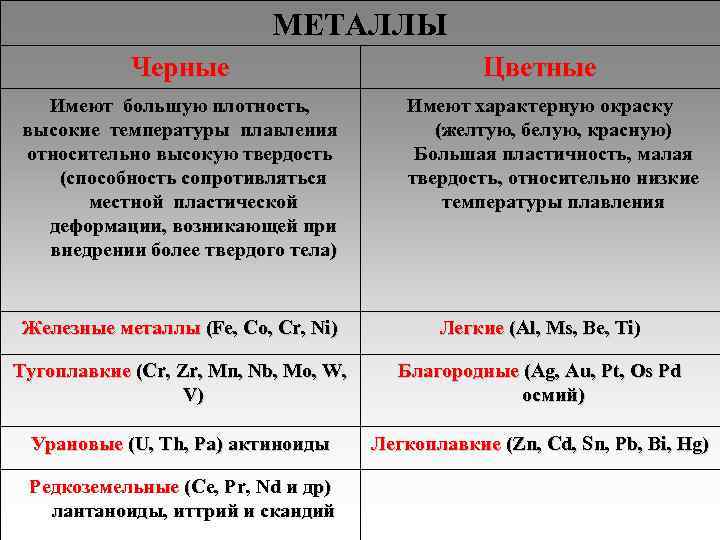
 МЕТАЛЛЫ Черные Цветные Имеют большую плотность, Имеют характерную окраску высокие температуры плавления (желтую, белую, красную) относительно высокую твердость Большая пластичность, малая (способность сопротивляться твердость, относительно низкие местной пластической температуры плавления деформации, возникающей при внедрении более твердого тела) Железные металлы (Fe, Co, Cr, Ni) Легкие (Al, Ms, Be, Ti) Тугоплавкие (Cr, Zr, Mn, Nb, Mo, W, Благородные (Ag, Au, Pt, Os Pd V) осмий) Урановые (U, Th, Pa) актиноиды Легкоплавкие (Zn, Cd, Sn, Pb, Bi, Hg) Редкоземельные (Ce, Pr, Nd и др) лантаноиды, иттрий и скандий
МЕТАЛЛЫ Черные Цветные Имеют большую плотность, Имеют характерную окраску высокие температуры плавления (желтую, белую, красную) относительно высокую твердость Большая пластичность, малая (способность сопротивляться твердость, относительно низкие местной пластической температуры плавления деформации, возникающей при внедрении более твердого тела) Железные металлы (Fe, Co, Cr, Ni) Легкие (Al, Ms, Be, Ti) Тугоплавкие (Cr, Zr, Mn, Nb, Mo, W, Благородные (Ag, Au, Pt, Os Pd V) осмий) Урановые (U, Th, Pa) актиноиды Легкоплавкие (Zn, Cd, Sn, Pb, Bi, Hg) Редкоземельные (Ce, Pr, Nd и др) лантаноиды, иттрий и скандий
 Все вещества в твердом состоянии могут иметь кристаллическое или аморфное строение. В аморфном веществе атомы расположены хаотичном, в кристаллическом — в строго определенном порядке. Все металлы в твердом состоянии имеют кристаллическое строение.
Все вещества в твердом состоянии могут иметь кристаллическое или аморфное строение. В аморфном веществе атомы расположены хаотичном, в кристаллическом — в строго определенном порядке. Все металлы в твердом состоянии имеют кристаллическое строение.
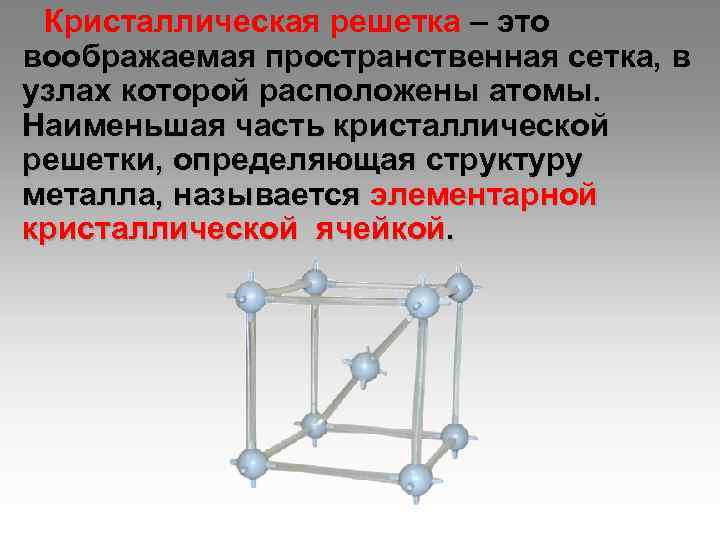
 Кристаллическая решетка – это воображаемая пространственная сетка, в узлах которой расположены атомы. Наименьшая часть кристаллической решетки, определяющая структуру металла, называется элементарной кристаллической ячейкой.
Кристаллическая решетка – это воображаемая пространственная сетка, в узлах которой расположены атомы. Наименьшая часть кристаллической решетки, определяющая структуру металла, называется элементарной кристаллической ячейкой.
 Базис кристаллической решетки – это таблица координат атомов, принадлежащих элементарной ячейке, рассматриваемой в пространственных координатных осях. В различных направлениях кристаллической решетки плотность расположения атомов различна, что влечет за собой различия в свойствах кристалла в зависимости от направления – анизотропию.
Базис кристаллической решетки – это таблица координат атомов, принадлежащих элементарной ячейке, рассматриваемой в пространственных координатных осях. В различных направлениях кристаллической решетки плотность расположения атомов различна, что влечет за собой различия в свойствах кристалла в зависимости от направления – анизотропию.
 В кубической объемноцентрированной решетке атомы расположены в узлах ячейки и один атом в центре куба (Cr, W, Mo, Fe).
В кубической объемноцентрированной решетке атомы расположены в узлах ячейки и один атом в центре куба (Cr, W, Mo, Fe).
 В кубической гранецентрированной решетке атомы расположены в вершинах куба и в центре каждой грани (Al, Cu, Ni, Au, Pt, Ag).
В кубической гранецентрированной решетке атомы расположены в вершинах куба и в центре каждой грани (Al, Cu, Ni, Au, Pt, Ag).
 В гексагональной плотноупакованной решетке атомы расположены в вершинах и в центрах оснований шестигранной призмы и три атома в середине призмы (Mg, Zn, Co).
В гексагональной плотноупакованной решетке атомы расположены в вершинах и в центрах оснований шестигранной призмы и три атома в середине призмы (Mg, Zn, Co).
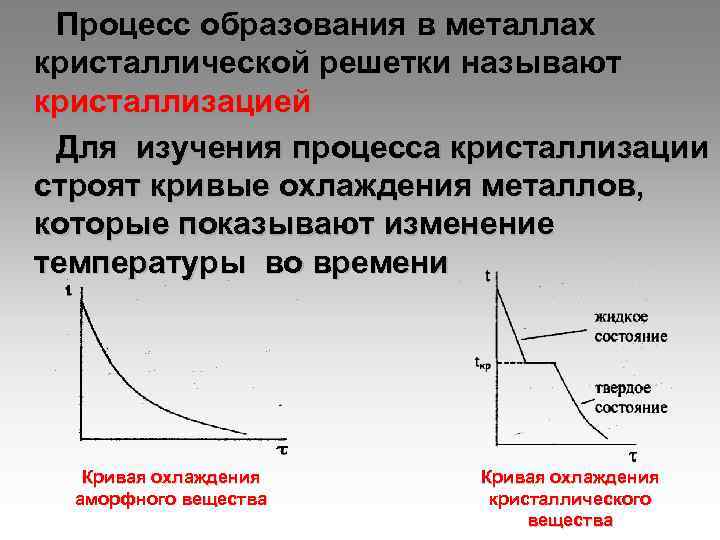
 Процесс образования в металлах кристаллической решетки называют кристаллизацией Для изучения процесса кристаллизации строят кривые охлаждения металлов, которые показывают изменение температуры во времени Кривая охлаждения аморфного вещества кристаллического вещества
Процесс образования в металлах кристаллической решетки называют кристаллизацией Для изучения процесса кристаллизации строят кривые охлаждения металлов, которые показывают изменение температуры во времени Кривая охлаждения аморфного вещества кристаллического вещества
 Кристаллизация металла происходит постепенно. Она объединяет два процесса, происходящих одновременно: • возникновение центров кристаллизации • рост кристаллов После окончания кристаллизации образуются кристаллы неправильной формы, которые называют зернами или кристаллитами.
Кристаллизация металла происходит постепенно. Она объединяет два процесса, происходящих одновременно: • возникновение центров кристаллизации • рост кристаллов После окончания кристаллизации образуются кристаллы неправильной формы, которые называют зернами или кристаллитами.
 Идеальное и реальное строение металлических материалов Под идеальным строением кристаллов подразумевают такое, при котором все атомы находятся строго в узлах кристаллической решетки. Теоретическая прочность такого кристалла чрезвычайно высока. Для осуществления пластического сдвига в таком кристалле требуется приложить усилие, которое можно подсчитать по формуле: Ƭсдв = G/2 П
Идеальное и реальное строение металлических материалов Под идеальным строением кристаллов подразумевают такое, при котором все атомы находятся строго в узлах кристаллической решетки. Теоретическая прочность такого кристалла чрезвычайно высока. Для осуществления пластического сдвига в таком кристалле требуется приложить усилие, которое можно подсчитать по формуле: Ƭсдв = G/2 П
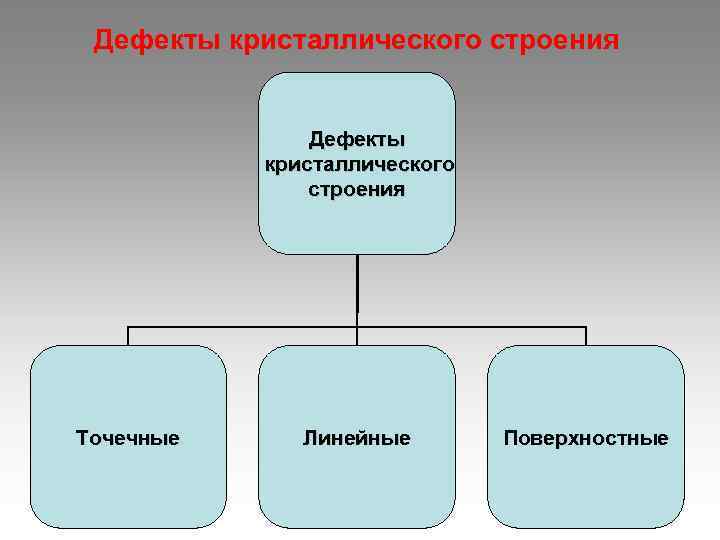
 Дефекты кристаллического строения Дефекты кристаллического строения Точечные Линейные Поверхностные
Дефекты кристаллического строения Дефекты кристаллического строения Точечные Линейные Поверхностные
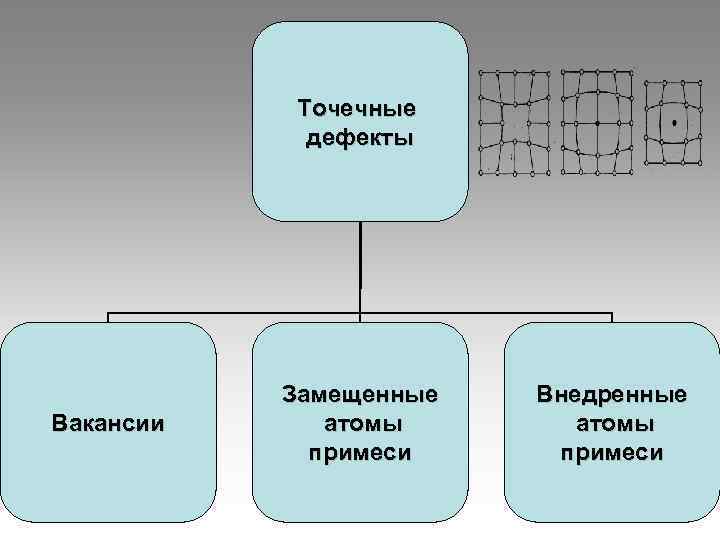
 Точечные дефекты Замещенные Внедренные Вакансии атомы примеси
Точечные дефекты Замещенные Внедренные Вакансии атомы примеси
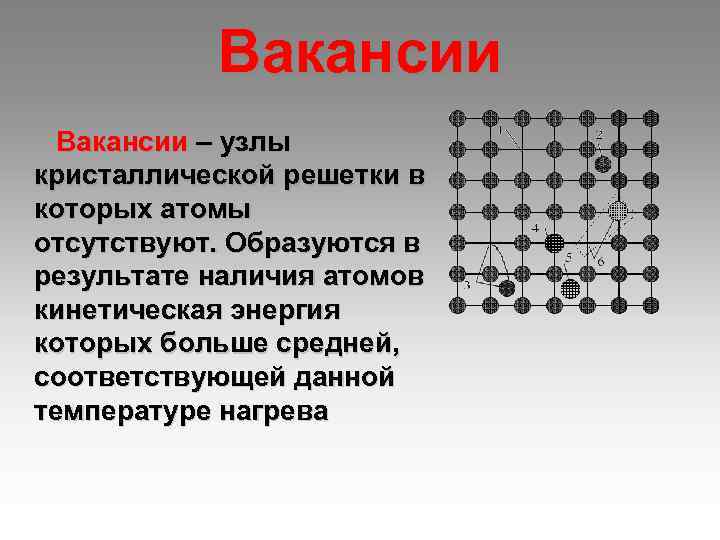
 Вакансии – узлы кристаллической решетки в которых атомы отсутствуют. Образуются в результате наличия атомов кинетическая энергия которых больше средней, соответствующей данной температуре нагрева
Вакансии – узлы кристаллической решетки в которых атомы отсутствуют. Образуются в результате наличия атомов кинетическая энергия которых больше средней, соответствующей данной температуре нагрева
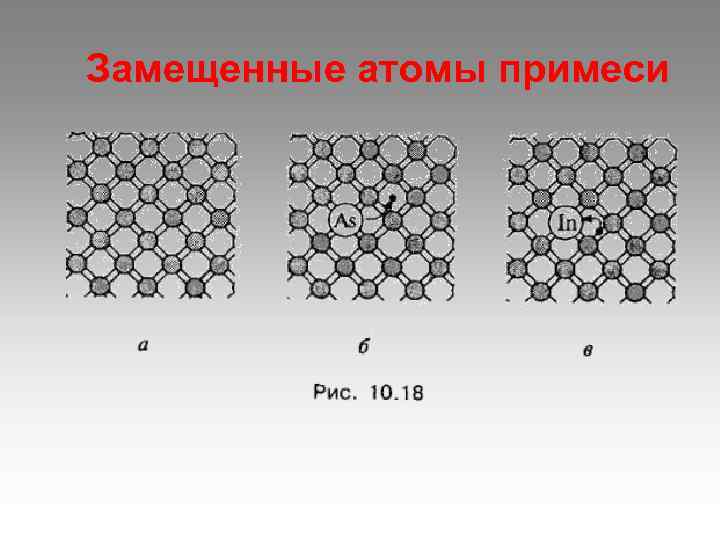
 Замещенные атомы примеси
Замещенные атомы примеси
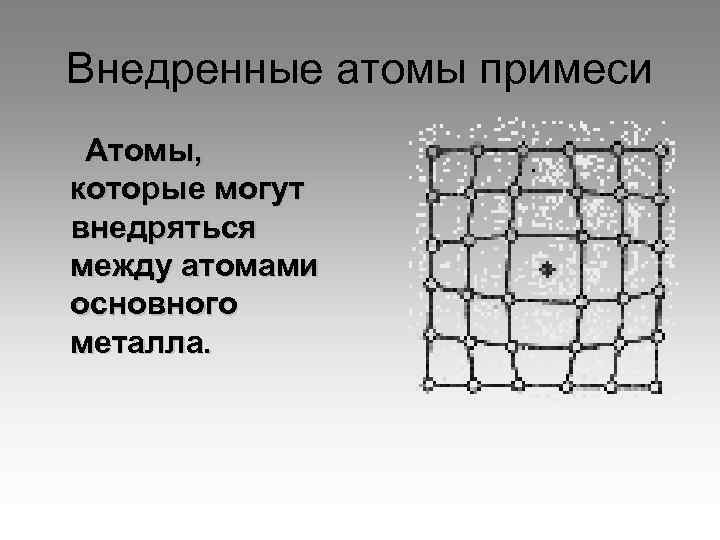
 Внедренные атомы примеси Атомы, которые могут внедряться между атомами основного металла.
Внедренные атомы примеси Атомы, которые могут внедряться между атомами основного металла.
 Линейные дефекты имеют малые размеры в двух измерениях и большую протяженность в третьем. Эти дефекты называют дислокациями. Дислокации : • краевые • винтовые
Линейные дефекты имеют малые размеры в двух измерениях и большую протяженность в третьем. Эти дефекты называют дислокациями. Дислокации : • краевые • винтовые
 Поверхностные дефекты – поверхности раздела между отдельными зернами. Граница зерна - переходная область, шириной до 10 межатомных расстояний, в которых решетка одного зерна, имеющего определенную кристаллографическую ориентацию, переходит в решетку другого зерна.
Поверхностные дефекты – поверхности раздела между отдельными зернами. Граница зерна - переходная область, шириной до 10 межатомных расстояний, в которых решетка одного зерна, имеющего определенную кристаллографическую ориентацию, переходит в решетку другого зерна.
 Деформация – изменение размеров и формы тела под действием приложенных к нему сил. Пластическая деформация не устраняется после снятия нагрузки и вызывает изменение структуры, объема и свойств металлов и сплавов и их внутреннего строения. Зерна разворачиваются, деформируются и сплющиваются, вытягиваясь в направлении деформации. Образуется волокнистая структура. При этом прочность и твердость металла возрастает, а пластичность и вязкость снижается.
Деформация – изменение размеров и формы тела под действием приложенных к нему сил. Пластическая деформация не устраняется после снятия нагрузки и вызывает изменение структуры, объема и свойств металлов и сплавов и их внутреннего строения. Зерна разворачиваются, деформируются и сплющиваются, вытягиваясь в направлении деформации. Образуется волокнистая структура. При этом прочность и твердость металла возрастает, а пластичность и вязкость снижается.
 Явление упрочнения металла при пластической деформации называют наклепом. Волокнистое строение и наклеп могут быть устранены при нагреве металла. Частичное снятие наклепа происходит уже при небольшом нагреве (железо — 300 -400°C), но волокнистая структура при этом сохраняется. При нагреве до более высокой температуры в металле происходит образование новых равноосных зерен. Этот процесс называется рекристаллизацией. Наклеп при этом снимается полностью.
Явление упрочнения металла при пластической деформации называют наклепом. Волокнистое строение и наклеп могут быть устранены при нагреве металла. Частичное снятие наклепа происходит уже при небольшом нагреве (железо — 300 -400°C), но волокнистая структура при этом сохраняется. При нагреве до более высокой температуры в металле происходит образование новых равноосных зерен. Этот процесс называется рекристаллизацией. Наклеп при этом снимается полностью.
 Температура, при которой начинается процесс рекристаллизации называется температурой рекристаллизации (tрекр. ). Абсолютная температура рекристаллизации Тр связана с абсолютной Т плавления зависимостью Тр=а·Тпл, где а —коэффициент, зависящий от состава и структуры металла. Для особо чистых металлов а=0, 2; для металлов технической чистоты а=0, 3 -0, 4; для сплавов а=0, 5 -0, 6.
Температура, при которой начинается процесс рекристаллизации называется температурой рекристаллизации (tрекр. ). Абсолютная температура рекристаллизации Тр связана с абсолютной Т плавления зависимостью Тр=а·Тпл, где а —коэффициент, зависящий от состава и структуры металла. Для особо чистых металлов а=0, 2; для металлов технической чистоты а=0, 3 -0, 4; для сплавов а=0, 5 -0, 6.
 Если деформирование металла происходит при температуре, которая выше tрекр, то наклеп после деформации не возникает. Такая деформация называется горячей. При горячей деформации идут одновременно процессы упрочнения и рекристаллизации. Деформация, которая происходит ниже tрекр называется холодной.
Если деформирование металла происходит при температуре, которая выше tрекр, то наклеп после деформации не возникает. Такая деформация называется горячей. При горячей деформации идут одновременно процессы упрочнения и рекристаллизации. Деформация, которая происходит ниже tрекр называется холодной.
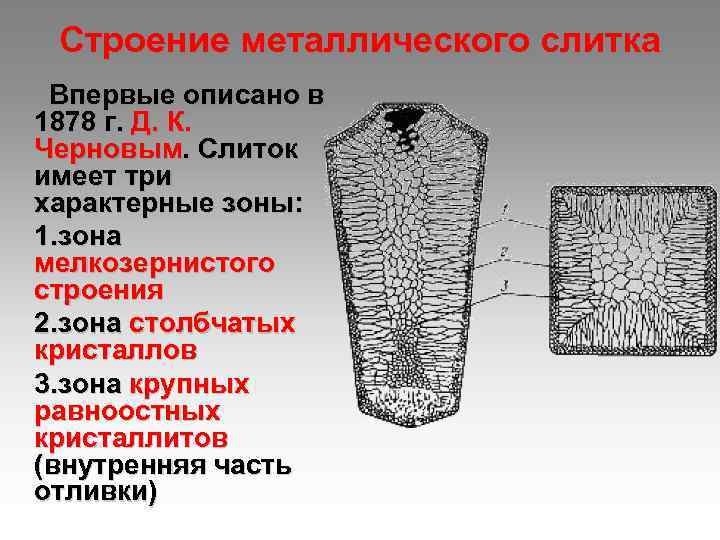
 Строение металлического слитка Впервые описано в 1878 г. Д. К. Черновым. Слиток имеет три характерные зоны: 1. зона мелкозернистого строения 2. зона столбчатых кристаллов 3. зона крупных равноостных кристаллитов (внутренняя часть отливки)
Строение металлического слитка Впервые описано в 1878 г. Д. К. Черновым. Слиток имеет три характерные зоны: 1. зона мелкозернистого строения 2. зона столбчатых кристаллов 3. зона крупных равноостных кристаллитов (внутренняя часть отливки)

