МЕТАЛЛЫ.ppt
- Количество слайдов: 102
 МЕТАЛЛЫ Классификация, строение, свойства
МЕТАЛЛЫ Классификация, строение, свойства
 l Металлы – наиболее распространенные и широко используемые материалы в производстве и в быту человека. l Термин «металл» произошёл от греческого слова métallon (от metalléuō – выкапываю, добываю из земли), которое означало первоначально копи, рудники (в этом смысле оно встречается у Геродота, 5 в. до н. э. ). То, что добывалось в рудниках, Платон называл metalléia.
l Металлы – наиболее распространенные и широко используемые материалы в производстве и в быту человека. l Термин «металл» произошёл от греческого слова métallon (от metalléuō – выкапываю, добываю из земли), которое означало первоначально копи, рудники (в этом смысле оно встречается у Геродота, 5 в. до н. э. ). То, что добывалось в рудниках, Платон называл metalléia.
 В древности и в средние века считалось, что существует только 7 металлов: l золото, l серебро, l медь, l олово, l свинец, l железо, l ртуть По алхимическим представлениям, металлы зарождались в земных недрах под влиянием лучей планет и постепенно крайне медленно совершенствовались, превращаясь в серебро и золото. Алхимики полагали, что металлы – вещества сложные, состоящие из «начала металличности» (ртути) и «начала горючести» (серы). l
В древности и в средние века считалось, что существует только 7 металлов: l золото, l серебро, l медь, l олово, l свинец, l железо, l ртуть По алхимическим представлениям, металлы зарождались в земных недрах под влиянием лучей планет и постепенно крайне медленно совершенствовались, превращаясь в серебро и золото. Алхимики полагали, что металлы – вещества сложные, состоящие из «начала металличности» (ртути) и «начала горючести» (серы). l
 l В начале 18 в. получила распространение гипотеза, согласно которой металлы состоят из земли и «начала горючести» – флогистона. М. В. Ломоносов насчитывал 6 металлов. (Au, Ag, Cu, Sn, Fe, Pb) и определял металл как «светлое тело, которое ковать можно» . В конце 18 в. А. Л. Лавуазье опроверг гипотезу флогистона и показал, что металлы – простые вещества. В 1789 Лавуазье в руководстве по химии дал список простых веществ, в который включил все известные тогда 17 металлов (Sb, Ag, As, Bi, Co, Cu, Sn, Fe, Mn, Hg, Mo, Ni, Au, Pt, Pb, W, Zn).
l В начале 18 в. получила распространение гипотеза, согласно которой металлы состоят из земли и «начала горючести» – флогистона. М. В. Ломоносов насчитывал 6 металлов. (Au, Ag, Cu, Sn, Fe, Pb) и определял металл как «светлое тело, которое ковать можно» . В конце 18 в. А. Л. Лавуазье опроверг гипотезу флогистона и показал, что металлы – простые вещества. В 1789 Лавуазье в руководстве по химии дал список простых веществ, в который включил все известные тогда 17 металлов (Sb, Ag, As, Bi, Co, Cu, Sn, Fe, Mn, Hg, Mo, Ni, Au, Pt, Pb, W, Zn).
 l В 1 й половине 19 в. были открыты спутники Pt, получены путём электролиза некоторые щелочные и щёлочноземельные металлы, положено начало разделению редкоземельных металлов, открыты неизвестные металлы при химическом анализе минералов. В 1860 63 методом спектрального анализа были открыты Cs, Rb, Tl, In. Блестяще подтвердилось существование металлов, предсказанных Д. И. Менделеевым на основе его периодического закона. Открытие радиоактивности в кон. 19 в. повлекло за собой поиски природных радиоактивных металлов, увенчавшиеся полным успехом. Наконец, методом ядерных превращений начиная с сер. 20 в. были искусственно получены радиоактивные металлы, в частности трансурановые элементы.
l В 1 й половине 19 в. были открыты спутники Pt, получены путём электролиза некоторые щелочные и щёлочноземельные металлы, положено начало разделению редкоземельных металлов, открыты неизвестные металлы при химическом анализе минералов. В 1860 63 методом спектрального анализа были открыты Cs, Rb, Tl, In. Блестяще подтвердилось существование металлов, предсказанных Д. И. Менделеевым на основе его периодического закона. Открытие радиоактивности в кон. 19 в. повлекло за собой поиски природных радиоактивных металлов, увенчавшиеся полным успехом. Наконец, методом ядерных превращений начиная с сер. 20 в. были искусственно получены радиоактивные металлы, в частности трансурановые элементы.
 l Основы современного металловедения были заложены выдающимися русскими металлургами П. П. Аносовым (1799– 1851) и Д. К. Черновым (1839– 1921), впервые установившими связь между строением и свойствами металлов и сплавов. П. П. Аносов заложил основы учения о стали, разработал научные принципы получения высококачественной стали, впервые в мире в 1831 г. применил микроскоп для исследования строения металлов. Д. К. Чернов продолжил труды П. П. Аносова. Он по праву считается основоположником металлографии – науки о строении металлов и сплавов. Его научные открытия легли в основу процессов ковки, прокатки, термической обработки стали. Открытые Д. К. Черновым критические точки в стали явились основой для построения современной диаграммы состояния системы железо – углерод.
l Основы современного металловедения были заложены выдающимися русскими металлургами П. П. Аносовым (1799– 1851) и Д. К. Черновым (1839– 1921), впервые установившими связь между строением и свойствами металлов и сплавов. П. П. Аносов заложил основы учения о стали, разработал научные принципы получения высококачественной стали, впервые в мире в 1831 г. применил микроскоп для исследования строения металлов. Д. К. Чернов продолжил труды П. П. Аносова. Он по праву считается основоположником металлографии – науки о строении металлов и сплавов. Его научные открытия легли в основу процессов ковки, прокатки, термической обработки стали. Открытые Д. К. Черновым критические точки в стали явились основой для построения современной диаграммы состояния системы железо – углерод.
 l Металлы – это вещества, обладающие в обычных условиях высокими электропроводностью (106— 107 Ом 1 см 1, уменьшается с ростом температуры) и теплопроводностью, ковкостью, «металлическим» блеском и др. свойствами, обусловленными наличием в их кристаллической решетке большого количества (1022— 1023 в 1 см 3) слабо связанных с атомными ядрами подвижных электронов.
l Металлы – это вещества, обладающие в обычных условиях высокими электропроводностью (106— 107 Ом 1 см 1, уменьшается с ростом температуры) и теплопроводностью, ковкостью, «металлическим» блеском и др. свойствами, обусловленными наличием в их кристаллической решетке большого количества (1022— 1023 в 1 см 3) слабо связанных с атомными ядрами подвижных электронов.
 Металлы и сплавы классифицируют по: l числу компонентов, l содержанию легирующих компонентов, l степени чистоты, l характеру компонентов. Компонентом называют химический элемент, входящий в состав металла или сплава. Компоненты подразделяют на основные и легирующие. Основным называют такой компонент, который преобладает в металле или сплаве. Легирующим компонентом называют компонент, вводимый в состав сплава для получения необходимых требуемых свойств.
Металлы и сплавы классифицируют по: l числу компонентов, l содержанию легирующих компонентов, l степени чистоты, l характеру компонентов. Компонентом называют химический элемент, входящий в состав металла или сплава. Компоненты подразделяют на основные и легирующие. Основным называют такой компонент, который преобладает в металле или сплаве. Легирующим компонентом называют компонент, вводимый в состав сплава для получения необходимых требуемых свойств.
 По числу компонентов металлы разделяют на простые металлы и металлические сплавы. l По содержанию легирующих компонентов сплавы делят на: низколегированные (содержащий в своем составе легирующих компонентов менее 2, 5%) среднелегированные (2, 5 10%) высоколегированные (более 10%). l По степени чистоты металлы и сплавы делят на металлы пониженной, средней, повышенной, высокой чистоты и особо чистые.
По числу компонентов металлы разделяют на простые металлы и металлические сплавы. l По содержанию легирующих компонентов сплавы делят на: низколегированные (содержащий в своем составе легирующих компонентов менее 2, 5%) среднелегированные (2, 5 10%) высоколегированные (более 10%). l По степени чистоты металлы и сплавы делят на металлы пониженной, средней, повышенной, высокой чистоты и особо чистые.
 Классификация металлов (по А. П. Гуляеву) Все металлы условно поделены на черные и цветные. Черные металл обычно имеют темно серый цвет, большую плотность (кроме щелочных), высокую температуру плавления, относительно высокую твердость. Наиболее типичным черным металлом является железо. l Цветные металлы имеют красную, желтую, белую окраску. Они обладаю большой пластичностью, малой твердостью, низкой температурой плавления. Типичный представитель медь. l
Классификация металлов (по А. П. Гуляеву) Все металлы условно поделены на черные и цветные. Черные металл обычно имеют темно серый цвет, большую плотность (кроме щелочных), высокую температуру плавления, относительно высокую твердость. Наиболее типичным черным металлом является железо. l Цветные металлы имеют красную, желтую, белую окраску. Они обладаю большой пластичностью, малой твердостью, низкой температурой плавления. Типичный представитель медь. l
 К черным металлам относятся: l железные металлы железо, кобальт, никель, марганец. Черные металлы составляют 95% металлопродукции.
К черным металлам относятся: l железные металлы железо, кобальт, никель, марганец. Черные металлы составляют 95% металлопродукции.
 К цветным металлам относятся: l l l l легкие бериллий, магний, алюминий; тяжелые – медь, свинец и др. благородные металлы рутений, радий, палладий, осмий, иридий, платина, золото, серебро и полублагородная медь; легкоплавкие металлы цинк, кадмий, ртуть, галлий, индий, талий, германий, олово, свинец, мышьяк, сурьма, висмут. тугоплавкие металлы; имеют температуру плавления выше чем у железа, т. е. более 15390 С титан, ванадий, хром, цирконий, ниобий, молибден, вольфрам, технеций, гафний, рений; урановые металлы (актиноиды) торий, актиний, уран, нептуний, плутоний и др. (с 89 до 103 элемента); редкоземельные металлы (с 57 71 элементы), лантан, церий, ниодим и д. р. ; щелочноземельные металлы литий, натрий, кальций, калий, рубидий, стронций, цезий, барий, франций, родий, скандий.
К цветным металлам относятся: l l l l легкие бериллий, магний, алюминий; тяжелые – медь, свинец и др. благородные металлы рутений, радий, палладий, осмий, иридий, платина, золото, серебро и полублагородная медь; легкоплавкие металлы цинк, кадмий, ртуть, галлий, индий, талий, германий, олово, свинец, мышьяк, сурьма, висмут. тугоплавкие металлы; имеют температуру плавления выше чем у железа, т. е. более 15390 С титан, ванадий, хром, цирконий, ниобий, молибден, вольфрам, технеций, гафний, рений; урановые металлы (актиноиды) торий, актиний, уран, нептуний, плутоний и др. (с 89 до 103 элемента); редкоземельные металлы (с 57 71 элементы), лантан, церий, ниодим и д. р. ; щелочноземельные металлы литий, натрий, кальций, калий, рубидий, стронций, цезий, барий, франций, родий, скандий.
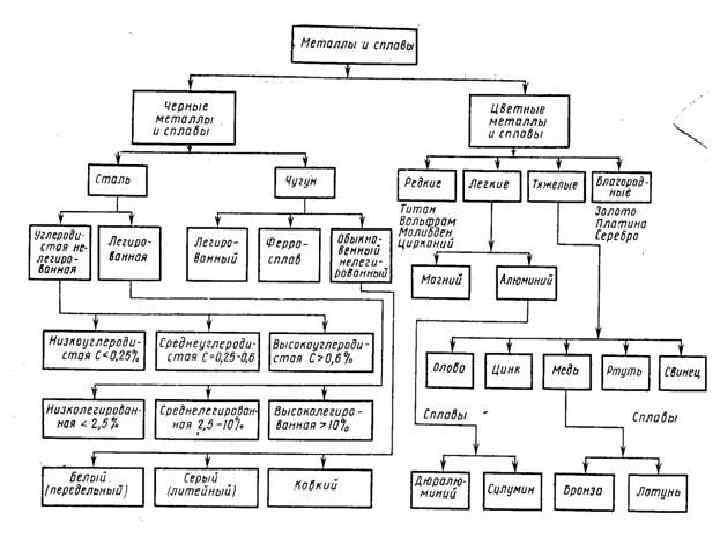
 СПЛАВЫ Сплавы системы «железо-углерод» Fe-C: v стали (углеродистые и легированные) v чугуны (серые, белые, высокопрочные, ковкие, спец. назначения) Сплавы на основе цветных металлов: v Al и его сплавы v Cu и его сплавы v Ti и его сплавы v Mg и его сплавы v сплавы на основе других элементов Порошковые сплавы: v твердые сплавы v антифрикционные и фрикционные сплавы v сплавы с особыми свойствами САПы, САСы Аморфные сплавы
СПЛАВЫ Сплавы системы «железо-углерод» Fe-C: v стали (углеродистые и легированные) v чугуны (серые, белые, высокопрочные, ковкие, спец. назначения) Сплавы на основе цветных металлов: v Al и его сплавы v Cu и его сплавы v Ti и его сплавы v Mg и его сплавы v сплавы на основе других элементов Порошковые сплавы: v твердые сплавы v антифрикционные и фрикционные сплавы v сплавы с особыми свойствами САПы, САСы Аморфные сплавы
 СТРОЕНИЕ МЕТАЛЛОВ
СТРОЕНИЕ МЕТАЛЛОВ
 У всех металлов и их сплавов строение кристаллическое. l Кристаллические зерна неопределенной формы не похожи на типичные кристаллы — многогранники, поэтому их называют зернами. l При затвердевании атомы металлов образуют кристаллы, которые можно рассматривать как геометрически правильные системы, построенные в виде кристаллических решеток. l Порядок расположения атомов в решетке может быть различным. l l Этот порядок определяется понятием кристаллическая решетка.
У всех металлов и их сплавов строение кристаллическое. l Кристаллические зерна неопределенной формы не похожи на типичные кристаллы — многогранники, поэтому их называют зернами. l При затвердевании атомы металлов образуют кристаллы, которые можно рассматривать как геометрически правильные системы, построенные в виде кристаллических решеток. l Порядок расположения атомов в решетке может быть различным. l l Этот порядок определяется понятием кристаллическая решетка.
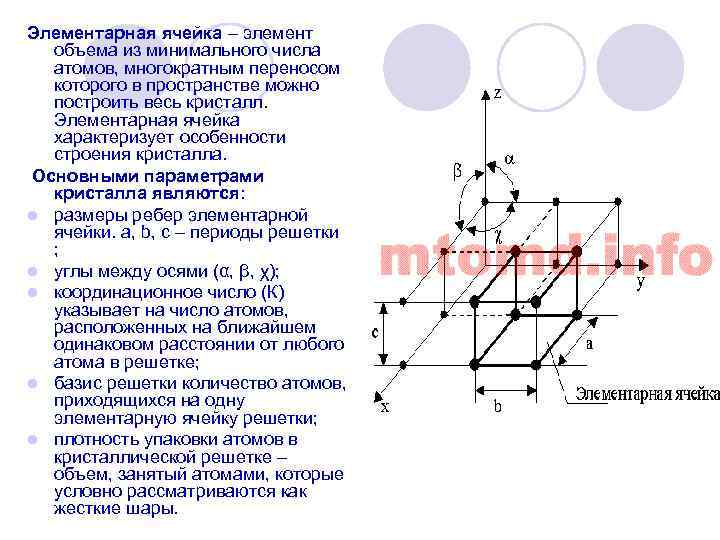 Элементарная ячейка – элемент объема из минимального числа атомов, многократным переносом которого в пространстве можно построить весь кристалл. Элементарная ячейка характеризует особенности строения кристалла. Основными параметрами кристалла являются: l размеры ребер элементарной ячейки. a, b, c – периоды решетки ; l углы между осями (α, β, χ); l координационное число (К) указывает на число атомов, расположенных на ближайшем одинаковом расстоянии от любого атома в решетке; l базис решетки количество атомов, приходящихся на одну элементарную ячейку решетки; l плотность упаковки атомов в кристаллической решетке – объем, занятый атомами, которые условно рассматриваются как жесткие шары.
Элементарная ячейка – элемент объема из минимального числа атомов, многократным переносом которого в пространстве можно построить весь кристалл. Элементарная ячейка характеризует особенности строения кристалла. Основными параметрами кристалла являются: l размеры ребер элементарной ячейки. a, b, c – периоды решетки ; l углы между осями (α, β, χ); l координационное число (К) указывает на число атомов, расположенных на ближайшем одинаковом расстоянии от любого атома в решетке; l базис решетки количество атомов, приходящихся на одну элементарную ячейку решетки; l плотность упаковки атомов в кристаллической решетке – объем, занятый атомами, которые условно рассматриваются как жесткие шары.
 l Большинство технических металлов имеют кристаллические решетки: l объемно центрированную кубическую, l кубическую гранецентрированную, l гексагональную.
l Большинство технических металлов имеют кристаллические решетки: l объемно центрированную кубическую, l кубическую гранецентрированную, l гексагональную.
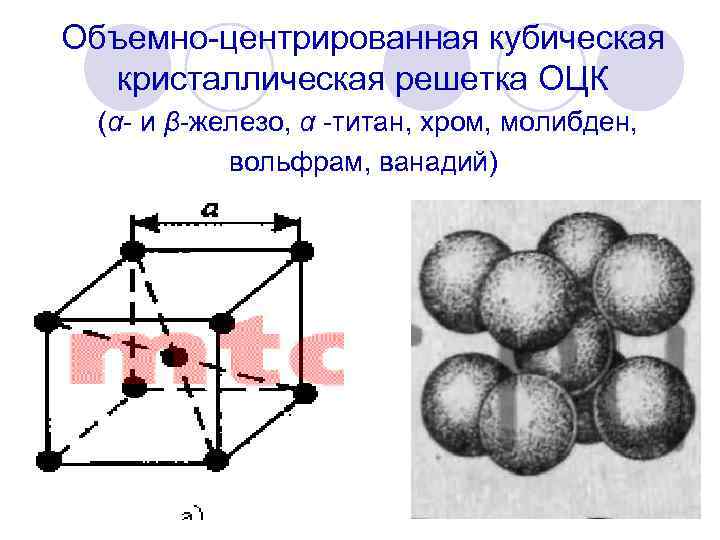 Объемно центрированная кубическая кристаллическая решетка ОЦК (α и β железо, α титан, хром, молибден, вольфрам, ванадий)
Объемно центрированная кубическая кристаллическая решетка ОЦК (α и β железо, α титан, хром, молибден, вольфрам, ванадий)
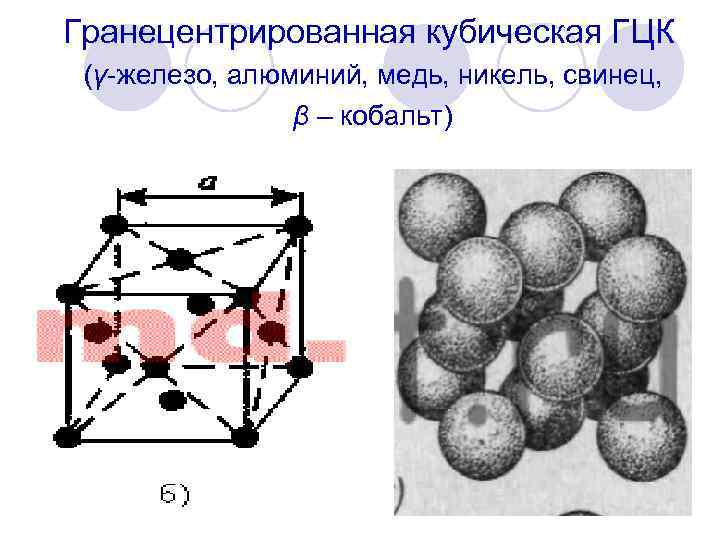 Гранецентрированная кубическая ГЦК (γ железо, алюминий, медь, никель, свинец, β – кобальт)
Гранецентрированная кубическая ГЦК (γ железо, алюминий, медь, никель, свинец, β – кобальт)
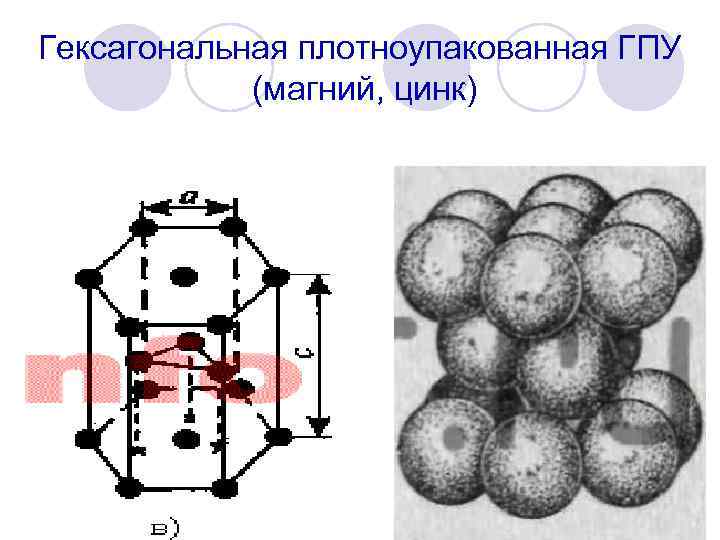 Гексагональная плотноупакованная ГПУ (магний, цинк)
Гексагональная плотноупакованная ГПУ (магний, цинк)
 l. В узлах решеток находятся положительно заряженные ионы. Ионы не находятся в покое, а непрерывно колеблются около положения равновесия. l С повышением температуры амплитуда колебаний увеличивается, что вызывает расширение кристаллов, а при температуре плавления колебания частиц усиливаются настолько, что кристаллическая решетка разрушается.
l. В узлах решеток находятся положительно заряженные ионы. Ионы не находятся в покое, а непрерывно колеблются около положения равновесия. l С повышением температуры амплитуда колебаний увеличивается, что вызывает расширение кристаллов, а при температуре плавления колебания частиц усиливаются настолько, что кристаллическая решетка разрушается.
 l l l Кристаллы имеют дефекты и их структура отличается от идеальных решеток. Точечными дефектами являются пустые узлы или вакансии и межузельные атомы; количество этих дефектов возрастает с повышением температуры. Важнейшими линейными дефектами являются дислокации (краевые и винтовые), представляющие как бы сдвиг части кристаллической решетки. Дислокации характеризуются большой протяженностью в одном направлении и малой в другом. Дефекты кристаллов оказывают существенное влияние на механические, физические, химические и технологические свойства металлов.
l l l Кристаллы имеют дефекты и их структура отличается от идеальных решеток. Точечными дефектами являются пустые узлы или вакансии и межузельные атомы; количество этих дефектов возрастает с повышением температуры. Важнейшими линейными дефектами являются дислокации (краевые и винтовые), представляющие как бы сдвиг части кристаллической решетки. Дислокации характеризуются большой протяженностью в одном направлении и малой в другом. Дефекты кристаллов оказывают существенное влияние на механические, физические, химические и технологические свойства металлов.
 l. В отдельных кристаллах свойства различны в разных направлениях. Это свойство кристаллов называют анизотропностью. l Анизотропность кристаллов объясняется особенностями расположения атомов в пространстве.
l. В отдельных кристаллах свойства различны в разных направлениях. Это свойство кристаллов называют анизотропностью. l Анизотропность кристаллов объясняется особенностями расположения атомов в пространстве.
 Аморфные тела изотропны, т. е. все эти свойства одинаковы во всех направлениях. Излом аморфного тела всегда имеет неправильную, искривленную, так называемую раковистую, поверхность. l Металлы, затвердевшие в обычных условиях, состоят не из одного кристалла, а из множества отдельных кристаллитов, различно ориентированных друг к другу, поэтому свойства литого металла приблизительно одинаковы во всех направлениях; это явление называют квазиизотропностью (кажущейся изотропностью). l
Аморфные тела изотропны, т. е. все эти свойства одинаковы во всех направлениях. Излом аморфного тела всегда имеет неправильную, искривленную, так называемую раковистую, поверхность. l Металлы, затвердевшие в обычных условиях, состоят не из одного кристалла, а из множества отдельных кристаллитов, различно ориентированных друг к другу, поэтому свойства литого металла приблизительно одинаковы во всех направлениях; это явление называют квазиизотропностью (кажущейся изотропностью). l
 Аллотропия металлов (или полиморфизм) — свойство перестраивать решетку при определенных температурах в процессе нагревания или охлаждения. l Аллотропию обнаруживают все элементы, меняющие валентность при изменении температуры, например железо, марганец, никель, олово и др. l Каждое аллотропическое превращение происходит при определенной температуре. Например, одно из превращений железа происходит при температуре 911°С, ниже которой атомы составляют решетку центрированного куба, а выше решетку гранецентрированного куба. l Структура, имеющая ту или иную решетку, называется аллотропической формой или модификацией. l
Аллотропия металлов (или полиморфизм) — свойство перестраивать решетку при определенных температурах в процессе нагревания или охлаждения. l Аллотропию обнаруживают все элементы, меняющие валентность при изменении температуры, например железо, марганец, никель, олово и др. l Каждое аллотропическое превращение происходит при определенной температуре. Например, одно из превращений железа происходит при температуре 911°С, ниже которой атомы составляют решетку центрированного куба, а выше решетку гранецентрированного куба. l Структура, имеющая ту или иную решетку, называется аллотропической формой или модификацией. l
 l Кристаллизацией металлов называется образование кристаллов в металлах (и сплавах) при переходе из жидкого состояния в твердое (первичная кристаллизация). l К вторичной кристаллизации относят превращения в затвердевшем металле при его остывании. Сюда относятся перекристаллизация из одной модификации в другую (полиморфные превращения), распад твердых растворов, распад (а также образование) химических соединении. l Температура, соответствующая какому либо превращению в металле, называется критической точкой.
l Кристаллизацией металлов называется образование кристаллов в металлах (и сплавах) при переходе из жидкого состояния в твердое (первичная кристаллизация). l К вторичной кристаллизации относят превращения в затвердевшем металле при его остывании. Сюда относятся перекристаллизация из одной модификации в другую (полиморфные превращения), распад твердых растворов, распад (а также образование) химических соединении. l Температура, соответствующая какому либо превращению в металле, называется критической точкой.
 Переход из жидкого состояния в твердое при охлаждении сопровождается образованием кристаллической решетки, т. е. кристаллизацией. Чтобы вызвать кристаллизацию, жидкий металл нужно переохладить несколько ниже температуры плавления. l При затвердевании и при аллотропическом превращении и металле вначале возникают зародыши кристалла (центры кристаллизации), вокруг которых группируются атомы, образуя соответствующую кристаллическую решетку. Центрами кристаллизации могут служить неметаллические включения. l Таким образом, процесс кристаллизации складывается из двух этапов: образования центров кристаллизации и роста кристаллов. l
Переход из жидкого состояния в твердое при охлаждении сопровождается образованием кристаллической решетки, т. е. кристаллизацией. Чтобы вызвать кристаллизацию, жидкий металл нужно переохладить несколько ниже температуры плавления. l При затвердевании и при аллотропическом превращении и металле вначале возникают зародыши кристалла (центры кристаллизации), вокруг которых группируются атомы, образуя соответствующую кристаллическую решетку. Центрами кристаллизации могут служить неметаллические включения. l Таким образом, процесс кристаллизации складывается из двух этапов: образования центров кристаллизации и роста кристаллов. l
 l. У каждого из возникающих кристаллов кристаллографические плоскости ориентированы случайно, кроме того, при первичной кристаллизации кристаллы могут поворачиваться, так как они окружены жидкостью. l Смежные кристаллы растут навстречу другу и точки их соприкосновения определяют границы зерен.
l. У каждого из возникающих кристаллов кристаллографические плоскости ориентированы случайно, кроме того, при первичной кристаллизации кристаллы могут поворачиваться, так как они окружены жидкостью. l Смежные кристаллы растут навстречу другу и точки их соприкосновения определяют границы зерен.
 ОСНОВНЫЕ СВОЙСТВА МЕТАЛЛОВ
ОСНОВНЫЕ СВОЙСТВА МЕТАЛЛОВ
 У металлов выделяют: l физические l механические, l химические l технологические, l эксплуатационные свойства
У металлов выделяют: l физические l механические, l химические l технологические, l эксплуатационные свойства
 Физические свойства l цвет, l плотность, l температура плавления, l электропроводность, l магнитные свойства, l теплопроводность, l теплоемкость, l расширение и сжатие при нагревании, охлаждении и при фазовых превращениях.
Физические свойства l цвет, l плотность, l температура плавления, l электропроводность, l магнитные свойства, l теплопроводность, l теплоемкость, l расширение и сжатие при нагревании, охлаждении и при фазовых превращениях.
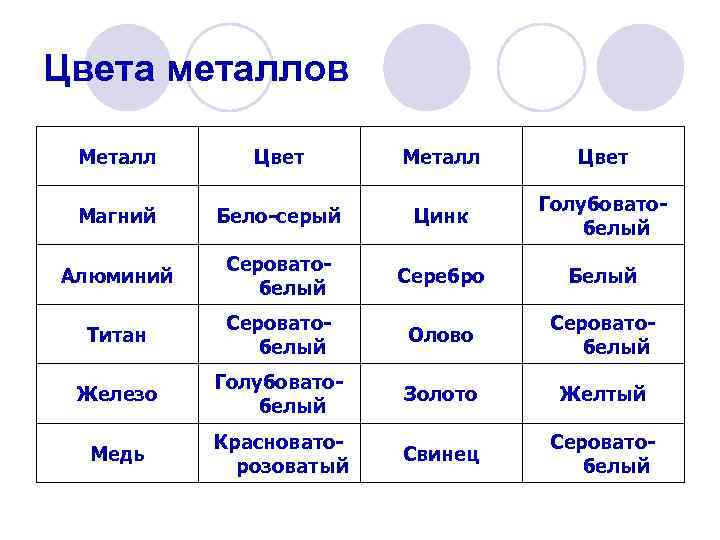 Цвета металлов Металл Цвет Магний Бело-серый Цинк Голубоватобелый Алюминий Сероватобелый Серебро Белый Титан Сероватобелый Олово Сероватобелый Железо Голубоватобелый Золото Желтый Медь Красноваторозоватый Свинец Сероватобелый
Цвета металлов Металл Цвет Магний Бело-серый Цинк Голубоватобелый Алюминий Сероватобелый Серебро Белый Титан Сероватобелый Олово Сероватобелый Железо Голубоватобелый Золото Желтый Медь Красноваторозоватый Свинец Сероватобелый
 Плотность. Это одна из важнейших характеристик металлов и сплавов. По плотности металлы делятся на следующие группы: l легкие (плотность не более 5 г/см 3) магний, алюминий, титан и др. : l тяжелые (плотность от 5 до 10 г/см 3) железо, никель, медь, цинк, олово и др. (это наиболее обширная группа); l очень тяжелые (плотность более 10 г/см 3) молибден, вольфрам, золото, свинец и др.
Плотность. Это одна из важнейших характеристик металлов и сплавов. По плотности металлы делятся на следующие группы: l легкие (плотность не более 5 г/см 3) магний, алюминий, титан и др. : l тяжелые (плотность от 5 до 10 г/см 3) железо, никель, медь, цинк, олово и др. (это наиболее обширная группа); l очень тяжелые (плотность более 10 г/см 3) молибден, вольфрам, золото, свинец и др.
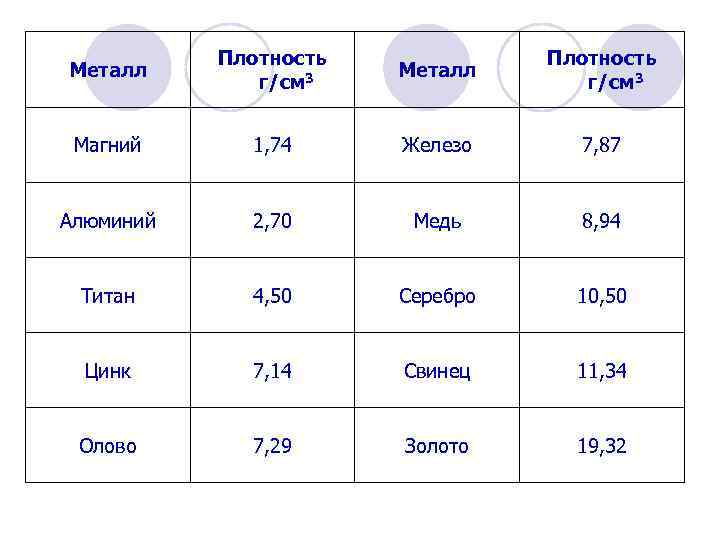 Металл Плотность г/см 3 Магний 1, 74 Железо 7, 87 Алюминий 2, 70 Медь 8, 94 Титан 4, 50 Серебро 10, 50 Цинк 7, 14 Свинец 11, 34 Олово 7, 29 Золото 19, 32
Металл Плотность г/см 3 Магний 1, 74 Железо 7, 87 Алюминий 2, 70 Медь 8, 94 Титан 4, 50 Серебро 10, 50 Цинк 7, 14 Свинец 11, 34 Олово 7, 29 Золото 19, 32
 Температура плавления В зависимости от температуры плавления металлы подразделяют на следующие группы: l легкоплавкие (температура плавления не превышает 600 o. С) цинк, олово, свинец, висмут и др. ; l среднеплавкие (от 600 o. С до 1600 o. С) к ним относятся почти половина металлов, в том числе магний, алюминий, железо, никель, медь, золото; l тугоплавкие ( более 1600 o. С) вольфрам, молибден, титан, хром и др.
Температура плавления В зависимости от температуры плавления металлы подразделяют на следующие группы: l легкоплавкие (температура плавления не превышает 600 o. С) цинк, олово, свинец, висмут и др. ; l среднеплавкие (от 600 o. С до 1600 o. С) к ним относятся почти половина металлов, в том числе магний, алюминий, железо, никель, медь, золото; l тугоплавкие ( более 1600 o. С) вольфрам, молибден, титан, хром и др.
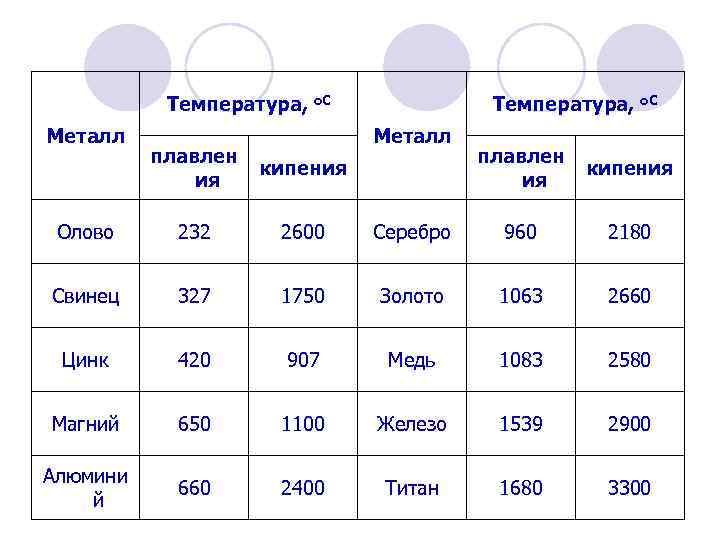 Температура, o. С Металл плавлен ия кипения Олово 232 2600 Серебро 960 2180 Свинец 327 1750 Золото 1063 2660 Цинк 420 907 Медь 1083 2580 Магний 650 1100 Железо 1539 2900 Алюмини й 660 2400 Титан 1680 3300
Температура, o. С Металл плавлен ия кипения Олово 232 2600 Серебро 960 2180 Свинец 327 1750 Золото 1063 2660 Цинк 420 907 Медь 1083 2580 Магний 650 1100 Железо 1539 2900 Алюмини й 660 2400 Титан 1680 3300
 Теплоемкость характеризует передачу тепловой энергии от оной части тела к другой, а точнее, молекулярной перенос теплоты в сплошной среде, обусловленный наличием градиента температуры. l Качество художественного литья тесно связано с теплопроводностью металла. В процессе выплавке важно не только обеспечить достаточно высокую температуру металла, но и добиться равномерного распределения температуры во всем объеме жидкой ванны. Чем выше теплопроводность, тем равномернее распределена температура. При электродуговой плавке, несмотря на высокую теплопроводность большинства металлов, перепад температуры по сечению ванны достигает 70 80 o. С, а для металла с низкой теплопроводностью этот перепад может достигать 200 o. С и более. l
Теплоемкость характеризует передачу тепловой энергии от оной части тела к другой, а точнее, молекулярной перенос теплоты в сплошной среде, обусловленный наличием градиента температуры. l Качество художественного литья тесно связано с теплопроводностью металла. В процессе выплавке важно не только обеспечить достаточно высокую температуру металла, но и добиться равномерного распределения температуры во всем объеме жидкой ванны. Чем выше теплопроводность, тем равномернее распределена температура. При электродуговой плавке, несмотря на высокую теплопроводность большинства металлов, перепад температуры по сечению ванны достигает 70 80 o. С, а для металла с низкой теплопроводностью этот перепад может достигать 200 o. С и более. l
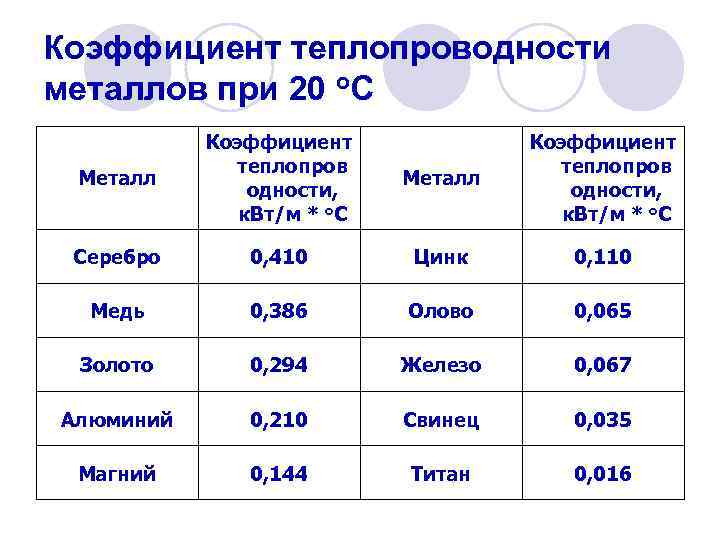 Коэффициент теплопроводности металлов при 20 o. С Металл Коэффициент теплопров одности, к. Вт/м * o. С Серебро 0, 410 Цинк 0, 110 Медь 0, 386 Олово 0, 065 Золото 0, 294 Железо 0, 067 Алюминий 0, 210 Свинец 0, 035 Магний 0, 144 Титан 0, 016
Коэффициент теплопроводности металлов при 20 o. С Металл Коэффициент теплопров одности, к. Вт/м * o. С Серебро 0, 410 Цинк 0, 110 Медь 0, 386 Олово 0, 065 Золото 0, 294 Железо 0, 067 Алюминий 0, 210 Свинец 0, 035 Магний 0, 144 Титан 0, 016
 l Теплопроводность металлов дает возможность равномерно нагревать их для обработки давлением, термической обработки; она обеспечивает также возможность пайки металлов, их сварки и т. п.
l Теплопроводность металлов дает возможность равномерно нагревать их для обработки давлением, термической обработки; она обеспечивает также возможность пайки металлов, их сварки и т. п.
 Коэффициент теплового расширения Эта величина, характеризующая изменение размеров образца длиной 1 м при нагревании на 1 o. С, имеет важное значение при эмальерных работах. l Коэффициенты теплового расширения металлической основы и эмали должны иметь по возможности близкие значения, чтобы после обжига эмаль не растрескивалась. Большинство эмалей, представляющих твердый коэффициент оксидов кремния и других элементов, имеют низкий коэффициент теплового расширения. Как показала практика, эмали очень хорошо держаться на железе, золоте, менее прочно на меди и серебре. l
Коэффициент теплового расширения Эта величина, характеризующая изменение размеров образца длиной 1 м при нагревании на 1 o. С, имеет важное значение при эмальерных работах. l Коэффициенты теплового расширения металлической основы и эмали должны иметь по возможности близкие значения, чтобы после обжига эмаль не растрескивалась. Большинство эмалей, представляющих твердый коэффициент оксидов кремния и других элементов, имеют низкий коэффициент теплового расширения. Как показала практика, эмали очень хорошо держаться на железе, золоте, менее прочно на меди и серебре. l
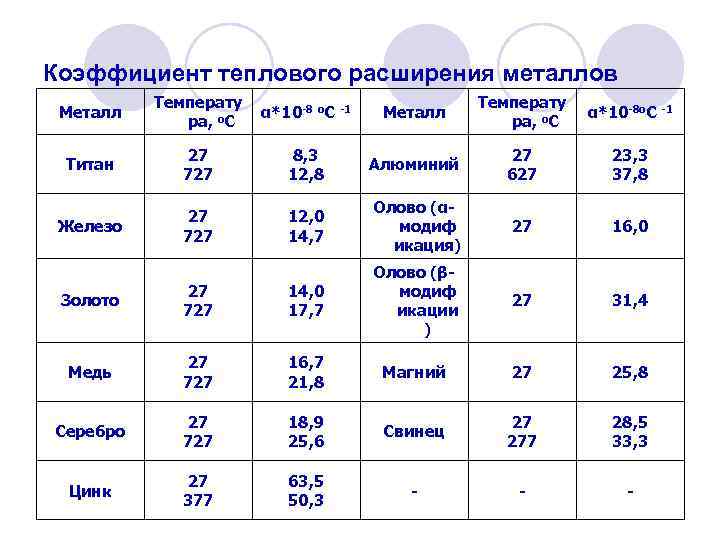 Коэффициент теплового расширения металлов Металл Температу ра, o. С α*10 -8 o. С -1 Металл Температу ра, o. С α*10 -8 o. С -1 Титан 27 727 8, 3 12, 8 Алюминий 27 627 23, 3 37, 8 Железо 27 727 12, 0 14, 7 Олово (αмодиф икация) 27 16, 0 27 31, 4 Золото 27 727 14, 0 17, 7 Олово (βмодиф икации ) Медь 27 727 16, 7 21, 8 Магний 27 25, 8 Серебро 27 727 18, 9 25, 6 Свинец 27 277 28, 5 33, 3 Цинк 27 377 63, 5 50, 3 - - -
Коэффициент теплового расширения металлов Металл Температу ра, o. С α*10 -8 o. С -1 Металл Температу ра, o. С α*10 -8 o. С -1 Титан 27 727 8, 3 12, 8 Алюминий 27 627 23, 3 37, 8 Железо 27 727 12, 0 14, 7 Олово (αмодиф икация) 27 16, 0 27 31, 4 Золото 27 727 14, 0 17, 7 Олово (βмодиф икации ) Медь 27 727 16, 7 21, 8 Магний 27 25, 8 Серебро 27 727 18, 9 25, 6 Свинец 27 277 28, 5 33, 3 Цинк 27 377 63, 5 50, 3 - - -
 l Некоторые сплавы металлов имеют коэффициент линейного расширения, близкий к нулю; такие сплавы применяют для изготовления точных приборов. l Расширение металлов должно приниматься во внимание при строительстве длинных сооружений, например мостов, трубопроводов. Нужно также учитывать, что две детали из металлов с разным коэффициентом расширения и скрепленные между собой при нагревании изгибаются.
l Некоторые сплавы металлов имеют коэффициент линейного расширения, близкий к нулю; такие сплавы применяют для изготовления точных приборов. l Расширение металлов должно приниматься во внимание при строительстве длинных сооружений, например мостов, трубопроводов. Нужно также учитывать, что две детали из металлов с разным коэффициентом расширения и скрепленные между собой при нагревании изгибаются.
 Отражательная способность. l Это способность металла отражать световые волны определенной длины, которая воспринимает человеческим глазом как цвет.
Отражательная способность. l Это способность металла отражать световые волны определенной длины, которая воспринимает человеческим глазом как цвет.
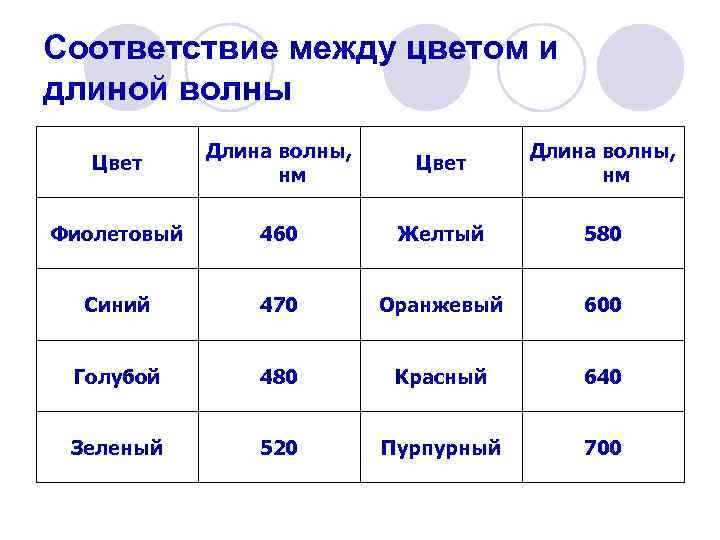 Соответствие между цветом и длиной волны Цвет Длина волны, нм Фиолетовый 460 Желтый 580 Синий 470 Оранжевый 600 Голубой 480 Красный 640 Зеленый 520 Пурпурный 700
Соответствие между цветом и длиной волны Цвет Длина волны, нм Фиолетовый 460 Желтый 580 Синий 470 Оранжевый 600 Голубой 480 Красный 640 Зеленый 520 Пурпурный 700
 Магнитные свойства металлов играют роль в электромашиностроении (электрические генераторы, электродвигатели, трансформаторы), в приборостроении (телефонные и телеграфные аппараты) и т. д. l У большинства металлов магнитная восприимчивость по абсолютной величине сравнительно мала (~ 10 9) и слабо зависит от температуры. l Среди металлов есть диамагнетики, напр. Bi (= — 1, 34. 10 9), и парамагнетики, причем все переходные металлы, кроме металлов I и II гр. , парамагнитны. l Некоторые из них при температурах точки Кюри переходят в магнитно упорядоченное состояние. Металлы триады Fe, а также Gd и некоторые другие лантаноиды ферромагнетики, тогда как Сr, Мn, большинство лантаноидов антиферромагнетики. l
Магнитные свойства металлов играют роль в электромашиностроении (электрические генераторы, электродвигатели, трансформаторы), в приборостроении (телефонные и телеграфные аппараты) и т. д. l У большинства металлов магнитная восприимчивость по абсолютной величине сравнительно мала (~ 10 9) и слабо зависит от температуры. l Среди металлов есть диамагнетики, напр. Bi (= — 1, 34. 10 9), и парамагнетики, причем все переходные металлы, кроме металлов I и II гр. , парамагнитны. l Некоторые из них при температурах точки Кюри переходят в магнитно упорядоченное состояние. Металлы триады Fe, а также Gd и некоторые другие лантаноиды ферромагнетики, тогда как Сr, Мn, большинство лантаноидов антиферромагнетики. l
 Механические свойства l прочность, l твердость, l упругость, l вязкость, l пластичность
Механические свойства l прочность, l твердость, l упругость, l вязкость, l пластичность
 l l l Прочность способность материала сопротивляться разрушению и появлению остаточных деформаций под действием внешних сил. Удельная прочность отношение предела прочности к плотности; для некоторых, например, алюминиевых сплавов или титана, она выше, чем для стали. Твердостью называется сопротивление тела деформации в поверхностном слое при местном силовом контактном воздействии. Упругость свойство материалов восстанавливать свою форму после прекращения действия внешних сил, вызвавших изменение формы (деформацию). Пластичность свойство металла деформироваться без разрушения под действием внешних сил и сохранять новую форму после прекращения действия сил. Пластичность свойство, обратное упругости. Вязкостью материала называют его способность поглощать механическую энергию и при этом проявлять значительную пластичность вплоть до разрушения. Вязкость свойство, обратное хрупкости.
l l l Прочность способность материала сопротивляться разрушению и появлению остаточных деформаций под действием внешних сил. Удельная прочность отношение предела прочности к плотности; для некоторых, например, алюминиевых сплавов или титана, она выше, чем для стали. Твердостью называется сопротивление тела деформации в поверхностном слое при местном силовом контактном воздействии. Упругость свойство материалов восстанавливать свою форму после прекращения действия внешних сил, вызвавших изменение формы (деформацию). Пластичность свойство металла деформироваться без разрушения под действием внешних сил и сохранять новую форму после прекращения действия сил. Пластичность свойство, обратное упругости. Вязкостью материала называют его способность поглощать механическую энергию и при этом проявлять значительную пластичность вплоть до разрушения. Вязкость свойство, обратное хрупкости.
 l Современными методами испытания металлов являются механические испытания, химический, спектральный, металлографический и рентгенографический анализы, технологические пробы, дефектоскопия, а также испытания на обрабатываемость резанием, коррозионные испытания металлов и др. Эти испытании дают возможность получить представление о природе металлов, их строении, составе и свойствах, а также определить качество готовых изделий.
l Современными методами испытания металлов являются механические испытания, химический, спектральный, металлографический и рентгенографический анализы, технологические пробы, дефектоскопия, а также испытания на обрабатываемость резанием, коррозионные испытания металлов и др. Эти испытании дают возможность получить представление о природе металлов, их строении, составе и свойствах, а также определить качество готовых изделий.
 Вязкие металлы применяют в тех случаях, когда детали при работе подвергаются ударной нагрузке. Пластичность металлов дает возможность обрабатывать их давлением (ковать, прокатывать). Механические испытания имеют важнейшее значение в промышленности. Детали машин, механизмов и сооружений работают под различного вида нагрузками: одни детали нагружены постоянно действующей в одном направлении силой, другие подвержены ударам, у третьих силы более или менее часто изменяются по своей величине и направлению. Некоторые детали машин подвергаются нагрузкам при повышенных или низких температурах, при действии коррозии и т. п. ; такие детали работают в сложных условиях.
Вязкие металлы применяют в тех случаях, когда детали при работе подвергаются ударной нагрузке. Пластичность металлов дает возможность обрабатывать их давлением (ковать, прокатывать). Механические испытания имеют важнейшее значение в промышленности. Детали машин, механизмов и сооружений работают под различного вида нагрузками: одни детали нагружены постоянно действующей в одном направлении силой, другие подвержены ударам, у третьих силы более или менее часто изменяются по своей величине и направлению. Некоторые детали машин подвергаются нагрузкам при повышенных или низких температурах, при действии коррозии и т. п. ; такие детали работают в сложных условиях.
 Наиболее распространенными испытаниями являются испытания на твердость, статическое растяжение, динамические испытания. l Статическими называют такие испытания, при которых испытуемый металл подвергают воздействию постоянной силы или силы, возрастающей медленно. l Динамическими называют испытания, при которых испытуемый металл подвергают воздействию удара или силы, возрастающей быстро. l Кроме того, иногда производят испытания на усталость, ползучесть и износ, которые дают более полное представление о свойствах металлов. l
Наиболее распространенными испытаниями являются испытания на твердость, статическое растяжение, динамические испытания. l Статическими называют такие испытания, при которых испытуемый металл подвергают воздействию постоянной силы или силы, возрастающей медленно. l Динамическими называют испытания, при которых испытуемый металл подвергают воздействию удара или силы, возрастающей быстро. l Кроме того, иногда производят испытания на усталость, ползучесть и износ, которые дают более полное представление о свойствах металлов. l
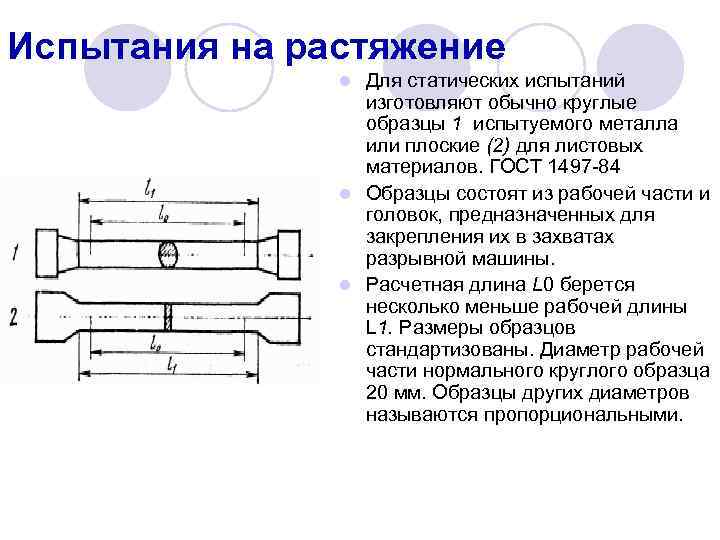 Испытания на растяжение Для статических испытаний изготовляют обычно круглые образцы 1 испытуемого металла или плоские (2) для листовых материалов. ГОСТ 1497 84 l Образцы состоят из рабочей части и головок, предназначенных для закрепления их в захватах разрывной машины. l Расчетная длина L 0 берется несколько меньше рабочей длины L 1. Размеры образцов стандартизованы. Диаметр рабочей части нормального круглого образца 20 мм. Образцы других диаметров называются пропорциональными. l
Испытания на растяжение Для статических испытаний изготовляют обычно круглые образцы 1 испытуемого металла или плоские (2) для листовых материалов. ГОСТ 1497 84 l Образцы состоят из рабочей части и головок, предназначенных для закрепления их в захватах разрывной машины. l Расчетная длина L 0 берется несколько меньше рабочей длины L 1. Размеры образцов стандартизованы. Диаметр рабочей части нормального круглого образца 20 мм. Образцы других диаметров называются пропорциональными. l
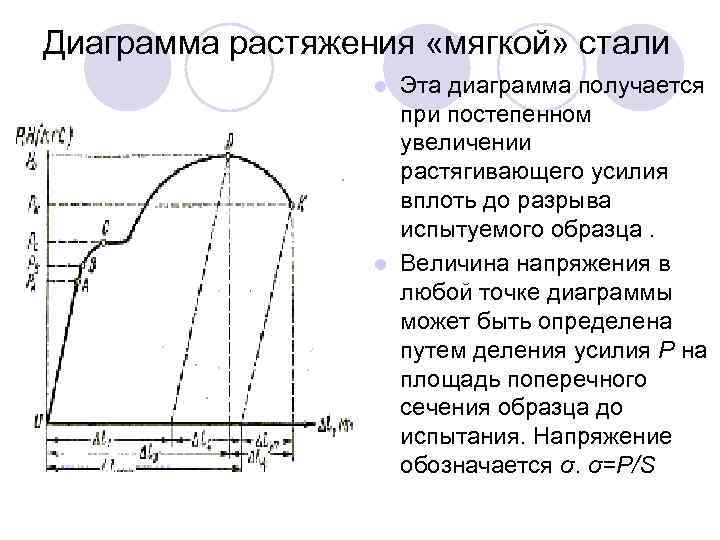 Диаграмма растяжения «мягкой» стали Эта диаграмма получается при постепенном увеличении растягивающего усилия вплоть до разрыва испытуемого образца. l Величина напряжения в любой точке диаграммы может быть определена путем деления усилия Р на площадь поперечного сечения образца до испытания. Напряжение обозначается σ. σ=Р/S l
Диаграмма растяжения «мягкой» стали Эта диаграмма получается при постепенном увеличении растягивающего усилия вплоть до разрыва испытуемого образца. l Величина напряжения в любой точке диаграммы может быть определена путем деления усилия Р на площадь поперечного сечения образца до испытания. Напряжение обозначается σ. σ=Р/S l
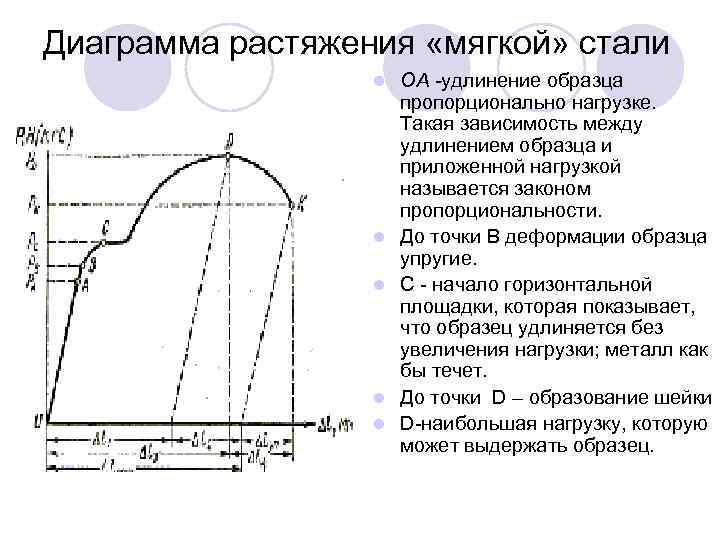 Диаграмма растяжения «мягкой» стали l l l ОА -удлинение образца пропорционально нагрузке. Такая зависимость между удлинением образца и приложенной нагрузкой называется законом пропорциональности. До точки В деформации образца упругие. С начало горизонтальной площадки, которая показывает, что образец удлиняется без увеличения нагрузки; металл как бы течет. До точки D – образование шейки D наибольшая нагрузку, которую может выдержать образец.
Диаграмма растяжения «мягкой» стали l l l ОА -удлинение образца пропорционально нагрузке. Такая зависимость между удлинением образца и приложенной нагрузкой называется законом пропорциональности. До точки В деформации образца упругие. С начало горизонтальной площадки, которая показывает, что образец удлиняется без увеличения нагрузки; металл как бы течет. До точки D – образование шейки D наибольшая нагрузку, которую может выдержать образец.
 Наименьшее напряжение, при котором без заметного увеличения нагрузки продолжается деформация испытуемого образца, называется физическим пределом текучести. Предел текучести т определяется по формуле: т = Pс / F 0, где Рc — нагрузка в точке С. l Условное напряжение, отвечающее наибольшей нагрузке, предшествовавшей разрушению образца, называется пределом прочности при растяжении (временным сопротивлением разрыву) и определяется по формуле σв = PD / F 0, где PD нагрузка в точке D. l
Наименьшее напряжение, при котором без заметного увеличения нагрузки продолжается деформация испытуемого образца, называется физическим пределом текучести. Предел текучести т определяется по формуле: т = Pс / F 0, где Рc — нагрузка в точке С. l Условное напряжение, отвечающее наибольшей нагрузке, предшествовавшей разрушению образца, называется пределом прочности при растяжении (временным сопротивлением разрыву) и определяется по формуле σв = PD / F 0, где PD нагрузка в точке D. l
 Абсолютное остаточное удлинение ∆lост сложится из удлинения равномерного ∆l 1 и удлинения местного ∆l 2 т. е. l ∆lост = ∆l 1 + ∆l 2. Для оценки пластичности металла важно знать относительное удлинение δ и относительное сужение площади поперечного сечения Ψ в процентах. l Относительное удлинение (%) определяют по формуле где l 1 длина образца после разрыва, мм; l 0 расчетная длина образца, мм. При удлинении одновременно уменьшается площадь поперечного сечения образца. В месте разрыва эта площадь будет наименьшей. Относительное сужение (%) определяют по формуле где F 0 начальная площадь поперечного сечения образца, мм 2; F 1 площадь в месте разрыва, мм 2. Таким образом, при статическом испытании на растяжение определяют характеристики прочности σyп, σт, σв и характеристики пластичности δ и Ψ.
Абсолютное остаточное удлинение ∆lост сложится из удлинения равномерного ∆l 1 и удлинения местного ∆l 2 т. е. l ∆lост = ∆l 1 + ∆l 2. Для оценки пластичности металла важно знать относительное удлинение δ и относительное сужение площади поперечного сечения Ψ в процентах. l Относительное удлинение (%) определяют по формуле где l 1 длина образца после разрыва, мм; l 0 расчетная длина образца, мм. При удлинении одновременно уменьшается площадь поперечного сечения образца. В месте разрыва эта площадь будет наименьшей. Относительное сужение (%) определяют по формуле где F 0 начальная площадь поперечного сечения образца, мм 2; F 1 площадь в месте разрыва, мм 2. Таким образом, при статическом испытании на растяжение определяют характеристики прочности σyп, σт, σв и характеристики пластичности δ и Ψ.
 Определение твердости Метод Бринелля l Стальной закаленный шарик диаметром D (10; 5 или 2, 5 мм) вдавливается в испытуемый образец силой Р. В результате на поверхности образца остается отпечаток в форме шарового сегмента диаметром d. Величина отпечатка будет тем меньше, чем тверже металл. Твердость по Бринеллю НВ вычисляется по формуле HB=P/F, где Р нагрузка на шарик, Н (кгс); F величина поверхности отпечатка, мм 2. Для испытания на твердость по Бринеллю в настоящее время применяют в основном рычажные прессы. l По методу Бринелля можно испытывать материалы с твердостью НВ до 4500 МПа; если материалы тверже, то стальной шарик может деформироваться. Этот метод непригоден также для испытаний тонколистового материала. l
Определение твердости Метод Бринелля l Стальной закаленный шарик диаметром D (10; 5 или 2, 5 мм) вдавливается в испытуемый образец силой Р. В результате на поверхности образца остается отпечаток в форме шарового сегмента диаметром d. Величина отпечатка будет тем меньше, чем тверже металл. Твердость по Бринеллю НВ вычисляется по формуле HB=P/F, где Р нагрузка на шарик, Н (кгс); F величина поверхности отпечатка, мм 2. Для испытания на твердость по Бринеллю в настоящее время применяют в основном рычажные прессы. l По методу Бринелля можно испытывать материалы с твердостью НВ до 4500 МПа; если материалы тверже, то стальной шарик может деформироваться. Этот метод непригоден также для испытаний тонколистового материала. l
 Метод Роквелла испытание на твердость производится путем вдавливания в образец стального шарика диаметром D = 1, 58 мм (1/16 дюйма) или алмазного конуса с углом 120°. Стальной шарик применяется для испытания мягких металлов (твердость по Бринеллю меньше 2200 МПа) при нагрузке 981 Н (100 кгс), алмазный конус — для испытания твердых металлов при нагрузке 1471 Н (150 кгс). l Число твердости по Роквеллу обозначается HR с добавлением индекса шкалы, по которой производилось испытание, например HRB или HRС. Для испытания очень твердых материалов применяют алмазный конус при нагрузке 588 Н (60 кгс), отсчеты производят по черной шкале, а число твердости обозначают HRA.
Метод Роквелла испытание на твердость производится путем вдавливания в образец стального шарика диаметром D = 1, 58 мм (1/16 дюйма) или алмазного конуса с углом 120°. Стальной шарик применяется для испытания мягких металлов (твердость по Бринеллю меньше 2200 МПа) при нагрузке 981 Н (100 кгс), алмазный конус — для испытания твердых металлов при нагрузке 1471 Н (150 кгс). l Число твердости по Роквеллу обозначается HR с добавлением индекса шкалы, по которой производилось испытание, например HRB или HRС. Для испытания очень твердых материалов применяют алмазный конус при нагрузке 588 Н (60 кгс), отсчеты производят по черной шкале, а число твердости обозначают HRA.
 Метод Виккерса позволяет измерять твердость как мягких, так и очень твердых металлов и сплавов; он пригоден для определения твердости тонких поверхностных слоев (например, при химико термической обработке). По этому методу в образец вдавливается четырехгранная алмазная пирамида с углом при вершине 136°. Нагрузка может применяться от 49 до 1170 Н (от 5 до 120 кгс). Замер отпечатка по диагонали производится с помощью микроскопа, находящегося приборе. Число твердости определяется по формуле: HV=P/d 2, где Р нагрузка, Н (кгс); d длина диагонали отпечатка, мм.
Метод Виккерса позволяет измерять твердость как мягких, так и очень твердых металлов и сплавов; он пригоден для определения твердости тонких поверхностных слоев (например, при химико термической обработке). По этому методу в образец вдавливается четырехгранная алмазная пирамида с углом при вершине 136°. Нагрузка может применяться от 49 до 1170 Н (от 5 до 120 кгс). Замер отпечатка по диагонали производится с помощью микроскопа, находящегося приборе. Число твердости определяется по формуле: HV=P/d 2, где Р нагрузка, Н (кгс); d длина диагонали отпечатка, мм.
 Испытания на ударный изгиб Применяются, если детали машины подвергается ударным нагрузкам. (динамическая нагрузка). l Для ударных испытаний на изгиб применяют образцы стандартной формы. При испытании образец устанавливают на опорах маятникового копра (рис. ). Маятник поднимают на высоту Н. Затем маятник освобождают, и он, свободно падая, ударяет по образцу и разрушает его; на это расходуется часть энергии. Оставшаяся энергия поднимает маятник на некоторую высоту h, которую определяют по шкале копра. l
Испытания на ударный изгиб Применяются, если детали машины подвергается ударным нагрузкам. (динамическая нагрузка). l Для ударных испытаний на изгиб применяют образцы стандартной формы. При испытании образец устанавливают на опорах маятникового копра (рис. ). Маятник поднимают на высоту Н. Затем маятник освобождают, и он, свободно падая, ударяет по образцу и разрушает его; на это расходуется часть энергии. Оставшаяся энергия поднимает маятник на некоторую высоту h, которую определяют по шкале копра. l
 Химические свойства l Коррозионная стойкость важна для изделий, работающих в химически активных средах (колосниковые решетки, детали машин в химической промышленности). Для деталей и сооружений, которые должны обладать высокой коррозионной стойкостью, производят специальные нержавеющие, кислотостойкие и жаростойкие стали. Для изделий также применяют защитные покрытия.
Химические свойства l Коррозионная стойкость важна для изделий, работающих в химически активных средах (колосниковые решетки, детали машин в химической промышленности). Для деталей и сооружений, которые должны обладать высокой коррозионной стойкостью, производят специальные нержавеющие, кислотостойкие и жаростойкие стали. Для изделий также применяют защитные покрытия.
 Технологические свойства l l l Технологические свойства имеют важное значение при тех или иных видах обработки (обработка давлением, сварки и др. ). Ковкость—свойство металла подвергаться ковке и другим видам обработки давлением; Жидкотекучесть — свойство расплавленного металла заполнять литейную форму во всех ее частях и давать плотные отливки точной конфигурации; Свариваемость — свойство металла давать прочные сварные соединения; Обрабатываемость резанием— свойство металлов подвергаться обработке режущими инструментами для придания деталям определенной формы, размеров и шероховатости поверхности.
Технологические свойства l l l Технологические свойства имеют важное значение при тех или иных видах обработки (обработка давлением, сварки и др. ). Ковкость—свойство металла подвергаться ковке и другим видам обработки давлением; Жидкотекучесть — свойство расплавленного металла заполнять литейную форму во всех ее частях и давать плотные отливки точной конфигурации; Свариваемость — свойство металла давать прочные сварные соединения; Обрабатываемость резанием— свойство металлов подвергаться обработке режущими инструментами для придания деталям определенной формы, размеров и шероховатости поверхности.
 Эксплуатационные свойства l Многие изделия, кроме общей прочности, должны обладать еще особыми свойствами, характерными для работы данного изделия. Например, режущие инструменты должны обладать высокой твердостью. Для изготовления режущих и других инструментов применяют инструментальные стали и сплавы, а для рессор и пружин стали и сплавы, обладающие высокой упругостью.
Эксплуатационные свойства l Многие изделия, кроме общей прочности, должны обладать еще особыми свойствами, характерными для работы данного изделия. Например, режущие инструменты должны обладать высокой твердостью. Для изготовления режущих и других инструментов применяют инструментальные стали и сплавы, а для рессор и пружин стали и сплавы, обладающие высокой упругостью.
 Макро- и микроанализ металлов
Макро- и микроанализ металлов
 Макроанализ Для макроанализа готовят образец шлиф или излом, по которому выявляют макроструктуру строение металла и сплава, видимое невооруженным глазом или в лупу. l Подготовка: выравнивании напильником или шлифованием наждачной бумагой поверхности. В случае необходимости шлиф травят кислотами, щелочами или растворами солей, которые по разному растворяют или окрашивают различные по составу или ориентации части на шлифе. l При макроисследовании определяют форму и расположение кристаллов в изделиях, полученных литьем или обработкой давлением; с помощью макроанализа можно обнаружить усадочные раковины и рыхлости, пустоты, трещины, неметаллические включения (шлак, графит в сером чугуне и т. д. ), наличие и характер расположения некоторых вредных примесей, например серы. l Изломы металла дают представление о величине зерен, характере строения и структуры. l
Макроанализ Для макроанализа готовят образец шлиф или излом, по которому выявляют макроструктуру строение металла и сплава, видимое невооруженным глазом или в лупу. l Подготовка: выравнивании напильником или шлифованием наждачной бумагой поверхности. В случае необходимости шлиф травят кислотами, щелочами или растворами солей, которые по разному растворяют или окрашивают различные по составу или ориентации части на шлифе. l При макроисследовании определяют форму и расположение кристаллов в изделиях, полученных литьем или обработкой давлением; с помощью макроанализа можно обнаружить усадочные раковины и рыхлости, пустоты, трещины, неметаллические включения (шлак, графит в сером чугуне и т. д. ), наличие и характер расположения некоторых вредных примесей, например серы. l Изломы металла дают представление о величине зерен, характере строения и структуры. l
 Микроанализ Шлиф для микроанализа приготовляют так же, как и для макроанализа, но после шлифования его полируют до зеркального блеска. l По шлифу, с помощью металлографического микроскопа, выявляют микроструктуру: наличие, количество и форму тех или иных структурных составляющих, загрязненность посторонними включениями. Наличие и размеры пор и неметаллических включений определяют по нетравленым шлифам; для выявления основной структуры шлиф подвергают травлению. l Наряду с обычным световым микроскопом широко применяют электронный микроскоп, в котором вместо световых лучей используются электронные; эти лучи испускает раскаленная вольфрамовая спираль. Электронный микроскоп обеспечивает электронно оптическое увеличение в несколько тысяч и десятков тысяч раз. l
Микроанализ Шлиф для микроанализа приготовляют так же, как и для макроанализа, но после шлифования его полируют до зеркального блеска. l По шлифу, с помощью металлографического микроскопа, выявляют микроструктуру: наличие, количество и форму тех или иных структурных составляющих, загрязненность посторонними включениями. Наличие и размеры пор и неметаллических включений определяют по нетравленым шлифам; для выявления основной структуры шлиф подвергают травлению. l Наряду с обычным световым микроскопом широко применяют электронный микроскоп, в котором вместо световых лучей используются электронные; эти лучи испускает раскаленная вольфрамовая спираль. Электронный микроскоп обеспечивает электронно оптическое увеличение в несколько тысяч и десятков тысяч раз. l
 ТЕОРИЯ СПЛАВОВ
ТЕОРИЯ СПЛАВОВ
 Металлическими сплавами называют сочетание двух или нескольких металлов и неметаллов, у которых сохраняются металлические свойства. Большинство сплавов получают в жидком состоянии (сплавлением), однако они могут быть получены также путем спекания, электролиза, конденсации (сгущения) из парообразного состояния и др. Компонентами называют химические элементы или их соединения в составе сплава. По числу компонентов сплавы делят на двойные, тройные и т. д. В зависимости от природы компонентов, составляющих сплав, различают: 1) сплав механическая смесь компонентов; 2) сплав твердый раствор компонентов; 3) сплав химическое соединение компонентов.
Металлическими сплавами называют сочетание двух или нескольких металлов и неметаллов, у которых сохраняются металлические свойства. Большинство сплавов получают в жидком состоянии (сплавлением), однако они могут быть получены также путем спекания, электролиза, конденсации (сгущения) из парообразного состояния и др. Компонентами называют химические элементы или их соединения в составе сплава. По числу компонентов сплавы делят на двойные, тройные и т. д. В зависимости от природы компонентов, составляющих сплав, различают: 1) сплав механическая смесь компонентов; 2) сплав твердый раствор компонентов; 3) сплав химическое соединение компонентов.
 Сплавы механические смеси неоднородны и представляют собой мельчайшую смесь кристаллитов компонентов. l Сплавы твердые растворы и сплавы химические соединения однородны, причем первые могут образовываться при различном соотношении компонентов, а вторые — только при строго определенном весовом соотношении компонентов, как всякое химическое соединение. l В сплавах твердых растворах атомы растворимого вещества замещают атомы растворителя в кристаллической решетке (рис. а) или выделяются в нее (рис. б); l сплавы химические соединения образуют новую, особую кристаллическую решетку. l
Сплавы механические смеси неоднородны и представляют собой мельчайшую смесь кристаллитов компонентов. l Сплавы твердые растворы и сплавы химические соединения однородны, причем первые могут образовываться при различном соотношении компонентов, а вторые — только при строго определенном весовом соотношении компонентов, как всякое химическое соединение. l В сплавах твердых растворах атомы растворимого вещества замещают атомы растворителя в кристаллической решетке (рис. а) или выделяются в нее (рис. б); l сплавы химические соединения образуют новую, особую кристаллическую решетку. l
 Системой называют совокупность веществ в твердом, жидком и газообразном состояниях. Системы бывают простые и сложные. Простая система состоит из одного компонента. Сложная система включает несколько компонентов и представляет все возможные количественные сочетания их при различных температурах. l Фазой называют однородную часть системы, отделенную от других составляющих (фаз) поверхностью раздела. Следовательно, фазами могут быть химические элементы, твердые и жидкие растворы и химические соединения. l В жидком состоянии однородная система содержит одну фазу; при затвердевании всегда имеются две фазы жидкая и твердая. После затвердевания образуется или одна фаза (химический элемент, химическое соединение, твердый раствор), или сплав, содержащий смесь фаз. l
Системой называют совокупность веществ в твердом, жидком и газообразном состояниях. Системы бывают простые и сложные. Простая система состоит из одного компонента. Сложная система включает несколько компонентов и представляет все возможные количественные сочетания их при различных температурах. l Фазой называют однородную часть системы, отделенную от других составляющих (фаз) поверхностью раздела. Следовательно, фазами могут быть химические элементы, твердые и жидкие растворы и химические соединения. l В жидком состоянии однородная система содержит одну фазу; при затвердевании всегда имеются две фазы жидкая и твердая. После затвердевания образуется или одна фаза (химический элемент, химическое соединение, твердый раствор), или сплав, содержащий смесь фаз. l
 Диаграммы состояния системы, компоненты которых полностью взаимно растворяются в жидком состоянии. Они характеризуют процессы затвердевания и структурного изменения различных сплавов и дают наглядное представление о фазах в любом сплаве данной системы. По диаграмме состояния сплавов данных компонентов можно заранее судить о свойствах всех сплавов системы. l Диаграмма состояния позволяет выбирать температуру нагрева сплава при термической обработке, обработке давлением, температуру нагрева для литья. Построение диаграмм состояния производится по кривым охлаждения, полученным посредством термического анализа. l Термический анализ сводится к выявлению критических точек при нагревании и охлаждении металлов и сплавов и обычно сопровождается построением кривых в координатах температура время. l Без фазовых превращений, кривая охлаждения (нагревания) будет плавной без перегибов и уступов; если же при охлаждении (или нагревании) металла в нем происходят фазовые превращения, которые сопровождаются выделением (при нагревании поглощением) тепла, на кривой появятся горизонтальные участки или изломы (т. е. изменения направления кривой). l
Диаграммы состояния системы, компоненты которых полностью взаимно растворяются в жидком состоянии. Они характеризуют процессы затвердевания и структурного изменения различных сплавов и дают наглядное представление о фазах в любом сплаве данной системы. По диаграмме состояния сплавов данных компонентов можно заранее судить о свойствах всех сплавов системы. l Диаграмма состояния позволяет выбирать температуру нагрева сплава при термической обработке, обработке давлением, температуру нагрева для литья. Построение диаграмм состояния производится по кривым охлаждения, полученным посредством термического анализа. l Термический анализ сводится к выявлению критических точек при нагревании и охлаждении металлов и сплавов и обычно сопровождается построением кривых в координатах температура время. l Без фазовых превращений, кривая охлаждения (нагревания) будет плавной без перегибов и уступов; если же при охлаждении (или нагревании) металла в нем происходят фазовые превращения, которые сопровождаются выделением (при нагревании поглощением) тепла, на кривой появятся горизонтальные участки или изломы (т. е. изменения направления кривой). l
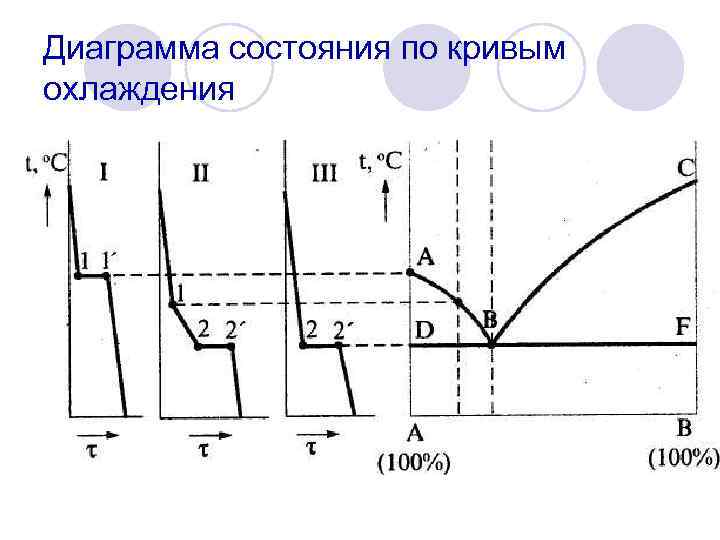 Диаграмма состояния по кривым охлаждения
Диаграмма состояния по кривым охлаждения
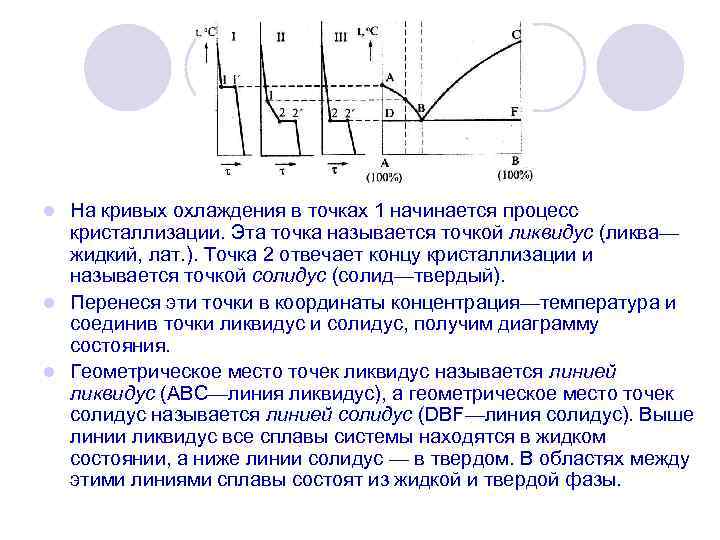 На кривых охлаждения в точках 1 начинается процесс кристаллизации. Эта точка называется точкой ликвидус (ликва— жидкий, лат. ). Точка 2 отвечает концу кристаллизации и называется точкой солидус (солид—твердый). l Перенеся эти точки в координаты концентрация—температура и соединив точки ликвидус и солидус, получим диаграмму состояния. l Геометрическое место точек ликвидус называется линией ликвидус (ABC—линия ликвидус), а геометрическое место точек солидус называется линией солидус (DBF—линия солидус). Выше линии ликвидус все сплавы системы находятся в жидком состоянии, а ниже линии солидус — в твердом. В областях между этими линиями сплавы состоят из жидкой и твердой фазы. l
На кривых охлаждения в точках 1 начинается процесс кристаллизации. Эта точка называется точкой ликвидус (ликва— жидкий, лат. ). Точка 2 отвечает концу кристаллизации и называется точкой солидус (солид—твердый). l Перенеся эти точки в координаты концентрация—температура и соединив точки ликвидус и солидус, получим диаграмму состояния. l Геометрическое место точек ликвидус называется линией ликвидус (ABC—линия ликвидус), а геометрическое место точек солидус называется линией солидус (DBF—линия солидус). Выше линии ликвидус все сплавы системы находятся в жидком состоянии, а ниже линии солидус — в твердом. В областях между этими линиями сплавы состоят из жидкой и твердой фазы. l
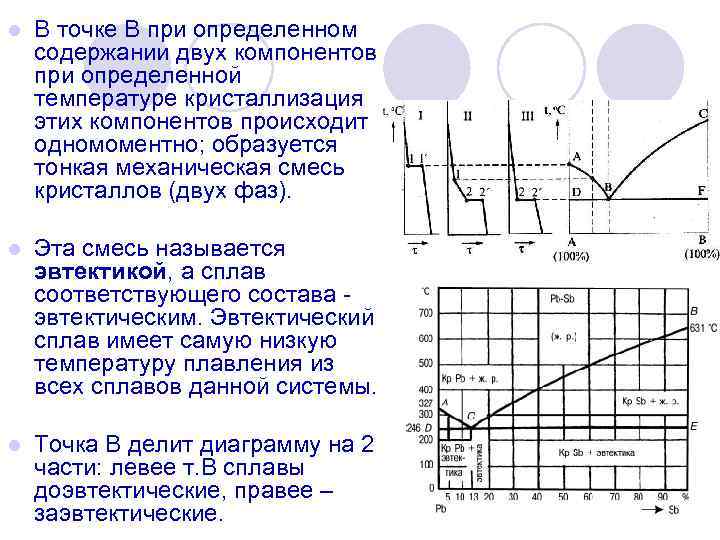 l В точке В при определенном содержании двух компонентов при определенной температуре кристаллизация этих компонентов происходит одномоментно; образуется тонкая механическая смесь кристаллов (двух фаз). l Эта смесь называется эвтектикой, а сплав соответствующего состава эвтектическим. Эвтектический сплав имеет самую низкую температуру плавления из всех сплавов данной системы. l Точка В делит диаграмму на 2 части: левее т. В сплавы доэвтектические, правее – заэвтектические.
l В точке В при определенном содержании двух компонентов при определенной температуре кристаллизация этих компонентов происходит одномоментно; образуется тонкая механическая смесь кристаллов (двух фаз). l Эта смесь называется эвтектикой, а сплав соответствующего состава эвтектическим. Эвтектический сплав имеет самую низкую температуру плавления из всех сплавов данной системы. l Точка В делит диаграмму на 2 части: левее т. В сплавы доэвтектические, правее – заэвтектические.
 РАСПОЗНАВАНИЕ МЕТАЛЛОВ И ИХ СПЛАВОВ
РАСПОЗНАВАНИЕ МЕТАЛЛОВ И ИХ СПЛАВОВ
 l Железоуглеродистые сплавы – стали и чугуны – важнейшие металлические сплавы современной техники. Объем их производства более чем в 10 раз превышает производство всех других металлов вместе взятых l Железо — белый металл с серебристым цветом, температура плавления чистого железа 1539 °С, плотность 7, 86 г/см 3, то есть металл тугоплавкий и тяжелый.
l Железоуглеродистые сплавы – стали и чугуны – важнейшие металлические сплавы современной техники. Объем их производства более чем в 10 раз превышает производство всех других металлов вместе взятых l Железо — белый металл с серебристым цветом, температура плавления чистого железа 1539 °С, плотность 7, 86 г/см 3, то есть металл тугоплавкий и тяжелый.
 l Железо имеет две полиморфные модификации и . В интервале температур 911 1392 °С существует Fe имеет решетку гексагональную, a Fe — кубическую объемно центрированную. При переходе Fe < > Fe изменяется тип решетки, изменяется плотность упаковки атомов, а следовательно, изменяется объем образца. Так, плотность Fe со ставляет 7, 55 г/см 3, а плотность Fe 7, 71 г/см 3.
l Железо имеет две полиморфные модификации и . В интервале температур 911 1392 °С существует Fe имеет решетку гексагональную, a Fe — кубическую объемно центрированную. При переходе Fe < > Fe изменяется тип решетки, изменяется плотность упаковки атомов, а следовательно, изменяется объем образца. Так, плотность Fe со ставляет 7, 55 г/см 3, а плотность Fe 7, 71 г/см 3.
 l Углерод является неметаллическим элементом. Он растворяется в железе и образует неустойчивое химическое соединение Fe 3 C— карбид железа, содержащий 6, 67%С и называемый цементитом. l Цементит соединение неустойчивое и при определенных условиях распадается с образованием свободного углерода в виде графита.
l Углерод является неметаллическим элементом. Он растворяется в железе и образует неустойчивое химическое соединение Fe 3 C— карбид железа, содержащий 6, 67%С и называемый цементитом. l Цементит соединение неустойчивое и при определенных условиях распадается с образованием свободного углерода в виде графита.
 Феррит- (Ф ) — твердый раствор углерода в Fe . Различают высокотемпературный феррит , существующий выше температуры 1392 °С, и низкотемпературный — ниже 911 °С. l Аустенит (А) — твердый раствор внедрения углерода в Fe . l Перлит – равномерная механическая смесь в сплаве феррита и цементита. Такое название эта смесь получила потому, что шлиф при ее травлении имеет перламутровый оттенок. l Железоуглеродистые сплавы, содержащие углерода менее 2, 14%, называются сталями, а более 2, 14% — чугуном. l
Феррит- (Ф ) — твердый раствор углерода в Fe . Различают высокотемпературный феррит , существующий выше температуры 1392 °С, и низкотемпературный — ниже 911 °С. l Аустенит (А) — твердый раствор внедрения углерода в Fe . l Перлит – равномерная механическая смесь в сплаве феррита и цементита. Такое название эта смесь получила потому, что шлиф при ее травлении имеет перламутровый оттенок. l Железоуглеродистые сплавы, содержащие углерода менее 2, 14%, называются сталями, а более 2, 14% — чугуном. l
 Чугун сплав железа с углеродом, в котором содержание последнего может быть от 2, 14 до 6, 67 %. Присутствие эвтектики в составе чугуна обуславливает его использование в качестве литейного сплава. Кроме углерода, в чугуне содержатся также примеси серы, фосфора, кремния. В зависимости от формы выделения углерода чугун подразделяют на белый и серый. l Белым называют чугун, в котором весь углерод находится в связанном состоянии в виде цементита. На свежем изломе белый чугун имеет светло серый цвет, высокую хрупкость (при ударе молотком раскалывается) и твердость (царапает стекло). Выделяют 3 группы: Доэвтектический (С 4, 3%) Эвтектический (С =4, 3%) Заэвтектический (С 4, 3%) l
Чугун сплав железа с углеродом, в котором содержание последнего может быть от 2, 14 до 6, 67 %. Присутствие эвтектики в составе чугуна обуславливает его использование в качестве литейного сплава. Кроме углерода, в чугуне содержатся также примеси серы, фосфора, кремния. В зависимости от формы выделения углерода чугун подразделяют на белый и серый. l Белым называют чугун, в котором весь углерод находится в связанном состоянии в виде цементита. На свежем изломе белый чугун имеет светло серый цвет, высокую хрупкость (при ударе молотком раскалывается) и твердость (царапает стекло). Выделяют 3 группы: Доэвтектический (С 4, 3%) Эвтектический (С =4, 3%) Заэвтектический (С 4, 3%) l
 l Серым называют чугун, в котором весь углерод или большая его часть находится в виде графита. Из за большого количества графита серый чугун на изломе имеет темно серый цвет, пачкает руки. Свежий излом такого чугуна характеризуется хрупкозернистой структурой. Изделия из серого чугуна вырабатывают только способом литья.
l Серым называют чугун, в котором весь углерод или большая его часть находится в виде графита. Из за большого количества графита серый чугун на изломе имеет темно серый цвет, пачкает руки. Свежий излом такого чугуна характеризуется хрупкозернистой структурой. Изделия из серого чугуна вырабатывают только способом литья.
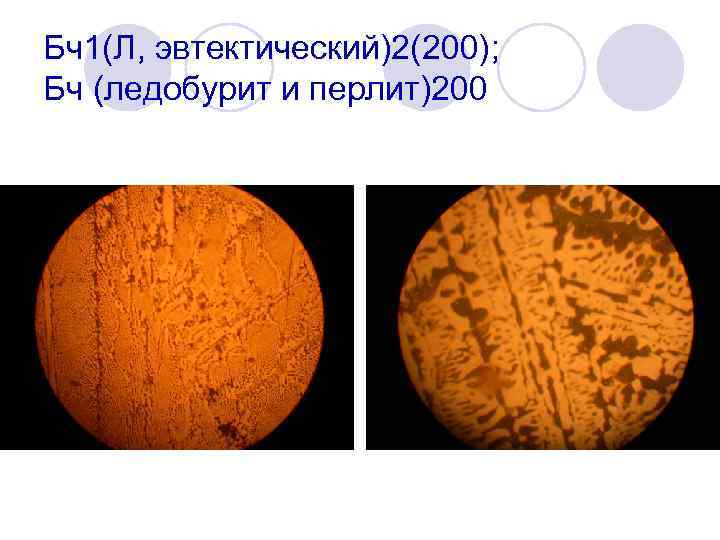 Бч1(Л, эвтектический)2(200); Бч (ледобурит и перлит)200
Бч1(Л, эвтектический)2(200); Бч (ледобурит и перлит)200
 Бч(Л, эвтектический)2(200) Бч(Л+Ц, заэвтектический)3(100)
Бч(Л, эвтектический)2(200) Бч(Л+Ц, заэвтектический)3(100)
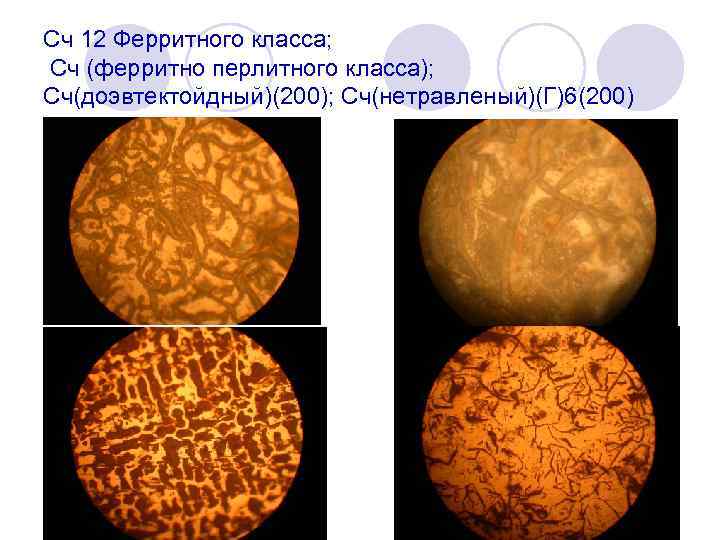 Сч 12 Ферритного класса; Сч (ферритно перлитного класса); Сч(доэвтектойдный)(200); Сч(нетравленый)(Г)6(200)
Сч 12 Ферритного класса; Сч (ферритно перлитного класса); Сч(доэвтектойдный)(200); Сч(нетравленый)(Г)6(200)
 Сталь сплав железа с углеродом, где содержание последнего может меняться от сотых долей процента до 2, 14 %. В стали также содержится незначительное количество примесей марганца, серы и фосфора. Различают сталь углеродистую и легированную. Углеродистая сталь имеет серовато серебристый оттенок, обладает мелкозернистой структурой на изломе, отличается прочностью, твердостью, пластичностью и достаточной вязкостью. Качественные углеродистые стали маркируют словом «сталь» и цифрами 08, 10, 15, 20, 85 (среднее содержание углерода в сотых долях %)
Сталь сплав железа с углеродом, где содержание последнего может меняться от сотых долей процента до 2, 14 %. В стали также содержится незначительное количество примесей марганца, серы и фосфора. Различают сталь углеродистую и легированную. Углеродистая сталь имеет серовато серебристый оттенок, обладает мелкозернистой структурой на изломе, отличается прочностью, твердостью, пластичностью и достаточной вязкостью. Качественные углеродистые стали маркируют словом «сталь» и цифрами 08, 10, 15, 20, 85 (среднее содержание углерода в сотых долях %)
 В зависимости от содержания углерода и примесей различают: Низкоуглеродистые стали(С 2, 5%) имеют высокую пластичность и невысокую прочность, используют для ответственных сварных конструкций. Спеднеуглеродистые (С=0. 3 0. 5 %) имеют высокую прочность, более низкую пластичность, применяют для поверхностной закалки разных деталей машин. Высокоуглеродистые качественные стали (С=0. 6 0. 8%), высокая прочность, износостойкость, упругость. Конструкционные и инструментальные углеродистые стали обыкновенного качества, качественные и высококачественные. В атмосферных условиях углеродистые стали подвержены коррозии, в результате чего на поверхности изделий может образовываться пленка ржавчины буро коричневого цвета. l
В зависимости от содержания углерода и примесей различают: Низкоуглеродистые стали(С 2, 5%) имеют высокую пластичность и невысокую прочность, используют для ответственных сварных конструкций. Спеднеуглеродистые (С=0. 3 0. 5 %) имеют высокую прочность, более низкую пластичность, применяют для поверхностной закалки разных деталей машин. Высокоуглеродистые качественные стали (С=0. 6 0. 8%), высокая прочность, износостойкость, упругость. Конструкционные и инструментальные углеродистые стали обыкновенного качества, качественные и высококачественные. В атмосферных условиях углеродистые стали подвержены коррозии, в результате чего на поверхности изделий может образовываться пленка ржавчины буро коричневого цвета. l
 l Легированные стали отличаются от углеродистых наличием в сплаве добавок хрома, никеля, вольфрама и т. д. Эти стали имеют серебристо белый с голубоватым оттенком цвет, характеризуются высокой стойкостью к коррозии, твердостью, прочностью, большим сопротивлением к износу и красивым внешним видом. Полированные изделия из легированных сталей долго сохраняют блеск.
l Легированные стали отличаются от углеродистых наличием в сплаве добавок хрома, никеля, вольфрама и т. д. Эти стали имеют серебристо белый с голубоватым оттенком цвет, характеризуются высокой стойкостью к коррозии, твердостью, прочностью, большим сопротивлением к износу и красивым внешним видом. Полированные изделия из легированных сталей долго сохраняют блеск.
 Цветные металлы и их сплавы находят широкое применение в машиностроении, электро и радиотехнике, приборостроении и других отраслях промышленности благодаря многим ценным физико химическим и механическим свойствам: большой электро и теплопроводности, антифрикционным свойствам, пластичности и т. п. l Цветные металлы применяются главным образом в виде сплавов, так как в чистом виде они обладают малой прочностью. Наибольшее распространение в промышленности получили сплавы на основе меди, алюминия, олова, магния и других металлов. l
Цветные металлы и их сплавы находят широкое применение в машиностроении, электро и радиотехнике, приборостроении и других отраслях промышленности благодаря многим ценным физико химическим и механическим свойствам: большой электро и теплопроводности, антифрикционным свойствам, пластичности и т. п. l Цветные металлы применяются главным образом в виде сплавов, так как в чистом виде они обладают малой прочностью. Наибольшее распространение в промышленности получили сплавы на основе меди, алюминия, олова, магния и других металлов. l
 Медь l l l Медь — металл красноватого цвета, кристаллизуется в решетку ГЦК. Плотность меди — 8, 94 г/см 3. Температура плавления — 1083°С. Медь обладает высокой пластичностью. Она прокатывается в тонкие листы, из неё получают тонкую проволоку. Медь обладает высокой теплопроводностью. Медь широко применяется в качестве проводникового материала На воздухе легко окисляется, поверхность покрывается пленкой темного с зеленоватым оттенком цвета. Низкое электрической сопротивление, высокая механическая прочность, хорошо сваривается. Из сплавов меди наиболее распространены бронза и латунью. По ГОСТ 859 78 в зависимости от содержания примесей различают следующие марки меди: М 00 (99, 99 % Си), МО (99, 97% Си), Ml(99, 9% Си), М 2(99, 7% Си), М 3(99, 5% Си).
Медь l l l Медь — металл красноватого цвета, кристаллизуется в решетку ГЦК. Плотность меди — 8, 94 г/см 3. Температура плавления — 1083°С. Медь обладает высокой пластичностью. Она прокатывается в тонкие листы, из неё получают тонкую проволоку. Медь обладает высокой теплопроводностью. Медь широко применяется в качестве проводникового материала На воздухе легко окисляется, поверхность покрывается пленкой темного с зеленоватым оттенком цвета. Низкое электрической сопротивление, высокая механическая прочность, хорошо сваривается. Из сплавов меди наиболее распространены бронза и латунью. По ГОСТ 859 78 в зависимости от содержания примесей различают следующие марки меди: М 00 (99, 99 % Си), МО (99, 97% Си), Ml(99, 9% Си), М 2(99, 7% Си), М 3(99, 5% Си).
 Алюминий — легкий, пластичный металл серебристо белого цвета, обладает небольшой плотностью (2, 7 г/см 3) и низкой температурой плавления (660 °С). Характерные свойства алюминия — высокая пластичность и низкая прочность. l Алюминий кристаллизуется в ГЦК решетку, обладает высокой коррозионной стойкостью, так как на поверхности образуется плотная пленка Аl 2 О 3. l Алюминий является вторым после меди проводниковым материалом. l l
Алюминий — легкий, пластичный металл серебристо белого цвета, обладает небольшой плотностью (2, 7 г/см 3) и низкой температурой плавления (660 °С). Характерные свойства алюминия — высокая пластичность и низкая прочность. l Алюминий кристаллизуется в ГЦК решетку, обладает высокой коррозионной стойкостью, так как на поверхности образуется плотная пленка Аl 2 О 3. l Алюминий является вторым после меди проводниковым материалом. l l
 Сплавы Al: Деформируемые (делятся на упрочняемые термической обработкой и неупрочняемые) Дюралюминий – светло белый цвет, изготавливают методом давления (штамповка, ковка). Литейные сплавы – сероватый оттенок (изделия изготавливают литьем) Сплавы, получаемые методом порошковой металлургии.
Сплавы Al: Деформируемые (делятся на упрочняемые термической обработкой и неупрочняемые) Дюралюминий – светло белый цвет, изготавливают методом давления (штамповка, ковка). Литейные сплавы – сероватый оттенок (изделия изготавливают литьем) Сплавы, получаемые методом порошковой металлургии.
 Латунь Сплав меди с цинком. В зависимости от содержания в сплаве цинка (от 4 до 47 %) его цвет изменяется от розовато красного до желто золотистого. Более прочная и пластичная чем медь. Имеет более низкую стоимость. В состав латуни могут входить Al, Ni, Mg для повышения коррозионной стойкости. Хорошо штампуется. Сплавы делят на: Деформируемые Литейные Л 59 – литейная латунь. ЛАН 59 3 2 – латунь с Al, Ni
Латунь Сплав меди с цинком. В зависимости от содержания в сплаве цинка (от 4 до 47 %) его цвет изменяется от розовато красного до желто золотистого. Более прочная и пластичная чем медь. Имеет более низкую стоимость. В состав латуни могут входить Al, Ni, Mg для повышения коррозионной стойкости. Хорошо штампуется. Сплавы делят на: Деформируемые Литейные Л 59 – литейная латунь. ЛАН 59 3 2 – латунь с Al, Ni
 Бронза сплав меди с оловом или другими металлами, например алюминием. Сплавы отличаются высокой твердостью, обладают хрупкостью. Бронзовые изделия вырабатывают только методом литья. l Выделяют оловянистые, свинцовистые, алюминиевые, кремнистые, бериллиевые бронзы. l По сравнению с медью у бронзы выше механическая прочность. l Маркировка: Бр Бр. А 5 Бр. АЖ 9 4 l Бронза
Бронза сплав меди с оловом или другими металлами, например алюминием. Сплавы отличаются высокой твердостью, обладают хрупкостью. Бронзовые изделия вырабатывают только методом литья. l Выделяют оловянистые, свинцовистые, алюминиевые, кремнистые, бериллиевые бронзы. l По сравнению с медью у бронзы выше механическая прочность. l Маркировка: Бр Бр. А 5 Бр. АЖ 9 4 l Бронза
 Мельхиор сплав меди с никелем. На изломе сплав с желтоватым оттенком, пластичен. Изделия вырабатывают методом давления и обязательно покрывают серебром и золотом. l Мельхиор
Мельхиор сплав меди с никелем. На изломе сплав с желтоватым оттенком, пластичен. Изделия вырабатывают методом давления и обязательно покрывают серебром и золотом. l Мельхиор
 Нейзильбер сплав меди, никеля и цинка. На изломе сплав имеет желтоватый оттенок. Он отличается пластичностью, стойкостью к коррозии, покрывают серебром и (или) золотом. l Нейзильбер
Нейзильбер сплав меди, никеля и цинка. На изломе сплав имеет желтоватый оттенок. Он отличается пластичностью, стойкостью к коррозии, покрывают серебром и (или) золотом. l Нейзильбер
 l Под действием влаги, химических веществ, неблагоприятных воздействий изделия из сплавов меняют цвет, внешний вид и свойства. l Это является следствием коррозии. l Коррозия может быть равномерная и межкристаллитная.
l Под действием влаги, химических веществ, неблагоприятных воздействий изделия из сплавов меняют цвет, внешний вид и свойства. l Это является следствием коррозии. l Коррозия может быть равномерная и межкристаллитная.
 ПОКРЫТИЯ НА МЕТАЛЛИЧЕСКИХ ИЗДЕЛИЯХ
ПОКРЫТИЯ НА МЕТАЛЛИЧЕСКИХ ИЗДЕЛИЯХ
 Защитные покрытия наносят для защиты металлических изделий от коррозии и улучшения их внешнего вида. К покрытиям предъявляются требования: 1. Прочное сцепление с металлом 2. Мелкая кристаллическая структура покрытия (для обеспечения лучших защитных свойств) 3. Равномерная толщина
Защитные покрытия наносят для защиты металлических изделий от коррозии и улучшения их внешнего вида. К покрытиям предъявляются требования: 1. Прочное сцепление с металлом 2. Мелкая кристаллическая структура покрытия (для обеспечения лучших защитных свойств) 3. Равномерная толщина
 При нанесении покрытия выполняются следующие условия: 1. Подготовка поверхности (шлифование, обработка органическими растворителями с целью обезжиривания; легкое травление – погружение изделия в раствор серной или соляной кислоты) 2. Нанесение покрытия 3. Промывка 4. Сушка
При нанесении покрытия выполняются следующие условия: 1. Подготовка поверхности (шлифование, обработка органическими растворителями с целью обезжиривания; легкое травление – погружение изделия в раствор серной или соляной кислоты) 2. Нанесение покрытия 3. Промывка 4. Сушка
 СПОСОБЫ НАНЕСЕНИЯ ПОКРЫТИЯ Гальванический – осаждение металла при электролизе водных растворов соответствующих солей. Химический – металлическое покрытие получают с помощью погружения в специальный раствор солей без электрического тока. Находящиеся в растворе ионы металлов осаждаются на деталь в виде металлической пленки. Химические меднение и никелирование, металлизация (толстые покрытия, детали либо погружаются целиком в расплав металла – горячая металлизация (в цинк, олово); горячее распыление – распыление металла из кристаллита распылителя. В качестве металлических покрытий применяются цинк, олово.
СПОСОБЫ НАНЕСЕНИЯ ПОКРЫТИЯ Гальванический – осаждение металла при электролизе водных растворов соответствующих солей. Химический – металлическое покрытие получают с помощью погружения в специальный раствор солей без электрического тока. Находящиеся в растворе ионы металлов осаждаются на деталь в виде металлической пленки. Химические меднение и никелирование, металлизация (толстые покрытия, детали либо погружаются целиком в расплав металла – горячая металлизация (в цинк, олово); горячее распыление – распыление металла из кристаллита распылителя. В качестве металлических покрытий применяются цинк, олово.
 Цинковые покрытия имеют серый цвет и характерный рисунок, напоминающий морозный узор на стекле. Наносят их чаще всего горячим способом. l Оловянное покрытие (лужение) получают также горячим способом. Оно имеет белый цвет, сильный блеск, высокую химическую устойчивость к органическим кислотам. l Никелевые и хромовые покрытия наносят гальваническим способом. Они белого цвета, с сильным металлическим блеском. Различают по оттенку: у никелевых покрытий оттенок желтоватый, а у хромовых голубоватый. l
Цинковые покрытия имеют серый цвет и характерный рисунок, напоминающий морозный узор на стекле. Наносят их чаще всего горячим способом. l Оловянное покрытие (лужение) получают также горячим способом. Оно имеет белый цвет, сильный блеск, высокую химическую устойчивость к органическим кислотам. l Никелевые и хромовые покрытия наносят гальваническим способом. Они белого цвета, с сильным металлическим блеском. Различают по оттенку: у никелевых покрытий оттенок желтоватый, а у хромовых голубоватый. l
 Неметаллические покрытия В качестве неметаллических покрытий применяют лаки и краски, силикатные эмали, оксидные пленки. Лакокрасочные покрытия наносят масляными или эмалевыми красками, они имеют различную цветовую гамму, используются в комбинации с разделками, например живопись красками. Силикатные эмали стекловидные покрытия, также обладающие широкой гаммой цветов, но отличающиеся от лакокрасочных покрытий высокой гладкостью, равномерностью нанесения покрытия, блеском, твердостью. Чаще их используют в комбинации с разделками, например трафаретом. Оксидные покрытия, создающие на поверхности изделия оксидные пленки металлов, применяют для защиты от коррозии алюминиевых (анодирование) и стальных (воронение) изделий. Анодированные алюминиевые изделия по сравнению с чистым алюминием имеют более гладкую поверхность, темновато серый оттенок. Их часто окрашивают в различные цвета золотистый, красный и т. д. Вороненая поверхность стальных изделий имеет черный цвет с синеватым оттенком.
Неметаллические покрытия В качестве неметаллических покрытий применяют лаки и краски, силикатные эмали, оксидные пленки. Лакокрасочные покрытия наносят масляными или эмалевыми красками, они имеют различную цветовую гамму, используются в комбинации с разделками, например живопись красками. Силикатные эмали стекловидные покрытия, также обладающие широкой гаммой цветов, но отличающиеся от лакокрасочных покрытий высокой гладкостью, равномерностью нанесения покрытия, блеском, твердостью. Чаще их используют в комбинации с разделками, например трафаретом. Оксидные покрытия, создающие на поверхности изделия оксидные пленки металлов, применяют для защиты от коррозии алюминиевых (анодирование) и стальных (воронение) изделий. Анодированные алюминиевые изделия по сравнению с чистым алюминием имеют более гладкую поверхность, темновато серый оттенок. Их часто окрашивают в различные цвета золотистый, красный и т. д. Вороненая поверхность стальных изделий имеет черный цвет с синеватым оттенком.


