 Металлы
Металлы
 Какой металл самый-самый? • • • Самый легкий металл – Li (ρ =0, 53 г/см 3). Самый тяжелый металл – Os (ρ=22, 5 г/см 3). Самый легкоплавкий металл – Hg (tпл = – 38, 87 °С). • Самый тугоплавкий металл – W (tпл = 3410 °С). • Самый мягкий металл – Cs. • Самый твердый металл – Cr.
Какой металл самый-самый? • • • Самый легкий металл – Li (ρ =0, 53 г/см 3). Самый тяжелый металл – Os (ρ=22, 5 г/см 3). Самый легкоплавкий металл – Hg (tпл = – 38, 87 °С). • Самый тугоплавкий металл – W (tпл = 3410 °С). • Самый мягкий металл – Cs. • Самый твердый металл – Cr.
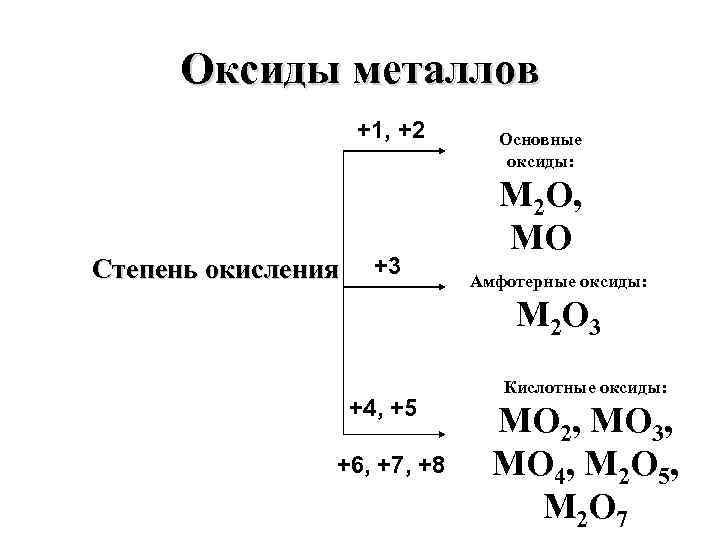 Оксиды металлов +1, +2 Степень окисления +3 Основные оксиды: M 2 O, MO Амфотерные оксиды: M 2 O 3 +4, +5 +6, +7, +8 Кислотные оксиды: MO 2, MO 3, MO 4, M 2 O 5, M 2 O 7
Оксиды металлов +1, +2 Степень окисления +3 Основные оксиды: M 2 O, MO Амфотерные оксиды: M 2 O 3 +4, +5 +6, +7, +8 Кислотные оксиды: MO 2, MO 3, MO 4, M 2 O 5, M 2 O 7
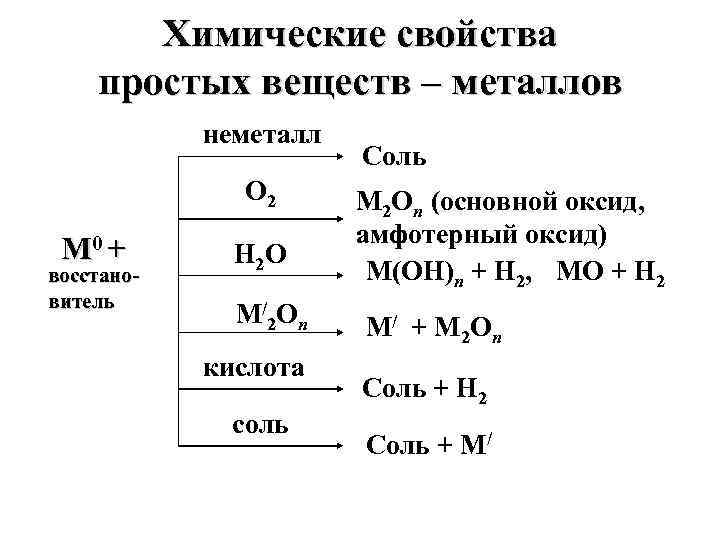 Химические свойства простых веществ – металлов неметалл O 2 M 0 + восстановитель H 2 O M / 2 O n кислота соль Cоль M 2 On (основной оксид, амфотерный оксид) M(OH)n + H 2, MO + H 2 M/ + M 2 On Cоль + H 2 Соль + M/
Химические свойства простых веществ – металлов неметалл O 2 M 0 + восстановитель H 2 O M / 2 O n кислота соль Cоль M 2 On (основной оксид, амфотерный оксид) M(OH)n + H 2, MO + H 2 M/ + M 2 On Cоль + H 2 Соль + M/
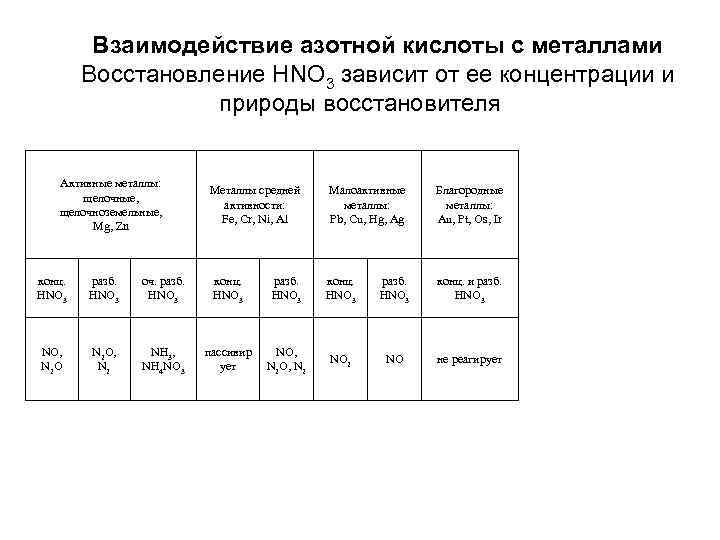 Взаимодействие азотной кислоты с металлами Восстановление НNО 3 зависит от ее концентрации и природы восстановителя Активные металлы: щелочные, щелочноземельные, Mg, Zn Металлы средней активности: Fe, Cr, Ni, Al Малоактивные металлы: Рb, Cu, Hg, Ag Благородные металлы: Аu, Pt, Os, Ir конц. НNО 3 разб. НNО 3 оч. разб. НNО 3 конц. НNО 3 разб. НNО 3 конц. и разб. НNО 3 NO, N 2 O, N 2 NH 3, NH 4 NO 3 пассивир ует NO, N 2 NO не реагирует
Взаимодействие азотной кислоты с металлами Восстановление НNО 3 зависит от ее концентрации и природы восстановителя Активные металлы: щелочные, щелочноземельные, Mg, Zn Металлы средней активности: Fe, Cr, Ni, Al Малоактивные металлы: Рb, Cu, Hg, Ag Благородные металлы: Аu, Pt, Os, Ir конц. НNО 3 разб. НNО 3 оч. разб. НNО 3 конц. НNО 3 разб. НNО 3 конц. и разб. НNО 3 NO, N 2 O, N 2 NH 3, NH 4 NO 3 пассивир ует NO, N 2 NO не реагирует
 Особенности взаимодействия концентрированной и разбавленной серной кислоты с металлами • Разбавленная серная кислота проявляет окислительные свойства за счет ионов водорода: 3 Н 2 SО 4(разб. ) + 2 Аl Аl 2(SО 4)3 + 3 Н 2; 6 Н+ + 2 Аl 3+ + 3 Н 2. • С металлами, расположенными в ряду стандартных электродных потенциалов металлов (ряду напряжений) после водорода, она не реагирует. • Концентрированная серная кислота является сильным окислителем за счет молекул Н 2 SО 4, в которых сера проявляет степень окисления +6. При этом в зависимости от силы восстановителя, концентрации кислоты и температуры могут образовываться разные продукты реакции: SО 2, S, Н 2 S: Zn + 2 Н 2 SО 4 Zn. SО 4 + SО 2 + 2 Н 2 О 3 Zn + 4 Н 2 SО 4 3 Zn. SО 4 + S + 4 Н 2 О 4 Zn + 5 Н 2 SО 4 4 Zn. SО 4 + Н 2 S + 4 Н 2 О концентрация кислоты уменьшается
Особенности взаимодействия концентрированной и разбавленной серной кислоты с металлами • Разбавленная серная кислота проявляет окислительные свойства за счет ионов водорода: 3 Н 2 SО 4(разб. ) + 2 Аl Аl 2(SО 4)3 + 3 Н 2; 6 Н+ + 2 Аl 3+ + 3 Н 2. • С металлами, расположенными в ряду стандартных электродных потенциалов металлов (ряду напряжений) после водорода, она не реагирует. • Концентрированная серная кислота является сильным окислителем за счет молекул Н 2 SО 4, в которых сера проявляет степень окисления +6. При этом в зависимости от силы восстановителя, концентрации кислоты и температуры могут образовываться разные продукты реакции: SО 2, S, Н 2 S: Zn + 2 Н 2 SО 4 Zn. SО 4 + SО 2 + 2 Н 2 О 3 Zn + 4 Н 2 SО 4 3 Zn. SО 4 + S + 4 Н 2 О 4 Zn + 5 Н 2 SО 4 4 Zn. SО 4 + Н 2 S + 4 Н 2 О концентрация кислоты уменьшается