Schyolochnozemelnye_metally_Mg_i_Be.pptx
- Количество слайдов: 51

МЕТАЛЛЫ II ГРУППЫ ЩЕЛОЧНОЗЕМЕЛЬНЫЕ МЕТАЛЛЫ, МАГНИЙ И БЕРИЛЛИЙ Щелочноземельными являются не все элементы IIА группы, а только начиная с кальция и вниз по группе. Оксиды этих элементов ( «земли» - по старинной терминологии) взаимодействуют с
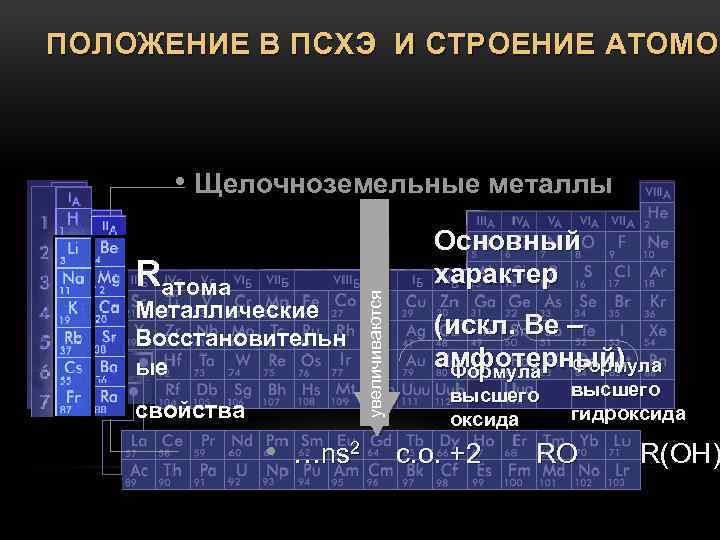
ПОЛОЖЕНИЕ В ПСХЭ И СТРОЕНИЕ АТОМОВ Rатома Металлические Восстановительн ые свойства увеличиваются • Щелочноземельные металлы Основный характер (искл. Ве – амфотерный) Формула высшего оксида высшего гидроксида • …ns 2 с. о. +2 RO R(OH)

ОБЩАЯ ХАРАКТЕРИСТИКА Be Mg Ca Sr Ba Ra Радиус атома и Заряд ядра ув-тся Максимальна я степень Металлические и окисления восстановительные +2 Щелочноземельные металлы св-ва ув-ся. Основные св-ва Оксидов и Гидроксидов ув-ся. Металлы химически активные, в природе встречаются только в виде соединений 2 Взаимодействуют с водой образуя щелочи. n S

II A Щелочноземельные металлы (Ca – Ra)

ФИЗИЧЕСКИЕ СВОЙСТВА МАГНИЯ, БЕРИЛЛИЯ И ЩЕЛОЧНО-ЗЕМЕЛЬНЫЕ МЕТАЛЛОВ • серебристо-белые вещества. • ковкие и пластичные, довольно мягкие, хотя тверже щелочных. Бериллий отличается значительной твердостью и ножом преимущественно не режутся (исключение — стронций). и хрупкостью, барий при резком ударе раскалывается. • Металлическая кристаллическая решетка обуславливает их высокую тепло- и электропроводность. • Металлы имеют температуры плавления и кипения выше, чем у щелочных металлов. • Бериллий и магний покрыты прочной оксидной пленкой и не изменяются на воздухе. • Щелочно-земельные металлы очень активны, их хранят в запаянных ампулах, под слоем вазелинового масла или
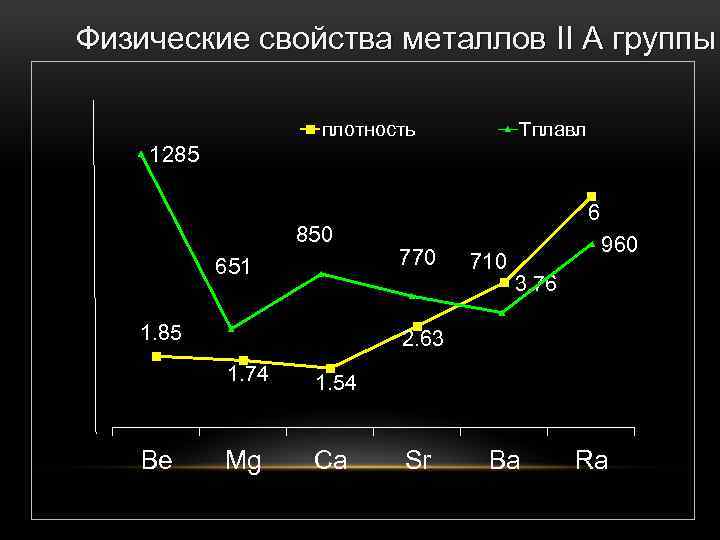
Физические свойства металлов II А группы плотность Тплавл 1285 850 651 1. 85 770 710 960 3. 76 2. 63 1. 74 Be 6 1. 54 Mg Ca Sr Ba Ra

й и Мягки ый ичн пласт Mg При комн а темп тной ерату покры ре тонча т йш оксид ей н плён ой кой Те м пл пе ав ра 65 ле тур 0 ни а С я ФИЗИЧЕСКИЕ СВОЙСТВА
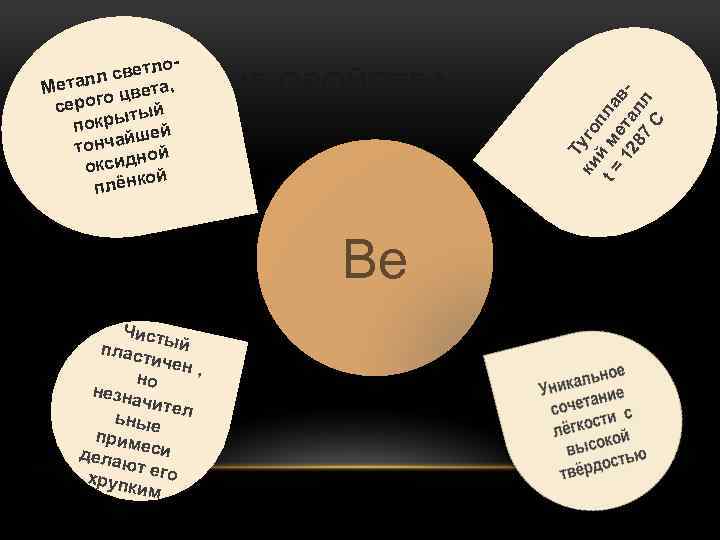
ФИЗИЧЕСКИЕ СВОЙСТВА Be Чист плас ый тичен , но незна чител ьные прим дела еси ют хрупк его им Т ки уго й п t = м ла 1 ета в 28 л 7 л C тлол све , Метал цвета о серог тый покры ей йш тонча ой н оксид й о плёнк

Лёгкий, беловатосерый, Пластичный металл Ca Температура плавления С Из –за достаточной твёрдости невозможно резать ножом, как щелочные металлы

ПОЛУЧЕНИЕ 1. Барий получают восстановлением оксида: 3 Ba. O + 2 Al = 3 Ba + Al 2 O 3 2. Остальные металлы получают электролизом расплавов хлоридов: Ca. Cl 2 = Ca + Cl 2 (эл. ток)

ХИМИЧЕСКИЕ СВОЙСТВА - ВОССТАНОВИТЕЛИ 1. С неметаллами образуют бинарные соединения • Реакция с кислородом. Все металлы образуют оксиды RO, барий может-пероксид – Ba. O 2: • Ba + O 2 = Ba. O 2 пероксид • Ca + O 2 = Ca. O • Ba + S = Ba. S сульфид • Ca + H 2 = Ca. H 2 гидрид • Ca + 2 C = Ca. C 2 карбид • 3 Ba + 2 P = Ba 3 P 2 фосфид • Ca + N 2 = Ca 3 N 2 нитрид • Ca + Cl 2 = Ca. Cl 2 хлорид

• 2. Реакция с водой. Образуют щелочи. В обычных условиях поверхность Be и Mg покрыты инертной оксидной пленкой, поэтому они устойчивы по отношению к воде. • Ca + 2 H 2 O = Ca(OH)2 + H 2 ( при о. у. ) • Mg + H 2 O = Mg(OH)2 + H 2 (при t )

• 3. Все металлы растворяются в кислотах: • Ca + 2 HCl = Ca. Cl 2 + H 2 • 4. С особыми кислотами (Be похож на Al) • Сa + HNO 3(к) = N 2 O + Ca(NO 3)2 + H 2 O • Ca + HNO 3(р) = NH 4 NO 3 + Ca(NO 3)2 + H 2 O (N 2 O, NH 3) • Ca + H 2 SO 4(к) = H 2 S + Ca. SO 4 + H 2 O • Be с азотной кислотой пассивирует, реакция на холоду не идет в независимости от концентрации кислоты

• 5. Сa, Mg с оксидами тяжелых металлов • Восстанавливают металлы из их оксидов - пирометаллургия (кальцетермия, магнетермия) • Ca + Cu. O = Cu + Ca. O ( t ) • 2 Mg + Ti. O 2 → 2 Mg. O + Ti • 5 Ca + V 2 O 5 → 5 Ca. O + 2 V • 2 Mg + CO 2 → 2 Mg. O + C горение Mg в углекислом газе

6. Качественная реакция на катионы щелочноземельных металлов – окрашивание пламени в следующие цвета: • Ca 2+ - темно-оранжевый • Sr 2+- темно-красный • Ba 2+ - светло-зеленый
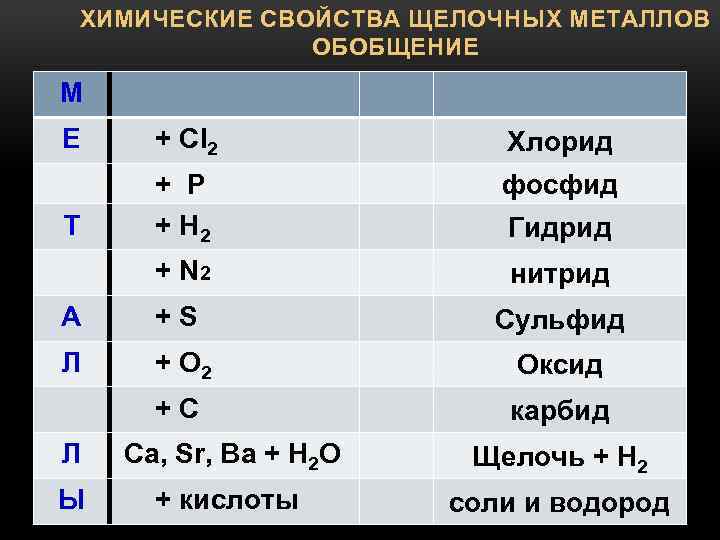
ХИМИЧЕСКИЕ СВОЙСТВА ЩЕЛОЧНЫХ МЕТАЛЛОВ ОБОБЩЕНИЕ М Е + Cl 2 Хлорид фосфид Т + P + H 2 + N 2 нитрид А + S Сульфид Л + O 2 Оксид + C карбид Л Ca, Sr, Ba + Н 2 О Ы + кислоты Гидрид Щелочь + Н 2 соли и водород

ВЗАИМОДЕЙСТВИЕ С ВОДОЙ Закончите уравнения реакций, назовите продукты реакций и составте о-в реакции. Ca + H 2 O Sr + H 2 O Ba + Н 2 О

ОКСИДЫ МЕТАЛЛОВ II ГРУППЫ общая формула оксидов - Me. O и пероксидов - Me. O 2 Оксиды металлов IIA группы являются основными оксидами, Ве. О проявляет амфотерные свойства.
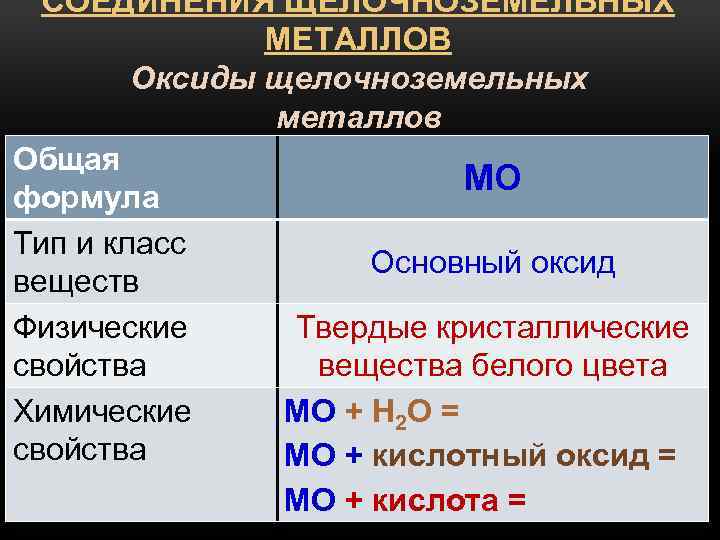
СОЕДИНЕНИЯ ЩЕЛОЧНОЗЕМЕЛЬНЫХ МЕТАЛЛОВ Оксиды щелочноземельных металлов Общая МО формула Тип и класс Основный оксид веществ Физические Твердые кристаллические свойства вещества белого цвета Химические МО + Н 2 О = свойства МО + кислотный оксид = МО + кислота =

ПОЛУЧЕНИЕ Окисление металлов (кроме Ba, который образует пероксид) • Ca + O 2 = Ca. O Термическое разложение нитрата магния или нерастворимых карбонатов • Ca. CO 3 → Ca. O + CO 2 t˚C 2 Mg(NO 3)2 → 2 Mg. O + 4 NO 2 + O 2 t˚C

ХИМИЧЕСКИЕ СВОЙСТВА • 1. С кислотным оксидом • 3 Ca. O + P 2 O 5 = Ca 3(PO 4)2 • 2. С водой • Ca. O + H 2 O = Ca(OH)2 (кроме Ве. О) • 3. С кислотой • Ca. O + HCl = Ca. Cl 2 + H 2 O • 4. С амфотерным оксидом • Ca. O + Zn. O = Ca. Zn. O 2

ОСОБЫЕ СВОЙСТВА ОКСИДОВ • 2 Ba. O + O 2 = 2 Ba. O 2 пероксид, только для бария • Ве. О проявляет амфотерные св-ва взаимодействует со щелочами: Be. O + 2 Na. OH = Na 2 Be. O 2 + H 2 O сплав Be. O + 2 Na. OH + H 2 O = Na 2[Be(OH)4] раствор Be. O + Na 2 CO 3 = Na 2 Be. O 2 + CO 2 сплав
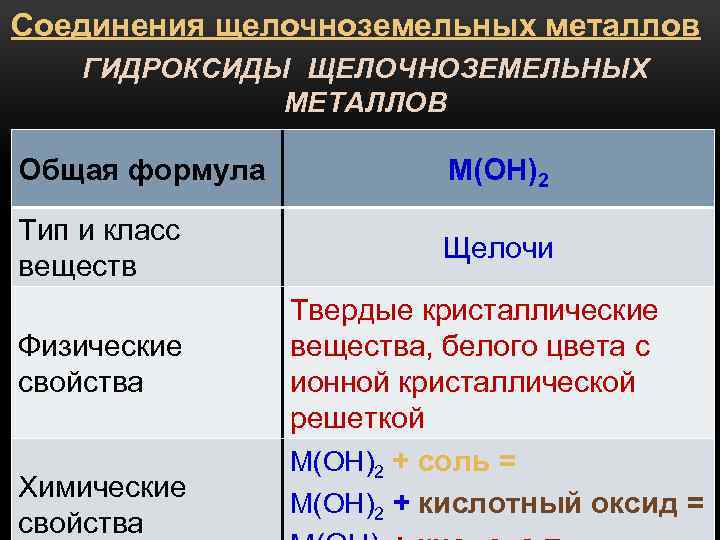
Соединения щелочноземельных металлов ГИДРОКСИДЫ ЩЕЛОЧНОЗЕМЕЛЬНЫХ МЕТАЛЛОВ Общая формула М(ОН)2 Тип и класс веществ Щелочи Физические свойства Химические свойства Твердые кристаллические вещества, белого цвета с ионной кристаллической решеткой М(ОН)2 + соль = М(ОН)2 + кислотный оксид =

ГИДРОКСИДЫ ЩЕЛОЧНОЗЕМЕЛЬНЫХ МЕТАЛЛОВ - ЩЕЛОЧИ • . • Гидроксиды R(OH)2 - белые кристаллические вещества, в воде растворимы хуже, чем гидроксиды щелочных металлов (растворимость гидроксидов уменьшается с уменьшением порядкового номера; Be(OH)2 – нерастворим в воде, растворяется в щелочах). Основность R(OH)2 увеличивается с увеличением атомного номера: Be(OH)2 – амфотерный гидроксид • Mg(OH)2 – слабое основание • Са(OH)2 - щелочь • остальные гидроксиды - сильные основания (щелочи).

ПОЛУЧЕНИЕ ГИДРОКСИДОВ 1. Реакции щелочноземельных металлов или их оксидов с водой: • Ba + 2 H 2 O Ba(OH)2 + H 2 • Ca. O + H 2 O Ca(OH)2 2. Электролиз растворов солей • Ca. Cl 2 + H 2 O Ca(OH)2 + Cl 2 + H 2 эл. ток 3. Be(OH)2 и Mg(OH)2 получают с помощью обменных реакций • Be. Cl 2 + 2 Na. OH = 2 Na. Cl + Be(OH)2

ХИМИЧЕСКИЕ СВОЙСТВА • 1. изменяют цвет индикатора • Лакмус – синий • Метилоранж – желтый • Фенолфталеин - малиновый • Гидроксиды щелочноземельных металлов в воде диссоциируют на

ХИМИЧЕСКИЕ СВОЙСТВА 2. Реакции с кислотными оксидами: • Ca(OH)2 + SO 2 Ca. SO 3 + H 2 O • Ba(OH)2 + CO 2 Ba. CO 3 + H 2 O • Ca(OH)2 +2 CO 2 CA(HCO 3)2 • Ca(OH)2 + CO 2 = Ca. CO 3 + H 2 O Качественная реакция на углекислый газ 3. Реакции с кислотами (нейтрализация) • Ba(OH)2 + 2 HNO 3 Ba(NO 3)2 + 2 H 2 O 4. Реакции обмена с солями: • Ba(OH)2 + K 2 SO 4 Ba. SO 4+ 2 KOH
![ХИМИЧЕСКИЕ СВОЙСТВА 5. C амфотерными металлами, оксидами, гидроксидами • Ca(OH)2 + Bе(OH)2 Ca[Be(OH)4] ( ХИМИЧЕСКИЕ СВОЙСТВА 5. C амфотерными металлами, оксидами, гидроксидами • Ca(OH)2 + Bе(OH)2 Ca[Be(OH)4] (](https://present5.com/presentation/2134497_172028174/image-28.jpg)
ХИМИЧЕСКИЕ СВОЙСТВА 5. C амфотерными металлами, оксидами, гидроксидами • Ca(OH)2 + Bе(OH)2 Ca[Be(OH)4] ( раствор) • Ca(OH)2 + Be(OH)2 Ca. Be. O 2 + H 2 O (сплав) • Ca(OH)2 + Be. O + H 2 O Ca[Be(OH)4] (раствор) • Ca(OH)2 + Be. O Ca. Be. O 2 + H 2 O (сплав) • Ca(OH)2 + Be Ca[Be(OH)4] + H 2 тетрагидроксобериллиат кальция

ТРИВИАЛЬНЫЕ НАЗВАНИЯ ВЕЩЕСТВ • Сa. O – негашеная известь • Ca(OH)2 –гашенная известь (известковая вода, молоко) • Ca. CO 3 – мел, мрамор, известняк • Ca. SO 4 * 2 H 2 O -- гипс • Ca(Cl. O)Cl – хлорная известь

СОЛИ ЩЕЛОЧНОЗЕМЕЛЬНЫХ МЕТАЛЛОВ • Растворимые соли Be и Ba – токсичны, ядовиты! • Катион Ba 2+ обычно открывают обменной реакцией с серной кислотой или ее солями: • Сульфат бария – белый осадок, нерастворимый в минеральных кислотами

КАЛЬЦИЙ В ПРИРОДЕ Кальциевые горные породы – известняк, мрамор, мел. • Вспомните формулу этих горных пород. • В чем их отличие?

МЕЛ, ИЗВЕСТНЯК, МРАМОР НЕ РАСТВОРЯЮТСЯ В ЧИСТОЙ ВОДЕ, НО РАСТВОРИМЫ В КИСЛЫХ РАСТВОРАХ, ДАЖЕ ТАКИХ СЛАБЫХ, КАК ПРИРОДНАЯ ВОДА. При просачивании воды с поверхности земли через залежи известняка происходят процессы: 1. образуются провалы, если порода залегает под тонким слоем почвы

2. Если породы залегают на большой глубине – возникают подземные карстовые пещеры. • Как называются отложения, свисающие в виде гигантских сосулек со свода пещеры? А растущие навстречу им со дна пещеры колонны? Какие химические реакции при этом происходят?

ИЗВЕСТНЯК И МРАМОР ИСПОЛЬЗУЮТ В АРХИТЕКТУРЕ И СКУЛЬПТУРЕ При воздействии кислотных дождей строения разрушаются. • Какие реакции при этом происходят?

КАЛЬЦИЙ В ОРГАНИЗМЕ ЧЕЛОВЕКА • • Минерал, содержащий фосфат кальция, играет важную роль в человеческом организме. Он строительным материалом костей человека, входит в состав эмали. • В сочетании с другими минералами поддерживает работу сердечно-сосудистой системы, предотвращает возникновение рака толстой кишки, регулирует функции нервов, способствует снижению холестерина. • В организме взрослого человека содержатся более 1 кг кальция в виде соединения Ca 3(PO 4)2.
• Ca. SO 4 -сульфат кальция, встречается в природе в виде минерала гипса Ca. SO 4*2 H 2 O, представляющего собой кристаллогидрат. • Используется в строительстве, медицине для наложения неподвижных гипсовых повязок, для получения слепков. Для этого применяют полуводный гипс 2 Ca. SO 4 -алебастр.

ПРОИСХОЖДЕНИЕ ЖЕМЧУГА • Жемчуг - продукт жизнедеятельности жемчугоносных моллюсков. • Жемчуг образуется в раковине моллюска, причем для зарождения этого камешка, моллюску обязательно должна быть причинена боль или неудобство. • В раковину внедряется чужеродное тело - песчинка, кусочек раковины или живой паразит. • Сопротивляясь вторжению, моллюск выделяет особое вещество - перламутр. Слой за слоем перламутр обволакивает "оккупанта". • Перламутровая защита постепенно становится все больше, и через

БЕРИЛЛИЙ Бериллий сходствует с алюминием и магнием…Получил своё название потому, что находится в минерале берилле. Металл называют также глицием от греческого слова «сладкий» , потому что соли его имеют сладковатый вкус. Д. И. Менделеев

СОЕДИНЕНИЯ БЕРИЛЛИЯ В ПРИРОДЕ • Хризоберилл Be. Al 2 O 4 • Изумруд • Аквамарин • Александрит

«Изумруд капризный, как женщина встречается совсем не там, где его ищут» Благодаря насыщенному зелёному цвету и твёрдости очень популярен у ювелиров, чудесная окраска вызвана наличием ионов хрома или ванадия. «Кажется, что если вглядеться в аквамарин, то увидишь тихое море с водой цвета звёзд» К. Г. Паустовский Такой цвет ему придаёт небольшая примесь двухвалентного железа

МАГНИЙ В ПРИРОДЕ • Магний входит в состав активного центра зелёного пигмента растений -хлорофилла • Автомобильная , авиационная и ракетная промышленность Магналий -твёрдый и прочный сплав с алюминием - 30 % Mg с добавками цинка,

МАГНИЙ В МЕДИЦИНЕ • В медицине карбонат магния и окись магния применяют • в качестве средств нейтрализующих соляную кислоту желудка и как легкие слабительные (Гастал, Ренни, Алмагель). • Сульфат магния ( «английская соль» ) применяется в качестве слабительного, желчегонного и болеутоляющего средства при спазмах желчного пузыря. • Раствор сернокислой магнезии вводят в качестве противосудорожного средства при эпилепсии и в качестве антиспастического лекарства при задержке мочеиспускания, бронхиальной астме, гипертонической болезни. • органические соли магния используют при изготовлении БАД и лекарственных препаратов с широким спектром лечебно-профилактического действия, таких как

ЖЕСТКОСТЬ ВОДЫ • Жёсткость воды — совокупность химических и физических свойств воды, связанных с содержанием в ней растворённых солей щёлочноземельных металлов, главным образом, кальция и магния (так называемых «солей жёсткости» ). • Потребление жёсткой или мягкой воды обычно не является опасным для здоровья, есть данные о том, что высокая жёсткость способствует образованию мочевых камней, а низкая — незначительно увеличивает риск сердечно-сосудистых заболеваний. Вкус природной

ЖЕСТКОСТЬ ВОДЫ • Жёсткая вода при умывании сушит кожу, в ней плохо образуется пена при использовании мыла. Использование жёсткой воды вызывает появление осадка (накипи) на стенках котлов, в трубах и т. п. В то же время, использование слишком мягкой воды может приводить к коррозии труб. • Жёсткость природных вод может варьироваться в довольно широких пределах и в течение года непостоянна. Увеличивается жёсткость из-за испарения воды, уменьшается в сезон дождей, а также в период таяния снега и льда.
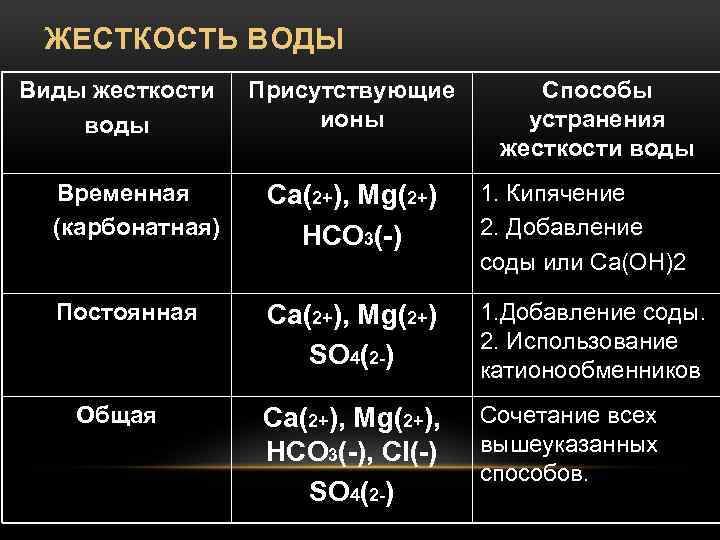
ЖЕСТКОСТЬ ВОДЫ Виды жесткости воды Присутствующие ионы Способы устранения жесткости воды Временная (карбонатная) Ca(2+), Mg(2+) HCO 3(-) 1. Кипячение 2. Добавление соды или Са(ОН)2 Постоянная Ca(2+), Mg(2+) SO 4(2 -) 1. Добавление соды. 2. Использование катионообменников Общая Ca(2+), Mg(2+), HCO 3(-), Cl(-) SO 4(2 -) Сочетание всех вышеуказанных способов.
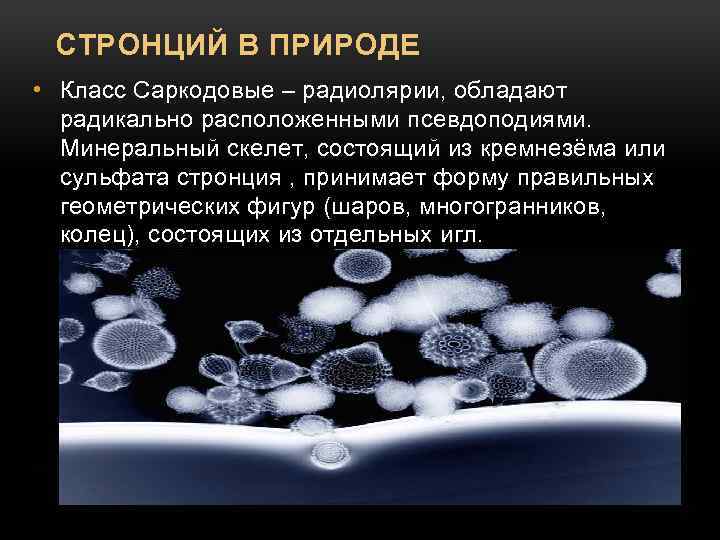
СТРОНЦИЙ В ПРИРОДЕ • Класс Саркодовые – радиолярии, обладают радикально расположенными псевдоподиями. Минеральный скелет, состоящий из кремнезёма или сульфата стронция , принимает форму правильных геометрических фигур (шаров, многогранников, колец), состоящих из отдельных игл.

ПРИМЕНЕНИЕ СОЛЕЙ СТРОНЦИЯ • Как коллекционный минерал целестин ценится высоко, но практически не используется в ювелирном деле из-за своей низкой твердости и высокой хрупкости. Характерны образцы целестина голубого, светло-голубого, серо-голубого и чуть голубоватого цветов; целестин может быть и бесцветным, а также белым, желтоватым, синеватозеленым, красноватым, коричневым, порой еле просвечивающим, иногда – с зональной окраской.

ПРИМЕНЕНИЕ СОЛЕЙ СТРОНЦИЯ • Соединения стронция использовались в пиротехнике; стоит бросить щепотку соли стронция в пламя – и оно окрасится в красный цвет. Все красные фейерверки и огни сигнальных ракет – все это благодаря стронцию. • Соединения стронция используются в стекольной, керамической промышленности для получения глазированных поверхностей,

ТАЙНЫ ЦЕЛЕСТИНА • Герр Хайнеман был доволен своей жизнью. Дела его шли хорошо, даже очень хорошо, если сравнить со многими другими эмигрантами, переехавшими в Соединенные Штаты. Его винный заводик на красивом озерном острове процветал, и вот, понадобилось сделать небольшой колодец для нужд производства. Со вчерашнего дня этим занимались его помощники, долбили породу. А сегодня один из них прибежал, мол, лучше ему взглянуть самому. Эх, все приходится делать самому. Герр Хайнеман спустился в подвал, где шли работы. • - Ну, что тут у вас? • - Вот, смотрите, мистер, долбили камень да наткнулись на пустоту… • - Дайте фонарь. • Герр Хайнеман спустился в яму в породе – результат работы целого дня. На дне ее и вправду зияла дыра. Он наклонился и посветил фонарем внутрь. И не поверил своим глазам: свет фонаря выхватил стенки обширной пещеры, покрытые огромными голубовато-белыми кристаллами. Герр Хайнеман уже было решил, что это подземная сокровищница троллей из сказок его родины, но ведь в США нет немецких троллей. Герр Хайнеман захихикал, поражаясь своей логике.
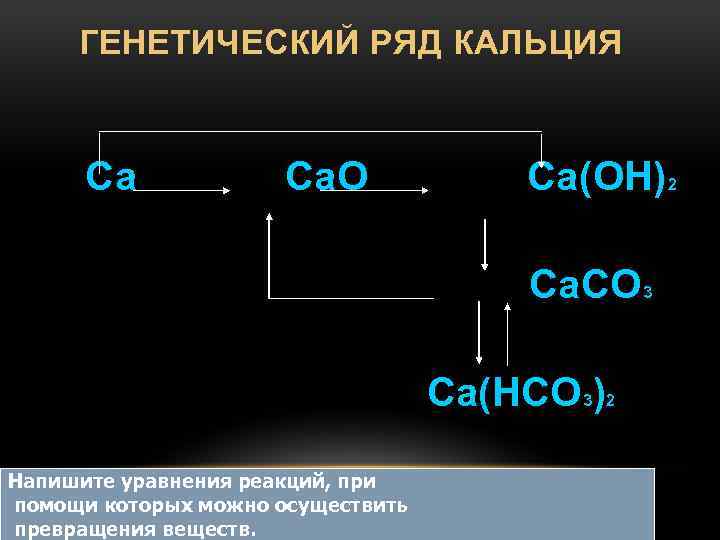
ГЕНЕТИЧЕСКИЙ РЯД КАЛЬЦИЯ Са. О Са(ОН) 2 Са. СО 3 Са(НСО 3)2 Напишите уравнения реакций, при помощи которых можно осуществить превращения веществ.

ЦЕПОЧКА ПРЕВРАЩЕНИЙ • Ca → Ca. O→ Ca. Cl 2→ Ca(OH)2 →Ca. CO 3 →Ca. O • Для реакций составить ионные уравнения и ок-восстановительные балансы.
Schyolochnozemelnye_metally_Mg_i_Be.pptx