138.ppt
- Количество слайдов: 32

Металлы IБ-подгруппы

Металлы IБ-подгруппы Основные вопросы, рассматриваемые в лекции þ Общая характеристика металлов IБ-подгруппы. Электронное строение, наиболее характерные степени окисления. þ Природные соединения þ Cu þ Свойства металлической меди þ Соединения Cu § Соединения Cu(+2) § Соединения Cu(+1) þ Ag и Au. þ Свойства металлов. þ Соединения серебра и золота. þ Комплексные соединения
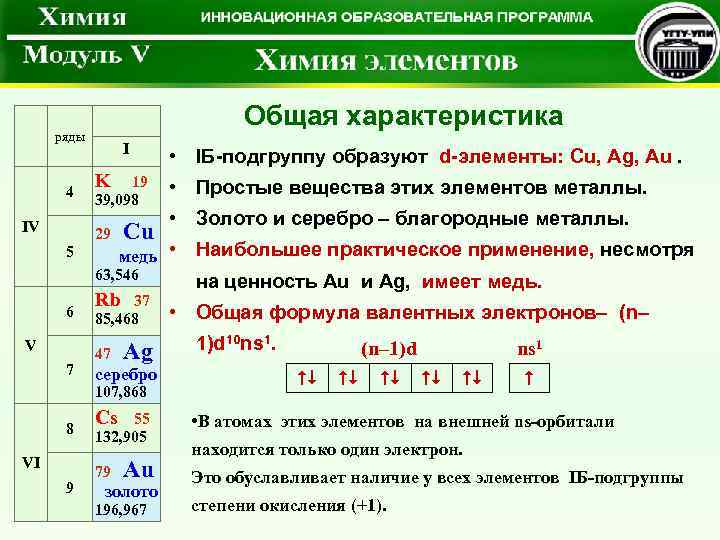
Общая характеристика ряды 4 IV 5 I K 19 39, 098 29 Cu • IБ-подгруппу образуют d-элементы: Cu, Ag, Au. • Простые вещества этих элементов металлы. • Золото и серебро – благородные металлы. медь • 63, 546 6 V 7 Rb 37 85, 468 47 Ag 8 VI 9 на ценность Au и Ag, имеет медь. • Общая формула валентных электронов– (n– серебро 107, 868 Cs 55 132, 905 79 Au золото 196, 967 Наибольшее практическое применение, несмотря 1)d 10 ns 1. (n– 1)d ns 1 • В атомах этих элементов на внешней ns-орбитали находится только один электрон. Это обуславливает наличие у всех элементов IБ-подгруппы степени окисления (+1).

Общая характеристика ряды 4 IV 5 I K 19 39, 098 V 7 медь • Rb 37 85, 468 47 VI серебро 9 Cs 55 132, 905 79 ns 1 Только у Ag степень окисления (+1) является устойчивой. Ag • У Cu степень окисления (+1) устойчива 107, 868 8 Cu 29 63, 546 6 (n– 1)d Au золото 196, 967 только при высоких температурах, а в обычных условиях устойчива +2. • У Au более устойчивая степень окисления +3.

Природные соединения • Содержание меди в земной коре невелико ~ 0, 01 масс. %, содержание Ag значительно меньше – 10– 5, а у Au – еще меньше – 5. 10– 7. • Все металлы в природе встречаются в самородном виде, но общее количество самородных металлов не велико. • В природе более распространены соединения меди с серой – минералы: халькопирит Cu. Fe. S 2, ковеллин Cu. S, халькозин Cu 2 S Около 80% меди получают из сульфидных руд, главным образом, из халькопирита Cu. Fe. S 2. Халькопирит Cu. Fe. S 2

Природные соединения Cu Реже чем сульфиды в природе встречаются: основные карбонаты: малахит Cu 2(CO 3)(OH)2 и азурит Cu 3(CO 3)2(OH)2; оксиды: куприт Cu 2 O и тенорит Cu. O; Малахит основные фосфаты – бирюза Cu. Al(PO 4)4(OH)8. 5 H 2 O;

Cu 29 медь Медь 3 d 3 d 104 s 1 63, 546 4 s 1 • Валентные электроны Cu – 3 d 104 s 1. • Медь в своих наиболее распространенных соединениях проявляет степени окисления: (+1) и (+2). • Степень окисления (+2) более устойчива в водных растворах. • Соединения меди (+1) более устойчивы при температуре выше 1000 о. С. Соединения меди (+2) в этих условиях разлагаются. • В природе встречаются как соединения меди в степени окисления (+1), так и в степени окисления (+2).

• Простое вещество Cu __ металл характерного красно-розового цвета. Cu • Температура плавления 1083 о. С, плотность – 8, 9 г/см 3. • Медь обладает высокой теплопроводностью и электропроводностью, уступая только серебру. • Медь – мягкий пластичный металл, легко вытягивается в проволоку и прокатывается в тонкие листы. • Сплавы меди отличаются большей твердостью, чем чистая медь. Самыми известными из медных сплавов являются: латунь (сплав Cu и Zn), бронза (сплав Cu и Sn), мельхиор (сплав Cu и Ni) и нейзильбер (Cu, Ni, Zn).

• Cu • Медь Простое вещество окисляется кислородом. При нагревании меди до 4000 С на воздухе образуется черный оксид Cu. O, а при более высокой температуре – Cu 2 O. Медь, находящаяся длительное время во влажном воздухе, покрывается пленкой основной соли (Cu. OH)2 CO 3. 2 Cu +O 2 + H 2 O +CO 2 = (Cu. OH)2 CO 3 • При нагревании медь взаимодействует с серой с образованием Cu 2 S, а также с галогенами с образованием галогенидов меди (+2). Фторид Cu. F 2 образуется на поверхности в виде очень плотной пленки, которая делает медь устойчивой к действию фтора.

Простое вещество • Электродный потенциал Ео (Cu 2+/Cu) = + 0, 34 В. • Ионы Н+ не могут окислить медь. Только при взаимодействии меди с кислотой HI выделяется Н 2 и образуется очень устойчивый комплекс H[Cu. I 2], в котором Cu имеет степень окисления (+1). • Медь растворяется в азотной и в концентрированной серной кислоте с образованием катионов Cu 2+. Cu + 2 H 2 SO 4 (конц. ) = Cu. SO 4 + SO 2 + 2 H 2 O Cu + 4 HNO 3 (конц. ) = Cu(NO 3)2 + 2 NO 2 + 2 H 2 O

Соединения меди (+2) • В водных растворах более устойчивы соединения Cu (+2). • Самое распространенное соединение Cu(+2) – Cu. SO 4. 5 H 2 O. • Ярко-голубые кристаллы Cu. SO 4. 5 H 2 O известны как медный купорос. Медный купорос ядовит. • Он хорошо растворяется в воде с образованием голубых растворов. В голубой цвет окрашены аквакомплексы [Cu(H 2 O)4]2+. Наиболее известное соединение Cu – медный купорос Cu. SO 4. 5 H 2 O

Соединения меди (+2) • Аквакатионы меди являются донорами протонов, и создают в водном растворе кислую среду. [Cu(H 2 O)4]2+ + H 2 O [Cu(OH)(H 2 O)3]+ + H 3 O+, или упрощенно, Cu 2+ + H 2 O Cu. OH+ + H+;

Соединения меди (+2) • Карбонаты и основные карбонаты, не растворяются в воде, но растворяются в кислотах. (Cu. OH)2 CO 3 + 4 H+ = 2 Cu 2+ + CO 2 + 3 H 2 O • Черный сульфид Cu. S выпадает при взаимодействии ионов Cu 2+ не только c растворимыми сульфидами, но и со слабой кислотой H 2 S. Cu 2+ + H 2 S = Cu. S +2 H+ • Кроме сульфидов и карбонатов, в воде не растворяются фосфаты, силикаты. Мало растворим фторид Cu. F 2.

Соединения меди (+2) • Гидроксид Cu(OH)2 образуется при добавлении щелочи к растворам солей Cu(+2) в форме студенистого голубого осадка. • При слабом нагревании гидроксид разлагается и переходит в черный оксид Cu. O. Cu(OH)2 Cu. O + H 2 O • Гидроксид и оксид Cu(+2) легко растворяются в кислотах. Cu(OH)2 +2 H+ = Cu 2+ +H 2 O Cu. O +2 H+ = Cu 2+ +H 2 O

Соединения меди (+2) • При взаимодействии концентрированной щелочи с очень разбавленными растворами Cu 2+ образуются темно-синие гидроксокомплексы [Cu(OH)4]2–. • При сплавлении Cu. O с щелочью образуются купраты Na 2 Cu. O 2. • Гидроксокомплексы и купраты разрушаются водой с образованием осадка Cu(OH)2. [Cu(OH)4]2– Cu(OH)2 + 2 OH– ; Cu. O 22– + 2 H 2 O Cu(OH)2 + 2 OH– • Таким образом, оксид и гидроксид Cu (+2) имеют преимущественно основной характер.

Соединения меди (+2) • Гидроксид и оксид Cu(+2) при взаимодействии с раствором аммиака, образуя синие амминные комплексы Cu(NH 3)4]2+. Cu(OH)2 + 4 NH 3 = [Cu(NH 3)4]2+ +2 OH • Катионы Cu 2+ образуют комплексные соединения, как правило, с координационным числом 4. • Примеры комплексных соединений Cu(+2): • голубые аквакомплексы [Cu(H 2 O)4]2+, • синие амминнокоплексы [Cu(NH 3)4]2+, • зеленые хлорокомплексы [Cu. Cl 4]2─.

Соединения меди (+2) • Катион Cu 2+, проявляет окислительные свойства. • Катионы Cu 2+ под действием металлов, более активных, чем медь, могут быть восстановлены до металлической меди. Cu 2+ + Fe = Cu + Fe 2+ • Эту реакцию используют для удаления Cu 2+ из технологических растворов. • Продуктами восстановления соединений Cu(+2) может быть не только металлическая медь, но и соединения Cu(+1).

Соединения меди (+1) • Соединения Cu (+1) можно получить при окислении металлической меди, если в растворе имеются вещества, образующие с Cu (+1) прочные комплексные соединения. 2 Cu + 2 H 2 O + 4 KCN = 2 K[Cu(CN)2] + 2 KOH + H 2 • Чаще всего соединения Cu (+1) получают, восстанавливая соли Cu (+2). • При добавлении к раствору Cu. SO 4 иодида калия выпадает белый осадок –иодид Cu. I. 2 Cu. SO 4+4 KI= 2 Cu. I+ I 2+ 2 K 2 SO 4

Соединения меди (+1) • Оксид Cu 2 O __ это основной оксид, его можно растворить в кислоте. • При растворении в кислоте Cu 2 O диспропорционирует на Cu 2+ и Сuо. • Cu 2 O также растворяется в водном растворе аммиака. При растворении Cu 2 O в аммиаке образуется бесцветный комплексный катион [Cu(NH 3)2]+. Cu 2 O + 4 NH 3 + H 2 O = 2[Cu(NH 3)2]OH • При добавлении Na 2 S к Cu 2 O образуется черный сульфид Cu 2 S. Cu 2 O + S 2– + H 2 O = Cu 2 S +2 OH– • Эта реакция демонстрирует высокое сродство меди к сере.

Соединения меди (+1) • Неустойчивые в водных растворах соединения Cu(+1) (легко окисляющиеся кислородом, или диспропорционирующие) становятся наиболее устойчивыми при температуре >1000 о. С. • В этих условиях соединения Cu(+2) преобразуются в соединения Cu(+1). 4 Cu. O (т. ) = 2 Cu 2 O (т. ) + O 2 (г. ); 4 Cu. S (т. ) = 2 Cu 2 S (т. ) + S 2 (г. ) • Оксид Cu 2 O имеет температуру плавления 1242 о. С, при 1800 о. С он разлагается. 2 Cu 2 O 4 Cu + O 2

Серебро и золото Ag 47 серебро 4 d 105 s 1 107, 868 79 Au золото 5 d 106 s 1 196, 966 • Элементы Ag и Au, имеющие во внешнем слое один электрон, проявляют степень окисления +1. • У Ag эта степень окисления является самой устойчивой. • У Au степень окисления (+3) устойчивее, чем (+1). • Катионы этих металлов являются очень сильными акцепторами электронных пар и образуют очень прочные комплексы. • Большинство соединений Au как в степени окисления +1, так и в +3 являются комплексными. • Перевести золото в раствор удается только за счет образования прочных комплексов.

Простые вещества • Золото – мягкий желтый блестящий металл. • Серебро – очень светлый металл с мягким блеском. • Золото и серебро обладают высокой пластичностью, прокатываются в чрезвычайно тонкие листы и вытягиваются в тончайшие нити. Блеск и высокая пластичность определяет использование этих металлов в ювелирном деле. • • Золото на кварце Золото и серебро не окисляются кислородом. Серебро на воздухе, содержащем H 2 S, темнеет из-за образования сульфида Ag 2 S. 4 Ag + O 2 + 2 H 2 S = 2 Ag 2 S + 2 H 2 O

• • • Простые вещества Серебро и золото реагируют с галогенами. С парами брома Au реагирует уже при комнатной температуре. 2 Au + 2 Br 2 = Au. Br + Au. Br 3 При 70 о. С Au реагирует с парами I 2. 2 Au + I 2 = 2 Au. I При более сильном нагревании золото окисляется хлором и фтором до Au(+3). Все галогены окисляют серебро до Ag(+1). Серебро реагирует с расплавленной серой с образованием Ag 2 S.

Ео, В Cu 2+ +0, 34 Cu Cu+ +0, 52 Ag Ag+ +0, 80 Au Au+ +1, 69 Au 3+ +1, 50 Простые вещества • Ионы Н+ из кислот не могут окислить ни Ag, ни Au. • Серебро лучше всего растворяется в азотной кислоте, но может растворяться и в концентрированной серной. Ag + 2 HNO 3 (конц. ) = Ag. NO 3+ NO 2 + H 2 O • Золото можно растворить при нагревании в 98% селеновой кислоте. 2 Au + 6 H 2 Se. O 4 = Au 2(Se. O 4)3 + 3 Se. O 2 + 6 H 2 O • Для растворения Au чаще всего используют «царскую водку» (смесь концентрированных кислот HNO 3 и HCl в объемном отношении 1 к 3). Au + HNO 3 + 4 HCl = H[Au. Cl 4] + NO +2 H 2 O

Соединения серебра • Нитрат серебра – бесцветное кристаллическое вещество, растворяется в воде. • При добавлении к бесцветному раствору Ag. NO 3 щелочи в осадок выпадает темно-коричневый оксид Ag 2 O. 2 Ag. NO 3 + 2 Na. OH = Ag 2 O+H 2 O +2 Na. NO 3 • Гидроксид Ag(+1), как и Cu(+1), не выделен. • Оксид Ag 2 O является основным, легко растворяется в кислоте. Ag 2 O + 2 HNO 3 = 2 Ag. NO 3 + H 2 O • При небольшом нагревании Ag 2 O разлагается. 2 Ag 2 O = 4 Ag + O 2

Соединения серебра • Галогениды: белый Ag. Cl, желтые Ag. Br и Ag. I в воде не растворяются, Ag. F – растворим. Под действием света галогениды разлагаются, • Сульфид Ag 2 S – черное, нерастворимое и наиболее прочное соединение Ag. • Катион Ag+ является достаточно сильным окислителем и легко восстанавливается.

Соединения серебра Комплексные соединения Ag (+1) • Катион Ag+ образует комплексные соединения со многими лигандами, в том числе: Cl–, Br –, I–, CN–, SCN– , S 2 O 32–, NH 3 и др. • Для Ag(+1), как и для Cu(+1) и Au(+1), характерно координационное число 2 и линейное строение комплексов. • Образование галогенидных комплексов позволяет растворять осадки Ag. Cl, Ag. Br и Ag. I, при избытке галогенид-ионов. Ag. Cl + HCl (изб. ) = H[Ag. Cl 2] • Сульфид Ag 2 S, перейдет в раствор в виде [Ag(CN)2]– при взаимодействии с Na. CN.

Соединения золота • Наиболее устойчивым соединением Au(+1) в водном растворе является цианидный комплекс [Au(CN)2]–. • Степень окисления (+1) проявляется также в галогенидах Au. I и Au. Br. • Большей устойчивостью отличаются соединения Au(+3).
![Соединения золота • Золотохлористоводородная кислота H[Au. Cl 4]. H 2 O. • Под Соединения золота • Золотохлористоводородная кислота H[Au. Cl 4]. H 2 O. • Под](https://present5.com/presentation/27360963_132774645/image-29.jpg)
Соединения золота • Золотохлористоводородная кислота H[Au. Cl 4]. H 2 O. • Под действовием щелочи на раствор этой кислоты выпадает оранжевый осадок, состава Au 2 O 3. 2 H 2 O или Au. O(OH). H 2 O. • Гидроксид Au(+3) является амфотерным. • При взаимодействии с HCl он растворится с образованием комплексного аниона [Au. Cl 4]–, • под действием щелочи образуется желтый комплекс [Au(OH)4]–. • Кислотные свойства гидроксида выражены сильнее, поэтому его часто называют золотой кислотой.

Соединения золота • При осторожном слабом нагревании гидроксида можно получить коричневый оксид Au 2 O 3. • Оксид неустойчив и легко разлагается 2 Au 2 O 3 4 Au + 3 O 2 • Металлическое золото является очень слабым восстановителем, а его соединения проявляют сильные окислительные свойства и легко восстанавливаются даже слабыми восстановителями.

Соединения золота Комплексные соединения золота • Фактически, химия Au – это химия комплексных соединений. • Катионы Au образуют множество комплексных соединений. • Для комплексов Au(+1) более характерно координационное число 2 и линейная структура, • Для Au(+3) характерно координационное число 4 и плоскоквадратная структура. • Цианидные комплексы используют для отделения Au и Ag от пустой породы, Цианидный способ извлечения Au и Ag является наиболее эффективным. 4 Au + O 2 + 8 Na. CN + 2 H 2 O = 4 Na[Au(CN)2] + 4 Na. OH

Рекомендуемая учебная литература § Степин Б. Д. , Цветков А. А. Неорганическая химия: Учебник для вузов / Б. Д. Степин, А. А. Цветков. – М. : Высш. шк. , 1994. - 608 с. : ил. § Карапетьянц М. Х. Общая и неорганическая химия: Учебник для студентов вузов / М. Х. Карапетьянц, С. И. Дракин. - 4 -е изд. , стер. - М. : Химия, 2000. - 592 с. : ил. § Угай Я. А. Общая и неорганическая химия: Учебник для студентов вузов, обучающихся по направлению и специальности "Химия" / Я. А. Угай. - 3 -е изд. , испр. - М. : Высш. шк. , 2007. - 527 с. : ил. § Никольский А. Б. , Суворов А. В. Химия. Учебник для вузов / А. Б. Никольский, А. В. Суворов. – СПб: Химиздат, 2001. - 512 с. : ил.
138.ppt