молибден-лекция 3.ppt
- Количество слайдов: 54

Металлургия молибдена Направление «Металлургия»

План лекции 5 -7 n n n n Свойства молибдена Свойства соединений молибдена: оксиды, кислоты, соли Минералы молибдена Типы молибденовых руд. Месторождения Обогащение молибденовых руд Способы переработки молибденитовых концентратов Окислительный обжиг МК q q n Окисление молибденита Окисление примесей Практика обжига: многоподовые печи, печь КС Технико-экономические показатели обжига Получение оксида вольфрама(+6) q q Способ возгонки Гидрометаллургический способ переработки огарков

Свойства молибдена n n n 1778 г. Открыт Шееле, 1781 получен металлический молибден 1910 нашел промышленное применение Т плавления 0 С 2620 Т кипения 0 С 4800 Плотность, г/см 3 10, 2

Химические свойства молибдена n n n Окисляется при 4000 С С водой 7000 С, Н 2 -при Тпл, N 2 -15000 C, Cl 2 -2500 C, CO-12000 C. n n Практически не растворим в конц. растворах кислот и щелочей Хорошо растворим при нагревании в царской водке
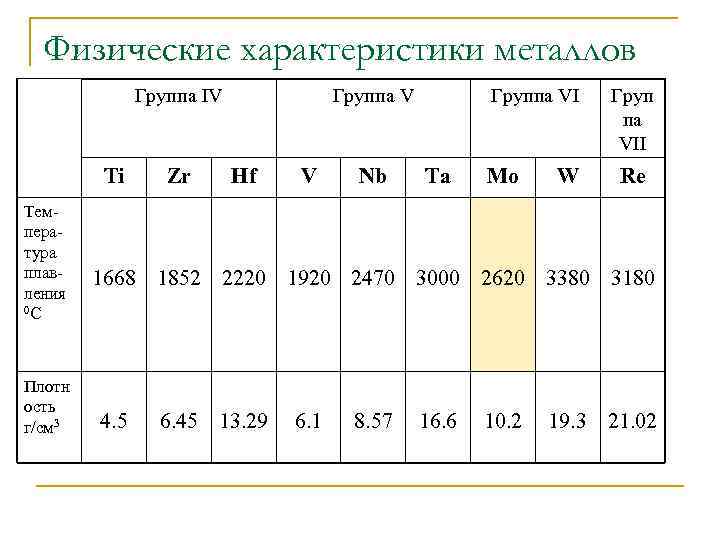
Физические характеристики металлов Группа IV Ti Температура плавления 0 С Плотн ость г/см 3 Zr Группа V Hf V Nb Группа VI Ta Mo W Груп па VII Re 1668 1852 2220 1920 2470 3000 2620 3380 3180 4. 5 6. 45 13. 29 6. 1 8. 57 16. 6 10. 2 19. 3 21. 02
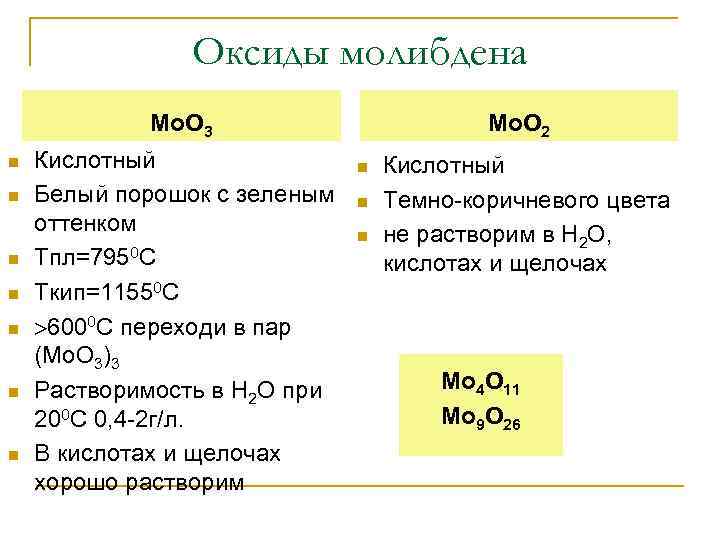
Оксиды молибдена Мо. О 3 n n n n Кислотный Белый порошок с зеленым оттенком Тпл=7950 С Ткип=11550 С 6000 С переходи в пар (Мо. О 3)3 Растворимость в Н 2 О при 200 С 0, 4 -2 г/л. В кислотах и щелочах хорошо растворим Мо. О 2 n n n Кислотный Темно-коричневого цвета не растворим в Н 2 О, кислотах и щелочах Мо 4 О 11 Мо 9 О 26
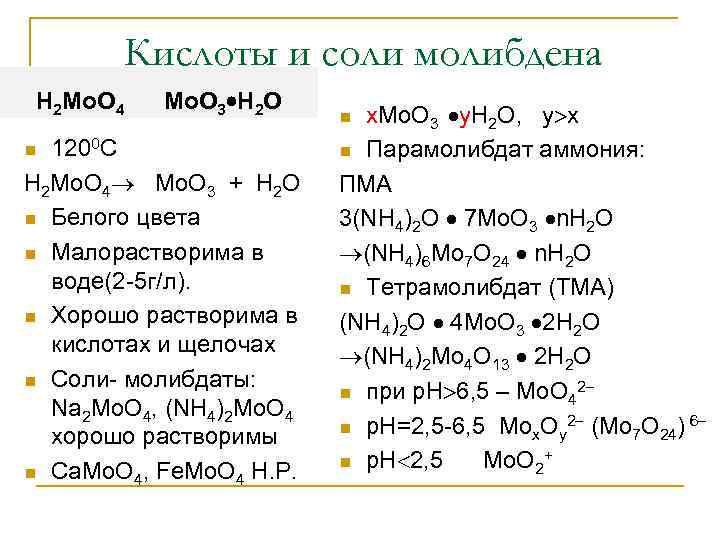
Кислоты и соли молибдена Н 2 Мо. О 4 Мо. О 3 Н 2 О 1200 С Н 2 Мо. О 4 Мо. О 3 + Н 2 О n Белого цвета n Малорастворима в воде(2 -5 г/л). n Хорошо растворима в кислотах и щелочах n Соли- молибдаты: Na 2 Mo. O 4, (NH 4)2 Mo. O 4 хорошо растворимы n Cа. Мо. О 4, Fe. Mo. O 4 Н. Р. n х. Мо. О 3 у. Н 2 О, у х n Парамолибдат аммония: ПМА 3(NH 4)2 О 7 Мo. O 3 n. Н 2 О (NH 4)6 Mo 7 O 24 n. Н 2 О n Тетрамолибдат (ТМА) (NH 4)2 О 4 Мo. O 3 2 Н 2 О (NH 4)2 Mo 4 O 13 2 Н 2 О n при р. Н 6, 5 – Мо. О 42 n р. Н=2, 5 -6, 5 Мох. Оу2 (Mo 7 O 24) 6 n р. Н 2, 5 Мо. О 2+ n

Области применения молибдена n n n Чистый металл 75% Жаростойкие и кислотоупорные сплавы (с Ni, Cr, Co) Производство электроламп, электроприборов Производство красок, лаков, окраски тканей (соединения) Стимуляторами роста растений служат оксиды Мо.
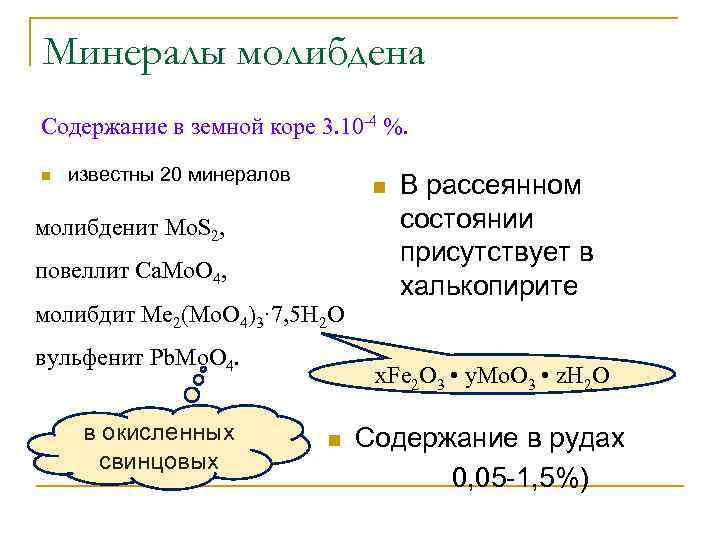
Минералы молибдена Содержание в земной коре 3 10 -4 %. n известны 20 минералов n молибденит Mo. S 2, повеллит Ca. Mo. O 4, молибдит Мe 2(Mo. O 4)3· 7, 5 H 2 O вульфенит Pb. Mo. O 4. в окисленных. свинцовых В рассеянном состоянии присутствует в халькопирите х. Fe 2 O 3 • у. Мо. О 3 • z. H 2 O n Содержание в рудах 0, 05 -1, 5%)

Молибденит n n n Это мягкий, свинцово-серого цвета минерал. Плотность 4, 7— 4, 8 г/см 3, твердость по минералогической шкале 1— 1, 5. Молибденит обладает гексагональной кристаллической решеткой слоистого типа. Встречается большей частью в кварцевых жилах, часто ассоциируется с шеелитом, касситеритом, вольфрамитом, висмутовым блеском, пиритом, халькопиритом, арсенопиритом.

Типы молибденовых руд n Простые кварце-молибденовые руды n Кварцево-молибдено-вольфрамитовые руды Скарновые руды ( шеелит, пирит, халькопирит) в кварцевых жилах (окремненных известняках). Медно-молибденовые руды (сульфиды меди и железа) n n

Месторождения n n n в западной части США, Мексике, Чили, Юго-Восточной части Канады, Южной Норвегии и восточных штатах Австралии. в России: на Северном Кавказе и в Закавказье, Красноярском крае (Хакассии, Сорский молибденовый комбинат), Северном Казахстане и других районах. Эксплуатируются руды с содержанием от 0, 05 до 1 -2 % молибдена.

Обогащение кварцево- молибденовых руд n Флотацией q q Коллективная флотация сульфидов Флотация молибденита n n Пенообразователи: сосновое масло Собиратели : керосин, трансформаторное масло Концентраты до 50% Несколько перечисток с 85 -95 % Mo. S 2 при извлечении из руды 90 %.

Обогащение медно-молибденовых руд n Коллективная флотация сульфидов q Медно-молибденовый концентрат n Разделение меди и молибдена: флотация молибдена при депрессировании сульфидов.

Состав молибденовых концентратов n n марки KMl, КМ 2 и КМ 3, содержание молибдена должно быть не ниже 50, 48 и 47 % соответственно. В них лимитируется содержание примесей P, As, Cu, Si. O 2, Sn.
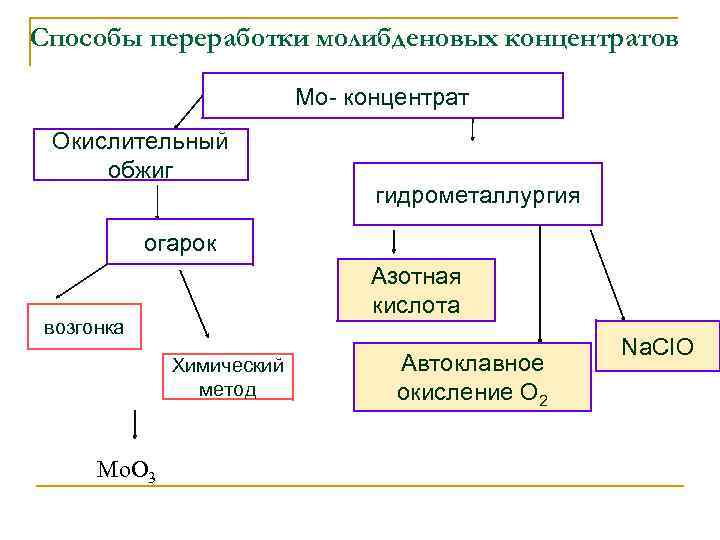
Способы переработки молибденовых концентратов Мо- концентрат Окислительный обжиг гидрометаллургия огарок Азотная кислота возгонка Химический метод Mo. O 3 Автоклавное окисление О 2 Na. CIO

Окислительный обжиг молибденитовых концентратов 1. 2. 3. 4. Окисление молибденита с образованием триоксида молибдена. Взаимодействие между триоксидом молибдена и молибденитом. Окисление сульфидных минералов сопутствующих элементов (меди, железа и др. ) с образованием оксидов и сульфатов. Взаимодействие между триоксидами Mo и оксидами, карбонатами, сульфатами элементовпримесей с образованием молибдатов.
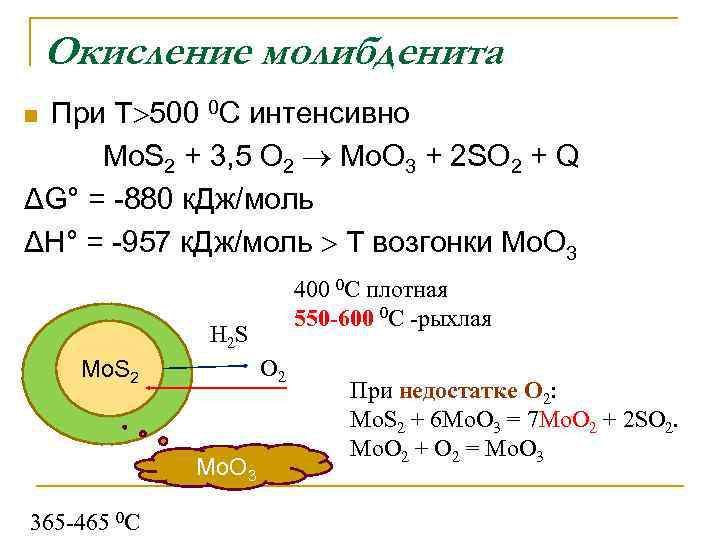
Окисление молибденита При T 500 0 С интенсивно Mo. S 2 + 3, 5 O 2 Mo. O 3 + 2 SO 2 + Q ΔG° = -880 к. Дж/моль ΔH° = -957 к. Дж/моль T возгонки Mo. O 3 n 400 0 C плотная 550 -600 0 С -рыхлая Н 2 S О 2 Mo. S 2 Мо. О 3 365 -465 0 C При недостатке О 2: Mo. S 2 + 6 Mo. O 3 = 7 Mo. O 2 + 2 SO 2. Mo. O 2 + O 2 = Mo. O 3

СТАДИИ ПРОЦЕССА n n Mo. S 2 + 3, 5 O 2 Mo. O 3 + 2 SO 2 + Q Mo. S 2 + 6 Mo. O 3 = 7 Mo. O 2 + 2 SO 2; (2) Mo. O 2 + 1/2 O 2 = Mo. O 3. Т= 600 0 С. (1)

Поведение примесей Сульфиды: Cu, Fe, Zn, Pb: Me. S +1, 5 O 2 = Me. O + SO 2 + O 2 2 SO 3, (kt=Mo. O 3) SO 3 + Me. O= Me. SO 4 Fe. SO 4 = Fe. O+ SO 3 (450 -500 0 C) Cu. SO 4 = Cu. O + SO 3 (600 -650 0 C) Zn. SO 4 = Zn. O + SO 3( 700 0 C) n Кальцит: Ca. СO 3 = Ca. O + СO 2
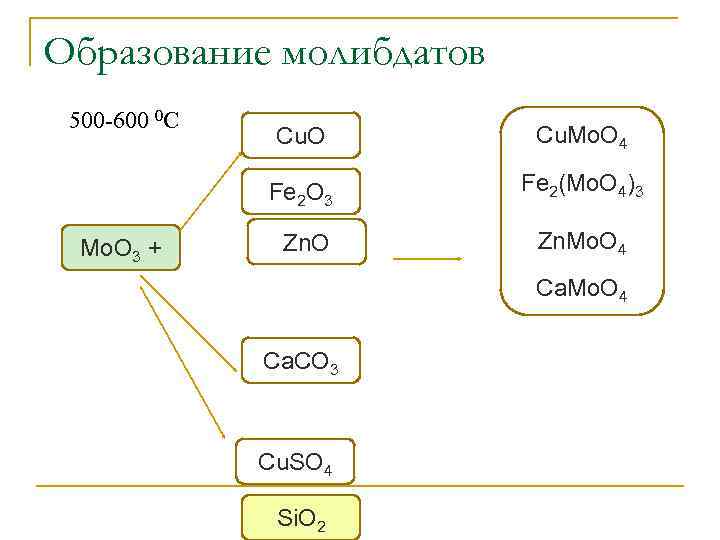
Образование молибдатов 500 -600 0 С Cu. Mo. О 4 Fe 2 О 3 Мо. О 3 + Cu. O Fe 2(Mo. О 4)3 Zn. O Zn. Mo. O 4 Ca. Mo. О 4 Ca. CО 3 Cu. SО 4 Si. О 2

Практика обжига n n n Многоподовых печах с механическим перегрибанием Печах кипящего слоя (560 -600 0 С) Барабанные печи- не обеспечивают необходимую температуру

обжиг в многоподовой печи I - под; II полый вал; III - держатель с гребками; IV окна для подачи воздуха; V дверки для чистки Схема 12 -подовой печи для обжига молибденитового концентрата (фирма Клаймакс, США):
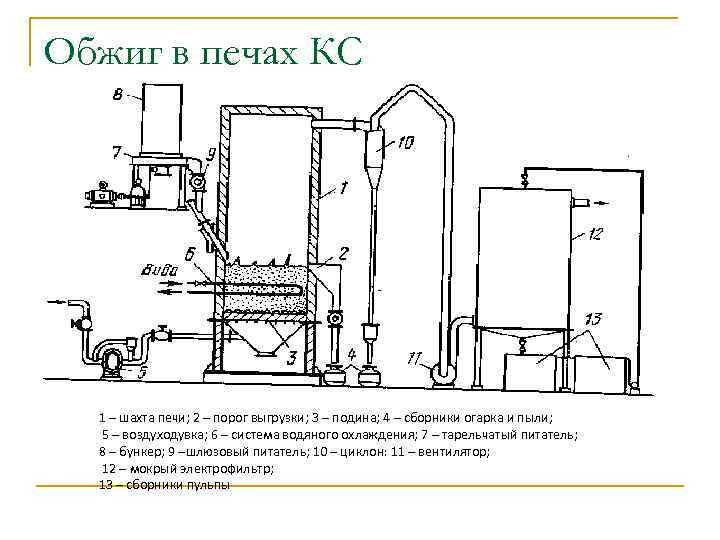
Обжиг в печах КС 1 – шахта печи; 2 – порог выгрузки; 3 – подина; 4 – сборники огарка и пыли; 5 – воздуходувка; 6 – система водяного охлаждения; 7 – тарельчатый питатель; 8 – бункер; 9 –шлюзовый питатель; 10 – циклон: 11 – вентилятор; 12 – мокрый электрофильтр; 13 – сборники пульпы

Технико-экономические показатели обжига показатели Производительность, кг/М 2 в сутки Многоподовая печь 70 -80 «КС» 1200 -1300 Пылеунос, % 10 -15 20 -40 Сод. S в огарке, % 0, 15 -0, 25 2 -2, 5 Сод. Мо. О 2 в огарке, % 4 -5 нет Сод. Молибдатов, % 1 -2 1 Отгонка Re 60 -70 90

Метод возгонки молибденовых огарков при Т кип. 11550 С возгонка Мо. О 3 n Т, 0 C 650 800 900 1000 1155 р, к. Па 0, 066 0, 233 1, 34 7, 15 26, 4 n 750 63, 4 101 800 -1100 0 С –тример в парах Мо 3 О 9. Скорость испарения из огарков, содержащих (48 – 50) % молибдена, при 1000 0 C и скорость потока воздуха (2 – 3) см/с составляют величину порядка (10 – 20) кг/(м 2·ч)

Скорость возгонки Мо. О 3 n n n Скорость испарения зависит от Т и V газа над поверхностью расплава Mo. O 3 плавится при 795 0 C. Даже при относительно малых скоростях воздуха (0, 2 – 0, 3 см/с) скорость испарения чистого Mo. O 3 значительна и возрастает от 12, 3 (900 0 C) до 110 кг/(м 2·ч) при 1100 0 C.

Поведение примесей при возгонки Мо. О 3 Сильно влияет на скорость возгонки: n Ca. O, Mg. O, Pb (прочные молибдаты) n Термически устойчив Fe 2(Mo. O 4)3 Мало влияет: n Cu. O (Cu. Mo. O 4 T paзл. 950 -11000 C) n Pb. Mo. O 4 испаряется, без разложения при 10500 C (Процесс: 900 - 950 0 С)
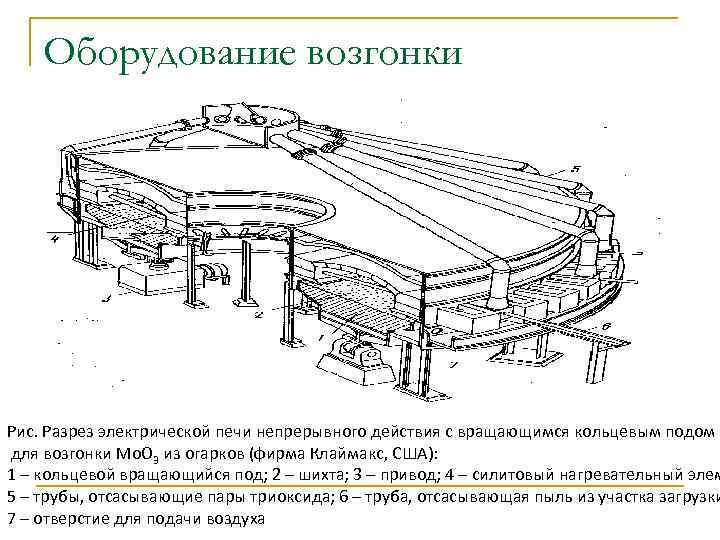
Оборудование возгонки Рис. Разрез электрической печи непрерывного действия с вращающимся кольцевым подом для возгонки Mo. O 3 из огарков (фирма Клаймакс, США): 1 – кольцевой вращающийся под; 2 – шихта; 3 – привод; 4 – силитовый нагревательный элем 5 – трубы, отсасывающие пары триоксида; 6 – труба, отсасывающая пыль из участка загрузки 7 – отверстие для подачи воздуха

Преимущества и недостатки возгонки Мо. О 3 За один оборот пода возгоняется ~(60 – 65)% Mo. O 3 n Производительность печи 3, 75 т чистого Mo. O 3 в сутки. n Чистота (99, 975 %) Mo. O 3 только из богатых концентратов с малым кол-м примесей, n Отсутствие реагентов, короткая техн. схема n дисперсен (насыпная масса ~0, 24 г/см 3) в производстве ~(0, 8 – 1, 0) г/см 3 n

Выплавка из огарка ферромолибдена n n (Fe и 55 -65%Mo) лигатурный сплав для добавки в сталь Т пл =1700 -1800 0 С. Селико-термический метод (Россия) Состав шихты: огарок (50%),

Выплавка из огарка ферромолибдена (Fe и 55 -65%Mo) лигатурный сплав для добавки в сталь n Т пл =1700 -1800 0 С. n Селико-термический метод (Россия) n Состав шихты (%): огарок (50), Fe-Si (20), Fe руда (15), Feстружка (10) AI стружка(2) Ca. O, Ca. F 2 (1 -1, 5) Mo. O 3 + Si= Mo + Si. O 2 + Q Mo. O 3 + AI= Fe 2 O 3 + Si= Fe + Si. O 2 + Q Fe 2 O 3 + AI= n
Плавка с верхним запалом • Через горн: 3 -4 т шихты • Делают 3 -4 лунки и в них засыпают запальную смесь (AI-Mg, AI- Na. NO 2)=1: 1: 1, 5 • Поджигают Fe-прутом • 30 -60 мин • Выдерживают 20 мин • Блок промывают водой • Дробят на куски
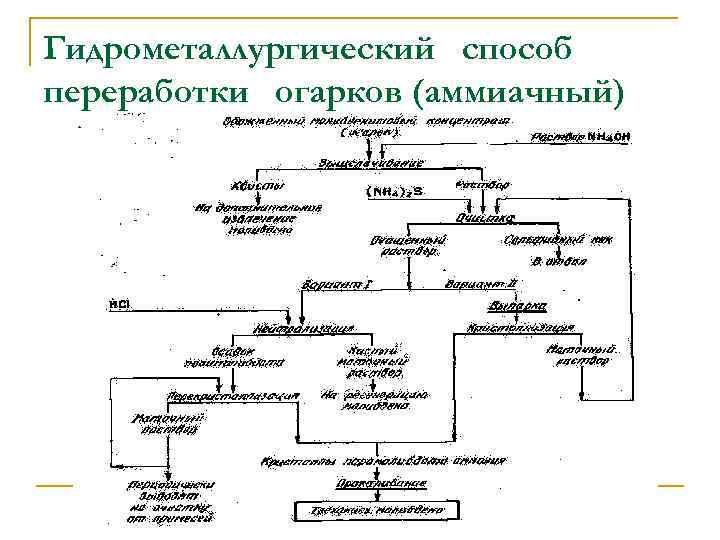
Гидрометаллургический способ переработки огарков (аммиачный)
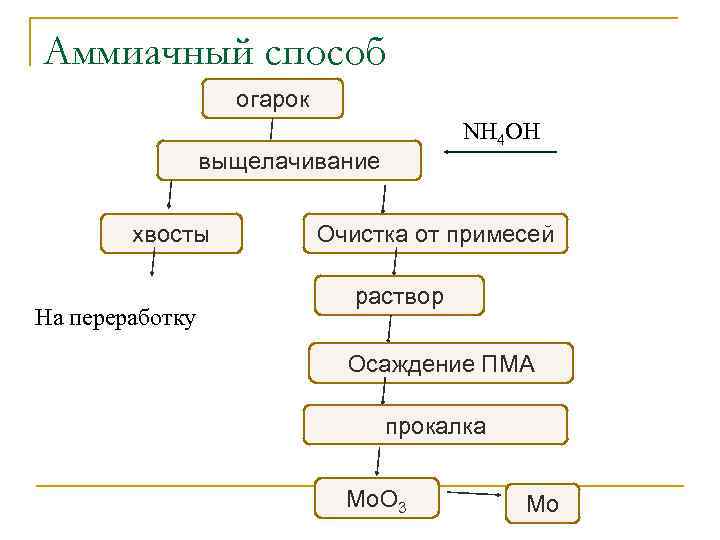
Аммиачный способ огарок NH 4 OH выщелачивание хвосты На переработку Очистка от примесей раствор Осаждение ПМА прокалка Мо. О 3 Мо

Выщелачивание n n n Mo. O 3 + 2 NH 4 OH = (NH 4)2 Mo. O 4 + H 2 O. Тепловой эффект ее равен 161 к. Дж/моль, реакция необратима и имеет первый порядок по концентрации аммиака: (d. GMo/d. T)Т = – KGMо. CNH 3 Энергия активации E = 79, 5 к. Дж/моль (кинетика, перемешивание) Степень извлечения Мо зависит от состава огарка

Примеси при выщелачивании огарка n n Практически нерастворимы в NH 3 H 2 O : Са. Мо. О 4, Мо. О 2, Mo. S 2 (хвосты выщелачивания) Fe. Mo. O 4 Fe(NH 3)6 2+, Fe(OH)2, Fe(OH)3 Молибдаты и сульфаты Сu 2+, Zn 2+, Ni 2+ легко Me(NH 3)n 2+, (к. ч. =4) Содержащийся в огарке в печи «КС» при выщелачивании Ca. SO 4 + Mo. O 2 -4 = Ca. Mo. O 4 + SO 2 -4. Для предотвращения этой реакции добавляют в раствор: Na 2 CO 3 или (NH 4)2 CO 3 Ca. SO 4 + Na 2 CO 3 = Са. СО 3 +Na 2 SO 4 n

Условия выщелачивания n n n n 8 -10% р-р аммиака – 120 или 140% к стехиометрии Стальные реакторы; холод или 50 -700 С Т: Ж= 1(3 -4) Остаточ. конц. 25 -30 г/л аммиака 4 стадии процесса. « 2 -(120 -140 г/л. Мо) 2 -оборот Извлечение 80 -95% Мо. Зависит от состава огарков. Выход хвостов 10 -25% (5 -25 %Мо) (отдельно на переработку)

Очистка от примесей n n n Аммиачные растворы (120 – 140) г/л Mo. O 3 и примеси ионов меди, железа, иногда цинка и никеля, ионы щелочных металлов. Для очистки от ионов меди и железа применяют осаждение их сульфидов сернистым аммонием. Перемешивание в гуммированных реакторах, холодные растворы, добавка реагента малыми дозами ПР(Cu. S)= 8, 5· 10 -45 (S= 9, 1 • 10 -23 моль/л). ПР (Fe. S) = 3, 7 • 10– 19
![Очистка от меди и железа n n Аммиачные комплексы меди-прочные Железа- непрочный [Cu(NH 3)4]2+ Очистка от меди и железа n n Аммиачные комплексы меди-прочные Железа- непрочный [Cu(NH 3)4]2+](https://present5.com/presentation/3/10739060_166266237.pdf-img/10739060_166266237.pdf-40.jpg)
Очистка от меди и железа n n Аммиачные комплексы меди-прочные Железа- непрочный [Cu(NH 3)4]2+ + NH 4 HS + 2 ОН– = Cu. S + 4 NH 3 + NH 4 OH + H 2 O. n Низкая концентрация S 2 -: оксисульфомолибдат (NH 4)2 Mo. O 4–x. Sx. n ПP Zn. S и Ni. S (6, 9· 10– 26 и 7, 9· 10– 26) –раствор.
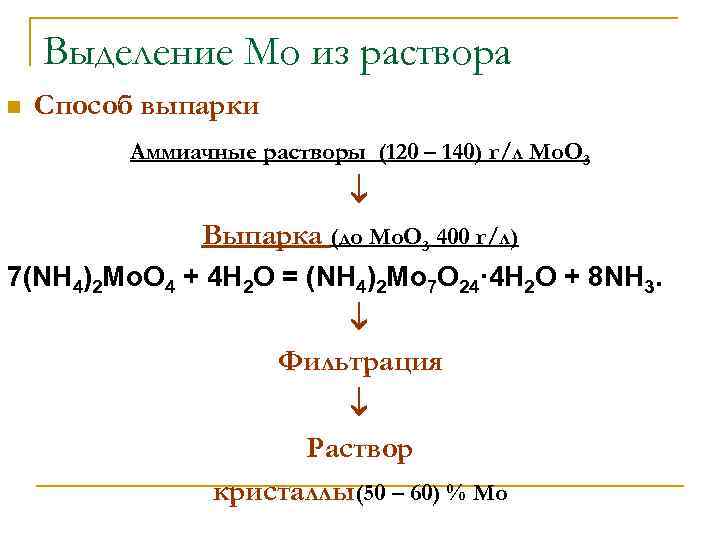
Выделение Мо из раствора n Способ выпарки Аммиачные растворы (120 – 140) г/л Mo. O 3 Выпарка (до Mo. O 3 400 г/л) 7(NH 4)2 Mo. O 4 + 4 H 2 O = (NH 4)2 Mo 7 O 24· 4 H 2 O + 8 NH 3. Фильтрация Раствор кристаллы(50 – 60) % Мо
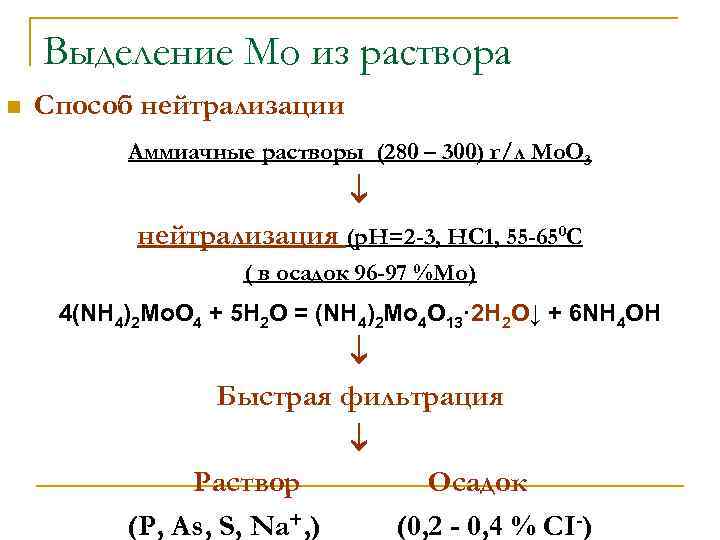
Выделение Мо из раствора n Способ нейтрализации Аммиачные растворы (280 – 300) г/л Mo. O 3 нейтрализация (р. Н=2 -3, НС 1, 55 -650 С ( в осадок 96 -97 %Mo) 4(NH 4)2 Mo. O 4 + 5 H 2 O = (NH 4)2 Mo 4 O 13· 2 H 2 O↓ + 6 NH 4 OH Быстрая фильтрация Раствор (P, As, S, Na+, ) Осадок (0, 2 - 0, 4 % СI-)
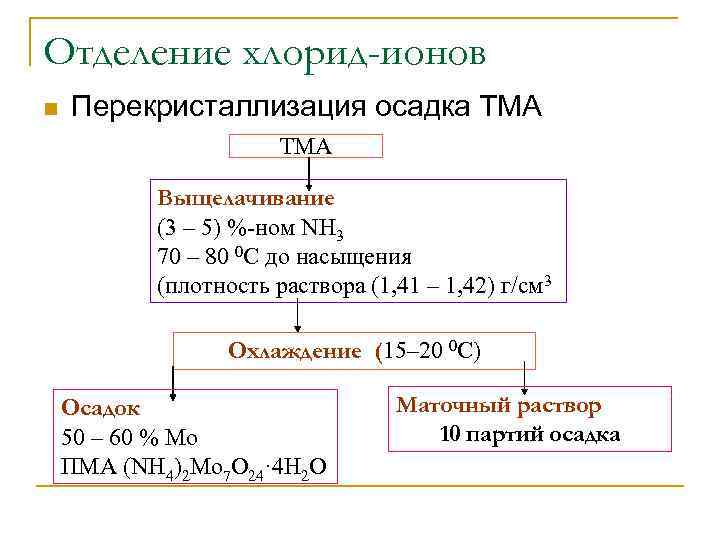
Отделение хлорид-ионов n Перекристаллизация осадка ТМА Выщелачивание (3 – 5) %-ном NH 3 70 – 80 0 C до насыщения (плотность раствора (1, 41 – 1, 42) г/см 3 Охлаждение (15– 20 0 C) Осадок 50 – 60 % Мо ПМА (NH 4)2 Mo 7 O 24· 4 H 2 O Маточный раствор 10 партий осадка

Содержание примесей в ПМА По отношению к молибдену, %: Sn, Pb, Bi, Cd <0, 0001; Zn, Mg, As, P, S, Ni, Cr, Ca <0, 001; Si, Al <0, 003; Fe < 0, 005. n

Маточный раствор n n n Мо = 3 – 4 % от исходного количества (что отвечает концентрации молибдена (6 – 10) г/л). После подкисления до р. Н = 2 и длительного стояния из них выделяются аморфные осадки полимолибдатов различного состава, возвращаемые на операции очистки от примесей. Из хвостовых маточных растворов, содержащих ~1 г/л Mo, последний извлекают сорбцией на анионообменных смолах.

Извлечение молибдена из хвостов аммиачного выщелачивания огарков Хвосты выщелачивания (5 – 25) % Мо Kомпоненты хвостов: n q q Ca. Mo. O 4, Fe. Mo. O 4, неокислившегося Mo. S 2, а также сорбированных анионов Mo. O 42 -. Fe. O, Fe 2 O 3, Si. O 2, иногда Ca. WO 4 или (Fe, Mn)WO 4. Для извлечения молибдена из хвостов применяют q щелочные способы: n n n спекание с содой, выщелачивание растворами соды в автоклавах или разложение соляной кислотой.

Спекание хвостов с содой n n n Много Mo. O 2 и Mo. S 2 Влажные хвосты смешивают с содой, полученную пастообразную массу нагревают на поду отражательной печи при (700 – 750) 0 C в течение (4 – 6) ч. Спек выщелачивают водой, получая растворы молибдата натрия.

Выщелачивание хвостов раствором соды в автоклавах n n n низкое Mo. O 2 и Mo. S 2 Условие: Т= 180 – 200 0 C. Na 2 Mo. O 4 + 2 NH 3 = (NH 4)2 Mo. O 4+ 2 Na. OH Молибден сорбируют на слабоосновной смоле (AH-I, ЭДЭ-10 П и др. ) при p. H=2÷ 4. Реэстракция Мо - раствором аммиака полученный аммиачный элюат присоединяется к основным растворам аммиачного выщелачивания огарков.
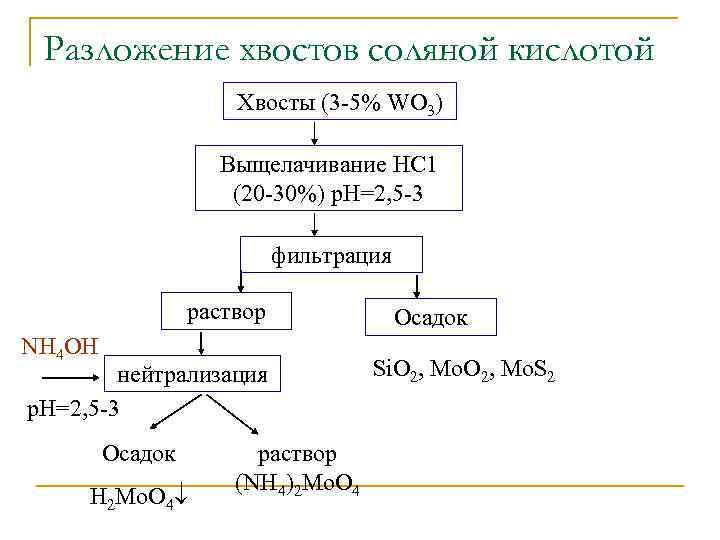
Разложение хвостов соляной кислотой Хвосты (3 -5% WO 3) Выщелачивание НС 1 (20 -30%) р. Н=2, 5 -3 фильтрация раствор NH 4 OH нейтрализация p. H=2, 5 -3 Осадок H 2 Mo. O 4 раствор (NH 4)2 Mo. O 4 Осадок Si. O 2, Mo. S 2
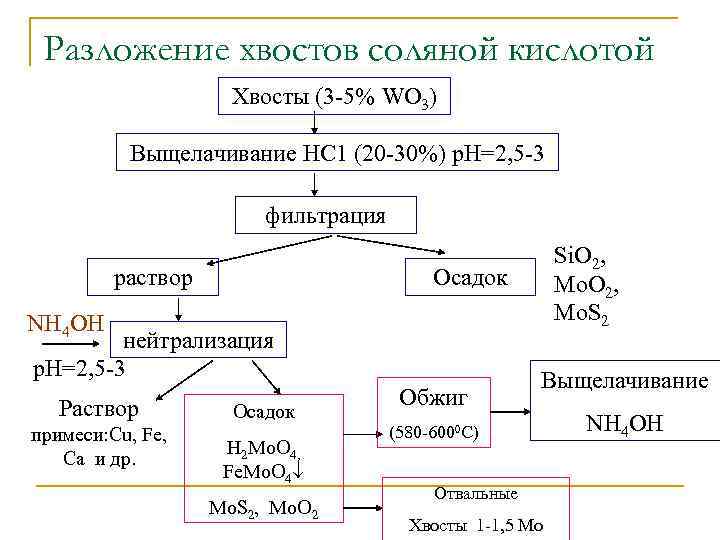
Разложение хвостов соляной кислотой Хвосты (3 -5% WO 3) Выщелачивание НС 1 (20 -30%) р. Н=2, 5 -3 фильтрация раствор Si. O 2, Mo. S 2 Осадок NH 4 OH нейтрализация p. H=2, 5 -3 Раствор примеси: Cu, Fe, Ca и др. Осадок H 2 Mo. O 4, Fe. Mo. O 4 Мо. S 2, Mo. O 2 Обжиг Выщелачивание (580 -6000 С) Отвальные Хвосты 1 -1, 5 Мо NH 4 OH

Термическое разложение парамолибдата аммония ПМА (450– 500) 0 C (NH 4)2 Mo 7 O 24· 4 H 2 O (NH 4)2 Mo 7 O 24 (NH 4)2 Mo 4 O 13 Mo. O 3. бледно-зеленого цвета Извлечение Мо в готовый продукт по гидрометаллургической схеме 94– 95%.

Азотнокислый способ переработки молибденитового концентрата n n n Mo. S 2 + 6 HNO 3 = H 2 Mo. O 4 + 2 H 2 SO 4 + 6 NO. Часть Мо остается в маточном растворе сульфатокомплекса [Mo. О 2(SО 4)n]2 n-2 Re –HRe. O 4 коагуляции H 2 Mo. O 4 способствует: С, Т. Если: 30 – 35%-ной HNO 3 при 90 % кислые маточные растворы содержат (12 – 14) г/л Mo, 54 %-ной кислотой – (2, 5 – 3) г/л Mo.

Расход азотной кислоты n Замкнутая система 2 NO + O 2 = 2 NO 2 Извлечение Мо 80 – 85% 2 NO 2 + H 2 O = HNO 2 + HNO 3 HNO 2 = ⅓HNO 3 + ⅔NO + ⅓H 2 O. Результирующая реакция абсорбции NO 2 3 NO 2 + H 2 O = 2 HNO 3 + NO Кислые маточные растворы содержат, г/л: Mo (10 – 15); Fe (5 – 10); Cu (1, 5 – 8); H 2 SO 4 (200 – 250); HNO 3 (30 – 50); Re (0, 01 – 0, 15).

Способ «сжигания» в пламени природного газа n n n При избытке газа оксиды восстанавливаются до элементарного азота: 4 NO + CH 4 = 2 N 2 + CO 2 + 2 H 2 O; 2 NO 2 + CH 4 = N 2 + CO 2 + 2 H 2 O.
молибден-лекция 3.ppt