b0aa89e10481b2ee88edae8ac5ef90eb.ppt
- Количество слайдов: 20
 Металлорганические соединения
Металлорганические соединения
 Лекция № 2. 1 1. 2. 3. Классификация и номенклатура металлорганических соединений. Методы получения металлорганических. соединений. Свойства металлорганических соединений и их использование в органическом синтезе. Литература: 1. 2. 3. Хельвинкель Д. Систематическая номенклатура органических соединений. М. : БИНОМ. Лаборатория знаний, 2012, 232 с. Смит В. А. , Дильман А. Д. Основы современного органического синтеза. М. : БИНОМ. Лаборатория знаний, 2009, с. 49. Сайт компании Аldrich - Sigma //www. sigmaaldrich. com
Лекция № 2. 1 1. 2. 3. Классификация и номенклатура металлорганических соединений. Методы получения металлорганических. соединений. Свойства металлорганических соединений и их использование в органическом синтезе. Литература: 1. 2. 3. Хельвинкель Д. Систематическая номенклатура органических соединений. М. : БИНОМ. Лаборатория знаний, 2012, 232 с. Смит В. А. , Дильман А. Д. Основы современного органического синтеза. М. : БИНОМ. Лаборатория знаний, 2009, с. 49. Сайт компании Аldrich - Sigma //www. sigmaaldrich. com
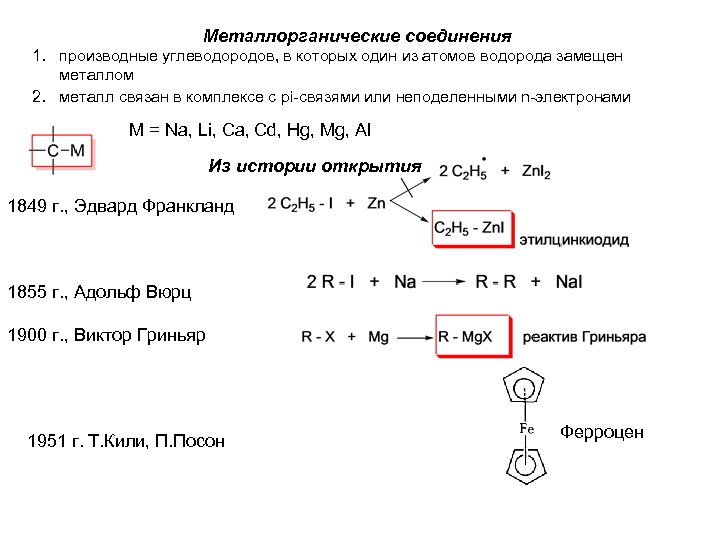 Металлорганическиe соединения 1. производные углеводородов, в которых один из атомов водорода замещен металлом 2. металл связан в комплексе с pi-связями или неподеленными n-электронами М = Na, Li, Ca, Cd, Hg, Mg, Al Из истории открытия 1849 г. , Эдвард Франкланд 1855 г. , Адольф Вюрц 1900 г. , Виктор Гриньяр 1951 г. Т. Кили, П. Посон Ферроцен
Металлорганическиe соединения 1. производные углеводородов, в которых один из атомов водорода замещен металлом 2. металл связан в комплексе с pi-связями или неподеленными n-электронами М = Na, Li, Ca, Cd, Hg, Mg, Al Из истории открытия 1849 г. , Эдвард Франкланд 1855 г. , Адольф Вюрц 1900 г. , Виктор Гриньяр 1951 г. Т. Кили, П. Посон Ферроцен
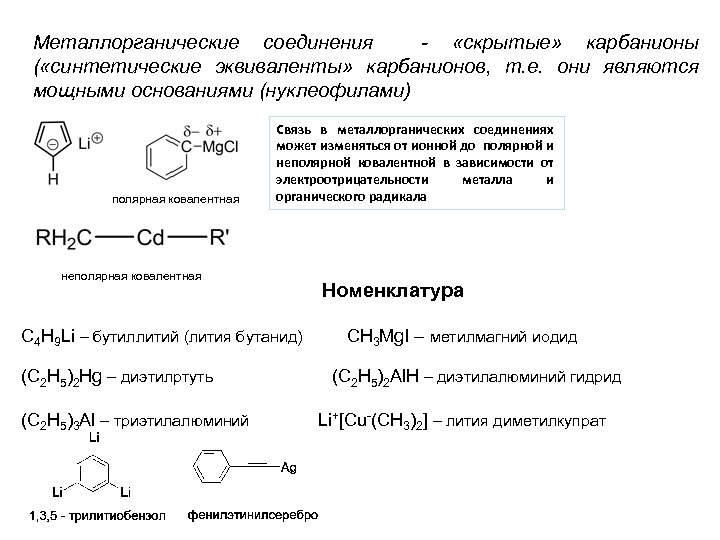 Металлорганические соединения - «скрытые» карбанионы ( «синтетические эквиваленты» карбанионов, т. е. они являются мощными основаниями (нуклеофилами) полярная ковалентная Связь в металлорганических соединениях может изменяться от ионной до полярной и неполярной ковалентной в зависимости от электроотрицательности металла и органического радикала неполярная ковалентная C 4 H 9 Li – бутиллитий (лития бутанид) (С 2 H 5)2 Hg – диэтилртуть (C 2 H 5)3 Al – триэтилалюминий Номенклатура CH 3 Mg. I – метилмагний иодид (C 2 H 5)2 Al. H – диэтилалюминий гидрид Li+[Cu-(CH 3)2] – лития диметилкупрат
Металлорганические соединения - «скрытые» карбанионы ( «синтетические эквиваленты» карбанионов, т. е. они являются мощными основаниями (нуклеофилами) полярная ковалентная Связь в металлорганических соединениях может изменяться от ионной до полярной и неполярной ковалентной в зависимости от электроотрицательности металла и органического радикала неполярная ковалентная C 4 H 9 Li – бутиллитий (лития бутанид) (С 2 H 5)2 Hg – диэтилртуть (C 2 H 5)3 Al – триэтилалюминий Номенклатура CH 3 Mg. I – метилмагний иодид (C 2 H 5)2 Al. H – диэтилалюминий гидрид Li+[Cu-(CH 3)2] – лития диметилкупрат
 n-Bu. Li, s-Bu. Li, t-Bu. Li, некоторые реагенты Гриньяра – коммерческие продукты (см. каталог компаний Aldrich - Sigma) Et 3 Al, Et 2 Al. Cl – производятся в большом масштабе Методы синтеза металлорганических соединений Метод А Восстановление Метод В Депротонирование Метод С Обмен Метод D Трансметаллирование Органические соединения лития и магния остаются ключевыми реагентами в тонком органическом синтезе
n-Bu. Li, s-Bu. Li, t-Bu. Li, некоторые реагенты Гриньяра – коммерческие продукты (см. каталог компаний Aldrich - Sigma) Et 3 Al, Et 2 Al. Cl – производятся в большом масштабе Методы синтеза металлорганических соединений Метод А Восстановление Метод В Депротонирование Метод С Обмен Метод D Трансметаллирование Органические соединения лития и магния остаются ключевыми реагентами в тонком органическом синтезе
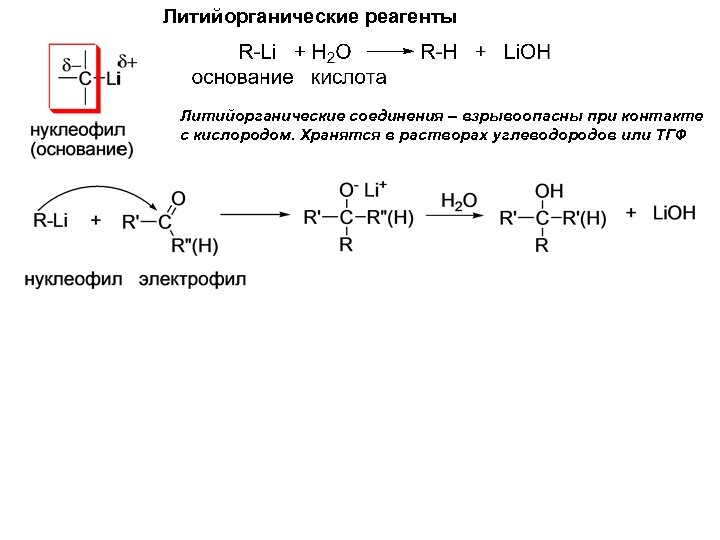 Литийорганические реагенты Литийорганические соединения – взрывоопасны при контакте с кислородом. Хранятся в растворах углеводородов или ТГФ
Литийорганические реагенты Литийорганические соединения – взрывоопасны при контакте с кислородом. Хранятся в растворах углеводородов или ТГФ
 Синтез литийорганических соединений Метод А Восстановление Классический способ получений литийорганических соединений Растворитель - алкан Механизм внедрение металла по связи углерод-галоген – процесс одноэлектронного переноса (SET, Single Electron transfer)
Синтез литийорганических соединений Метод А Восстановление Классический способ получений литийорганических соединений Растворитель - алкан Механизм внедрение металла по связи углерод-галоген – процесс одноэлектронного переноса (SET, Single Electron transfer)
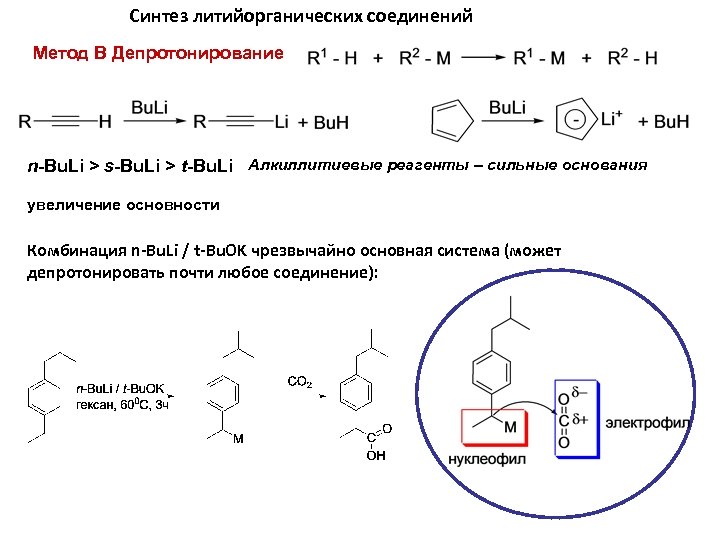 Синтез литийорганических соединений Метод В Депротонирование n-Bu. Li > s-Bu. Li > t-Bu. Li Алкиллитиевые реагенты – сильные основания увеличение основности Комбинация n-Bu. Li / t-Bu. OK чрезвычайно основная система (может депротонировать почти любое соединение):
Синтез литийорганических соединений Метод В Депротонирование n-Bu. Li > s-Bu. Li > t-Bu. Li Алкиллитиевые реагенты – сильные основания увеличение основности Комбинация n-Bu. Li / t-Bu. OK чрезвычайно основная система (может депротонировать почти любое соединение):
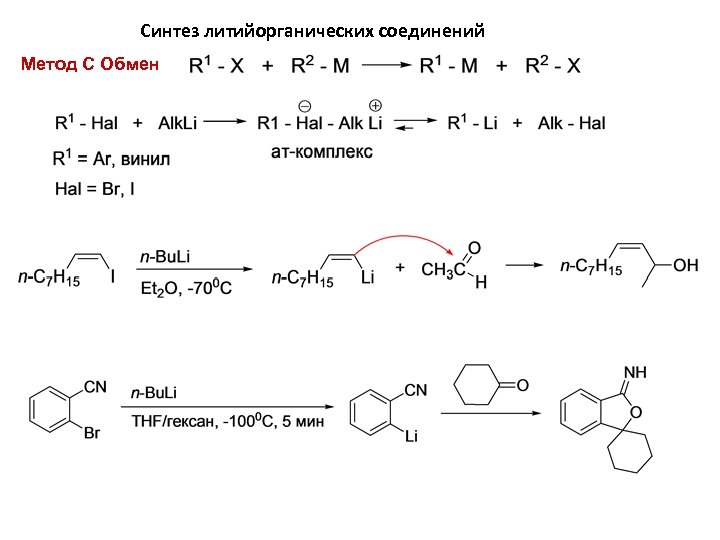 Синтез литийорганических соединений Метод С Обмен
Синтез литийорганических соединений Метод С Обмен
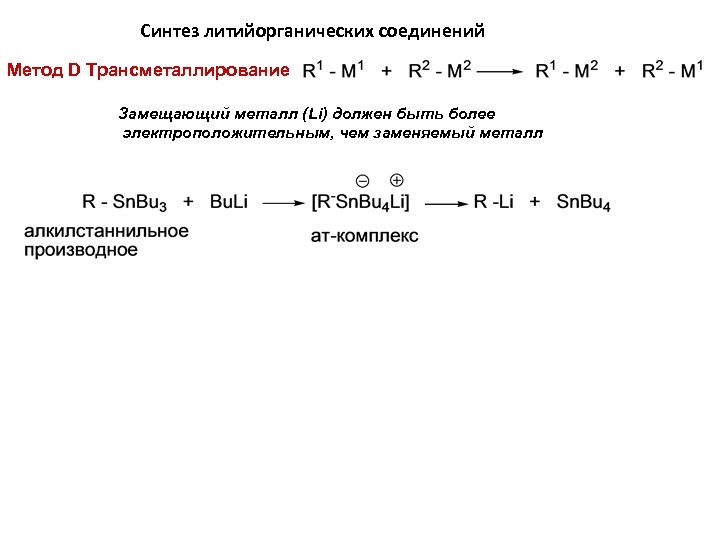 Синтез литийорганических соединений Метод D Трансметаллирование Замещающий металл (Li) должен быть более электроположительным, чем заменяемый металл
Синтез литийорганических соединений Метод D Трансметаллирование Замещающий металл (Li) должен быть более электроположительным, чем заменяемый металл
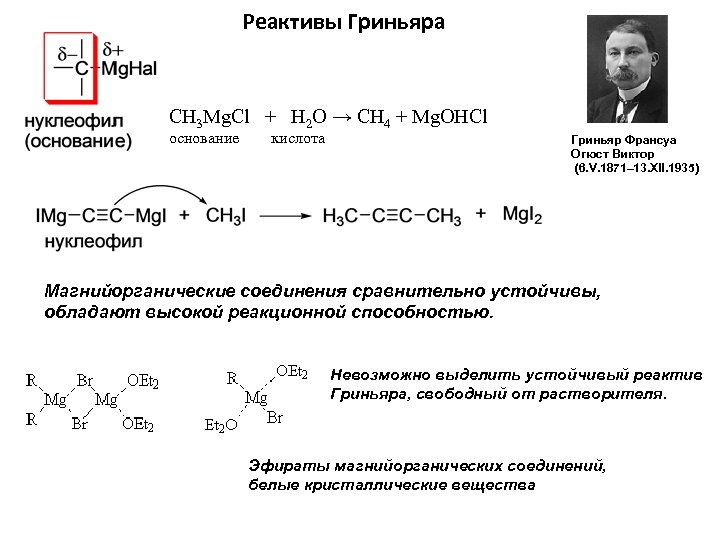 Реактивы Гриньяра CH 3 Mg. Cl + H 2 O → CH 4 + Mg. OHCl основание кислота Гриньяр Франсуа Огюст Виктор (6. V. 1871– 13. XII. 1935) Магнийорганические соединения сравнительно устойчивы, обладают высокой реакционной способностью. Невозможно выделить устойчивый реактив Гриньяра, свободный от растворителя. Эфираты магнийорганических соединений, белые кристаллические вещества
Реактивы Гриньяра CH 3 Mg. Cl + H 2 O → CH 4 + Mg. OHCl основание кислота Гриньяр Франсуа Огюст Виктор (6. V. 1871– 13. XII. 1935) Магнийорганические соединения сравнительно устойчивы, обладают высокой реакционной способностью. Невозможно выделить устойчивый реактив Гриньяра, свободный от растворителя. Эфираты магнийорганических соединений, белые кристаллические вещества
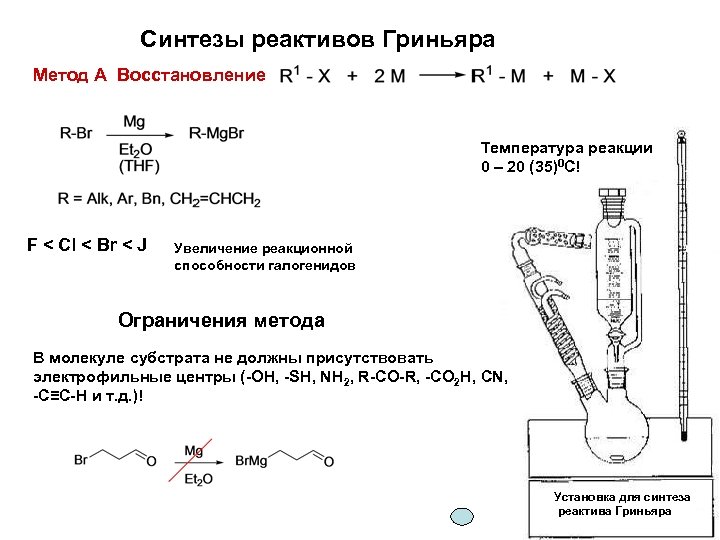 Синтезы реактивов Гриньяра Метод А Восстановление Температура реакции 0 – 20 (35)0 С! F < Cl < Br < J Увеличение реакционной способности галогенидов Ограничения метода В молекуле субстрата не должны присутствовать электрофильные центры (-OH, -SH, NH 2, R-CO-R, -CO 2 H, CN, -C≡C-H и т. д. )! Установка для синтеза реактива Гриньяра
Синтезы реактивов Гриньяра Метод А Восстановление Температура реакции 0 – 20 (35)0 С! F < Cl < Br < J Увеличение реакционной способности галогенидов Ограничения метода В молекуле субстрата не должны присутствовать электрофильные центры (-OH, -SH, NH 2, R-CO-R, -CO 2 H, CN, -C≡C-H и т. д. )! Установка для синтеза реактива Гриньяра
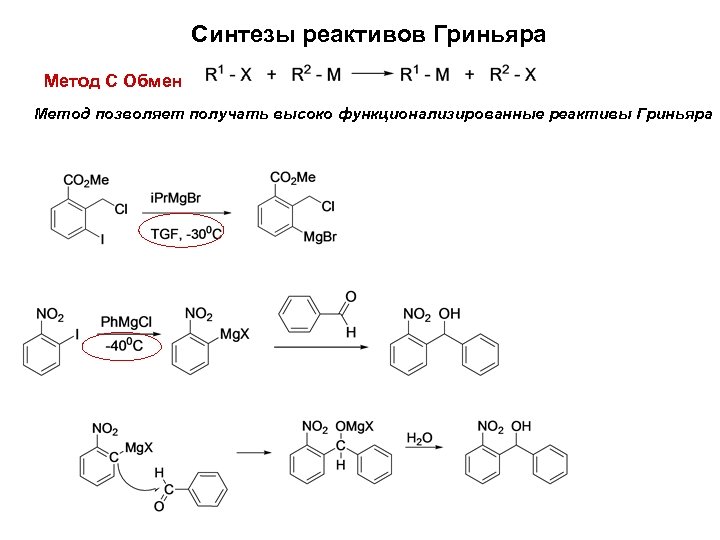 Синтезы реактивов Гриньяра Метод С Обмен Метод позволяет получать высоко функционализированные реактивы Гриньяра
Синтезы реактивов Гриньяра Метод С Обмен Метод позволяет получать высоко функционализированные реактивы Гриньяра
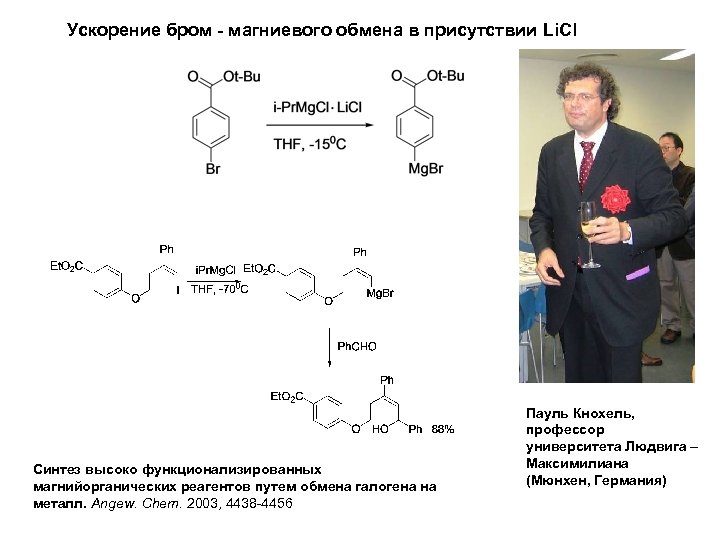 Ускорение бром - магниевого обмена в присутствии Li. Cl Синтез высоко функционализированных магнийорганических реагентов путем обмена галогена на металл. Angew. Chem. 2003, 4438 -4456 Пауль Кнохель, профессор университета Людвига – Максимилиана (Мюнхен, Германия)
Ускорение бром - магниевого обмена в присутствии Li. Cl Синтез высоко функционализированных магнийорганических реагентов путем обмена галогена на металл. Angew. Chem. 2003, 4438 -4456 Пауль Кнохель, профессор университета Людвига – Максимилиана (Мюнхен, Германия)
 Лаборатория органического синтеза (университета Людвига Максимилиана , г. Мюнхен
Лаборатория органического синтеза (университета Людвига Максимилиана , г. Мюнхен
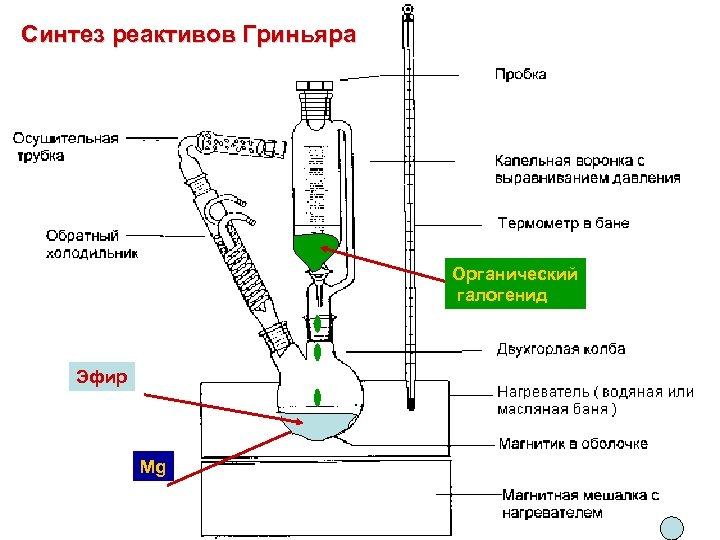 Синтез реактивов Гриньяра Органический галогенид Эфир Mg
Синтез реактивов Гриньяра Органический галогенид Эфир Mg
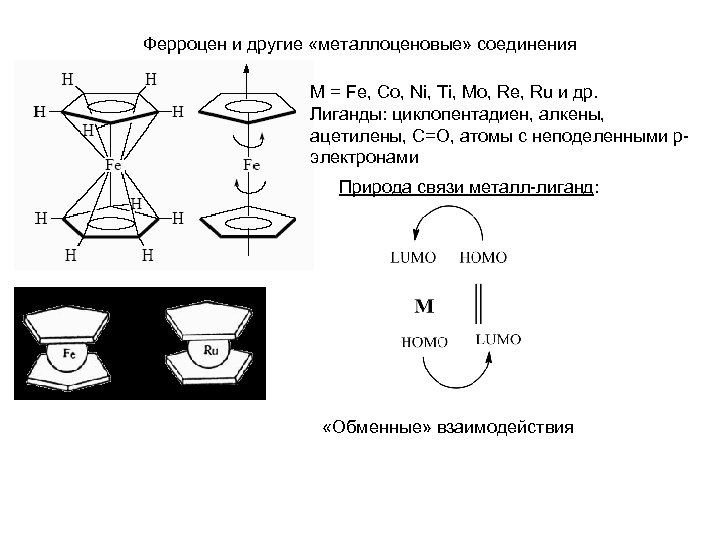 Ферроцен и другие «металлоценовые» соединения М = Fe, Co, Ni, Ti, Mo, Re, Ru и др. Лиганды: циклопентадиен, алкены, ацетилены, С=О, атомы с неподеленными pэлектронами Природа связи металл-лиганд: «Обменные» взаимодействия
Ферроцен и другие «металлоценовые» соединения М = Fe, Co, Ni, Ti, Mo, Re, Ru и др. Лиганды: циклопентадиен, алкены, ацетилены, С=О, атомы с неподеленными pэлектронами Природа связи металл-лиганд: «Обменные» взаимодействия
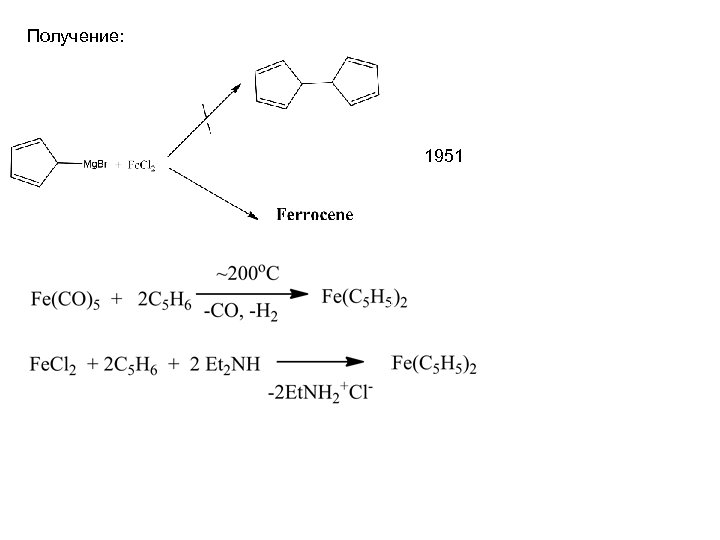 Получение: 1951
Получение: 1951
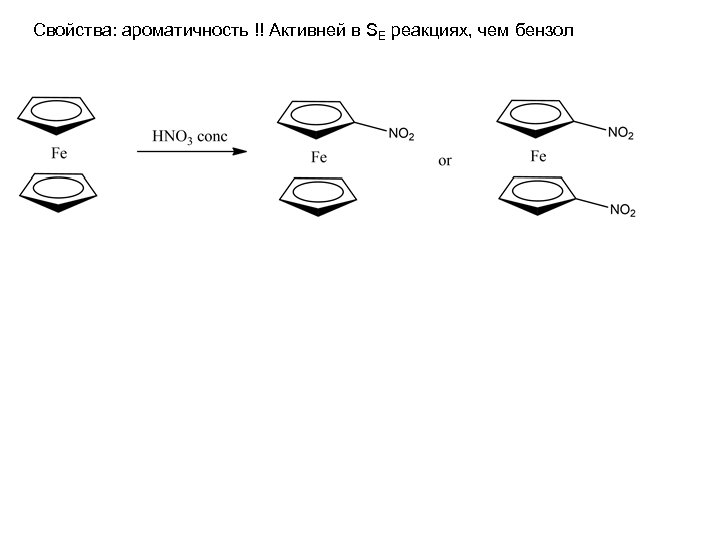 Свойства: ароматичность !! Активней в SE реакциях, чем бензол
Свойства: ароматичность !! Активней в SE реакциях, чем бензол
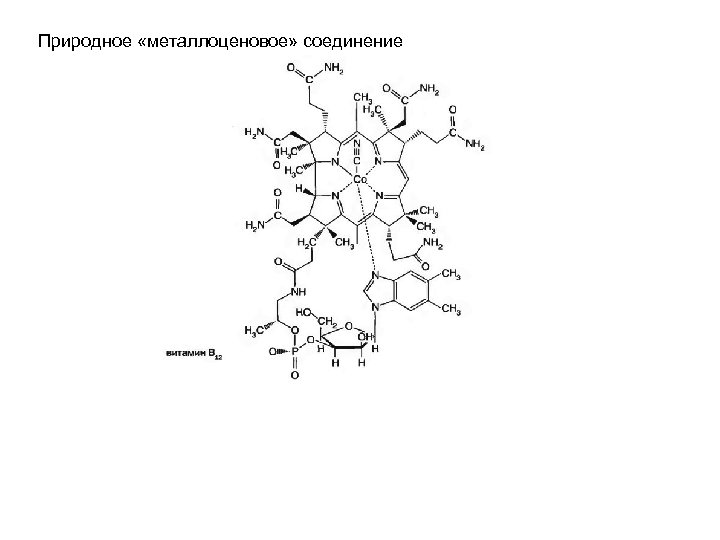 Природное «металлоценовое» соединение
Природное «металлоценовое» соединение


