lecture_4_2013.ppt
- Количество слайдов: 33
 Металлоорганические соединения металлов 2 и 12 групп (2 M и 12 M) 1
Металлоорганические соединения металлов 2 и 12 групп (2 M и 12 M) 1
 2 -я группа ns 2 12 -я группа (n-1)d 10 ns 2 Ba Sr Ca Mg Be 2 M Zn Cd Hg 12 M 2
2 -я группа ns 2 12 -я группа (n-1)d 10 ns 2 Ba Sr Ca Mg Be 2 M Zn Cd Hg 12 M 2
 Сравнение металлов 2 и 12 групп M Электроотр. Ковалентный радиус, Å E 0(M 2+/M), В Температура плавления, o. C 2 ая группа (электронная конфигурация ns 2) Ba 0. 9 2. 15 2. 91 727 Sr 1. 0 1. 95 2. 89 777 Ca 1. 0 1. 76 2. 79 842 Mg 1. 3 1. 41 2. 37 650 Be 1. 6 0. 96 1. 97 1287 12 ая группа (электронная конфигурация (n– 1)d 10 ns 2) Zn 1. 7 1. 22 0. 76 420 Cd 1. 7 1. 44 0. 40 321 Hg 2. 0 1. 32 + 0. 85 39 3
Сравнение металлов 2 и 12 групп M Электроотр. Ковалентный радиус, Å E 0(M 2+/M), В Температура плавления, o. C 2 ая группа (электронная конфигурация ns 2) Ba 0. 9 2. 15 2. 91 727 Sr 1. 0 1. 95 2. 89 777 Ca 1. 0 1. 76 2. 79 842 Mg 1. 3 1. 41 2. 37 650 Be 1. 6 0. 96 1. 97 1287 12 ая группа (электронная конфигурация (n– 1)d 10 ns 2) Zn 1. 7 1. 22 0. 76 420 Cd 1. 7 1. 44 0. 40 321 Hg 2. 0 1. 32 + 0. 85 39 3
 Сравнение металлов 2 и 12 групп Редокс-свойства характерные степени окисления: 0 и 2+ R–M–X, R–M–R Zn+, Cd+, Mg+ - получены в последние 10 лет! R–M–M–R для неорганических соединений ртути характерна ст. ок. 1+ (Hg 22+), но органические производные Hg 1+ неполучены соединения 2 M 2+, Zn 2+ и Cd 2+ могут обладать восстановительными свойствами только за счет лигандов которые проявляют редокс-активность; соединения Hg 2+ могут быть окислителями за счет самого Hg 2+ соединения Mg 1+, Zn 1+ – сильные восстановители, сравнимые с щелочными металлами! 4
Сравнение металлов 2 и 12 групп Редокс-свойства характерные степени окисления: 0 и 2+ R–M–X, R–M–R Zn+, Cd+, Mg+ - получены в последние 10 лет! R–M–M–R для неорганических соединений ртути характерна ст. ок. 1+ (Hg 22+), но органические производные Hg 1+ неполучены соединения 2 M 2+, Zn 2+ и Cd 2+ могут обладать восстановительными свойствами только за счет лигандов которые проявляют редокс-активность; соединения Hg 2+ могут быть окислителями за счет самого Hg 2+ соединения Mg 1+, Zn 1+ – сильные восстановители, сравнимые с щелочными металлами! 4
 Сравнение металлов 2 и 12 групп Полярность связи M–C: для Zn и Cd – того же порядка, что и Be–C; для Hg – связь ковалентная малополярная Склонность к образованию многоцентровых связей M–C–M : в отличие от Be и Mg, для 12 M менее характерна, причем уменьшается от Zn к Hg Льюисовская кислотность: для Zn – того же порядка, что и для Mg; уменьшается от Zn к Hg 5
Сравнение металлов 2 и 12 групп Полярность связи M–C: для Zn и Cd – того же порядка, что и Be–C; для Hg – связь ковалентная малополярная Склонность к образованию многоцентровых связей M–C–M : в отличие от Be и Mg, для 12 M менее характерна, причем уменьшается от Zn к Hg Льюисовская кислотность: для Zn – того же порядка, что и для Mg; уменьшается от Zn к Hg 5
 Сравнение металлов 2 и 12 групп Активность как источника нуклеофильного фрагмента R– : соединения Zn и Cd являются таковыми, но «мягче» , чем 2 M; для Hg – нет, только за счет восстановления Hg 2+ до Hg 0 Чувствительность к H+, H 2 O и O 2: соединения Zn и Cd чувствительны, но меньше, чем 2 M; для Hg – нет 6
Сравнение металлов 2 и 12 групп Активность как источника нуклеофильного фрагмента R– : соединения Zn и Cd являются таковыми, но «мягче» , чем 2 M; для Hg – нет, только за счет восстановления Hg 2+ до Hg 0 Чувствительность к H+, H 2 O и O 2: соединения Zn и Cd чувствительны, но меньше, чем 2 M; для Hg – нет 6
 Магнийорганические соединения
Магнийорганические соединения
 Методы синтеза магнийорганических соединений Реактивы Гриньяра Mg + RX + n. Et 2 O RMg. X(Et 2 O)n (X = Br, I) [1 a] Можно синтезировать также в ТГФ или смеси ТГФ/петролейный эфир. Для арилхлоридов только ТГФ или смесь ТГФ/петролейный эфир. 8
Методы синтеза магнийорганических соединений Реактивы Гриньяра Mg + RX + n. Et 2 O RMg. X(Et 2 O)n (X = Br, I) [1 a] Можно синтезировать также в ТГФ или смеси ТГФ/петролейный эфир. Для арилхлоридов только ТГФ или смесь ТГФ/петролейный эфир. 8
 Методы синтеза магнийорганических соединений «Гриньяры» с функциональными заместителями Функциональные группы FG = Br, CONR 2, CO 2 Et Замещение йода на Mg. Br – аналогично литиированию галогенарилов 9
Методы синтеза магнийорганических соединений «Гриньяры» с функциональными заместителями Функциональные группы FG = Br, CONR 2, CO 2 Et Замещение йода на Mg. Br – аналогично литиированию галогенарилов 9
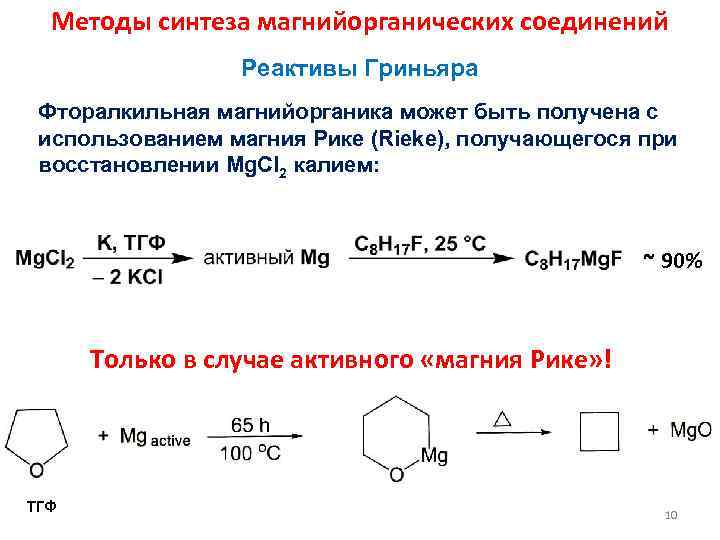 Методы синтеза магнийорганических соединений Реактивы Гриньяра Фторалкильная магнийорганика может быть получена с использованием магния Рике (Rieke), получающегося при восстановлении Mg. Cl 2 калием: ~ 90% Только в случае активного «магния Рике» ! ТГФ 10
Методы синтеза магнийорганических соединений Реактивы Гриньяра Фторалкильная магнийорганика может быть получена с использованием магния Рике (Rieke), получающегося при восстановлении Mg. Cl 2 калием: ~ 90% Только в случае активного «магния Рике» ! ТГФ 10
 Методы синтеза магнийорганических соединений Реактивы Гриньяра Несольватированные «Гриньяры» получены только в аргоновой матрице соконденсацией из газовой фазы: Mg(г) + RX (г) RMg. X (при – 196 о. С) Запомните! Чуть позже к этому вернемся! 11
Методы синтеза магнийорганических соединений Реактивы Гриньяра Несольватированные «Гриньяры» получены только в аргоновой матрице соконденсацией из газовой фазы: Mg(г) + RX (г) RMg. X (при – 196 о. С) Запомните! Чуть позже к этому вернемся! 11
 Методы синтеза магнийорганических соединений Бинарные магний органические соединения Mg. R 2 Трансметаллирование: Mg + R 2 Hg R 2 Mg + Hg [2] 12
Методы синтеза магнийорганических соединений Бинарные магний органические соединения Mg. R 2 Трансметаллирование: Mg + R 2 Hg R 2 Mg + Hg [2] 12
 Методы синтеза магнийорганических соединений Бинарные магний органические соединения Mg. R 2 Равновесие Шленка (Schlenk) Константа равновесия K = 0. 2 в случае Et. Mg. Br Сдвиг равновесия «диспропорционирования» за счет образования осадка: 1, 4 - диоксан 13
Методы синтеза магнийорганических соединений Бинарные магний органические соединения Mg. R 2 Равновесие Шленка (Schlenk) Константа равновесия K = 0. 2 в случае Et. Mg. Br Сдвиг равновесия «диспропорционирования» за счет образования осадка: 1, 4 - диоксан 13
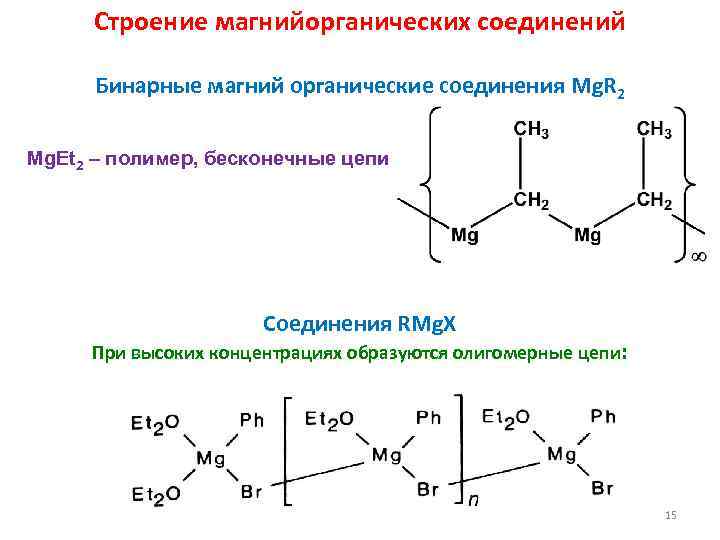 Строение магнийорганических соединений Бинарные магний органические соединения Mg. R 2 Mg. Et 2 – полимер, бесконечные цепи Cоединения RMg. X При высоких концентрациях образуются олигомерные цепи: 15
Строение магнийорганических соединений Бинарные магний органические соединения Mg. R 2 Mg. Et 2 – полимер, бесконечные цепи Cоединения RMg. X При высоких концентрациях образуются олигомерные цепи: 15
 Реакции магнийорганических соединений Поведение реактивов Гриньяра RMg. X в растворе Растворы RMg. X в Et 2 O – слабо, но проводят ток! Электролиз растворов реактивов Гриньяра: Если радикалы достаточно долгоживущие, происходит их рекомбинация путем сдваивания: 17
Реакции магнийорганических соединений Поведение реактивов Гриньяра RMg. X в растворе Растворы RMg. X в Et 2 O – слабо, но проводят ток! Электролиз растворов реактивов Гриньяра: Если радикалы достаточно долгоживущие, происходит их рекомбинация путем сдваивания: 17
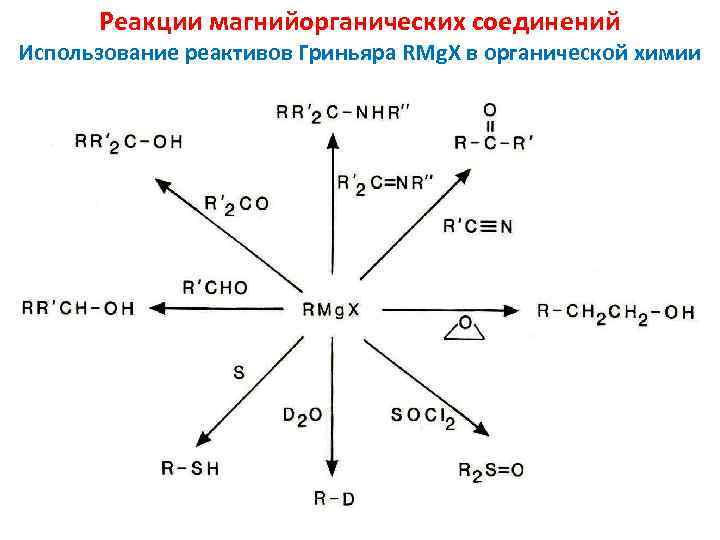 Реакции магнийорганических соединений Использование реактивов Гриньяра RMg. X в органической химии 18
Реакции магнийорганических соединений Использование реактивов Гриньяра RMg. X в органической химии 18
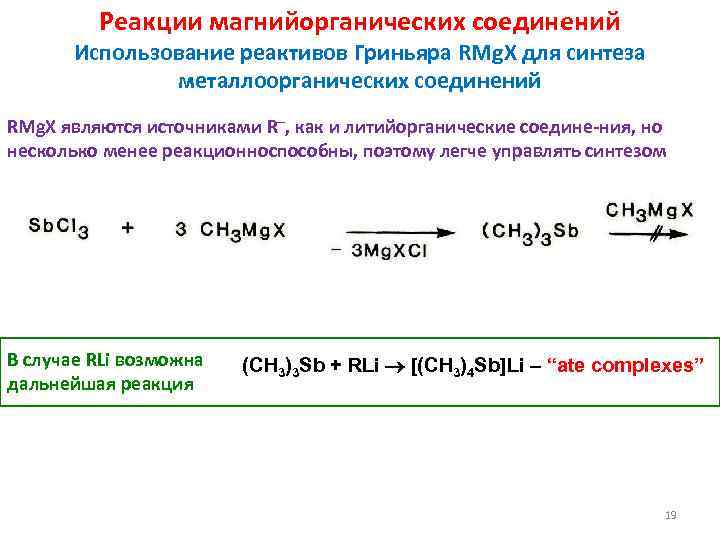 Реакции магнийорганических соединений Использование реактивов Гриньяра RMg. X для синтеза металлоорганических соединений RMg. X являются источниками R , как и литийорганические соедине-ния, но несколько менее реакционноспособны, поэтому легче управлять синтезом В случае RLi возможна дальнейшая реакция (CH 3)3 Sb + RLi [(CH 3)4 Sb]Li – “ate complexes” 19
Реакции магнийорганических соединений Использование реактивов Гриньяра RMg. X для синтеза металлоорганических соединений RMg. X являются источниками R , как и литийорганические соедине-ния, но несколько менее реакционноспособны, поэтому легче управлять синтезом В случае RLi возможна дальнейшая реакция (CH 3)3 Sb + RLi [(CH 3)4 Sb]Li – “ate complexes” 19
 Реакции магнийорганических соединений Бинарные магнийорганические соединения Mg. R 2 В основном: Mg. R 2 – источник R–. Химия подобна той, которуюпроявляют RMg. X Преимущество по сравнению с RMg. X: очень хорошая растворимость в углеводородах (алканы, ароматика). Недостаток: существенно сложнее синтезировать. 20
Реакции магнийорганических соединений Бинарные магнийорганические соединения Mg. R 2 В основном: Mg. R 2 – источник R–. Химия подобна той, которуюпроявляют RMg. X Преимущество по сравнению с RMg. X: очень хорошая растворимость в углеводородах (алканы, ароматика). Недостаток: существенно сложнее синтезировать. 20
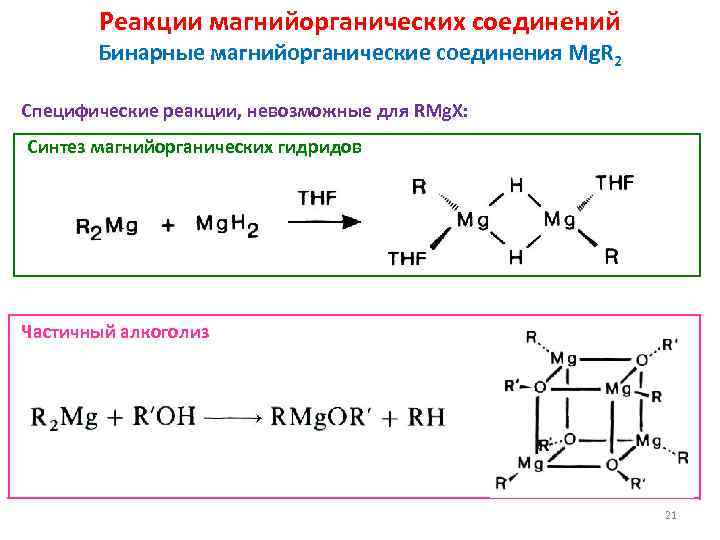 Реакции магнийорганических соединений Бинарные магнийорганические соединения Mg. R 2 Специфические реакции, невозможные для RMg. X: Синтез магнийорганических гидридов Частичный алкоголиз 21
Реакции магнийорганических соединений Бинарные магнийорганические соединения Mg. R 2 Специфические реакции, невозможные для RMg. X: Синтез магнийорганических гидридов Частичный алкоголиз 21
![Сэндвичи [Cp*22 M] Для Ca, Sr, Ba: Для Be и Mg: R 2 M Сэндвичи [Cp*22 M] Для Ca, Sr, Ba: Для Be и Mg: R 2 M](https://present5.com/presentation/5652994_177566267/image-20.jpg) Сэндвичи [Cp*22 M] Для Ca, Sr, Ba: Для Be и Mg: R 2 M + 2 Cp*H 2 RH + Cp*2 M в углеводородах 23
Сэндвичи [Cp*22 M] Для Ca, Sr, Ba: Для Be и Mg: R 2 M + 2 Cp*H 2 RH + Cp*2 M в углеводородах 23
![Сэндвичи [Cp*22 M] особенности строения MCp*2 M Кристалл Газ MF 2 Газ (Диффракция электронов) Сэндвичи [Cp*22 M] особенности строения MCp*2 M Кристалл Газ MF 2 Газ (Диффракция электронов)](https://present5.com/presentation/5652994_177566267/image-21.jpg) Сэндвичи [Cp*22 M] особенности строения MCp*2 M Кристалл Газ MF 2 Газ (Диффракция электронов) (РСА) (Диффракция электронов) Mg 180 180 Ca 147 154 140 149 108 148 100 Sr Ba 131 24
Сэндвичи [Cp*22 M] особенности строения MCp*2 M Кристалл Газ MF 2 Газ (Диффракция электронов) (РСА) (Диффракция электронов) Mg 180 180 Ca 147 154 140 149 108 148 100 Sr Ba 131 24
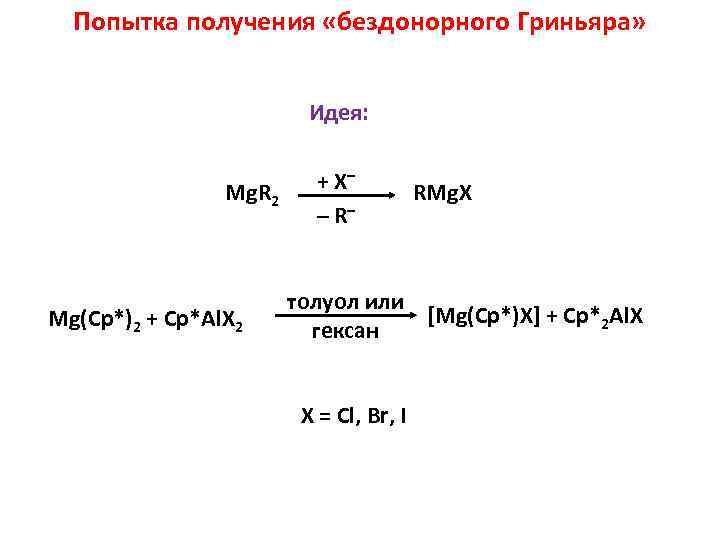 Попытка получения «бездонорного Гриньяра» Идея: Mg. R 2 Mg(Cp*)2 + Cp*Al. X 2 + X– – R– RMg. X толуол или [Mg(Cp*)X] + Cp*2 Al. X гексан X = Cl, Br, I
Попытка получения «бездонорного Гриньяра» Идея: Mg. R 2 Mg(Cp*)2 + Cp*Al. X 2 + X– – R– RMg. X толуол или [Mg(Cp*)X] + Cp*2 Al. X гексан X = Cl, Br, I
![6 Mg(Cp*)2 + 7 Cp*Al. Br 2 [Al. Cp*2]+[Mg 6 Cp*5 Br 8] + 6 Mg(Cp*)2 + 7 Cp*Al. Br 2 [Al. Cp*2]+[Mg 6 Cp*5 Br 8] +](https://present5.com/presentation/5652994_177566267/image-23.jpg) 6 Mg(Cp*)2 + 7 Cp*Al. Br 2 [Al. Cp*2]+[Mg 6 Cp*5 Br 8] + 6 Cp*2 Al. Br [Mg 6 Br 8 Cp*5] 3 Mg(Cp*)2 + 3 Cp*Al. Cl 2 [Al. Cp*2]+[Mg 3 Cp*3 Cl 4] + 2 Cp*2 Al. Cl [Mg 3 Cp*3 Cl 4]
6 Mg(Cp*)2 + 7 Cp*Al. Br 2 [Al. Cp*2]+[Mg 6 Cp*5 Br 8] + 6 Cp*2 Al. Br [Mg 6 Br 8 Cp*5] 3 Mg(Cp*)2 + 3 Cp*Al. Cl 2 [Al. Cp*2]+[Mg 3 Cp*3 Cl 4] + 2 Cp*2 Al. Cl [Mg 3 Cp*3 Cl 4]
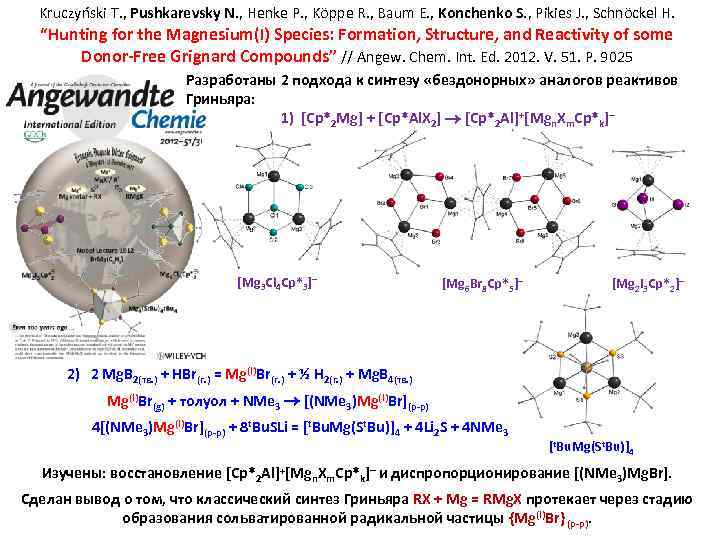 Kruczyński T. , Pushkarevsky N. , Henke P. , Köppe R. , Baum E. , Konchenko S. , Pikies J. , Schnöckel H. “Hunting for the Magnesium(I) Species: Formation, Structure, and Reactivity of some Donor-Free Grignard Compounds” // Angew. Chem. Int. Ed. 2012. V. 51. P. 9025 Разработаны 2 подхода к синтезу «бездонорных» аналогов реактивов Гриньяра: 1) [Cp*2 Mg] + [Cp*Al. X 2] [Cp*2 Al]+[Mgn. Xm. Cp*k] [Mg 3 Cl 4 Cp*3] [Mg 6 Br 8 Cp*5] [Mg 2 I 3 Cp*2] 2) 2 Mg. B 2(тв. ) + HBr(г. ) = Mg(I)Br(г. ) + ½ H 2(г. ) + Mg. B 4(тв. ) Mg(I)Br(g) + толуол + NMe 3 [(NMe 3)Mg(I)Br](р-р) 4[(NMe 3)Mg(I)Br](р-р) + 8 t. Bu. SLi = [t. Bu. Mg(St. Bu)]4 + 4 Li 2 S + 4 NMe 3 [t. Bu. Mg(St. Bu)]4 Изучены: восстановление [Cp*2 Al]+[Mgn. Xm. Cp*k] и диспропорционирование [(NMe 3)Mg. Br]. Сделан вывод о том, что классический синтез Гриньяра RX + Mg = RMg. X протекает через стадию образования сольватированной радикальной частицы {Mg(I)Br} (р-р).
Kruczyński T. , Pushkarevsky N. , Henke P. , Köppe R. , Baum E. , Konchenko S. , Pikies J. , Schnöckel H. “Hunting for the Magnesium(I) Species: Formation, Structure, and Reactivity of some Donor-Free Grignard Compounds” // Angew. Chem. Int. Ed. 2012. V. 51. P. 9025 Разработаны 2 подхода к синтезу «бездонорных» аналогов реактивов Гриньяра: 1) [Cp*2 Mg] + [Cp*Al. X 2] [Cp*2 Al]+[Mgn. Xm. Cp*k] [Mg 3 Cl 4 Cp*3] [Mg 6 Br 8 Cp*5] [Mg 2 I 3 Cp*2] 2) 2 Mg. B 2(тв. ) + HBr(г. ) = Mg(I)Br(г. ) + ½ H 2(г. ) + Mg. B 4(тв. ) Mg(I)Br(g) + толуол + NMe 3 [(NMe 3)Mg(I)Br](р-р) 4[(NMe 3)Mg(I)Br](р-р) + 8 t. Bu. SLi = [t. Bu. Mg(St. Bu)]4 + 4 Li 2 S + 4 NMe 3 [t. Bu. Mg(St. Bu)]4 Изучены: восстановление [Cp*2 Al]+[Mgn. Xm. Cp*k] и диспропорционирование [(NMe 3)Mg. Br]. Сделан вывод о том, что классический синтез Гриньяра RX + Mg = RMg. X протекает через стадию образования сольватированной радикальной частицы {Mg(I)Br} (р-р).
 Как создать связь металл-металл? 28
Как создать связь металл-металл? 28
 Вариант 1: добавим избыток восстановителя, но не добавим лиганда Mn+ + ne = Mn+ M 0 M 0 Mn+ M 0 Mn+ M 0 Mn+ Mn+ M 0
Вариант 1: добавим избыток восстановителя, но не добавим лиганда Mn+ + ne = Mn+ M 0 M 0 Mn+ M 0 Mn+ M 0 Mn+ Mn+ M 0
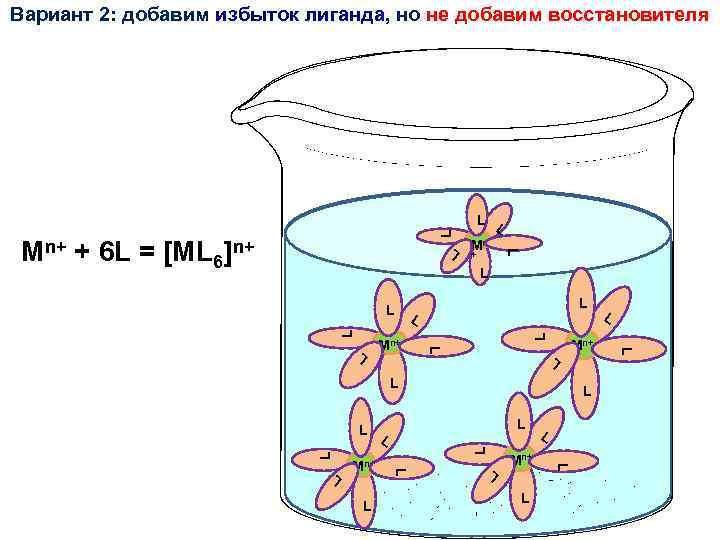 Вариант 2: добавим избыток лиганда, но не добавим восстановителя L Mn+ L M L L n+ L L L Mn+ n+ L M L L n+ ML L L Mn+ L L n+ n+ MM Mn+L M L L L Mn+ Mn+ n+ L Mn+ L L L + L Mn+ L L + 6 L = [ML 6 ]n+ L L n+ n M M L Mn+
Вариант 2: добавим избыток лиганда, но не добавим восстановителя L Mn+ L M L L n+ L L L Mn+ n+ L M L L n+ ML L L Mn+ L L n+ n+ MM Mn+L M L L L Mn+ Mn+ n+ L Mn+ L L L + L Mn+ L L + 6 L = [ML 6 ]n+ L L n+ n M M L Mn+
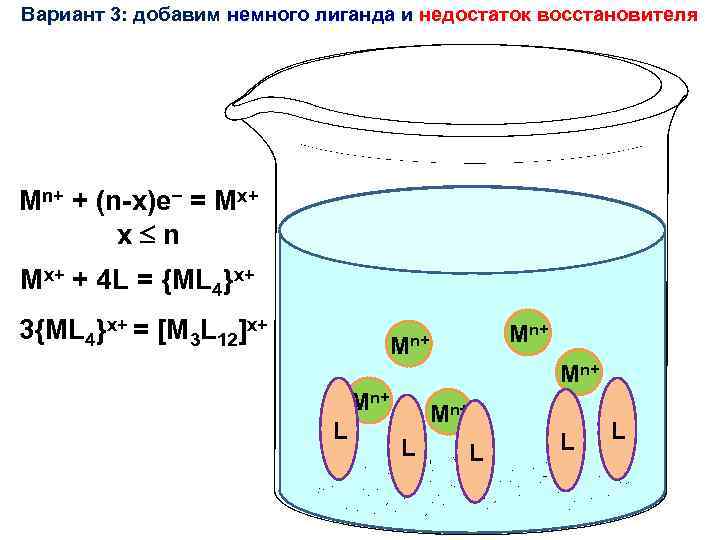 Вариант 3: добавим немного лиганда и недостаток восстановителя Mn+ + (n-x)e = Mx+ x n n+ Mn+ L L L n+ L x+ Mx+ x+ M Mn+ L L Mn+M M Mn+ L M L L L Mn+ Mx+ L L x+ L Mn+ n+ L L Mx+ M Mn+ L Mn+ n+ L M 3{ML 4}x+ = [M 3 L 12]x+ n+ L Mx+ + 4 L = {ML 4}x+ M M Кластер. M !!! n+ ML L
Вариант 3: добавим немного лиганда и недостаток восстановителя Mn+ + (n-x)e = Mx+ x n n+ Mn+ L L L n+ L x+ Mx+ x+ M Mn+ L L Mn+M M Mn+ L M L L L Mn+ Mx+ L L x+ L Mn+ n+ L L Mx+ M Mn+ L Mn+ n+ L M 3{ML 4}x+ = [M 3 L 12]x+ n+ L Mx+ + 4 L = {ML 4}x+ M M Кластер. M !!! n+ ML L
 Вопросы, которые нужно решить при планировании синтеза кластера 1. Из чего исходить, чтобы получить нужные фрагменты? 2. Что есть «недостаток» восстановителя и «немного» лиганда? 3. Какие среду и условия нужно выбрать для проведения синтеза?
Вопросы, которые нужно решить при планировании синтеза кластера 1. Из чего исходить, чтобы получить нужные фрагменты? 2. Что есть «недостаток» восстановителя и «немного» лиганда? 3. Какие среду и условия нужно выбрать для проведения синтеза?
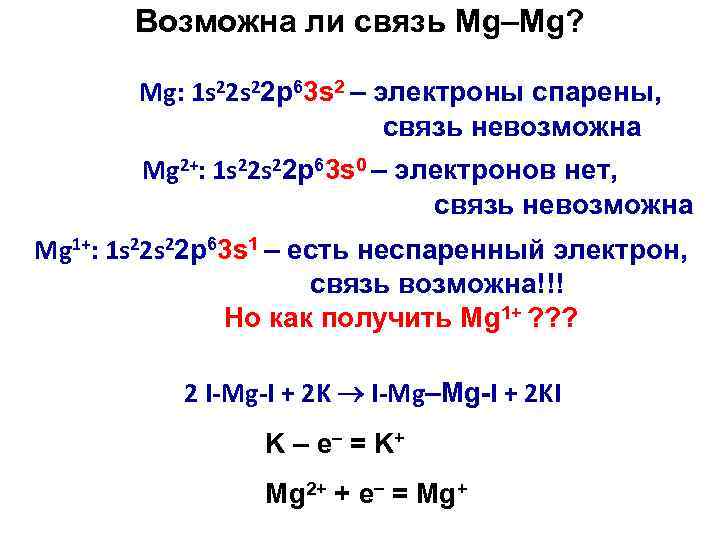 Возможна ли связь Mg–Mg? Mg: 1 s 22 p 63 s 2 – электроны спарены, связь невозможна Mg 2+: 1 s 22 p 63 s 0 – электронов нет, связь невозможна Mg 1+: 1 s 22 p 63 s 1 – есть неспаренный электрон, связь возможна!!! Но как получить Mg 1+ ? ? ? 2 I-Mg-I + 2 K I-Mg–Mg-I + 2 KI K – e = K + Mg 2+ + e = Mg+
Возможна ли связь Mg–Mg? Mg: 1 s 22 p 63 s 2 – электроны спарены, связь невозможна Mg 2+: 1 s 22 p 63 s 0 – электронов нет, связь невозможна Mg 1+: 1 s 22 p 63 s 1 – есть неспаренный электрон, связь возможна!!! Но как получить Mg 1+ ? ? ? 2 I-Mg-I + 2 K I-Mg–Mg-I + 2 KI K – e = K + Mg 2+ + e = Mg+
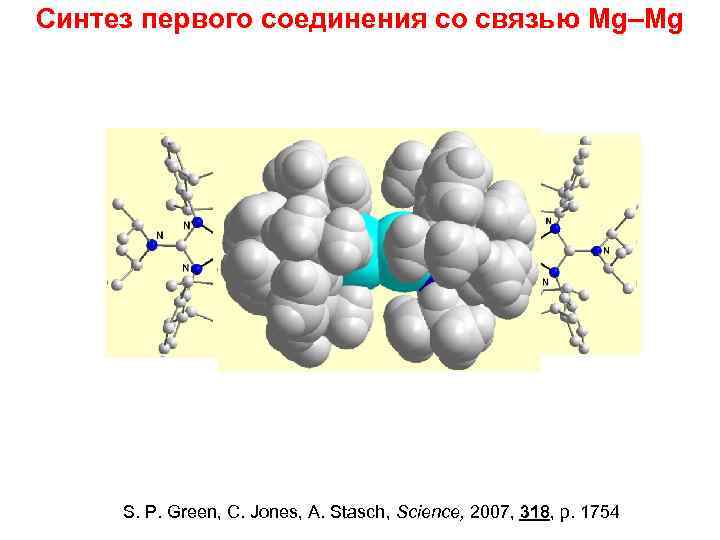 Синтез первого соединения со связью Mg–Mg 2 KI 2 K S. P. Green, C. Jones, A. Stasch, Science, 2007, 318, p. 1754
Синтез первого соединения со связью Mg–Mg 2 KI 2 K S. P. Green, C. Jones, A. Stasch, Science, 2007, 318, p. 1754
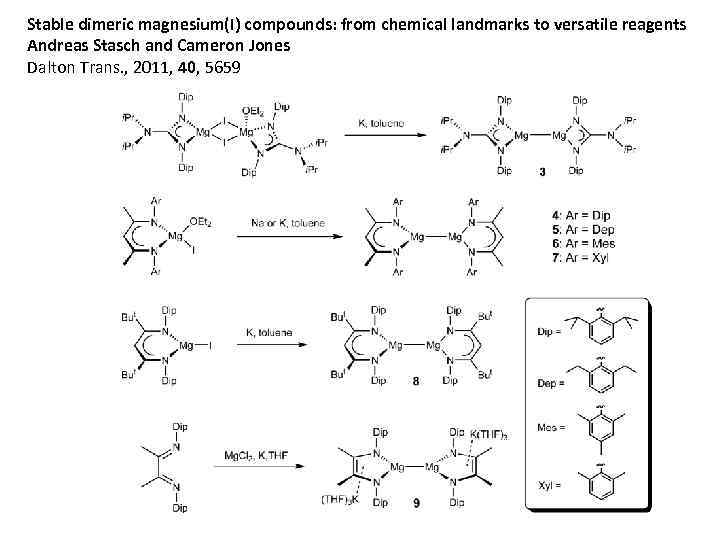 Stable dimeric magnesium(I) compounds: from chemical landmarks to versatile reagents Andreas Stasch and Cameron Jones Dalton Trans. , 2011, 40, 5659
Stable dimeric magnesium(I) compounds: from chemical landmarks to versatile reagents Andreas Stasch and Cameron Jones Dalton Trans. , 2011, 40, 5659
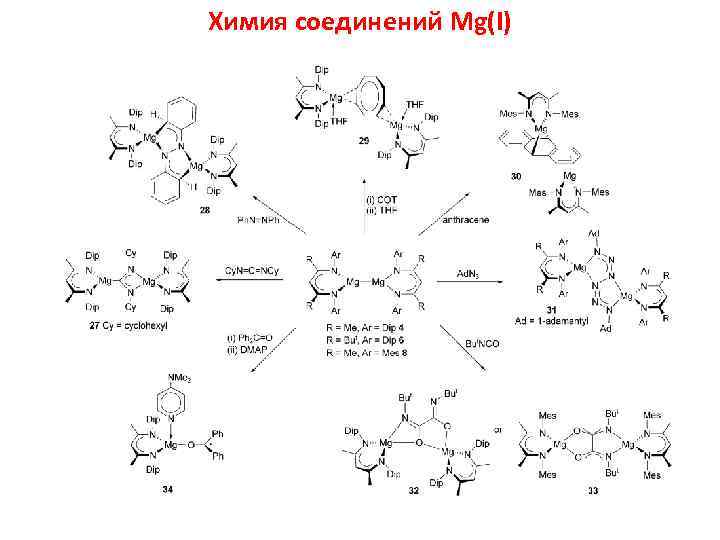 Химия соединений Mg(I)
Химия соединений Mg(I)


