Металлокомплексный катализ.посл.исправленный.ppt
- Количество слайдов: 61
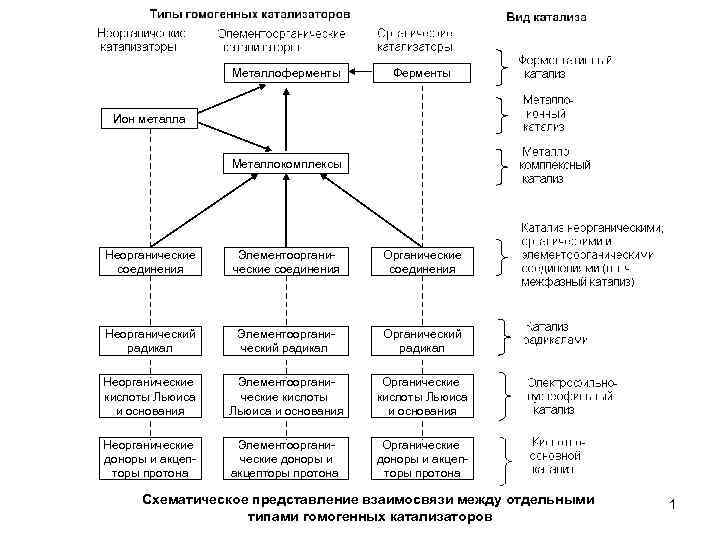 Металлоферменты Ферменты Ион металла Металлокомплексы Неорганические соединения Элементоорганические соединения Органические соединения Неорганический радикал Элементоорганический радикал Органический радикал Неорганические кислоты Льюиса и основания Элементоорганические кислоты Льюиса и основания Органические кислоты Льюиса и основания Неорганические доноры и акцепторы протона Элементоорганические доноры и акцепторы протона Органические доноры и акцепторы протона Схематическое представление взаимосвязи между отдельными типами гомогенных катализаторов 1
Металлоферменты Ферменты Ион металла Металлокомплексы Неорганические соединения Элементоорганические соединения Органические соединения Неорганический радикал Элементоорганический радикал Органический радикал Неорганические кислоты Льюиса и основания Элементоорганические кислоты Льюиса и основания Органические кислоты Льюиса и основания Неорганические доноры и акцепторы протона Элементоорганические доноры и акцепторы протона Органические доноры и акцепторы протона Схематическое представление взаимосвязи между отдельными типами гомогенных катализаторов 1
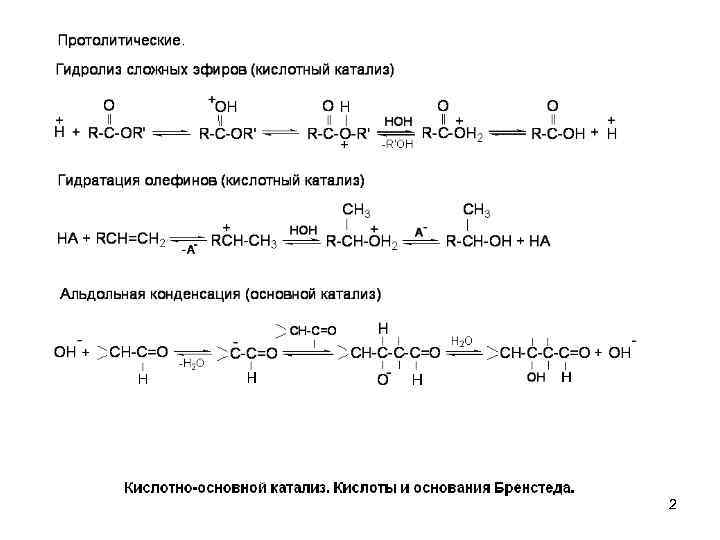 2
2
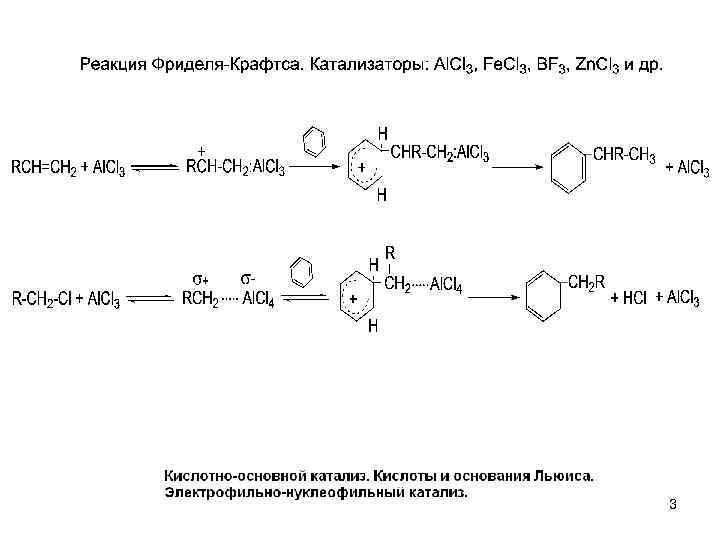 3
3
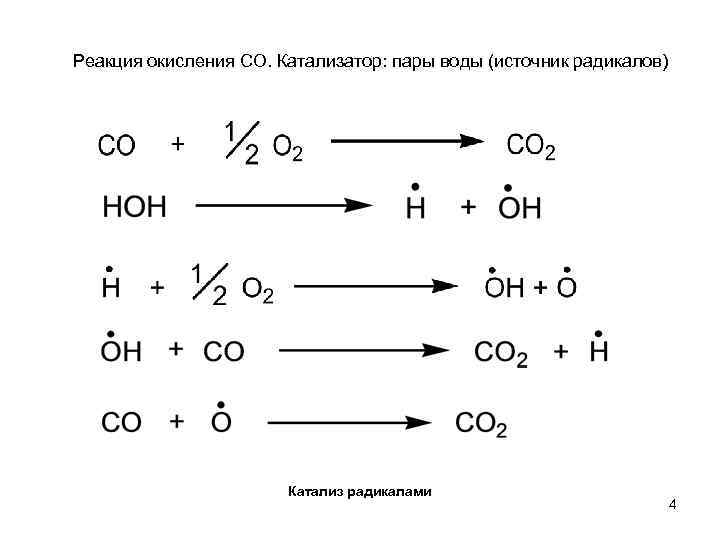 Реакция окисления СО. Катализатор: пары воды (источник радикалов) Катализ радикалами 4
Реакция окисления СО. Катализатор: пары воды (источник радикалов) Катализ радикалами 4
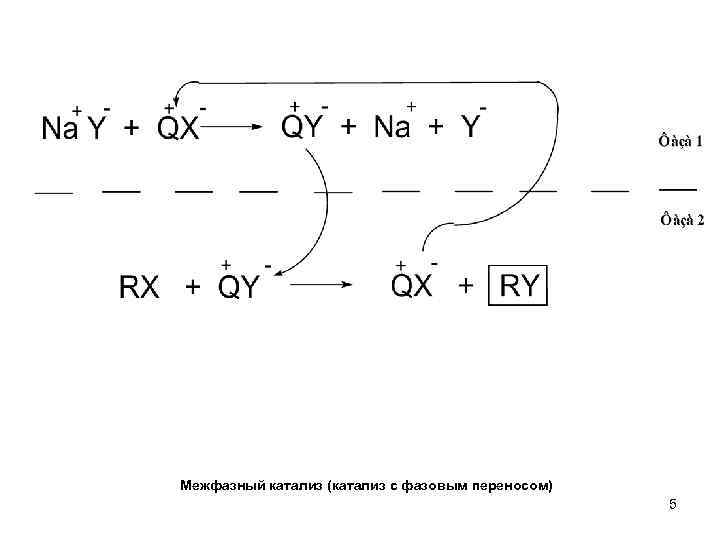 Межфазный катализ (катализ с фазовым переносом) 5
Межфазный катализ (катализ с фазовым переносом) 5
 Начало зарождения: Конец 30 -х годов ХХ в. Работы О. Релена (оксосинтез) и В. Реппе (синтезы Реппе). Начало интенсивных исследований и развития: 50 -60 годы ХХ в. Открытие Вакерпроцесса. Открытие катализаторов Циглера-Натта. Бурное развитие в эти годы химии металлоорганических соединений (синтез ферроцена-дициклопентадиенилжелеза). Координационно-комплексный катализ. Металлокомплексный катализ 6
Начало зарождения: Конец 30 -х годов ХХ в. Работы О. Релена (оксосинтез) и В. Реппе (синтезы Реппе). Начало интенсивных исследований и развития: 50 -60 годы ХХ в. Открытие Вакерпроцесса. Открытие катализаторов Циглера-Натта. Бурное развитие в эти годы химии металлоорганических соединений (синтез ферроцена-дициклопентадиенилжелеза). Координационно-комплексный катализ. Металлокомплексный катализ 6
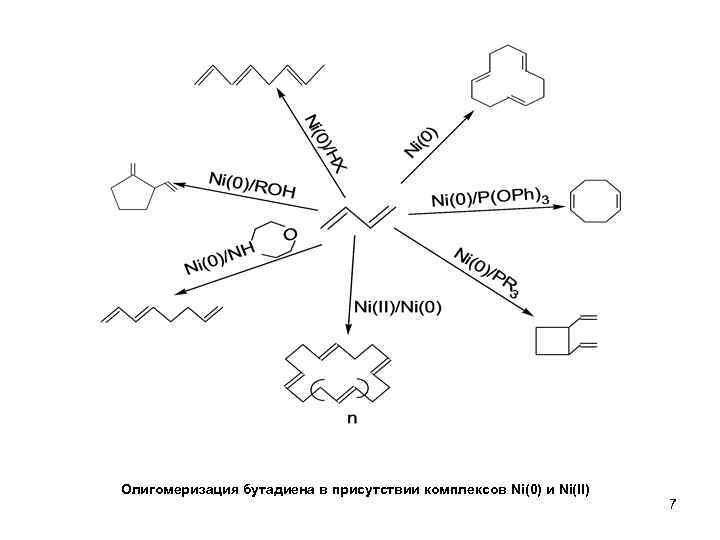 Олигомеризация бутадиена в присутствии комплексов Ni(0) и Ni(II) 7
Олигомеризация бутадиена в присутствии комплексов Ni(0) и Ni(II) 7
 Координационная теория Альфреда Вернера (1893 г. ) Присуждение Нобелевской премии (1913 г. ) Основные понятия. Центральный ион (или атом). Лиганда. Внутренняя сфера комплекса. Внешняя сфера комплекса. Координационное число. Комплексные соединения – химические соединения, состоящие из ионов или молекул, способные к самостоятельному существованию, к образующиеся в результате координации лигандов к центральному атому. Комплексные соединения могут существовать и сохранять свою структуру в растворах, в кристаллах и, в некоторых случаях, в газообразном состоянии. Известно, что квантовая механика является наиболее общей физической теорией, приложимой ко всем явлениям микро- и макромира. Аналогично координационная теория является общей теорией образования и строения химических соединений. Как в области синтеза, так и в области изучения строения соединении и химической связи химия комплексов объединяет в себе принципы теоретической, неорганической, физической и органической химии. Координационные свойства проявляются всеми элементами. Но у некоторых из них, например у переходных металлов, способность к комплексообразованию настолько велика, что химия этих металлов является, по существу, химией их комплексных соединений. Комплексные соединения. 8
Координационная теория Альфреда Вернера (1893 г. ) Присуждение Нобелевской премии (1913 г. ) Основные понятия. Центральный ион (или атом). Лиганда. Внутренняя сфера комплекса. Внешняя сфера комплекса. Координационное число. Комплексные соединения – химические соединения, состоящие из ионов или молекул, способные к самостоятельному существованию, к образующиеся в результате координации лигандов к центральному атому. Комплексные соединения могут существовать и сохранять свою структуру в растворах, в кристаллах и, в некоторых случаях, в газообразном состоянии. Известно, что квантовая механика является наиболее общей физической теорией, приложимой ко всем явлениям микро- и макромира. Аналогично координационная теория является общей теорией образования и строения химических соединений. Как в области синтеза, так и в области изучения строения соединении и химической связи химия комплексов объединяет в себе принципы теоретической, неорганической, физической и органической химии. Координационные свойства проявляются всеми элементами. Но у некоторых из них, например у переходных металлов, способность к комплексообразованию настолько велика, что химия этих металлов является, по существу, химией их комплексных соединений. Комплексные соединения. 8
 Комплексные соединения. Исторические сведения История координационной химии – это фактически история самой химии, поскольку до определенного времени человечество оперировало с комплексными соединениями, даже не подозревая об этом. 1 период. С древнейших времен до начало XVIII в. ученые и ремесленники (аптекари, красильщики, кожевники и др. ) использовали и даже синтезировали комплексные соединения, хотя и неосознанно. 2 период. С начало XVIII в. до 1893 г. идет целенаправленный синтез комплексных соединений и появляются многочисленные теории, стремящиеся объяснить их строение и свойства. 3 период. С 1893 по 1940 г – создание, обоснование и победа координационной теории А. Вернера. 4 период. Современный с 1940 по настоящее время – это период укрепления и всестороннего развития координационной теории с использованием достижений и успехов химии, физики и математики. В этот период главной целью является выяснение природы химической связи в комплексных соединениях. 9
Комплексные соединения. Исторические сведения История координационной химии – это фактически история самой химии, поскольку до определенного времени человечество оперировало с комплексными соединениями, даже не подозревая об этом. 1 период. С древнейших времен до начало XVIII в. ученые и ремесленники (аптекари, красильщики, кожевники и др. ) использовали и даже синтезировали комплексные соединения, хотя и неосознанно. 2 период. С начало XVIII в. до 1893 г. идет целенаправленный синтез комплексных соединений и появляются многочисленные теории, стремящиеся объяснить их строение и свойства. 3 период. С 1893 по 1940 г – создание, обоснование и победа координационной теории А. Вернера. 4 период. Современный с 1940 по настоящее время – это период укрепления и всестороннего развития координационной теории с использованием достижений и успехов химии, физики и математики. В этот период главной целью является выяснение природы химической связи в комплексных соединениях. 9
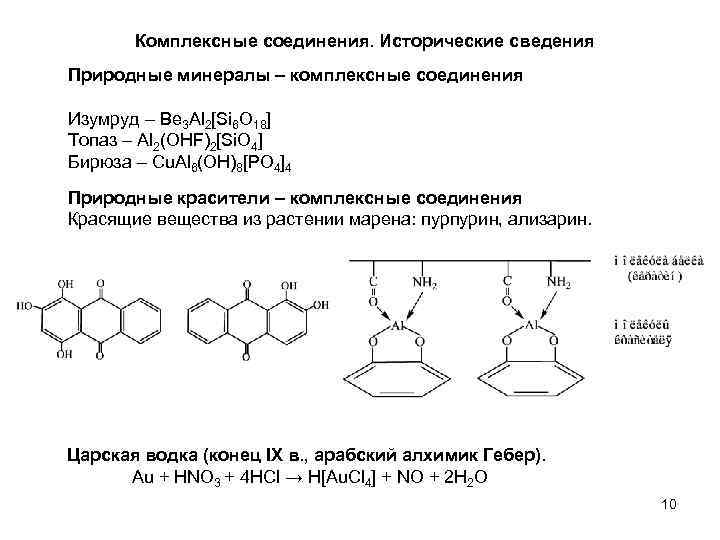 Комплексные соединения. Исторические сведения Природные минералы – комплексные соединения Изумруд – Be 3 Al 2[Si 6 O 18] Топаз – Al 2(OHF)2[Si. O 4] Бирюза – Cu. Al 6(OH)8[PO 4]4 Природные красители – комплексные соединения Красящие вещества из растении марена: пурпурин, ализарин. Царская водка (конец IX в. , арабский алхимик Гебер). Au + HNO 3 + 4 HCl → H[Au. Cl 4] + NO + 2 H 2 O 10
Комплексные соединения. Исторические сведения Природные минералы – комплексные соединения Изумруд – Be 3 Al 2[Si 6 O 18] Топаз – Al 2(OHF)2[Si. O 4] Бирюза – Cu. Al 6(OH)8[PO 4]4 Природные красители – комплексные соединения Красящие вещества из растении марена: пурпурин, ализарин. Царская водка (конец IX в. , арабский алхимик Гебер). Au + HNO 3 + 4 HCl → H[Au. Cl 4] + NO + 2 H 2 O 10
![Рациональная номенклатура комплексных соединений [Cu. En 2]Cl 2 – хлорид бис(этилендиамин) меди (II) K Рациональная номенклатура комплексных соединений [Cu. En 2]Cl 2 – хлорид бис(этилендиамин) меди (II) K](https://present5.com/presentation/3/209208944_248430947.pdf-img/209208944_248430947.pdf-11.jpg) Рациональная номенклатура комплексных соединений [Cu. En 2]Cl 2 – хлорид бис(этилендиамин) меди (II) K 4[Fe(CN)6] – гексациано (II) феррат калия Na[Co(CO]4] – тетракарбонил (-I) кобальтат натрия [Pt(NH 3)3 NO 2 Cl]SO 4 – сульфат хлоронитротриамминплатины (IV) [Pt. N 2 H 5 NH 3 Cl]Cl 2 – хлорид хлороаммингидразиниумплатины (II) [Co(NH 3)3(NO 2)3] – тринитротриамминкобальт Pd. Cl 2(PPh 3)2 – бисхлоридобис(трифенилфосфин)палладий Pd(PPh 3)4 – тетракис(трифенилфосфин)палладий При написании формул комплексных соединений в квадратных скобках первыми пишут комплексообразователь, потом лиганды в порядке, обратном их перечислению при названии. Внутри квадратных скобок могут быть другие скобки, например: [Ni{P(OC 6 H 4 CH 3)3}3] – трис(три-о-толил)фосфитникель. 11
Рациональная номенклатура комплексных соединений [Cu. En 2]Cl 2 – хлорид бис(этилендиамин) меди (II) K 4[Fe(CN)6] – гексациано (II) феррат калия Na[Co(CO]4] – тетракарбонил (-I) кобальтат натрия [Pt(NH 3)3 NO 2 Cl]SO 4 – сульфат хлоронитротриамминплатины (IV) [Pt. N 2 H 5 NH 3 Cl]Cl 2 – хлорид хлороаммингидразиниумплатины (II) [Co(NH 3)3(NO 2)3] – тринитротриамминкобальт Pd. Cl 2(PPh 3)2 – бисхлоридобис(трифенилфосфин)палладий Pd(PPh 3)4 – тетракис(трифенилфосфин)палладий При написании формул комплексных соединений в квадратных скобках первыми пишут комплексообразователь, потом лиганды в порядке, обратном их перечислению при названии. Внутри квадратных скобок могут быть другие скобки, например: [Ni{P(OC 6 H 4 CH 3)3}3] – трис(три-о-толил)фосфитникель. 11
 Координационное соединение. Координационная связь Координационное соединение или координационная связь может образоваться между любым атомом или ионом, способным принять пару электронов (акцептор) и другим атомом или ионом, который может предоставить для совместного обладания эту пару (донор). Резкой границы между атомами-донорами и атомами-акцепторами провести нельзя. Многие элементы проявляют донорно-акцептурную двойственность, выполняя в одних соединениях роль комплексообразователя, а в других – лиганда. Например, в комплексах Na 2[SS 2] и Na 2[Sn. S 3]; K[I(I 2)3] и K 2[Hg. I 4] ионы S 2 - и I- являются или центральными атомами, или донорами. Иногда в одном и том же соединении центральный атом может быть одновременно и акцептором, принимая электронные пары от лигандов, и донором, участвуя в обратном процессе образования -связи. По этой же причине и лиганд проявляет донорно-акцепторную двойственность. Согласно электронной теории кислот и оснований Льюиса, реакции образования многих комплексов можно отнести к кислотно-основными взаимодействиям. В соответствии с этой теорией, кислотами называют вещества, молекулы которых способны присоединять неподеленные пары электронов (акцепторы), а основания – вещества, способные их давать (доноры). В результаты кислотно-основной реакции образуются координационные связи и координационное соединение: А + кислота (акцептор) Мn+ : В → основание (донор) + L А: В координационное соединение → MLn+ 12
Координационное соединение. Координационная связь Координационное соединение или координационная связь может образоваться между любым атомом или ионом, способным принять пару электронов (акцептор) и другим атомом или ионом, который может предоставить для совместного обладания эту пару (донор). Резкой границы между атомами-донорами и атомами-акцепторами провести нельзя. Многие элементы проявляют донорно-акцептурную двойственность, выполняя в одних соединениях роль комплексообразователя, а в других – лиганда. Например, в комплексах Na 2[SS 2] и Na 2[Sn. S 3]; K[I(I 2)3] и K 2[Hg. I 4] ионы S 2 - и I- являются или центральными атомами, или донорами. Иногда в одном и том же соединении центральный атом может быть одновременно и акцептором, принимая электронные пары от лигандов, и донором, участвуя в обратном процессе образования -связи. По этой же причине и лиганд проявляет донорно-акцепторную двойственность. Согласно электронной теории кислот и оснований Льюиса, реакции образования многих комплексов можно отнести к кислотно-основными взаимодействиям. В соответствии с этой теорией, кислотами называют вещества, молекулы которых способны присоединять неподеленные пары электронов (акцепторы), а основания – вещества, способные их давать (доноры). В результаты кислотно-основной реакции образуются координационные связи и координационное соединение: А + кислота (акцептор) Мn+ : В → основание (донор) + L А: В координационное соединение → MLn+ 12
 Центральные атомы. Металлы Природа центрального атома определяет многие свойства комплексного соединения: цвет, устойчивость, магнетизм и др. Наиболее важными характеристиками центрального атома являются: электронная конфигурация, размер, степень окисления, ионный потенциал (отношение заряда иона к его радиусу). В зависимости от электронной конфигурации металлы делятся на несколько групп. В одну группу можно объединить металлы, которые в своих комплексах имеют конфигурацию инертного газа ns 2 np 6, например щелочные и щелочноземельные металлы, Be 2+, Mg 2+, Al 3+, Sc 3+, лантаноиды и актиноиды в состоянии окисления +3, Ti 4+, Zr 4+, V 5+, Nb 5+, Cr 6+, Mo 6+, Mn 7+, Re 7+, Os 8+, Ru 8+ и др. Для них характерно образование наиболее прочных комплексов с кислород- и фторсодержащими лигандами. Другие металлы, имеющие в своих комплексах конфигурацию псевдоинертного газа, т. е. (n-1)d 10, где n=4, 5 или 6 (например, Ag+, Cu+, Au, Zn 2+, Cd 2+ и др. ) проявляют наибольшую тенденцию к координации с азотсодержащими лигандами. Самая большая и разнообразная группа комплексообразователей включает атомы или ионы металлов, имеющих в своих комплексах не полностью заполненные d-орбитали, т. е. (n-1)d 1 -9. В эту группу попадают переходные металлы со всеми степенями окисления, кроме названных выше. Они образуют комплексы как с кислород-, азотсодержащими лигандами, так и с содержащими серу, фосфор и атомы других элементов. 13
Центральные атомы. Металлы Природа центрального атома определяет многие свойства комплексного соединения: цвет, устойчивость, магнетизм и др. Наиболее важными характеристиками центрального атома являются: электронная конфигурация, размер, степень окисления, ионный потенциал (отношение заряда иона к его радиусу). В зависимости от электронной конфигурации металлы делятся на несколько групп. В одну группу можно объединить металлы, которые в своих комплексах имеют конфигурацию инертного газа ns 2 np 6, например щелочные и щелочноземельные металлы, Be 2+, Mg 2+, Al 3+, Sc 3+, лантаноиды и актиноиды в состоянии окисления +3, Ti 4+, Zr 4+, V 5+, Nb 5+, Cr 6+, Mo 6+, Mn 7+, Re 7+, Os 8+, Ru 8+ и др. Для них характерно образование наиболее прочных комплексов с кислород- и фторсодержащими лигандами. Другие металлы, имеющие в своих комплексах конфигурацию псевдоинертного газа, т. е. (n-1)d 10, где n=4, 5 или 6 (например, Ag+, Cu+, Au, Zn 2+, Cd 2+ и др. ) проявляют наибольшую тенденцию к координации с азотсодержащими лигандами. Самая большая и разнообразная группа комплексообразователей включает атомы или ионы металлов, имеющих в своих комплексах не полностью заполненные d-орбитали, т. е. (n-1)d 1 -9. В эту группу попадают переходные металлы со всеми степенями окисления, кроме названных выше. Они образуют комплексы как с кислород-, азотсодержащими лигандами, так и с содержащими серу, фосфор и атомы других элементов. 13
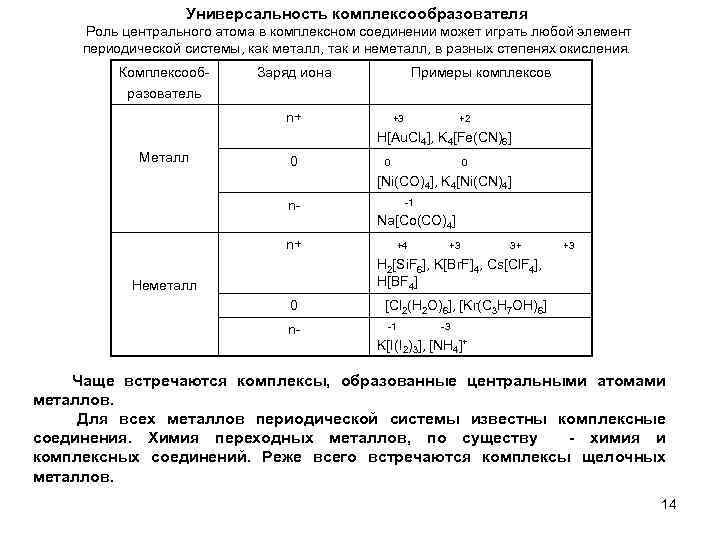 Универсальность комплексообразователя Роль центрального атома в комплексном соединении может играть любой элемент периодической системы, как металл, так и неметалл, в разных степенях окисления. Комплексообразователь Заряд иона Примеры комплексов n+ +3 +2 H[Au. Cl 4], K 4[Fe(CN)6] Металл 0 0 0 [Ni(CO)4], K 4[Ni(CN)4] nn+ -1 Na[Co(CO)4] +4 +3 3+ +3 H 2[Si. F 6], K[Br. F]4, Cs[Cl. F 4], H[BF 4] Неметалл 0 n- [Cl 2(H 2 O)6], [Kr(C 3 H 7 OH)6] -1 -3 K[I(I 2)3], [NH 4]+ Чаще встречаются комплексы, образованные центральными атомами металлов. Для всех металлов периодической системы известны комплексные соединения. Химия переходных металлов, по существу - химия и комплексных соединений. Реже всего встречаются комплексы щелочных металлов. 14
Универсальность комплексообразователя Роль центрального атома в комплексном соединении может играть любой элемент периодической системы, как металл, так и неметалл, в разных степенях окисления. Комплексообразователь Заряд иона Примеры комплексов n+ +3 +2 H[Au. Cl 4], K 4[Fe(CN)6] Металл 0 0 0 [Ni(CO)4], K 4[Ni(CN)4] nn+ -1 Na[Co(CO)4] +4 +3 3+ +3 H 2[Si. F 6], K[Br. F]4, Cs[Cl. F 4], H[BF 4] Неметалл 0 n- [Cl 2(H 2 O)6], [Kr(C 3 H 7 OH)6] -1 -3 K[I(I 2)3], [NH 4]+ Чаще встречаются комплексы, образованные центральными атомами металлов. Для всех металлов периодической системы известны комплексные соединения. Химия переходных металлов, по существу - химия и комплексных соединений. Реже всего встречаются комплексы щелочных металлов. 14
 Центральные атомы. Неметаллы также обладают способностью образовывать комплексы, выполняя функцию центрального атома. Так, ион аммония можно рассматривать как комплекс азота [NH 4]+, ион гидроксония – как ион, содержащий в качестве центрального атома кислород [OH 3]+ и т. д. Кислород может иметь различные координационные числа: два, например в соединении [O(CH 3)2]+, три в ионах [OH 3]+, [R 2 OH]+, [ROH 2]+, [R 3 O]+. Трехфтористый бор является одним из самых активных акцепторов, т. е. сильной кислотой по Льюису. Он легко соединятся с водой, эфирами, спиртами, аминами, фосфорными и т. д. , образуя продукты присоединения, например: Даже для прежде «неприступных» инертных газов получены комплексные соединения. Ксенон образует довольно устойчивые фторидные комплексы: Октафтороксенаты рубидия и цезия являются наиболее устойчивыми из полученных в настоящее время соединений инертных газов. Они разлагаются при температуре выше 4000 С. 15
Центральные атомы. Неметаллы также обладают способностью образовывать комплексы, выполняя функцию центрального атома. Так, ион аммония можно рассматривать как комплекс азота [NH 4]+, ион гидроксония – как ион, содержащий в качестве центрального атома кислород [OH 3]+ и т. д. Кислород может иметь различные координационные числа: два, например в соединении [O(CH 3)2]+, три в ионах [OH 3]+, [R 2 OH]+, [ROH 2]+, [R 3 O]+. Трехфтористый бор является одним из самых активных акцепторов, т. е. сильной кислотой по Льюису. Он легко соединятся с водой, эфирами, спиртами, аминами, фосфорными и т. д. , образуя продукты присоединения, например: Даже для прежде «неприступных» инертных газов получены комплексные соединения. Ксенон образует довольно устойчивые фторидные комплексы: Октафтороксенаты рубидия и цезия являются наиболее устойчивыми из полученных в настоящее время соединений инертных газов. Они разлагаются при температуре выше 4000 С. 15
 Дентатность лигандов. Амбидентатные лиганды. Число донорных атомов в лиганде определяет его координационную емкость или дентатность. Полидентантные хелатные лиганды. Название Координационная емкость Диметилглиоксим 2 Триаминопропан 3 Триаминотриэтиламин 4 ЭДТА 6 Хелатные комплексы Формула Амбидентантные лиганды NO 2 -, SCN-, CO, CN-, (CH 3)2 SO, (NH 2)2 CS. M–ONO – нитритокомплесксы M–SCN – тиоцианитные комплесксы M-NO 2 – нитрокомплексы M-NCS – изотиоцианатые комплексы 16
Дентатность лигандов. Амбидентатные лиганды. Число донорных атомов в лиганде определяет его координационную емкость или дентатность. Полидентантные хелатные лиганды. Название Координационная емкость Диметилглиоксим 2 Триаминопропан 3 Триаминотриэтиламин 4 ЭДТА 6 Хелатные комплексы Формула Амбидентантные лиганды NO 2 -, SCN-, CO, CN-, (CH 3)2 SO, (NH 2)2 CS. M–ONO – нитритокомплесксы M–SCN – тиоцианитные комплесксы M-NO 2 – нитрокомплексы M-NCS – изотиоцианатые комплексы 16
 Мягкие и жесткие лиганды Основность лиганда – это его способность предоставлять металлу неподеленную пару электронов. По этой характеристике лиганды делят на мягкие, способные к поляризации, и жесткие, которые не поляризуются. Самые жесткие лиганды содержат в качестве донорных атомов фтор, кислород и азот. Чем больше основность лиганда, тем более прочные комплексы он образует. У мягких лигандов доноры – элементы V, VI и VII групп, начиная с третьего периода и ниже (Cl-, Br-, I-, S 2 -, Se 2 -, P 3 -, As 3 - и др. ). У них имеются свободные dорбитали и они могут принимать электроны от металла с образованием -связи, в этом проявляется их донорно-акцепторный амфотерный характер. Электростатическое влияние заряда и размеров лиганда на устойчивость комплексов очень важно. Например, небольшие фторид-ионы образуют более устойчивые комплексы. Большой перхлорат-ион CCO 4 с зарядом -1 проявляет очень слабую тенденцию к комплексообразованию с металлами. 17
Мягкие и жесткие лиганды Основность лиганда – это его способность предоставлять металлу неподеленную пару электронов. По этой характеристике лиганды делят на мягкие, способные к поляризации, и жесткие, которые не поляризуются. Самые жесткие лиганды содержат в качестве донорных атомов фтор, кислород и азот. Чем больше основность лиганда, тем более прочные комплексы он образует. У мягких лигандов доноры – элементы V, VI и VII групп, начиная с третьего периода и ниже (Cl-, Br-, I-, S 2 -, Se 2 -, P 3 -, As 3 - и др. ). У них имеются свободные dорбитали и они могут принимать электроны от металла с образованием -связи, в этом проявляется их донорно-акцепторный амфотерный характер. Электростатическое влияние заряда и размеров лиганда на устойчивость комплексов очень важно. Например, небольшие фторид-ионы образуют более устойчивые комплексы. Большой перхлорат-ион CCO 4 с зарядом -1 проявляет очень слабую тенденцию к комплексообразованию с металлами. 17
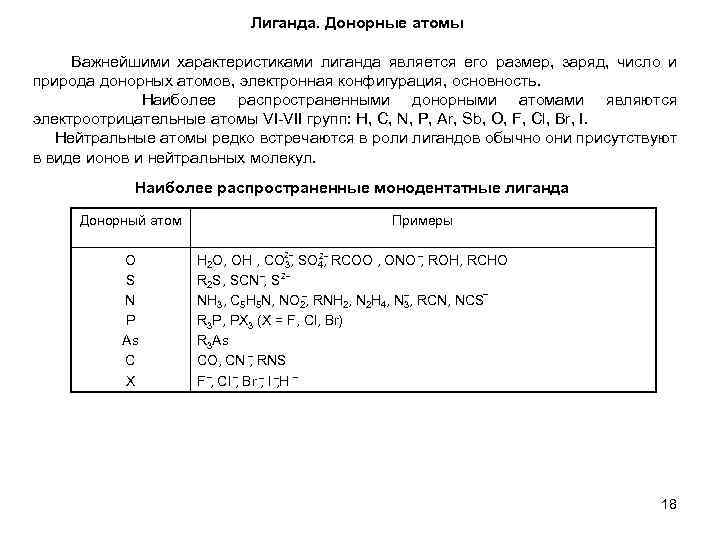 Лиганда. Донорные атомы Важнейшими характеристиками лиганда является его размер, заряд, число и природа донорных атомов, электронная конфигурация, основность. Наиболее распространенными донорными атомами являются электроотрицательные атомы VI-VII групп: H, C, N, P, Ar, Sb, O, F, Cl, Br, I. Нейтральные атомы редко встречаются в роли лигандов обычно они присутствуют в виде ионов и нейтральных молекул. Наиболее распространенные монодентатные лиганда Донорный атом O S N P As C X Примеры H 2 O, OH , CO 3, SO 4, RCOO , ONO , ROH, RCHO R 2 S, SCN , S NH 3, C 5 H 5 N, NO 2, RNH 2, N 2 H 4, N 3, RCN, NCS R 3 P, PX 3 (X = F, Cl, Br) R 3 As CO, CN , RNS F , Cl , Br , I , H 18
Лиганда. Донорные атомы Важнейшими характеристиками лиганда является его размер, заряд, число и природа донорных атомов, электронная конфигурация, основность. Наиболее распространенными донорными атомами являются электроотрицательные атомы VI-VII групп: H, C, N, P, Ar, Sb, O, F, Cl, Br, I. Нейтральные атомы редко встречаются в роли лигандов обычно они присутствуют в виде ионов и нейтральных молекул. Наиболее распространенные монодентатные лиганда Донорный атом O S N P As C X Примеры H 2 O, OH , CO 3, SO 4, RCOO , ONO , ROH, RCHO R 2 S, SCN , S NH 3, C 5 H 5 N, NO 2, RNH 2, N 2 H 4, N 3, RCN, NCS R 3 P, PX 3 (X = F, Cl, Br) R 3 As CO, CN , RNS F , Cl , Br , I , H 18
 N - ЛИГАНДЫ Комплексы с азотсодержащими лигандами – наиболее распространенный, один из первых полученных и изученных классов. Аммиакаты известны почти для всех металлов: [Cu(NH 3)4]2+, [Ag(NH 3)2]Cl, [Cu(NH 3)8]Cl 2, [Co(NH 3)6]Cl 3. Устойчивость их различна. В отношении донорных свойств азот сравним лишь с кислородом. Многие комплексы кроме аммиака содержат в координационной сфере другие лиганды: например [Pt(NH 3)2 Br 2] и т. д. Гидразин N 2 H 4, гидроксиламин NH 2 OH также могут играть роль лигандов: [Pt(N 2 H 4)2 Cl 2], [Pt(NH 2 OH)4 SO 4]. Число комплексов с этими лигандами ограничивается их восстановительными свойствами. Органические азотсодержащие лиганды весьма многочисленны и разнообразны. Наиболее важные из них – пиридин, этилендиамин, различные полидентантные лиганды (слайд 16), алифатические амины: [Ni. Py 4](SCN)2, [Co. En 3]Cl 3, [Pt(CH 3 NH 2)2 Cl 2]. 19
N - ЛИГАНДЫ Комплексы с азотсодержащими лигандами – наиболее распространенный, один из первых полученных и изученных классов. Аммиакаты известны почти для всех металлов: [Cu(NH 3)4]2+, [Ag(NH 3)2]Cl, [Cu(NH 3)8]Cl 2, [Co(NH 3)6]Cl 3. Устойчивость их различна. В отношении донорных свойств азот сравним лишь с кислородом. Многие комплексы кроме аммиака содержат в координационной сфере другие лиганды: например [Pt(NH 3)2 Br 2] и т. д. Гидразин N 2 H 4, гидроксиламин NH 2 OH также могут играть роль лигандов: [Pt(N 2 H 4)2 Cl 2], [Pt(NH 2 OH)4 SO 4]. Число комплексов с этими лигандами ограничивается их восстановительными свойствами. Органические азотсодержащие лиганды весьма многочисленны и разнообразны. Наиболее важные из них – пиридин, этилендиамин, различные полидентантные лиганды (слайд 16), алифатические амины: [Ni. Py 4](SCN)2, [Co. En 3]Cl 3, [Pt(CH 3 NH 2)2 Cl 2]. 19
 О – ЛИГАНДЫ Комплексы с кислородсодержащими лигандами образуют почти все элементы периодической системы. Прежде всего это кристаллогидраты. Соединения, содержащие в составе комплексного иона молекулы воды, называются аквокомплексами. Спирты и эфиры значительно меньше склонны к образованию комплексов, чем вода, но все же получены соединения с метанолом, этиленгликолем: [Mg(CH 3 OH)6]Cl 2, [Ca(C 2 H 5 OH)6]Cl 2 и др. Карбонильная группа альдегидов, эфиров, кетонов обладает довольно слабыми донорными свойствами. 1, 3 -Дикарбонильные соединения (β-дикетоны) благодаря своей енолизации образуют прочные циклические группировки с большим атомов металлов. Например, однозарядный анион ацетилацетона CH 3 C(OH)=CHCOCH 3, образованный отщеплением енольного протона, реагирует со многими ионами металлов с образованием нейтральных комплексов: Аналогичные комплексы образуют дибензоилметан, бензоилацетон, ацетоуксусный эфир. Кислород входит в состав огромного числа оксоанионов различного типа: NO 3 -, SO 42 -, Cr. O 42 -, CO 32 -, Cl. O 4 -, P 2 O 74 -. Все они обладают донорными свойствами, хотя и в очень различной степени. Многие анионы органических кислот образуют устойчивые координационные соединения. 20
О – ЛИГАНДЫ Комплексы с кислородсодержащими лигандами образуют почти все элементы периодической системы. Прежде всего это кристаллогидраты. Соединения, содержащие в составе комплексного иона молекулы воды, называются аквокомплексами. Спирты и эфиры значительно меньше склонны к образованию комплексов, чем вода, но все же получены соединения с метанолом, этиленгликолем: [Mg(CH 3 OH)6]Cl 2, [Ca(C 2 H 5 OH)6]Cl 2 и др. Карбонильная группа альдегидов, эфиров, кетонов обладает довольно слабыми донорными свойствами. 1, 3 -Дикарбонильные соединения (β-дикетоны) благодаря своей енолизации образуют прочные циклические группировки с большим атомов металлов. Например, однозарядный анион ацетилацетона CH 3 C(OH)=CHCOCH 3, образованный отщеплением енольного протона, реагирует со многими ионами металлов с образованием нейтральных комплексов: Аналогичные комплексы образуют дибензоилметан, бензоилацетон, ацетоуксусный эфир. Кислород входит в состав огромного числа оксоанионов различного типа: NO 3 -, SO 42 -, Cr. O 42 -, CO 32 -, Cl. O 4 -, P 2 O 74 -. Все они обладают донорными свойствами, хотя и в очень различной степени. Многие анионы органических кислот образуют устойчивые координационные соединения. 20
 S – ЛИГАНДЫ Серусодержащие комплексы встречаются реже. Донорные свойства серы ограничены и избирательны в отношении природы атомаакцептора. Серусодержащие лиганды координируются и образуют устойчивые комплексы с металлами, которые в природе встречаются в виде сульфидов. Особенностями серы как донора являются, с одной стороны, наличие у нее нескольких неподеленных пар электронов, с другой стороны – возможность использовать d-орбиталм для образования связей. Органические сульфиды легко координируются вокруг ионов металлов. Из органических дитиоэфиров RS(CH 2)n. SR (где n=0, 1, 2, 3, 5) наиболее устойчивые соединения образуются при n=2. Тиоэфиры легко образуют комплексы с Cu(II), Ni(II), Zn(II) и особенно с Pt(II) и Pd(II). Например, диэтилсульфид образует с хлоридом платины (II) соединение эмпирической формулы [Pt{(C 2 H 5)2 S}2 Cl 2], которое имее три изомера: α- и β-изомеры являются соответственно транс- и циссоединениями, а γ-изомер – димером [Pt{(C 2 H 5)2 S}4]Pt. Cl 4. Тиомочевина CS(NH 2)2 образует комплексы с рядом металлов, например [Hg{CS(NH 2)2}4]Cl 2. 21
S – ЛИГАНДЫ Серусодержащие комплексы встречаются реже. Донорные свойства серы ограничены и избирательны в отношении природы атомаакцептора. Серусодержащие лиганды координируются и образуют устойчивые комплексы с металлами, которые в природе встречаются в виде сульфидов. Особенностями серы как донора являются, с одной стороны, наличие у нее нескольких неподеленных пар электронов, с другой стороны – возможность использовать d-орбиталм для образования связей. Органические сульфиды легко координируются вокруг ионов металлов. Из органических дитиоэфиров RS(CH 2)n. SR (где n=0, 1, 2, 3, 5) наиболее устойчивые соединения образуются при n=2. Тиоэфиры легко образуют комплексы с Cu(II), Ni(II), Zn(II) и особенно с Pt(II) и Pd(II). Например, диэтилсульфид образует с хлоридом платины (II) соединение эмпирической формулы [Pt{(C 2 H 5)2 S}2 Cl 2], которое имее три изомера: α- и β-изомеры являются соответственно транс- и циссоединениями, а γ-изомер – димером [Pt{(C 2 H 5)2 S}4]Pt. Cl 4. Тиомочевина CS(NH 2)2 образует комплексы с рядом металлов, например [Hg{CS(NH 2)2}4]Cl 2. 21
 F-, Cl-, Br-, I- КАК ЛИГАНДЫ Галогенокомплексы – один из наиболее обширных и разнообразных комплексов. Галогенид – ионы координируются элементами разных групп и периодов периодической системы: [Be. F 4]2 -, [Zn. Cl 4]2 -, [Cd. CL 6]4 -, [PF 6]-, [Al. F 6]3 -, [Tl. Cl 4]-, [Co. Cl 4]2 -, [Pt. Cl 6]2 -, [Ag. Cl 2]- и тд. Еще многочисленные и разнообразные смешанные галогенокомплексы, например [Co(NH 3)5 Cl]2+, [Pt. Cl 5(OH)]2 -, [Cr(H 2 O)4 Cl 2]+. Устойчивость их различна. Для галогенокомплексов некоторых металлов характерны высокие координационные числа: [Ta. F 8]3 -, [Zr. F 7]3 -, [Re. F 9]4 -. В ряде комплексов, например в (Be. Cl 2)n, [Tl 2 Cl 9]3 -, [W 2 Cl 9]3 -, галогенидионы выполняют роль мостиков. Интересную группу составляют полигалогенидные комплексы, содержащие в качестве центрального атома галогенид-ион X-, а в качестве лигандов – молекулы галогенов, например M[Br 3], M[I 5], M[I 7], M[I 9], где М- большой однозарядный катион, как Cs+, (CH 3)4 N+ и др. 22
F-, Cl-, Br-, I- КАК ЛИГАНДЫ Галогенокомплексы – один из наиболее обширных и разнообразных комплексов. Галогенид – ионы координируются элементами разных групп и периодов периодической системы: [Be. F 4]2 -, [Zn. Cl 4]2 -, [Cd. CL 6]4 -, [PF 6]-, [Al. F 6]3 -, [Tl. Cl 4]-, [Co. Cl 4]2 -, [Pt. Cl 6]2 -, [Ag. Cl 2]- и тд. Еще многочисленные и разнообразные смешанные галогенокомплексы, например [Co(NH 3)5 Cl]2+, [Pt. Cl 5(OH)]2 -, [Cr(H 2 O)4 Cl 2]+. Устойчивость их различна. Для галогенокомплексов некоторых металлов характерны высокие координационные числа: [Ta. F 8]3 -, [Zr. F 7]3 -, [Re. F 9]4 -. В ряде комплексов, например в (Be. Cl 2)n, [Tl 2 Cl 9]3 -, [W 2 Cl 9]3 -, галогенидионы выполняют роль мостиков. Интересную группу составляют полигалогенидные комплексы, содержащие в качестве центрального атома галогенид-ион X-, а в качестве лигандов – молекулы галогенов, например M[Br 3], M[I 5], M[I 7], M[I 9], где М- большой однозарядный катион, как Cs+, (CH 3)4 N+ и др. 22
 PR 3, As. R 3, Sb. R 3 – ЛИГАНДЫ Широко распространены лиганды состава PR 3, As. R 3, Sb. R 3 (где R – галоген, алкил или арил). Донорные свойства этих молекул обусловлены наличием свободной пары электронов и дополняются тем, что атомы P, As и Sb в отличие от азота, имеют свободные d-орбитали с довольно низкими энергиями. Когда центральный атом, которому P, As и Sb отдают пару электронов, имеет электроны на орбиталях той же симметрии, что и свободные орбитали атомов лигандов, то за счет обратной отдачи электронов образуется кратная -связь. Галогениды фосфора PCl 3, PBr 3 образуют комплексы со многими металлами, например [Au(PCl 3)Cl], [Pt(PF 3)2 Cl 2], [Pt(PCl 3)2 Cl 2], [Ni(PCl 3)4]. Особенный интерес представляет координация металлами третичных фосфинов и арсинов: [Cu(PR 3)3 X], [Au(PR 3)X], [Pt{P(CH 3)3}2 Cl 2], где Х=Cl-, Br-, J-, a R= алкил или арил. H 2, O 2, N 2 КАК ЛИГАНДЫ Синтезированы комплексы, содержащие в качестве лигандов молекулы H 2, O 2, N 2. Некоторые из них, в частности [Cu(H 2)2 Cl 2], [Ir. Co{P(C 6 H 5)3}2(O 2)J], MP{P(C 6 H 5)3}2(O 2)], (где М=Ni 0, Pd 0, Pt 0), [Ru(NH 3)5 N 2]X 2, [Os(NH 3)5 N 2]Br 2 и др. , играют важную роль в катализе и имеют большое будущее в химической технологии. 23
PR 3, As. R 3, Sb. R 3 – ЛИГАНДЫ Широко распространены лиганды состава PR 3, As. R 3, Sb. R 3 (где R – галоген, алкил или арил). Донорные свойства этих молекул обусловлены наличием свободной пары электронов и дополняются тем, что атомы P, As и Sb в отличие от азота, имеют свободные d-орбитали с довольно низкими энергиями. Когда центральный атом, которому P, As и Sb отдают пару электронов, имеет электроны на орбиталях той же симметрии, что и свободные орбитали атомов лигандов, то за счет обратной отдачи электронов образуется кратная -связь. Галогениды фосфора PCl 3, PBr 3 образуют комплексы со многими металлами, например [Au(PCl 3)Cl], [Pt(PF 3)2 Cl 2], [Pt(PCl 3)2 Cl 2], [Ni(PCl 3)4]. Особенный интерес представляет координация металлами третичных фосфинов и арсинов: [Cu(PR 3)3 X], [Au(PR 3)X], [Pt{P(CH 3)3}2 Cl 2], где Х=Cl-, Br-, J-, a R= алкил или арил. H 2, O 2, N 2 КАК ЛИГАНДЫ Синтезированы комплексы, содержащие в качестве лигандов молекулы H 2, O 2, N 2. Некоторые из них, в частности [Cu(H 2)2 Cl 2], [Ir. Co{P(C 6 H 5)3}2(O 2)J], MP{P(C 6 H 5)3}2(O 2)], (где М=Ni 0, Pd 0, Pt 0), [Ru(NH 3)5 N 2]X 2, [Os(NH 3)5 N 2]Br 2 и др. , играют важную роль в катализе и имеют большое будущее в химической технологии. 23
 - ЛИГАНДЫ Переходные металлы d-группы способны взаимодействовать с молекулами NO, CO, N 2, O 2 замещенными фосфинами, стибинами, арсинами или сульфидами, окисью азота, непредельными органическими соединениями. В комплексах с такими лигандами атомы металлов часто находятся в состоянии низкой степени окисления – положительной, нулевой или даже отрицательной. Но эти лиганды способны стабилизировать низкие состояния окисления металлов, так как атом-донор наряду с неподеленными парами электронов имеет также вакантные орбитали, которые могут принимать электроны с заполненных орбиталей атома металла. Образующаяся при этом -связь дополняет связь, возникающую за счет неподеленной пары электронов лиганда. Таким образом, высокая плотность на атоме металла, являющаяся следствием образования им -связей с лигандами, делокализуется на лиганды. Подобные лиганды можно разделить на 2 группы. 1 -ый тип. Лиганды -акцепторного типа образуют связи с атомом металла за счет не только -орбиталей, но и -орбиталей, лежащих в тех же узловых плоскостях, в которых расположены оси -связи. Атом металла лежит либо на оси линейного лиганда, либо в плоскости самого лиганда. Примерами лигандов этого типа являются СО, NO, изоцианиды, R 2 S, PX 3, As. X 3, Sb. X 3. 2 -ой тип. Ко второму типу -лигандов относятся многие ненасыщенные органические молекулы – циклопентадиен, С 5 Н 6, олефины, ацетилен и его производные. Комплексы с подобными лигандами называют -комплексами, выделяя их в особый класс, так как по типу связи они представляют качественно отличные соединения. Лиганды в -комплексах предоставляют центральному атому неподеленную пару электронов, расположенную на -орбитали, и принимают электроны от центрального атома также на -орбиталь. Центральный атом располагается вне плоскости молекулы лиганда. 24
- ЛИГАНДЫ Переходные металлы d-группы способны взаимодействовать с молекулами NO, CO, N 2, O 2 замещенными фосфинами, стибинами, арсинами или сульфидами, окисью азота, непредельными органическими соединениями. В комплексах с такими лигандами атомы металлов часто находятся в состоянии низкой степени окисления – положительной, нулевой или даже отрицательной. Но эти лиганды способны стабилизировать низкие состояния окисления металлов, так как атом-донор наряду с неподеленными парами электронов имеет также вакантные орбитали, которые могут принимать электроны с заполненных орбиталей атома металла. Образующаяся при этом -связь дополняет связь, возникающую за счет неподеленной пары электронов лиганда. Таким образом, высокая плотность на атоме металла, являющаяся следствием образования им -связей с лигандами, делокализуется на лиганды. Подобные лиганды можно разделить на 2 группы. 1 -ый тип. Лиганды -акцепторного типа образуют связи с атомом металла за счет не только -орбиталей, но и -орбиталей, лежащих в тех же узловых плоскостях, в которых расположены оси -связи. Атом металла лежит либо на оси линейного лиганда, либо в плоскости самого лиганда. Примерами лигандов этого типа являются СО, NO, изоцианиды, R 2 S, PX 3, As. X 3, Sb. X 3. 2 -ой тип. Ко второму типу -лигандов относятся многие ненасыщенные органические молекулы – циклопентадиен, С 5 Н 6, олефины, ацетилен и его производные. Комплексы с подобными лигандами называют -комплексами, выделяя их в особый класс, так как по типу связи они представляют качественно отличные соединения. Лиганды в -комплексах предоставляют центральному атому неподеленную пару электронов, расположенную на -орбитали, и принимают электроны от центрального атома также на -орбиталь. Центральный атом располагается вне плоскости молекулы лиганда. 24
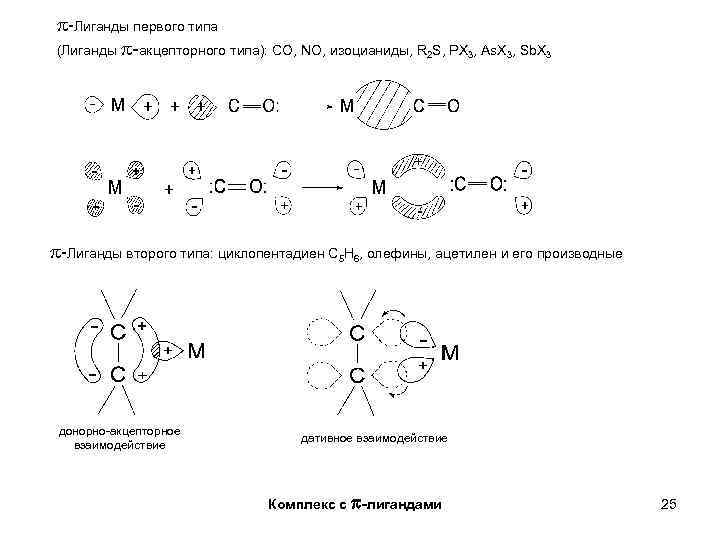 -Лиганды первого типа (Лиганды -акцепторного типа): СО, NO, изоцианиды, R 2 S, PX 3, As. X 3, Sb. X 3 -Лиганды второго типа: циклопентадиен С 5 Н 6, олефины, ацетилен и его производные донорно-акцепторное взаимодействие дативное взаимодействие Комплекс с -лигандами 25
-Лиганды первого типа (Лиганды -акцепторного типа): СО, NO, изоцианиды, R 2 S, PX 3, As. X 3, Sb. X 3 -Лиганды второго типа: циклопентадиен С 5 Н 6, олефины, ацетилен и его производные донорно-акцепторное взаимодействие дативное взаимодействие Комплекс с -лигандами 25
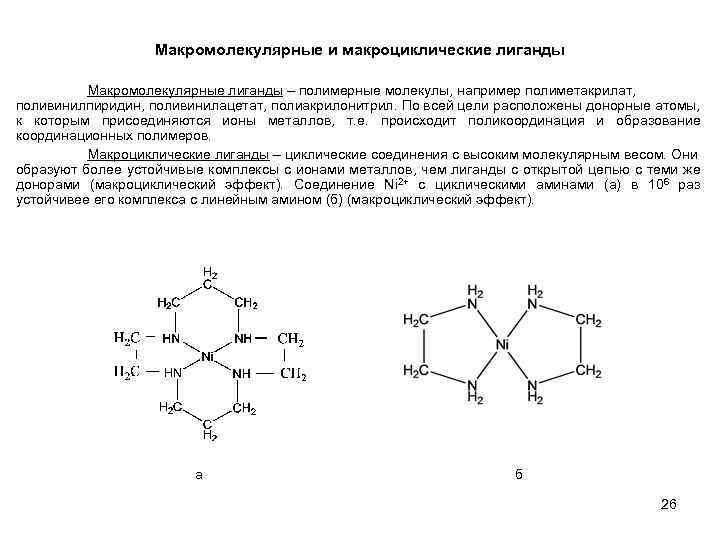 Макромолекулярные и макроциклические лиганды Макромолекулярные лиганды – полимерные молекулы, например полиметакрилат, поливинилпиридин, поливинилацетат, полиакрилонитрил. По всей цели расположены донорные атомы, к которым присоединяются ионы металлов, т. е. происходит поликоординация и образование координационных полимеров. Макроциклические лиганды – циклические соединения с высоким молекулярным весом. Они образуют более устойчивые комплексы с ионами металлов, чем лиганды с открытой цепью с теми же донорами (макроциклический эффект). Соединение Ni 2+ с циклическими аминами (а) в 106 раз устойчивее его комплекса с линейным амином (б) (макроциклический эффект). а б 26
Макромолекулярные и макроциклические лиганды Макромолекулярные лиганды – полимерные молекулы, например полиметакрилат, поливинилпиридин, поливинилацетат, полиакрилонитрил. По всей цели расположены донорные атомы, к которым присоединяются ионы металлов, т. е. происходит поликоординация и образование координационных полимеров. Макроциклические лиганды – циклические соединения с высоким молекулярным весом. Они образуют более устойчивые комплексы с ионами металлов, чем лиганды с открытой цепью с теми же донорами (макроциклический эффект). Соединение Ni 2+ с циклическими аминами (а) в 106 раз устойчивее его комплекса с линейным амином (б) (макроциклический эффект). а б 26
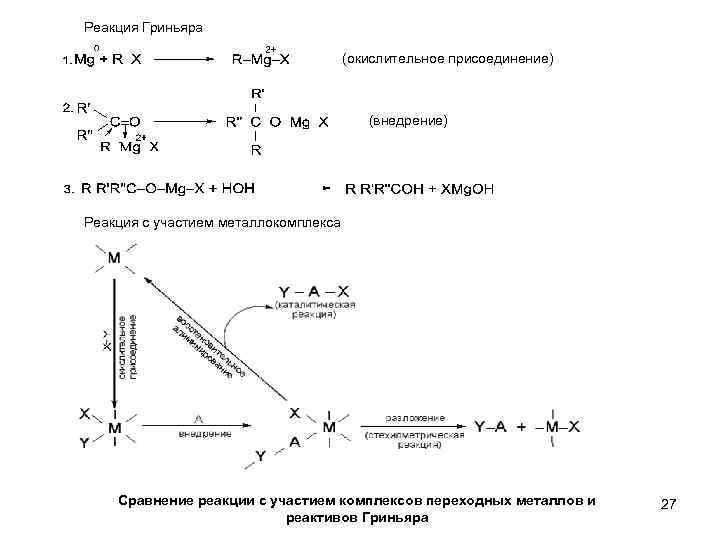 Реакция Гриньяра (окислительное присоединение) (внедрение) Реакция с участием металлокомплекса Сравнение реакции с участием комплексов переходных металлов и реактивов Гриньяра 27
Реакция Гриньяра (окислительное присоединение) (внедрение) Реакция с участием металлокомплекса Сравнение реакции с участием комплексов переходных металлов и реактивов Гриньяра 27
 Реакция характерна для комплексов переходных металлов, имеющих электронную конфигурацию d 8 и d 10. Образование -связей с атомами переходных металлов. Реакция окислительного присоединения. 28
Реакция характерна для комплексов переходных металлов, имеющих электронную конфигурацию d 8 и d 10. Образование -связей с атомами переходных металлов. Реакция окислительного присоединения. 28
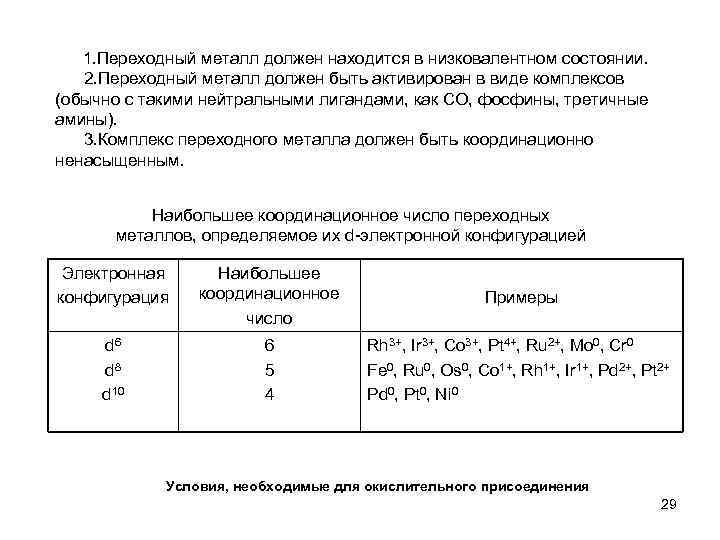 1. Переходный металл должен находится в низковалентном состоянии. 2. Переходный металл должен быть активирован в виде комплексов (обычно с такими нейтральными лигандами, как СО, фосфины, третичные амины). 3. Комплекс переходного металла должен быть координационно ненасыщенным. Наибольшее координационное число переходных металлов, определяемое их d-электронной конфигурацией Электронная конфигурация Наибольшее координационное число Примеры d 6 d 8 d 10 6 5 4 Rh 3+, Ir 3+, Co 3+, Pt 4+, Ru 2+, Mo 0, Cr 0 Fe 0, Ru 0, Os 0, Co 1+, Rh 1+, Ir 1+, Pd 2+, Pt 2+ Pd 0, Pt 0, Ni 0 Условия, необходимые для окислительного присоединения 29
1. Переходный металл должен находится в низковалентном состоянии. 2. Переходный металл должен быть активирован в виде комплексов (обычно с такими нейтральными лигандами, как СО, фосфины, третичные амины). 3. Комплекс переходного металла должен быть координационно ненасыщенным. Наибольшее координационное число переходных металлов, определяемое их d-электронной конфигурацией Электронная конфигурация Наибольшее координационное число Примеры d 6 d 8 d 10 6 5 4 Rh 3+, Ir 3+, Co 3+, Pt 4+, Ru 2+, Mo 0, Cr 0 Fe 0, Ru 0, Os 0, Co 1+, Rh 1+, Ir 1+, Pd 2+, Pt 2+ Pd 0, Pt 0, Ni 0 Условия, необходимые для окислительного присоединения 29
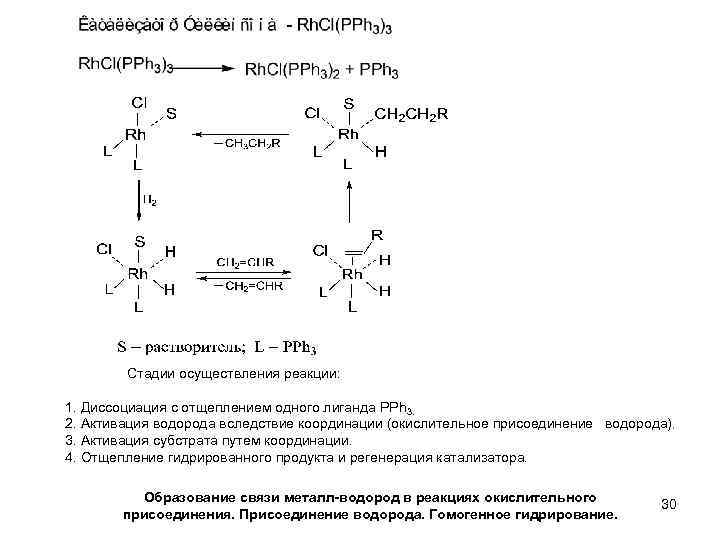 Стадии осуществления реакции: 1. Диссоциация с отщеплением одного лиганда PPh 3. 2. Активация водорода вследствие координации (окислительное присоединение водорода). 3. Активация субстрата путем координации. 4. Отщепление гидрированного продукта и регенерация катализатора. Образование связи металл-водород в реакциях окислительного присоединения. Присоединение водорода. Гомогенное гидрирование. 30
Стадии осуществления реакции: 1. Диссоциация с отщеплением одного лиганда PPh 3. 2. Активация водорода вследствие координации (окислительное присоединение водорода). 3. Активация субстрата путем координации. 4. Отщепление гидрированного продукта и регенерация катализатора. Образование связи металл-водород в реакциях окислительного присоединения. Присоединение водорода. Гомогенное гидрирование. 30
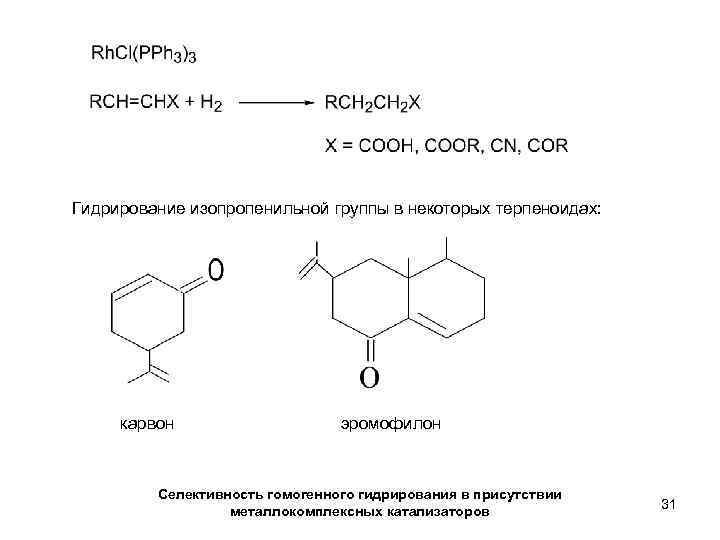 Гидрирование изопропенильной группы в некоторых терпеноидах: карвон эромофилон Селективность гомогенного гидрирования в присутствии металлокомплексных катализаторов 31
Гидрирование изопропенильной группы в некоторых терпеноидах: карвон эромофилон Селективность гомогенного гидрирования в присутствии металлокомплексных катализаторов 31
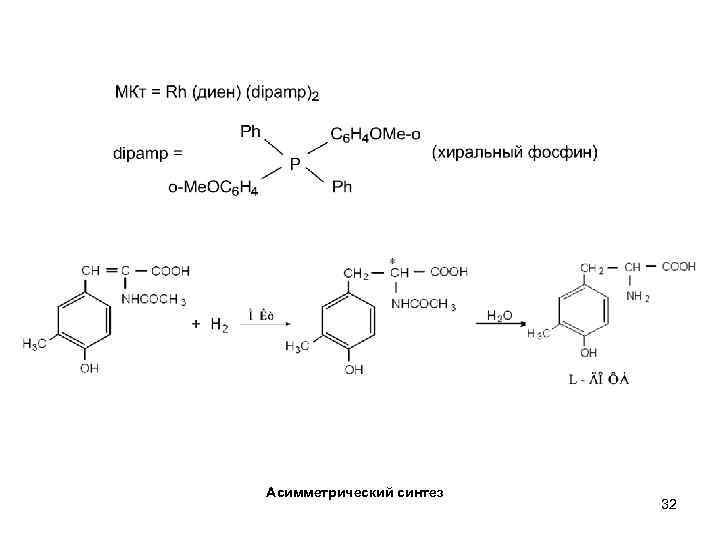 Асимметрический синтез 32
Асимметрический синтез 32
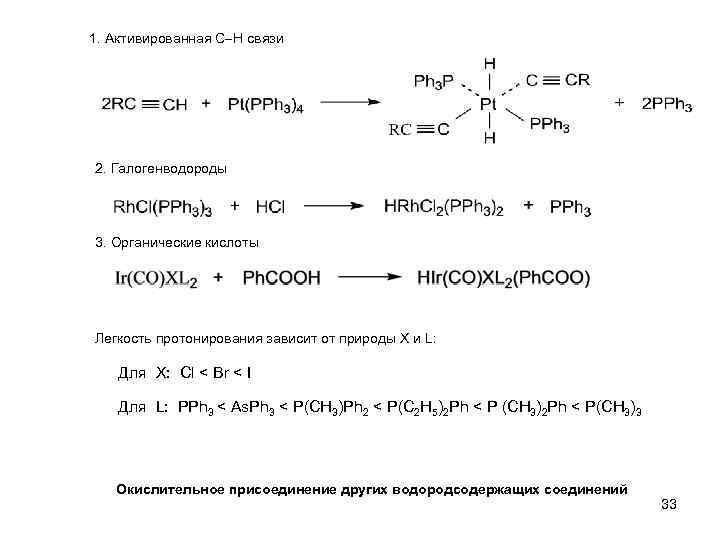 1. Активированная С Н связи 2. Галогенводороды 3. Органические кислоты Легкость протонирования зависит от природы Х и L: Для Х: Cl < Br < I Для L: PPh 3 < As. Ph 3 < P(CH 3)Ph 2 < P(C 2 H 5)2 Ph < P (CH 3)2 Ph < P(CH 3)3 Окислительное присоединение других водородсодержащих соединений 33
1. Активированная С Н связи 2. Галогенводороды 3. Органические кислоты Легкость протонирования зависит от природы Х и L: Для Х: Cl < Br < I Для L: PPh 3 < As. Ph 3 < P(CH 3)Ph 2 < P(C 2 H 5)2 Ph < P (CH 3)2 Ph < P(CH 3)3 Окислительное присоединение других водородсодержащих соединений 33
 К настоящему времени известно ограниченные примеры образования связи М С путем расщепления связи С С. Примеры: Образование связи металл-углерод в реакциях окислительного присоединения 34
К настоящему времени известно ограниченные примеры образования связи М С путем расщепления связи С С. Примеры: Образование связи металл-углерод в реакциях окислительного присоединения 34
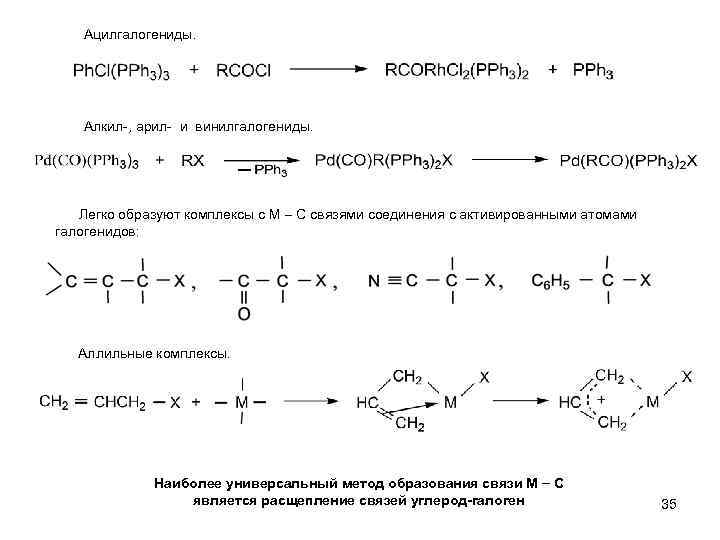 Ацилгалогениды. Алкил-, арил- и винилгалогениды. Легко образуют комплексы с М С связями соединения с активированными атомами галогенидов: Аллильные комплексы. Наиболее универсальный метод образования связи М С является расщепление связей углерод-галоген 35
Ацилгалогениды. Алкил-, арил- и винилгалогениды. Легко образуют комплексы с М С связями соединения с активированными атомами галогенидов: Аллильные комплексы. Наиболее универсальный метод образования связи М С является расщепление связей углерод-галоген 35
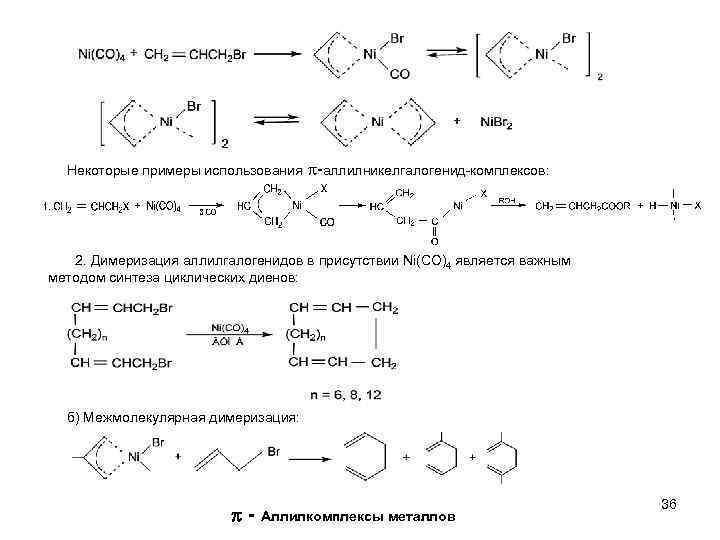 Некоторые примеры использования -аллилникелгалогенид-комплексов: 2. Димеризация аллилгалогенидов в присутствии Ni(CO)4 является важным методом синтеза циклических диенов: б) Межмолекулярная димеризация: - Аллилкомплексы металлов 36
Некоторые примеры использования -аллилникелгалогенид-комплексов: 2. Димеризация аллилгалогенидов в присутствии Ni(CO)4 является важным методом синтеза циклических диенов: б) Межмолекулярная димеризация: - Аллилкомплексы металлов 36
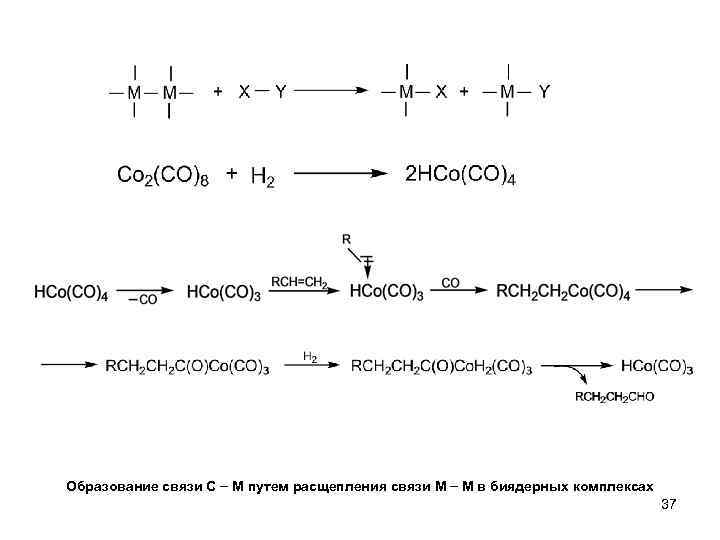 Образование связи С М путем расщепления связи М М в биядерных комплексах 37
Образование связи С М путем расщепления связи М М в биядерных комплексах 37
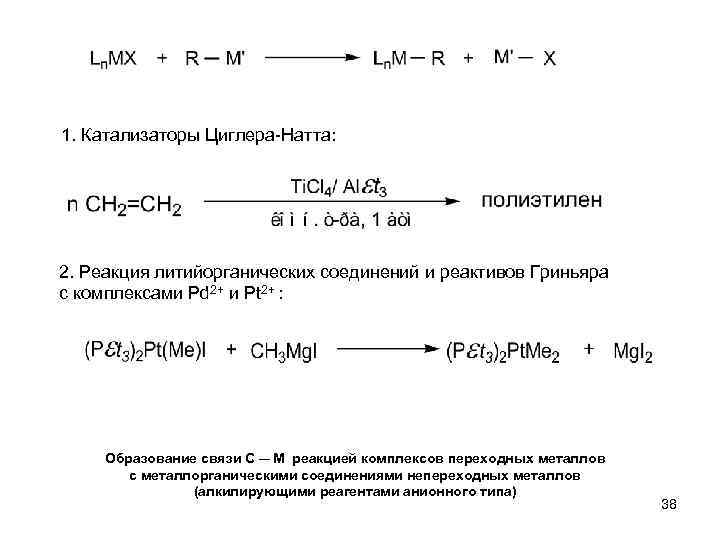 1. Катализаторы Циглера-Натта: 2. Реакция литийорганических соединений и реактивов Гриньяра с комплексами Pd 2+ и Pt 2+ : Образование связи С М реакцией комплексов переходных металлов с металлорганическими соединениями непереходных металлов (алкилирующими реагентами анионного типа) 38
1. Катализаторы Циглера-Натта: 2. Реакция литийорганических соединений и реактивов Гриньяра с комплексами Pd 2+ и Pt 2+ : Образование связи С М реакцией комплексов переходных металлов с металлорганическими соединениями непереходных металлов (алкилирующими реагентами анионного типа) 38
 Факторы, влияющие на характер связи М С в металлокомплексах: 1. Природа атома металла. 2. Степень окисления металла и его электроотрицательность. 3. Число и природа лигандов. 4. Реакционная среда. 5. Природа субстрата, с которым комплекс вступает в реакцию. В зависимости от того, связан ли атом Ni с атомом углерода алкильной, винильной, этинильной, арильной или ацильной группы, связь Ni C расщепляется различным образом. а) Под действием нуклеофильных реагентов (вода, спирты, различные анионы) Ni C связь ацильной группы расщепляется следующим образом: б) Аллильная, винильная или арильные группы, связанные с атомом Ni, обычно взаимодействуют с электрофильными реагентами: Реакционная способность -связи с атомами переходных металлов 39
Факторы, влияющие на характер связи М С в металлокомплексах: 1. Природа атома металла. 2. Степень окисления металла и его электроотрицательность. 3. Число и природа лигандов. 4. Реакционная среда. 5. Природа субстрата, с которым комплекс вступает в реакцию. В зависимости от того, связан ли атом Ni с атомом углерода алкильной, винильной, этинильной, арильной или ацильной группы, связь Ni C расщепляется различным образом. а) Под действием нуклеофильных реагентов (вода, спирты, различные анионы) Ni C связь ацильной группы расщепляется следующим образом: б) Аллильная, винильная или арильные группы, связанные с атомом Ni, обычно взаимодействуют с электрофильными реагентами: Реакционная способность -связи с атомами переходных металлов 39
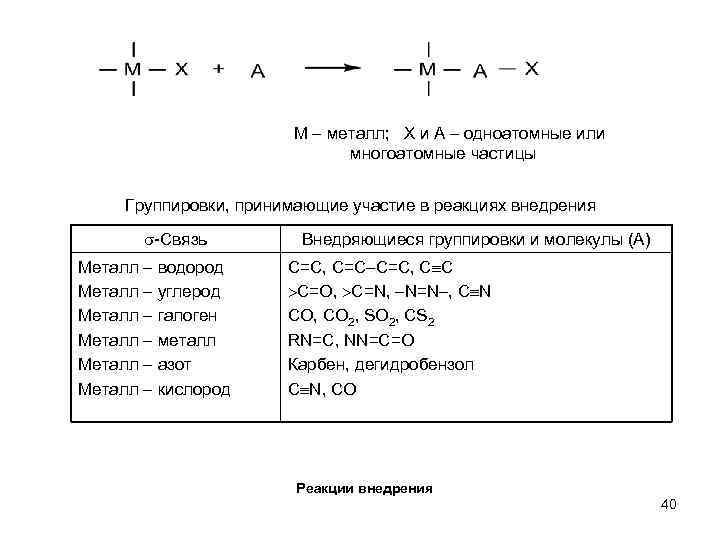 М – металл; Х и А – одноатомные или многоатомные частицы Группировки, принимающие участие в реакциях внедрения -Связь Металл – водород Металл – углерод Металл – галоген Металл – металл Металл – азот Металл – кислород Внедряющиеся группировки и молекулы (А) С=С, С С С=О, С=N, N=N , C N CO, CO 2, SO 2, CS 2 RN=C, NN=C=O Карбен, дегидробензол С N, CO Реакции внедрения 40
М – металл; Х и А – одноатомные или многоатомные частицы Группировки, принимающие участие в реакциях внедрения -Связь Металл – водород Металл – углерод Металл – галоген Металл – металл Металл – азот Металл – кислород Внедряющиеся группировки и молекулы (А) С=С, С С С=О, С=N, N=N , C N CO, CO 2, SO 2, CS 2 RN=C, NN=C=O Карбен, дегидробензол С N, CO Реакции внедрения 40
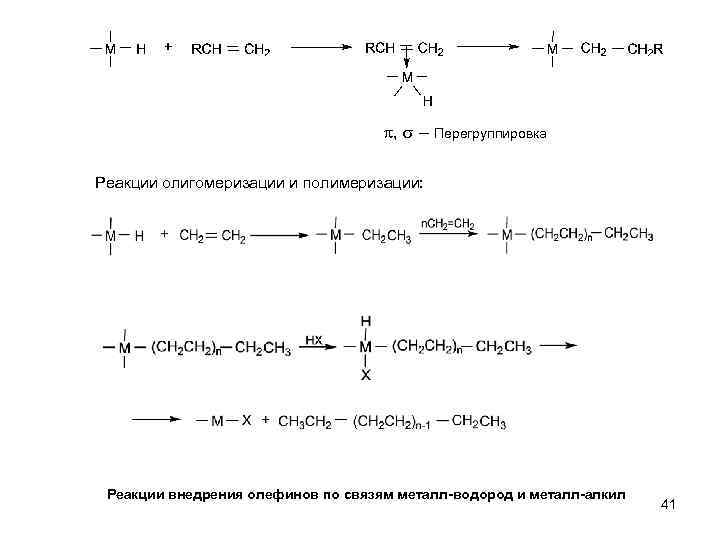 , Перегруппировка Реакции олигомеризации и полимеризации: Реакции внедрения олефинов по связям металл-водород и металл-алкил 41
, Перегруппировка Реакции олигомеризации и полимеризации: Реакции внедрения олефинов по связям металл-водород и металл-алкил 41
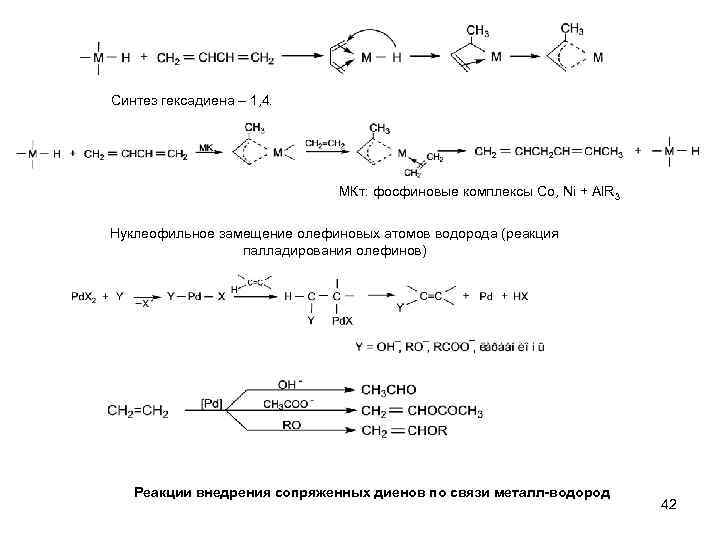 Синтез гексадиена – 1, 4. МКт: фосфиновые комплексы Co, Ni + Al. R 3 Нуклеофильное замещение олефиновых атомов водорода (реакция палладирования олефинов) Реакции внедрения сопряженных диенов по связи металл-водород 42
Синтез гексадиена – 1, 4. МКт: фосфиновые комплексы Co, Ni + Al. R 3 Нуклеофильное замещение олефиновых атомов водорода (реакция палладирования олефинов) Реакции внедрения сопряженных диенов по связи металл-водород 42
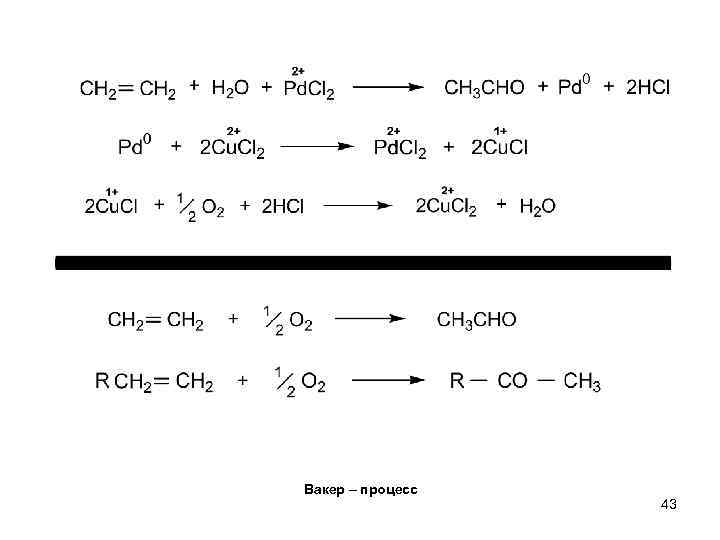 Вакер – процесс 43
Вакер – процесс 43
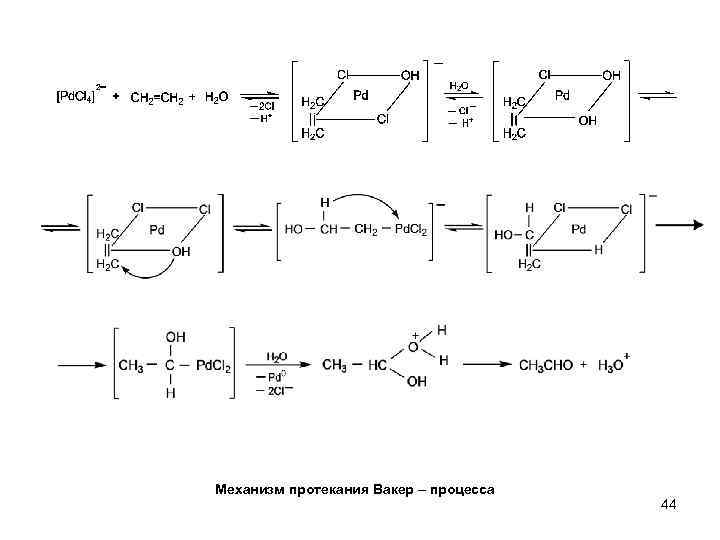 Механизм протекания Вакер – процесса 44
Механизм протекания Вакер – процесса 44
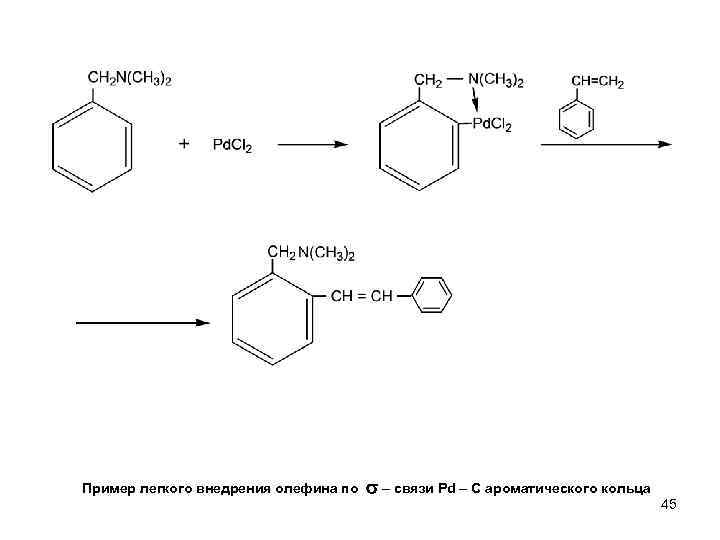 Пример легкого внедрения олефина по связи Pd C ароматического кольца 45
Пример легкого внедрения олефина по связи Pd C ароматического кольца 45
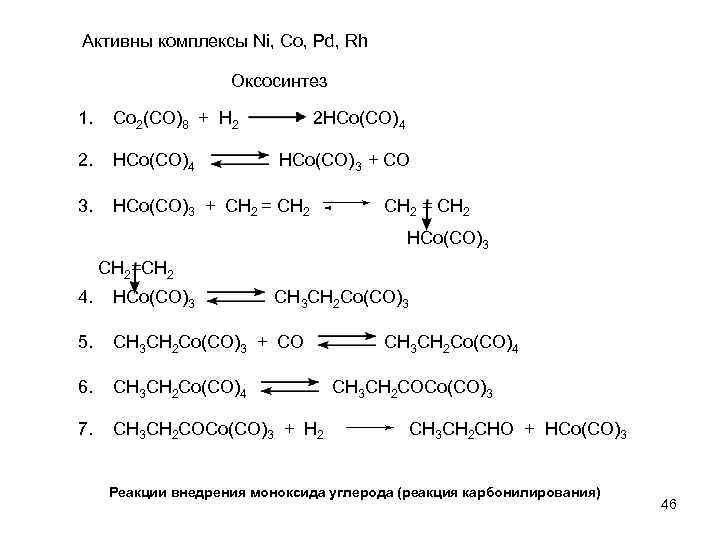 Активны комплексы Ni, Co, Pd, Rh Оксосинтез 1. Co 2(CO)8 + H 2 2 HCo(CO)4 2. HCo(CO)4 3. HCo(CO)3 + CH 2 = CH 2 HCo(CO)3 + CO CH 2 = CH 2 HCo(CO)3 CH 2=CH 2 4. HCo(CO)3 CH 3 CH 2 Co(CO)3 5. CH 3 CH 2 Co(CO)3 + CO 6. CH 3 CH 2 Co(CO)4 7. CH 3 CH 2 COCo(CO)3 + H 2 CH 3 CH 2 Co(CO)4 CH 3 CH 2 COCo(CO)3 CH 3 CH 2 CHO + HCo(CO)3 Реакции внедрения моноксида углерода (реакция карбонилирования) 46
Активны комплексы Ni, Co, Pd, Rh Оксосинтез 1. Co 2(CO)8 + H 2 2 HCo(CO)4 2. HCo(CO)4 3. HCo(CO)3 + CH 2 = CH 2 HCo(CO)3 + CO CH 2 = CH 2 HCo(CO)3 CH 2=CH 2 4. HCo(CO)3 CH 3 CH 2 Co(CO)3 5. CH 3 CH 2 Co(CO)3 + CO 6. CH 3 CH 2 Co(CO)4 7. CH 3 CH 2 COCo(CO)3 + H 2 CH 3 CH 2 Co(CO)4 CH 3 CH 2 COCo(CO)3 CH 3 CH 2 CHO + HCo(CO)3 Реакции внедрения моноксида углерода (реакция карбонилирования) 46
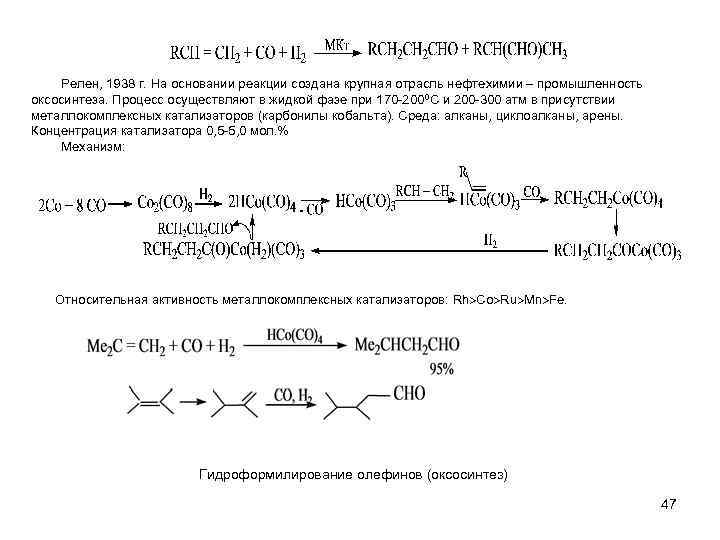 Релен, 1938 г. На основании реакции создана крупная отрасль нефтехимии – промышленность оксосинтеза. Процесс осуществляют в жидкой фазе при 170 -200 0 С и 200 -300 атм в присутствии металлокомплексных катализаторов (карбонилы кобальта). Среда: алканы, циклоалканы, арены. Концентрация катализатора 0, 5 -5, 0 мол. % Механизм: Относительная активность металлокомплексных катализаторов: Rh Co Ru Mn Fe. Гидроформилирование олефинов (оксосинтез) 47
Релен, 1938 г. На основании реакции создана крупная отрасль нефтехимии – промышленность оксосинтеза. Процесс осуществляют в жидкой фазе при 170 -200 0 С и 200 -300 атм в присутствии металлокомплексных катализаторов (карбонилы кобальта). Среда: алканы, циклоалканы, арены. Концентрация катализатора 0, 5 -5, 0 мол. % Механизм: Относительная активность металлокомплексных катализаторов: Rh Co Ru Mn Fe. Гидроформилирование олефинов (оксосинтез) 47
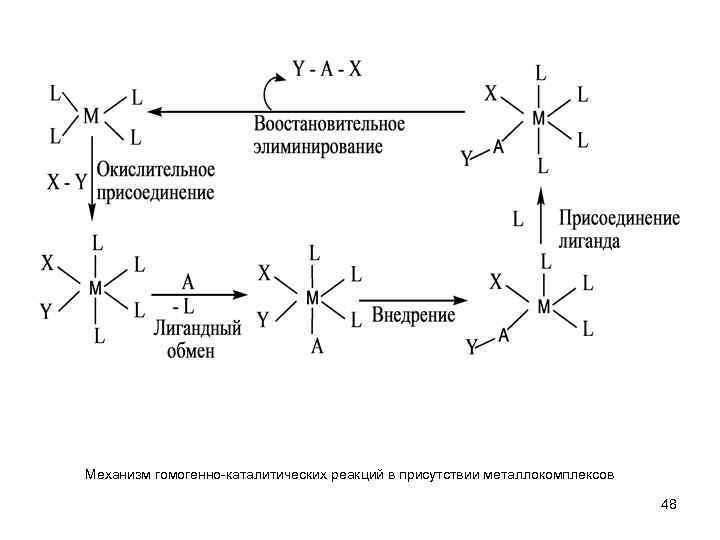 Механизм гомогенно-каталитических реакций в присутствии металлокомплексов 48
Механизм гомогенно-каталитических реакций в присутствии металлокомплексов 48
 Синтезы Реппе. Конец 30 -х годов XIX в. Реакция СО с ненасыщенными соединениями или соединениями с активной связью С-Х (где Х=ОН, OR, галоген) с последующей нуклеофильной атакой реагента, содержащего подвижный атом Н, приводящее к образованию карбоновых кислот и их производных. Карбонилирование алкинов. Катализаторы: В основном Ni-катализаторы. Применяются также Pd-катализаторы. Механизм: Наиболее крупными промышленными процессами являются получение акриловой кислоты и ее эфиров Синтезы Реппе. Карбонилирование алкинов 49
Синтезы Реппе. Конец 30 -х годов XIX в. Реакция СО с ненасыщенными соединениями или соединениями с активной связью С-Х (где Х=ОН, OR, галоген) с последующей нуклеофильной атакой реагента, содержащего подвижный атом Н, приводящее к образованию карбоновых кислот и их производных. Карбонилирование алкинов. Катализаторы: В основном Ni-катализаторы. Применяются также Pd-катализаторы. Механизм: Наиболее крупными промышленными процессами являются получение акриловой кислоты и ее эфиров Синтезы Реппе. Карбонилирование алкинов 49
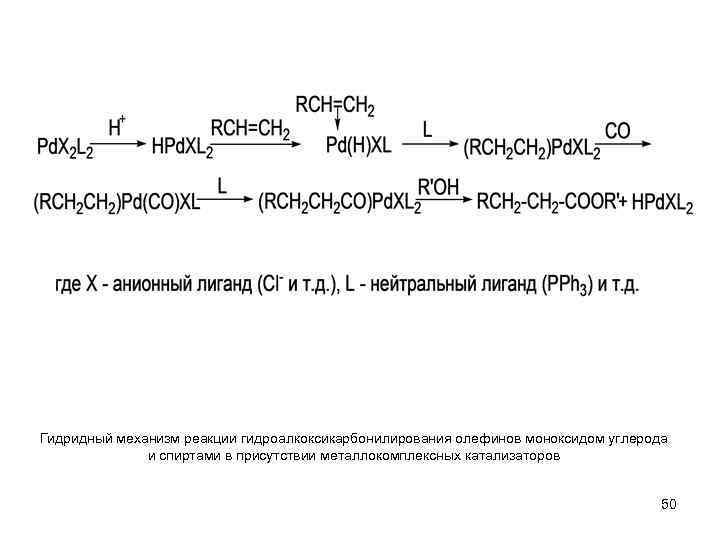 Гидридный механизм реакции гидроалкоксикарбонилирования олефинов моноксидом углерода и спиртами в присутствии металлокомплексных катализаторов 50
Гидридный механизм реакции гидроалкоксикарбонилирования олефинов моноксидом углерода и спиртами в присутствии металлокомплексных катализаторов 50
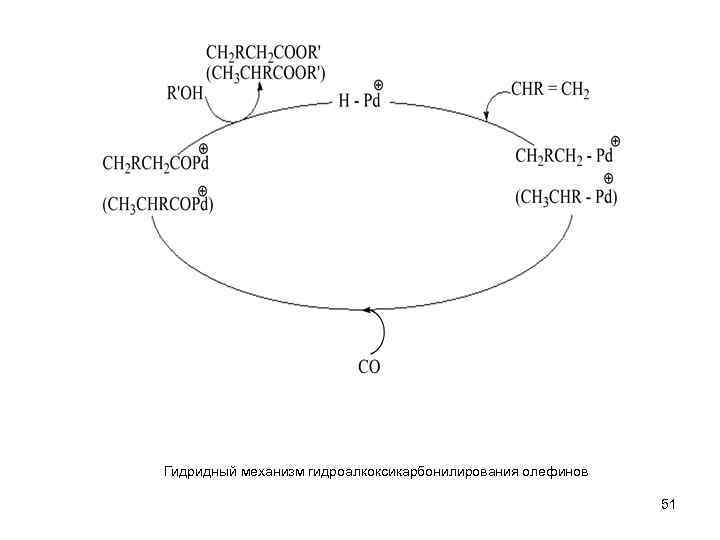 Гидридный механизм гидроалкоксикарбонилирования олефинов 51
Гидридный механизм гидроалкоксикарбонилирования олефинов 51
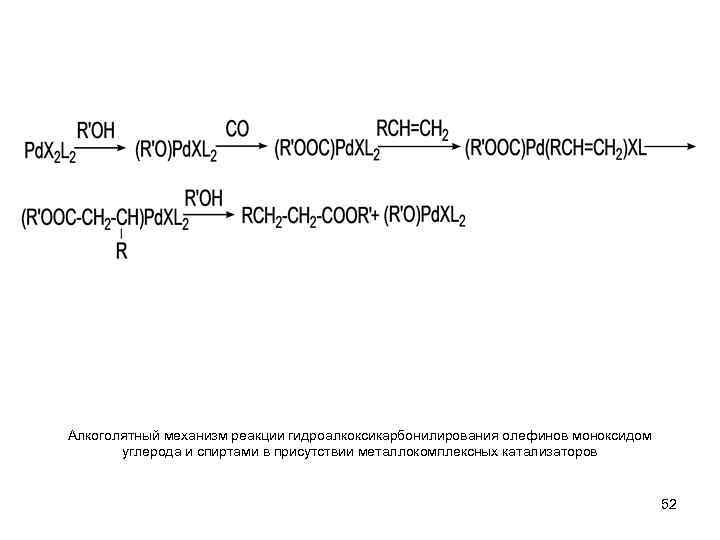 Алкоголятный механизм реакции гидроалкоксикарбонилирования олефинов моноксидом углерода и спиртами в присутствии металлокомплексных катализаторов 52
Алкоголятный механизм реакции гидроалкоксикарбонилирования олефинов моноксидом углерода и спиртами в присутствии металлокомплексных катализаторов 52
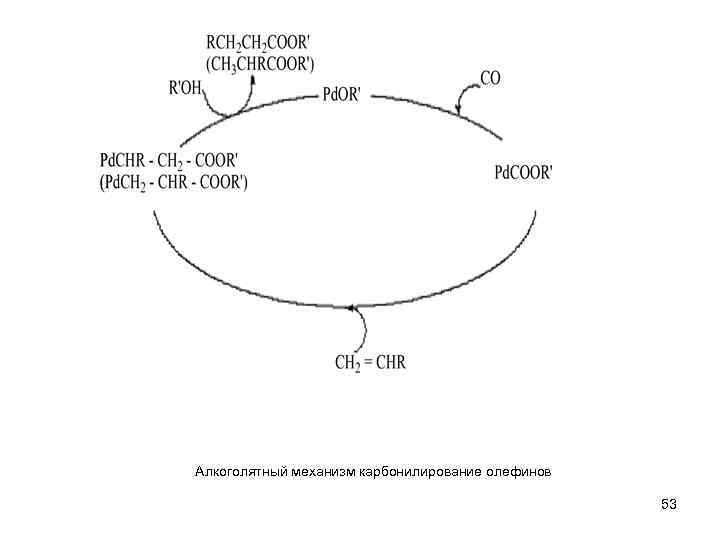 Алкоголятный механизм карбонилирование олефинов 53
Алкоголятный механизм карбонилирование олефинов 53
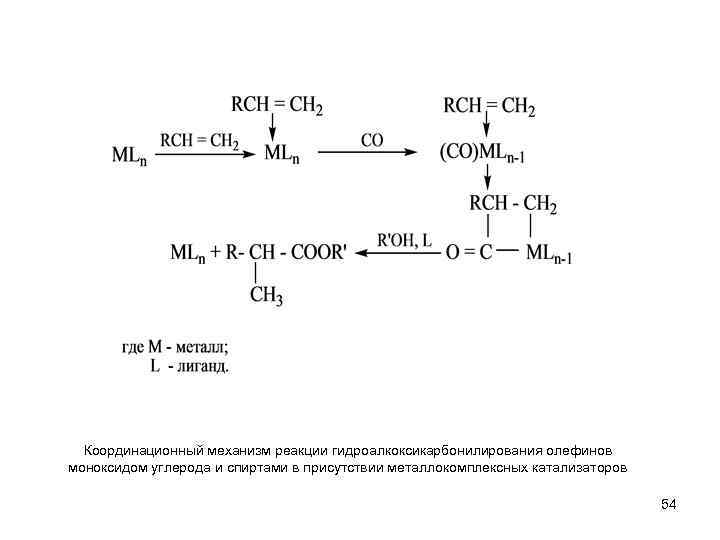 Координационный механизм реакции гидроалкоксикарбонилирования олефинов моноксидом углерода и спиртами в присутствии металлокомплексных катализаторов 54
Координационный механизм реакции гидроалкоксикарбонилирования олефинов моноксидом углерода и спиртами в присутствии металлокомплексных катализаторов 54
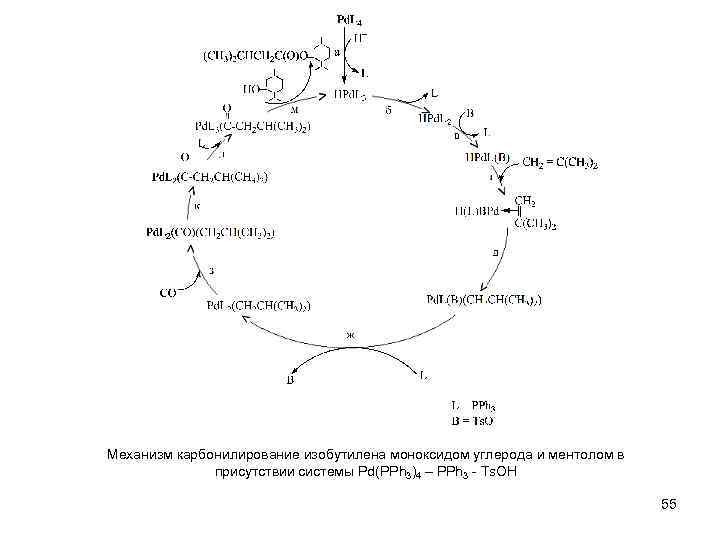 Механизм карбонилирование изобутилена моноксидом углерода и ментолом в присутствии системы Pd(PPh 3)4 – PPh 3 - Ts. OH 55
Механизм карбонилирование изобутилена моноксидом углерода и ментолом в присутствии системы Pd(PPh 3)4 – PPh 3 - Ts. OH 55
 Примеры уникальной возможности реакции карбонилирования как синтетического метода 56
Примеры уникальной возможности реакции карбонилирования как синтетического метода 56
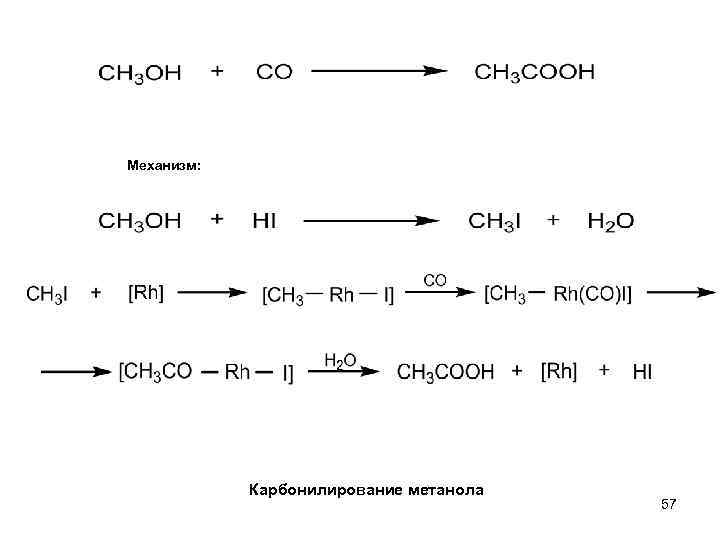 Механизм: Карбонилирование метанола 57
Механизм: Карбонилирование метанола 57
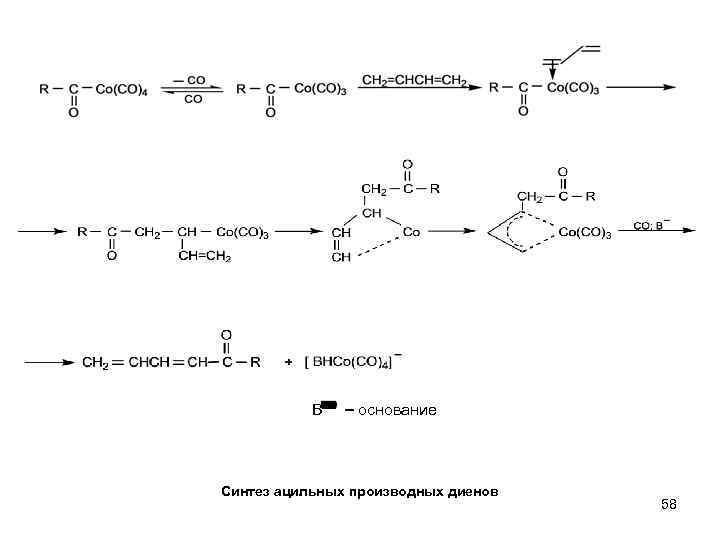 В основание Синтез ацильных производных диенов 58
В основание Синтез ацильных производных диенов 58
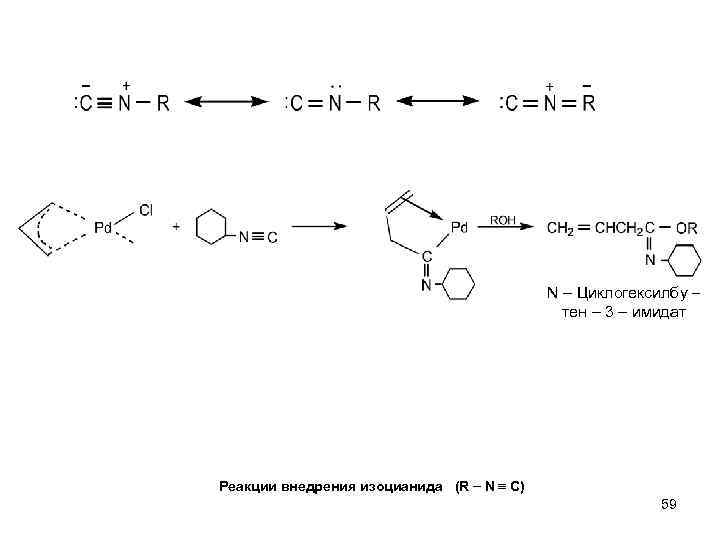 N – Циклогексилбу тен – 3 – имидат Реакции внедрения изоцианида (R N C) 59
N – Циклогексилбу тен – 3 – имидат Реакции внедрения изоцианида (R N C) 59
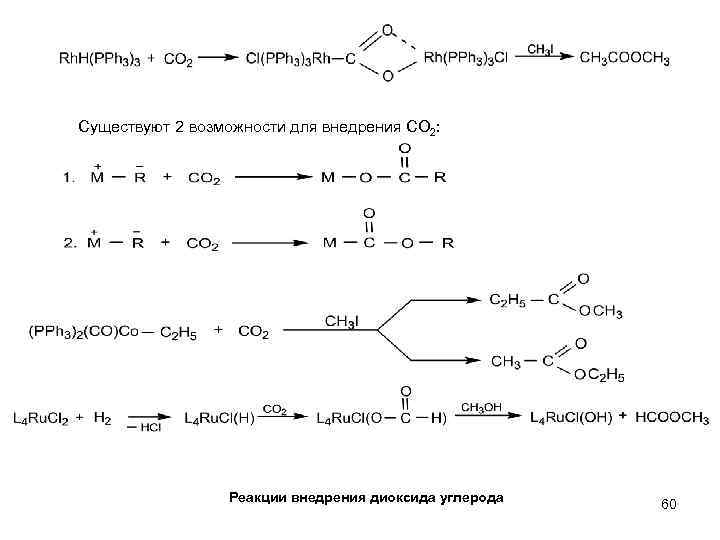 Существуют 2 возможности для внедрения СО 2: Реакции внедрения диоксида углерода 60
Существуют 2 возможности для внедрения СО 2: Реакции внедрения диоксида углерода 60
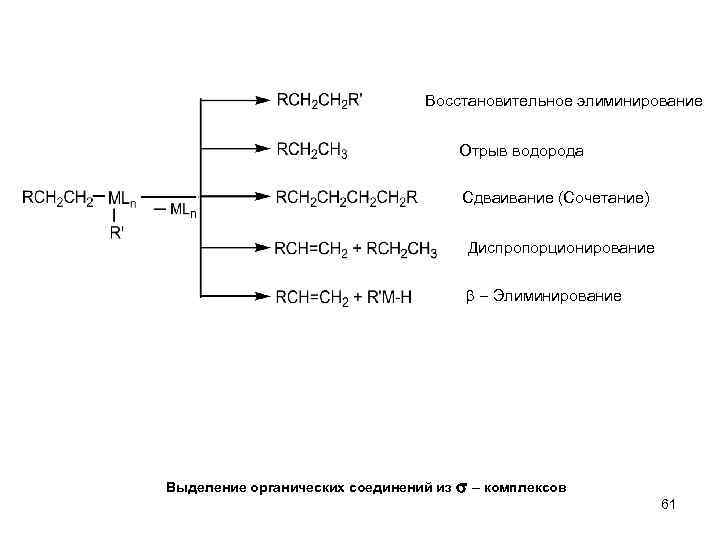 Восстановительное элиминирование Отрыв водорода Сдваивание (Сочетание) Диспропорционирование Элиминирование Выделение органических соединений из комплексов 61
Восстановительное элиминирование Отрыв водорода Сдваивание (Сочетание) Диспропорционирование Элиминирование Выделение органических соединений из комплексов 61


