Металлические и неметаллические покрытия Лекция 8.ppt
- Количество слайдов: 17
 Металлические и неметаллические покрытия Плетнев Михаил Андреевич
Металлические и неметаллические покрытия Плетнев Михаил Андреевич
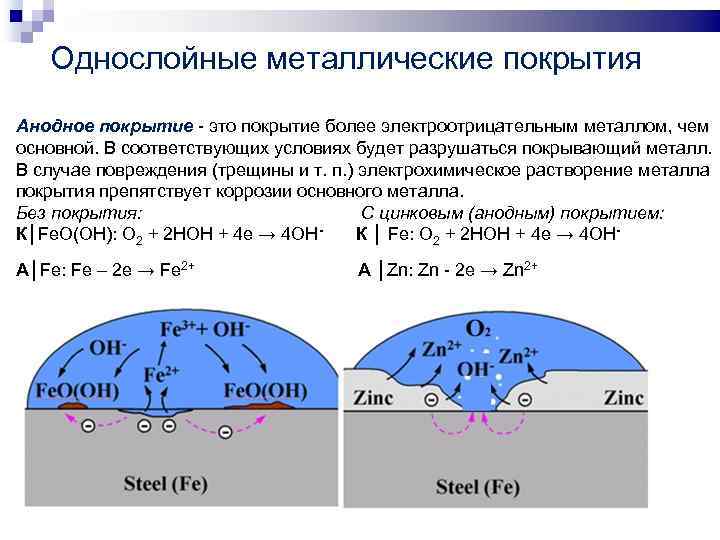 Однослойные металлические покрытия Анодное покрытие - это покрытие более электроотрицательным металлом, чем основной. В соответствующих условиях будет разрушаться покрывающий металл. В случае повреждения (трещины и т. п. ) электрохимическое растворение металла покрытия препятствует коррозии основного металла. Без покрытия: С цинковым (анодным) покрытием: К│Fe. O(OH): O 2 + 2 HOH + 4 e → 4 OH- К │ Fe: O 2 + 2 HOH + 4 e → 4 OHA│Fe: Fe – 2 e → Fe 2+ А │Zn: Zn - 2 e → Zn 2+
Однослойные металлические покрытия Анодное покрытие - это покрытие более электроотрицательным металлом, чем основной. В соответствующих условиях будет разрушаться покрывающий металл. В случае повреждения (трещины и т. п. ) электрохимическое растворение металла покрытия препятствует коррозии основного металла. Без покрытия: С цинковым (анодным) покрытием: К│Fe. O(OH): O 2 + 2 HOH + 4 e → 4 OH- К │ Fe: O 2 + 2 HOH + 4 e → 4 OHA│Fe: Fe – 2 e → Fe 2+ А │Zn: Zn - 2 e → Zn 2+
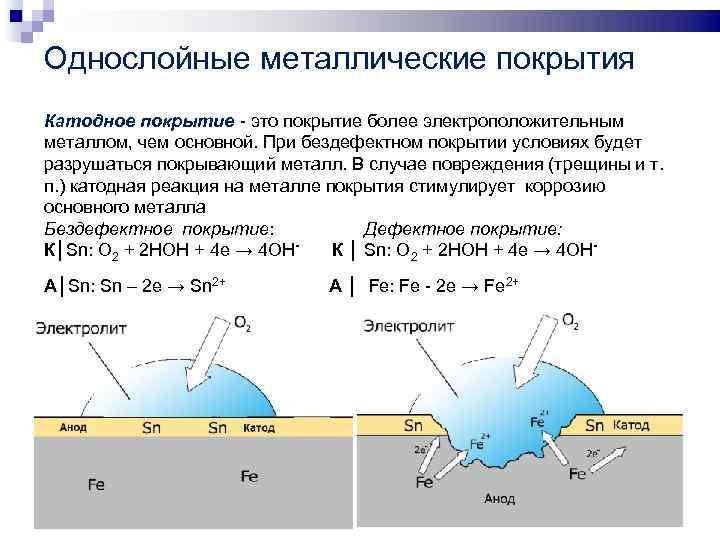 Однослойные металлические покрытия Катодное покрытие - это покрытие более электроположительным металлом, чем основной. При бездефектном покрытии условиях будет разрушаться покрывающий металл. В случае повреждения (трещины и т. п. ) катодная реакция на металле покрытия стимулирует коррозию основного металла Бездефектное покрытие: Дефектное покрытие: К│Sn: O 2 + 2 HOH + 4 e → 4 OH- К │ Sn: O 2 + 2 HOH + 4 e → 4 OHA│Sn: Sn – 2 e → Sn 2+ А │ Fe: Fe - 2 e → Fe 2+
Однослойные металлические покрытия Катодное покрытие - это покрытие более электроположительным металлом, чем основной. При бездефектном покрытии условиях будет разрушаться покрывающий металл. В случае повреждения (трещины и т. п. ) катодная реакция на металле покрытия стимулирует коррозию основного металла Бездефектное покрытие: Дефектное покрытие: К│Sn: O 2 + 2 HOH + 4 e → 4 OH- К │ Sn: O 2 + 2 HOH + 4 e → 4 OHA│Sn: Sn – 2 e → Sn 2+ А │ Fe: Fe - 2 e → Fe 2+
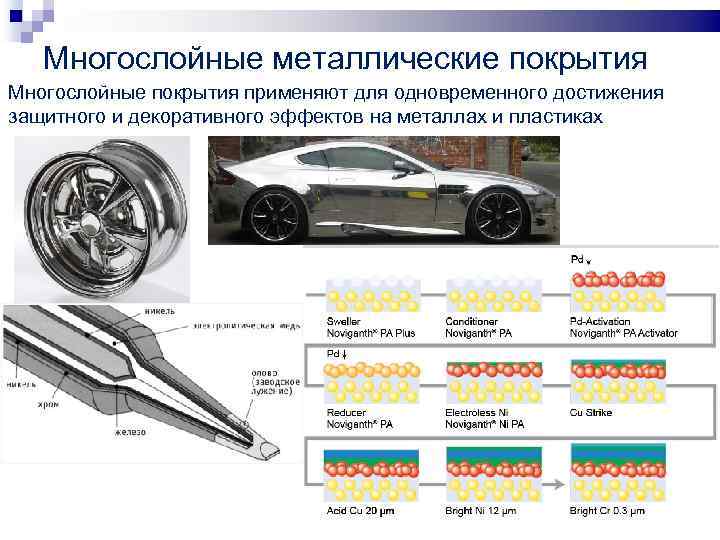 Многослойные металлические покрытия Многослойные покрытия применяют для одновременного достижения защитного и декоративного эффектов на металлах и пластиках
Многослойные металлические покрытия Многослойные покрытия применяют для одновременного достижения защитного и декоративного эффектов на металлах и пластиках
 Неметаллические покрытия Виды неметаллических покрытий: -неорганические (оксидные, фосфатные, эмалевые) -лакокрасочные -битумные и комбинированные на битумной основе -полимерные -комплексные
Неметаллические покрытия Виды неметаллических покрытий: -неорганические (оксидные, фосфатные, эмалевые) -лакокрасочные -битумные и комбинированные на битумной основе -полимерные -комплексные
 Оксидирование Химическое оксидирование осуществляют обработкой изделия в растворах (расплавах) окислителей (хроматы, нитраты и др. ). Fe + [О] + 2 Na. OH Na 2 Fe. О 2 + H 2 О Na 2 Fe. О 2 + Na 2 Fe 2 О 4 + 2 Н 2 О Fe 3 О 4 + 4 Na. OH 1.
Оксидирование Химическое оксидирование осуществляют обработкой изделия в растворах (расплавах) окислителей (хроматы, нитраты и др. ). Fe + [О] + 2 Na. OH Na 2 Fe. О 2 + H 2 О Na 2 Fe. О 2 + Na 2 Fe 2 О 4 + 2 Н 2 О Fe 3 О 4 + 4 Na. OH 1.
 Оксидирование Электрохимическое оксидирование или анодирование - процесс образования оксидной пленки на металле по действием анодной поляризации. Анодирование применяют для получения защитных и декоративных слоев на поверхностях различных металлов и сплавов наиболее часто на алюминии ,
Оксидирование Электрохимическое оксидирование или анодирование - процесс образования оксидной пленки на металле по действием анодной поляризации. Анодирование применяют для получения защитных и декоративных слоев на поверхностях различных металлов и сплавов наиболее часто на алюминии ,
 Фосфатирование, создание химическим путём на поверхности металлических изделий плёнки нерастворимых фосфатов, предохраняющей металл (при дополнительном нанесении лакокрасочного покрытия) от атмосферной коррозии Me + 2 Н 3 РО 4 = Me(H 2 PO 4)2 + H 2↑, в результате которой образуются однозамещенные фосфаты металла. Концентрация ортофосфорной кислоты, а следовательно, кислотность раствора уменьшаются. При этом происходит гидролиз однозамещенных фосфатов с образованием двух- и трехзамещенных солей: Me(H 2 PО 4)2= Ме. НРО 4 + Н 3 РО 4, 3 Ме (Н 2 РО 4)2 =Ме 3 (РО 4) 2↓ + 4 Н 3 РО 4. Плёнка (толщиной 2– 5 мкм) хорошо удерживает смазку, что снижает коэффициент трения; благодаря высокому удельному электрическому сопротивлению фосфатные покрытия выдерживают напряжение 300– 500 в и сохраняют устойчивость до 400– 500 °С. Ф. осуществляется погружением изделий в нагретый до 90– 100 °С раствор фосфатов железа, марганца и цинка.
Фосфатирование, создание химическим путём на поверхности металлических изделий плёнки нерастворимых фосфатов, предохраняющей металл (при дополнительном нанесении лакокрасочного покрытия) от атмосферной коррозии Me + 2 Н 3 РО 4 = Me(H 2 PO 4)2 + H 2↑, в результате которой образуются однозамещенные фосфаты металла. Концентрация ортофосфорной кислоты, а следовательно, кислотность раствора уменьшаются. При этом происходит гидролиз однозамещенных фосфатов с образованием двух- и трехзамещенных солей: Me(H 2 PО 4)2= Ме. НРО 4 + Н 3 РО 4, 3 Ме (Н 2 РО 4)2 =Ме 3 (РО 4) 2↓ + 4 Н 3 РО 4. Плёнка (толщиной 2– 5 мкм) хорошо удерживает смазку, что снижает коэффициент трения; благодаря высокому удельному электрическому сопротивлению фосфатные покрытия выдерживают напряжение 300– 500 в и сохраняют устойчивость до 400– 500 °С. Ф. осуществляется погружением изделий в нагретый до 90– 100 °С раствор фосфатов железа, марганца и цинка.
 Эмалирование Силикатные грунтовые и покровные эмали (фритты) представляют собой силикатное стекло, содержат в основе окислы кремния, бора, натрия, алюминия и т. д. : Si. O 2 + Ca. O → Ca. Si. O 3 Современные эмали состоят из двуокиси кремния Si. O 2, борного ангидрида B 2 O 3, окиси титана Ti. O 2, окиси алюминия Al 2 O 3, окислов щелочных и щёлочноземельных металлов, цинка, свинца, различных фторидов. Эмалевые покрытия используются везде, где надо добиться долговременной химической стойкости покрытия - трубы, химические реакторы и т. д.
Эмалирование Силикатные грунтовые и покровные эмали (фритты) представляют собой силикатное стекло, содержат в основе окислы кремния, бора, натрия, алюминия и т. д. : Si. O 2 + Ca. O → Ca. Si. O 3 Современные эмали состоят из двуокиси кремния Si. O 2, борного ангидрида B 2 O 3, окиси титана Ti. O 2, окиси алюминия Al 2 O 3, окислов щелочных и щёлочноземельных металлов, цинка, свинца, различных фторидов. Эмалевые покрытия используются везде, где надо добиться долговременной химической стойкости покрытия - трубы, химические реакторы и т. д.
 Лакокрасочные покрытия Лаки – коллоидные растворы высыхающих масел, смол, эфиров, целлюлозы в органических растворителях Краски - суспензии минеральных пигментов в органических связующих пленкообразователях. Краски подразделяются: масляные, эмульсионные и эмалевые Грунтовки - это материалы, состоящие из растворителя, связующего и различных добавок. Грунтовки являются обязательным составляющим межслойной подготовки и служат для улучшения адгезии финишных покрытий, экономии последующих слоев ЛКМ, увеличения износостойкости и водостойкости покрытия, защищают основание от вредного воздействия влаги.
Лакокрасочные покрытия Лаки – коллоидные растворы высыхающих масел, смол, эфиров, целлюлозы в органических растворителях Краски - суспензии минеральных пигментов в органических связующих пленкообразователях. Краски подразделяются: масляные, эмульсионные и эмалевые Грунтовки - это материалы, состоящие из растворителя, связующего и различных добавок. Грунтовки являются обязательным составляющим межслойной подготовки и служат для улучшения адгезии финишных покрытий, экономии последующих слоев ЛКМ, увеличения износостойкости и водостойкости покрытия, защищают основание от вредного воздействия влаги.
 Полимерные покрытия а) асфальтобитумные композиции в виде мастик, каменноугольного пека, руберокса с добавкой наполнителей — асбестового волокна, кислотоупорного цемента и др. Мастика наносится на предварительно нагретую поверхность в расплавленном состоянии толщиной слоя 3— 5 мм. Такие покрытия устойчивы в растворах солей (сульфидов и хлоридов), в минеральных кислотах слабой и средней концентрации, в едких щелочах 20%-ной концентрации и в воде; б) фенол-формальдегидные композиции применяются в виде паст или листового материала. Они устойчивы в большинстве органических растворителей и минеральных кислот за исключением азотной, хромовой и серной кислоты высокой концентрации; в) виниловые смолы и фактис, представляющие собой продукт вулканизации растительных масел с хлористой серой, смешанной с наполнителями (окисью магния и бария). 1 – лист стальной 2 – цинковое покрытие 3 – покрытие антикоррозийное 4 – грунтовка 5 – полимерное покрытие (полиэстер, призма и др. ) 6 – защитный лак
Полимерные покрытия а) асфальтобитумные композиции в виде мастик, каменноугольного пека, руберокса с добавкой наполнителей — асбестового волокна, кислотоупорного цемента и др. Мастика наносится на предварительно нагретую поверхность в расплавленном состоянии толщиной слоя 3— 5 мм. Такие покрытия устойчивы в растворах солей (сульфидов и хлоридов), в минеральных кислотах слабой и средней концентрации, в едких щелочах 20%-ной концентрации и в воде; б) фенол-формальдегидные композиции применяются в виде паст или листового материала. Они устойчивы в большинстве органических растворителей и минеральных кислот за исключением азотной, хромовой и серной кислоты высокой концентрации; в) виниловые смолы и фактис, представляющие собой продукт вулканизации растительных масел с хлористой серой, смешанной с наполнителями (окисью магния и бария). 1 – лист стальной 2 – цинковое покрытие 3 – покрытие антикоррозийное 4 – грунтовка 5 – полимерное покрытие (полиэстер, призма и др. ) 6 – защитный лак
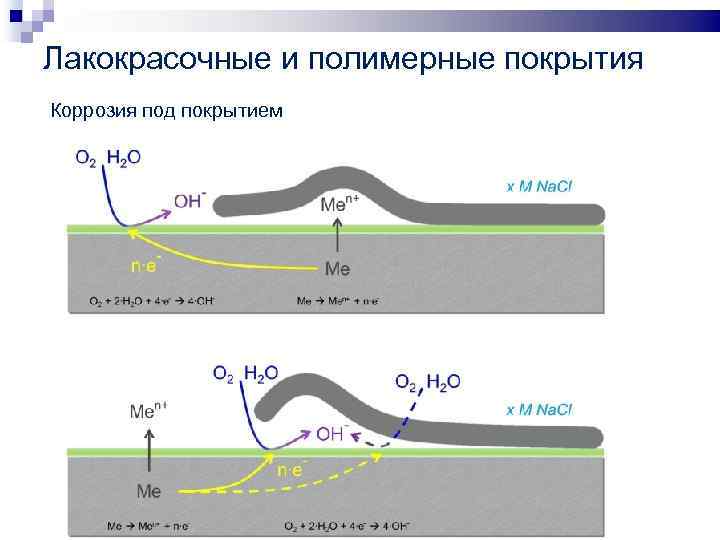 Лакокрасочные и полимерные покрытия Коррозия под покрытием
Лакокрасочные и полимерные покрытия Коррозия под покрытием
 Ингибиторы коррозии Согласно стандарту ISO 8044 -1986, ингибиторами коррозии (ИК) называют химические соединения, которые, присутствуя в коррозионной системе в достаточной концентрации, уменьшают скорость коррозии без значительного изменения концентрации любого коррозионного реагента. Эффективность ингибиторов коррозии оценивается степенью защиты Z (в %) (относительный показатель) и коэффициентом торможения Υ (абсолютный показатель) и определяется по формулам: Z = [(K 1– K 2)/K 1]· 100% = [(i 1 – i 2)/i 1] · 100 % Z = (1 – 1/ γ) · 100%. γ = K 1/K 2 = i 1/i 2
Ингибиторы коррозии Согласно стандарту ISO 8044 -1986, ингибиторами коррозии (ИК) называют химические соединения, которые, присутствуя в коррозионной системе в достаточной концентрации, уменьшают скорость коррозии без значительного изменения концентрации любого коррозионного реагента. Эффективность ингибиторов коррозии оценивается степенью защиты Z (в %) (относительный показатель) и коэффициентом торможения Υ (абсолютный показатель) и определяется по формулам: Z = [(K 1– K 2)/K 1]· 100% = [(i 1 – i 2)/i 1] · 100 % Z = (1 – 1/ γ) · 100%. γ = K 1/K 2 = i 1/i 2
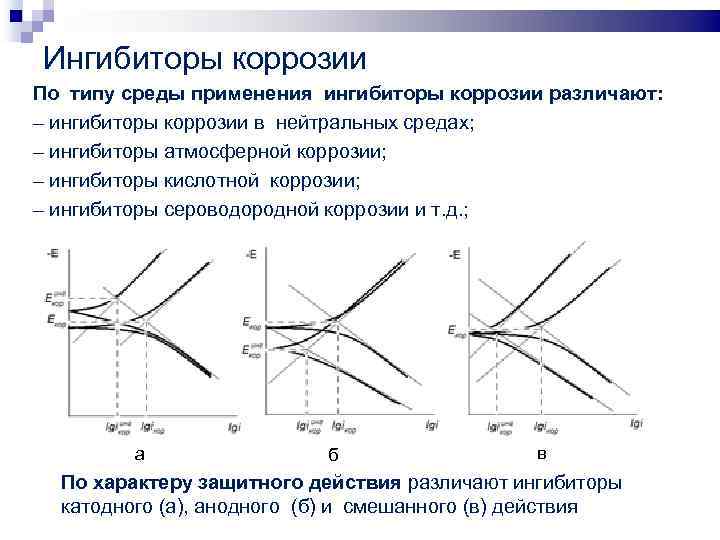 Ингибиторы коррозии По типу среды применения ингибиторы коррозии различают: – ингибиторы коррозии в нейтральных средах; – ингибиторы атмосферной коррозии; – ингибиторы кислотной коррозии; – ингибиторы сероводородной коррозии и т. д. ; а б в По характеру защитного действия различают ингибиторы катодного (а), анодного (б) и смешанного (в) действия
Ингибиторы коррозии По типу среды применения ингибиторы коррозии различают: – ингибиторы коррозии в нейтральных средах; – ингибиторы атмосферной коррозии; – ингибиторы кислотной коррозии; – ингибиторы сероводородной коррозии и т. д. ; а б в По характеру защитного действия различают ингибиторы катодного (а), анодного (б) и смешанного (в) действия
 Ингибиторы коррозии - это, как правило, композиции из неорганических или (и) органических соединений. Ингибиторы кислотной и сероводородной коррозии: Среди них наиболее эффективны амиды и амины или их производные, в т. ч. гетероалкилированные, четвертичные соединения аммония и фосфония, высокомолярные и ацетиленовые спирты, некоторые альдегиды и многие серосодержащие соединения. Механизм действия – адсорбция на границе металл-коррозионная среда и торможение скорости коррозионных процессов (катодного, анодного или обоих)
Ингибиторы коррозии - это, как правило, композиции из неорганических или (и) органических соединений. Ингибиторы кислотной и сероводородной коррозии: Среди них наиболее эффективны амиды и амины или их производные, в т. ч. гетероалкилированные, четвертичные соединения аммония и фосфония, высокомолярные и ацетиленовые спирты, некоторые альдегиды и многие серосодержащие соединения. Механизм действия – адсорбция на границе металл-коррозионная среда и торможение скорости коррозионных процессов (катодного, анодного или обоих)
 Ингибиторы атмосферной коррозии Летучие ингибиторы коррозии (ЛИК) Метод ингибирования коррозии с помощью ЛИК материалов основан на свойстве некоторых веществ, добавленных в малых количествах в коррозионную среду, тормозить или полностью подавлять коррозионные процессы. Существует большой класс органических соединений, используемых в качестве летучих ингибиторов коррозии - аминокарбоксилатов, давление насыщенных паров которых лежит в диапазоне: Р = 10 -3 -10 -5 мм рт. ст. Этот класс соединений характеризуется способностью к хемосорбции на поверхности черных и цветных металлов.
Ингибиторы атмосферной коррозии Летучие ингибиторы коррозии (ЛИК) Метод ингибирования коррозии с помощью ЛИК материалов основан на свойстве некоторых веществ, добавленных в малых количествах в коррозионную среду, тормозить или полностью подавлять коррозионные процессы. Существует большой класс органических соединений, используемых в качестве летучих ингибиторов коррозии - аминокарбоксилатов, давление насыщенных паров которых лежит в диапазоне: Р = 10 -3 -10 -5 мм рт. ст. Этот класс соединений характеризуется способностью к хемосорбции на поверхности черных и цветных металлов.
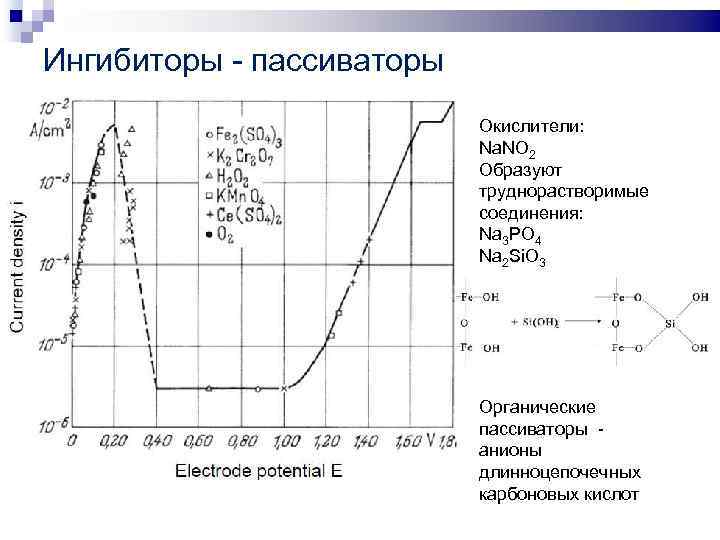 Ингибиторы - пассиваторы Окислители: Na. NO 2 Образуют труднорастворимые соединения: Na 3 PO 4 Na 2 Si. O 3 Органические пассиваторы - анионы длинноцепочечных карбоновых кислот
Ингибиторы - пассиваторы Окислители: Na. NO 2 Образуют труднорастворимые соединения: Na 3 PO 4 Na 2 Si. O 3 Органические пассиваторы - анионы длинноцепочечных карбоновых кислот


