3-А гр.ppt
- Количество слайдов: 25
 Металлические элементы 3 -А группы
Металлические элементы 3 -А группы
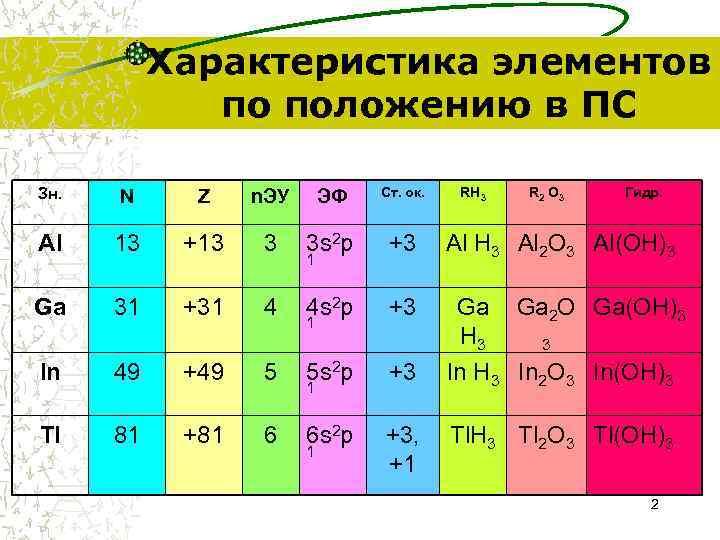 Характеристика элементов по положению в ПС Зн. N Z n. ЭУ ЭФ Ст. ок. Al 13 +13 3 3 s 2 p +3 Ga 31 +31 4 4 s 2 p +3 1 1 RH 3 R 2 O 3 Гидр. Al Н 3 Al 2 O 3 Al(ОН)3 Ga Н 3 Ga 2 O Ga(ОН)3 3 In 49 +49 5 5 s 2 p +3 In Н 3 In 2 O 3 In(ОН)3 Tl 81 +81 6 6 s 2 p +3, +1 Tl. Н 3 Tl 2 O 3 Tl(ОН)3 1 1 2
Характеристика элементов по положению в ПС Зн. N Z n. ЭУ ЭФ Ст. ок. Al 13 +13 3 3 s 2 p +3 Ga 31 +31 4 4 s 2 p +3 1 1 RH 3 R 2 O 3 Гидр. Al Н 3 Al 2 O 3 Al(ОН)3 Ga Н 3 Ga 2 O Ga(ОН)3 3 In 49 +49 5 5 s 2 p +3 In Н 3 In 2 O 3 In(ОН)3 Tl 81 +81 6 6 s 2 p +3, +1 Tl. Н 3 Tl 2 O 3 Tl(ОН)3 1 1 2
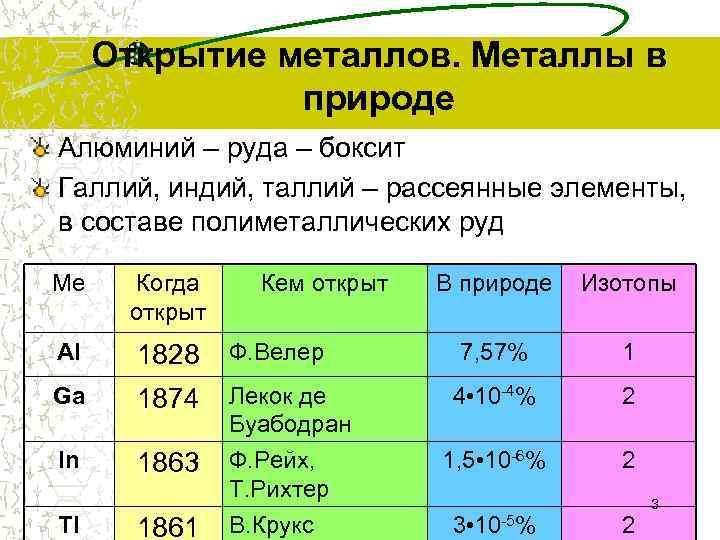 Открытие металлов. Металлы в природе Алюминий – руда – боксит Галлий, индий, таллий – рассеянные элементы, в составе полиметаллических руд Ме Когда открыт Al 1828 Ф. Велер Ga 1874 Лекок де Буабодран In 1863 Ф. Рейх, Т. Рихтер В. Крукс Tl 1861 Кем открыт В природе Изотопы 7, 57% 1 4 • 10 -4% 2 1, 5 • 10 -6% 2 3 • 10 -5% 2 3
Открытие металлов. Металлы в природе Алюминий – руда – боксит Галлий, индий, таллий – рассеянные элементы, в составе полиметаллических руд Ме Когда открыт Al 1828 Ф. Велер Ga 1874 Лекок де Буабодран In 1863 Ф. Рейх, Т. Рихтер В. Крукс Tl 1861 Кем открыт В природе Изотопы 7, 57% 1 4 • 10 -4% 2 1, 5 • 10 -6% 2 3 • 10 -5% 2 3
![Получение металлов Al – электролиз расплава оксида с добавлением криолита Na 3[Al. F 6] Получение металлов Al – электролиз расплава оксида с добавлением криолита Na 3[Al. F 6]](https://present5.com/presentation/3/-20477212_164674107.pdf-img/-20477212_164674107.pdf-4.jpg) Получение металлов Al – электролиз расплава оксида с добавлением криолита Na 3[Al. F 6] Ga, In, Tl - рассеянные элементы, для выделения используют пирометаллургические, гидрометаллургические и электролитические методы 4
Получение металлов Al – электролиз расплава оксида с добавлением криолита Na 3[Al. F 6] Ga, In, Tl - рассеянные элементы, для выделения используют пирометаллургические, гидрометаллургические и электролитические методы 4
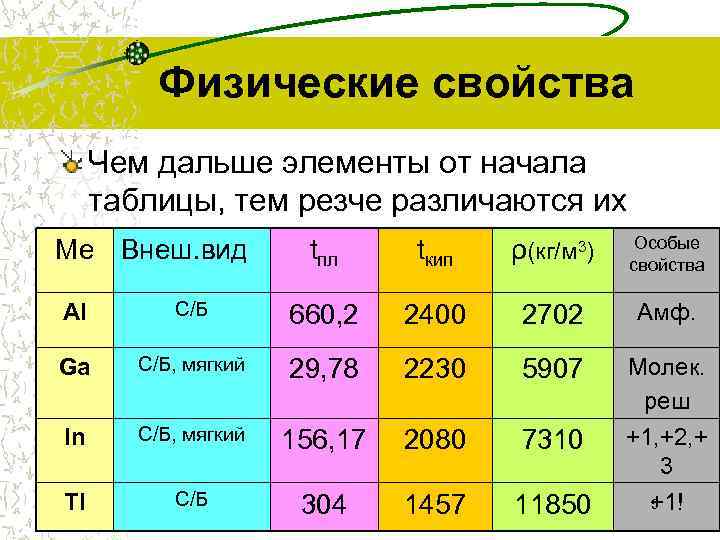 Физические свойства Чем дальше элементы от начала таблицы, тем резче различаются их свойства… Ме Внеш. вид t t ρ(кг/м 3) Особые пл кип свойства Al С/Б 660, 2 2400 2702 Амф. Ga С/Б, мягкий 29, 78 2230 5907 Молек. реш In С/Б, мягкий 156, 17 2080 7310 Tl С/Б 304 1457 11850 +1, +2, + 3 5 +1!
Физические свойства Чем дальше элементы от начала таблицы, тем резче различаются их свойства… Ме Внеш. вид t t ρ(кг/м 3) Особые пл кип свойства Al С/Б 660, 2 2400 2702 Амф. Ga С/Б, мягкий 29, 78 2230 5907 Молек. реш In С/Б, мягкий 156, 17 2080 7310 Tl С/Б 304 1457 11850 +1, +2, + 3 5 +1!
 Характеристика химических свойств элементов и их соединений Алюминий Галлий Индий Таллий
Характеристика химических свойств элементов и их соединений Алюминий Галлий Индий Таллий
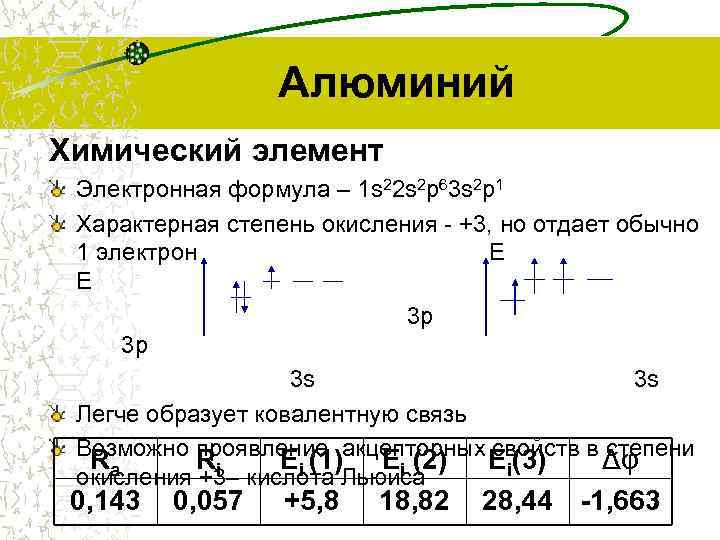 Алюминий Химический элемент Электронная формула – 1 s 22 s 2 p 63 s 2 p 1 Характерная степень окисления - +3, но отдает обычно 1 электрон E E 3 p 3 p 3 s 3 s Легче образует ковалентную связь Возможно проявление акцепторных свойств в степени Ra Ri Ei (1) Ei (2) Ei(3) Δφ окисления +3– кислота Льюиса 0, 143 0, 057 +5, 8 18, 82 28, 44 7 -1, 663
Алюминий Химический элемент Электронная формула – 1 s 22 s 2 p 63 s 2 p 1 Характерная степень окисления - +3, но отдает обычно 1 электрон E E 3 p 3 p 3 s 3 s Легче образует ковалентную связь Возможно проявление акцепторных свойств в степени Ra Ri Ei (1) Ei (2) Ei(3) Δφ окисления +3– кислота Льюиса 0, 143 0, 057 +5, 8 18, 82 28, 44 7 -1, 663
 Алюминий Простое вещество 1. Взаимодействие с кислотами: 2 Al + 6 H+ = Al 3+ + 3 H 2 2. Взаимодействие с водой: 2 Al + 6 H 2 О = 2 Al(ОН)3 + 3 H 2 3. Взаимодействие с кислородом: 4 Al + 3 О 2 = 2 Al 2 О 3; ΔН = -1676 к. Дж/моль, tпл = 20500 С 4. Взаимодействие с галогенами: 2 Al +3 Gal 2 = 2 Al. Gal 3 5. Взаимодействие с оксидами металлов: 2 Al +Fe 2 O 3 = 2 Fe + Al 2 O 3 8
Алюминий Простое вещество 1. Взаимодействие с кислотами: 2 Al + 6 H+ = Al 3+ + 3 H 2 2. Взаимодействие с водой: 2 Al + 6 H 2 О = 2 Al(ОН)3 + 3 H 2 3. Взаимодействие с кислородом: 4 Al + 3 О 2 = 2 Al 2 О 3; ΔН = -1676 к. Дж/моль, tпл = 20500 С 4. Взаимодействие с галогенами: 2 Al +3 Gal 2 = 2 Al. Gal 3 5. Взаимодействие с оксидами металлов: 2 Al +Fe 2 O 3 = 2 Fe + Al 2 O 3 8
 Оксид алюминия Al 2 O 3 – типичный амфотерный оксид С кислотами образует соли: Al 2 О 3 + 3 H+ = 2 Al 3+ + 3 H 2 О, в растворе – [Al(H 2 О)6 ]3+ С растворами щелочей образует комплексные соединения: Al 2 О 3 + 2 Na. OH + 7 H 2 О = 2 Na[Al(OH)4 (H 2 О)2 ] При сплавлении со щелочами образует безводные метаалюминаты: Al 2 О 3 + 2 Na. OH = 2 Na. Al. О 2 Взаимодействует с кислотными и основными оксидами с образованием солей: Al 2 О 3 + 3 N 2 O 5 = 2 Al(NO 3)3 ; Al 2 О 3 + Сa. O = Сa(Al. О)2 9 Взаимодействует с солями, растворы которых имеют кислую или щелочную среду:
Оксид алюминия Al 2 O 3 – типичный амфотерный оксид С кислотами образует соли: Al 2 О 3 + 3 H+ = 2 Al 3+ + 3 H 2 О, в растворе – [Al(H 2 О)6 ]3+ С растворами щелочей образует комплексные соединения: Al 2 О 3 + 2 Na. OH + 7 H 2 О = 2 Na[Al(OH)4 (H 2 О)2 ] При сплавлении со щелочами образует безводные метаалюминаты: Al 2 О 3 + 2 Na. OH = 2 Na. Al. О 2 Взаимодействует с кислотными и основными оксидами с образованием солей: Al 2 О 3 + 3 N 2 O 5 = 2 Al(NO 3)3 ; Al 2 О 3 + Сa. O = Сa(Al. О)2 9 Взаимодействует с солями, растворы которых имеют кислую или щелочную среду:
 Гидроксид алюминия Типичный амфотерный гидроксид С кислотами образует соли: Al(ОН)3 + 3 H 3 О+ = [Al(H 2 О)6 ]3+ С растворами щелочей образует соли: Al(ОН)3 + 3 Na. OH = Na 3[Al(OH)6 ] Термически неустойчив: Al(ОН)3 = Al. О(ОН) + Н 2 О – метагидроксид, t = 2000 С 2 Al. О(ОН) = Al 2 О 3 + Н 2 О, t = 4000 С При сплавлении со щелочами образуются соли орто- и метаалюминиевых кислот: Al(ОН)3 + КОН = К Al. О 2 + 2 Н 2 О 10
Гидроксид алюминия Типичный амфотерный гидроксид С кислотами образует соли: Al(ОН)3 + 3 H 3 О+ = [Al(H 2 О)6 ]3+ С растворами щелочей образует соли: Al(ОН)3 + 3 Na. OH = Na 3[Al(OH)6 ] Термически неустойчив: Al(ОН)3 = Al. О(ОН) + Н 2 О – метагидроксид, t = 2000 С 2 Al. О(ОН) = Al 2 О 3 + Н 2 О, t = 4000 С При сплавлении со щелочами образуются соли орто- и метаалюминиевых кислот: Al(ОН)3 + КОН = К Al. О 2 + 2 Н 2 О 10
 Соли алюминия Галогениды – белые кристаллические, хорошо растворимы в воде, гидролизуются по катиону, Al. Cl 3 – промышленный катализатор Сульфат алюминия - Al 2(SО 4)3 • 18 Н 2 О – бесцветное кристаллическое вещество, хорошо растворим, используется для протравки тканей перед крашением и для удаления из воды взвешенных примесей (коагулянт) 11 Природные алюмосиликаты – драгоценные
Соли алюминия Галогениды – белые кристаллические, хорошо растворимы в воде, гидролизуются по катиону, Al. Cl 3 – промышленный катализатор Сульфат алюминия - Al 2(SО 4)3 • 18 Н 2 О – бесцветное кристаллическое вещество, хорошо растворим, используется для протравки тканей перед крашением и для удаления из воды взвешенных примесей (коагулянт) 11 Природные алюмосиликаты – драгоценные
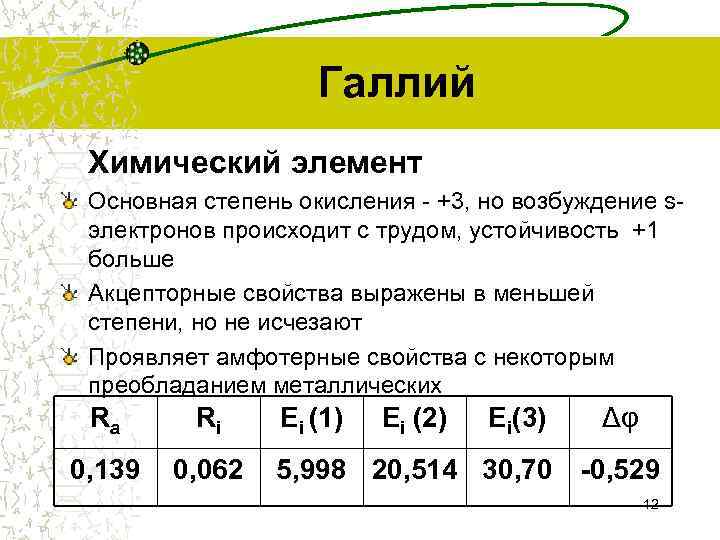 Галлий Химический элемент Основная степень окисления - +3, но возбуждение sэлектронов происходит с трудом, устойчивость +1 больше Акцепторные свойства выражены в меньшей степени, но не исчезают Проявляет амфотерные свойства с некоторым преобладанием металлических Ra Ri 0, 139 0, 062 Ei (1) Ei (2) Ei(3) 5, 998 20, 514 30, 70 Δφ -0, 529 12
Галлий Химический элемент Основная степень окисления - +3, но возбуждение sэлектронов происходит с трудом, устойчивость +1 больше Акцепторные свойства выражены в меньшей степени, но не исчезают Проявляет амфотерные свойства с некоторым преобладанием металлических Ra Ri 0, 139 0, 062 Ei (1) Ei (2) Ei(3) 5, 998 20, 514 30, 70 Δφ -0, 529 12
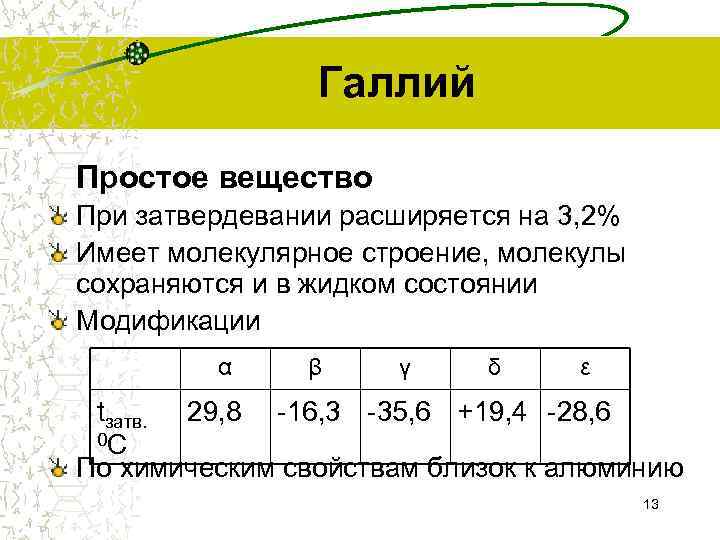 Галлий Простое вещество При затвердевании расширяется на 3, 2% Имеет молекулярное строение, молекулы сохраняются и в жидком состоянии Модификации α β γ δ ε tзатв. 29, 8 -16, 3 -35, 6 +19, 4 -28, 6 0 С По химическим свойствам близок к алюминию 13
Галлий Простое вещество При затвердевании расширяется на 3, 2% Имеет молекулярное строение, молекулы сохраняются и в жидком состоянии Модификации α β γ δ ε tзатв. 29, 8 -16, 3 -35, 6 +19, 4 -28, 6 0 С По химическим свойствам близок к алюминию 13
 Оксиды галлия Ga 2 O 3 – типичный амфотерный оксид, по свойствам аналогичен оксиду алюминия (К. Ч. =4), получается непосредственным взаимодействием с кислородом, образует пленку на поверхности металла Ga 2 O – темно-коричневый, почти черный: Ga 2 O 3 + 4 Ga = 3 Ga 2 O Сильный восстановитель: 2 Ga 2 O + 7 H 2 SO 4 = 2 Ga 2(SO 4)3 + H 2 S +146
Оксиды галлия Ga 2 O 3 – типичный амфотерный оксид, по свойствам аналогичен оксиду алюминия (К. Ч. =4), получается непосредственным взаимодействием с кислородом, образует пленку на поверхности металла Ga 2 O – темно-коричневый, почти черный: Ga 2 O 3 + 4 Ga = 3 Ga 2 O Сильный восстановитель: 2 Ga 2 O + 7 H 2 SO 4 = 2 Ga 2(SO 4)3 + H 2 S +146
 Гидроксид галлия Ga(OН)3 – идеально амфотерен, осадок белого цвета, аналог гидроксида алюминия При взаимодействии с растворами щелочей образует галлаты (координационные соединения), причем осадок должен быть свежим, координационное число равно 4 Может быть получен взаимодействием 15 оксида с водой
Гидроксид галлия Ga(OН)3 – идеально амфотерен, осадок белого цвета, аналог гидроксида алюминия При взаимодействии с растворами щелочей образует галлаты (координационные соединения), причем осадок должен быть свежим, координационное число равно 4 Может быть получен взаимодействием 15 оксида с водой
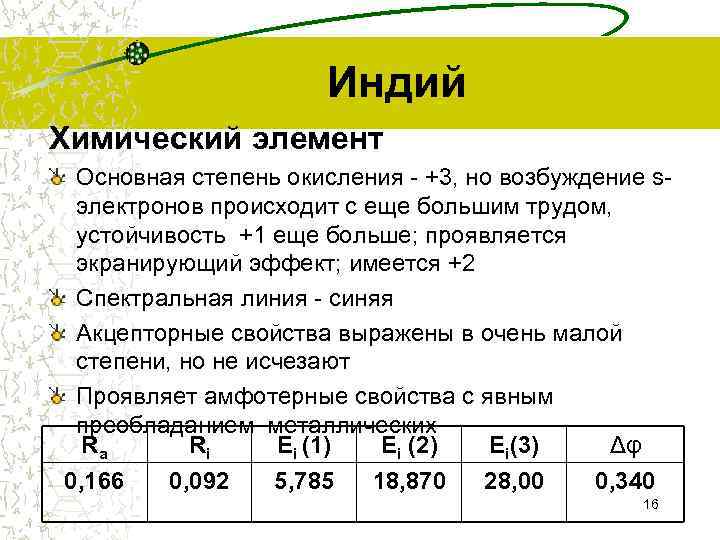 Индий Химический элемент Основная степень окисления - +3, но возбуждение sэлектронов происходит с еще большим трудом, устойчивость +1 еще больше; проявляется экранирующий эффект; имеется +2 Спектральная линия - синяя Акцепторные свойства выражены в очень малой степени, но не исчезают Проявляет амфотерные свойства с явным преобладанием металлических Ra Ri Ei (1) Ei (2) Ei(3) Δφ 0, 166 0, 092 5, 785 18, 870 28, 00 0, 340 16
Индий Химический элемент Основная степень окисления - +3, но возбуждение sэлектронов происходит с еще большим трудом, устойчивость +1 еще больше; проявляется экранирующий эффект; имеется +2 Спектральная линия - синяя Акцепторные свойства выражены в очень малой степени, но не исчезают Проявляет амфотерные свойства с явным преобладанием металлических Ra Ri Ei (1) Ei (2) Ei(3) Δφ 0, 166 0, 092 5, 785 18, 870 28, 00 0, 340 16
 Индий Простое вещество 1. Неординарное сочетание мягкости, прочности и хрупкости: в 20 раз пластичнее золота как графит, оставляет черную черту на бумаге при ударе может разрушаться, прочность на разрыв в 6 раз меньше, чем у свинца 2. По химическим свойствам – металл, расположен в РАМ между железом и оловом, взаимодействует с кислотами: 2 In + 6 HCl =2 In. Cl 3 + 3 H 2 3. Со щелочами образует индаты – Ме 3[In(OH)6] • 2 H 2 O 4. С кислородом и неметаллами взаимодействует при 17 нагревании с образованием соединений In+3
Индий Простое вещество 1. Неординарное сочетание мягкости, прочности и хрупкости: в 20 раз пластичнее золота как графит, оставляет черную черту на бумаге при ударе может разрушаться, прочность на разрыв в 6 раз меньше, чем у свинца 2. По химическим свойствам – металл, расположен в РАМ между железом и оловом, взаимодействует с кислотами: 2 In + 6 HCl =2 In. Cl 3 + 3 H 2 3. Со щелочами образует индаты – Ме 3[In(OH)6] • 2 H 2 O 4. С кислородом и неметаллами взаимодействует при 17 нагревании с образованием соединений In+3
 Оксиды индия Трем степеням окисления соответствуют три оксида: In 2 О 3 , In. О, In 2 О 3: 4 In + 3 О 2 = 2 In 2 О 3; ΔН = -928 к. Дж/моль вещество желтого цвета, при 8500 С переходит в In 3 О 4 In. О – в твердом состоянии не обнаружен, не изучен, получается в парáх: In О = In. О + О 18
Оксиды индия Трем степеням окисления соответствуют три оксида: In 2 О 3 , In. О, In 2 О 3: 4 In + 3 О 2 = 2 In 2 О 3; ΔН = -928 к. Дж/моль вещество желтого цвета, при 8500 С переходит в In 3 О 4 In. О – в твердом состоянии не обнаружен, не изучен, получается в парáх: In О = In. О + О 18
 Гидроксид индия In(ОН)3 По внешнему виду похож на гидроксид алюминия Обладает амфотерными свойствами, но в кислотах растворяется легче, в щелочах – при высоких концентрациях и нагревании При нагревании разлагается с образованием оксида 19
Гидроксид индия In(ОН)3 По внешнему виду похож на гидроксид алюминия Обладает амфотерными свойствами, но в кислотах растворяется легче, в щелочах – при высоких концентрациях и нагревании При нагревании разлагается с образованием оксида 19
 Соединения индия Используются редко, только в лабораторной практике Ионы индия – In 3+ - бесцветны, в растворах гидратированы (К. Ч. =6) Соли подвергаются гидролизу по катиону Наиболее интересны: 1. Нитрат – In(NO 3)3 – при нагревании разлагается с образованием оксида, возгоняется 2. Хлорид – In. Cl 3 – возгоняется без разложения 3. Сульфат – In 2(SO 4)3 – образует 20 кристаллогидраты – квасцы со щелочными
Соединения индия Используются редко, только в лабораторной практике Ионы индия – In 3+ - бесцветны, в растворах гидратированы (К. Ч. =6) Соли подвергаются гидролизу по катиону Наиболее интересны: 1. Нитрат – In(NO 3)3 – при нагревании разлагается с образованием оксида, возгоняется 2. Хлорид – In. Cl 3 – возгоняется без разложения 3. Сульфат – In 2(SO 4)3 – образует 20 кристаллогидраты – квасцы со щелочными
 Таллий Химический элемент Основная степень окисления - +1, но имеется и +3 причина – сильное не только d- но и fсжатие Акцепторные свойства. Eприсутствуют, к. ч. Ra Ri Ei (1) Ei(3) Δφ i (2) =6, 7, 8 0, 171 0, 136 6, 108 20, 428 29, 80 Проявляет металлические свойства 0, 340 0, 105 21
Таллий Химический элемент Основная степень окисления - +1, но имеется и +3 причина – сильное не только d- но и fсжатие Акцепторные свойства. Eприсутствуют, к. ч. Ra Ri Ei (1) Ei(3) Δφ i (2) =6, 7, 8 0, 171 0, 136 6, 108 20, 428 29, 80 Проявляет металлические свойства 0, 340 0, 105 21
 Таллий Простое вещество 1. Белый металл с голубоватым оттенком: 2. По химическим свойствам – металл, расположен в РАМ до водорода, сравним со щелочными металлами: взаимодействует с водой: 2 Tl + H 2 O + O = 2 Tl. OH вытесняет водород из спиртов: 2 Tl +2 C 2 H 5 OH + O = 2 C 2 H 5 OTl + H 2 O взаимодействует с кислотами (кроме соляной, хлорид не растворим) 3. Со щелочами не взаимодействует 4. С кислородом и неметаллами взаимодействует при 22 +1 нагревании с образованием соединений In
Таллий Простое вещество 1. Белый металл с голубоватым оттенком: 2. По химическим свойствам – металл, расположен в РАМ до водорода, сравним со щелочными металлами: взаимодействует с водой: 2 Tl + H 2 O + O = 2 Tl. OH вытесняет водород из спиртов: 2 Tl +2 C 2 H 5 OH + O = 2 C 2 H 5 OTl + H 2 O взаимодействует с кислотами (кроме соляной, хлорид не растворим) 3. Со щелочами не взаимодействует 4. С кислородом и неметаллами взаимодействует при 22 +1 нагревании с образованием соединений In
 Оксиды и гидроксиды таллия 1. Tl 2 O – вещество черного цвета, основный оксид 2. Tl 2 O 3 – вещество бурого цвета, основный оксид 3. Tl 3 O 4 – промежуточный оксид Tl 2 O + О 2 Tl 2 O 3 Гидроксиды Tl. OН – аналогичен гидроксидам щелочных металлов; вещество желтого цвета, устойчив, раствор поглощает СО 2 Tl(OН)3 – неустойчив, осадок бурого цвета, основание Из соединений интересны галогениды – образуют 23 комплексы между собой: 3 Tl. Cl = Tl[Tl. Cl ]+Cl
Оксиды и гидроксиды таллия 1. Tl 2 O – вещество черного цвета, основный оксид 2. Tl 2 O 3 – вещество бурого цвета, основный оксид 3. Tl 3 O 4 – промежуточный оксид Tl 2 O + О 2 Tl 2 O 3 Гидроксиды Tl. OН – аналогичен гидроксидам щелочных металлов; вещество желтого цвета, устойчив, раствор поглощает СО 2 Tl(OН)3 – неустойчив, осадок бурого цвета, основание Из соединений интересны галогениды – образуют 23 комплексы между собой: 3 Tl. Cl = Tl[Tl. Cl ]+Cl
 Применение 1. Алюминий – сплавы, электротехника 2. Галлий – полупроводники, оптика 3. Индий – полупроводники, легкоплавкие сплавы, отражатели, атомная энергетика 4. Таллий – яды-зооциды, оптика, низкотемпературные сплавы, кислотоустойчивые сплавы 24
Применение 1. Алюминий – сплавы, электротехника 2. Галлий – полупроводники, оптика 3. Индий – полупроводники, легкоплавкие сплавы, отражатели, атомная энергетика 4. Таллий – яды-зооциды, оптика, низкотемпературные сплавы, кислотоустойчивые сплавы 24
 Спасибо за внимание! 25
Спасибо за внимание! 25


