2-А гр.ppt
- Количество слайдов: 20
 Металлические элементы 2 -А группы Щелочноземельные металлы
Металлические элементы 2 -А группы Щелочноземельные металлы
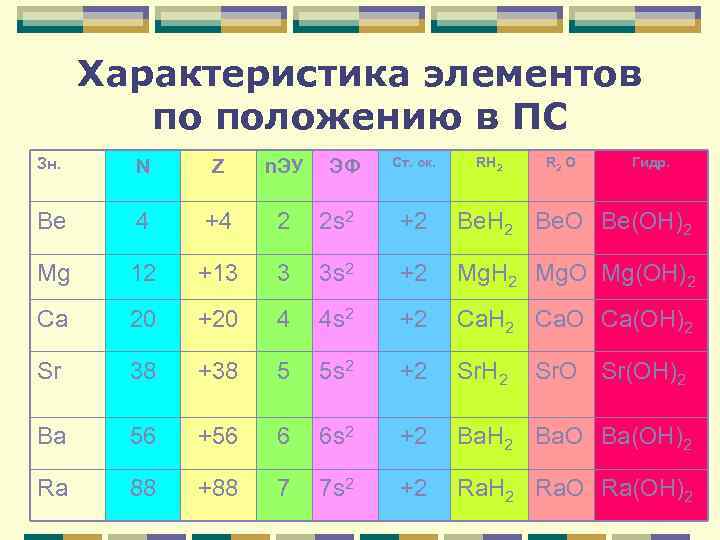 Характеристика элементов по положению в ПС Ст. ок. RH 2 R 2 O Гидр. Зн. N Z n. ЭУ Be 4 +4 2 2 s 2 +2 Be. Н 2 Be. О Be(ОН)2 Mg 12 +13 3 3 s 2 +2 Mg. Н 2 Mg. О Mg(ОН)2 Ca 20 +20 4 4 s 2 +2 Ca. Н 2 Ca. О Ca(ОН)2 Sr 38 +38 5 5 s 2 +2 Sr. Н 2 Ba 56 +56 6 6 s 2 +2 Ba. Н 2 Ba. О Ba(ОН)2 Ra 88 +88 7 7 s 2 +2 Ra. Н 2 Ra. О Ra(ОН)2 ЭФ Sr. О Sr(ОН)2
Характеристика элементов по положению в ПС Ст. ок. RH 2 R 2 O Гидр. Зн. N Z n. ЭУ Be 4 +4 2 2 s 2 +2 Be. Н 2 Be. О Be(ОН)2 Mg 12 +13 3 3 s 2 +2 Mg. Н 2 Mg. О Mg(ОН)2 Ca 20 +20 4 4 s 2 +2 Ca. Н 2 Ca. О Ca(ОН)2 Sr 38 +38 5 5 s 2 +2 Sr. Н 2 Ba 56 +56 6 6 s 2 +2 Ba. Н 2 Ba. О Ba(ОН)2 Ra 88 +88 7 7 s 2 +2 Ra. Н 2 Ra. О Ra(ОН)2 ЭФ Sr. О Sr(ОН)2
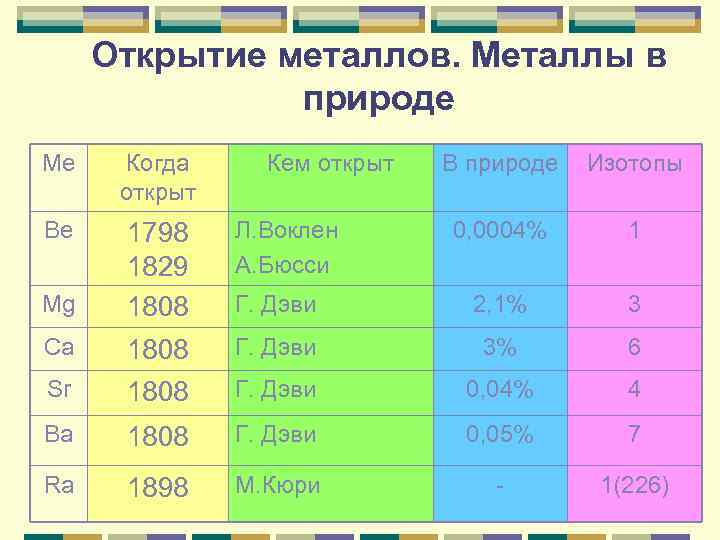 Открытие металлов. Металлы в природе Ме Когда открыт Кем открыт В природе Изотопы Be Л. Воклен А. Бюсси Mg 1798 1829 1808 0, 0004% 1 Г. Дэви 2, 1% 3 Ca 1808 Г. Дэви 3% 6 Sr 1808 Г. Дэви 0, 04% 4 Ba 1808 Г. Дэви 0, 05% 7 Ra 1898 М. Кюри - 1(226)
Открытие металлов. Металлы в природе Ме Когда открыт Кем открыт В природе Изотопы Be Л. Воклен А. Бюсси Mg 1798 1829 1808 0, 0004% 1 Г. Дэви 2, 1% 3 Ca 1808 Г. Дэви 3% 6 Sr 1808 Г. Дэви 0, 04% 4 Ba 1808 Г. Дэви 0, 05% 7 Ra 1898 М. Кюри - 1(226)
 Получение металлов Ве: восстановление фторида бериллия металлическим магнием Mg: восстановление из оксида углем и электролиз хлорида Са: электролиз хлорида Sr: восстановление алюминием из оксида Ba: электролиз хлорида, восстановление алюминием из оксида Ra: ядерный синтез
Получение металлов Ве: восстановление фторида бериллия металлическим магнием Mg: восстановление из оксида углем и электролиз хлорида Са: электролиз хлорида Sr: восстановление алюминием из оксида Ba: электролиз хлорида, восстановление алюминием из оксида Ra: ядерный синтез
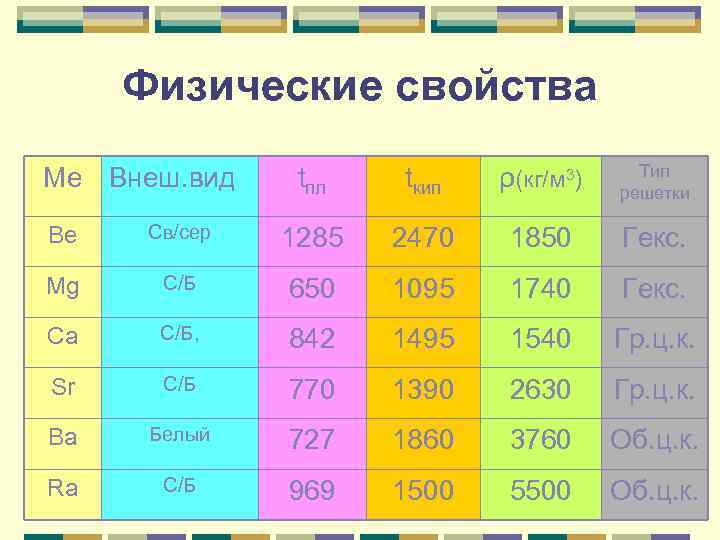 Физические свойства Ме Внеш. вид tпл tкип ρ(кг/м 3) Тип решетки Be Св/сер 1285 2470 1850 Гекс. Mg С/Б 650 1095 1740 Гекс. Ca С/Б, 842 1495 1540 Гр. ц. к. Sr С/Б 770 1390 2630 Гр. ц. к. Ba Белый 727 1860 3760 Об. ц. к. Ra С/Б 969 1500 5500 Об. ц. к.
Физические свойства Ме Внеш. вид tпл tкип ρ(кг/м 3) Тип решетки Be Св/сер 1285 2470 1850 Гекс. Mg С/Б 650 1095 1740 Гекс. Ca С/Б, 842 1495 1540 Гр. ц. к. Sr С/Б 770 1390 2630 Гр. ц. к. Ba Белый 727 1860 3760 Об. ц. к. Ra С/Б 969 1500 5500 Об. ц. к.
 Химические свойства Общая характеристика восстановительных свойств Окисление Взаимодействие с неметаллами Взаимодействие с водой Взаимодействие с кислотами
Химические свойства Общая характеристика восстановительных свойств Окисление Взаимодействие с неметаллами Взаимодействие с водой Взаимодействие с кислотами
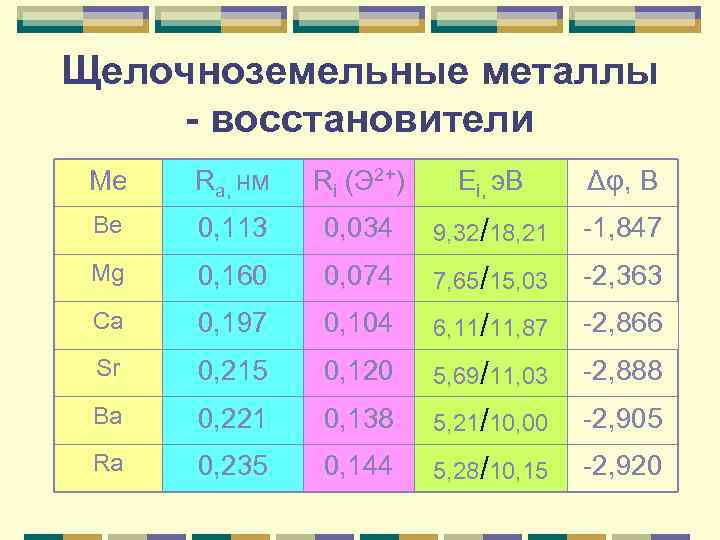 Щелочноземельные металлы - восстановители Me Ra, нм Ri (Э 2+) Ei, э. В Δφ, В Be 0, 113 0, 034 9, 32/18, 21 -1, 847 Mg 0, 160 0, 074 7, 65/15, 03 -2, 363 Ca 0, 197 0, 104 6, 11/11, 87 -2, 866 Sr 0, 215 0, 120 5, 69/11, 03 -2, 888 Ba 0, 221 0, 138 5, 21/10, 00 -2, 905 Ra 0, 235 0, 144 5, 28/10, 15 -2, 920
Щелочноземельные металлы - восстановители Me Ra, нм Ri (Э 2+) Ei, э. В Δφ, В Be 0, 113 0, 034 9, 32/18, 21 -1, 847 Mg 0, 160 0, 074 7, 65/15, 03 -2, 363 Ca 0, 197 0, 104 6, 11/11, 87 -2, 866 Sr 0, 215 0, 120 5, 69/11, 03 -2, 888 Ba 0, 221 0, 138 5, 21/10, 00 -2, 905 Ra 0, 235 0, 144 5, 28/10, 15 -2, 920
 Взаимодействие с кислородом Активно взаимодействуют с кислородом с образованием оксидов: 2 Ме + O 2 = 2 Ме. O Оксиды –твердые, белые , тугоплавкие вещества, типичные основные оксиды Стронций и барий образуют пероксиды (? ) 2 Ва. О + О 2 = 2 Ва. О 2
Взаимодействие с кислородом Активно взаимодействуют с кислородом с образованием оксидов: 2 Ме + O 2 = 2 Ме. O Оксиды –твердые, белые , тугоплавкие вещества, типичные основные оксиды Стронций и барий образуют пероксиды (? ) 2 Ва. О + О 2 = 2 Ва. О 2
 Взаимодействие с неметаллами С галогенами образуют галогениды: Ме + Gal 2 = Me. Gal 2 С серой взаимодействуют при незначительном нагревании : Me + S = Me. S С углем, азотом взаимодействуют при нагревании: Me + 2 С = Me. С 2 3 Me +N 2 = Me 3 N 2 С водородом взаимодействуют при нагревании (кроме бериллия): Me +Н 2 = Me. Н 2
Взаимодействие с неметаллами С галогенами образуют галогениды: Ме + Gal 2 = Me. Gal 2 С серой взаимодействуют при незначительном нагревании : Me + S = Me. S С углем, азотом взаимодействуют при нагревании: Me + 2 С = Me. С 2 3 Me +N 2 = Me 3 N 2 С водородом взаимодействуют при нагревании (кроме бериллия): Me +Н 2 = Me. Н 2
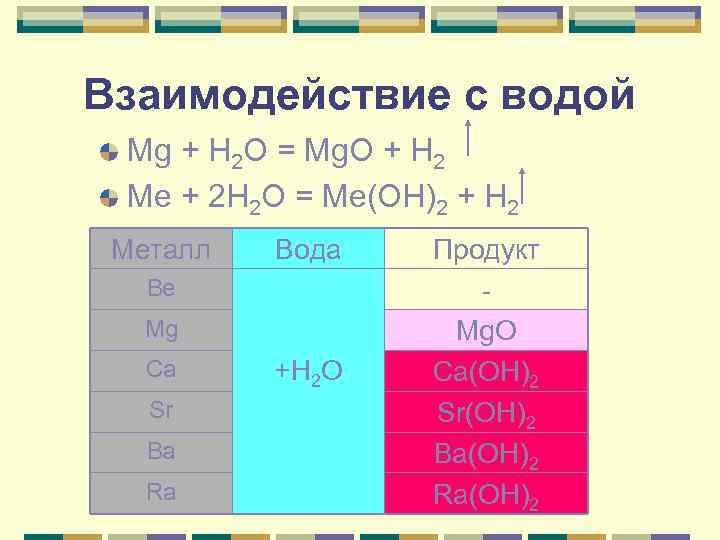 Взаимодействие с водой Mg + Н 2 О = Mg. О + Н 2 Ме + 2 Н 2 О = Ме(ОН)2 + Н 2 Металл Вода Be Mg Ca Sr Ba Ra +Н 2 О Продукт Mg. О Са(OH)2 Sr(OH)2 Ва(OH)2 Rа(OH)2
Взаимодействие с водой Mg + Н 2 О = Mg. О + Н 2 Ме + 2 Н 2 О = Ме(ОН)2 + Н 2 Металл Вода Be Mg Ca Sr Ba Ra +Н 2 О Продукт Mg. О Са(OH)2 Sr(OH)2 Ва(OH)2 Rа(OH)2
 Взаимодействие с кислотами Ме + 2 Н+ = Ме 2+ + Н 2 Взаимодействуют с растворами кислот (кроме кальция) Бериллий взаимодействует с растворами кислот и щелочей (амфотерность, диагональное сходство с алюминием): Ве + 2 Н+ + 4 Н 2 О = [Ве(Н 2 О)4]2+ +Н 2 Ве + 2 ОН-+ 2 Н 2 О = [Ве(ОН)4]2 - +Н 2
Взаимодействие с кислотами Ме + 2 Н+ = Ме 2+ + Н 2 Взаимодействуют с растворами кислот (кроме кальция) Бериллий взаимодействует с растворами кислот и щелочей (амфотерность, диагональное сходство с алюминием): Ве + 2 Н+ + 4 Н 2 О = [Ве(Н 2 О)4]2+ +Н 2 Ве + 2 ОН-+ 2 Н 2 О = [Ве(ОН)4]2 - +Н 2
 Соединения щелочноземельных элементов Кислородные соединения Гидроксиды Галогениды Карбонаты и жесткость воды Соли кислородсодержащих кислот Определение щелочноземельных металлов Применение щелочноземельных металлов
Соединения щелочноземельных элементов Кислородные соединения Гидроксиды Галогениды Карбонаты и жесткость воды Соли кислородсодержащих кислот Определение щелочноземельных металлов Применение щелочноземельных металлов
 Кислородные соединения Оксиды – Ме. О При взаимодействии с водой образуют щелочи (кроме Ве. О): Ме. О +Н 2 О = Ме (ОН)2 Взаимодействуют с кислотами с образованием соли и воды: Ме. О +2 Н+ = Ме 2+ + Н 2 О Ве. О взаимодействует с кислотами и щелочами с образованием комплексных соединений: Ве. О + 2 Н+ + 3 Н 2 О = [Ве(Н 2 О)4]2+ Ве. О + 2 ОН-+ Н 2 О = [Ве(ОН)4]2 -
Кислородные соединения Оксиды – Ме. О При взаимодействии с водой образуют щелочи (кроме Ве. О): Ме. О +Н 2 О = Ме (ОН)2 Взаимодействуют с кислотами с образованием соли и воды: Ме. О +2 Н+ = Ме 2+ + Н 2 О Ве. О взаимодействует с кислотами и щелочами с образованием комплексных соединений: Ве. О + 2 Н+ + 3 Н 2 О = [Ве(Н 2 О)4]2+ Ве. О + 2 ОН-+ Н 2 О = [Ве(ОН)4]2 -
 Гидроксиды Ме(ОН)2 – щелочи, хорошо растворимы в воде, изменяют окраску индикаторов (кроме гидроксида бериллия) Ве (ОН)2 – амфотерный Растворимость гидроксидов увеличивается в подгруппе сверху вниз Щелочные свойства гидроксидов изменяются в подгруппе сверху вниз
Гидроксиды Ме(ОН)2 – щелочи, хорошо растворимы в воде, изменяют окраску индикаторов (кроме гидроксида бериллия) Ве (ОН)2 – амфотерный Растворимость гидроксидов увеличивается в подгруппе сверху вниз Щелочные свойства гидроксидов изменяются в подгруппе сверху вниз
 Галогениды Образуют соединения со всеми галогенами Соли, хорошо растворимые в воде, растворимость изменяется в зависимости от положения металла в подгруппе (? ) Фториды обладают меньшей растворимостью, поэтому встречаются в природе в виде залежей (Са. F 2, - флюорит) Наибольшее значение имеют хлориды (сырье для производства металлов)
Галогениды Образуют соединения со всеми галогенами Соли, хорошо растворимые в воде, растворимость изменяется в зависимости от положения металла в подгруппе (? ) Фториды обладают меньшей растворимостью, поэтому встречаются в природе в виде залежей (Са. F 2, - флюорит) Наибольшее значение имеют хлориды (сырье для производства металлов)
 Карбонаты и жесткость воды Са. СО 3 – кальцит (мел, известняк, мрамор) Mg. CO 3 – магнезит Са(НСО 3)2 и Mg(НCO 3)2 – встречаются в солевом составе природных вод, обусловливают временную (карбонатную) жесткость воды Постоянная жесткость обусловлена содержанием сульфатов и хлоридов
Карбонаты и жесткость воды Са. СО 3 – кальцит (мел, известняк, мрамор) Mg. CO 3 – магнезит Са(НСО 3)2 и Mg(НCO 3)2 – встречаются в солевом составе природных вод, обусловливают временную (карбонатную) жесткость воды Постоянная жесткость обусловлена содержанием сульфатов и хлоридов
 Соли кислородсодержащих кислот Сульфаты –плохо растворяются в воде или не растворяются (сульфат бария) В природе: гипс – Са. SO 4 • 2 H 2 O, ангидрит - Са. SO 4 целестин - Sr. SO 4, барит - Ва. SO 4 Нитраты – все хорошо растворимы, Са(NO 3)2 – норвежская селитра Фосфаты – не растворяются, в природе образуют залежи (фосфорит, апатит Са 5[PO 4]3(F, Cl, ОН) )
Соли кислородсодержащих кислот Сульфаты –плохо растворяются в воде или не растворяются (сульфат бария) В природе: гипс – Са. SO 4 • 2 H 2 O, ангидрит - Са. SO 4 целестин - Sr. SO 4, барит - Ва. SO 4 Нитраты – все хорошо растворимы, Са(NO 3)2 – норвежская селитра Фосфаты – не растворяются, в природе образуют залежи (фосфорит, апатит Са 5[PO 4]3(F, Cl, ОН) )
 Определение соединений щелочноземельных металлов Изменение окраски пламени: • Кальций – кирпично-красный • Стронций – карминово-красный • Барий – желтовато-зеленый Магний – обнаруживается в реакции с гидрофосфатом натрия при добавлении гидроксида аммония – белый осадок Бериллий – сульфат растворим в воде, растворы солей имеют кислую среду
Определение соединений щелочноземельных металлов Изменение окраски пламени: • Кальций – кирпично-красный • Стронций – карминово-красный • Барий – желтовато-зеленый Магний – обнаруживается в реакции с гидрофосфатом натрия при добавлении гидроксида аммония – белый осадок Бериллий – сульфат растворим в воде, растворы солей имеют кислую среду
 Применение щелочноземельных металлов Сплавы с заданными свойствами (Ве, Mg, Са ) Металлотермия, сплавы с низкими температурами плавления (Са) Атомная энергетика (Ва, Ra) Металлургия и очистка металлов от примесей ( Са, Sr) Широкое применения находят соединения щелочноземельных элементов
Применение щелочноземельных металлов Сплавы с заданными свойствами (Ве, Mg, Са ) Металлотермия, сплавы с низкими температурами плавления (Са) Атомная энергетика (Ва, Ra) Металлургия и очистка металлов от примесей ( Са, Sr) Широкое применения находят соединения щелочноземельных элементов
 Спасибо за внимание!
Спасибо за внимание!


