1-А гр.ppt
- Количество слайдов: 23
 Металлические элементы 1 -А группы Щелочные металлы 1
Металлические элементы 1 -А группы Щелочные металлы 1
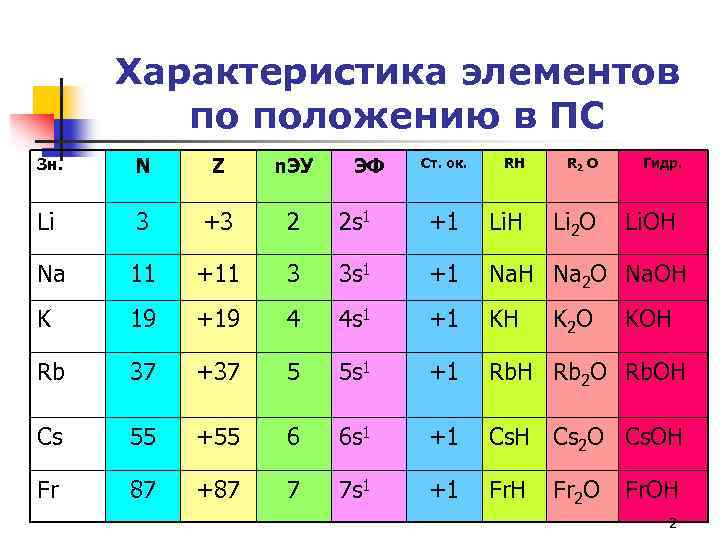 Характеристика элементов по положению в ПС Зн. N Z n. ЭУ ЭФ Li 3 +3 2 2 s 1 Na 11 +11 3 K 19 +19 Rb 37 Cs Fr Ст. ок. RH R 2 O +1 Li. Н Li 2 О 3 s 1 +1 Na. Н Na 2 О Na. ОН 4 4 s 1 +1 KН +37 5 5 s 1 +1 Rb. Н Rb 2 О Rb. ОН 55 +55 6 6 s 1 +1 Cs. Н Cs 2 О Cs. ОН 87 +87 7 7 s 1 +1 Fr. Н K 2 О Fr 2 О Гидр. Li. ОН KОН Fr. ОН 2
Характеристика элементов по положению в ПС Зн. N Z n. ЭУ ЭФ Li 3 +3 2 2 s 1 Na 11 +11 3 K 19 +19 Rb 37 Cs Fr Ст. ок. RH R 2 O +1 Li. Н Li 2 О 3 s 1 +1 Na. Н Na 2 О Na. ОН 4 4 s 1 +1 KН +37 5 5 s 1 +1 Rb. Н Rb 2 О Rb. ОН 55 +55 6 6 s 1 +1 Cs. Н Cs 2 О Cs. ОН 87 +87 7 7 s 1 +1 Fr. Н K 2 О Fr 2 О Гидр. Li. ОН KОН Fr. ОН 2
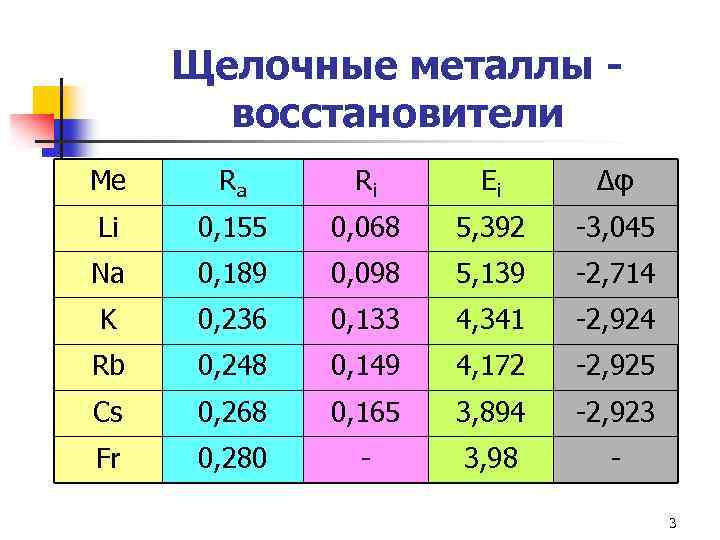 Щелочные металлы восстановители Me Ra Ri Ei Δφ Li 0, 155 0, 068 5, 392 -3, 045 Na 0, 189 0, 098 5, 139 -2, 714 K 0, 236 0, 133 4, 341 -2, 924 Rb 0, 248 0, 149 4, 172 -2, 925 Cs 0, 268 0, 165 3, 894 -2, 923 Fr 0, 280 - 3, 98 3
Щелочные металлы восстановители Me Ra Ri Ei Δφ Li 0, 155 0, 068 5, 392 -3, 045 Na 0, 189 0, 098 5, 139 -2, 714 K 0, 236 0, 133 4, 341 -2, 924 Rb 0, 248 0, 149 4, 172 -2, 925 Cs 0, 268 0, 165 3, 894 -2, 923 Fr 0, 280 - 3, 98 3
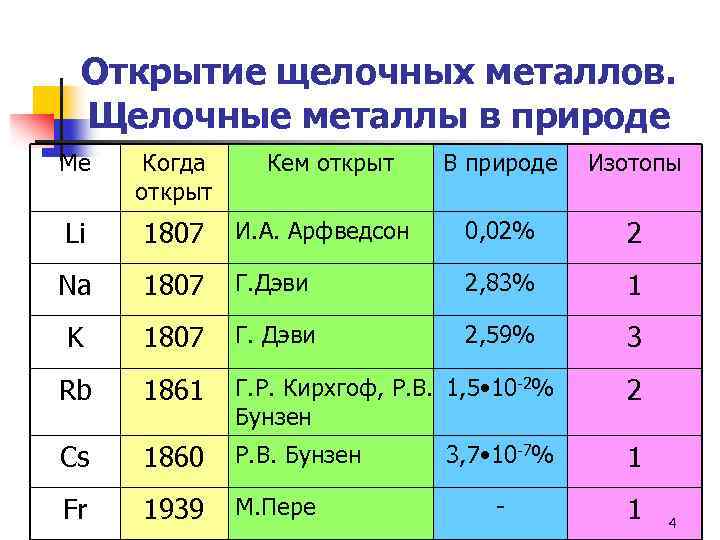 Открытие щелочных металлов. Щелочные металлы в природе Ме Когда открыт Li 1807 Na Кем открыт В природе Изотопы И. А. Арфведсон 0, 02% 2 1807 Г. Дэви 2, 83% 1 K 1807 Г. Дэви 2, 59% 3 Rb 1861 Г. Р. Кирхгоф, Р. В. 1, 5 • 10 -2% Бунзен 2 Cs 1860 Р. В. Бунзен 3, 7 • 10 -7% 1 Fr 1939 М. Пере - 1 4
Открытие щелочных металлов. Щелочные металлы в природе Ме Когда открыт Li 1807 Na Кем открыт В природе Изотопы И. А. Арфведсон 0, 02% 2 1807 Г. Дэви 2, 83% 1 K 1807 Г. Дэви 2, 59% 3 Rb 1861 Г. Р. Кирхгоф, Р. В. 1, 5 • 10 -2% Бунзен 2 Cs 1860 Р. В. Бунзен 3, 7 • 10 -7% 1 Fr 1939 М. Пере - 1 4
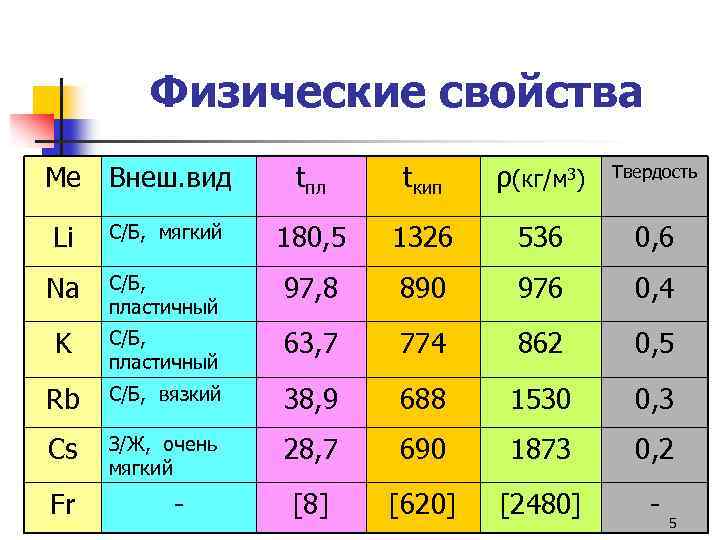 Физические свойства Ме Внеш. вид tпл tкип ρ(кг/м 3) Твердость Li С/Б, мягкий 180, 5 1326 536 0, 6 Na С/Б, пластичный 97, 8 890 976 0, 4 K С/Б, пластичный 63, 7 774 862 0, 5 Rb С/Б, вязкий 38, 9 688 1530 0, 3 Cs З/Ж, очень мягкий 28, 7 690 1873 0, 2 [8] [620] [2480] - Fr - 5
Физические свойства Ме Внеш. вид tпл tкип ρ(кг/м 3) Твердость Li С/Б, мягкий 180, 5 1326 536 0, 6 Na С/Б, пластичный 97, 8 890 976 0, 4 K С/Б, пластичный 63, 7 774 862 0, 5 Rb С/Б, вязкий 38, 9 688 1530 0, 3 Cs З/Ж, очень мягкий 28, 7 690 1873 0, 2 [8] [620] [2480] - Fr - 5
 Получение щелочных металлов n n n Na: электролиз расплава 40% Na. Cl и 60% Ca. Cl 2, 5800 С, 7 В, фильтрация металлического кальция при 1100 С, электролиз расплава Na. OH при ~3500 С, электролиз водных растворов с использованием ртути (амальгамный, большое перенапряжение). K: Na + KCl = K + Na. Cl Электролиз расплава K 2 CO 3 – KCl, катод – расплав свинца, перегонка в вакууме Li, Rb, Cs: электролиз расплава галогенидов, цирконийтермия 2 M 2 CO 3 + Zr = 4 M + Zr. O 2 + 2 CO 2 6
Получение щелочных металлов n n n Na: электролиз расплава 40% Na. Cl и 60% Ca. Cl 2, 5800 С, 7 В, фильтрация металлического кальция при 1100 С, электролиз расплава Na. OH при ~3500 С, электролиз водных растворов с использованием ртути (амальгамный, большое перенапряжение). K: Na + KCl = K + Na. Cl Электролиз расплава K 2 CO 3 – KCl, катод – расплав свинца, перегонка в вакууме Li, Rb, Cs: электролиз расплава галогенидов, цирконийтермия 2 M 2 CO 3 + Zr = 4 M + Zr. O 2 + 2 CO 2 6
 Химические свойства щелочных металлов Взаимодействие с кислородом Взаимодействие с другими неметаллами Взаимодействие с водой Взаимодействие с кислотами Сплавы щелочных металлов 7
Химические свойства щелочных металлов Взаимодействие с кислородом Взаимодействие с другими неметаллами Взаимодействие с водой Взаимодействие с кислотами Сплавы щелочных металлов 7
 Взаимодействие с кислородом n n Активно окисляются на воздухе Литий – единственный образует оксид 4 Li + O 2 = 2 Li 2 O Натрий образует пероксид Na + O 2 = Na 2 O 2 Калий, рубидий, цезий образуют надпероксиды K + O 2 = KO 2 Rb + O 2 = Rb. O 2 Cs + O 2 = Cs. O 2 8
Взаимодействие с кислородом n n Активно окисляются на воздухе Литий – единственный образует оксид 4 Li + O 2 = 2 Li 2 O Натрий образует пероксид Na + O 2 = Na 2 O 2 Калий, рубидий, цезий образуют надпероксиды K + O 2 = KO 2 Rb + O 2 = Rb. O 2 Cs + O 2 = Cs. O 2 8
 Взаимодействие с неметаллами n С галогенами образуют галогениды: 2 Ме + Gal 2 = 2 Me. Gal n n n С серой взаимодействуют при незначительном нагревании или обычных условиях: 2 Me + S = Me 2 S С углем, азотом взаимодействуют при нагревании: 2 Me + 2 С = Me 2 С 2 6 Me +N 2 = 2 Me 3 N С водородом взаимодействуют при нагревании: 2 Me +Н 2 = 2 Me. Н 9
Взаимодействие с неметаллами n С галогенами образуют галогениды: 2 Ме + Gal 2 = 2 Me. Gal n n n С серой взаимодействуют при незначительном нагревании или обычных условиях: 2 Me + S = Me 2 S С углем, азотом взаимодействуют при нагревании: 2 Me + 2 С = Me 2 С 2 6 Me +N 2 = 2 Me 3 N С водородом взаимодействуют при нагревании: 2 Me +Н 2 = 2 Me. Н 9
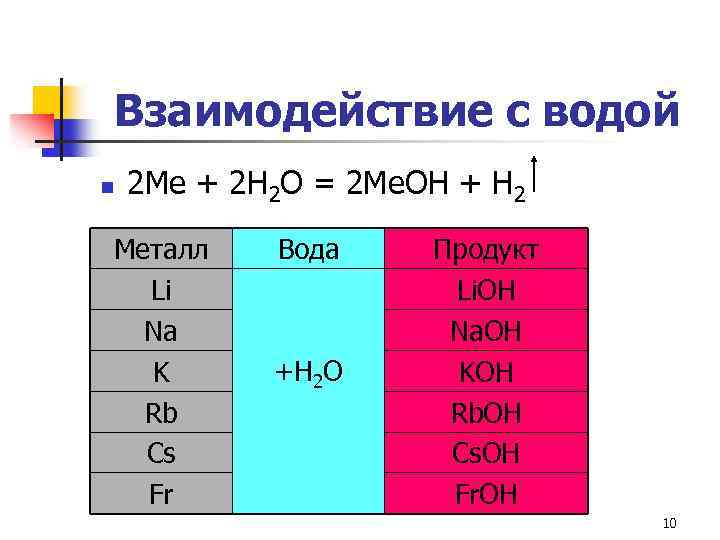 Взаимодействие с водой n 2 Ме + 2 Н 2 О = 2 Ме. ОН + Н 2 Металл Li Na K Rb Cs Fr Вода +Н 2 О Продукт Li. OH Na. OH KOH Rb. OH Cs. OH Fr. OH 10
Взаимодействие с водой n 2 Ме + 2 Н 2 О = 2 Ме. ОН + Н 2 Металл Li Na K Rb Cs Fr Вода +Н 2 О Продукт Li. OH Na. OH KOH Rb. OH Cs. OH Fr. OH 10
 Взаимодействие с кислотами n n n 2 Ме + 2 Н+ = 2 Ме+ + Н 2 Щелочные металлы с растворами кислот не взаимодействуют! (? ) При взаимодействии с концентрированными кислотами или газообразными веществами, растворы которых являются кислотами, реакции протекают с выделением водорода 11
Взаимодействие с кислотами n n n 2 Ме + 2 Н+ = 2 Ме+ + Н 2 Щелочные металлы с растворами кислот не взаимодействуют! (? ) При взаимодействии с концентрированными кислотами или газообразными веществами, растворы которых являются кислотами, реакции протекают с выделением водорода 11
 Сплавы щелочных металлов n n Образуют интерметаллические соединения Образуют эвтектические сплавы (24% Na и 76% К – жидкость, Тпл = -12, 60 С) Могут образовывать амальгамы Сплав, содержащий щелочной металл, всегда имеет более низкую температуру плавления 12
Сплавы щелочных металлов n n Образуют интерметаллические соединения Образуют эвтектические сплавы (24% Na и 76% К – жидкость, Тпл = -12, 60 С) Могут образовывать амальгамы Сплав, содержащий щелочной металл, всегда имеет более низкую температуру плавления 12
 Соединения щелочных металлов Кислородные соединения Гидроксиды Галогениды Гидриды Сульфиды Соли кислородсодержащих кислот Определение щелочных металлов Применение щелочных металлов 13
Соединения щелочных металлов Кислородные соединения Гидроксиды Галогениды Гидриды Сульфиды Соли кислородсодержащих кислот Определение щелочных металлов Применение щелочных металлов 13
 Кислородные соединения n Оксиды – Ме 2 О при взаимодействии с водой образуют щелочи n n n Пероксиды – Ме 2 О 2, сильные окислители Надпероксиды – Ме. О 2, сильные окислители Озониды –Ме. О 3 , сильные окислители, нестойкие, разлагаются с образованием надпероксидов: 2 Ме. О 3 = 2 Ме. О 2 + О 2 14
Кислородные соединения n Оксиды – Ме 2 О при взаимодействии с водой образуют щелочи n n n Пероксиды – Ме 2 О 2, сильные окислители Надпероксиды – Ме. О 2, сильные окислители Озониды –Ме. О 3 , сильные окислители, нестойкие, разлагаются с образованием надпероксидов: 2 Ме. О 3 = 2 Ме. О 2 + О 2 14
 Свойства кислородных соединений щелочных металлов 15
Свойства кислородных соединений щелочных металлов 15
 Гидроксиды n n n Ме. ОН – щелочи, хорошо растворимы в воде, изменяют окраску индикаторов: Щелочные свойства изменяются в подгруппе сверху вниз (? ) Гигроскопичны, при нагревании возгоняются без разложения (кроме гидроксида лития, разлагается) 16
Гидроксиды n n n Ме. ОН – щелочи, хорошо растворимы в воде, изменяют окраску индикаторов: Щелочные свойства изменяются в подгруппе сверху вниз (? ) Гигроскопичны, при нагревании возгоняются без разложения (кроме гидроксида лития, разлагается) 16
 Галогениды n n Щелочные металлы образуют соединения со всеми галогенами: Бесцветные , кристаллические вещества, не плавятся, кристаллические решетки гранецентрированные и кубические Соли, хорошо растворимые в воде (кроме фторида лития), растворимость изменяется в зависимости от положения металла в подгруппе Имеют широкое применение 17
Галогениды n n Щелочные металлы образуют соединения со всеми галогенами: Бесцветные , кристаллические вещества, не плавятся, кристаллические решетки гранецентрированные и кубические Соли, хорошо растворимые в воде (кроме фторида лития), растворимость изменяется в зависимости от положения металла в подгруппе Имеют широкое применение 17
 Гидриды Гидрид-ион стабилен только при контакте со слабо поляризующими катионами, поэтому ионные гидриды характерны для щелочных и щелочно-земельных металлов, а также редкоземельных элементов и некоторых актинидов. 18
Гидриды Гидрид-ион стабилен только при контакте со слабо поляризующими катионами, поэтому ионные гидриды характерны для щелочных и щелочно-земельных металлов, а также редкоземельных элементов и некоторых актинидов. 18
 Сульфиды Подобно соединениям с кислородом, образуется ряд сульфидов: 1. Сульфиды – Ме 2 S 2. Персульфиды (полисульфиды) – Ме 2 S 2, Ме 2 S 3, Ме 2 S 4, Ме 2 S 5, (Ме 2 Sn) n: для лития-2, натрия – 5, калия-цезия-6 n Устойчивость полисульфидов увеличивается в ряду литийцезий Нитриды, фосфиды и сульфиды имеют ионный характер, в водных растворах гидролизуются. n Получают их прямым синтезом. 19
Сульфиды Подобно соединениям с кислородом, образуется ряд сульфидов: 1. Сульфиды – Ме 2 S 2. Персульфиды (полисульфиды) – Ме 2 S 2, Ме 2 S 3, Ме 2 S 4, Ме 2 S 5, (Ме 2 Sn) n: для лития-2, натрия – 5, калия-цезия-6 n Устойчивость полисульфидов увеличивается в ряду литийцезий Нитриды, фосфиды и сульфиды имеют ионный характер, в водных растворах гидролизуются. n Получают их прямым синтезом. 19
 Соли кислородсодержащих кислот n n n Карбонаты – сода, поташ Сульфаты – сульфат натрия Нитраты – селитры Фосфаты – полифосфаты натрия Силикаты – жидкое стекло Хлораты – бертоллетова соль 20
Соли кислородсодержащих кислот n n n Карбонаты – сода, поташ Сульфаты – сульфат натрия Нитраты – селитры Фосфаты – полифосфаты натрия Силикаты – жидкое стекло Хлораты – бертоллетова соль 20
 Определение соединений щелочных металлов Li – карминово-красный Na – желтый K – фиолетово-розовый Rb – розовый Cs - фиолетово-розовый 21
Определение соединений щелочных металлов Li – карминово-красный Na – желтый K – фиолетово-розовый Rb – розовый Cs - фиолетово-розовый 21
 Применение щелочных металлов n n n Фотоэлементы Источники света Сплавы с низкими температурами плавления Атомная энергетика Металлургия Лабораторная практика 22
Применение щелочных металлов n n n Фотоэлементы Источники света Сплавы с низкими температурами плавления Атомная энергетика Металлургия Лабораторная практика 22
 Спасибо за внимание! 23
Спасибо за внимание! 23


