 Метали
Метали
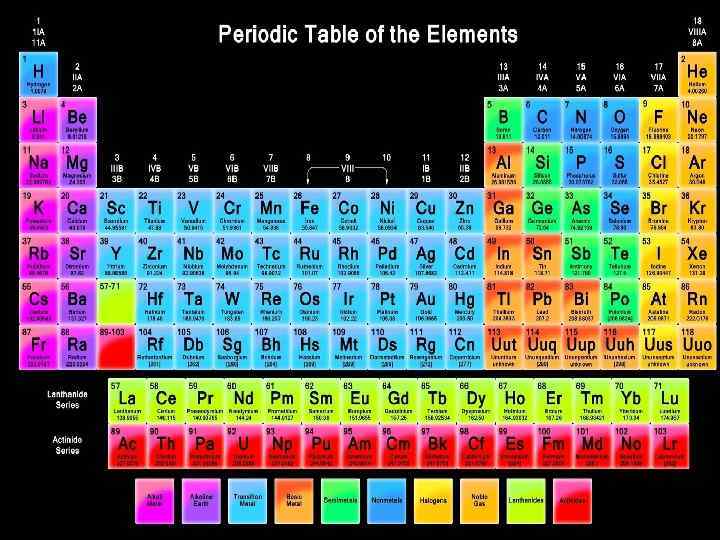
 Термін «метал» - грецького походження : «metallon» означає «шахта» . Металам притаманні такі властивості: висока електро- та теплопровідність, характерний блиск, ковкість та пластичність. Відносну межу між металами і неметалами встановлює лінія Цинтля (Al – Ge – Sb – Po).
Термін «метал» - грецького походження : «metallon» означає «шахта» . Металам притаманні такі властивості: висока електро- та теплопровідність, характерний блиск, ковкість та пластичність. Відносну межу між металами і неметалами встановлює лінія Цинтля (Al – Ge – Sb – Po).
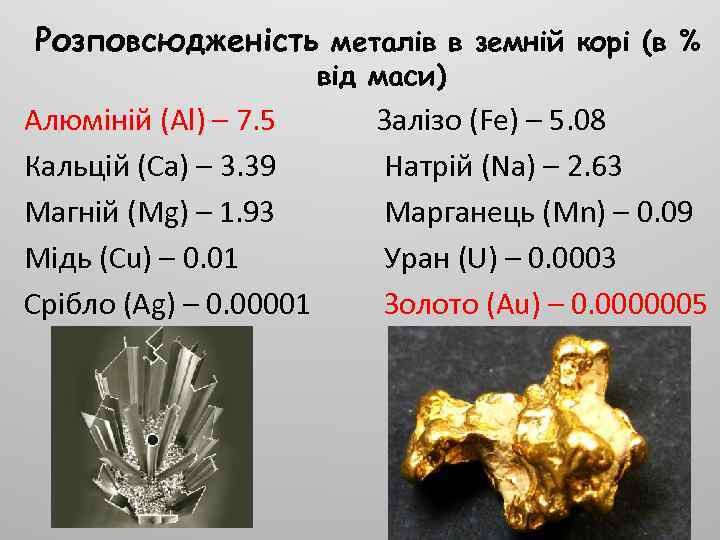 Розповсюдженість металів в земній корі (в % від маси) Алюміній (Al) – 7. 5 Залізо (Fe) – 5. 08 Кальцій (Ca) – 3. 39 Натрій (Na) – 2. 63 Магній (Mg) – 1. 93 Марганець (Mn) – 0. 09 Мідь (Cu) – 0. 01 Уран (U) – 0. 0003 Срібло (Ag) – 0. 00001 Золото (Au) – 0. 0000005
Розповсюдженість металів в земній корі (в % від маси) Алюміній (Al) – 7. 5 Залізо (Fe) – 5. 08 Кальцій (Ca) – 3. 39 Натрій (Na) – 2. 63 Магній (Mg) – 1. 93 Марганець (Mn) – 0. 09 Мідь (Cu) – 0. 01 Уран (U) – 0. 0003 Срібло (Ag) – 0. 00001 Золото (Au) – 0. 0000005
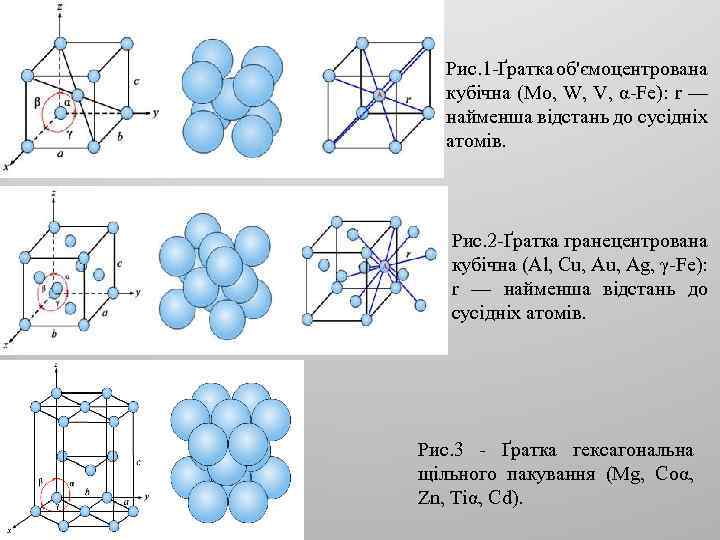 Рис. 1 -Ґратка об'ємоцентрована кубічна (Mo, W, V, α-Fe): r — найменша відстань до сусідніх атомів. Рис. 2 -Ґратка гранецентрована кубічна (Al, Cu, Ag, γ-Fe): r — найменша відстань до сусідніх атомів. Рис. 3 - Ґратка гексагональна щільного пакування (Mg, Coα, Zn, Tiα, Cd).
Рис. 1 -Ґратка об'ємоцентрована кубічна (Mo, W, V, α-Fe): r — найменша відстань до сусідніх атомів. Рис. 2 -Ґратка гранецентрована кубічна (Al, Cu, Ag, γ-Fe): r — найменша відстань до сусідніх атомів. Рис. 3 - Ґратка гексагональна щільного пакування (Mg, Coα, Zn, Tiα, Cd).
 Дефекти у кристалах виникають у процесі їх росту, під впливом теплових, механічних і електричних полів, а також у разі опромінювання кристалів нейтронами, електронами, рентгенівськими променями та ультрафіолетовим випромінюванням (радіаційні дефекти). Розрізняють точкові дефекти (нульвимірні); лінійні (одновимірні) дефекти; дефекти, що утворюють у кристалі поверхні (двовимірні) і об’ємні дефекти (тривимірні). Рис. 4 – Механізми росту кристалів.
Дефекти у кристалах виникають у процесі їх росту, під впливом теплових, механічних і електричних полів, а також у разі опромінювання кристалів нейтронами, електронами, рентгенівськими променями та ультрафіолетовим випромінюванням (радіаційні дефекти). Розрізняють точкові дефекти (нульвимірні); лінійні (одновимірні) дефекти; дефекти, що утворюють у кристалі поверхні (двовимірні) і об’ємні дефекти (тривимірні). Рис. 4 – Механізми росту кристалів.
 Рис. 5 – Схема утворення вакансії: а – вихід приповерхневого атома та його адсорбція на поверхні кристала; б – перехід іншого атома у кристалографічне положення першого атома.
Рис. 5 – Схема утворення вакансії: а – вихід приповерхневого атома та його адсорбція на поверхні кристала; б – перехід іншого атома у кристалографічне положення першого атома.
 Нульвимірні дефекти (точкові) характеризуються порушенням структури у вузлах або міжвузлах кристалічної гратки. Ці дефекти зумовлені, перш за все, невпорядкованим розміщенням власних атомів кристалу, а також атомами домішок. o o o До них відносяться: вакансія – вільний, незайнятий атомом вузол кристалічної гратки; домішковий атом заміщення – заміна атома одного типу атомом іншого типу у вузлі кристалічної гратки; домішковий атом упровадження – атом домішки, що розташовується в міжвузлі кристалічної гратки; міжвузловий атом – атом основного кристалу, що знаходиться у міжвузловій позиції елементарної комірки; пара Френкеля – вакансія і міжвузловий атом; дефект Шотткі – вакансія, що виникла за рахунок виходу атома з вузла на поверхню кристала або за яку-небудь границю.
Нульвимірні дефекти (точкові) характеризуються порушенням структури у вузлах або міжвузлах кристалічної гратки. Ці дефекти зумовлені, перш за все, невпорядкованим розміщенням власних атомів кристалу, а також атомами домішок. o o o До них відносяться: вакансія – вільний, незайнятий атомом вузол кристалічної гратки; домішковий атом заміщення – заміна атома одного типу атомом іншого типу у вузлі кристалічної гратки; домішковий атом упровадження – атом домішки, що розташовується в міжвузлі кристалічної гратки; міжвузловий атом – атом основного кристалу, що знаходиться у міжвузловій позиції елементарної комірки; пара Френкеля – вакансія і міжвузловий атом; дефект Шотткі – вакансія, що виникла за рахунок виходу атома з вузла на поверхню кристала або за яку-небудь границю.
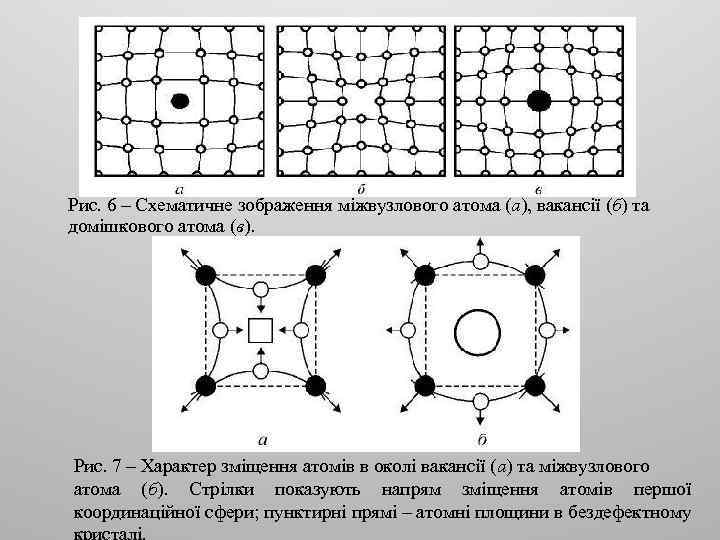 Рис. 6 – Схематичне зображення міжвузлового атома (а), вакансії (б) та домішкового атома (в). Рис. 7 – Характер зміщення атомів в околі вакансії (а) та міжвузлового атома (б). Стрілки показують напрям зміщення атомів першої координаційної сфери; пунктирні прямі – атомні площини в бездефектному
Рис. 6 – Схематичне зображення міжвузлового атома (а), вакансії (б) та домішкового атома (в). Рис. 7 – Характер зміщення атомів в околі вакансії (а) та міжвузлового атома (б). Стрілки показують напрям зміщення атомів першої координаційної сфери; пунктирні прямі – атомні площини в бездефектному
 Властивості металів: o фізичні o механічні o технологічні o хімічні o експлуатаційні (спеціальні)
Властивості металів: o фізичні o механічні o технологічні o хімічні o експлуатаційні (спеціальні)
 За властивостями метали класифікують: - за густиною - легкі – ρ < 3 г/см 3 (Li, Be, Mg, Al, Ti, …) - важкі – ρ > 3 г/см 3 (Os, Ru, Rh, Pb, …) - за температурою плавлення (по відношенню до Тпл заліза =1539 °С) - легкоплавкі (Тпл < Тпл(Fe)) - Zn, Cd, Hg, Sn, Sb, Pb, Bi, In, Ga, Ce, … - тугоплавкі (Тпл > Тпл(Fe)) – Ti, Cr, Zr, Nb, Mo, W, V, Lu, Re, … - за хімічними властивостями (чи розміщенням в періодичній системі) - лужні (Li, Na, K, Rb, Cs) - лужноземельні (Ca, Sr, Ba) - рідкісноземельні (РЗМ) (La, Ce, Pr, …, Lu) – лантаноїди - трансуранові (Th, Pa, U, Pu) – актиноїди - шляхетні (Ru, Rh, Pd, Ag, Os, Ir, Pt, Au).
За властивостями метали класифікують: - за густиною - легкі – ρ < 3 г/см 3 (Li, Be, Mg, Al, Ti, …) - важкі – ρ > 3 г/см 3 (Os, Ru, Rh, Pb, …) - за температурою плавлення (по відношенню до Тпл заліза =1539 °С) - легкоплавкі (Тпл < Тпл(Fe)) - Zn, Cd, Hg, Sn, Sb, Pb, Bi, In, Ga, Ce, … - тугоплавкі (Тпл > Тпл(Fe)) – Ti, Cr, Zr, Nb, Mo, W, V, Lu, Re, … - за хімічними властивостями (чи розміщенням в періодичній системі) - лужні (Li, Na, K, Rb, Cs) - лужноземельні (Ca, Sr, Ba) - рідкісноземельні (РЗМ) (La, Ce, Pr, …, Lu) – лантаноїди - трансуранові (Th, Pa, U, Pu) – актиноїди - шляхетні (Ru, Rh, Pd, Ag, Os, Ir, Pt, Au).
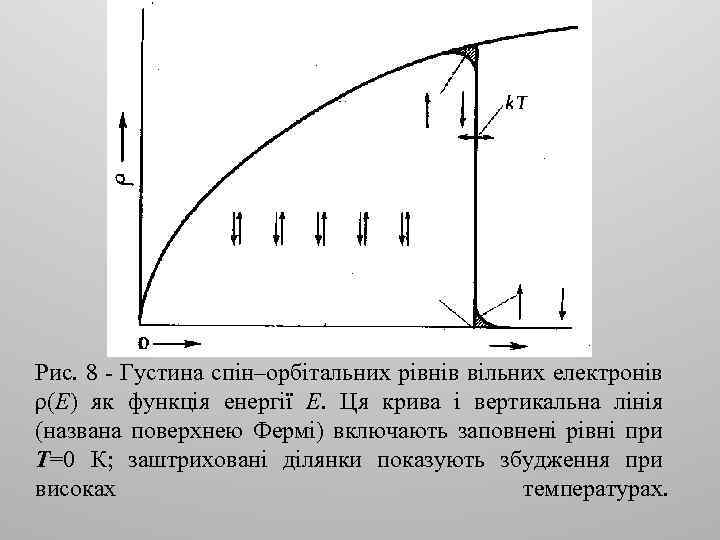 Рис. 8 - Густина спін–орбітальних рівнів вільних електронів ρ(Е) як функція енергії Е. Ця крива і вертикальна лінія (названа поверхнею Фермі) включають заповнені рівні при Т=0 К; заштриховані ділянки показують збудження при високах температурах.
Рис. 8 - Густина спін–орбітальних рівнів вільних електронів ρ(Е) як функція енергії Е. Ця крива і вертикальна лінія (названа поверхнею Фермі) включають заповнені рівні при Т=0 К; заштриховані ділянки показують збудження при високах температурах.
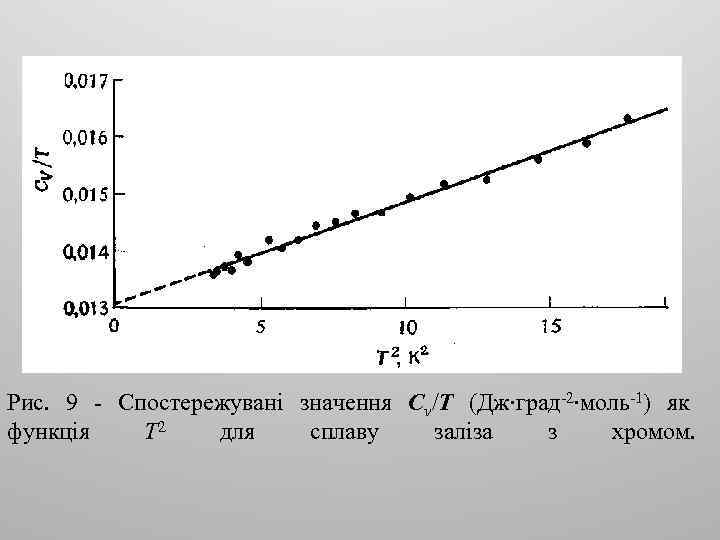 Рис. 9 - Спостережувані значення Сv/Т (Дж∙град-2∙моль-1) як функція Т 2 для сплаву заліза з хромом.
Рис. 9 - Спостережувані значення Сv/Т (Дж∙град-2∙моль-1) як функція Т 2 для сплаву заліза з хромом.
 o Металеві сплави – матеріали, які мають усі характерні властивості металів, але не є хімічно чистими, тобто містять у собі атоми як мінімум двох компонентів. o Сплав вважається металевим тоді, коли основним компонентом є метал, а переважаючим типом зв’язку – металевий. Інші компоненти сплаву можуть бути метали або неметали. У промислових – залізовуглецевих сплавах – другим компонентом є неметал – вуглець. o Будь-який сплав складається з однієї або декількох фаз. Ними можуть бути: 1. чисті компоненти; 2. хімічні сполуки; 3. тверді розчини; 4. проміжні фази. o Твердими розчинами називаються фази, в яких атоми розчиненого компонента або заміщують атоми розчинника в його кристалічній гратці, або розташовуються між ними, або утворюють особливий тип розчину з дефектною кристалічною ґраткою. o Тверді розчини поділяють - заміщення, включення (проникнення) та віднімання (вилучення).
o Металеві сплави – матеріали, які мають усі характерні властивості металів, але не є хімічно чистими, тобто містять у собі атоми як мінімум двох компонентів. o Сплав вважається металевим тоді, коли основним компонентом є метал, а переважаючим типом зв’язку – металевий. Інші компоненти сплаву можуть бути метали або неметали. У промислових – залізовуглецевих сплавах – другим компонентом є неметал – вуглець. o Будь-який сплав складається з однієї або декількох фаз. Ними можуть бути: 1. чисті компоненти; 2. хімічні сполуки; 3. тверді розчини; 4. проміжні фази. o Твердими розчинами називаються фази, в яких атоми розчиненого компонента або заміщують атоми розчинника в його кристалічній гратці, або розташовуються між ними, або утворюють особливий тип розчину з дефектною кристалічною ґраткою. o Тверді розчини поділяють - заміщення, включення (проникнення) та віднімання (вилучення).
 Тверді розчини заміщення ü Утворюються на основі як компонентів сплаву, так і хімічних сполук. Можуть бути як необмеженими, так і обмеженими. ü Загальні правила щодо розчинності у твердому стані (згідно У. Юм-Розері) 1. Якщо атомні радіуси компонентів відрізняються більш ніж на 14. . . 15%, розчинність може бути лише обмеженою (розмірний фактор). 2. Область обмежених твердих розчинів звужується при утворенні стійких проміжних фаз. Ймовірність цього визначається хімічною спорідненістю компонентів сплаву і тим більша, чим більш електронегативним є один із компонентів сплаву та електропозитивним другий (ефект електронегативної валентності). 3. Взаємна розчинність двох елементів пов’язана з їх валентністю, причому розчинність в елементі з меншою валентністю виявляється завжди більшою, ніж в елементі з більшою валентністю (ефект відносної валентності). 4. Необхідною, але недостатньою умовою необмеженої взаємної розчинності, є ізоморфність граток. Прикладом можуть бути системи Cu-Au (>410°C) та Cu-Ag. У першій з них розчинність необмежена (>410°C), у другій не перевищує 9%, хоч у обох випадках ∆r=12, 5%. ü При утворенні твердих розчинів заміщення, зберігається кристалічна гратка розчинника. Але незважаючи на малу ∆r, в ній створюються викривлення, які призводять до деформації – в результаті стиснення або розтягнення гратки (рис. 10). При цьому змінюються не лише міжатомні і міжплощинні відстані, а й періоди ґратки.
Тверді розчини заміщення ü Утворюються на основі як компонентів сплаву, так і хімічних сполук. Можуть бути як необмеженими, так і обмеженими. ü Загальні правила щодо розчинності у твердому стані (згідно У. Юм-Розері) 1. Якщо атомні радіуси компонентів відрізняються більш ніж на 14. . . 15%, розчинність може бути лише обмеженою (розмірний фактор). 2. Область обмежених твердих розчинів звужується при утворенні стійких проміжних фаз. Ймовірність цього визначається хімічною спорідненістю компонентів сплаву і тим більша, чим більш електронегативним є один із компонентів сплаву та електропозитивним другий (ефект електронегативної валентності). 3. Взаємна розчинність двох елементів пов’язана з їх валентністю, причому розчинність в елементі з меншою валентністю виявляється завжди більшою, ніж в елементі з більшою валентністю (ефект відносної валентності). 4. Необхідною, але недостатньою умовою необмеженої взаємної розчинності, є ізоморфність граток. Прикладом можуть бути системи Cu-Au (>410°C) та Cu-Ag. У першій з них розчинність необмежена (>410°C), у другій не перевищує 9%, хоч у обох випадках ∆r=12, 5%. ü При утворенні твердих розчинів заміщення, зберігається кристалічна гратка розчинника. Але незважаючи на малу ∆r, в ній створюються викривлення, які призводять до деформації – в результаті стиснення або розтягнення гратки (рис. 10). При цьому змінюються не лише міжатомні і міжплощинні відстані, а й періоди ґратки.
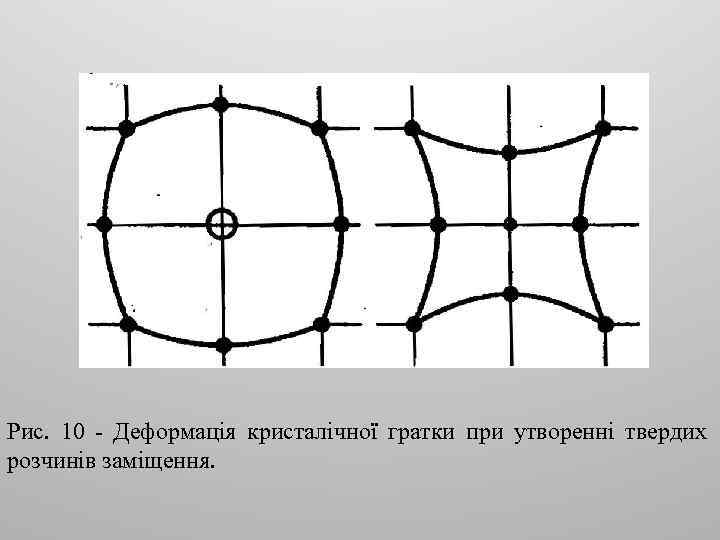 Рис. 10 - Деформація кристалічної гратки при утворенні твердих розчинів заміщення.
Рис. 10 - Деформація кристалічної гратки при утворенні твердих розчинів заміщення.
 Тверді розчини включення (проникнення) ü Утворюються при розміщенні атомів розчиненого компонента у вільних проміжках між атомами розчинника. Тому: - тип кристалічної гратки ТРВ визначається типом гратки розчинника; - розчинність лише обмежена, тому що заповнюються тільки пустоти вихідної структури; - періоди гратки завжди збільшуються. ü Тверді розчини включення утворюються, головним чином, на основі компонентів сплаву, хоча зустрічаються розчини на основі хімічних сполук, наприклад Ni в Ni. Sb. ü Правило Г. Хегга - тверді розчини включення утворюються при співвідношенні r. B/r. A≤ 0, 59. ü Тверді розчини заміщення утворюються при r. B/r. A > 0, 85, включення при r. B/r. A ≤ 0, 59, а інтервал r. B/r. A = 0, 59. . . 0, 85 є несприятливим для утворення твердих розчинів. ü Утворюються лише на основі хімічних сполук і характеризуються наявністю вакантних вузлів у кристалічній гратці, через що там існують значні викривлення, які створюють напруження розтягнення. Це призводить, у свою чергу, до зменшення періодів гратки. ü Уперше тверді розчини віднімання були виявлені при дослідженні окислення заліза та його сплавів.
Тверді розчини включення (проникнення) ü Утворюються при розміщенні атомів розчиненого компонента у вільних проміжках між атомами розчинника. Тому: - тип кристалічної гратки ТРВ визначається типом гратки розчинника; - розчинність лише обмежена, тому що заповнюються тільки пустоти вихідної структури; - періоди гратки завжди збільшуються. ü Тверді розчини включення утворюються, головним чином, на основі компонентів сплаву, хоча зустрічаються розчини на основі хімічних сполук, наприклад Ni в Ni. Sb. ü Правило Г. Хегга - тверді розчини включення утворюються при співвідношенні r. B/r. A≤ 0, 59. ü Тверді розчини заміщення утворюються при r. B/r. A > 0, 85, включення при r. B/r. A ≤ 0, 59, а інтервал r. B/r. A = 0, 59. . . 0, 85 є несприятливим для утворення твердих розчинів. ü Утворюються лише на основі хімічних сполук і характеризуються наявністю вакантних вузлів у кристалічній гратці, через що там існують значні викривлення, які створюють напруження розтягнення. Це призводить, у свою чергу, до зменшення періодів гратки. ü Уперше тверді розчини віднімання були виявлені при дослідженні окислення заліза та його сплавів.
 Упорядковані тверді розчини ü При утворенні твердих розчинів заміщення атоми другого компонента можуть заміщувати будь-які з атомів розчинника, розташовуючись у вузлах ґратки цілком довільно. Такі тверді розчини називаються неупорядкованими (статистичними). ü У ряді металічних систем у результаті повільного охолодження або тривалого відпалу при певних температурах розташування атомів компонентів у кристалічній гратці твердого розчину змінюється і заміщення іде лише в певні положення, тоді утворюється – упорядкований твердий розчин або надструктура ü На рентгенограмах таких сплавів з’являються додаткові (надструктурні) лінії. ü Явище впорядкування у твердих розчинах відкрив М. Курнаков (1916 р. ) при дослідженні сплавів системи Cu-Au. ü Температура при якій настає повне розупорядкування - критична температура упорядкування (Тс) – точка Курнакова.
Упорядковані тверді розчини ü При утворенні твердих розчинів заміщення атоми другого компонента можуть заміщувати будь-які з атомів розчинника, розташовуючись у вузлах ґратки цілком довільно. Такі тверді розчини називаються неупорядкованими (статистичними). ü У ряді металічних систем у результаті повільного охолодження або тривалого відпалу при певних температурах розташування атомів компонентів у кристалічній гратці твердого розчину змінюється і заміщення іде лише в певні положення, тоді утворюється – упорядкований твердий розчин або надструктура ü На рентгенограмах таких сплавів з’являються додаткові (надструктурні) лінії. ü Явище впорядкування у твердих розчинах відкрив М. Курнаков (1916 р. ) при дослідженні сплавів системи Cu-Au. ü Температура при якій настає повне розупорядкування - критична температура упорядкування (Тс) – точка Курнакова.
 Інтерметаліди Інтерметалі чні сполу ки - це хімічні сполуки між металами, які утворюються в результаті взаємодії компонентів при сплавлені, конденсації з пари, а також при реакціях у твердому стані внаслідок взаємної дифузії (при хіміко-термічній обробці), при розпаді пересиченого твердого розчину одного металу в іншому, в результаті інтенсивної пластичної деформації. Застосування: ü ü ü Магнітні матеріали — Sm. Co 5, Fe 3 Ni, Mn. Cu 2 Al, Nd 2 Fe 14 B. Надпровідники — Nb 3 Sn, Nb 3 Ge, V 3 Si. Напівпровідники — Ga. As, Cr. Si 2, Mg 2 Sn. Акумулятори водню — La. Ni 5, Ce. Mg 12. Меркуриди Au. Hg 2, Au 2 Hg, Au 3 Hg застосовуються для вилучення золота.
Інтерметаліди Інтерметалі чні сполу ки - це хімічні сполуки між металами, які утворюються в результаті взаємодії компонентів при сплавлені, конденсації з пари, а також при реакціях у твердому стані внаслідок взаємної дифузії (при хіміко-термічній обробці), при розпаді пересиченого твердого розчину одного металу в іншому, в результаті інтенсивної пластичної деформації. Застосування: ü ü ü Магнітні матеріали — Sm. Co 5, Fe 3 Ni, Mn. Cu 2 Al, Nd 2 Fe 14 B. Надпровідники — Nb 3 Sn, Nb 3 Ge, V 3 Si. Напівпровідники — Ga. As, Cr. Si 2, Mg 2 Sn. Акумулятори водню — La. Ni 5, Ce. Mg 12. Меркуриди Au. Hg 2, Au 2 Hg, Au 3 Hg застосовуються для вилучення золота.
 Основні методи дослідження металів і їх сплавів § Злам (Фрактографія) § Термічний аналіз § Макроструктура § Мікроскопічний аналіз
Основні методи дослідження металів і їх сплавів § Злам (Фрактографія) § Термічний аналіз § Макроструктура § Мікроскопічний аналіз

 Фото з поверхні мікрошліфа та монокристала отримані з допомогою скануючого електронного мікроскопа Leica 420 i
Фото з поверхні мікрошліфа та монокристала отримані з допомогою скануючого електронного мікроскопа Leica 420 i


