lekcia 11 Метали.ppt
- Количество слайдов: 35
 МЕТАЛИ План 1. Розташування металів у періодичній системі. Фізичні властивості металів. 2. Хімічні властивості металів. 3. Корозія металів і методи боротьби з нею.
МЕТАЛИ План 1. Розташування металів у періодичній системі. Фізичні властивості металів. 2. Хімічні властивості металів. 3. Корозія металів і методи боротьби з нею.
 1. Розташування металів у періодичній системі. Фізичні властивості металів До металів відносять елементи періодичної системи, які мають на зовнішньому енергетичному рівні малу кількість електронів (від 1 до 3), багато вільних електронних орбіталей, великі радіуси атомів, низьку енергію йонізації, низьку електро-негативність. Для металів характерний особливий тип хімічного зв’язку – металічний зв’язок.
1. Розташування металів у періодичній системі. Фізичні властивості металів До металів відносять елементи періодичної системи, які мають на зовнішньому енергетичному рівні малу кількість електронів (від 1 до 3), багато вільних електронних орбіталей, великі радіуси атомів, низьку енергію йонізації, низьку електро-негативність. Для металів характерний особливий тип хімічного зв’язку – металічний зв’язок.
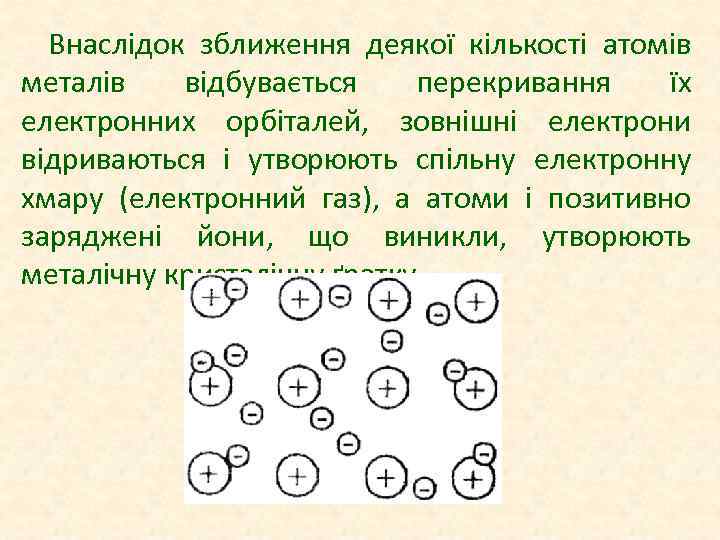 Внаслідок зближення деякої кількості атомів металів відбувається перекривання їх електронних орбіталей, зовнішні електрони відриваються і утворюють спільну електронну хмару (електронний газ), а атоми і позитивно заряджені йони, що виникли, утворюють металічну кристалічну ґратку.
Внаслідок зближення деякої кількості атомів металів відбувається перекривання їх електронних орбіталей, зовнішні електрони відриваються і утворюють спільну електронну хмару (електронний газ), а атоми і позитивно заряджені йони, що виникли, утворюють металічну кристалічну ґратку.
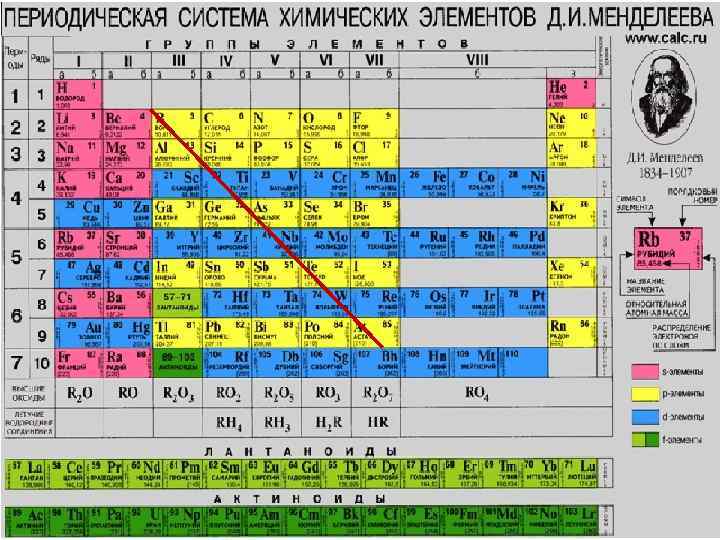
 До металів відносять понад 80 елементів періодичної системи Д. І. Менделєєва. Метали становлять головні підгрупи І, ІІ та ІІІ груп (за винятком Гідрогену, Гелію та Бору), усі побічні підгрупи. Металами є майже усі s-елементи (за винятком Гідрогену і Гелію), усі d- і f- елементи, частина p-елементів (Алюміній, Галій, Індій, Талій, Станум, Стибій, Плюмбум, Бісмут, Полоній). Якщо умовно провести діагональ від Бору до Астату, то всі елементи, розташовані нижче цієї діагоналі, а також ті, що розташовані вище неї у побічних підгрупах, будуть металами.
До металів відносять понад 80 елементів періодичної системи Д. І. Менделєєва. Метали становлять головні підгрупи І, ІІ та ІІІ груп (за винятком Гідрогену, Гелію та Бору), усі побічні підгрупи. Металами є майже усі s-елементи (за винятком Гідрогену і Гелію), усі d- і f- елементи, частина p-елементів (Алюміній, Галій, Індій, Талій, Станум, Стибій, Плюмбум, Бісмут, Полоній). Якщо умовно провести діагональ від Бору до Астату, то всі елементи, розташовані нижче цієї діагоналі, а також ті, що розташовані вище неї у побічних підгрупах, будуть металами.
 Фізичні властивості металів: - твердий агрегатний стан; - характерний металічний блиск у компактному стані; - електро- та теплопровідність; - ковкість, пластичність.
Фізичні властивості металів: - твердий агрегатний стан; - характерний металічний блиск у компактному стані; - електро- та теплопровідність; - ковкість, пластичність.
 2. Хімічні властивості металів Усі метали у вільному стані є відновниками. Відновна здатність металу визначається величиною його стандартного електродного потенціалу. Електрохімічний ряд напруг металів (ряд активності) Li, K, Ba, Ca, Na, Mg, Al, Mn, Zn, Cr, Fe, Ni, Sn, Pb, H, Bi, Cu, Hg, Ag, Pt, Au
2. Хімічні властивості металів Усі метали у вільному стані є відновниками. Відновна здатність металу визначається величиною його стандартного електродного потенціалу. Електрохімічний ряд напруг металів (ряд активності) Li, K, Ba, Ca, Na, Mg, Al, Mn, Zn, Cr, Fe, Ni, Sn, Pb, H, Bi, Cu, Hg, Ag, Pt, Au
 Правила користування електрохімічним рядом напруг: • Метали, розташовані у ряді напруг лівіше за водень, можуть витісняти його з розведених розчинів кислот-неокисників; метали, що розташовані у ряді напруг до Al включно, здатні витісняти його також з води. Метали, які стоять у ряді напруг правіше водню, з кислотаминеокисниками не взаємодіють. • Метали, розташовані у ряді напруг лівіше, можуть витісняти метали, розташовані у цьому ряді правіше, з розчинів їх солей. • Під час електрохімічного відновлення металів з їх
Правила користування електрохімічним рядом напруг: • Метали, розташовані у ряді напруг лівіше за водень, можуть витісняти його з розведених розчинів кислот-неокисників; метали, що розташовані у ряді напруг до Al включно, здатні витісняти його також з води. Метали, які стоять у ряді напруг правіше водню, з кислотаминеокисниками не взаємодіють. • Метали, розташовані у ряді напруг лівіше, можуть витісняти метали, розташовані у цьому ряді правіше, з розчинів їх солей. • Під час електрохімічного відновлення металів з їх
 Метали взаємодіють з неметалами, кислотами, водою, розчинами лугів, солей. І. Взаємодія металів з неметалами 1. Більшість металів (за винятком золота і металів платинової групи) в звичайних умовах або при нагріванні взаємодіють з киснем, утворюючи, як правило, оксиди (лужні метали, крім літію, у цій реакції дають пероксиди і надпероксиди): Mg + O 2 → Mg. O ; Al + O 2 → Al 2 O 3 ; Cu + O 2 → Cu. O ; Fe + O 2 → Fe 3 O 4 ; Li + O 2 → Li 2 O ; Mo + O 2 → Mo. O 3 ; але Na + O 2 → Na 2 O 2 ; K + O 2 → K 2 O 4
Метали взаємодіють з неметалами, кислотами, водою, розчинами лугів, солей. І. Взаємодія металів з неметалами 1. Більшість металів (за винятком золота і металів платинової групи) в звичайних умовах або при нагріванні взаємодіють з киснем, утворюючи, як правило, оксиди (лужні метали, крім літію, у цій реакції дають пероксиди і надпероксиди): Mg + O 2 → Mg. O ; Al + O 2 → Al 2 O 3 ; Cu + O 2 → Cu. O ; Fe + O 2 → Fe 3 O 4 ; Li + O 2 → Li 2 O ; Mo + O 2 → Mo. O 3 ; але Na + O 2 → Na 2 O 2 ; K + O 2 → K 2 O 4
 2. Більшість металів в звичайних умовах або при нагріванні взаємодіють з галогенами (фтором, хлором, бромом, йодом), утворюючи галогеніди (фториди, хлориди, броміди, йодиди): Fe + Cl 2 → Fe. Cl 3 ; Mg + F 2 → Mg. F 2 ; Al + I 2 → Al. I 3 ; Zn + Br 2 → Zn. Br 2 3. Більшість металів, як правило, при нагріванні взаємодіють з сіркою з утворенням сульфідів: Na + S → Na 2 S ; Zn + S → Zn. S ; Hg + S → Hg. S
2. Більшість металів в звичайних умовах або при нагріванні взаємодіють з галогенами (фтором, хлором, бромом, йодом), утворюючи галогеніди (фториди, хлориди, броміди, йодиди): Fe + Cl 2 → Fe. Cl 3 ; Mg + F 2 → Mg. F 2 ; Al + I 2 → Al. I 3 ; Zn + Br 2 → Zn. Br 2 3. Більшість металів, як правило, при нагріванні взаємодіють з сіркою з утворенням сульфідів: Na + S → Na 2 S ; Zn + S → Zn. S ; Hg + S → Hg. S
 4. Метали початку ряду активності взаємодіють з воднем з утворенням гідридів: Са + Н 2 → Са. Н 2 ; Na + H 2 → Na. H 5. Метали початку ряду активності взаємодіють з азотом з утворенням нітридів: Li + N 2 → Li 3 N ; Ca + N 2 → Ca 3 N 2 6. Метали початку ряду активності взаємодіють з бором з утворенням боридів: Mg + B → Mg 3 B 2
4. Метали початку ряду активності взаємодіють з воднем з утворенням гідридів: Са + Н 2 → Са. Н 2 ; Na + H 2 → Na. H 5. Метали початку ряду активності взаємодіють з азотом з утворенням нітридів: Li + N 2 → Li 3 N ; Ca + N 2 → Ca 3 N 2 6. Метали початку ряду активності взаємодіють з бором з утворенням боридів: Mg + B → Mg 3 B 2
 7. Метали початку ряду активності взаємодіють з фосфором з утворенням фосфідів: Zn + P → Zn 3 P 2 8. Метали початку ряду активності взаємодіють з кремнієм з утворенням силіцидів: Mg + Si → Mg 2 Si 9. Метали взаємодіють з вуглецем з утворенням карбідів: Ca + C → Ca. C 2
7. Метали початку ряду активності взаємодіють з фосфором з утворенням фосфідів: Zn + P → Zn 3 P 2 8. Метали початку ряду активності взаємодіють з кремнієм з утворенням силіцидів: Mg + Si → Mg 2 Si 9. Метали взаємодіють з вуглецем з утворенням карбідів: Ca + C → Ca. C 2
 ІІ. Взаємодія металів з кислотами 1. Взаємодія металів з кислотами-неокисниками (розбавлена H 2 SO 4, HCl, HBr, HI, H 3 PO 4, HNO 2, CH 3 COOH та ін. кислоти, у яких окисні властивості кислотного залишка слабші, ніж у йону Н+ або зовсім відсутні). З кислотами-неокисниками можуть взаємодіяти лише метали, розташовані в ряді напруг до водню. Окисником у таких реакціх є йон Н+. Продукти реакції - сіль відповідного металу і водень: Al + HCl → Al. Cl 3 + H 2 ; Mg + H 2 SO 4 (розб. ) → Mg. SO 4 + H 2 ; Zn + CH 3 COOH → Zn(CH 3 COO)2 + H 2
ІІ. Взаємодія металів з кислотами 1. Взаємодія металів з кислотами-неокисниками (розбавлена H 2 SO 4, HCl, HBr, HI, H 3 PO 4, HNO 2, CH 3 COOH та ін. кислоти, у яких окисні властивості кислотного залишка слабші, ніж у йону Н+ або зовсім відсутні). З кислотами-неокисниками можуть взаємодіяти лише метали, розташовані в ряді напруг до водню. Окисником у таких реакціх є йон Н+. Продукти реакції - сіль відповідного металу і водень: Al + HCl → Al. Cl 3 + H 2 ; Mg + H 2 SO 4 (розб. ) → Mg. SO 4 + H 2 ; Zn + CH 3 COOH → Zn(CH 3 COO)2 + H 2
 2. Взамодія металів з кислотами-окисниками (нітратна кислота будь-якої концентрації, концентрована сульфатна кислота, суміші деяких концентрованих кислот (конц. HNO 3 і конц. HCl (1: 3) – «царська водка» ) та ін. кислоти, у яких окисні властивості кислотного залишку виявлені сильніше, ніж у йону Гідрогену). Такі кислоти взаємодіють з металами за рахунок відновлення аніону кислотного залишку. З кислотами-окисниками взаємодіють як більшість металів, розташованих у ряді напруг до водню, так і частина металів, розташованих після водню (мідь, ртуть, срібло). Водень при взаємодії металів з кислотами-окисниками не виділяється, а утворюються сіль відповідного металу, вода і продукт відновлення кислотного залишку, який визначається як природою металу, так і концентрацією кислоти.
2. Взамодія металів з кислотами-окисниками (нітратна кислота будь-якої концентрації, концентрована сульфатна кислота, суміші деяких концентрованих кислот (конц. HNO 3 і конц. HCl (1: 3) – «царська водка» ) та ін. кислоти, у яких окисні властивості кислотного залишку виявлені сильніше, ніж у йону Гідрогену). Такі кислоти взаємодіють з металами за рахунок відновлення аніону кислотного залишку. З кислотами-окисниками взаємодіють як більшість металів, розташованих у ряді напруг до водню, так і частина металів, розташованих після водню (мідь, ртуть, срібло). Водень при взаємодії металів з кислотами-окисниками не виділяється, а утворюються сіль відповідного металу, вода і продукт відновлення кислотного залишку, який визначається як природою металу, так і концентрацією кислоти.
 а) нітратна кислота • концентрована (димляча) нітратна кислота пасивує деякі метали (Cr, Ni, Al, Fe); • концентрована нітратна кислота з малоактивними металами, розташованими у ряді напруг правіше Sn, дає сіль, воду і NO 2: Ag + HNO 3 (конц. ) → Ag. NO 3 + H 2 O + NO 2 • концентрована нітратна кислота з активними металами, розташованими у ряді напруг до Al, дає сіль, воду і N 2 O: Mg + HNO 3 (конц. ) → Mg(NO 3)2 + N 2 O + H 2 O
а) нітратна кислота • концентрована (димляча) нітратна кислота пасивує деякі метали (Cr, Ni, Al, Fe); • концентрована нітратна кислота з малоактивними металами, розташованими у ряді напруг правіше Sn, дає сіль, воду і NO 2: Ag + HNO 3 (конц. ) → Ag. NO 3 + H 2 O + NO 2 • концентрована нітратна кислота з активними металами, розташованими у ряді напруг до Al, дає сіль, воду і N 2 O: Mg + HNO 3 (конц. ) → Mg(NO 3)2 + N 2 O + H 2 O
 • розбавлена нітратна кислота з малоактивними металами дає сіль, воду і NO: Hg + HNO 3 (розб. ) → Hg(NO 3)2 + NO + H 2 O • розбавлена нітратна кислота з активними металами дає сіль, воду і NH 4 NO 3: Ca + HNO 3 (розб. ) → Ca(NO 3)2 + NH 4 NO 3 + H 2 O • Для металів середини ряду активності в залежності від концентрації кислоти можуть бути різні продукти відновленя кислотного залишку.
• розбавлена нітратна кислота з малоактивними металами дає сіль, воду і NO: Hg + HNO 3 (розб. ) → Hg(NO 3)2 + NO + H 2 O • розбавлена нітратна кислота з активними металами дає сіль, воду і NH 4 NO 3: Ca + HNO 3 (розб. ) → Ca(NO 3)2 + NH 4 NO 3 + H 2 O • Для металів середини ряду активності в залежності від концентрації кислоти можуть бути різні продукти відновленя кислотного залишку.
 • • б) концентрована сульфатна кислота (олеум), пасивує деякі метали (алюміній, нікель, залізо та ін. ); концентрована сульфатна кислота з малоактивними металами дає сіль, воду і SO 2: Cu + H 2 SO 4 (конц. )→ Cu. SO 4 + H 2 O + SO 2 концентрована сульфатна кислота з активними металами дає сіль, воду і H 2 S: Ca + H 2 SO 4 (конц. ) → Ca. SO 4 + H 2 O + H 2 S концентрована сульфатна кислота з металами середини ряду активності дає сіль, воду і, залежно від концентрації кислоти, або SO 2, або S, або H 2 S: Zn + H 2 SO 4 (98%) → Zn. SO 4 + H 2 O + SO 2; Zn + H 2 SO 4 (70%) → Zn. SO 4 + H 2 O+ S; Zn + H 2 SO 4 (50%) → Zn. SO 4 + H 2 O + H 2 S
• • б) концентрована сульфатна кислота (олеум), пасивує деякі метали (алюміній, нікель, залізо та ін. ); концентрована сульфатна кислота з малоактивними металами дає сіль, воду і SO 2: Cu + H 2 SO 4 (конц. )→ Cu. SO 4 + H 2 O + SO 2 концентрована сульфатна кислота з активними металами дає сіль, воду і H 2 S: Ca + H 2 SO 4 (конц. ) → Ca. SO 4 + H 2 O + H 2 S концентрована сульфатна кислота з металами середини ряду активності дає сіль, воду і, залежно від концентрації кислоти, або SO 2, або S, або H 2 S: Zn + H 2 SO 4 (98%) → Zn. SO 4 + H 2 O + SO 2; Zn + H 2 SO 4 (70%) → Zn. SO 4 + H 2 O+ S; Zn + H 2 SO 4 (50%) → Zn. SO 4 + H 2 O + H 2 S
 ІІІ. Взаємодія металів з водою Метали початку ряду активності (до Al включно) можуть витісняти водень з води, утворюючи при цьому відповідні гідроксиди: Li + H 2 O → Li. OH + H 2 ; Ca + H 2 O → Ca(OH)2 + H 2 ІV. Взаємодія металів з лугами Метали, які мають амфотерні оксиди і гідроксиди, можуть взаємодіяти з розчинами лугів (краще при нагріванні). При цьому виділяється водень і утворюються солі (точніше, гідроксокомплекси): Zn + KOH → K 2 Zn. O 2 + H 2; Zn + KOH + H 2 O → K 2 Zn(OH)4 + H 2
ІІІ. Взаємодія металів з водою Метали початку ряду активності (до Al включно) можуть витісняти водень з води, утворюючи при цьому відповідні гідроксиди: Li + H 2 O → Li. OH + H 2 ; Ca + H 2 O → Ca(OH)2 + H 2 ІV. Взаємодія металів з лугами Метали, які мають амфотерні оксиди і гідроксиди, можуть взаємодіяти з розчинами лугів (краще при нагріванні). При цьому виділяється водень і утворюються солі (точніше, гідроксокомплекси): Zn + KOH → K 2 Zn. O 2 + H 2; Zn + KOH + H 2 O → K 2 Zn(OH)4 + H 2
 V. Взаємодія металів з розчинами солей інших металів Метали, розташовані у ряді активності металів лівіше, можуть витісняти метали, розташовані правіше, з розчинів їх солей: Fe + Cu. SO 4 → Fe. SO 4 + Cu; Zn + Pb(CH 3 COO)2 → Zn(CH 3 COO)2 + Pb; Cu + Fe. SO 4 →
V. Взаємодія металів з розчинами солей інших металів Метали, розташовані у ряді активності металів лівіше, можуть витісняти метали, розташовані правіше, з розчинів їх солей: Fe + Cu. SO 4 → Fe. SO 4 + Cu; Zn + Pb(CH 3 COO)2 → Zn(CH 3 COO)2 + Pb; Cu + Fe. SO 4 →
 3. Корозія металів і методи боротьби з нею Корозія металів – це гетерогенний окисновідновний процес, який відбувається на границі поділу фаз метал – газ або метал-розчин (розчинник). Корозія металів – процес довільного руйнування металів, зумовлений їх поверхневим окисненням внаслідок хімічної або електрохімічної взаємодії з оточуючим середовищем. Корозію класифікують за характером руйнування і за фізико-хімічним механізмом взаємодії металів з середовищем.
3. Корозія металів і методи боротьби з нею Корозія металів – це гетерогенний окисновідновний процес, який відбувається на границі поділу фаз метал – газ або метал-розчин (розчинник). Корозія металів – процес довільного руйнування металів, зумовлений їх поверхневим окисненням внаслідок хімічної або електрохімічної взаємодії з оточуючим середовищем. Корозію класифікують за характером руйнування і за фізико-хімічним механізмом взаємодії металів з середовищем.
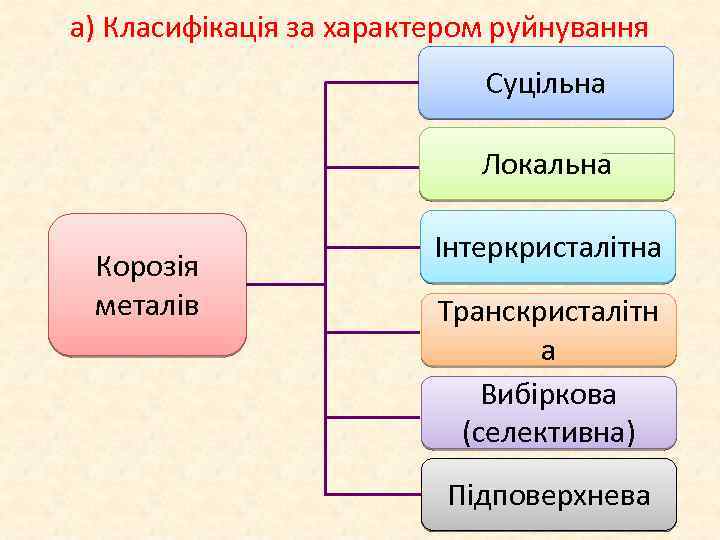 а) Класифікація за характером руйнування Суцільна Локальна Корозія металів Інтеркристалітна Транскристалітн а Вибіркова (селективна) Підповерхнева
а) Класифікація за характером руйнування Суцільна Локальна Корозія металів Інтеркристалітна Транскристалітн а Вибіркова (селективна) Підповерхнева
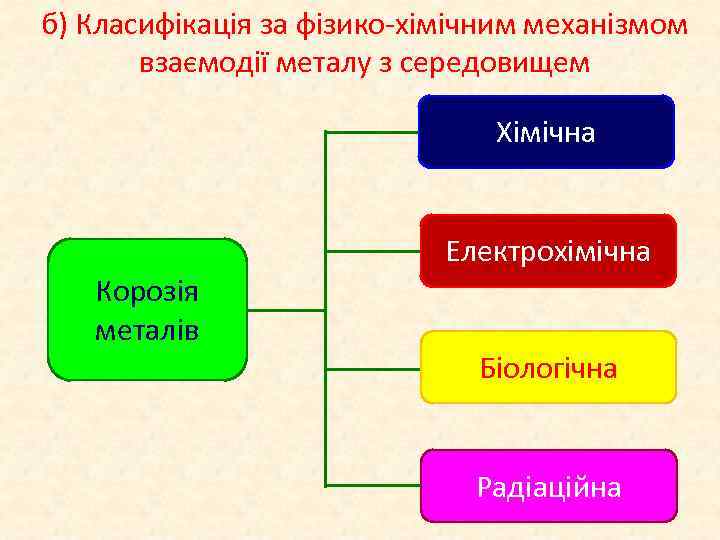 б) Класифікація за фізико-хімічним механізмом взаємодії металу з середовищем Хімічна Електрохімічна Корозія металів Біологічна Радіаційна
б) Класифікація за фізико-хімічним механізмом взаємодії металу з середовищем Хімічна Електрохімічна Корозія металів Біологічна Радіаційна
 Хімічна корозія – процес довільного руйнування металів під впливом навколишнього середовища, який полягає у безпосередньому хімічному окисненні металу агресивним середовищем, відбувається, як правило, при високих температурах і не супроводжується виникненням у системі електричного струму. При хімічній корозії електрони безпосередньо відновника (металу) переходять до окисника, а продукти корозії залишаються на поверхні металу або сплаву.
Хімічна корозія – процес довільного руйнування металів під впливом навколишнього середовища, який полягає у безпосередньому хімічному окисненні металу агресивним середовищем, відбувається, як правило, при високих температурах і не супроводжується виникненням у системі електричного струму. При хімічній корозії електрони безпосередньо відновника (металу) переходять до окисника, а продукти корозії залишаються на поверхні металу або сплаву.
 Хімічна корозія Газова В середовищі неелектроліт ів
Хімічна корозія Газова В середовищі неелектроліт ів
 Електрохімічна корозія – процес довільного руйнування металів під впливом навколишнього середовища, який відбувається у середовищі електролітів і супроводжується виникненням у системі електричного струму. Електрохімічна корозія має місце під час контактування різних металів у присутності води, у вологому повітрі, в середовищі електролітів: кислот, солей, лугів.
Електрохімічна корозія – процес довільного руйнування металів під впливом навколишнього середовища, який відбувається у середовищі електролітів і супроводжується виникненням у системі електричного струму. Електрохімічна корозія має місце під час контактування різних металів у присутності води, у вологому повітрі, в середовищі електролітів: кислот, солей, лугів.
 У разі електрохімічної корозії процеси окиснення і відновлення просторово розділені і відбуваються на різних ділянках металу. Переміщення електронів відновника до окисника обумовлює виникнення електричного струму. Ділянки з більш негативним потенціалом – анодні, на них відбувається анодний процес окиснення металу Ме = Меn+.
У разі електрохімічної корозії процеси окиснення і відновлення просторово розділені і відбуваються на різних ділянках металу. Переміщення електронів відновника до окисника обумовлює виникнення електричного струму. Ділянки з більш негативним потенціалом – анодні, на них відбувається анодний процес окиснення металу Ме = Меn+.
 Ділянки з більш позитивним потенціалом – катодні. На них відбуваються катодні процеси – відновлення йонів Гідрогену або молекул розчиненого у воді кисню. Характер катодного процесу залежить від р. Н середовища. У кислому середовищі відбувається воднева деполяризація катода, яка супроводжується виділенням водню 2 Н+ + = Н 2. У нейтральному та лужному середовищі відбувається киснева деполяризація катода О 2 + 2 Н 2 О + = 4 ОН–.
Ділянки з більш позитивним потенціалом – катодні. На них відбуваються катодні процеси – відновлення йонів Гідрогену або молекул розчиненого у воді кисню. Характер катодного процесу залежить від р. Н середовища. У кислому середовищі відбувається воднева деполяризація катода, яка супроводжується виділенням водню 2 Н+ + = Н 2. У нейтральному та лужному середовищі відбувається киснева деполяризація катода О 2 + 2 Н 2 О + = 4 ОН–.
 Виникнення електрохімічної корозії Гальванічний елемент: (–) Fe || 2 н. H 2 SO 4 || Cu (+) Процеси, що відбуваються: Fe - = Fe 2+ Fe – анод 2 H+ + = H 2 Cu – катод
Виникнення електрохімічної корозії Гальванічний елемент: (–) Fe || 2 н. H 2 SO 4 || Cu (+) Процеси, що відбуваються: Fe - = Fe 2+ Fe – анод 2 H+ + = H 2 Cu – катод
 Електрохімічна корозія металів – результат дії численних гальванічних мікроелементів, які виникають під час стикання металу з агресивним середовищем. У випадку корозії з кисневою деполяризацією можливі вторинні процеси. Це приводить до утворення вторинних продуктів корозії.
Електрохімічна корозія металів – результат дії численних гальванічних мікроелементів, які виникають під час стикання металу з агресивним середовищем. У випадку корозії з кисневою деполяризацією можливі вторинні процеси. Це приводить до утворення вторинних продуктів корозії.
 Біологічна корозія – процес корозії металів, що відбувається за рахунок мікроорганізмів (водневі, залізобактерії, тіобактерії, азотфіксуючі бактерії тощо). Біокорозія сприяє хімічній корозії, зміщуючи рівновагу цього процесу у бік хімічної корозії. Вона вражає металеві поверхні у місцях знаходження продуктів хімічної корозії, що призводить до оголення металевої поверхні і тим самим до подальшого перебігу хімічної корозії.
Біологічна корозія – процес корозії металів, що відбувається за рахунок мікроорганізмів (водневі, залізобактерії, тіобактерії, азотфіксуючі бактерії тощо). Біокорозія сприяє хімічній корозії, зміщуючи рівновагу цього процесу у бік хімічної корозії. Вона вражає металеві поверхні у місцях знаходження продуктів хімічної корозії, що призводить до оголення металевої поверхні і тим самим до подальшого перебігу хімічної корозії.
 Радіаційна корозія – руйнування металів, що відбувається внаслідок дії на них радіаційного або йонізуючого опромінення. Радіаційне опромінення призводить до порушення структури металу і тим самим сприяє розвитку інших корозійних процесів (хімічної та електрохімічної корозії).
Радіаційна корозія – руйнування металів, що відбувається внаслідок дії на них радіаційного або йонізуючого опромінення. Радіаційне опромінення призводить до порушення структури металу і тим самим сприяє розвитку інших корозійних процесів (хімічної та електрохімічної корозії).
 Методи боротьби з корозією металів 1). Застосування металів високої чистоти; 2). Створення захисних покриттів Захисне покриття металічне неметалічне анодне катодне
Методи боротьби з корозією металів 1). Застосування металів високої чистоти; 2). Створення захисних покриттів Захисне покриття металічне неметалічне анодне катодне
 Анодне покриття – покриття металу плівкою більш активного металу. В разі пошкодження анодного покриття виникає гальванічна пара покриття/метал (покриття відіграє роль анода, а захищуваний метал – катода). Відбувається розчинення покриття, захищуваний метал не руйнується.
Анодне покриття – покриття металу плівкою більш активного металу. В разі пошкодження анодного покриття виникає гальванічна пара покриття/метал (покриття відіграє роль анода, а захищуваний метал – катода). Відбувається розчинення покриття, захищуваний метал не руйнується.
 Катодне покриття – покриття металу плівкою менш активного металу. У разі пошкодження катодного покриття, виникає гальванічна пара метал/покриття, (захищуваний метал у є анодом, він розчиняється, а покриття – катодом і залишається незмінним). Висновок: катодне покриття захищає метал від корозії лише до порушення своєї цілісності. Пошкодження катодного покриття приводить до підповерхневої корозі захищуваного металу.
Катодне покриття – покриття металу плівкою менш активного металу. У разі пошкодження катодного покриття, виникає гальванічна пара метал/покриття, (захищуваний метал у є анодом, він розчиняється, а покриття – катодом і залишається незмінним). Висновок: катодне покриття захищає метал від корозії лише до порушення своєї цілісності. Пошкодження катодного покриття приводить до підповерхневої корозі захищуваного металу.
 3). Створення антикорозійних сплавів; 4). Зміна складу середовища; 5). Електрохімічні методи захисту: - протекторний захист; - катодний захист.
3). Створення антикорозійних сплавів; 4). Зміна складу середовища; 5). Електрохімічні методи захисту: - протекторний захист; - катодний захист.


