метал нов.ppt
- Количество слайдов: 51

Металдар мен бейметалдардың табиғатта таралуы. ҚР-дағы кен орындары

Сабақтың мақсаты: 1. Бейметалдар мен металдардың периодтық жүйедегі орны және электрондық құрылысы, физикалық қасиеттері, бейметалдар мен металдардың және олардың қосылыстарының Қазақстанның аймақтарында таралуы туралы білімдерін бекіту. 2. Бейметалдар мен металдарды алу әдістері туралы білімдерін тереңдету. Элемент, жай және күрделі заттар туралы білімдерін кеңейту. 3. Оқушылардың ғылыми дүниетанымын қалыптастыру.

Сабақтың түрі : Жаңа сабақ, бекіту Сабақтың әдісі: Сұрақ жауап, баяндау, жеке, жалпы Пәнаралық байланыс: география, биология Сабақтың көрнекілігі: интерактивті тақта Сабақтың барысы: І. Ұйымдастыру кезеңі а) оқушылармен амандасу б) оқушыларды түгендеу
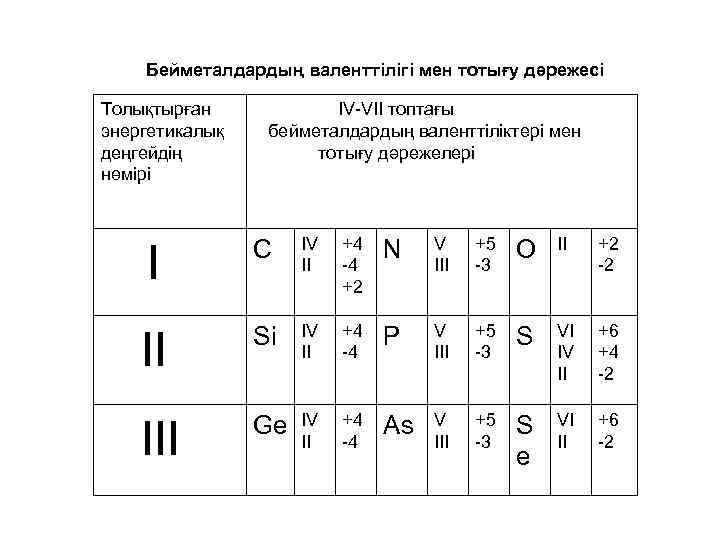
Бейметалдардың валенттілігі мен тотығу дәрежесі Толықтырған энергетикалық деңгейдің нөмірі IV-VII топтағы бейметалдардың валенттіліктері мен тотығу дәрежелері I C IV II +4 -4 +2 N V III +5 -3 O II +2 -2 II Si IV II +4 -4 P V III +5 -3 S VI IV II +6 +4 -2 III Ge IV II +4 -4 As V III +5 -3 S e VI II +6 -2
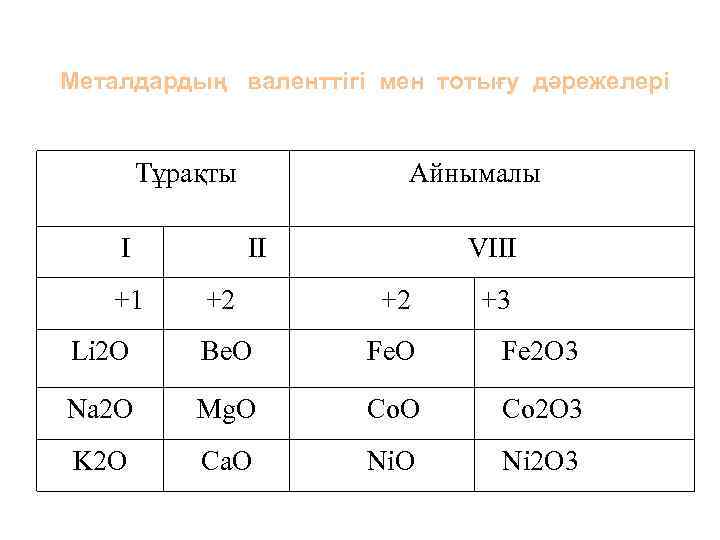
Металдардың валенттігі мен тотығу дәрежелері Тұрақты I +1 Айнымалы II VIII +2 +2 +3 Li 2 O Be. O Fe 2 O 3 Na 2 O Mg. O Co 2 O 3 K 2 O Ca. O Ni 2 O 3
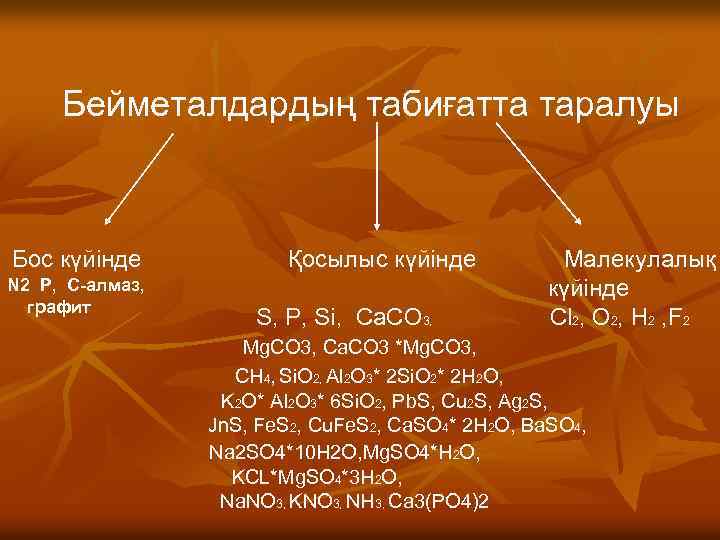
Бейметалдардың табиғатта таралуы Бос күйінде N 2 P, C-алмаз, графит Қосылыс күйінде S, P, Si, Ca. CO 3, Малекулалық күйінде Cl 2, O 2, H 2 , F 2 Mg. CO 3, Ca. CO 3 *Mg. CO 3, CH 4, Si. O 2, Al 2 O 3* 2 Si. O 2* 2 H 2 O, K 2 O* Al 2 O 3* 6 Si. O 2, Pb. S, Cu 2 S, Ag 2 S, Jn. S, Fe. S 2, Cu. Fe. S 2, Ca. SO 4* 2 H 2 O, Ba. SO 4, Na 2 SO 4*10 H 2 O, Mg. SO 4*H 2 O, KCL*Mg. SO 4*3 H 2 O, Na. NO 3, KNO 3, NH 3, Ca 3(PO 4)2
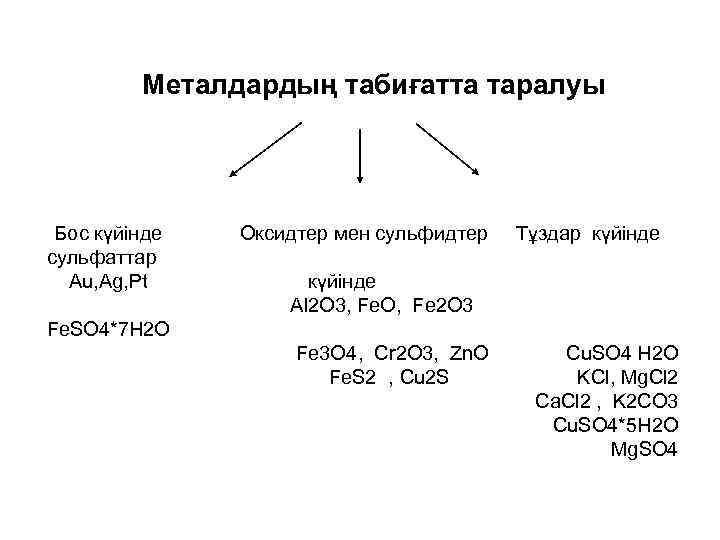
Металдардың табиғатта таралуы Бос күйінде сульфаттар Au, Ag, Pt Оксидтер мен сульфидтер Тұздар күйінде Al 2 O 3, Fe. O, Fe 2 O 3 Fe. SO 4*7 H 2 O Fe 3 O 4, Cr 2 O 3, Zn. O Fe. S 2 , Cu 2 S Cu. SO 4 H 2 O KCl, Mg. Cl 2 Ca. Cl 2 , K 2 CO 3 Cu. SO 4*5 H 2 O Mg. SO 4
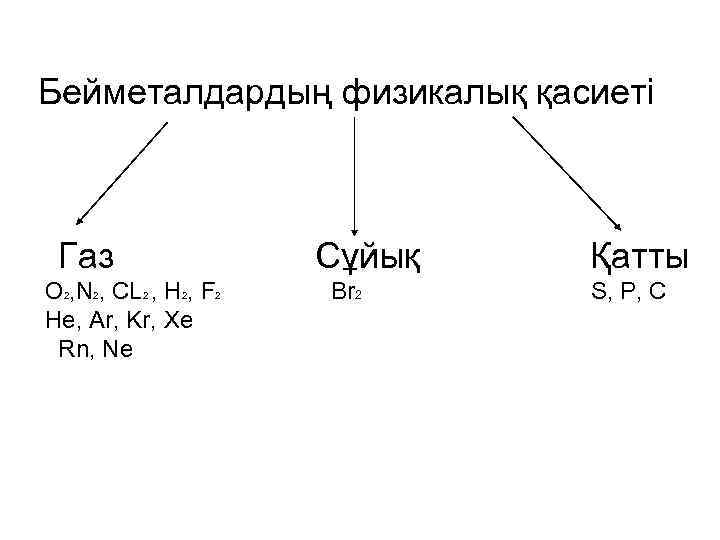
Бейметалдардың физикалық қасиеті Газ O 2, N 2, CL 2 , H 2, F 2 He, Ar, Kr, Xe Rn, Ne Сұйық Br 2 Қатты S, P, C
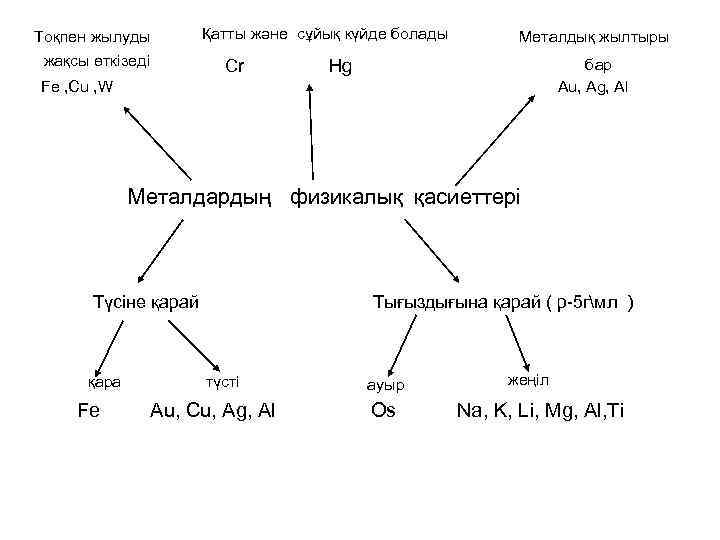
Тоқпен жылуды жақсы өткізеді Қатты және сұйық күйде болады Cr Металдық жылтыры бар Au, Ag, Al Hg Fe , Cu , W Металдардың физикалық қасиеттері Түсіне қарай қара Fe Тығыздығына қарай ( p-5 гмл ) түсті Au, Cu, Ag, Al ауыр Os жеңіл Na, K, Li, Mg, Al, Ti

Балқу температурасына ( t-1000°C ) оңай балқитын Ga-30°C Cs-28°C Hg-(-39°C) қиын балқитын W-3370°C Re-3170°C Ta-3000°C
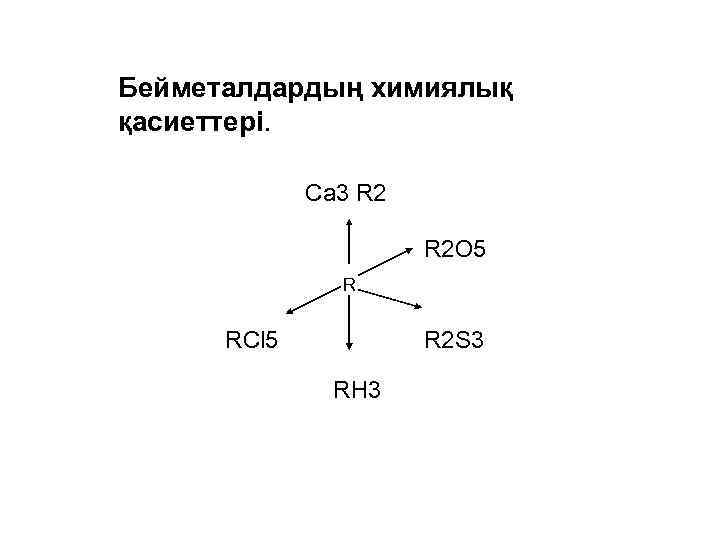
Бейметалдардың химиялық қасиеттері. Ca 3 R 2 O 5 R RCl 5 R 2 S 3 RH 3
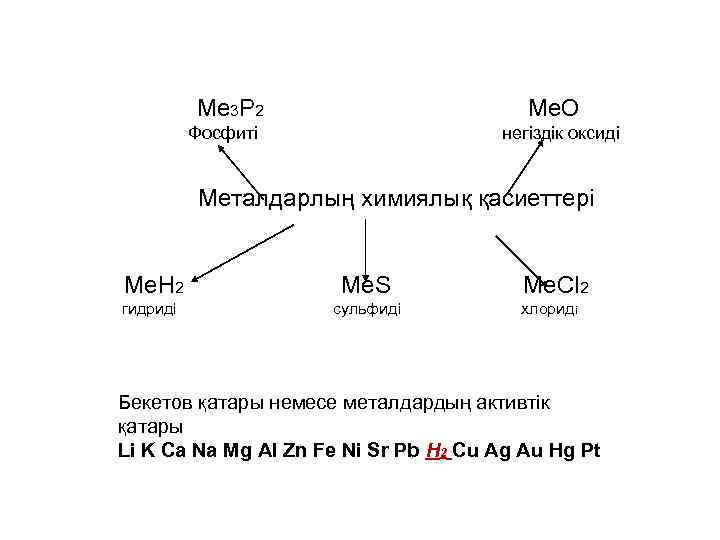
Me 3 P 2 Me. O Фосфиті негіздік оксиді Металдарлың химиялық қасиеттері Me. H 2 Me. S гидриді сульфиді Me. Cl 2 хлориді Бекетов қатары немесе металдардың активтік қатары Li K Ca Na Mg Al Zn Fe Ni Sr Pb H 2 Cu Ag Au Hg Pt

Li k Ca Mg Al Zn Cr Fe Ni Sn Pb H Cu Hg Ag Pt Au Атомдардың тотықсыздандырғыш қабілеті артады Кәдімгі жағдайда Қыздырғанда тотығады Қыздырғанда да тотығады тотықпайды Сумен кәдімгі жағдайда Сумен қыздырғанда Сумен әрекеттеспейді әрекеттеседі Ме(ОН)n әрекеттеседі Ме. О ж/е Н 2 түзіледі Қышқылдармен (концентрациялы H 2 SO 4 ж/е HNO 3 тен басқалары) H 2 бөле әрекеттеседі Қышқылдармен (концентрациялы H 2 SO 4 ж/е HNO 3 - тен басқалары) әрекеттеспейді Белсендірек металл өзінен белсенділігі төмен металды тұздарының ерітіндісінен ығыстырып шығарады: Me 1 + Me 2 = Me 1 + Me 2 Табиғатта тек қосылыстар түрінде кездеседі(тұздар мен оксидтер) Табиғатта қосылыстар түрінде де, бос күйінде де

Ba. SO 4 Тұздары SO 2, SO 3 Оксидтері H 2 SO 4 Күкірт қышқылы S H 2 S Күкіртсутек қышқылы H 2 SO 3 Күкіртті қышқыл
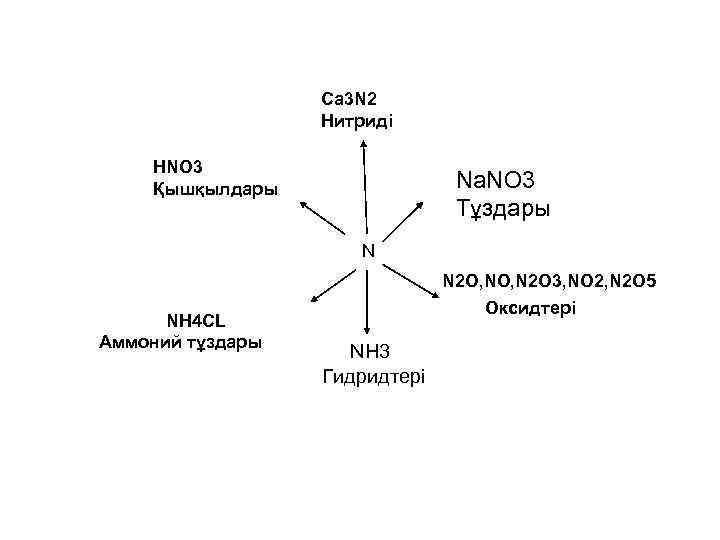
Ca 3 N 2 Нитриді HNO 3 Қышқылдары Na. NO 3 Тұздары N NH 4 CL Аммоний тұздары N 2 O, N 2 O 3, NO 2, N 2 O 5 Оксидтері NH 3 Гидридтері
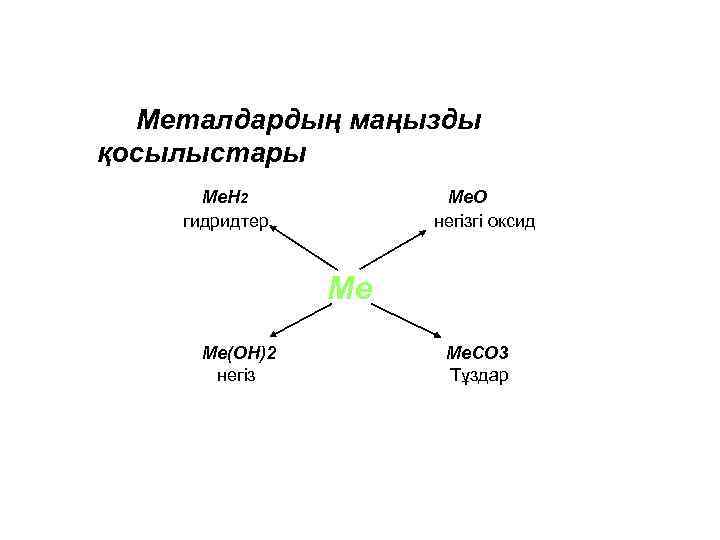
Металдардың маңызды қосылыстары Me. H 2 гидридтер Me. O негізгі оксид Ме Me(OH)2 негіз Me. CO 3 Тұздар
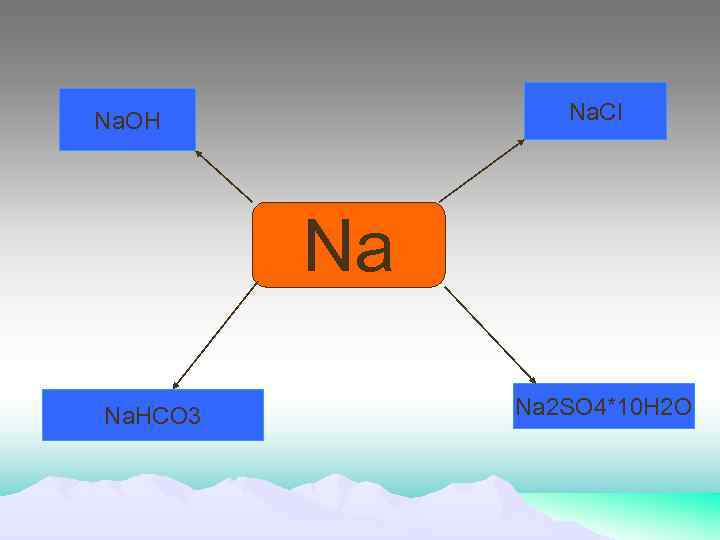
Na. Cl Na. OH Na Na. HCO 3 Na 2 SO 4*10 H 2 O
KCl. O 3 KOH K KNO 3 KMn. O 4

Ca. O Ca(OH)2 Ca Ca. CO 3 Ca. SO 4*2 H 2 O
O N Бейметалдардың қолданылуы P S Si J Cl
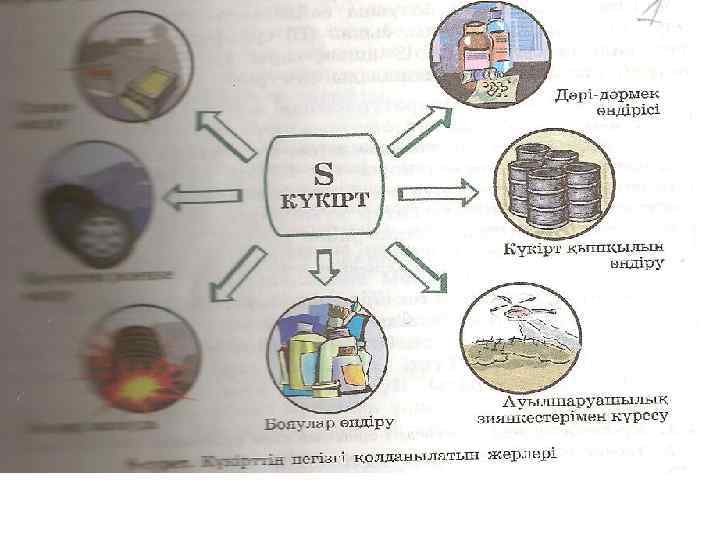
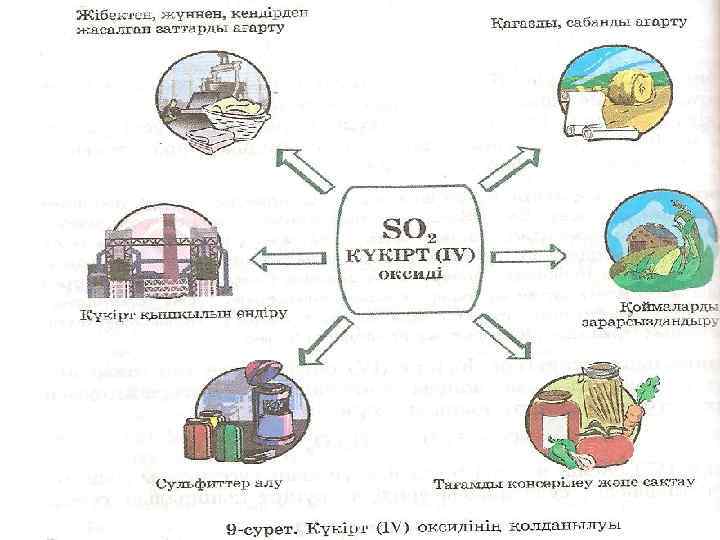

Na K Металдардың қолданылуы Ca Ag Cu Fe Zn Al Cr

Алтын мен күмістен жасалған әшекей бұйымдар

Тайқазан Алтын адам

Көне мәрмәр мүсін(Греция

Сталактиттер мен сталагмиттер Құрамында кальций бар табиғи қосылыстар: жұмыртқа қабығы, маржандар, ұлутастар

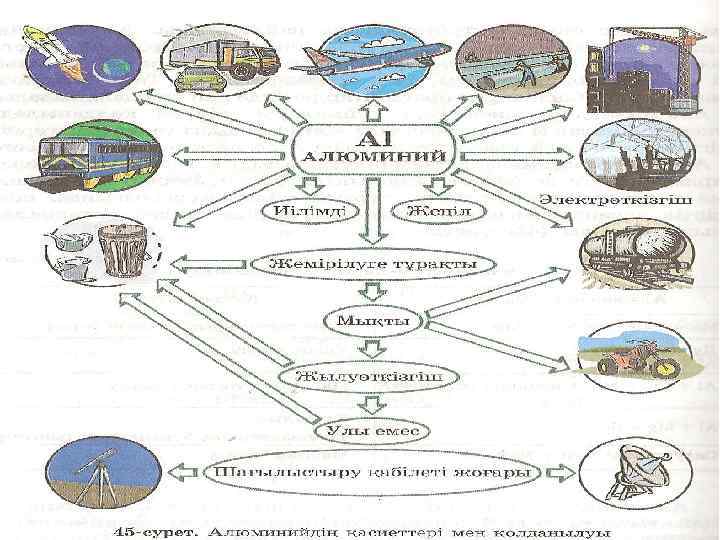



Бейметалдардың және олардың қосылыстарының Қазақстанда шоғырланған аймақтары Элемент C N P Таралуы Бос күйінде алмаз, графит, карбин Ауаның Қосылыс күйінде Корбанаттар мен гидрокорбанаттар. Мұнай, тас көмір, газ. Селитраларда, нәруызда, Қазақстанның қай аймақтарында кездеседі? Маңғыстау, Екібастұз, Қарағанды. Ақтауда тыңайтқыштары, Теміртада 78% N 2 нуклеин қышқылында Қызыл фосфор Р 4 Фосфорит Ca 3(PO 4)2 апатит Ca 5(PO 4)3 OH нуклеин қышқылдарында Ақтөбе, Қаратау, Шымкент тыңайтқыштары. Өндірісі Тараз, Жаңатас S Вулкан газдарында Сульфидтер Fes, Zns Сульфаттар Ca. SO 4*2 H 2 O Mg. SO 4*7 H 2 O Балқаш, Шығыс Қазақстан. Мұнайдың құрамында Маңғыстау, Қостанай Si Жер қыртысында Si. O 2 (кварц) силикаттар Қостанай, Жетіқара.
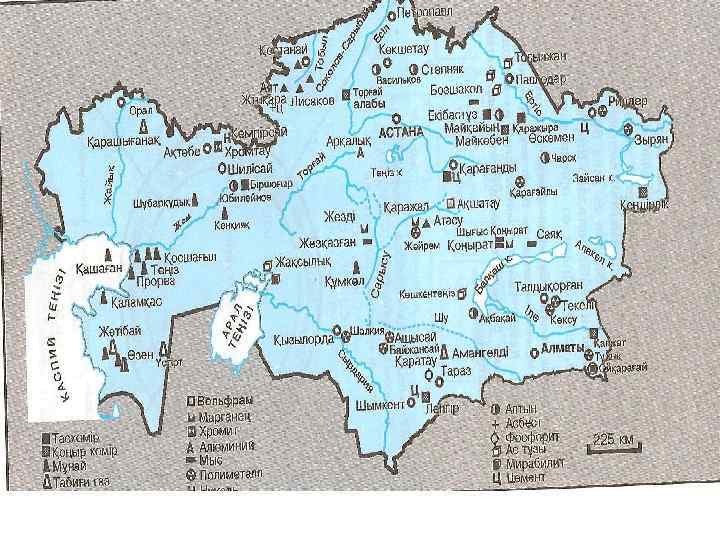

Қазақстандағы металдардың кендері және металл өндірісінің шоғырланған аймақтары Pb, Zn-Текелі, Мелеевск, Ащысай, Шымкент, Өскемен. Mg, Zn, In, Be, Ta, Nb-Өскеменде өндіріледі. Mn-Қаражал жезді, Жәйрем Қарағанды обл. Cr-Кемпірсайда, Ақтөбе обл. Cu- Жезқазған, Ақтоғай, Айдарлы, Балқаш, Ақсу, Семей обл. W, Mo-Ағадыр, Қатонқарағайда Sn-Көкшетауда(Сырымбет), Қорғалжың Ru-Большевик, Бестөбе, Бақыршық, Өскемен обл.

Бейметалдардың биохимиялық ролі С- көміртек тірі организмдер үшін ең басты органоген. Бірақ күйе түріндегі көміртек және оның монооксиді СО адам үшін зиянды. Ұзақ уақыт күйемен Немесе көмір шаңымен жұмыс істегенде қатерлі тері ісігін тудырады. Көміртек монооксиді СО өте улы. СО-ның уландырғыш әсері, ол қанның Гемоглобиніне жеңілқосылып, оны оттекті өкпеден ұлпаларға тасымалдауға Қабілетсіз етеді. СО – мен уланғанда антидот ретінде карбоген деп аталатын 35% -ті СО 2 мен О 2 –нің қоспасы қолданылады. Бұл қоспадағы О 2 –нің жоғары қысымы Ұлпадан СО-ны ығыстырады, ал СО 2 -нің қанды қышқылдандыру, сондай –ақ СО 2 СО-ның ығыстырады. Карбонаттары Са. СО 3, Na. HCO 3 медициналық Препараттардың антиацидтік /қышқылға қарсы/ әсері бар және асқазан сөлінің Қышқылдығын төмендету үшін қолданылады. Si- кремний қоспа элемент деп аталады. Оның адам организміндегі мөлшері өте аз Және 10 -3 –тін құрайды. Кремнийдің бауырда, бүйректе, шашта және көздің Қарашығында болатыны анықталған.

Р- адам организмдегі мөлшері бойынша(0, 95%) макрозлементке жатады. Фосфор-органоген-элемент және зат алмасуда маңызды рол атқарады. Ол жануар қаңқасының құрамына-кальций ортофосфаты, гидроксилапатит, тіс құрамына- гидроксилапатит, фторапатит ретінде кіреді. S-Белок құрамына SH-атомымен байланысқан SH-тобы түрінде кіреді. Көптеген құрамында күкірті бар қосылыстар дәрі ретінде қолданылады. Күкірт S цианидпен уланғанда(CN) қолданылады. Күкірттің газтектес қосылыстары H 2 S және SO 2 – улылығы жоғары заттар. Күкіртсутек H 2 S зиянды әсері тыныс алу тізбнгіне электрондарда тасымалдауға жауапты цитохромоксидозаның ферментінің қызметін тежейді және H 2 S-тің организмге түсуі тыныс алу циклін бұзады.

Металдардың биохимиялық ролі Сu- өсімдік және жануарлар организмінде 10 -5 тен 10 -3 %-ке аралықта болады. Мысқа кейбір омыртқасыздар – былқылдақ денелер мен бунақаяқтылар / теңіз шаяндары , кальмарлар, сегізаяқтылар/ бай болады. ХІХ ғасырдың өзінде ұлулардың көгілдір қанын зерттегенде ғалымдар мынадай қорытындыға келді: көгілдір түс қанда мыстың болуын көрсетеді. Ол адамның қанында шамамен 0, 001 мг/л мөлшерде болады. Жануар мен адам организмінде мыс бауырда концентрленеді. Ол қан түзу процесін күшейтетін ферменттердің құрамына кіреді, көмір алмасуын, және майлар синтезін, витаминдердің түзілуін қамтамасыз етеді. Мыс өсімдіктерге де қажет. Адам организмінде мыс жетпесе, қаназдық /анемия/ ауруы пайда болады, ал өсімдіктерде мыс жетпесе, олардың дамуы мен жеміс беруі нашарлайды. Бірақ оның артық мөлшері де зиянды. Адам үшін мыстың барлық улы. Мыс қосылыстарын өсімдіктердің зиянкестеріне және саңырауқұлақтарға қарсы күресте қолданады.

Zn –адам организмінде мырыштың жетіспеуі иіс және дәм сезуді толық өзгертеді. Мырыш қызыл қан түйіршіктерінде болады және организмнен органикалық заттардың негізгі тотығу өнімдерін шығаруға әсер ететін ферментердің құрамына кіреді. Көптеген теңіз омыртқасыздар мырышты жинақтаушы. Әсіресе устрицада мырыш көп, мөлшері 0, 7%-ке жетеді. Жер бетіндегі өсімдіктерден мырышқа саңырауқұлақтар –түлкі және майқұлақ бай. Топырақта мырыш жетпесе, өсімдіктің өсуі баяулайды. Сондықтан мырыш микроэлементтері бар арнайы тыңайтқыштардың құрамына кіреді. Fe- темір тірі организмдерде болады. Үлкен адамның денесінде 4 -5 г темір болады, ал оның 65% -і қанның гемоглобинінде. Қанда темірдің жетіспеуі адаманың денсаулығына әсер етеді, қаназдық пайда болады. Байланысқан темір көптеген тамақ өнімдерінде : қара нанда, картопта, ашада, өрікте, қарақұмықта болады. Бұл өнімдерді қаназдықтың алдын алу үшін тамақ рационына енгізу керек

Есептер шығару. Массасы 3, 42 грамм сілтілік металл сумен әрекеттескенде (қ. ж. ) 0, 448 л сутегі бөлінді. Бұл қандай металл? Массасы 13, 7 грамм металл заряды +2 -ге тең катион түзіп сумен реакцияласқанда қалыпты жағдайда 2, 24 л газ бөлінеді. Бұл қандай металл?

метал нов.ppt