Лекция_обмен железа_06_02_2015.ppt
- Количество слайдов: 47

Метаболизм железа в организме человека Лабораторная диагностика нарушений обмена железа

г. Брюссель Атомиум - увеличенная в 165 миллиардов раз модель кристаллической решетки атомов железа (высота - 102 м)

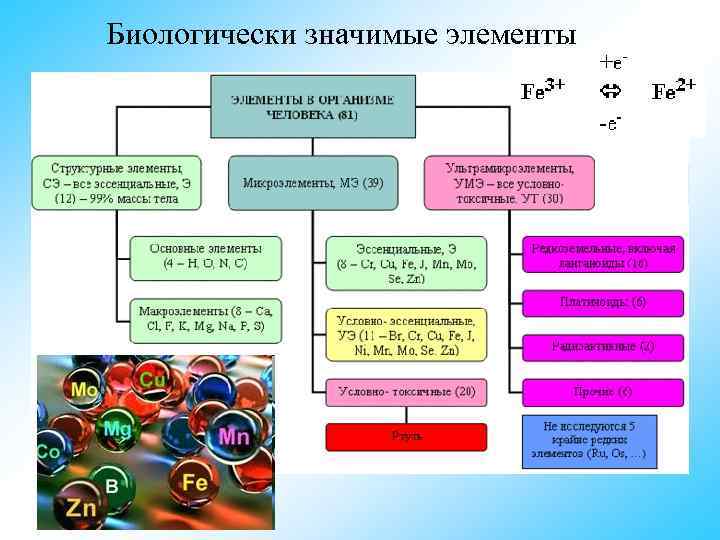
Биологически значимые элементы
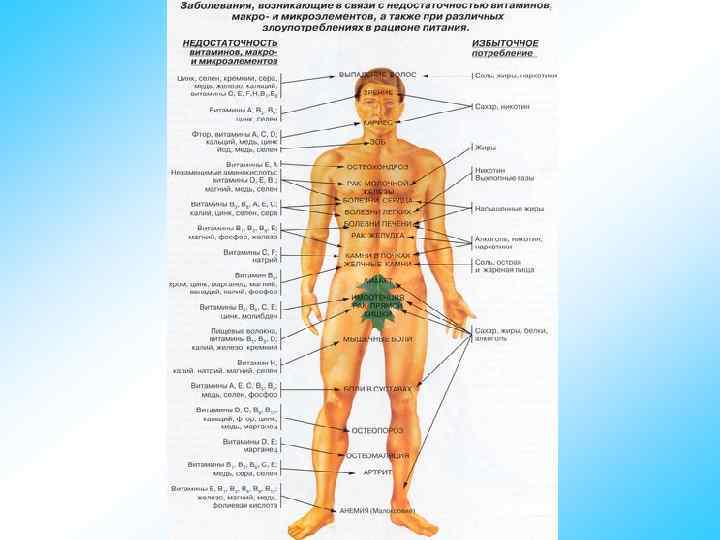
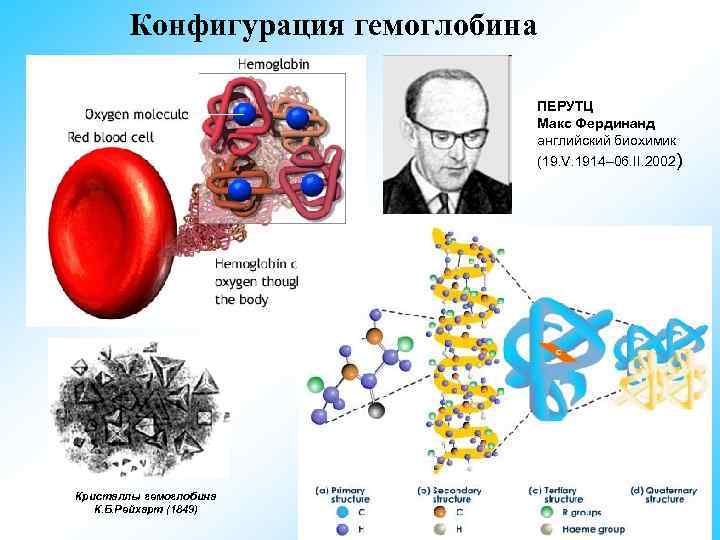
Конфигурация гемоглобина ПЕРУТЦ Макс Фердинанд английский биохимик (19. V. 1914– 06. II. 2002) Кристаллы гемоглобина К. Б. Рейхарт (1849)
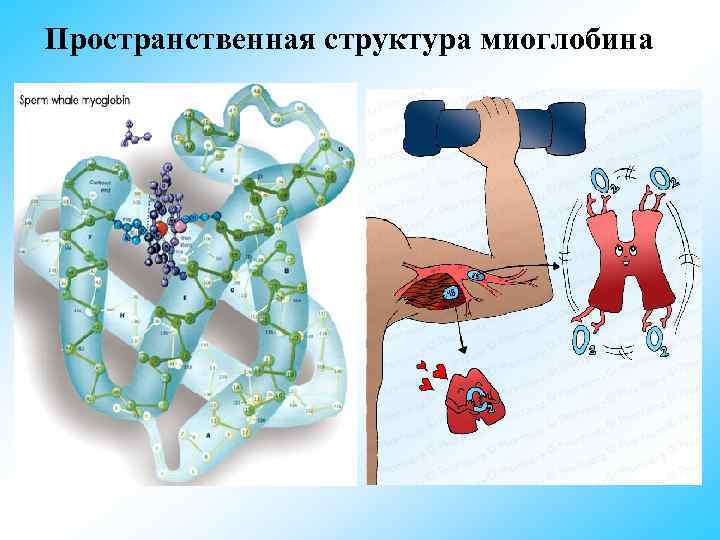
Пространственная структура миоглобина
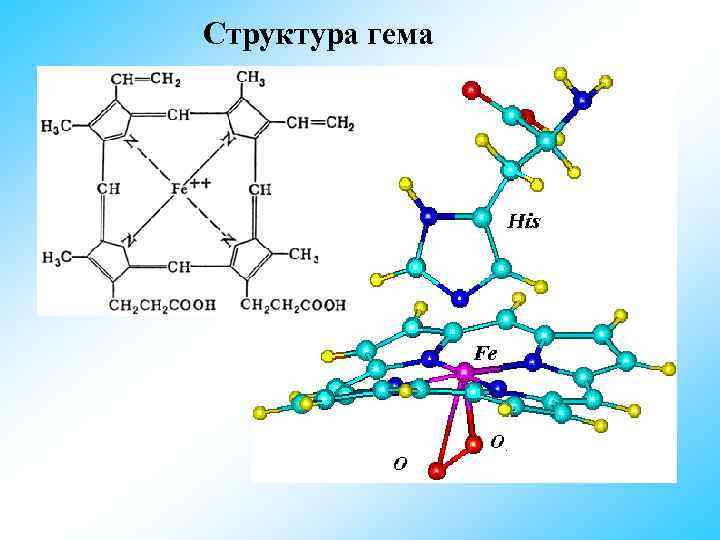
Структура гема
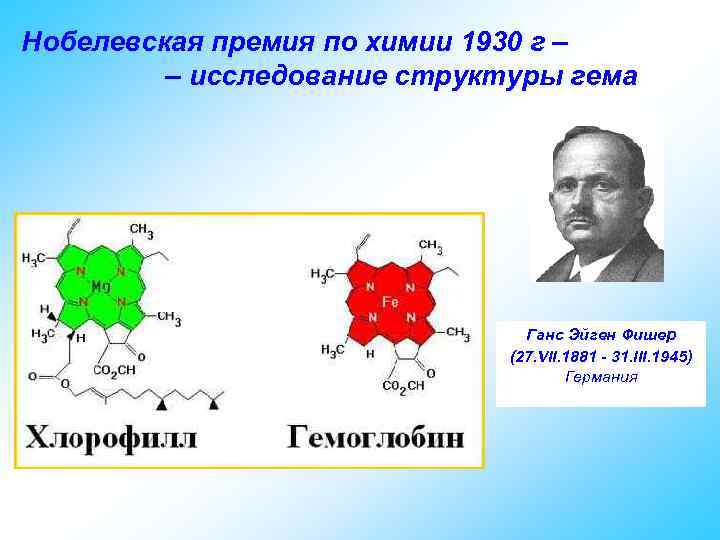
Нобелевская премия по химии 1930 г – – исследование структуры гема Ганс Эйген Фишер (27. VII. 1881 - 31. III. 1945) Германия

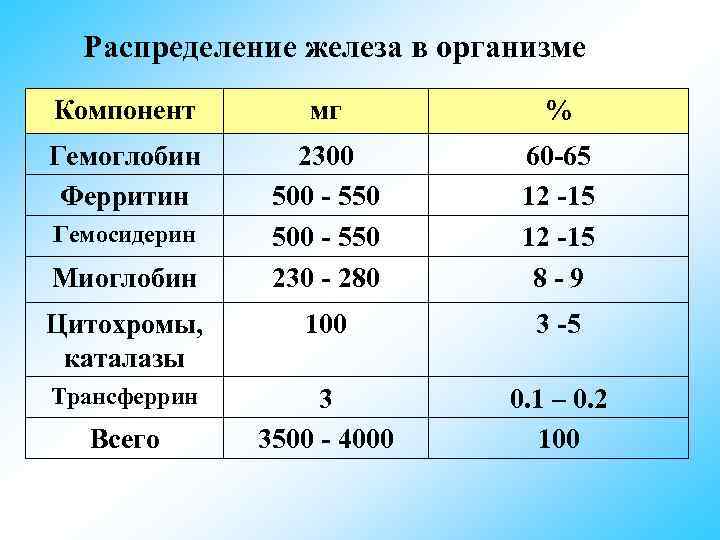
Распределение железа в организме Компонент мг % Гемоглобин 2300 60 -65 Ферритин 500 - 550 12 -15 Гемосидерин 500 - 550 12 -15 Миоглобин 230 - 280 8 -9 Цитохромы, 100 3 -5 каталазы Трансферрин 3 0. 1 – 0. 2 Всего 3500 - 4000 100
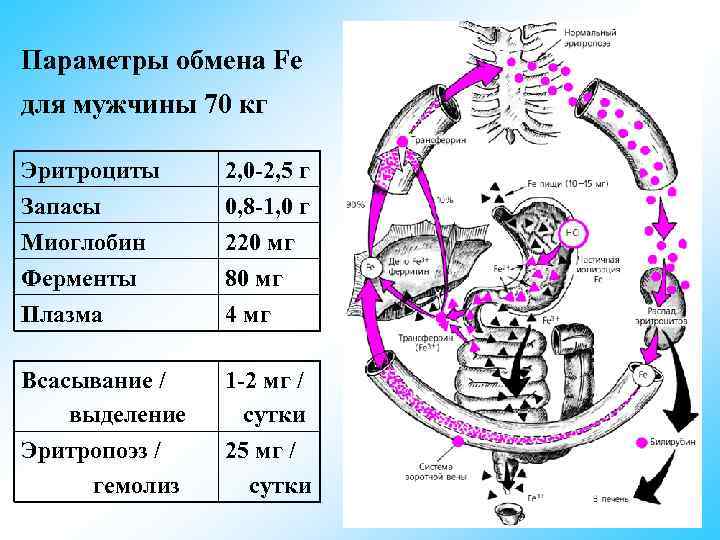
Параметры обмена Fe для мужчины 70 кг Эритроциты 2, 0 -2, 5 г Запасы 0, 8 -1, 0 г Миоглобин 220 мг Ферменты 80 мг Плазма 4 мг Всасывание / 1 -2 мг / выделение сутки Эритропоэз / 25 мг / гемолиз сутки


Суточная потребность в железе § Ежедневная потребность в железе зависит от возраста и пола (мг/день) : § Новорожденные – 0. 5 -1. 5 § Дети – 0. 4 -1. 0 § Мальчики и девочки в пубертатном периоде – 1. 0 – 2. 0 § Мужчины, женщины в период менопаузы – 0. 5 -1. 0 § Женщины детородного возраста – 0. 7 - 2. 0 § Беременные женщины – 2. 0 – 5. 0 § По данным ВОЗ примерно 50% женщин детородного возраста в западных странах страдает дефицитом железа

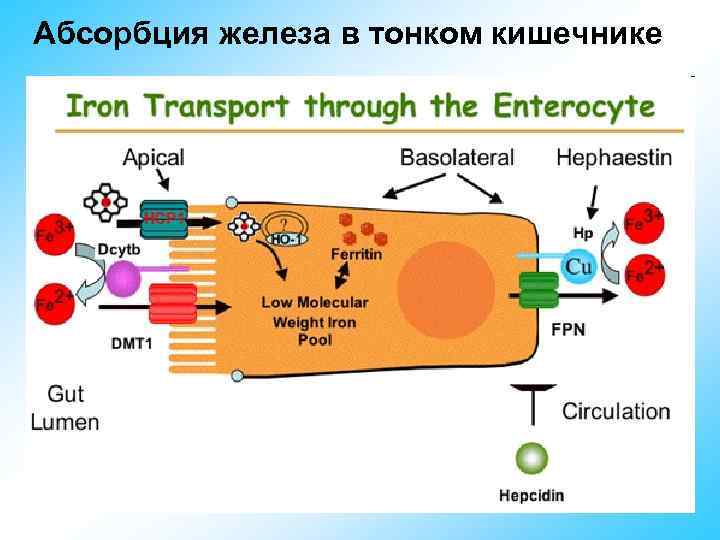
Абсорбция железа в тонком кишечнике
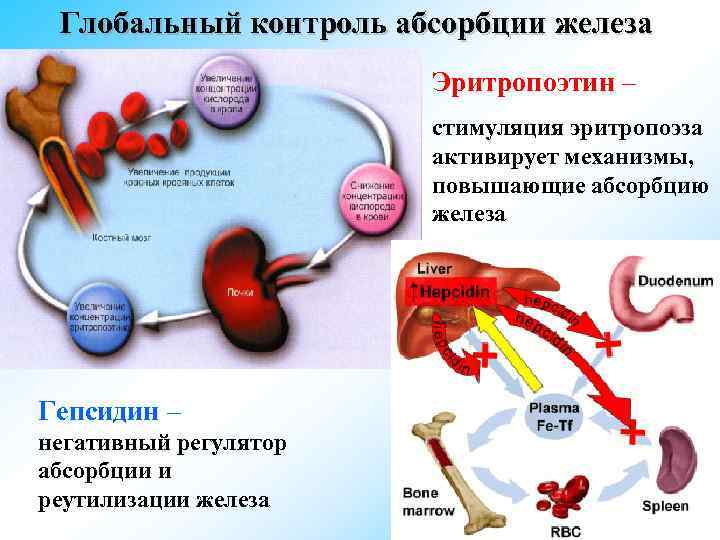
Глобальный контроль абсорбции железа Эритропоэтин – стимуляция эритропоэза активирует механизмы, повышающие абсорбцию железа Гепсидин – негативный регулятор абсорбции и реутилизации железа
Транспорт железа Трансферрин (референтный диапазон - от 2 до 4 г/л) - металл-связывающий транспортный белок (фракция: бета-глобулины белков сыворотки крови) - каждая молекула трансферрина может связать максимум 2 иона железа Fe 3+, связанного с бикарбонатом
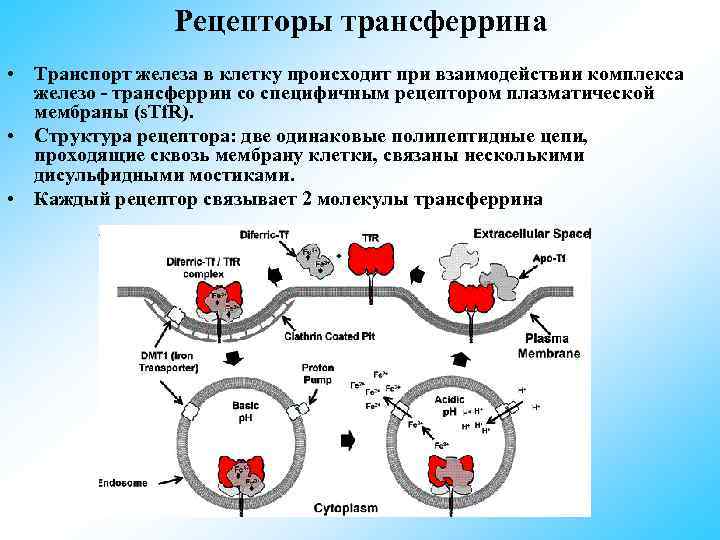
Рецепторы трансферрина • Транспорт железа в клетку происходит при взаимодействии комплекса железо - трансферрин со специфичным рецептором плазматической мембраны (s. Tf. R). • Структура рецептора: две одинаковые полипептидные цепи, проходящие сквозь мембрану клетки, связаны несколькими дисульфидными мостиками. • Каждый рецептор связывает 2 молекулы трансферрина
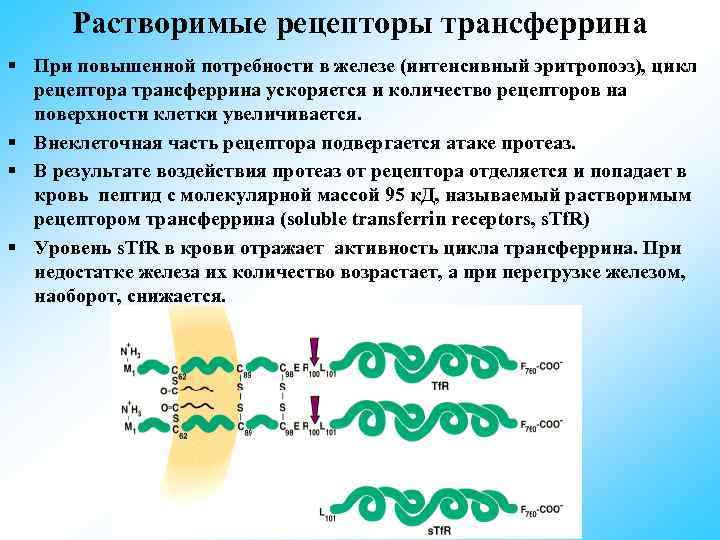
Растворимые рецепторы трансферрина § При повышенной потребности в железе (интенсивный эритропоэз), цикл рецептора трансферрина ускоряется и количество рецепторов на поверхности клетки увеличивается. § Внеклеточная часть рецептора подвергается атаке протеаз. § В результате воздействия протеаз от рецептора отделяется и попадает в кровь пептид с молекулярной массой 95 к. Д, называемый растворимым рецептором трансферрина (soluble transferrin receptors, s. Tf. R) § Уровень s. Tf. R в крови отражает активность цикла трансферрина. При недостатке железа их количество возрастает, а при перегрузке железом, наоборот, снижается.
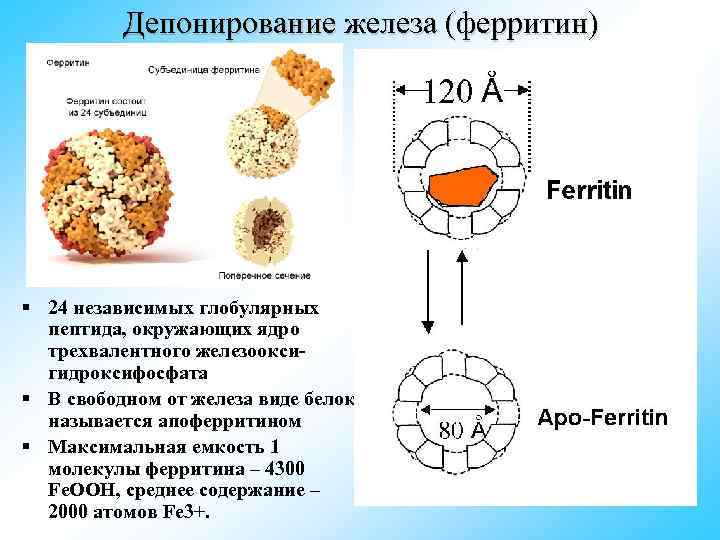
Депонирование железа (ферритин) § 24 независимых глобулярных пептида, окружающих ядро трехвалентного железоокси- гидроксифосфата § В свободном от железа виде белок называется апоферритином § Максимальная емкость 1 молекулы ферритина – 4300 Fe. OOH, среднее содержание – 2000 атомов Fe 3+.
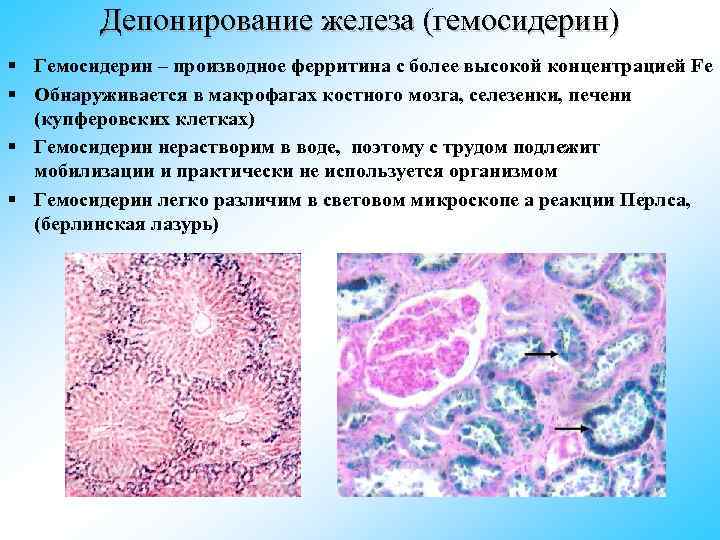
Депонирование железа (гемосидерин) § Гемосидерин – производное ферритина с более высокой концентрацией Fe § Обнаруживается в макрофагах костного мозга, селезенки, печени (купферовских клетках) § Гемосидерин нерастворим в воде, поэтому с трудом подлежит мобилизации и практически не используется организмом § Гемосидерин легко различим в световом микроскопе а реакции Перлса, (берлинская лазурь)
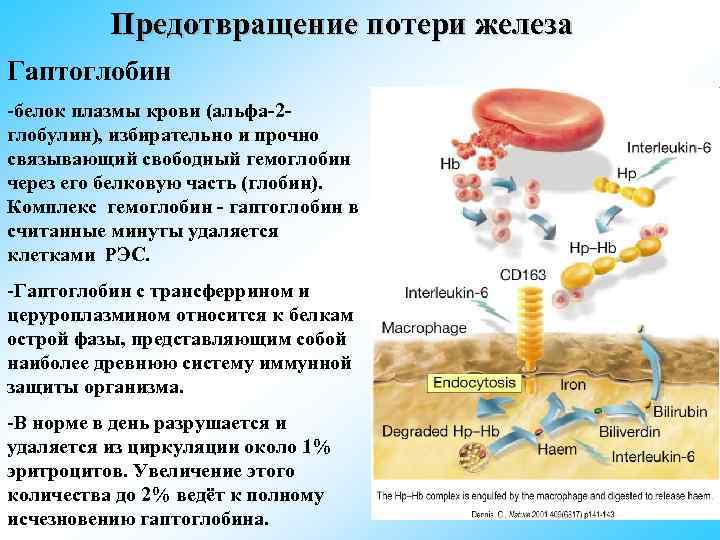
Предотвращение потери железа Гаптоглобин -белок плазмы крови (альфа-2 - глобулин), избирательно и прочно связывающий свободный гемоглобин через его белковую часть (глобин). Комплекс гемоглобин - гаптоглобин в считанные минуты удаляется клетками РЭС. -Гаптоглобин с трансферрином и церуроплазмином относится к белкам острой фазы, представляющим собой наиболее древнюю систему иммунной защиты организма. -В норме в день разрушается и удаляется из циркуляции около 1% эритроцитов. Увеличение этого количества до 2% ведёт к полному исчезновению гаптоглобина.

Нарушение обмена железа § Нарушения обмена железа могут быть связаны как с дефицитом, так и перегрузкой. § Дефицит железа клинически проявляется железодефицитной анемией (ЖДА), перегрузка – гемохроматозом § Железодефицитные состояния (гипосидероз) – одно из наиболее распространенных заболеваний человека от которой страдают около 500 млн. человек в мире. § ЖДА является причиной снижения работоспособности у взрослых, увеличения восприимчивости к вирусным инфекциям, вызывает задержку роста и развития у детей § В связи с этим важное значение имеет своевременная диагностика нарушений обмена железа, железодефицитной анемии, мониторинг в процессе лечения и профилактики дефицита железа у населения

Железодефицитная анемия Причины ЖДА: 1. Хроническая кровопотеря: § Кровопотеря у женщин (меноррагии, метрорагии, роды) § Кровопотери из ЖКТ (язвенная болезнь, язвенный колит, опухоли, полипы, геморрой, глистные инвазии и др. ) 2. Повышенная потребность в железе § Беременность (суммарная потеря железа составляет 1400 мг, для ее восполнения требуется 1. 5 - 2. 0 года). Лактация § Быстрый рост в пубертатном периоде 3. Донорство (сдача 300 мл крови лишает организм 150 мг железа) 4. Нарушение транспорта железа § Наследственная атрансферинемия (отсутствие синтеза трансферрина) § Приобретенная гипотрансферинемия (нарушение белоксинтезирующей функции печени) 5. Нарушение всасывания (хронический энтерит, резекция тонкой кишки, лямблиоз, глистные инвазии)

Железодефицитная анемия Стадии развития ЖДА Истощение запасов (латентный железодефицит) Уменьшение уровня транспортного железа Снижение активности железосодержащих ферментов Нарушение синтеза гемоглобина
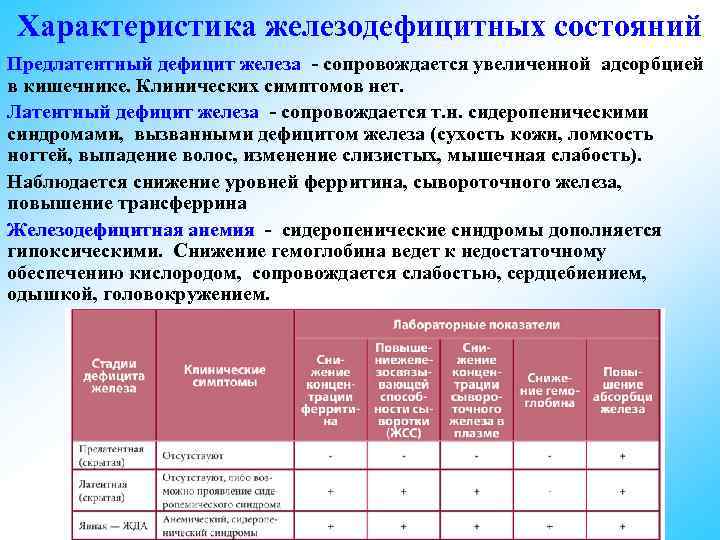
Характеристика железодефицитных состояний Предлатентный дефицит железа - сопровождается увеличенной адсорбцией в кишечнике. Клинических симптомов нет. Латентный дефицит железа - сопровождается т. н. сидеропеническими синдромами, вызванными дефицитом железа (сухость кожи, ломкость ногтей, выпадение волос, изменение слизистых, мышечная слабость). Наблюдается снижение уровней ферритина, сывороточного железа, повышение трансферрина Железодефицитная анемия - сидеропенические снндромы дополняется гипоксическими. Снижение гемоглобина ведет к недостаточному обеспечению кислородом, сопровождается слабостью, сердцебиением, одышкой, головокружением.


Анемия хронических заболеваний (АХЗ) Анемия, возникающая у пациентов с инфекцией, воспалением, неоплазиями и продолжающаяся более 1 - 2 месяца, обозначается как анемия хронических заболеваний (АХЗ) — анемия воспаления, цитокинопосредованная анемия. Характерной чертой этого типа анемии является сочетание пониженного уровня железа сыворотки (гипоферремия) с достаточными его запасами в ретикулоэндотелиальной системе (РЭС).
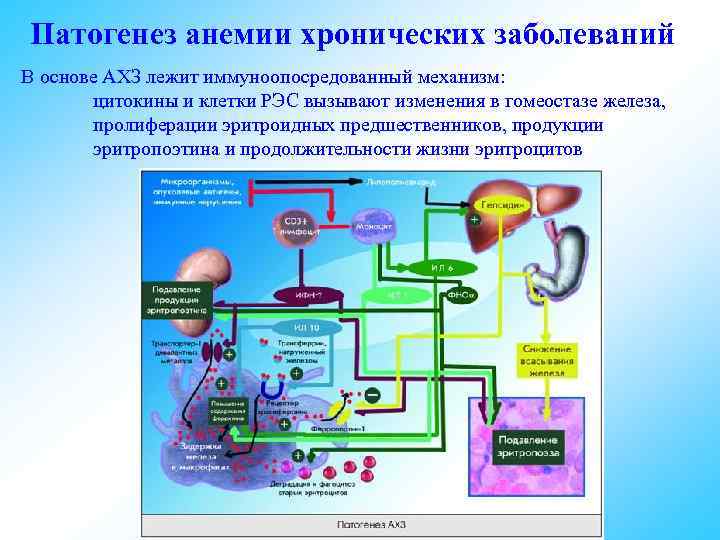
Патогенез анемии хронических заболеваний В основе АХЗ лежит иммуноопосредованный механизм: цитокины и клетки РЭС вызывают изменения в гомеостазе железа, пролиферации эритроидных предшественников, продукции эритропоэтина и продолжительности жизни эритроцитов

Дифференциальная диагностика АХЗ Характерны снижение уровня железа в сыворотке крови, насыщение железом трансферрина ниже нормы. Сывороточный уровень ферритина у пациентов с АХЗ повышен, при сопутствующем дефиците железа (~30%) он снижается, но никогда не бывает таким низким, как при ЖДА. Дефицитом железа у таких больных можно считать уровень ферритина в сыворотке крови < 30 мкг/л, отсутствует дефицит при уровне > 200 мкг/л Важность разграничения АХЗ и ЖДА: некорректная трактовка пациента с АХЗ как имеющего дефицит железа влечет за собой неэффективную терапию железом с риском развития осложнений (перегрузки железом).


Перегрузка железом § Перегрузка железом приводит к физиологическому и функциональному повреждению клеток. § Патогенетические механизмы процесса: процесса 1. Свободные ионы железа обладают прямым токсическим действием на ферменты окислительно-восстановительных систем клеток. 2. Увеличенное отложение железа в форме ферритина и гемосидерина приводит к перегрузке и повреждению лизосом, высвобождающиеся лизосомальные ферменты вызывают повреждение органелл и клеточных структур 3. Электронный перенос на свободных ионах железа( Fe 3+/Fe 2+) приводит к образованию свободных радикалов, которые индуцируют перекисное окисление липидов, чрезмерное увеличение проницаемости клеточных мембран и гибель клеток.
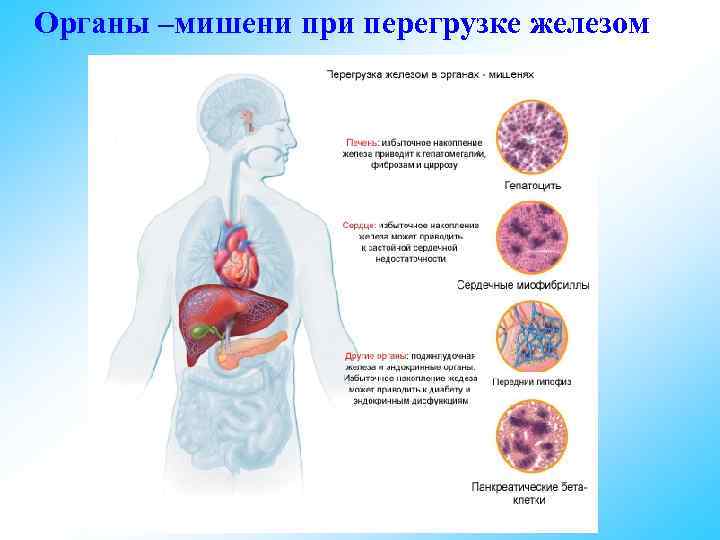
Органы –мишени при перегрузке железом
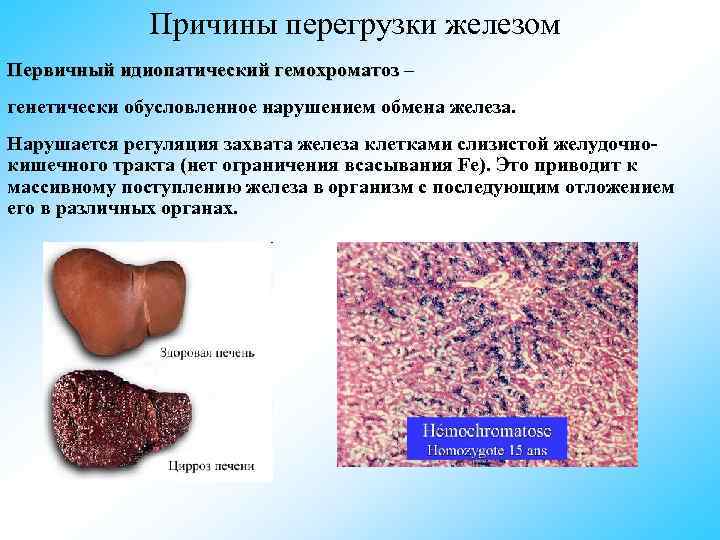
Причины перегрузки железом Первичный идиопатический гемохроматоз – генетически обусловленное нарушением обмена железа. Нарушается регуляция захвата железа клетками слизистой желудочно- кишечного тракта (нет ограничения всасывания Fe). Это приводит к массивному поступлению железа в организм с последующим отложением его в различных органах.
Вторичный приобретенный гемохроматоз возможен при: - гемолитических анемиях, - неэффективном эритропоэзе (сидеробластной и апластической анемиях, талессемии) - малярии, - интоксикациях (свинец, олово) - алкогольном циррозе, - хроническом вирусном гепатите - многократных трансфузиях крови.

Лабораторная оценка метаболизма железа
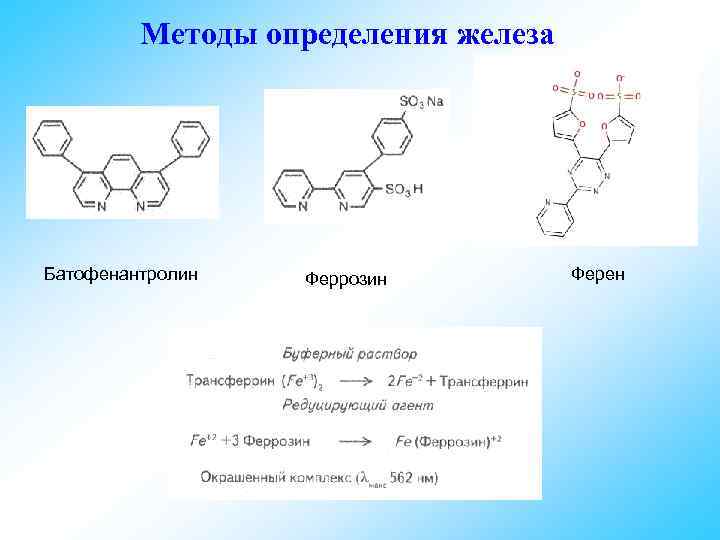
Методы определения железа Батофенантролин Феррозин Ферен

Особенности преаналитического этапа: § Взятие крови проводится спустя 10 -12 дней после отмены препаратов железа § При взятии крови и выполнении анализа необходимо исключить попадание железа извне в реакционную смесь. § В качестве пробы используют сыворотку или гепаринизированную плазму. Проба не должна иметь следов гемолиза

Почему недостаточно определять только сывороточное железо: § Содержание железа в сыворотке крови составляет 0. 2 - 0. 5% всего железа в организме § Выраженное снижение концентрации железа в сыворотке крови может быть отмечено при дефиците железа в организме, но для диагностики латентной анемии недостаточно только его определения § Уровень железа в сыворотке имеет циркадные ритмы: суточные, недельные и сезонные. Различия в содержании железа утром и вечером достигают 0. 5 мг/л. Взятие крови на определение железа должно быть стандартизовано по времени (в утренние часы)

Общая и ненасыщенная железосвязывающая способность НЖСС (ненасыщенная железосвязывающая способность сыворотки) - дополнительное количество Fe, которое может связаться с трансферрином. ОЖСС (общая железосвязывающая способностью сыворотки) - максимальное количество Fe, которое может присоединить трансферрин до полного насыщения. ОЖСС= Сывороточное железо + НЖСС Коэффициент насыщения трансферрина КНТ, % = Железо мкмоль/л / ОЖСС мкмоль/л x 100 КНТ, % = Железо мкмоль/л / Трансферрин г/л x 3, 98 ЖСС - альтернатива прямого измерения трансферрина
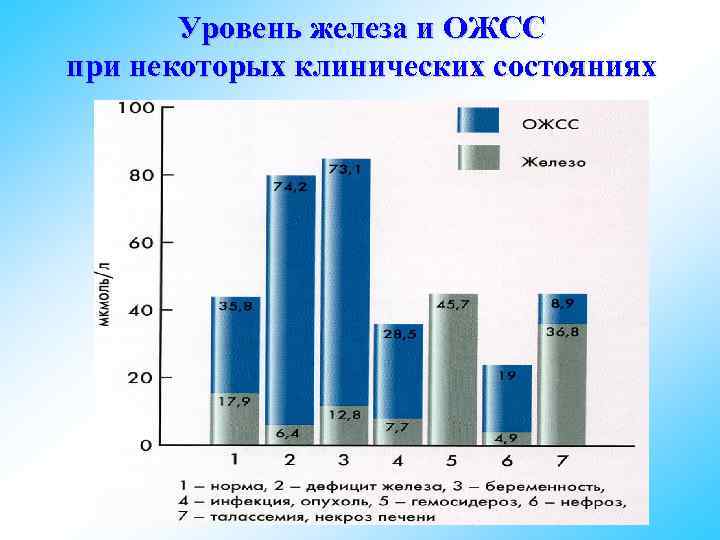
Уровень железа и ОЖСС при некоторых клинических состояниях

Трансферрин и ОЖСС Недостатки метода определения ОЖСС: § Используемый в методике ОЖСС Fe. Cl 3 насыщает не только места связывания трансферрина, но также связывается с преальбумином, альбумином и глобулинами сыворотки. Поэтому измеряемая ОЖСС на 15 -20 % выше, чем истинная связывающая способность трансферрина. § Определение ОЖСС требует много больше крови, чем иммунохимическое определение трансферрина. Это важно в педиатрии и для больных , находящихся на диализе. § Выражение насыщения трансферрина в процентах более показательно для определения скрытого недостатка железа, чем ОЖСС и концентрация железа. § Насыщение трансферрина <15% у взрослых, <10%у детей и <8% у пожилых людей (в сочетании с концентрацией трансферрина <45 мкг/л) указывает на ЖДА § Насыщение трансферрина >55 % указывает на избыток железа в организме.

Трансферрин и ферритин при патологиях • Трансферрин – Возрастает при дефиците железа, беременности, лечении эстрогенами – Уменьшается при реакциях острой фазы (инфекциях, хронических воспалениях, опухолях) • Ферритин – Возрастает при перегрузке железом – Возрастает при реакциях острой фазы (инфекциях, хронических воспалениях, опухолях) – Повышается при гемодиализе – Снижается при железодефицитных состояниях

Витамин B 12 и фолиевая кислота

Витамин B 12 и фолиевая кислота
Клиническая лабораторная диагностика Multum in parvo Многое в малом
Лекция_обмен железа_06_02_2015.ppt