МЕТАБОЛИЗМ ГЛЮКОЗЫ ПРИ ГИПОКСИИ.ppt
- Количество слайдов: 34

МЕТАБОЛИЗМ ГЛЮКОЗЫ ПРИ ГИПОКСИИ

Обмен глюкозы в клетках при гипоксии Дефицит О 2 в клетках, наблюдающийся при различных гипоксических состояниях, ведет к тяжелым нарушениям обмена глюкозы и повреждению органов и тканей в условиях ишемии:

n n в условиях дефицита О 2 в клетках метаболизм углеводов перестраивается с аэробного на анаэробный, и следовательно основным путем становится гликолиз, идущий с накоплением молочной кислоты; для полноценного обеспечения клеток энергией в виде АТФ за счет гликолиза расходуется гораздо больше глюкозы, чем при аэробном окислении. Это сопровождается значительным накоплением лактата, в меньшей степени пирувата и дефицитом глюкозы;

n Дефицит пирувата и глюкозы замедляет активность метаболизма глюкозы, что приводит к резкому снижению в клетках концентрации АТФ

n n n в условиях малого количества АТФ клетки не могут поддерживать мембранный градиент концентрации ионов Na+ , К+ и Са++ , активный транспорт которых сопряжен с гидролизом АТФ. В частности нарушается активное выкачивание ионов Са++ ; рост концентрации ионов Са++ в клетках приводит к активации мембранных фосфолипаз и интенсификации процессов ПОЛ; накопление лизофосфолипидов и окисленных липидов существенно увеличивает проницаемость биологических мембран, вызывает их распад и гибель клеток.

2. ПАТОБИОХИМИЯ САХАРНОГО ДИАБЕТА n n n Эндокринная часть поджелудочной железы – совокупность островков Лангерганса, занимает 1 -2 % от всего объема pancreas. В островках синтезируются и секретируются в кровь: инсулин (ß-клетки) глюкагон (α-клетки) соматостатин (δ-клетки) панкреатический полипептид (РР-клетки) гастрин (G-клетки) у детей. ß-клетки составляют около 20 % от общего количества островковых клеток и вырабатывают 30 -50 единиц инсулина в сутки
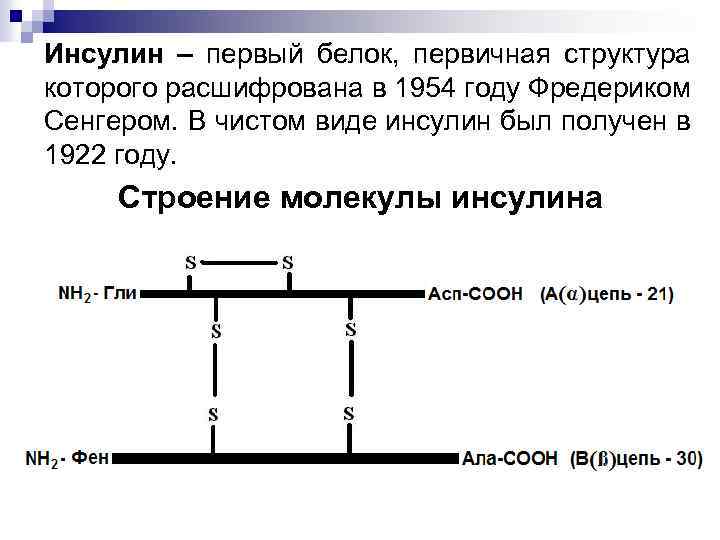
Инсулин – первый белок, первичная структура которого расшифрована в 1954 году Фредериком Сенгером. В чистом виде инсулин был получен в 1922 году. Строение молекулы инсулина

Механизм действия инсулина на ткани-мишени. Главные мишени для инсулина – инсулинзависимые ткани – скелетные мышцы, жировая ткань. Число инсулиновых рецепторов на разных клетках колеблется от 40 до 300 тыс. на клетках органов-мишеней. Инсулиновые рецепторы постоянно синтезируются и распадаются. Время полужизни рецептора составляет 7 -12 часов.

Инсулин стимулирует следующие процессы: n мембранный транспорт глюкозы, т. е. перенос глюкозы через клеточные мембраны в мышцах и жировой ткани с помощью специальных трансмембранных белковпереносчиков глюкозы. В печени инсулин активирует гексокиназу и глюкокиназу, что также ускоряет проникновение глюкозы в клетку; n синтез гликогена и триглицеридов за счет активации гликогенсинтетазы и глюкозо-6 фосфатдегидрогеназы, продуцирующей НАДФН 2, кофермент синтеза ВЖК и глицерофосфата;

n n гликолиз; пентозофосфатный путь распада углеводов; аэробный распад углеводов, в том числе цикл Кребса; синтез АТФ, ДНК и РНК, что проявляется ускоренной пролиферацией клеток

Инсулин подавляет следующие процессы: n n синтез ключевых ферментов глюконеогенеза (фосфоенолпируваткарбоксикиназы и фруктозо- 1, 6 -дифосфатазы); распад гликогена в печени за счет снижения активности фосфорилазы; образование свободной глюкозы из фосфорилированных форм глюкозы (глюкозо 6 -фосфат, глюкозо-1 -фосфат); распад липидов за счет снижения активности триглицеридлипазы.

Комплексное воздействие инсулина на ткани организма Влияние на жировую ткань: n n n Увеличивает поступление глюкозы; Повышает синтез жирных кислот и глицерофосфатов; Увеличивает депонирование триглицеридов; Активирует липопротеинлипазу; Ингибирует гормоночувствительную липазу; Увеличивает поглощение ионов калия.

Влияние на мышечную ткань: n Повышает поступление глюкозы; n Увеличивает синтез гликогена; n Повышает поглощение аминокислот; n Увеличивает белковый синтез в рибосомах n Снижает катаболизм белков; n Повышает поглощение кетоновых тел.

Влияние на печень: n синтеза белков; n синтеза жиров; n кетогенез; n выброс глюкозы вследствие уменьшения глюконеогенеза.

При недостаточной секреции инсулина или его неадекватном действии на ткани-мишени развивается сахарный диабет. В 1981 г. ВОЗ определила сахарный диабет как синдром хронической гипергликемии, развивающийся вследствие абсолютного или относительного дефицита инсулина.

Молекулярные дефекты, приводящие к развитию сахарного диабета. 1) нарушение превращения проинсулина в инсулин (Связано с мутацией в участках соединения α- и β-цепей с С-пептидом в молекуле проинсулина). В крови много проинсулина. 2) дефект молекулярной структуры инсулина (замена фен на лей в бета-цепи, что снижает активность инсулина на порядок) 3) дефект рецепторов инсулина, нарушается связывание инсулина с мембраной клетокмишеней

4) дефект молекулярной структуры инсулина (замена фен на лей в бета-цепи, что снижает активность инсулина на порядок) 5) дефект рецепторов инсулина, нарушающий связывание инсулина с мембраной клетокмишеней. 6) дефект сопряжения между инсулинрецепторным комплексом и вторым звеном передачи сигнала в клетку при нормальной продукции инсулина и обычном количестве инсулиновых рецепторов в клетках-мишенях. 7) чрезмерная активность инсулиназы

Биохимические изменения при сахарном диабете: n n Гипергликемия вызвана нарушением транспорта глюкозы в клетки, усиленным распадом гликогена, активацией глюконеогенеза. Глюкозурия. Нарушается способность почечных канальцев к реабсорбции глюкозы.

n Полиурия и полидипсия. С глюкозой выделяется много воды, что приводит к чувству жажды и голода (полифагия). n Кетонемия и кетонурия связаны с более интенсивным использованием в качестве источника энергии липидов. Ацетил-Ко. А, образующийся при распаде жиров не сгорает в ЦТК, часть его идет на синтез кетоновых тел.

n Метаболический кетоацидоз И ИИИИИ обусловлен накоплением кислых продуктов, в первую очередь кетоновых тел. n Отрицательный азотистый баланс связан с усиленным использованием гликогенных аминокислот в процессе глюконеогенеза. Это приводит, с одной стороны, к потере аминокислот, а с другой – к росту синтеза мочевины.

n n Гиперосмолярная дегидратация возникает в связи с выделением с мочой больших количеств растворимых (глюкозы, кетоновых тел, азотсодержащих соединений, ионов Na+). Гиперлипидемия.

Острые нарушения обмена веществ при диабете: 1. 2. 3. 4. 5. Диабетический кетоацидоз; Диабетический лактоацидоз; Гиперосмолярная кома; Мозговая кома; инсулиновая гипогликемия.

1. Диабетический кетоацидоз В основе нарушения лежат следующие факторы: n гипергликемия; n глюкозурия; n метаболический ацидоз; n электролитные нарушения.

2. Диабетический лактоацидоз Способствуют сопутствующие заболевания, протекающие с гипоксией и нарушением кислотноосновного состояния. Дефицит инсулина, ацидоз, гипоксия тормозят аэробное окисление глюкозы, что приводит к активации гликолиза. Развитию лактоацидоза может способствовать применение бигуанидов в терапии диабета.

3. Гиперосмолярная кома связана с нарушением деятельности нервной системы вследствие гиперосмолярности крови и дегидратацией нервных клеток.

4. Мозговая (первично-церебральная) кома Развивается у детей при лечении гипергликемической комы инсулином. При этом быстрое снижение гликемии сдвигает равновесие между осмоляльностью плазмы крови и мозга, возникший градиент осмоляльности способствует поступлению воды в мозг, что приводит к отеку. 5. Инсулиновая гипогликемия.
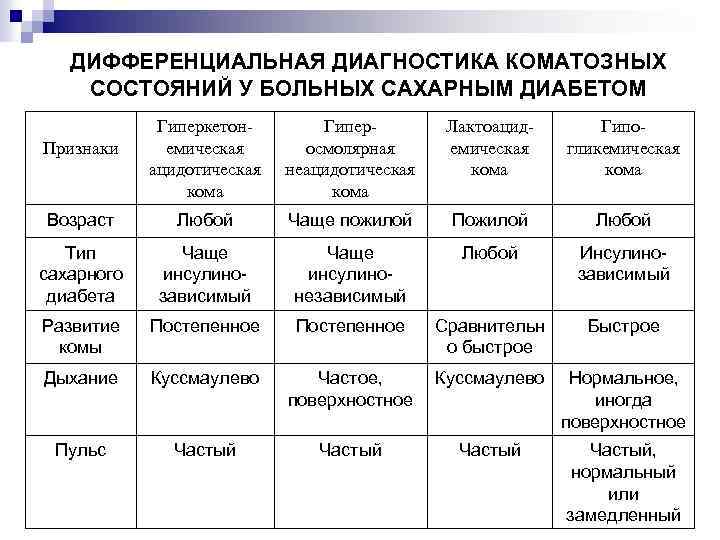
ДИФФЕРЕНЦИАЛЬНАЯ ДИАГНОСТИКА КОМАТОЗНЫХ СОСТОЯНИЙ У БОЛЬНЫХ САХАРНЫМ ДИАБЕТОМ Гиперкетонемическая ацидотическая кома Гиперосмолярная неацидотическая кома Лактоацидемическая кома Гипогликемическая кома Возраст Любой Чаще пожилой Пожилой Любой Тип сахарного диабета Чаще инсулинозависимый Чаще инсулинонезависимый Любой Инсулинозависимый Развитие комы Постепенное Сравнительн о быстрое Быстрое Дыхание Куссмаулево Частое, поверхностное Куссмаулево Нормальное, иногда поверхностное Пульс Частый, нормальный или замедленный Признаки
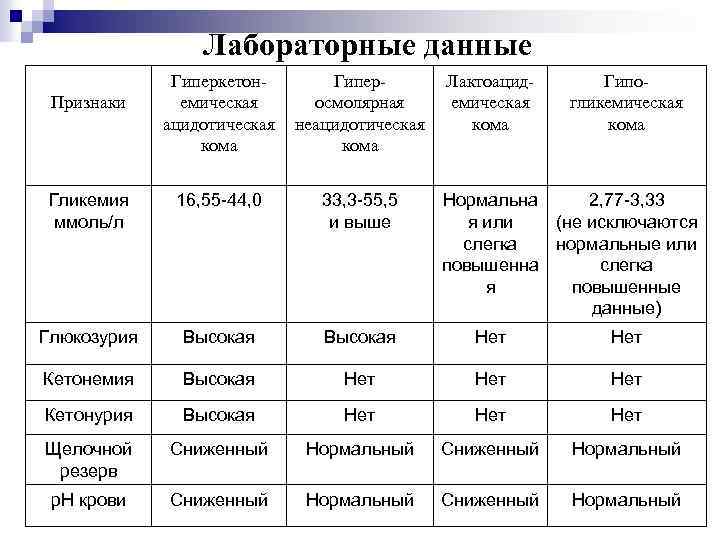
Лабораторные данные Гиперкетонемическая ацидотическая кома Гиперосмолярная неацидотическая кома Гликемия ммоль/л 16, 55 -44, 0 33, 3 -55, 5 и выше Глюкозурия Высокая Нет Кетонемия Высокая Нет Нет Кетонурия Высокая Нет Нет Щелочной резерв Сниженный Нормальный р. Н крови Сниженный Нормальный Признаки Лактоацидемическая кома Гипогликемическая кома Нормальна 2, 77 -3, 33 я или (не исключаются слегка нормальные или повышенна слегка я повышенные данные)

Поздние осложнения сахарного диабета Являются следствием длительной гипергликемии и гликозилирования белков крови. Основные патогенетические процессы при хронических осложнениях сахарного диабета развиваются в кровеносных сосудах, в первую очередь поражаются коронарные артерии, сосуды мозга и нижних конечностей, почек, сетчатки глаза.

Механизмы повреждения: усиленное гликозилирование белков в плазме крови приводит к депонированию их в стенках сосудов, что способствует агрегации тромбоцитов, миграции и адгезии моноцитов и макрофагов; n активируется тирозиновое фосфорилирование ряда белков клетки, в результате чего происходят гиперплазия и гипертрофия клеток сосудистой стенки и крови. n

Степень гликозилирования белков зависит от скорости их обновления. В медленно обновляющихся белках происходят большие изменения, чем в быстрообновляемых. Так, основной причиной диабетических микроангиопатий, проявляющихся снижением эластичности сосудов, является гликозилирование белков межклеточного матрикса – коллагена и эластина.

Тест на толерантность к глюкозе проводят с целью выяснения способности регулировать содержание глюкозы в крови

Последовательность проведения: 1) Первая проба крови берется натощак после ночного голодания 2) Больному дают выпить раствор глюкозы из расчета 1 г глюкозы на кг массы тела в 200 мл теплой воды (сахарная нагрузка). 3) Определение содержания глюкозы в крови через 60 и 120 мин. Диагноз Норма Сахарный диабет Содержание глюкозы в крови (моль/л) Натощак Через 60 Через 120 мин Ниже 5, 55 Больше 6 Ниже 8, 88 Больше 10 Ниже 6, 66 Больше 8
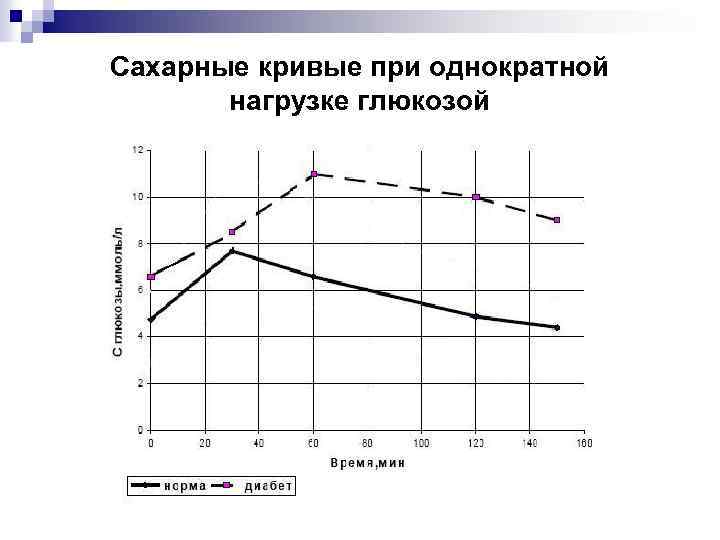
Сахарные кривые при однократной нагрузке глюкозой
МЕТАБОЛИЗМ ГЛЮКОЗЫ ПРИ ГИПОКСИИ.ppt