75_Termodinamika.pptx
- Количество слайдов: 18

 Мета: повторення основних понять, законів і формул ТЕРМОДИНАМІКИ відповідно до кодифікатора ЄДІ. Елементи змісту, що перевіряються на ЄДІ 2010 : 1. 2. 3. 4. 5. 6. 7. 8. 9. Внутрішня енергія Тепловий баланс Теплопередача. Види теплопередачі Кількість теплоти. Питома теплоємність речовини Перший закон термодинаміки Другий закон термодинаміки ККД теплової машини Принципи дії теплових машин Теплові двигуни та охорона навколишнього середовища
Мета: повторення основних понять, законів і формул ТЕРМОДИНАМІКИ відповідно до кодифікатора ЄДІ. Елементи змісту, що перевіряються на ЄДІ 2010 : 1. 2. 3. 4. 5. 6. 7. 8. 9. Внутрішня енергія Тепловий баланс Теплопередача. Види теплопередачі Кількість теплоти. Питома теплоємність речовини Перший закон термодинаміки Другий закон термодинаміки ККД теплової машини Принципи дії теплових машин Теплові двигуни та охорона навколишнього середовища
 Термодинаміка. Основні поняття. Термодинаміка - це наука про теплові явища. Термодинаміка розглядає ізольовані системи тіл, що перебувають у стані термодинамічної рівноваги - в таких системах припинилися всі спостережувані макроскопічні процеси. Основна властивість термодинамічно рівноважної системи - вирівнювання температури всіх її частин; Термодинамічний процес - перехід з одного в інше рівноважний стан. Процеси, що складаються з послідовності рівноважних станів, називаються квазистатическими.
Термодинаміка. Основні поняття. Термодинаміка - це наука про теплові явища. Термодинаміка розглядає ізольовані системи тіл, що перебувають у стані термодинамічної рівноваги - в таких системах припинилися всі спостережувані макроскопічні процеси. Основна властивість термодинамічно рівноважної системи - вирівнювання температури всіх її частин; Термодинамічний процес - перехід з одного в інше рівноважний стан. Процеси, що складаються з послідовності рівноважних станів, називаються квазистатическими.
 Внутрішня енергія речовини складається з кінетичної енергії всіх атомів і молекул і потенційної енергії їх взаємодії один з одним; Внутрішня енергія U тіла однозначно визначається параметрами макроскопическими, що характеризують стан тіла; Внутрішня енергія U тіла залежить поряд з температурою T також і від обсягу V; Внутрішня енергія є функцією стану; U = U(T, V) Внутрішня енергія тіла може змінюватися, якщо діють на нього зовнішні сили здійснюють роботу (позитивну або негативну). Враховуючи рівняння i – ступінь стану ідеального газу свободи
Внутрішня енергія речовини складається з кінетичної енергії всіх атомів і молекул і потенційної енергії їх взаємодії один з одним; Внутрішня енергія U тіла однозначно визначається параметрами макроскопическими, що характеризують стан тіла; Внутрішня енергія U тіла залежить поряд з температурою T також і від обсягу V; Внутрішня енергія є функцією стану; U = U(T, V) Внутрішня енергія тіла може змінюватися, якщо діють на нього зовнішні сили здійснюють роботу (позитивну або негативну). Враховуючи рівняння i – ступінь стану ідеального газу свободи
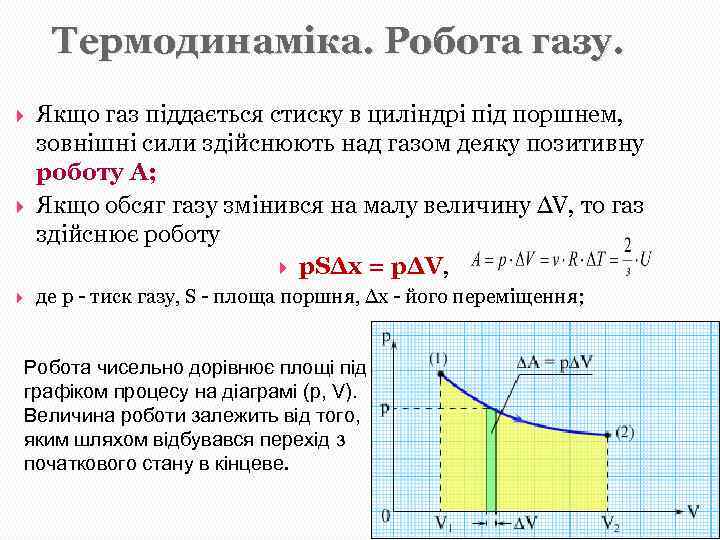 Термодинаміка. Робота газу. Якщо газ піддається стиску в циліндрі під поршнем, зовнішні сили здійснюють над газом деяку позитивну роботу A; Якщо обсяг газу змінився на малу величину ΔV, то газ здійснює роботу p. SΔx = pΔV, де p - тиск газу, S - площа поршня, Δx - його переміщення; Робота чисельно дорівнює площі під графіком процесу на діаграмі (p, V). Величина роботи залежить від того, яким шляхом відбувався перехід з початкового стану в кінцеве.
Термодинаміка. Робота газу. Якщо газ піддається стиску в циліндрі під поршнем, зовнішні сили здійснюють над газом деяку позитивну роботу A; Якщо обсяг газу змінився на малу величину ΔV, то газ здійснює роботу p. SΔx = pΔV, де p - тиск газу, S - площа поршня, Δx - його переміщення; Робота чисельно дорівнює площі під графіком процесу на діаграмі (p, V). Величина роботи залежить від того, яким шляхом відбувався перехід з початкового стану в кінцеве.
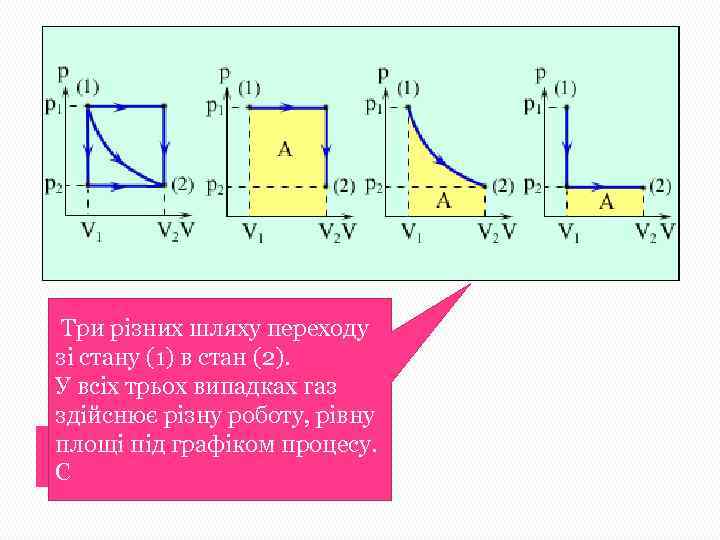 Три різних шляху переходу зі стану (1) в стан (2). У всіх трьох випадках газ здійснює різну роботу, рівну площі під графіком процесу. С
Три різних шляху переходу зі стану (1) в стан (2). У всіх трьох випадках газ здійснює різну роботу, рівну площі під графіком процесу. С
 Тепловий баланс При тепловому контакті дві системи приходять в стан теплового рівноваги. Дві системи перебувають у стані теплового балансу, якщо при контакті через диатермическую перегородку параметри стану обох систем не змінюються;
Тепловий баланс При тепловому контакті дві системи приходять в стан теплового рівноваги. Дві системи перебувають у стані теплового балансу, якщо при контакті через диатермическую перегородку параметри стану обох систем не змінюються;
 Теплопередача. Види теплопередачі
Теплопередача. Види теплопередачі
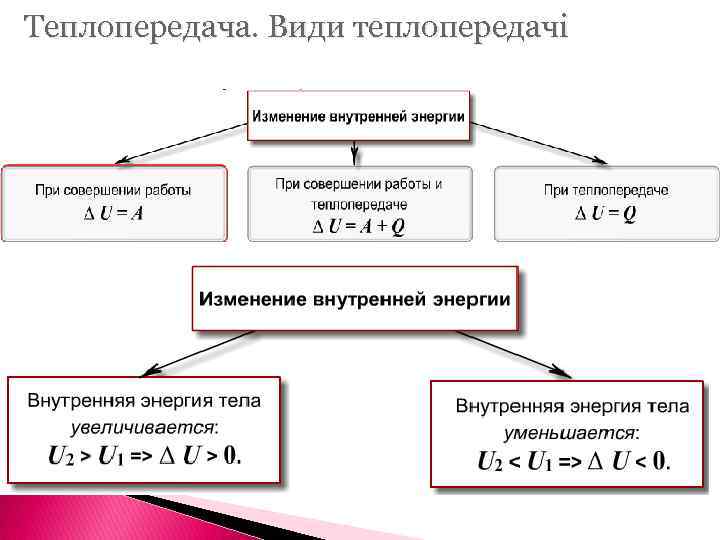
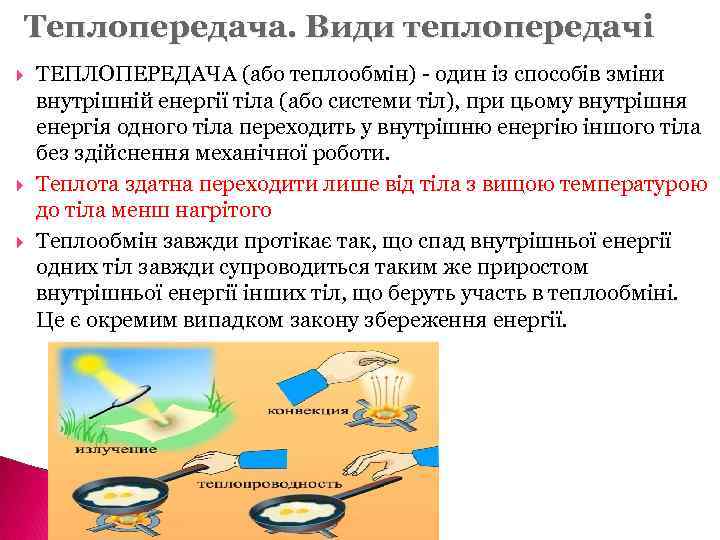 Теплопередача. Види теплопередачі ТЕПЛОПЕРЕДАЧА (або теплообмін) - один із способів зміни внутрішній енергії тіла (або системи тіл), при цьому внутрішня енергія одного тіла переходить у внутрішню енергію іншого тіла без здійснення механічної роботи. Теплота здатна переходити лише від тіла з вищою температурою до тіла менш нагрітого Теплообмін завжди протікає так, що спад внутрішньої енергії одних тіл завжди супроводиться таким же приростом внутрішньої енергії інших тіл, що беруть участь в теплообміні. Це є окремим випадком закону збереження енергії.
Теплопередача. Види теплопередачі ТЕПЛОПЕРЕДАЧА (або теплообмін) - один із способів зміни внутрішній енергії тіла (або системи тіл), при цьому внутрішня енергія одного тіла переходить у внутрішню енергію іншого тіла без здійснення механічної роботи. Теплота здатна переходити лише від тіла з вищою температурою до тіла менш нагрітого Теплообмін завжди протікає так, що спад внутрішньої енергії одних тіл завжди супроводиться таким же приростом внутрішньої енергії інших тіл, що беруть участь в теплообміні. Це є окремим випадком закону збереження енергії.
 Види теплопередачі. Теплопровідність - перенесення енергії від більш нагрітих ділянок тіла до менш нагрітим за рахунок теплового руху і взаємодії мікрочасток (атомів, молекул, іонів і тому подібне), який приводить до вирівнювання температури тіла. Не супроводиться перенесенням речовини! Цей вигляд передачі внутрішньої енергії характерний як для твердих речовин, так і для рідин і газів. Теплопровідність різних речовин різна. Метали володіють найвищою теплопровідністю, причому в різних металів теплопровідність відрізняється. Рідини володіють меншою теплопровідністю, чим тверді тіла, а гази меншою, ніж рідини.
Види теплопередачі. Теплопровідність - перенесення енергії від більш нагрітих ділянок тіла до менш нагрітим за рахунок теплового руху і взаємодії мікрочасток (атомів, молекул, іонів і тому подібне), який приводить до вирівнювання температури тіла. Не супроводиться перенесенням речовини! Цей вигляд передачі внутрішньої енергії характерний як для твердих речовин, так і для рідин і газів. Теплопровідність різних речовин різна. Метали володіють найвищою теплопровідністю, причому в різних металів теплопровідність відрізняється. Рідини володіють меншою теплопровідністю, чим тверді тіла, а гази меншою, ніж рідини.
 Види теплопередачі. Конвекція - вигляд теплопередачі, при якому енергія передається потоками (струменями) речовини. Характерна для рідин і газів.
Види теплопередачі. Конвекція - вигляд теплопередачі, при якому енергія передається потоками (струменями) речовини. Характерна для рідин і газів.
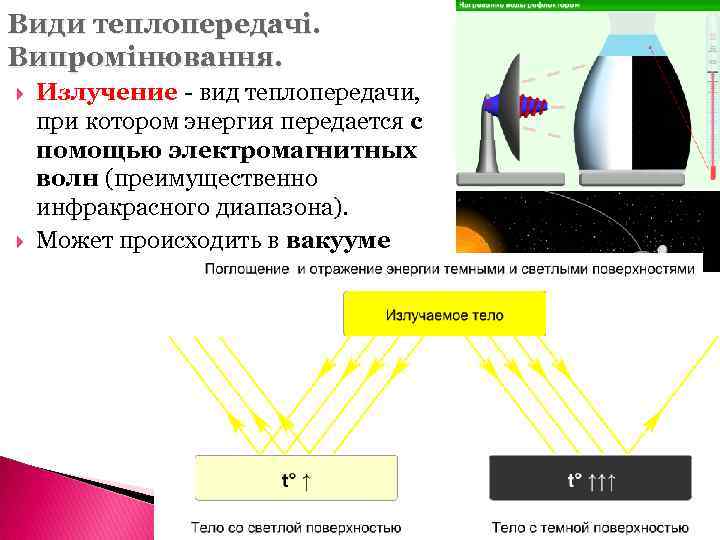 Види теплопередачі. Випромінювання. Излучение - вид теплопередачи, при котором энергия передается с помощью электромагнитных волн (преимущественно инфракрасного диапазона). Может происходить в вакууме
Види теплопередачі. Випромінювання. Излучение - вид теплопередачи, при котором энергия передается с помощью электромагнитных волн (преимущественно инфракрасного диапазона). Может происходить в вакууме
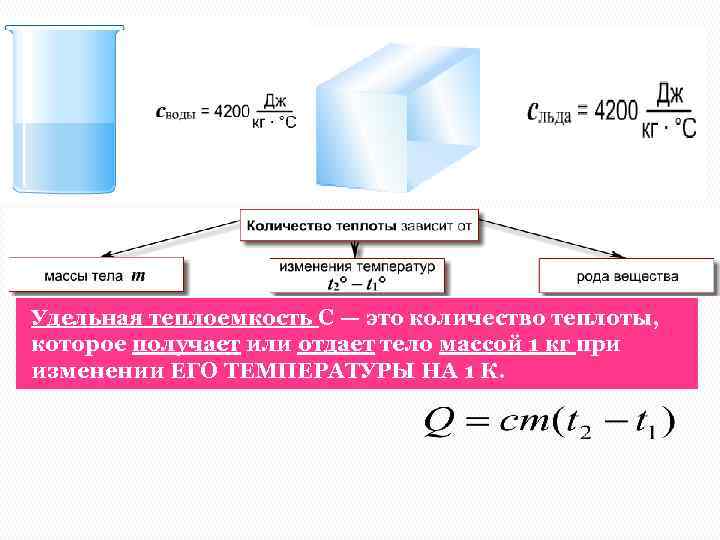 Количество теплоты. Удельная теплоемкость вещества Энергия, переносимая от одной системы к другой только за счет разницы в температурах этих систем, называется количеством теплоты Удельная теплоемкость С — это количество теплоты, которое получает или отдает тело массой 1 кг при изменении ЕГО ТЕМПЕРАТУРЫ НА 1 К.
Количество теплоты. Удельная теплоемкость вещества Энергия, переносимая от одной системы к другой только за счет разницы в температурах этих систем, называется количеством теплоты Удельная теплоемкость С — это количество теплоты, которое получает или отдает тело массой 1 кг при изменении ЕГО ТЕМПЕРАТУРЫ НА 1 К.
 Кількість теплоти. Питома теплоємність речовини. Енергія, що переноситься від однієї системи до іншої тільки за рахунок різниці в температурах цих систем, називається кількістю теплоти. Количество теплоты, необходимое для . нагревания (выделившаяся при остывании) тела Количество теплоты, необходимое для плавления (выделившаяся при кристаллизации) тела Количество теплоты, необходимое для парообразования (выделившаяся при конденсации) тела Испарение Плавление Нагревание Конденсация Кристаллизация Остывание
Кількість теплоти. Питома теплоємність речовини. Енергія, що переноситься від однієї системи до іншої тільки за рахунок різниці в температурах цих систем, називається кількістю теплоти. Количество теплоты, необходимое для . нагревания (выделившаяся при остывании) тела Количество теплоты, необходимое для плавления (выделившаяся при кристаллизации) тела Количество теплоты, необходимое для парообразования (выделившаяся при конденсации) тела Испарение Плавление Нагревание Конденсация Кристаллизация Остывание
 Первый закон термодинамики Обмен энергией между термодинамической системой и окружающими телами в результате теплообмена и совершаемой работы Q = ΔU + A I закон термодинамики: Количество теплоты, полученное системой, идет на изменение ее внутренней энергии и совершение работы над внешними телами Важным следствием первого закона термодинамики является утверждение о невозможности создания машины, способной совершать полезную работу без потребления энергии извне и без каких-либо изменений внутри самой машины. Такая гипотетическая машина получила название вечного двигателя (perpetuum mobile) первого рода.
Первый закон термодинамики Обмен энергией между термодинамической системой и окружающими телами в результате теплообмена и совершаемой работы Q = ΔU + A I закон термодинамики: Количество теплоты, полученное системой, идет на изменение ее внутренней энергии и совершение работы над внешними телами Важным следствием первого закона термодинамики является утверждение о невозможности создания машины, способной совершать полезную работу без потребления энергии извне и без каких-либо изменений внутри самой машины. Такая гипотетическая машина получила название вечного двигателя (perpetuum mobile) первого рода.
 Первый закон термодинамики I закон термодинамики: Количество теплоты, полученное системой, идет на изменение ее внутренней энергии и совершение работы над внешними телами В В В изохорном изобарном изотермическом адиабатическом процессе Q = 0 (V = const) (p = const) температура газа не изменяется, газ работы не следовательно, не совершает, изменяется и внутренняя энергия A = 0 газа, Q = ΔU = 0 A = –ΔU Q = ΔU + pΔV Q = A В Адиабатический процесс - процесс, протекающий в отсутствие теплообмена с окружающими телами
Первый закон термодинамики I закон термодинамики: Количество теплоты, полученное системой, идет на изменение ее внутренней энергии и совершение работы над внешними телами В В В изохорном изобарном изотермическом адиабатическом процессе Q = 0 (V = const) (p = const) температура газа не изменяется, газ работы не следовательно, не совершает, изменяется и внутренняя энергия A = 0 газа, Q = ΔU = 0 A = –ΔU Q = ΔU + pΔV Q = A В Адиабатический процесс - процесс, протекающий в отсутствие теплообмена с окружающими телами
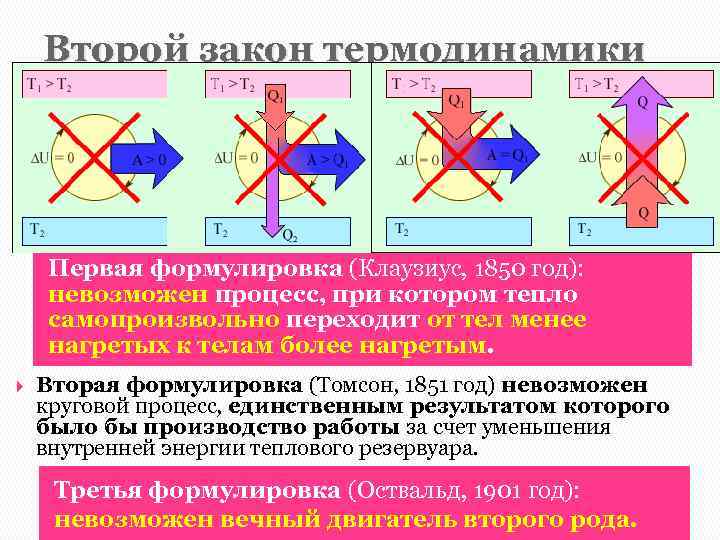 Второй закон термодинамики Многие тепловые процессы могут протекать только в одном направлении. Такие процессы называются необратимыми. Обратимыми процессами называют процессы перехода системы из одного равновесного состояния в другое, которые можно провести в обратном направлении через ту же последовательность промежуточных равновесных состояний. Первая формулировка (Клаузиус, 1850 год): невозможен процесс, при котором тепло самопроизвольно переходит от тел менее нагретых к телам более нагретым. Вторая формулировка (Томсон, 1851 год) невозможен круговой процесс, единственным результатом которого было бы производство работы за счет уменьшения внутренней энергии теплового резервуара. Третья формулировка (Оствальд, 1901 год): невозможен вечный двигатель второго рода.
Второй закон термодинамики Многие тепловые процессы могут протекать только в одном направлении. Такие процессы называются необратимыми. Обратимыми процессами называют процессы перехода системы из одного равновесного состояния в другое, которые можно провести в обратном направлении через ту же последовательность промежуточных равновесных состояний. Первая формулировка (Клаузиус, 1850 год): невозможен процесс, при котором тепло самопроизвольно переходит от тел менее нагретых к телам более нагретым. Вторая формулировка (Томсон, 1851 год) невозможен круговой процесс, единственным результатом которого было бы производство работы за счет уменьшения внутренней энергии теплового резервуара. Третья формулировка (Оствальд, 1901 год): невозможен вечный двигатель второго рода.
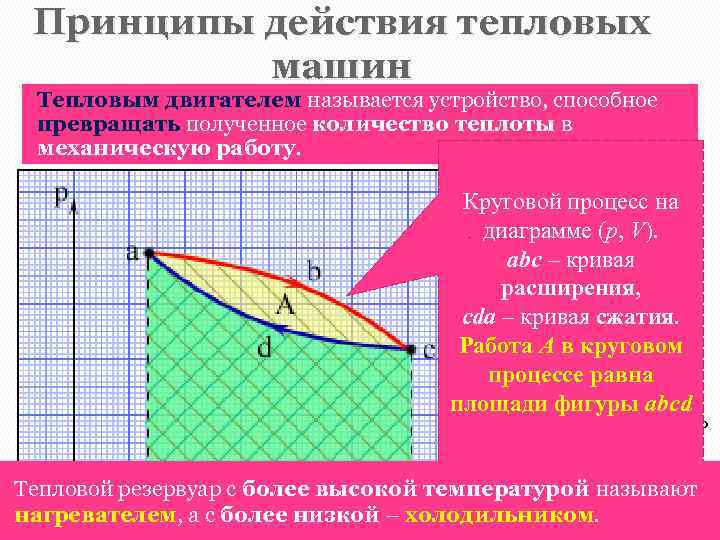 Принципы действия тепловых машин Тепловым двигателем называется устройство, способное превращать полученное количество теплоты в механическую работу. Механическая работа в тепловых двигателях производится Круговой процесс на в процессе расширения некоторого вещества, которое . диаграмме (p, V). называется рабочим телом. abc – кривая Реально существующие тепловые двигатели (паровые расширения, машины, двигатели внутреннего сгорания и т. д. ) работают cda – кривая сжатия. циклически. Работа A в круговом Процесс теплопередачи и преобразования полученного процессе равна количества теплоты в работу периодически площади фигуры abcd повторяется. Для этого рабочее тело должно совершать круговой процесс или термодинамический цикл, при котором периодически восстанавливается Тепловой резервуар с более высокой температурой называют исходное состояние. нагревателем, а с более низкой – холодильником.
Принципы действия тепловых машин Тепловым двигателем называется устройство, способное превращать полученное количество теплоты в механическую работу. Механическая работа в тепловых двигателях производится Круговой процесс на в процессе расширения некоторого вещества, которое . диаграмме (p, V). называется рабочим телом. abc – кривая Реально существующие тепловые двигатели (паровые расширения, машины, двигатели внутреннего сгорания и т. д. ) работают cda – кривая сжатия. циклически. Работа A в круговом Процесс теплопередачи и преобразования полученного процессе равна количества теплоты в работу периодически площади фигуры abcd повторяется. Для этого рабочее тело должно совершать круговой процесс или термодинамический цикл, при котором периодически восстанавливается Тепловой резервуар с более высокой температурой называют исходное состояние. нагревателем, а с более низкой – холодильником.


