40e9ead410e24e61631e4dbe15999ddc.ppt
- Количество слайдов: 64

Мембранный транспорт
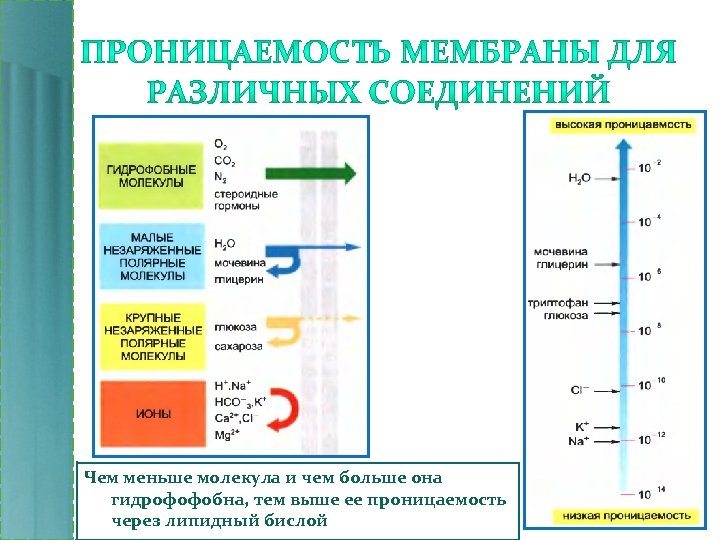
Чем меньше молекула и чем больше она гидрофофобна, тем выше ее проницаемость через липидный бислой

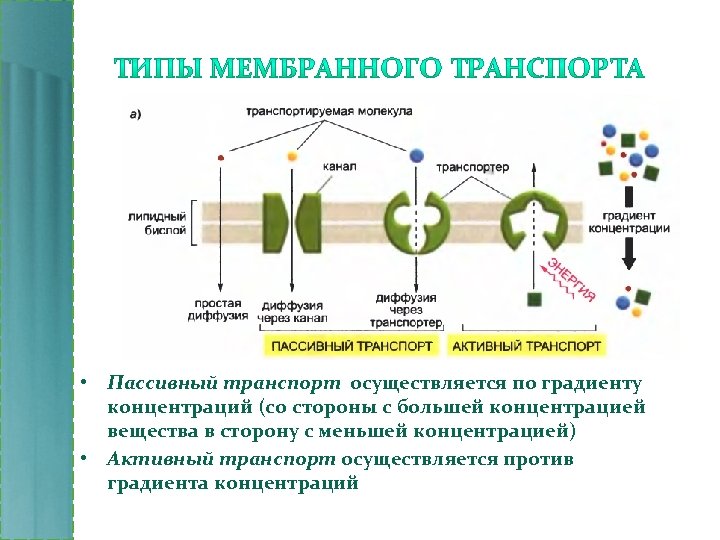
• Пассивный транспорт осуществляется по градиенту концентраций (со стороны с большей концентрацией вещества в сторону с меньшей концентрацией) • Активный транспорт осуществляется против градиента концентраций

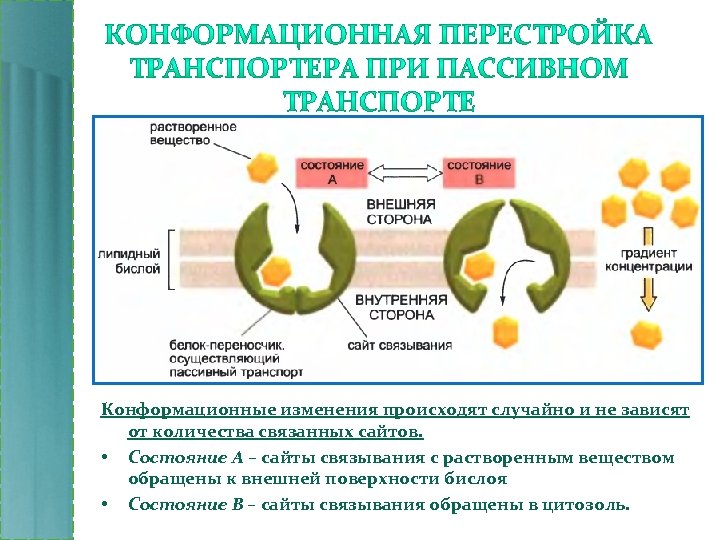
Конформационные изменения происходят случайно и не зависят от количества связанных сайтов. • Состояние А – сайты связывания с растворенным веществом обращены к внешней поверхности бислоя • Состояние В – сайты связывания обращены в цитозоль.
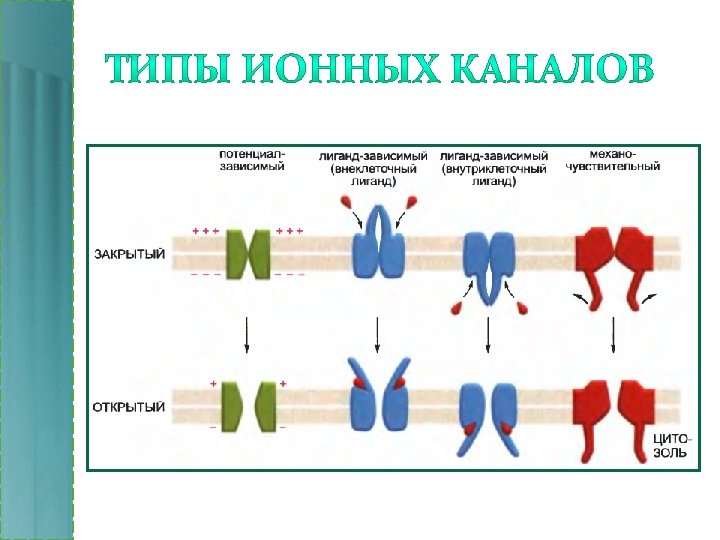
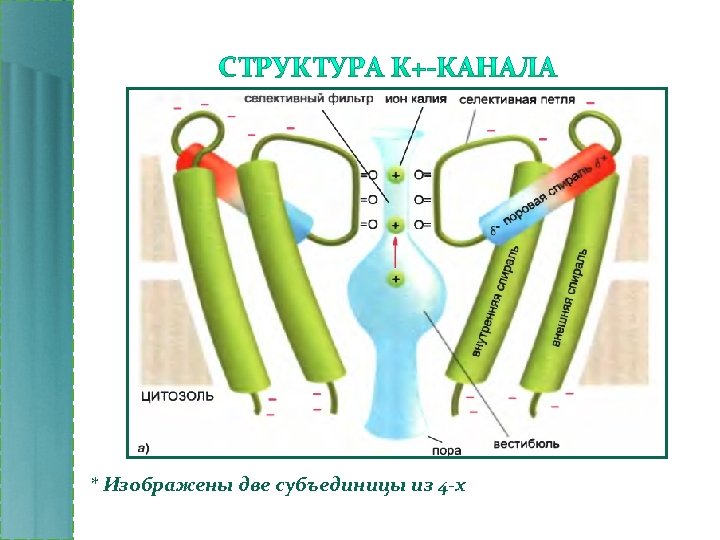
* Изображены две субъединицы из 4 -х
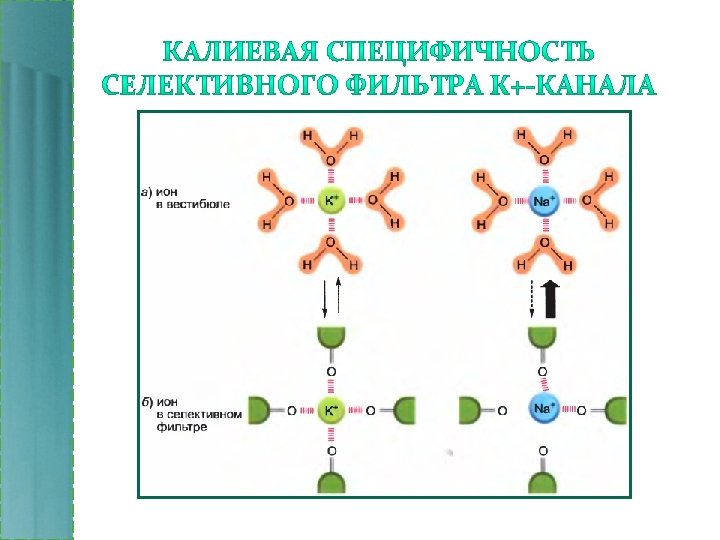

• «Ворота» – α-спирали субъединиц. • Типы движения ворот: изгиб, наклон, вращение. • Изменение направления движения ворот приводит к открытию-закрытию канала.
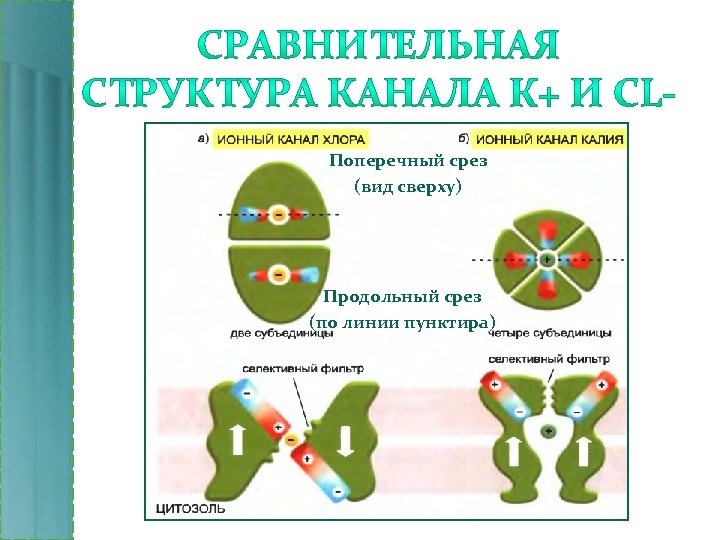
Поперечный срез (вид сверху) Продольный срез (по линии пунктира)
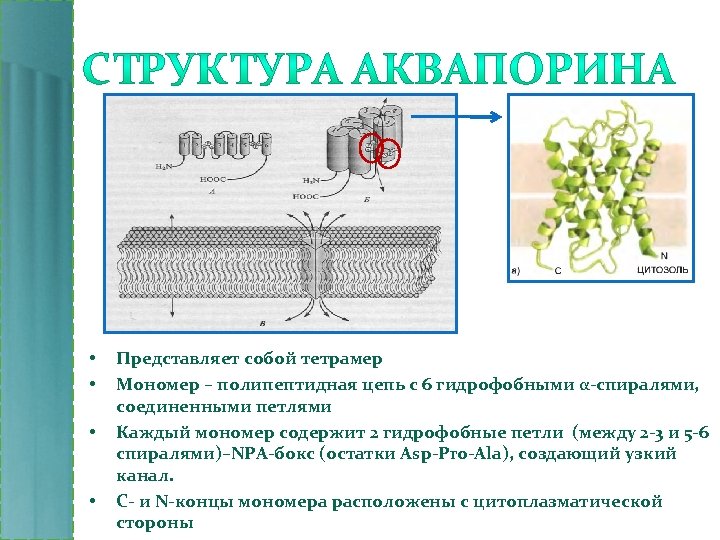
• • Представляет собой тетрамер Мономер – полипептидная цепь с 6 гидрофобными α-спиралями, соединенными петлями Каждый мономер содержит 2 гидрофобные петли (между 2 -3 и 5 -6 спиралями)–NPA-бокс (остатки Asp-Pro-Ala), создающий узкий канал. С- и N-концы мономера расположены с цитоплазматической стороны

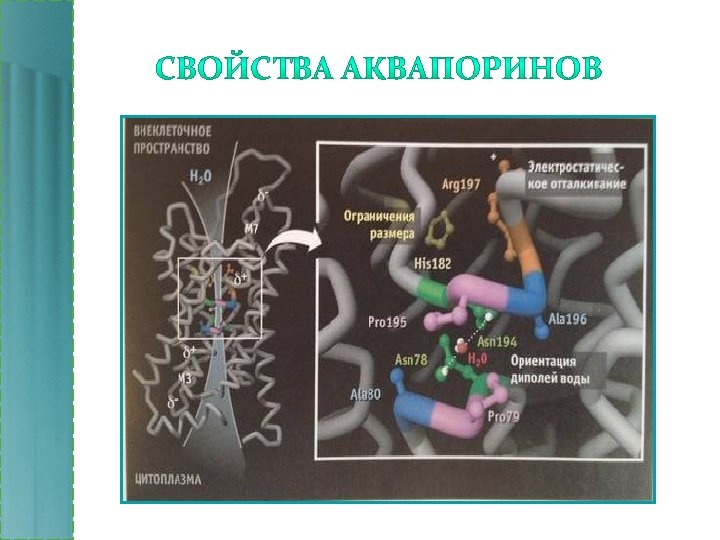
Свойства аквапоринов направлены на быстрый и селективный транспорт воды и ограничение транспорта ионов и протонизированной воды. Ограничения размера транспортируемых молекул. В области собственно поры устье достигает очень узкого размера (область сжатия). Проходимость сохраняется только для молекул воды по одиночке. • Электростатическое отталкивание. Положительно заряженные остатки Arg 197 препятствуют прохождению протонов и протонизированной воды (H 3 O+). • Ориентация диполей воды. Молекулы ориентированы (-)-полюсом по направлению к (+) полюсу аминокислот (Asn 78, 194) селективного фильтра. •


За счет активного транспорта в организме создаются • разности концентраций, • разности электрических потенциалов • разности давления поддерживающие жизненные процессы. Активный транспорт удерживает организм в неравновесном состоянии, т. к. равновесие – смерть организма.
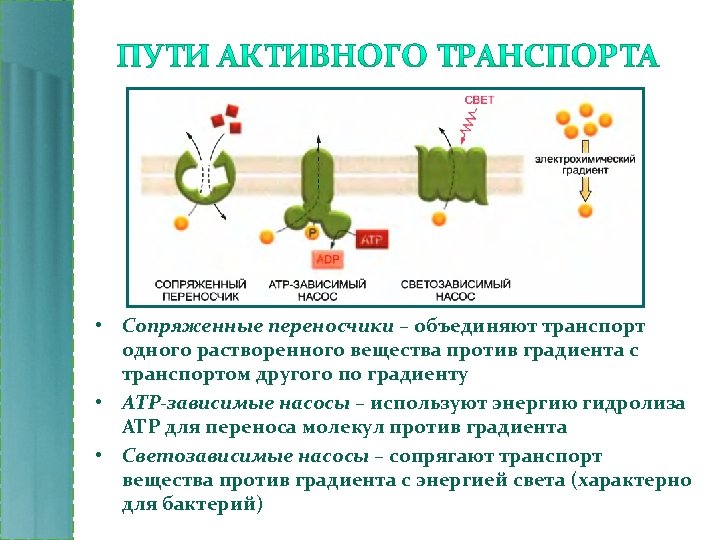
• Сопряженные переносчики – объединяют транспорт одного растворенного вещества против градиента с транспортом другого по градиенту • АТР-зависимые насосы – используют энергию гидролиза АТР для переноса молекул против градиента • Светозависимые насосы – сопрягают транспорт вещества против градиента с энергией света (характерно для бактерий)
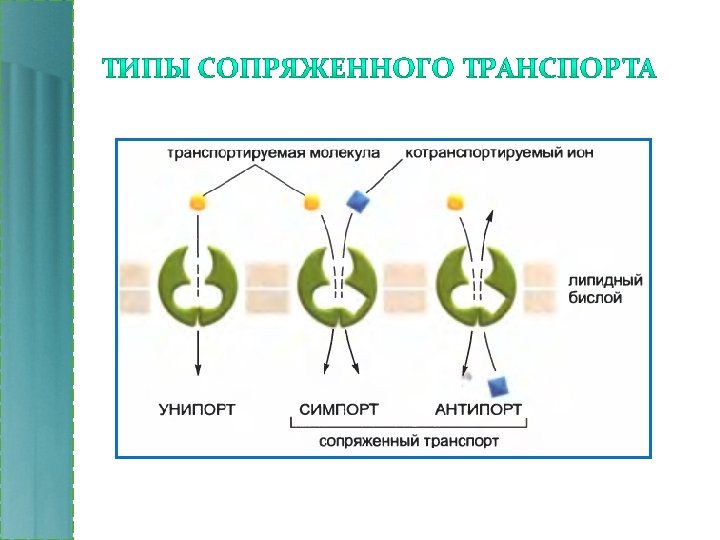
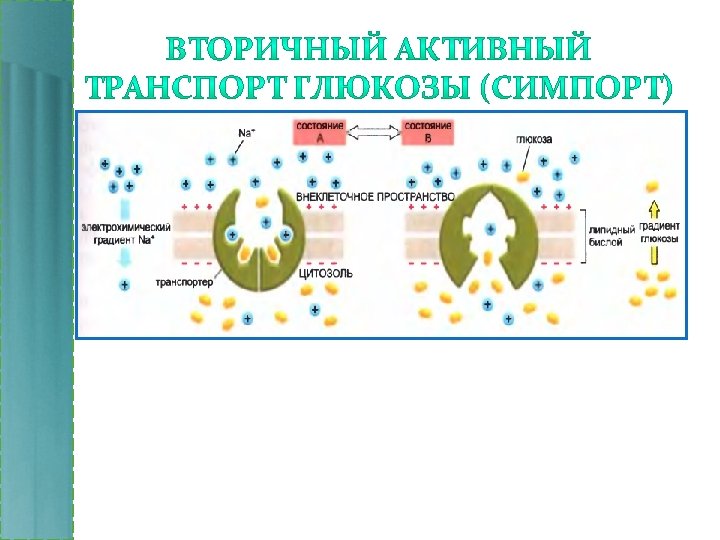
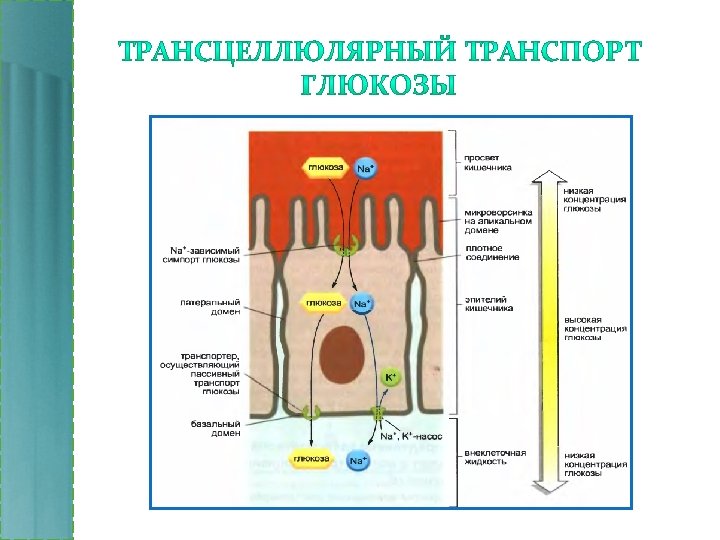

АТР-зависимые насосы
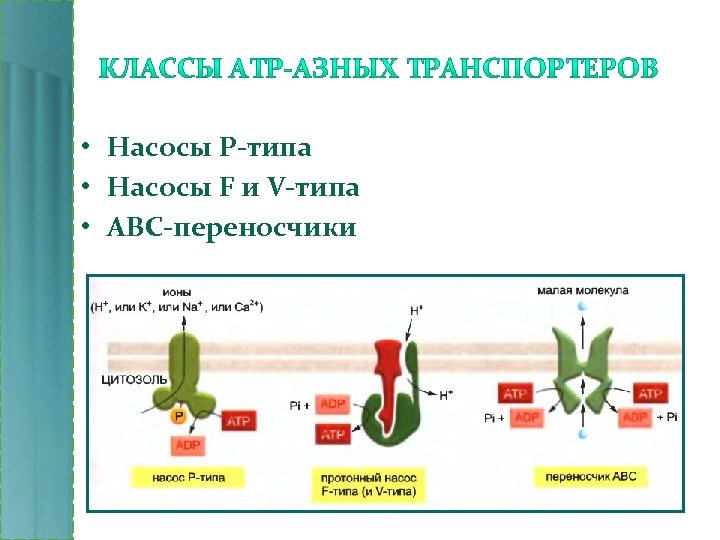
• Насосы Р-типа • Насосы F и V-типа • ABC-переносчики

• Структурно и функционально родственные многопроходные белки. • Обладают способностью к фосфорилированию «самих себя» . • Ответственны за поддержание градиента концентрации ионов: Na+, K+, H+, Ca 2+. Насосы Р-типа: ü Са 2+ - АТФ-аза ü K+ - Na+ - АТФ-аза ü Н+ - АТФ-аза.
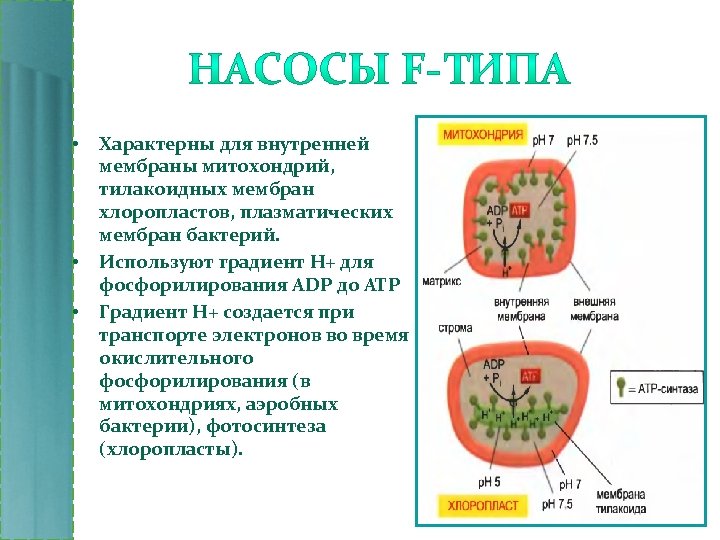
• • • Характерны для внутренней мембраны митохондрий, тилакоидных мембран хлоропластов, плазматических мембран бактерий. Используют градиент Н+ для фосфорилирования ADР до АТР Градиент Н+ создается при транспорте электронов во время окислительного фосфорилирования (в митохондриях, аэробных бактерии), фотосинтеза (хлоропласты).
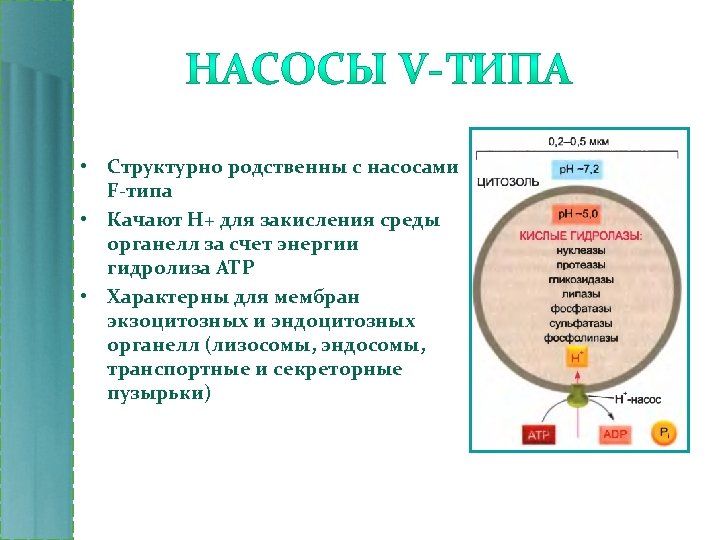
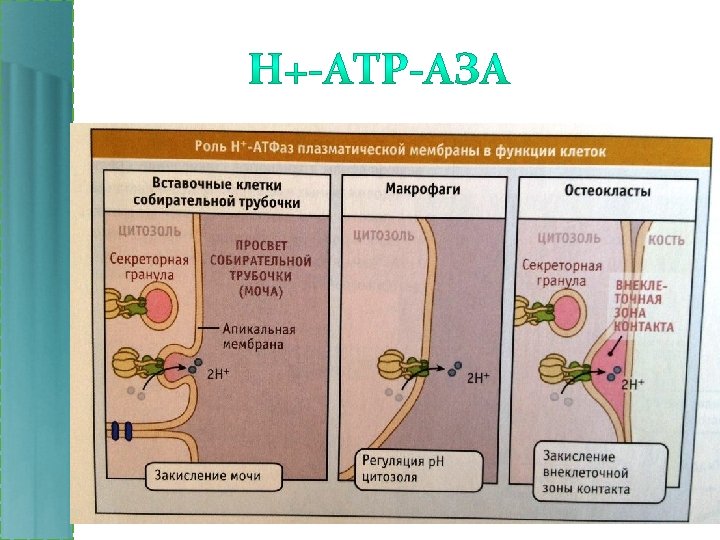
• Структурно родственны с насосами F-типа • Качают H+ для закисления среды органелл за счет энергии гидролиза АТР • Характерны для мембран экзоцитозных и эндоцитозных органелл (лизосомы, эндосомы, транспортные и секреторные пузырьки)

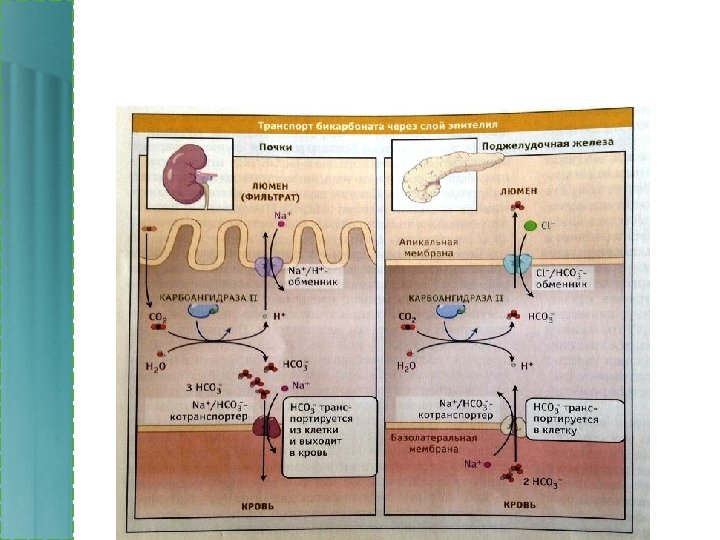
• Са 2+ - АТФ-аза • K+ / Na+ - АТФ-аза • Н+ - АТФ-аза.

СА 2+ - АТФ-АЗА • Содержит 10 трансмембранных α-спиралей, 3 из которых образуют центральный канал, пересекающий липидный бислой. • Составляет 90% белков саркоплазматического ретикулума в скелетных мышцах. • Обеспечивает обратную закачку Са 2+ из цитозоля в СПР. • ЭПС немышечных клеток несет Са-насосы подобного действия и строения, но в меньших количествах.
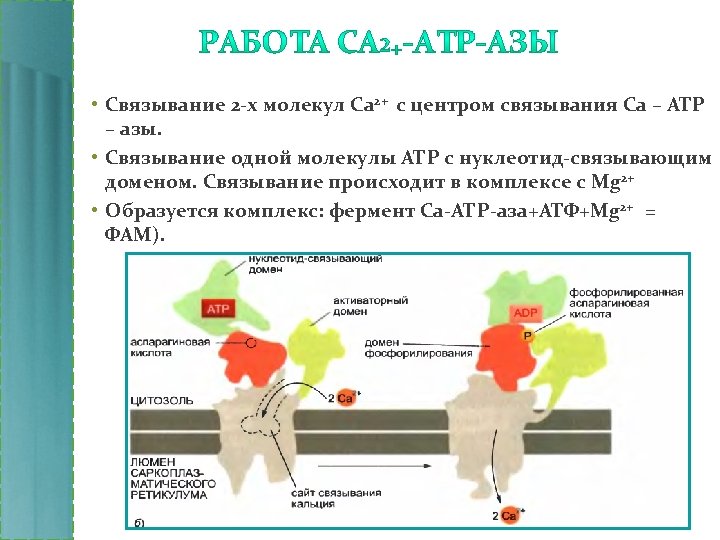
• Связывание 2 -х молекул Ca 2+ с центром связывания Ca – АТР – азы. • Связывание одной молекулы АТР с нуклеотид-связывающим доменом. Связывание происходит в комплексе с Mg 2+ • Образуется комплекс: фермент Ca-АТР-аза+АТФ+Mg 2+ = ФАМ).
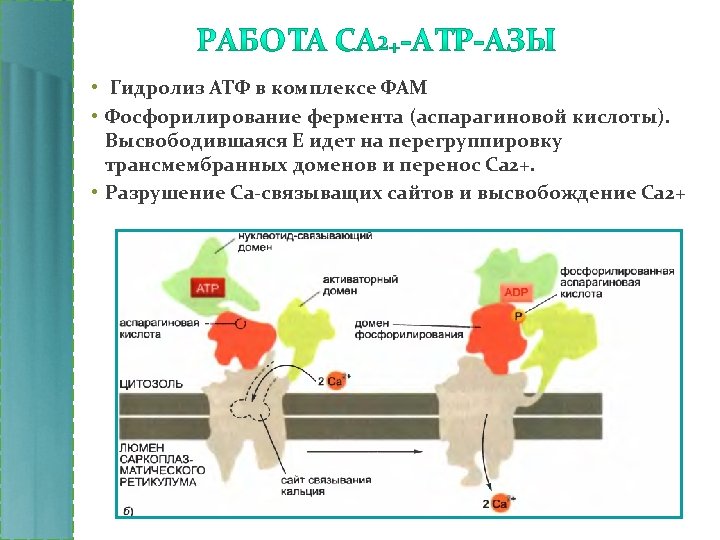
• Гидролиз АТФ в комплексе ФАМ • Фосфорилирование фермента (аспарагиновой кислоты). Высвободившаяся Е идет на перегруппировку трансмембранных доменов и перенос Са 2+. • Разрушение Са-связыващих сайтов и высвобождение Са 2+
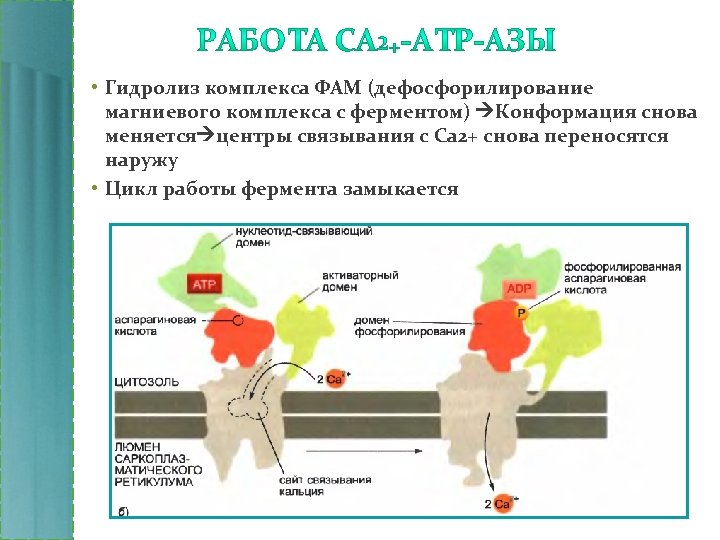
• Гидролиз комплекса ФАМ (дефосфорилирование магниевого комплекса с ферментом) Конформация снова меняется центры связывания с Са 2+ снова переносятся наружу • Цикл работы фермента замыкается
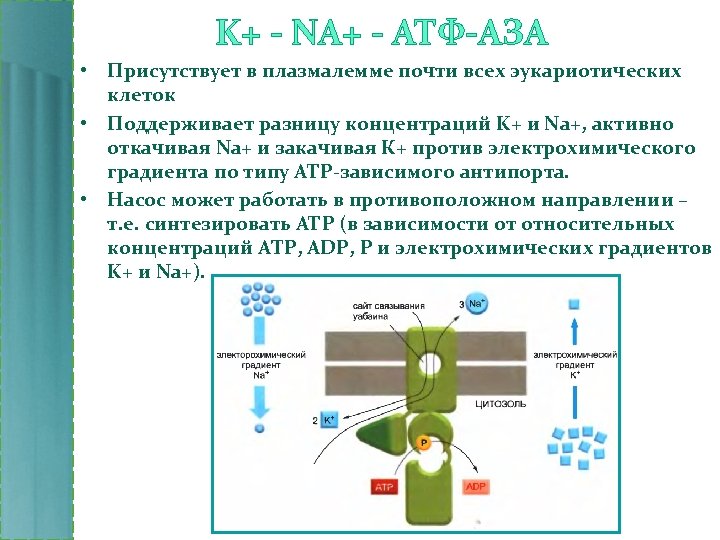
K+ - NA+ - АТФ-АЗА • Присутствует в плазмалемме почти всех эукариотических клеток • Поддерживает разницу концентраций K+ и Na+, активно откачивая Na+ и закачивая К+ против электрохимического градиента по типу АТР-зависимого антипорта. • Насос может работать в противоположном направлении – т. е. синтезировать АТР (в зависимости от относительных концентраций ATP, ADP, P и электрохимических градиентов K+ и Na+).
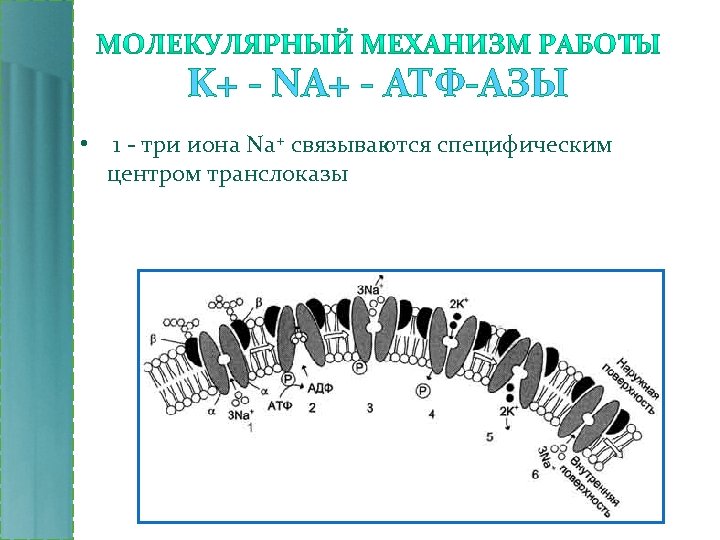
K+ - NA+ - АТФ-АЗЫ • 1 - три иона Na+ связываются специфическим центром транслоказы
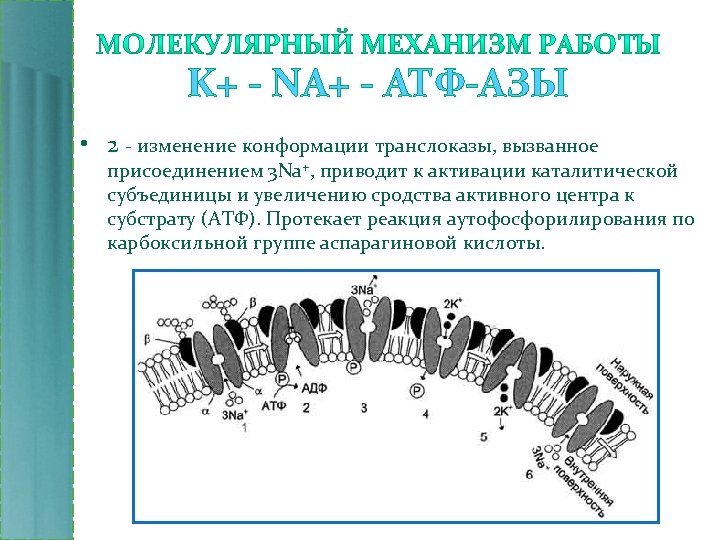
K+ - NA+ - АТФ-АЗЫ • 2 - изменение конформации транслоказы, вызванное присоединением 3 Na+, приводит к активации каталитической субъединицы и увеличению сродства активного центра к субстрату (АТФ). Протекает реакция аутофосфорилирования по карбоксильной группе аспарагиновой кислоты.
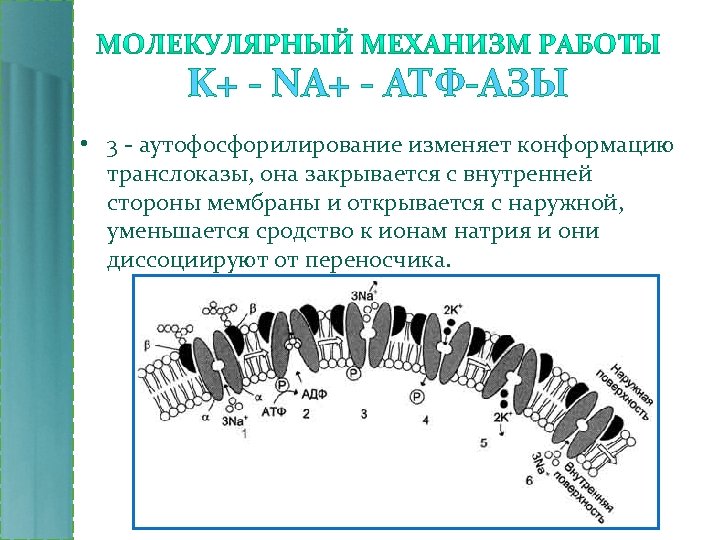
K+ - NA+ - АТФ-АЗЫ • 3 - аутофосфорилирование изменяет конформацию транслоказы, она закрывается с внутренней стороны мембраны и открывается с наружной, уменьшается сродство к ионам натрия и они диссоциируют от переносчика.
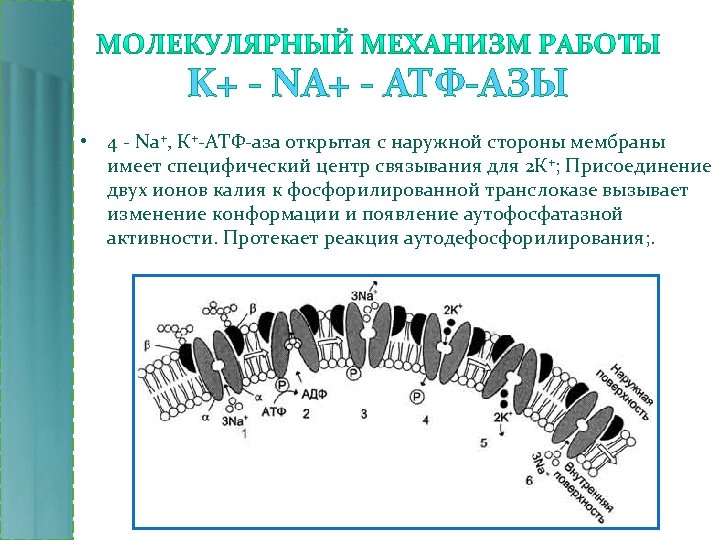
K+ - NA+ - АТФ-АЗЫ • 4 - Na+, К+-АТФ-аза открытая с наружной стороны мембраны имеет специфический центр связывания для 2 К+; Присоединение двух ионов калия к фосфорилированной транслоказе вызывает изменение конформации и появление аутофосфатазной активности. Протекает реакция аутодефосфорилирования; .
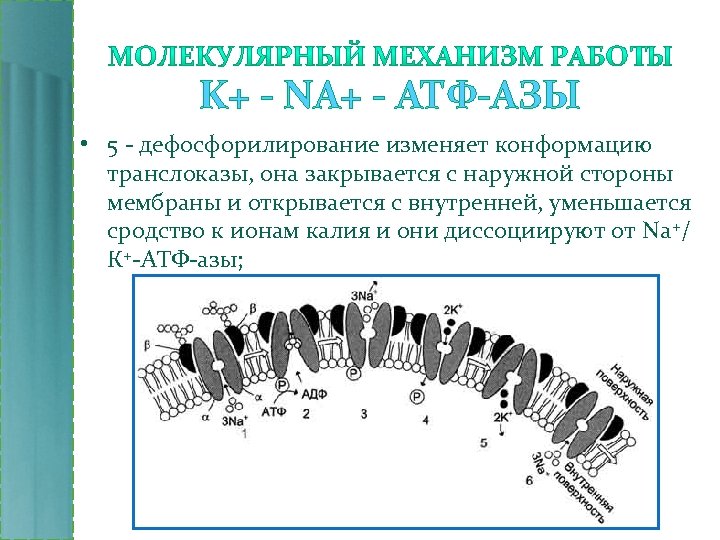
K+ - NA+ - АТФ-АЗЫ • 5 - дефосфорилирование изменяет конформацию транслоказы, она закрывается с наружной стороны мембраны и открывается с внутренней, уменьшается сродство к ионам калия и они диссоциируют от Na +/ К+-АТФ-азы;
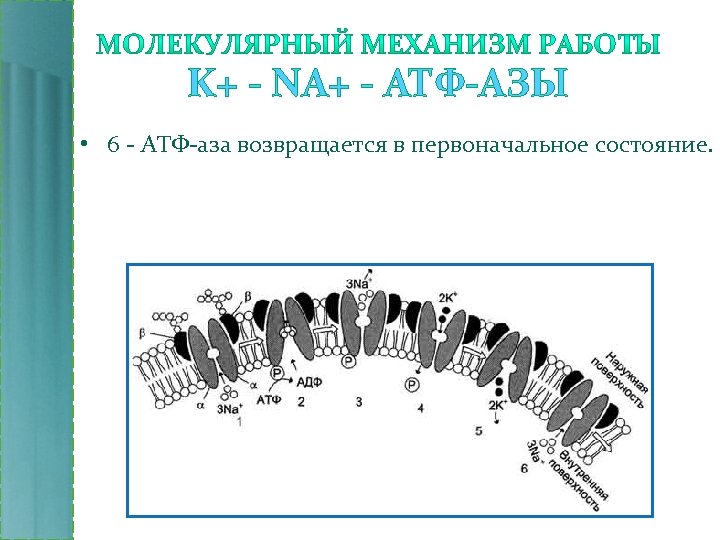
K+ - NA+ - АТФ-АЗЫ • 6 - АТФ-аза возвращается в первоначальное состояние.

РОЛЬ НАСОСА K+ - NA+ - АТФ-АЗА • Вносит вклад в полярность мембраны, хотя этот вклад составляет всего 10%. • Влияет на концентрацию растворенных веществ в цитозоле, т. е. играет роль в контролировании осмолярности (тоничности) цитозоля.

• Самое большое семейство мембранных транспортных белков. • Транспортируемые субстраты: неорганические ионы, аминокислоты, моно- и полисахариды, белки. Включают: • 2 гидрофобных домена: каждый состоит из 6 трансмембранных сегментов, формирующих путь переноса и определяющих субстратную специфичность • 2 высококонсервативных АТР-азных домена (АТР-связывающие кассеты/ АТР-Binding-Cassete)
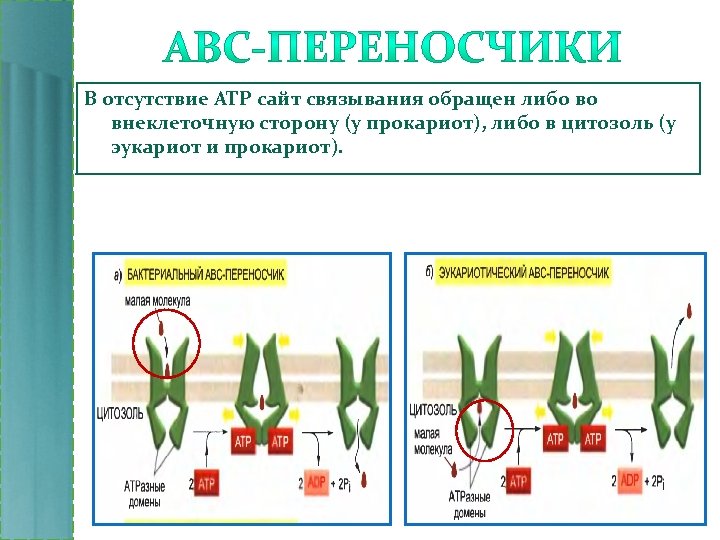
В отсутствие АТР сайт связывания обращен либо во внеклеточную сторону (у прокариот), либо в цитозоль (у эукариот и прокариот).
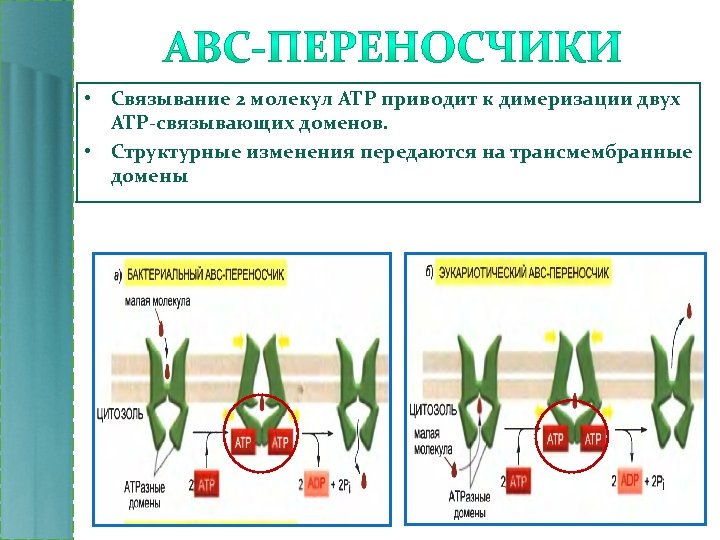
• Связывание 2 молекул АТР приводит к димеризации двух АТР-связывающих доменов. • Структурные изменения передаются на трансмембранные домены
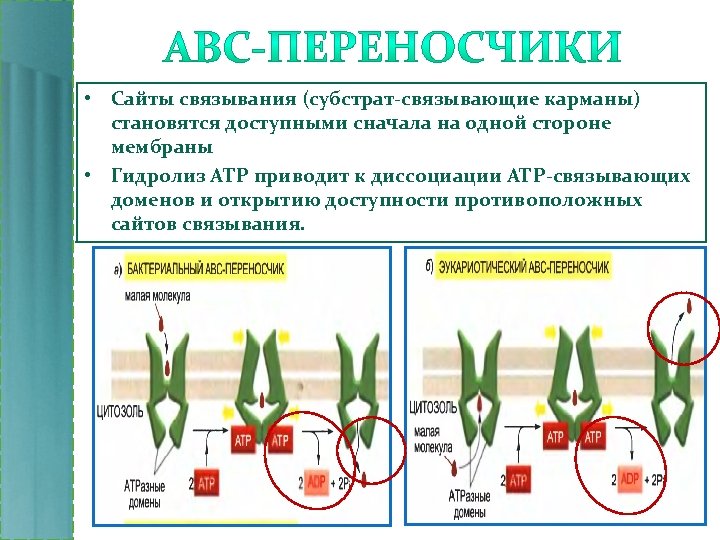
• Сайты связывания (субстрат-связывающие карманы) становятся доступными сначала на одной стороне мембраны • Гидролиз АТР приводит к диссоциации АТР-связывающих доменов и открытию доступности противоположных сайтов связывания.
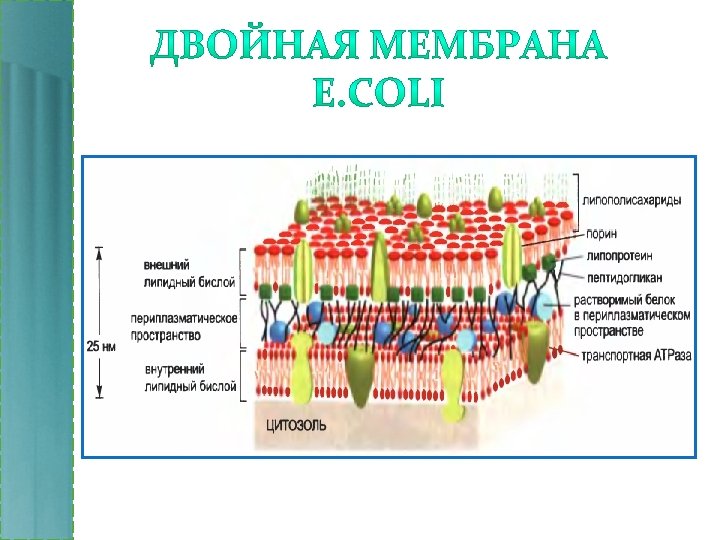
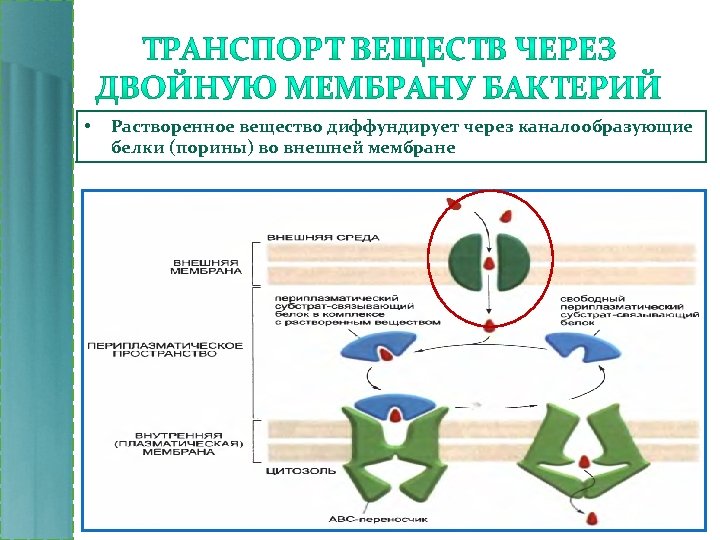
• Растворенное вещество диффундирует через каналообразующие белки (порины) во внешней мембране
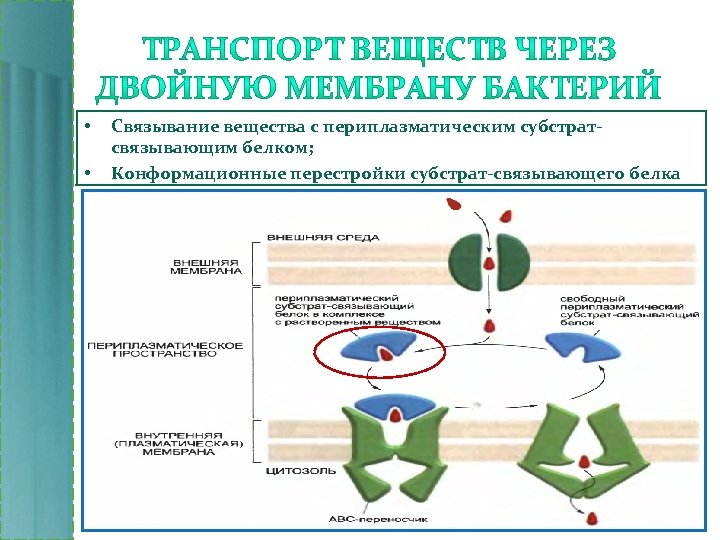
• • Связывание вещества с периплазматическим субстратсвязывающим белком; Конформационные перестройки субстрат-связывающего белка
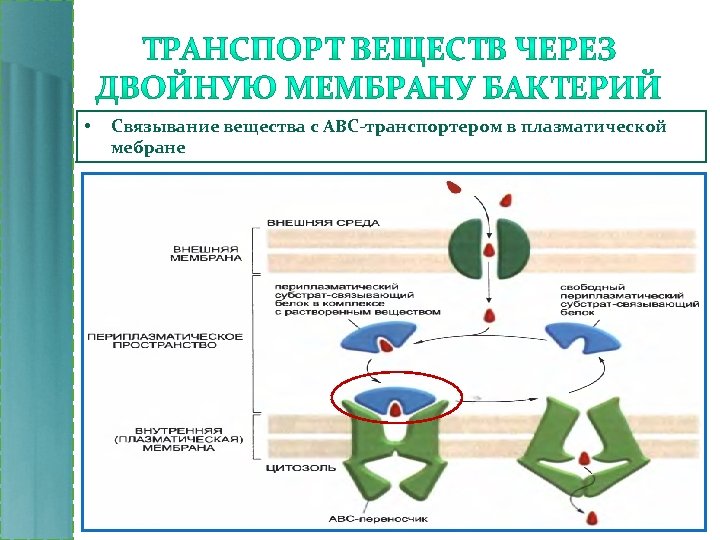
• Связывание вещества с АВС-транспортером в плазматической мебране
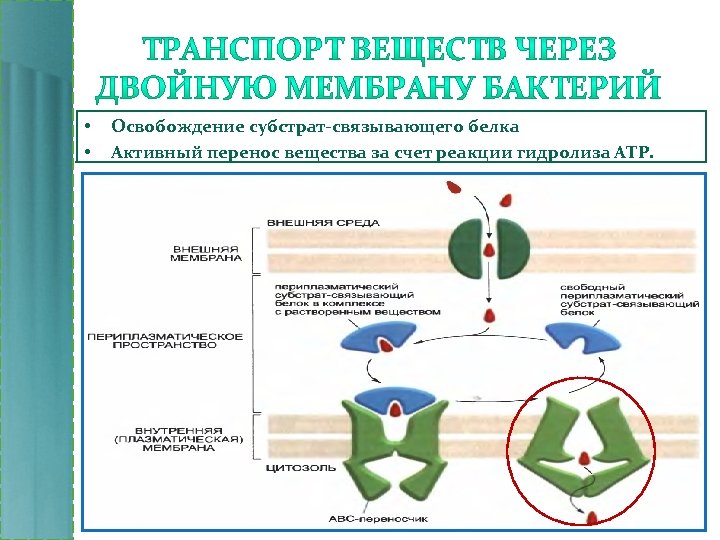
• • Освобождение субстрат-связывающего белка Активный перенос вещества за счет реакции гидролиза АТР.

• Белок множественной лекарственной устойчивости (MDRбелок) • Сверхэкспрессия белка в раковых клетках приводит к высокой устойчивости к ряду препаратов, используемых в химиотерапии рака (за счет откачки лекарств из клетки), что ведет к выживанию и разрастанию раковых клеток. *До 40% раковых состояний человека развивают множественную устойчивость, создавая большие препятствия в лечении данного заболевания.
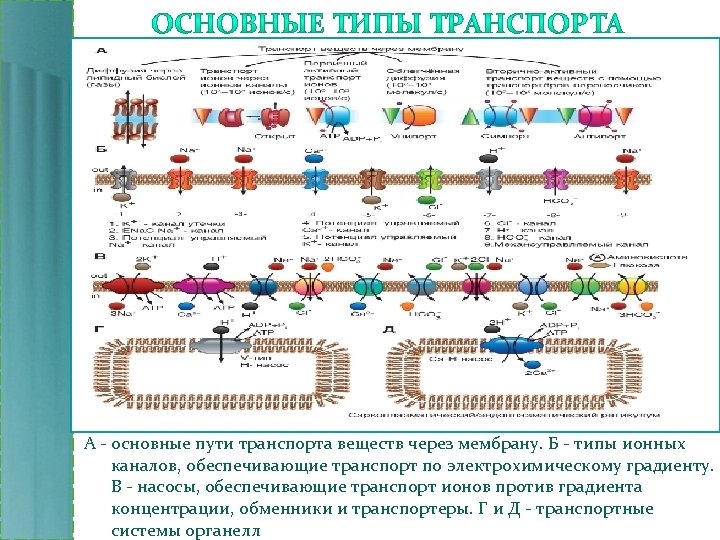
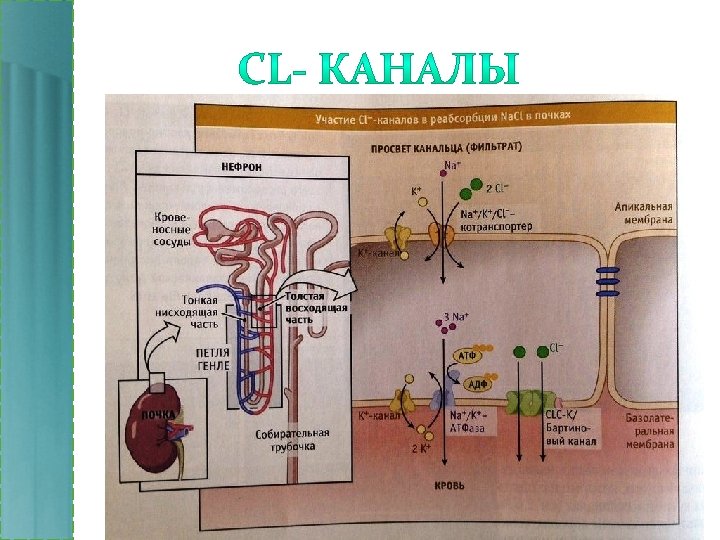
А - основные пути транспорта веществ через мембрану. Б - типы ионных каналов, обеспечивающие транспорт по электрохимическому градиенту. В - насосы, обеспечивающие транспорт ионов против градиента концентрации, обменники и транспортеры. Г и Д - транспортные системы органелл



40e9ead410e24e61631e4dbe15999ddc.ppt