MedChem12_1.ppt
- Количество слайдов: 74
 Медицинская химия
Медицинская химия
 Ефимов Павел Викторович
Ефимов Павел Викторович
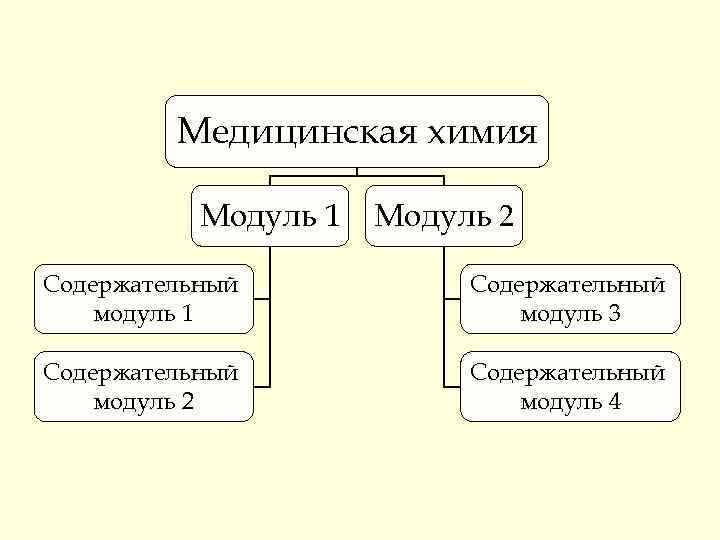 Медицинская химия Модуль 1 Модуль 2 Содержательный модуль 1 Содержательный модуль 3 Содержательный модуль 2 Содержательный модуль 4
Медицинская химия Модуль 1 Модуль 2 Содержательный модуль 1 Содержательный модуль 3 Содержательный модуль 2 Содержательный модуль 4
 Модуль 1 «Основные типы равновесий в растворах электролитов и в биологических системах. Соединения биоэлементов в организме человека, их биологическое значение и использование в медицине» 5 пар лекций ауд. 5 -84 10 пар практических занятий и 2 контрольные работы ауд. 7 -85, 7 -88 (Центральный корпус)
Модуль 1 «Основные типы равновесий в растворах электролитов и в биологических системах. Соединения биоэлементов в организме человека, их биологическое значение и использование в медицине» 5 пар лекций ауд. 5 -84 10 пар практических занятий и 2 контрольные работы ауд. 7 -85, 7 -88 (Центральный корпус)
 Модуль 1 Оценивание Практические занятия. Тестовый контроль. Итого: Баллы 180 -200 166 -179 150 -165 136 -149 120 -135 <120 Максимум 120 баллов. Максимум 2× 40=80 баллов. Максимум 200 баллов. ECTS A B C D E F Оценка Відмінно Добре Задовільно Незадовільно
Модуль 1 Оценивание Практические занятия. Тестовый контроль. Итого: Баллы 180 -200 166 -179 150 -165 136 -149 120 -135 <120 Максимум 120 баллов. Максимум 2× 40=80 баллов. Максимум 200 баллов. ECTS A B C D E F Оценка Відмінно Добре Задовільно Незадовільно
 Модуль 1 • Классы неорганических соединений. Общие закономерности протекания химических реакций. • Общая характеристика растворов и растворов электролитов. • Кислотно-основные равновесия в растворах и биологических системах. • Комплексные соединения, равновесия комплексообразования в растворах и биологических системах. • Окислительновосстановительные процессы в растворах и биологических системах • Равновесия в растворах малорастворимых электролитов • Соединения биоэлементов в биологических системах, их биологическое значение и использование в медицине
Модуль 1 • Классы неорганических соединений. Общие закономерности протекания химических реакций. • Общая характеристика растворов и растворов электролитов. • Кислотно-основные равновесия в растворах и биологических системах. • Комплексные соединения, равновесия комплексообразования в растворах и биологических системах. • Окислительновосстановительные процессы в растворах и биологических системах • Равновесия в растворах малорастворимых электролитов • Соединения биоэлементов в биологических системах, их биологическое значение и использование в медицине
 Самостоятельная подготовка • Классы неорганических соединений. Общие закономерности протекания химических реакций.
Самостоятельная подготовка • Классы неорганических соединений. Общие закономерности протекания химических реакций.
 Общая характеристика растворов и растворов электролитов.
Общая характеристика растворов и растворов электролитов.
 • Раствор - система переменного состава, состоящая из двух или более компонентов • Гомогенная система – система, состоящая из одной фазы. Гетерогенная система – система, состоящая из двух или большего числа фаз.
• Раствор - система переменного состава, состоящая из двух или более компонентов • Гомогенная система – система, состоящая из одной фазы. Гетерогенная система – система, состоящая из двух или большего числа фаз.
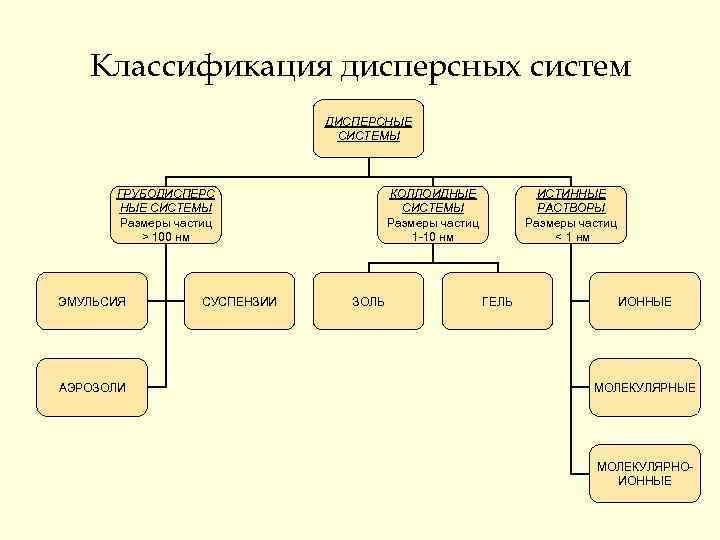 Классификация дисперсных систем ДИСПЕРСНЫЕ СИСТЕМЫ ГРУБОДИСПЕРС НЫЕ СИСТЕМЫ Размеры частиц > 100 нм ЭМУЛЬСИЯ АЭРОЗОЛИ СУСПЕНЗИИ КОЛЛОИДНЫЕ СИСТЕМЫ Размеры частиц 1 -10 нм ЗОЛЬ ИСТИННЫЕ РАСТВОРЫ Размеры частиц < 1 нм ГЕЛЬ ИОННЫЕ МОЛЕКУЛЯРНОИОННЫЕ
Классификация дисперсных систем ДИСПЕРСНЫЕ СИСТЕМЫ ГРУБОДИСПЕРС НЫЕ СИСТЕМЫ Размеры частиц > 100 нм ЭМУЛЬСИЯ АЭРОЗОЛИ СУСПЕНЗИИ КОЛЛОИДНЫЕ СИСТЕМЫ Размеры частиц 1 -10 нм ЗОЛЬ ИСТИННЫЕ РАСТВОРЫ Размеры частиц < 1 нм ГЕЛЬ ИОННЫЕ МОЛЕКУЛЯРНОИОННЫЕ
 Истинные растворы ь Молекулярные – это водные растворы неэлектролитов – органических веществ (спирта, глюкозы, сахарозы и т. д. ); ь Ионные – это растворы сильных электролитов (щелочей, солей, кислот – Na. OH, K 2 SO 4. HNO 3, HCl. O 4); ь Молекулярно – ионные – это растворы слабых электролитов (азотистой, сероводородной кислот и др. ).
Истинные растворы ь Молекулярные – это водные растворы неэлектролитов – органических веществ (спирта, глюкозы, сахарозы и т. д. ); ь Ионные – это растворы сильных электролитов (щелочей, солей, кислот – Na. OH, K 2 SO 4. HNO 3, HCl. O 4); ь Молекулярно – ионные – это растворы слабых электролитов (азотистой, сероводородной кислот и др. ).
 Способы выражения состава растворов • Массовая доля • Мольная доля • Молярность • Моляльность ω Х С Сm
Способы выражения состава растворов • Массовая доля • Мольная доля • Молярность • Моляльность ω Х С Сm
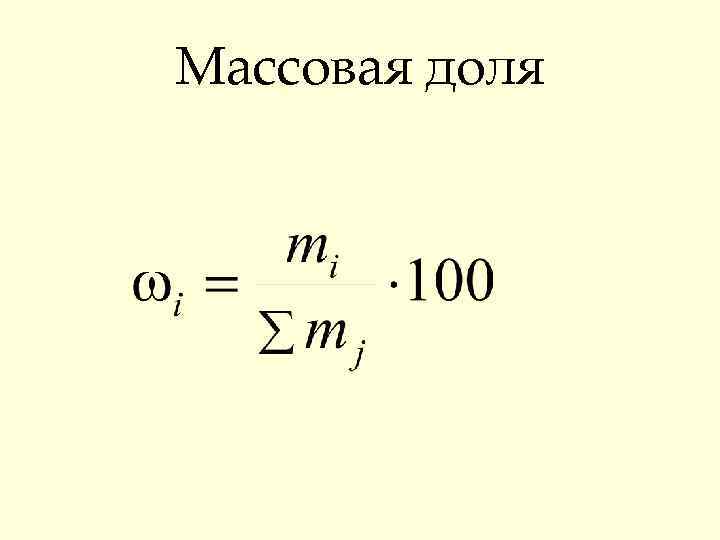 Массовая доля
Массовая доля
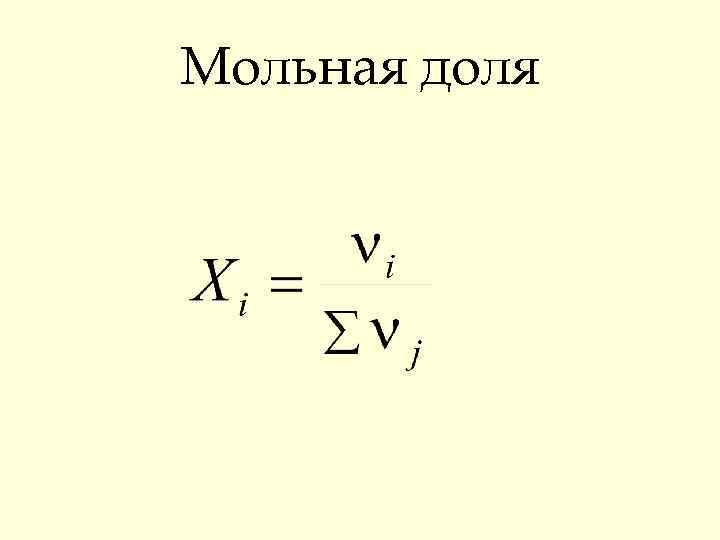 Мольная доля
Мольная доля
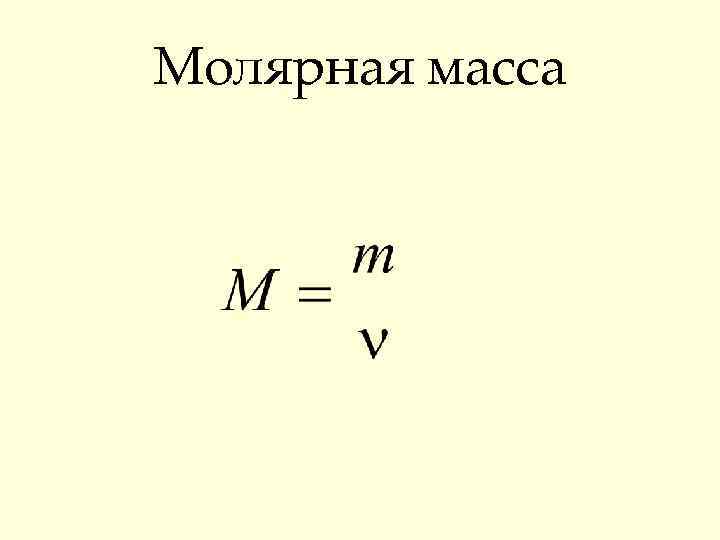 Молярная масса
Молярная масса
 Молярная концентрация
Молярная концентрация
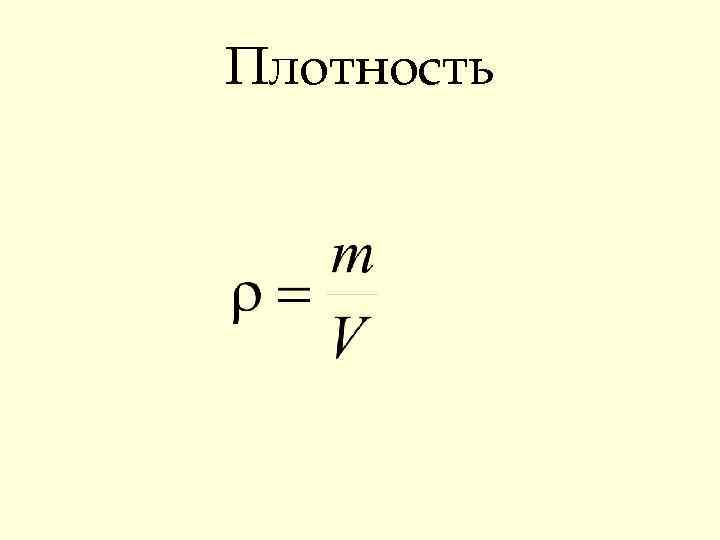 Плотность
Плотность
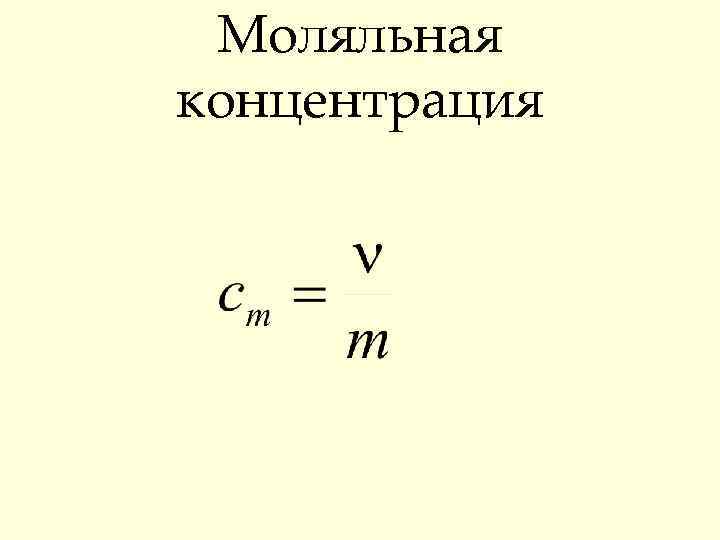 Моляльная концентрация
Моляльная концентрация
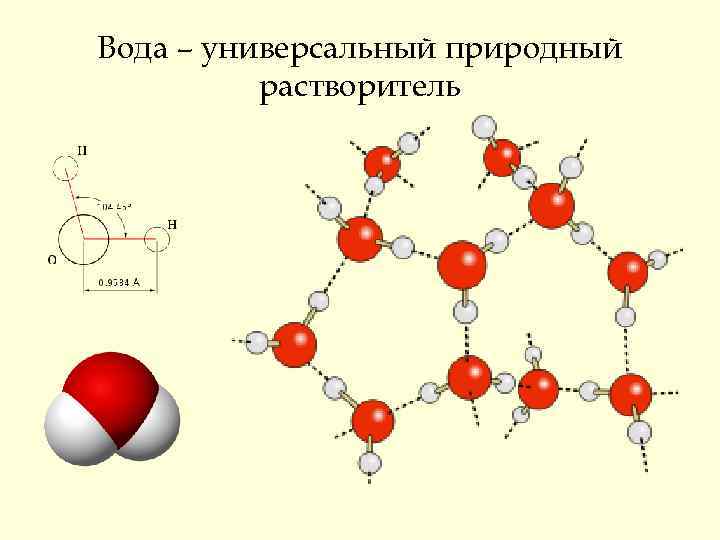 Вода – универсальный природный растворитель
Вода – универсальный природный растворитель
 В биохимических процессах вода выступает как : 1. Растворитель 2. Реагент 3. Продукт реакции
В биохимических процессах вода выступает как : 1. Растворитель 2. Реагент 3. Продукт реакции
 Существование межмолекулярных водородных связей определяет аномальные физические свойства воды: 1. Высокая теплоемкость 2. Высокая температура кипения 3. Большая теплота испарения 4. Высокое поверхностное натяжение 5. Высокая вязкость 6. Более высокая плотность в жидком состоянии, чем в твердом Высокая диэлектрическая проницаемость (ε = 80) …
Существование межмолекулярных водородных связей определяет аномальные физические свойства воды: 1. Высокая теплоемкость 2. Высокая температура кипения 3. Большая теплота испарения 4. Высокое поверхностное натяжение 5. Высокая вязкость 6. Более высокая плотность в жидком состоянии, чем в твердом Высокая диэлектрическая проницаемость (ε = 80) …
 Термодинамика процесса растворения Растворение – процесс самопроизвольный, поэтому ∆Gрастворения < 0. ∆ Gрастворения = ∆Н растворения –Т ∆Sрастворения
Термодинамика процесса растворения Растворение – процесс самопроизвольный, поэтому ∆Gрастворения < 0. ∆ Gрастворения = ∆Н растворения –Т ∆Sрастворения
 Энергетическая характеристика растворения 1. Рассмотрим растворение твердого вещества с ионной связью в воде. ∆Н растворения = ∆Н фаз. перехода + ∆Н гидратации > 0 < 0 Разрушение к. р. – эндотермический процесс Образование хим. связи –экзотермический процесс
Энергетическая характеристика растворения 1. Рассмотрим растворение твердого вещества с ионной связью в воде. ∆Н растворения = ∆Н фаз. перехода + ∆Н гидратации > 0 < 0 Разрушение к. р. – эндотермический процесс Образование хим. связи –экзотермический процесс
 1. Если |∆Н ф. п. |> |∆Н гидр. |, то ∆Н растворения > 0, эндо-процесс, раствор охлаждается (КNO 3, NH 4 NO 3) 2. Если |∆Н ф. п. |<|∆Н гидр. |, то ∆Н растворения < 0, экзо-процесс, раствор нагревается (Na. OH ) Т. о. при растворении тв. /ж. 0 < ∆ Н растворения < 0
1. Если |∆Н ф. п. |> |∆Н гидр. |, то ∆Н растворения > 0, эндо-процесс, раствор охлаждается (КNO 3, NH 4 NO 3) 2. Если |∆Н ф. п. |<|∆Н гидр. |, то ∆Н растворения < 0, экзо-процесс, раствор нагревается (Na. OH ) Т. о. при растворении тв. /ж. 0 < ∆ Н растворения < 0
 Энтропийная характеристика растворения ∆Sрастворения = ∆S фаз. перехода + ∆S гидратации >> 0 < 0, т. к. уменьшается число частиц в единице объёма Т. о. , |∆S ф. п. |> |∆S гидр. |, поэтому ∆Sрастворения тв. вещ-в > 0
Энтропийная характеристика растворения ∆Sрастворения = ∆S фаз. перехода + ∆S гидратации >> 0 < 0, т. к. уменьшается число частиц в единице объёма Т. о. , |∆S ф. п. |> |∆S гидр. |, поэтому ∆Sрастворения тв. вещ-в > 0
 2. Рассмотрим растворение газообразного вещества в воде. Обычно ∆Sрастворения газов < 0, ∆Gрастворения = ∆Н растворения – Т ∆Sрастворения ∆Нрастворения=∆G растворения + Т ∆Sрастворения ∆Gраств. < 0 и ∆Sраств. < 0 ; ∆Н растворения газов < 0
2. Рассмотрим растворение газообразного вещества в воде. Обычно ∆Sрастворения газов < 0, ∆Gрастворения = ∆Н растворения – Т ∆Sрастворения ∆Нрастворения=∆G растворения + Т ∆Sрастворения ∆Gраств. < 0 и ∆Sраств. < 0 ; ∆Н растворения газов < 0
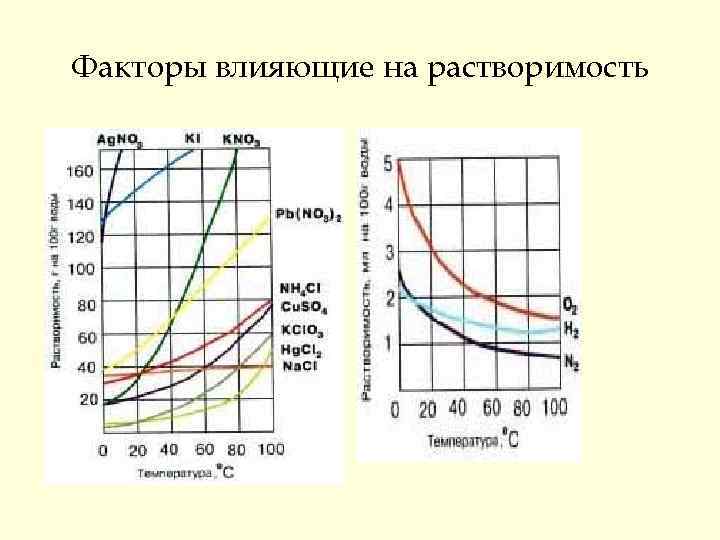 Факторы влияющие на растворимость
Факторы влияющие на растворимость
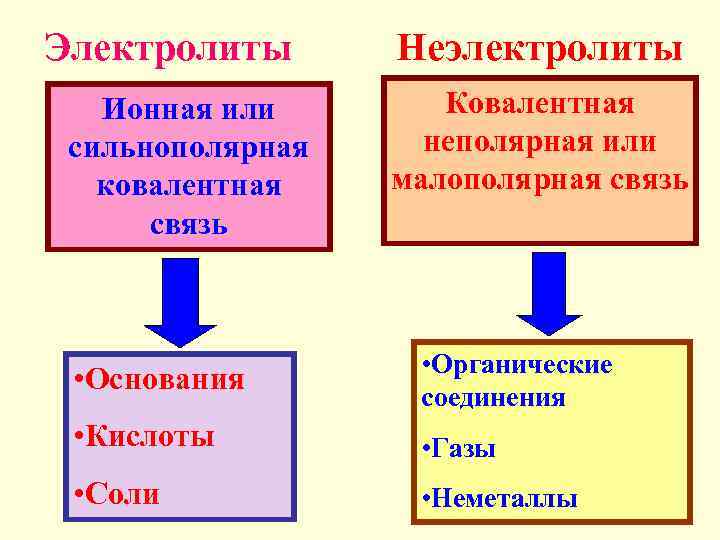 Электролиты Ионная или сильнополярная ковалентная связь Неэлектролиты Ковалентная неполярная или малополярная связь • Основания • Органические соединения • Кислоты • Газы • Соли • Неметаллы
Электролиты Ионная или сильнополярная ковалентная связь Неэлектролиты Ковалентная неполярная или малополярная связь • Основания • Органические соединения • Кислоты • Газы • Соли • Неметаллы
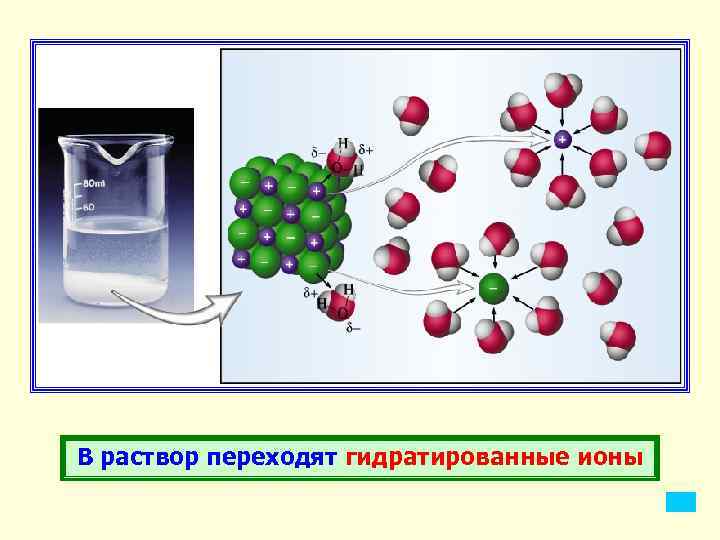 В раствор переходят гидратированные ионы
В раствор переходят гидратированные ионы
 неэлектролит сильный электролит слабый электролит
неэлектролит сильный электролит слабый электролит
 Количественная характеристика процесса диссоциации Отношение числа распавшихся молекул к общему числу молекул в растворе Сила электролита
Количественная характеристика процесса диссоциации Отношение числа распавшихся молекул к общему числу молекул в растворе Сила электролита
 С- исходная молярная концентрация кислоты, моль/л; - степень диссоциации; С - число продиссоциировавших молекул; (С- С ) – число не продиссоциировавших (оставшихся) молекул; [H+] = [CH 3 COO -] = С
С- исходная молярная концентрация кислоты, моль/л; - степень диссоциации; С - число продиссоциировавших молекул; (С- С ) – число не продиссоциировавших (оставшихся) молекул; [H+] = [CH 3 COO -] = С
 для слабых электролитов 0 и (1 - ) 1, тогда закон разведения Оствальда (1888 г. )
для слабых электролитов 0 и (1 - ) 1, тогда закон разведения Оствальда (1888 г. )
 Теория электролитической диссоциации (ТЭД) электролитов Аррениуса -это теория растворов слабых электролитов. Факторы, влияющие на : 1. природа вещества а) растворителя (дипольный момент , диэлектрическая проницаемость) б) характер хим. связи в молекуле растворенного вещества. 2. концентрация вещества ( с С, ↓) 3. температура (с Т, )
Теория электролитической диссоциации (ТЭД) электролитов Аррениуса -это теория растворов слабых электролитов. Факторы, влияющие на : 1. природа вещества а) растворителя (дипольный момент , диэлектрическая проницаемость) б) характер хим. связи в молекуле растворенного вещества. 2. концентрация вещества ( с С, ↓) 3. температура (с Т, )
 4. наличие одноименных ионов – принцип Ле. Шателье: а) НCl, H+, х. р. , б) СН 3 СООNa, х. р. , в) Na. OH, OH-, х. р. , Т. о. , = f (C, Т)
4. наличие одноименных ионов – принцип Ле. Шателье: а) НCl, H+, х. р. , б) СН 3 СООNa, х. р. , в) Na. OH, OH-, х. р. , Т. о. , = f (C, Т)
 К дис. зависит: 1. от природы электролита 2. от температуры: Т , Кдис Т. к. Кдис. f (C) , то ее сравнивают для разных электролитов. Чем больше Кдис. , тем сильнее электролит.
К дис. зависит: 1. от природы электролита 2. от температуры: Т , Кдис Т. к. Кдис. f (C) , то ее сравнивают для разных электролитов. Чем больше Кдис. , тем сильнее электролит.
 Диссоциация воды. Ионное произведение воды. Н+ Н 2 О Н+ + ОН-
Диссоциация воды. Ионное произведение воды. Н+ Н 2 О Н+ + ОН-
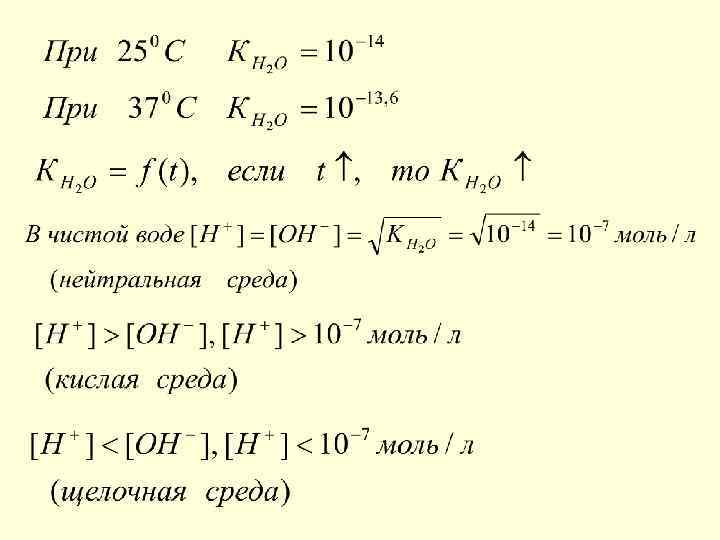
 Водородный показатель (р. Н) 1909 г. Серенсен
Водородный показатель (р. Н) 1909 г. Серенсен
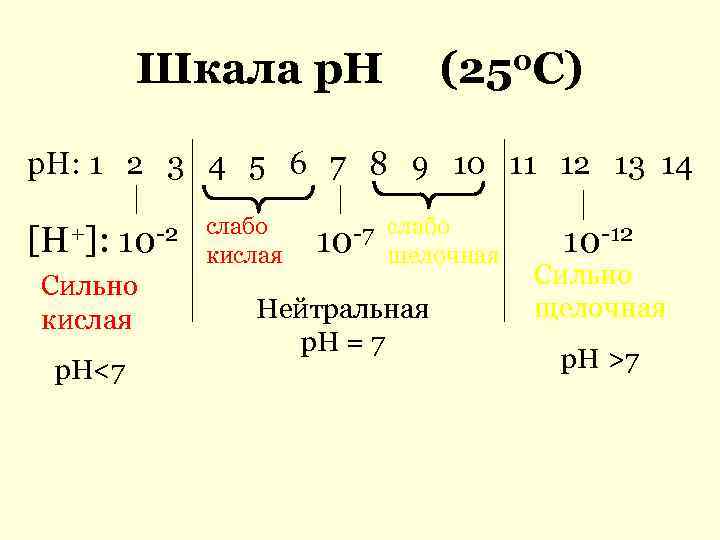 Шкала р. Н (250 С) р. Н: 1 2 3 4 5 6 7 8 9 10 11 12 13 14 [H+]: 10 -2 Сильно кислая р. Н<7 слабо кислая -7 слабо 10 щелочная Нейтральная р. Н = 7 10 -12 Сильно щелочная р. Н >7
Шкала р. Н (250 С) р. Н: 1 2 3 4 5 6 7 8 9 10 11 12 13 14 [H+]: 10 -2 Сильно кислая р. Н<7 слабо кислая -7 слабо 10 щелочная Нейтральная р. Н = 7 10 -12 Сильно щелочная р. Н >7
 Расчет р. Н растворов I. Сильных кислот и оснований fa 1
Расчет р. Н растворов I. Сильных кислот и оснований fa 1
 II. Слабых кислот и оснований
II. Слабых кислот и оснований
![Если неизвестно: [СН 3 СОО-]=[Н+] В справочнике Если неизвестно: [СН 3 СОО-]=[Н+] В справочнике](https://present5.com/presentation/3/-43958340_132542874.pdf-img/-43958340_132542874.pdf-43.jpg) Если неизвестно: [СН 3 СОО-]=[Н+] В справочнике
Если неизвестно: [СН 3 СОО-]=[Н+] В справочнике
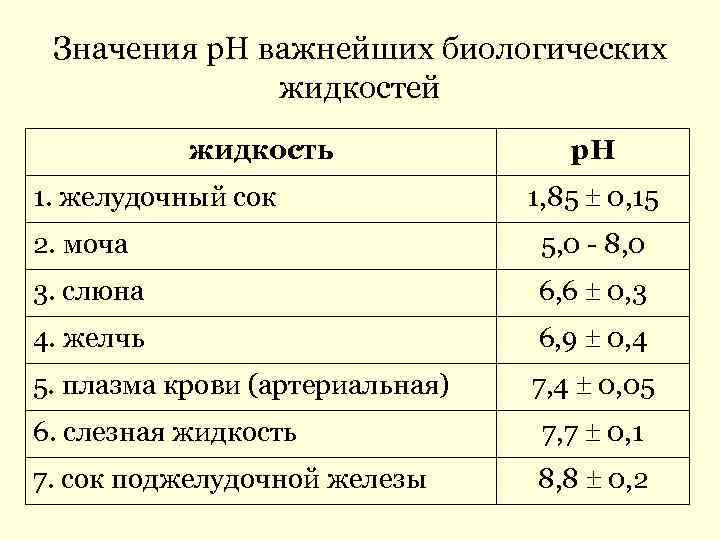 Значения р. Н важнейших биологических жидкостей жидкость 1. желудочный сок р. Н 1, 85 0, 15 2. моча 5, 0 - 8, 0 3. слюна 6, 6 0, 3 4. желчь 6, 9 0, 4 5. плазма крови (артериальная) 7, 4 0, 05 6. слезная жидкость 7, 7 0, 1 7. сок поджелудочной железы 8, 8 0, 2
Значения р. Н важнейших биологических жидкостей жидкость 1. желудочный сок р. Н 1, 85 0, 15 2. моча 5, 0 - 8, 0 3. слюна 6, 6 0, 3 4. желчь 6, 9 0, 4 5. плазма крови (артериальная) 7, 4 0, 05 6. слезная жидкость 7, 7 0, 1 7. сок поджелудочной железы 8, 8 0, 2
 Теория растворов сильных электролитов (1923 г, Дебай, Хюккель) 1. 2. 3. Сильные электролиты в водных растворах диссоциируют полностью, т. е. для них = 1 или 100 % , молекул электролита нет. Поэтому, ни Кд к сильным электролитам неприменимы. В растворах за счет сильного ион-дипольного взаимодействия с молекулами Н 2 О образуются гидратные оболочки иона. Сильное ион-ионное взаимодействие создает ионные атмосферы (каждый гидратированный ион окружен гидратированными ионами противоположного заряда).
Теория растворов сильных электролитов (1923 г, Дебай, Хюккель) 1. 2. 3. Сильные электролиты в водных растворах диссоциируют полностью, т. е. для них = 1 или 100 % , молекул электролита нет. Поэтому, ни Кд к сильным электролитам неприменимы. В растворах за счет сильного ион-дипольного взаимодействия с молекулами Н 2 О образуются гидратные оболочки иона. Сильное ион-ионное взаимодействие создает ионные атмосферы (каждый гидратированный ион окружен гидратированными ионами противоположного заряда).
 Активность (а) Аналитическая концентрация Коэффициент активности- … Для реальных растворов fa < 1. В сильно разбавленных растворах fa 1.
Активность (а) Аналитическая концентрация Коэффициент активности- … Для реальных растворов fa < 1. В сильно разбавленных растворах fa 1.
 fa зависит от : 1. концентрации раствора а) С , fa б) С 0, fa 1. 2. природы иона (заряд и радиус): Z , fa ; r , fa , если Z = cоnst; 3. температуры: Т , fa 4. природа растворителя ( , ) 5. ионной силы раствора (I ): I , fa
fa зависит от : 1. концентрации раствора а) С , fa б) С 0, fa 1. 2. природы иона (заряд и радиус): Z , fa ; r , fa , если Z = cоnst; 3. температуры: Т , fa 4. природа растворителя ( , ) 5. ионной силы раствора (I ): I , fa
 Ионная сила раствора (I) для разбавленных растворов Сm ~ Cм I биологических жидкостей, например плазмы крови ~0, 15 моль/кг. Изотонический раствор 0, 85% (0, 15 М) р-р Na. Cl , I= 0, 15 моль/кг. Сm (Na. Cl) = 0, 15 моль/ кг
Ионная сила раствора (I) для разбавленных растворов Сm ~ Cм I биологических жидкостей, например плазмы крови ~0, 15 моль/кг. Изотонический раствор 0, 85% (0, 15 М) р-р Na. Cl , I= 0, 15 моль/кг. Сm (Na. Cl) = 0, 15 моль/ кг
 Для разбавленных растворов, в которых I ≤ 0, 01: Предельный з-н Дебая-Хюккеля Для растворов электролитов одинаковозарядных (Mg. SO 4):
Для разбавленных растворов, в которых I ≤ 0, 01: Предельный з-н Дебая-Хюккеля Для растворов электролитов одинаковозарядных (Mg. SO 4):
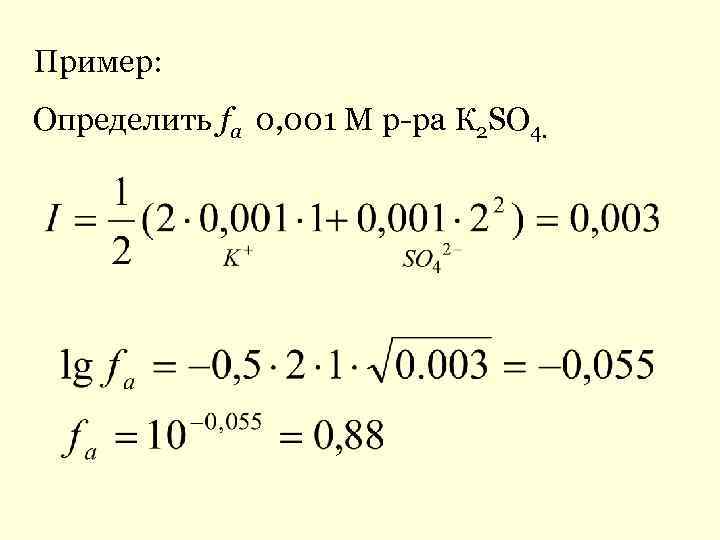 Пример: Определить fa 0, 001 М р-ра К 2 SO 4.
Пример: Определить fa 0, 001 М р-ра К 2 SO 4.
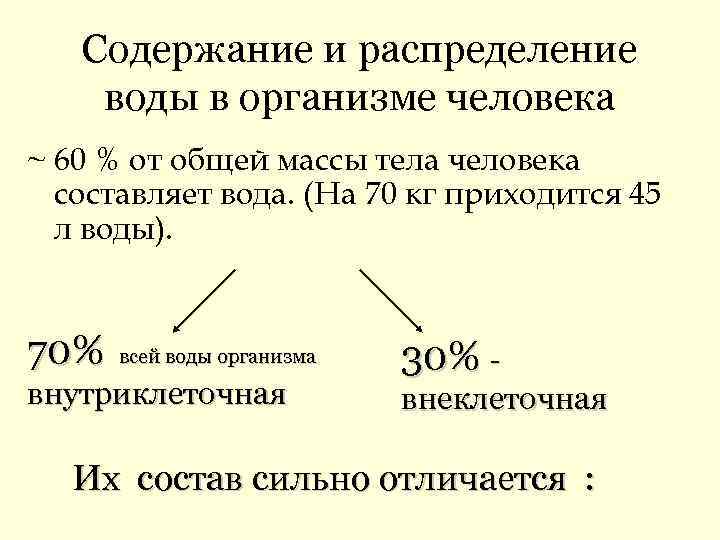 Содержание и распределение воды в организме человека ~ 60 % от общей массы тела человека составляет вода. (На 70 кг приходится 45 л воды). 70% всей воды организма внутриклеточная 30% внеклеточная Их состав сильно отличается :
Содержание и распределение воды в организме человека ~ 60 % от общей массы тела человека составляет вода. (На 70 кг приходится 45 л воды). 70% всей воды организма внутриклеточная 30% внеклеточная Их состав сильно отличается :
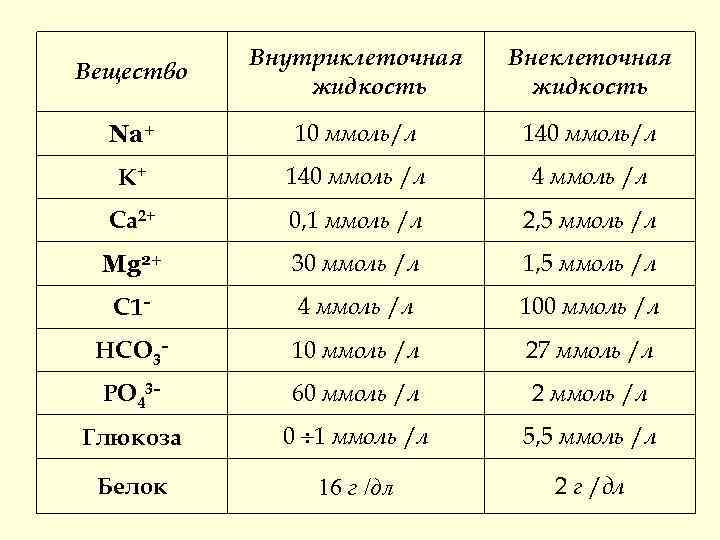 Вещество Внутриклеточная жидкость Внеклеточная жидкость Na+ 10 ммоль/л 140 ммоль/л К+ 140 ммоль /л 4 ммоль /л Са 2+ 0, 1 ммоль /л 2, 5 ммоль /л Mg 2+ 30 ммоль /л 1, 5 ммоль /л С 1– 4 ммоль /л 100 ммоль /л НСО 3– 10 ммоль /л 27 ммоль /л РO 43– 60 ммоль /л 2 ммоль /л Глюкоза 0 ¸ 1 ммоль /л 5, 5 ммоль /л Белок 16 г /дл 2 г /дл
Вещество Внутриклеточная жидкость Внеклеточная жидкость Na+ 10 ммоль/л 140 ммоль/л К+ 140 ммоль /л 4 ммоль /л Са 2+ 0, 1 ммоль /л 2, 5 ммоль /л Mg 2+ 30 ммоль /л 1, 5 ммоль /л С 1– 4 ммоль /л 100 ммоль /л НСО 3– 10 ммоль /л 27 ммоль /л РO 43– 60 ммоль /л 2 ммоль /л Глюкоза 0 ¸ 1 ммоль /л 5, 5 ммоль /л Белок 16 г /дл 2 г /дл
 Внеклеточная жидкость (30%) Внутрисосудистая (7%) Межклеточная тканевая (23 %) Их состав почти одинаков, разница лишь в содержании белков. ( больше белка во внутрисосудистой жидкости)
Внеклеточная жидкость (30%) Внутрисосудистая (7%) Межклеточная тканевая (23 %) Их состав почти одинаков, разница лишь в содержании белков. ( больше белка во внутрисосудистой жидкости)
 Гидролиз – это реакция обменного разложения веществ водой. • Частицы растворенного вещества в воде окружены гидратной оболочкой. В некоторых случаях это приводит к химическому взаимодействию с образованием новых веществ, к реакции гидролиза. • hydro – вода, lysis - распад
Гидролиз – это реакция обменного разложения веществ водой. • Частицы растворенного вещества в воде окружены гидратной оболочкой. В некоторых случаях это приводит к химическому взаимодействию с образованием новых веществ, к реакции гидролиза. • hydro – вода, lysis - распад
 Гидролиз Органических Неорганических веществ Солей
Гидролиз Органических Неорганических веществ Солей
 Гидролиз солей • Сущность гидролиза сводится к обменному химическому взаимодействию катионов или анионов соли с молекулами воды. В результате образуется слабый электролит. • Любая соль – это продукт взаимодействия основания с кислотой. В зависимости от силы основания и кислоты выделяют 4 типа солей.
Гидролиз солей • Сущность гидролиза сводится к обменному химическому взаимодействию катионов или анионов соли с молекулами воды. В результате образуется слабый электролит. • Любая соль – это продукт взаимодействия основания с кислотой. В зависимости от силы основания и кислоты выделяют 4 типа солей.
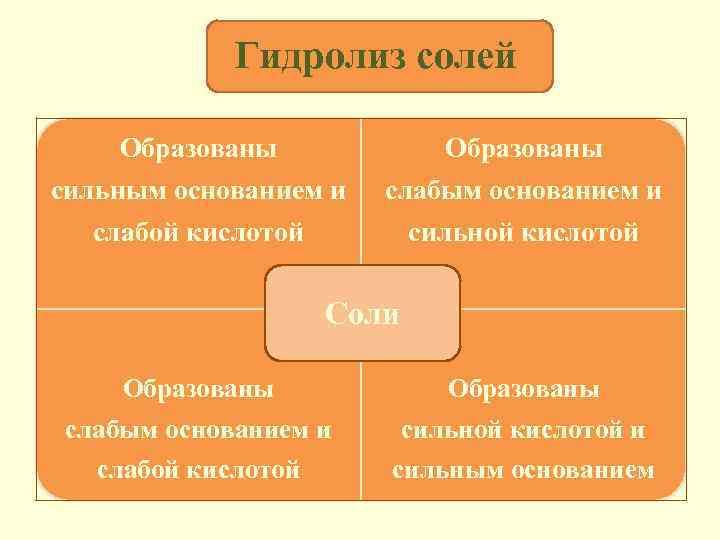 Гидролиз солей Образованы сильным основанием и слабой кислотой слабым основанием и сильной кислотой Соли Образованы слабым основанием и слабой кислотой сильной кислотой и сильным основанием
Гидролиз солей Образованы сильным основанием и слабой кислотой слабым основанием и сильной кислотой Соли Образованы слабым основанием и слабой кислотой сильной кислотой и сильным основанием
 Гидролиз солей, образованных основанием и слабой кислотой : Na 2 S H 2 O = Na+ = OH─ сильным + S 2─ + H 2 O = OH ─ + HS─ Na 2 S + H 2 O = Na. OH + Na. HS Характер среды – щелочная, избыток гидроксиданионов.
Гидролиз солей, образованных основанием и слабой кислотой : Na 2 S H 2 O = Na+ = OH─ сильным + S 2─ + H 2 O = OH ─ + HS─ Na 2 S + H 2 O = Na. OH + Na. HS Характер среды – щелочная, избыток гидроксиданионов.
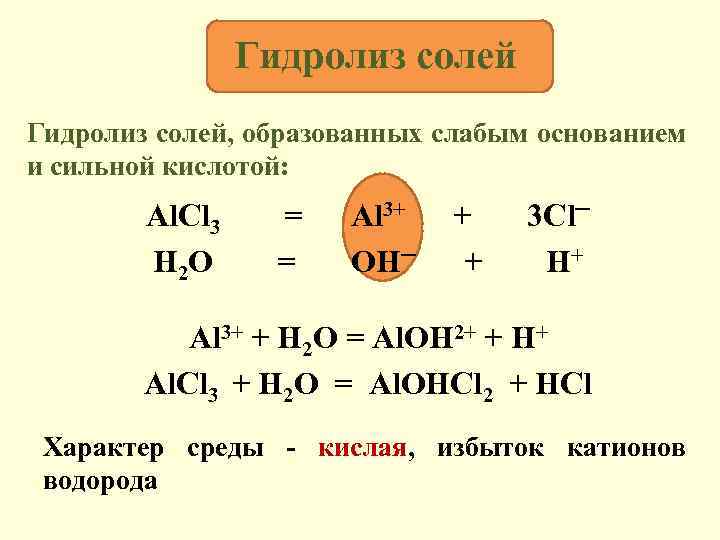 Гидролиз солей, образованных слабым основанием и сильной кислотой: Al. Cl 3 H 2 O = = Al 3+ OH─ + + 3 Cl─ H+ Al 3+ + H 2 O = Al. OH 2+ + H+ Al. Cl 3 + H 2 O = Al. OHCl 2 + HCl Характер среды - кислая, избыток катионов водорода
Гидролиз солей, образованных слабым основанием и сильной кислотой: Al. Cl 3 H 2 O = = Al 3+ OH─ + + 3 Cl─ H+ Al 3+ + H 2 O = Al. OH 2+ + H+ Al. Cl 3 + H 2 O = Al. OHCl 2 + HCl Характер среды - кислая, избыток катионов водорода
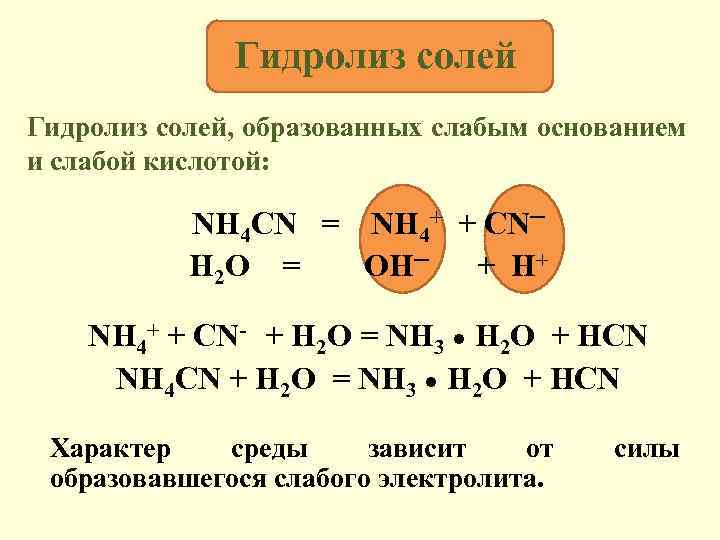 Гидролиз солей, образованных слабым основанием и слабой кислотой: NH 4 CN = NH 4+ + CN─ H 2 O = OH─ + H+ NH 4+ + CN- + H 2 O = NH 3 ● H 2 O + HCN NH 4 CN + H 2 O = NH 3 ● H 2 O + HCN Характер среды зависит от образовавшегося слабого электролита. силы
Гидролиз солей, образованных слабым основанием и слабой кислотой: NH 4 CN = NH 4+ + CN─ H 2 O = OH─ + H+ NH 4+ + CN- + H 2 O = NH 3 ● H 2 O + HCN NH 4 CN + H 2 O = NH 3 ● H 2 O + HCN Характер среды зависит от образовавшегося слабого электролита. силы
 Гидролиз солей Необратимый гидролиз солей, образованных слабым основанием и слабой кислотой: Например, соли, которые нельзя получить реакцией обмена между водными растворами двух солей (в ТР – разлагаются в водной среде) Fe 2(CO 3)3 2 Fe. Cl 3 + 3 Na 2 CO 3 + 3 H 2 O =2 Fe(OH)3↓ +3 CO 2↑+ 6 Na. Cl Fe 2(CO 3)3 + 3 H 2 O = 2 Fe(OH)3↓ +3 CO 2↑ Реакция между двумя растворами (Fe. Cl 3 и Na 2 CO 3) будет необратимой, а карбонат железа (+3) не образуется.
Гидролиз солей Необратимый гидролиз солей, образованных слабым основанием и слабой кислотой: Например, соли, которые нельзя получить реакцией обмена между водными растворами двух солей (в ТР – разлагаются в водной среде) Fe 2(CO 3)3 2 Fe. Cl 3 + 3 Na 2 CO 3 + 3 H 2 O =2 Fe(OH)3↓ +3 CO 2↑+ 6 Na. Cl Fe 2(CO 3)3 + 3 H 2 O = 2 Fe(OH)3↓ +3 CO 2↑ Реакция между двумя растворами (Fe. Cl 3 и Na 2 CO 3) будет необратимой, а карбонат железа (+3) не образуется.
 Гидролиз солей, образованных основанием и сильной кислотой: сильным KCl = K+ + Cl. Слабых ионов нет, гидролиз не идет, среда нейтральная.
Гидролиз солей, образованных основанием и сильной кислотой: сильным KCl = K+ + Cl. Слабых ионов нет, гидролиз не идет, среда нейтральная.
 Гидролиз солей Соли, не подвергающиеся гидролизу Соли, подвергающиеся гидролизу Обратимо, со смещением равновесия Влево Нерастворимые соли и соли, обр. Со + Ск Со + Сл. к Сл. о + Ск Гидролиз по аниону; Среда раствора щелочная (р. Н >7) Гидролиз по катиону; Среда раствора кислотная (р. Н<7) Необратимо Вправо Сл. о + Сл. к Гидролиз по катиону и аниону; Среда раствора зависит от константы диссоциации образующихся при гидролизе основания и кислоты.
Гидролиз солей Соли, не подвергающиеся гидролизу Соли, подвергающиеся гидролизу Обратимо, со смещением равновесия Влево Нерастворимые соли и соли, обр. Со + Ск Со + Сл. к Сл. о + Ск Гидролиз по аниону; Среда раствора щелочная (р. Н >7) Гидролиз по катиону; Среда раствора кислотная (р. Н<7) Необратимо Вправо Сл. о + Сл. к Гидролиз по катиону и аниону; Среда раствора зависит от константы диссоциации образующихся при гидролизе основания и кислоты.
 Гидролиз солей Условия смещения реакций обратимого гидролиза (согласно принципу Ле Шателье). Усилить гидролиз соли можно следующими способами: 1. Добавить воды (уменьшить концентрацию раствора; 2. Нагреть раствор; 3. Связать один из продуктов гидролиза в труднорастворимое соединение или удалить один из продуктов в газовую фазу.
Гидролиз солей Условия смещения реакций обратимого гидролиза (согласно принципу Ле Шателье). Усилить гидролиз соли можно следующими способами: 1. Добавить воды (уменьшить концентрацию раствора; 2. Нагреть раствор; 3. Связать один из продуктов гидролиза в труднорастворимое соединение или удалить один из продуктов в газовую фазу.
 Гидролиз Роль гидролиза: В природе: преобразование земной коры; обеспечение слабощелочной среды морской воды. В народном хозяйстве: порча производственного оборудования; выработка из непищевого сырья ценных продуктов (бумага, мыло, спирт, глюкоза, белковые дрожжи); очистка промышленных стоков и питьевой воды; подготовка тканей к окрашиванию; известкование почв. В повседневной жизни: стирка; мытье посуды; умывание с мылом; процессы пищеварения.
Гидролиз Роль гидролиза: В природе: преобразование земной коры; обеспечение слабощелочной среды морской воды. В народном хозяйстве: порча производственного оборудования; выработка из непищевого сырья ценных продуктов (бумага, мыло, спирт, глюкоза, белковые дрожжи); очистка промышленных стоков и питьевой воды; подготовка тканей к окрашиванию; известкование почв. В повседневной жизни: стирка; мытье посуды; умывание с мылом; процессы пищеварения.
 Гетерогенные ионные равновесия М+ + А – МА(т) • МА(т) М+ + А– • Для малорастворимых сильных электролитов: • Kс = [M+][A–] = ПР(МА) (произведение растворимости) В общем виде: Мх. Ау(т) х Ма+ + у Аb– Тогда ПР = [Ma+]x [Ab–]y ПР = const при T = const ПР = f(T) 67
Гетерогенные ионные равновесия М+ + А – МА(т) • МА(т) М+ + А– • Для малорастворимых сильных электролитов: • Kс = [M+][A–] = ПР(МА) (произведение растворимости) В общем виде: Мх. Ау(т) х Ма+ + у Аb– Тогда ПР = [Ma+]x [Ab–]y ПР = const при T = const ПР = f(T) 67
![Растворимость (L), моль/л Мх. Ау(т) х Ма+ + у Аb– [Ma+] = x L; Растворимость (L), моль/л Мх. Ау(т) х Ма+ + у Аb– [Ma+] = x L;](https://present5.com/presentation/3/-43958340_132542874.pdf-img/-43958340_132542874.pdf-67.jpg) Растворимость (L), моль/л Мх. Ау(т) х Ма+ + у Аb– [Ma+] = x L; [Ab–] = y L ПР(Мх. Ау) = (x L)x (y L)y = xx yy Lx+y 68
Растворимость (L), моль/л Мх. Ау(т) х Ма+ + у Аb– [Ma+] = x L; [Ab–] = y L ПР(Мх. Ау) = (x L)x (y L)y = xx yy Lx+y 68
 Задача Рассчитать растворимость сульфата серебра, если ПР(Ag 2 SO 4) = 1, 2. 10– 5 • Ag 2 SO 4(т) 2 Ag+ + SO 42– L 2 L L • ПР = [Ag+ ]2 [SO 42–] = (2 L)2 L = 4 L 3 69
Задача Рассчитать растворимость сульфата серебра, если ПР(Ag 2 SO 4) = 1, 2. 10– 5 • Ag 2 SO 4(т) 2 Ag+ + SO 42– L 2 L L • ПР = [Ag+ ]2 [SO 42–] = (2 L)2 L = 4 L 3 69
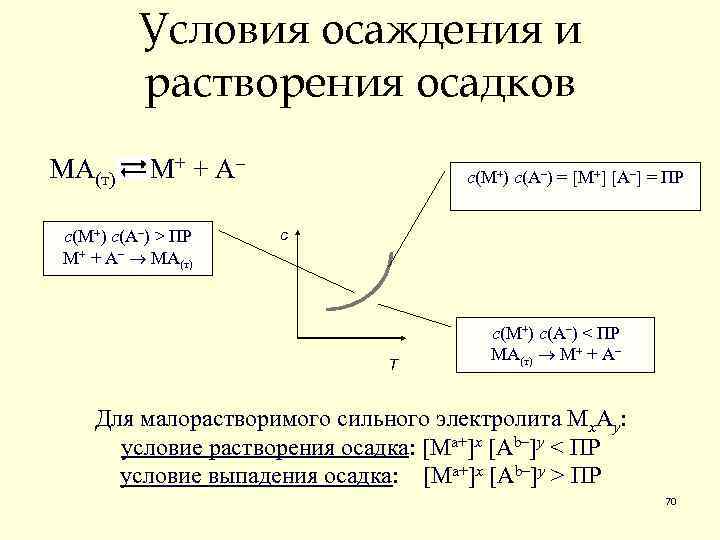 Условия осаждения и растворения осадков МА(т) М+ + А – с(М+) с(А–) > ПР М+ + А– МА(т) с(М+) с(А–) = [M+] [А–] = ПР с Т с(М+) с(А–) < ПР МА(т) М+ + А– Для малорастворимого сильного электролита Мх. Ay условие растворения осадка: [Ma+]x [Ab–]y < ПР условие выпадения осадка: [Ma+]x [Ab–]y > ПР 70
Условия осаждения и растворения осадков МА(т) М+ + А – с(М+) с(А–) > ПР М+ + А– МА(т) с(М+) с(А–) = [M+] [А–] = ПР с Т с(М+) с(А–) < ПР МА(т) М+ + А– Для малорастворимого сильного электролита Мх. Ay условие растворения осадка: [Ma+]x [Ab–]y < ПР условие выпадения осадка: [Ma+]x [Ab–]y > ПР 70
 Введение одноименного иона Мх. Ау(т) х Ма+ + у Аb– Увеличение с(Ма+) или с(Аb–) Сдвиг равновесия в сторону образования осадка 71
Введение одноименного иона Мх. Ау(т) х Ма+ + у Аb– Увеличение с(Ма+) или с(Аb–) Сдвиг равновесия в сторону образования осадка 71
 Удаление одноименного иона Мх. Ау(т) х Ма+ + у Аb– Уменьшение с(Ма+) или с(Аb–) Сдвиг равновесия в сторону растворения осадка 72
Удаление одноименного иона Мх. Ау(т) х Ма+ + у Аb– Уменьшение с(Ма+) или с(Аb–) Сдвиг равновесия в сторону растворения осадка 72
 Удаление одноименного иона • Связывание в виде менее растворимого вещества (осадок Ag. Cl осадок Ag. I) • Связывание в виде комплексного иона (осадок Pb. SO 4 [Pb(OH)4]2–) • Перевод в другую форму (осадок Cr. O 4 2– Cr 2 O 72–) 73
Удаление одноименного иона • Связывание в виде менее растворимого вещества (осадок Ag. Cl осадок Ag. I) • Связывание в виде комплексного иона (осадок Pb. SO 4 [Pb(OH)4]2–) • Перевод в другую форму (осадок Cr. O 4 2– Cr 2 O 72–) 73
 В каком минимальном объеме раствора можно растворить 1 г гипса? • Условие задачи • • V(H 2 O) = ? m(Ca. SO 4. 2 H 2 O) = 1 г ПР(Ca. SO 4) = 4. 10– 5 M(Ca. SO 4. 2 H 2 O) = 172 г/моль • Уравнение фазового равновесия • Са 2+ + SО 42– ПР(Ca. SO 4) = [Ca 2+] [SO 42–] = c 2 Ca. SO 4(т) __ V(раствора) = n / c = m / (M c) = m / (M ПР) ~ 0, 920 л 74
В каком минимальном объеме раствора можно растворить 1 г гипса? • Условие задачи • • V(H 2 O) = ? m(Ca. SO 4. 2 H 2 O) = 1 г ПР(Ca. SO 4) = 4. 10– 5 M(Ca. SO 4. 2 H 2 O) = 172 г/моль • Уравнение фазового равновесия • Са 2+ + SО 42– ПР(Ca. SO 4) = [Ca 2+] [SO 42–] = c 2 Ca. SO 4(т) __ V(раствора) = n / c = m / (M c) = m / (M ПР) ~ 0, 920 л 74
 Выпадет ли осадок при сливании равных объемов миллимолярных растворов нитрата серебра(I) и хлорида натрия? c 0(Ag. NO 3) = c 0(Na. Cl) = 1. 10– 3 моль/л V(p. Ag. NO 3) = V(p. Na. Cl) ПР(Ag. Cl) = 1, 78 10– 10 Для малорастворимого сильного электролита Мх. Ay условие выпадения осадка: [Ma+]x [Ab–]y > ПР После смешивания растворов: c(Ag+) = c 0(Ag+) V(p. Ag. NO 3) / (V(p. Ag. NO 3) + V(p. Na. Cl)) = = 1/2 c 0(Ag+) = 1/2 c 0(Ag. NO 3) c(Cl–) = 1/2 c 0(Na. Cl) 1 2 c 0(Ag. NO 3) 1/2 c 0(Na. Cl) = 2, 5 10– 7 > ПР(Ag. Cl) Осадок выпадет 75
Выпадет ли осадок при сливании равных объемов миллимолярных растворов нитрата серебра(I) и хлорида натрия? c 0(Ag. NO 3) = c 0(Na. Cl) = 1. 10– 3 моль/л V(p. Ag. NO 3) = V(p. Na. Cl) ПР(Ag. Cl) = 1, 78 10– 10 Для малорастворимого сильного электролита Мх. Ay условие выпадения осадка: [Ma+]x [Ab–]y > ПР После смешивания растворов: c(Ag+) = c 0(Ag+) V(p. Ag. NO 3) / (V(p. Ag. NO 3) + V(p. Na. Cl)) = = 1/2 c 0(Ag+) = 1/2 c 0(Ag. NO 3) c(Cl–) = 1/2 c 0(Na. Cl) 1 2 c 0(Ag. NO 3) 1/2 c 0(Na. Cl) = 2, 5 10– 7 > ПР(Ag. Cl) Осадок выпадет 75


