Медицинская генетика.ppt
- Количество слайдов: 73

 МЕДИЦИНСКАЯ ГЕНЕТИКА
МЕДИЦИНСКАЯ ГЕНЕТИКА
 ПЛАН ЛЕКЦИИ • Значение медицинской генетики для врача. • Особенности человека как объекта генетических исследований. • Методы изучения генетики человека: – – – – клинико-генеалогический цитогенетический биохимический популяционно-статистический близнецовый метод биологического моделирования методы генетики соматических клеток дерматоглифический анализ • Методы пренатальной диагностики наследственных болезней.
ПЛАН ЛЕКЦИИ • Значение медицинской генетики для врача. • Особенности человека как объекта генетических исследований. • Методы изучения генетики человека: – – – – клинико-генеалогический цитогенетический биохимический популяционно-статистический близнецовый метод биологического моделирования методы генетики соматических клеток дерматоглифический анализ • Методы пренатальной диагностики наследственных болезней.
 У Бернарда Шоу есть выражение: «Профессия есть заговор непросвещённых» Это в первую очередь можно отнести к генетике. Медицинская генетика, восстановленная в своих правах лишь 3 десятилетия тому назад, пока ещё не заняла в умах и в профессиональной деятельности большинства врачей того места, которое ей принадлежит по праву.
У Бернарда Шоу есть выражение: «Профессия есть заговор непросвещённых» Это в первую очередь можно отнести к генетике. Медицинская генетика, восстановленная в своих правах лишь 3 десятилетия тому назад, пока ещё не заняла в умах и в профессиональной деятельности большинства врачей того места, которое ей принадлежит по праву.
 Однако, это настоятельно необходимо. Если в 1956 году было известно 700 наследственных форм болезней, то в настоящее время одних только генных заболеваний насчитывается более 3, 5 тысяч, которые встречаются с частотой 1%. • Хромосомных болезней известно около 200 с частотой встречаемости 0, 5%. • Врождённые пороки с хорошо выраженной генетической природой встречаются в 2%. Болезни со значительной генетической компонентой, но проявляющиеся в позднем возрасте встречаются с частотой 1%.
Однако, это настоятельно необходимо. Если в 1956 году было известно 700 наследственных форм болезней, то в настоящее время одних только генных заболеваний насчитывается более 3, 5 тысяч, которые встречаются с частотой 1%. • Хромосомных болезней известно около 200 с частотой встречаемости 0, 5%. • Врождённые пороки с хорошо выраженной генетической природой встречаются в 2%. Болезни со значительной генетической компонентой, но проявляющиеся в позднем возрасте встречаются с частотой 1%.
 Суммируя всё это, мы получаем 5%, что составляет генетический груз или груз наследственной патологии. Большая часть генетических дефектов элиминируется на ранних стадиях развития. Ежегодно этот список пополняется в среднем описанием ещё 100 новых форм.
Суммируя всё это, мы получаем 5%, что составляет генетический груз или груз наследственной патологии. Большая часть генетических дефектов элиминируется на ранних стадиях развития. Ежегодно этот список пополняется в среднем описанием ещё 100 новых форм.
 • По приблизительным расчётам в мире рождается в год более 2 млн. детей с тяжёлыми формами наследственных болезней. • Наследственные болезни встречаются в практической деятельности врача любой специальности, так как у 11 -16 % больных поступающих в педиатрические отделения клиник диагностируют генетические заболевания.
• По приблизительным расчётам в мире рождается в год более 2 млн. детей с тяжёлыми формами наследственных болезней. • Наследственные болезни встречаются в практической деятельности врача любой специальности, так как у 11 -16 % больных поступающих в педиатрические отделения клиник диагностируют генетические заболевания.
 • В популяции человека спонтанные аборты составляют 50% всех зачатий, мертворождения – 3%, ранняя детская смертность – 2%, 20% людей не вступают в брак, 10% браков бесплодны. • Таким образом, 75% людей не вносят свой вклад в генофонд будущих поколений. • Для мыслящего врача генетические представления могут быть «путеводной звездой» как в диагностике, так и в лечении многих заболеваний.
• В популяции человека спонтанные аборты составляют 50% всех зачатий, мертворождения – 3%, ранняя детская смертность – 2%, 20% людей не вступают в брак, 10% браков бесплодны. • Таким образом, 75% людей не вносят свой вклад в генофонд будущих поколений. • Для мыслящего врача генетические представления могут быть «путеводной звездой» как в диагностике, так и в лечении многих заболеваний.
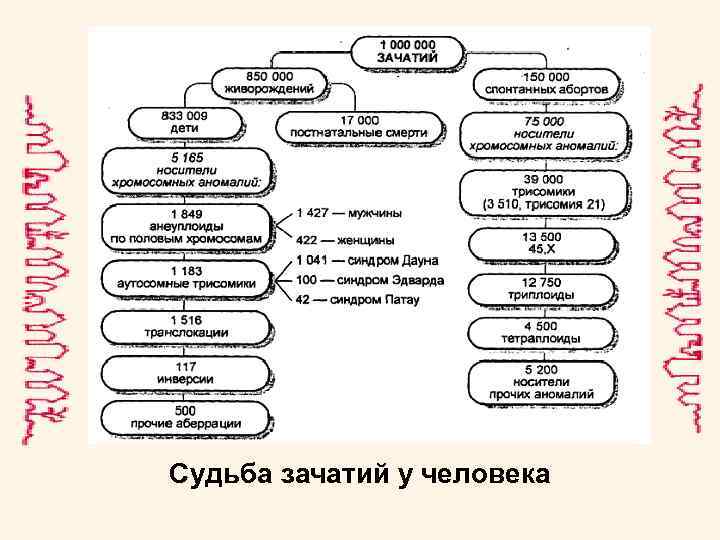 Судьба зачатий у человека
Судьба зачатий у человека
 ЧЕЛОВЕК КАК СПЕЦИФИЧЕСКИЙ ОБЪЕКТ ГЕНЕТИЧЕСКОГО АНАЛИЗА Генетика человека изучает закономерности наследования нормальных и патологических признаков и зависимость их проявления от генотипа и факторов внешней среды.
ЧЕЛОВЕК КАК СПЕЦИФИЧЕСКИЙ ОБЪЕКТ ГЕНЕТИЧЕСКОГО АНАЛИЗА Генетика человека изучает закономерности наследования нормальных и патологических признаков и зависимость их проявления от генотипа и факторов внешней среды.
 Задачами медицинской генетики являются • Изучение патогенеза, клиники, диагностики, лечения и профилактики наследственных болезней человека. • Исследование механизмов наследственной предрасположенности и врожденной резистентности к мультифакториальным заболеваниям. • Разработка генетических аспектов иммунитета, аллергии, трансплантологии, канцерогенеза, генной инженерии и другие.
Задачами медицинской генетики являются • Изучение патогенеза, клиники, диагностики, лечения и профилактики наследственных болезней человека. • Исследование механизмов наследственной предрасположенности и врожденной резистентности к мультифакториальным заболеваниям. • Разработка генетических аспектов иммунитета, аллергии, трансплантологии, канцерогенеза, генной инженерии и другие.
 • • • Изучение генетики человека связано с рядом особенностей и объективных трудностей: Сложный кариотип. Позднее половое созревание и редкая смена поколений. Малое число потомков. Невозможность экспериментирования. Невозможность создания одинаковых условий жизни.
• • • Изучение генетики человека связано с рядом особенностей и объективных трудностей: Сложный кариотип. Позднее половое созревание и редкая смена поколений. Малое число потомков. Невозможность экспериментирования. Невозможность создания одинаковых условий жизни.
 Несмотря на указанные сложности, генетика человека изучена на сегодня лучше, чем генетика многих других организмов (например, млекопитающих). Этому способствовали растущие потребности медицины и разнообразия современных методов исследования.
Несмотря на указанные сложности, генетика человека изучена на сегодня лучше, чем генетика многих других организмов (например, млекопитающих). Этому способствовали растущие потребности медицины и разнообразия современных методов исследования.
 С целью обследования больных и решения вопросов патогенеза наследственных заболеваний в медицинской генетике широко применяются обще-клинические методы: • электрокардиография, электроэнцефалография • электромиография • биохимические анализы биологических жидкостей • биопсия тканей и другие Однако, имеется целый ряд специфических методов, с помощью которых можно изучить вопросы возникновения, развития, распространения, механизмы передачи из
С целью обследования больных и решения вопросов патогенеза наследственных заболеваний в медицинской генетике широко применяются обще-клинические методы: • электрокардиография, электроэнцефалография • электромиография • биохимические анализы биологических жидкостей • биопсия тканей и другие Однако, имеется целый ряд специфических методов, с помощью которых можно изучить вопросы возникновения, развития, распространения, механизмы передачи из
 МЕТОДЫ ИССЛЕДОВАНИЯ ГЕНЕТИКИ ЧЕЛОВЕКА Клинико-генеалогический метод • Клинико-генеалогический метод был предложен в конце XIX века Ф. Гальтоном. • Он основан на построении родословных и прослеживании в ряду поколений передачи наследственного признака.
МЕТОДЫ ИССЛЕДОВАНИЯ ГЕНЕТИКИ ЧЕЛОВЕКА Клинико-генеалогический метод • Клинико-генеалогический метод был предложен в конце XIX века Ф. Гальтоном. • Он основан на построении родословных и прослеживании в ряду поколений передачи наследственного признака.
 Метод позволяет установить: • • • Является ли данный признак наследственным (по проявлению его у родственников). Тип и характер наследования (доминантный, рецессивный или аутосомный). Зиготность лиц родословной (гомо- или гетерозиготность). Пенетрантность гена (частота его проявления). Вероятность рождения ребёнка с наследственной патологией (генетический риск).
Метод позволяет установить: • • • Является ли данный признак наследственным (по проявлению его у родственников). Тип и характер наследования (доминантный, рецессивный или аутосомный). Зиготность лиц родословной (гомо- или гетерозиготность). Пенетрантность гена (частота его проявления). Вероятность рождения ребёнка с наследственной патологией (генетический риск).
 Этапы генеалогического анализа • • • Сбор данных обо всех родственниках обследуемого (анамнез). Построение родословной. Анализ родословной и выводы.
Этапы генеалогического анализа • • • Сбор данных обо всех родственниках обследуемого (анамнез). Построение родословной. Анализ родословной и выводы.
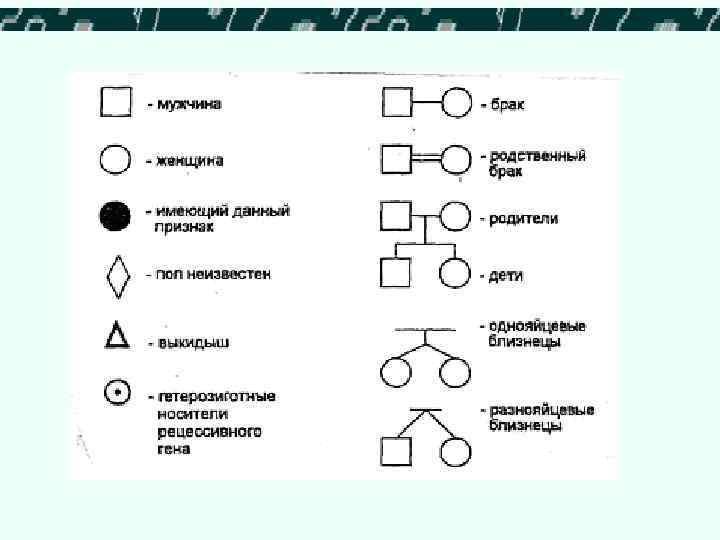
 • Сложность сбора анамнеза заключается в том, что пробанд должен хорошо знать родственников по линии матери и отца не менее трёх поколений и состояние их здоровья. • Основой родословной является пробанд - лицо, с которого начинается исследование семьи. В родословной пробанд помечается знаком .
• Сложность сбора анамнеза заключается в том, что пробанд должен хорошо знать родственников по линии матери и отца не менее трёх поколений и состояние их здоровья. • Основой родословной является пробанд - лицо, с которого начинается исследование семьи. В родословной пробанд помечается знаком .
 Типы наследования Аутосомно-доминантный тип наследования • • • характеризуется следующими признаками: Больные в каждом поколении. Больной ребёнок у больных родителей. Болеют в равной степени мужчины и женщины. Проявление признака (болезни) наблюдается в вертикальной и горизонтальной части родословной. Вероятность наследования 100% (если хотя бы один родитель гомозиготен), 75% (если оба родителя гетерозиготны), 50% (если один родитель гетерозиготен). Так наследуются у человека полидактилия (шестипалость),
Типы наследования Аутосомно-доминантный тип наследования • • • характеризуется следующими признаками: Больные в каждом поколении. Больной ребёнок у больных родителей. Болеют в равной степени мужчины и женщины. Проявление признака (болезни) наблюдается в вертикальной и горизонтальной части родословной. Вероятность наследования 100% (если хотя бы один родитель гомозиготен), 75% (если оба родителя гетерозиготны), 50% (если один родитель гетерозиготен). Так наследуются у человека полидактилия (шестипалость),
 • При неполном доминировании у потомков будет проявляться промежуточная форма наследования. • При неполной пенетрантности гена больные могут быть не в каждом поколении
• При неполном доминировании у потомков будет проявляться промежуточная форма наследования. • При неполной пенетрантности гена больные могут быть не в каждом поколении
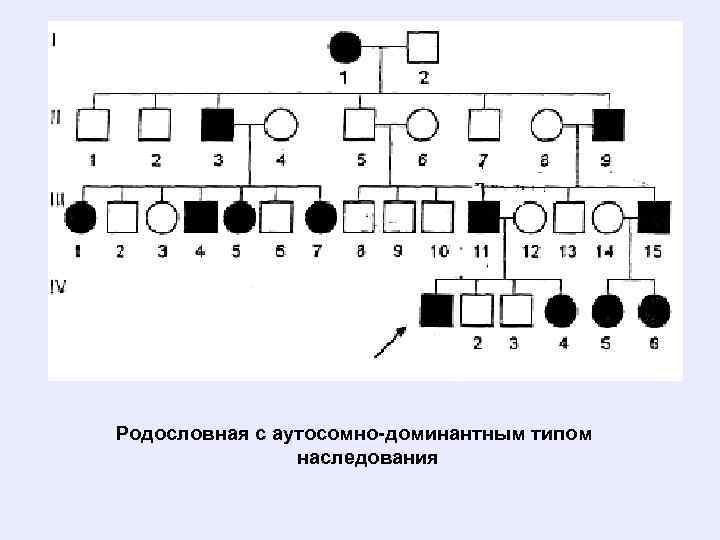 Родословная с аутосомно-доминантным типом наследования
Родословная с аутосомно-доминантным типом наследования
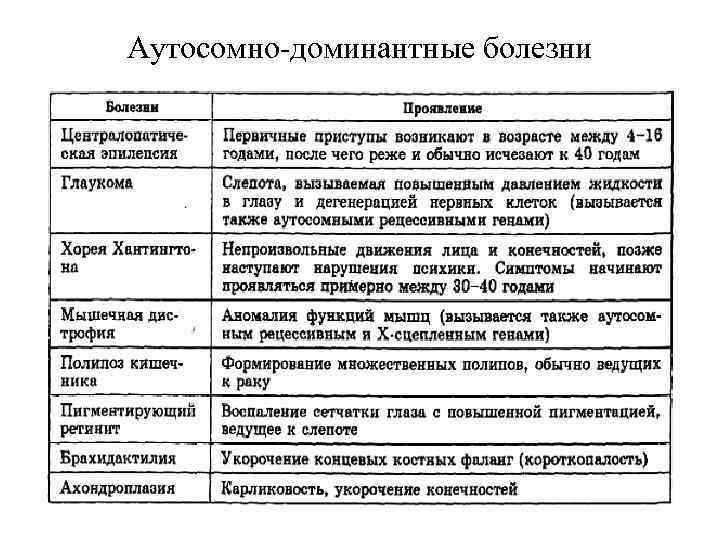 Аутосомно-доминантные болезни
Аутосомно-доминантные болезни
 • • • Аутосомно-рецессивный тип наследования характеризуется следующими признаками: В восходящей части родословной обычно нет больных с аналогичной патологией. Больной ребёнок (гомозигота) рождается у здоровых родителей (гетерозигот). Болеют в равной степени мужчины и женщины. Проявление признака (болезни) наблюдается в горизонтальной части родословной. Вероятность наследования 25% (если оба родителя гетерозиготны), 50% (если один родитель гетерозиготен, а второй – гомозиготен по рецессивному признаку) и 100% (если оба родителя рецессивны и гомозиготны). Так наследуются у человека фенилкетонурия, серповидно-клеточная анемия, голубой цвет глаз и другие
• • • Аутосомно-рецессивный тип наследования характеризуется следующими признаками: В восходящей части родословной обычно нет больных с аналогичной патологией. Больной ребёнок (гомозигота) рождается у здоровых родителей (гетерозигот). Болеют в равной степени мужчины и женщины. Проявление признака (болезни) наблюдается в горизонтальной части родословной. Вероятность наследования 25% (если оба родителя гетерозиготны), 50% (если один родитель гетерозиготен, а второй – гомозиготен по рецессивному признаку) и 100% (если оба родителя рецессивны и гомозиготны). Так наследуются у человека фенилкетонурия, серповидно-клеточная анемия, голубой цвет глаз и другие
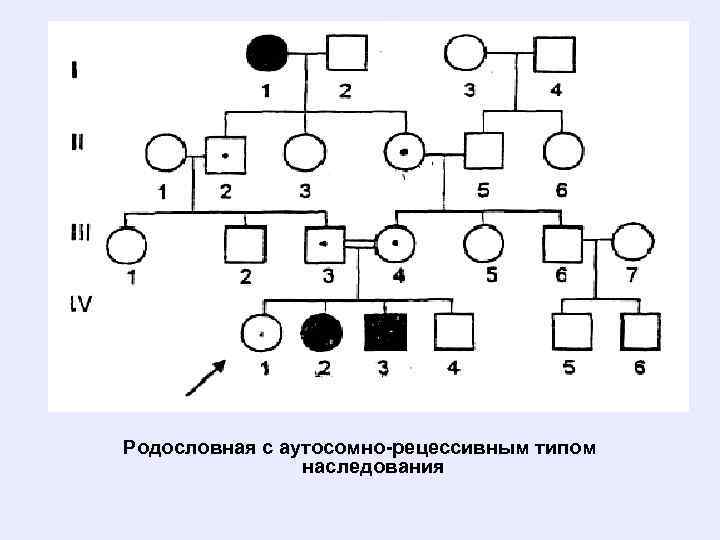 Родословная с аутосомно-рецессивным типом наследования
Родословная с аутосомно-рецессивным типом наследования
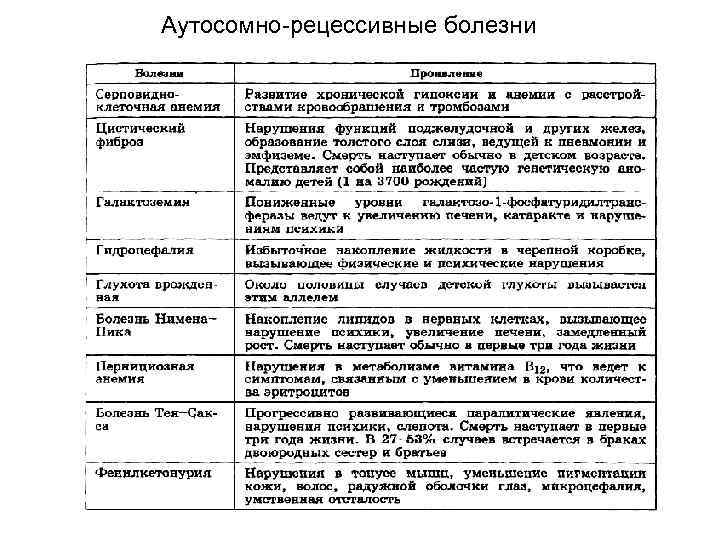 Аутосомно-рецессивные болезни
Аутосомно-рецессивные болезни
 Х-сцепленный рецессивный тип наследования характеризуется следующими признаками: • Больные появляются не в каждом поколении. • Больной ребёнок рождается у здоровых родителей. • Болеют преимущественно мужчины. • Проявление признака (болезни) наблюдается преимущественно в горизонтальной части родословной. • Вероятность наследования - у 25% всех детей, в том числе у 50% мальчиков. Так наследуются у человека гемофилия, дальтонизм, наследственная анемия, мышечная дистрофия и другие.
Х-сцепленный рецессивный тип наследования характеризуется следующими признаками: • Больные появляются не в каждом поколении. • Больной ребёнок рождается у здоровых родителей. • Болеют преимущественно мужчины. • Проявление признака (болезни) наблюдается преимущественно в горизонтальной части родословной. • Вероятность наследования - у 25% всех детей, в том числе у 50% мальчиков. Так наследуются у человека гемофилия, дальтонизм, наследственная анемия, мышечная дистрофия и другие.
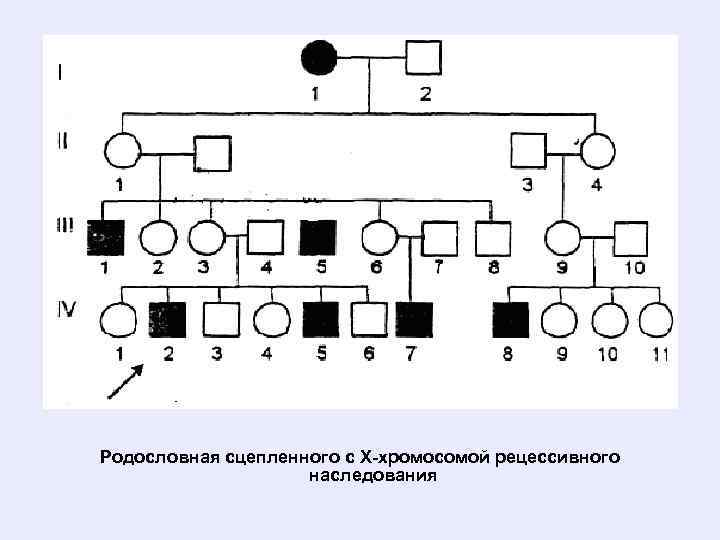 Родословная сцепленного с Х-хромосомой рецессивного наследования
Родословная сцепленного с Х-хромосомой рецессивного наследования
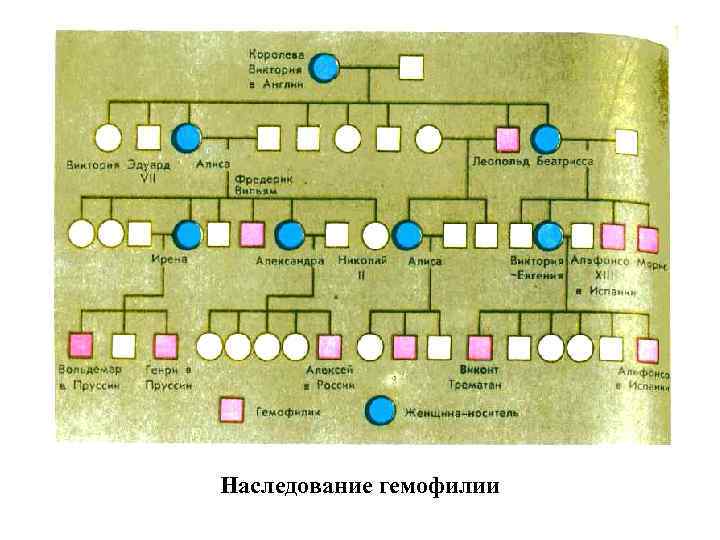 Наследование гемофилии
Наследование гемофилии
 Черепаховая окраска кошки ХВ (ХВ ХВ)– чёрная, Хв (Хв Хв)- рыжая, ХВХв - черепаховая
Черепаховая окраска кошки ХВ (ХВ ХВ)– чёрная, Хв (Хв Хв)- рыжая, ХВХв - черепаховая
 Голандрический тип наследования характеризуется следующими признаками: • • Больные во всех поколениях. Болеют только мужчины. У больного отца больны все его сыновья. Вероятность наследования у мальчиков 100%. Так наследуются у человека некоторые формы ихтиоза, обволошенность наружных слуховых проходов и средних фаланг пальцев, некоторые формы синдактилии (перепонки между пальцами ног) и другие.
Голандрический тип наследования характеризуется следующими признаками: • • Больные во всех поколениях. Болеют только мужчины. У больного отца больны все его сыновья. Вероятность наследования у мальчиков 100%. Так наследуются у человека некоторые формы ихтиоза, обволошенность наружных слуховых проходов и средних фаланг пальцев, некоторые формы синдактилии (перепонки между пальцами ног) и другие.
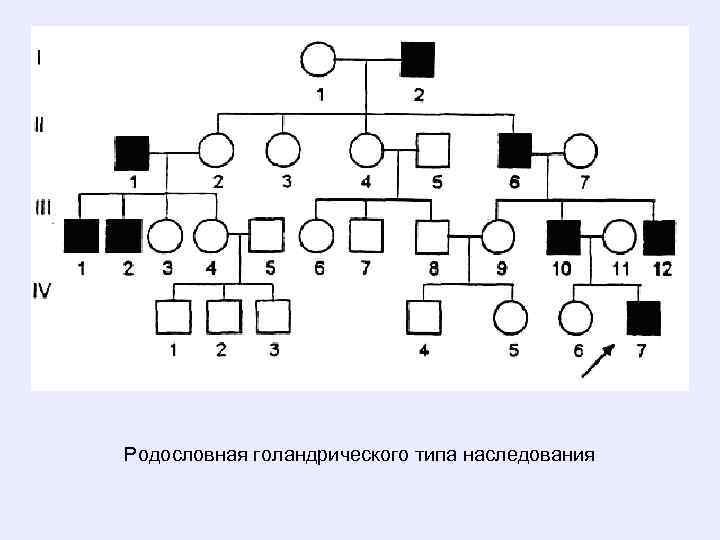 Родословная голандрического типа наследования
Родословная голандрического типа наследования
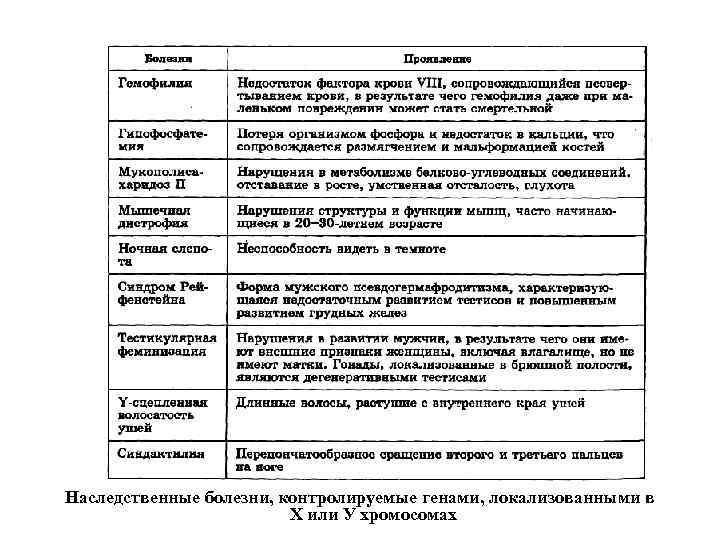 Наследственные болезни, контролируемые генами, локализованными в Х или У хромосомах
Наследственные болезни, контролируемые генами, локализованными в Х или У хромосомах
 ЦИТОГЕНЕТИЧЕСКИЙ МЕТОД основан на микроскопическом исследовании кариотипа Его использование даёт следующие возможности: • Изучать морфологию хромосом и кариотипы, процессы мутагенеза на уровне хромосом и кариотипа. • Определять генетический пол. • Диагностировать различные хромосомные болезни, связанные с изменением числа и структуры хромосом. Например, болезнь Дауна у мальчика: 47, ХУ, 21+; синдром «кошачьего крика» у девочки: 46, ХХ, 5 р-. • В медико-генетическом консультировании – для цели пренатальной диагностики хромосомных болезней, что позволяет путём своевременного прерывания беременности предупредить появление потомства с грубыми нарушениями развития.
ЦИТОГЕНЕТИЧЕСКИЙ МЕТОД основан на микроскопическом исследовании кариотипа Его использование даёт следующие возможности: • Изучать морфологию хромосом и кариотипы, процессы мутагенеза на уровне хромосом и кариотипа. • Определять генетический пол. • Диагностировать различные хромосомные болезни, связанные с изменением числа и структуры хромосом. Например, болезнь Дауна у мальчика: 47, ХУ, 21+; синдром «кошачьего крика» у девочки: 46, ХХ, 5 р-. • В медико-генетическом консультировании – для цели пренатальной диагностики хромосомных болезней, что позволяет путём своевременного прерывания беременности предупредить появление потомства с грубыми нарушениями развития.
 Этапы исследования: • Культивирование клеток человека (чаще лимфоцитов). • Стимуляция митозов фитогемагглютинином (ФГА). • Добавление колхицина (разрушает нити веретена деления) для остановки митоза на стадии метафазы. • Обработка клеток гипотоническим раствором, вследствие чего хромосомы «рассыпаются» и лежат свободно. • Окрашивание хромосом. • Изучение под микроскопом и фотографирование. • Вырезание отдельных хромосом и построение идиограммы.
Этапы исследования: • Культивирование клеток человека (чаще лимфоцитов). • Стимуляция митозов фитогемагглютинином (ФГА). • Добавление колхицина (разрушает нити веретена деления) для остановки митоза на стадии метафазы. • Обработка клеток гипотоническим раствором, вследствие чего хромосомы «рассыпаются» и лежат свободно. • Окрашивание хромосом. • Изучение под микроскопом и фотографирование. • Вырезание отдельных хромосом и построение идиограммы.
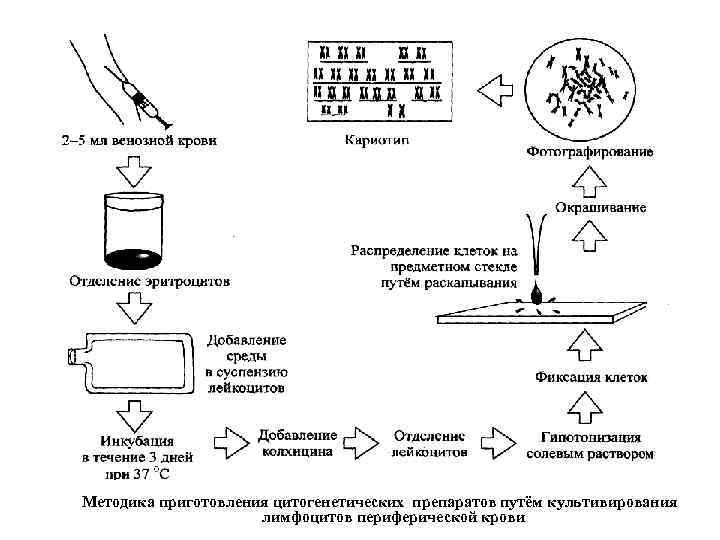 Методика приготовления цитогенетических препаратов путём культивирования лимфоцитов периферической крови
Методика приготовления цитогенетических препаратов путём культивирования лимфоцитов периферической крови
 БИОХИМИЧЕСКИЕ МЕТОДЫ • Биохимические методы направлены на выявление биохимического фенотипа организма. Эти методы позволяют диагностировать наследственные болезни, обусловленные генными мутациями. • Биохимические показатели (первичный белковый продукт гена, накопление патологических метаболитов внутри клетки) отражают сущность болезни более адекватно, чем клинические симптомы.
БИОХИМИЧЕСКИЕ МЕТОДЫ • Биохимические методы направлены на выявление биохимического фенотипа организма. Эти методы позволяют диагностировать наследственные болезни, обусловленные генными мутациями. • Биохимические показатели (первичный белковый продукт гена, накопление патологических метаболитов внутри клетки) отражают сущность болезни более адекватно, чем клинические симптомы.
 С помощью биохимических методов описано более 1000 врождённых болезней обмена веществ. • Наиболее распространёнными среди таких заболеваний являются болезни, связанные с дефектами ферментов, которые устанавливают путём определения содержания в биологических средах (например, моче и крови), продуктов метаболизма, являющихся продуктом функционирования данного белка. Применяют хроматографические, флюорометрические, радиоиммунологические и некоторые другие методы.
С помощью биохимических методов описано более 1000 врождённых болезней обмена веществ. • Наиболее распространёнными среди таких заболеваний являются болезни, связанные с дефектами ферментов, которые устанавливают путём определения содержания в биологических средах (например, моче и крови), продуктов метаболизма, являющихся продуктом функционирования данного белка. Применяют хроматографические, флюорометрические, радиоиммунологические и некоторые другие методы.
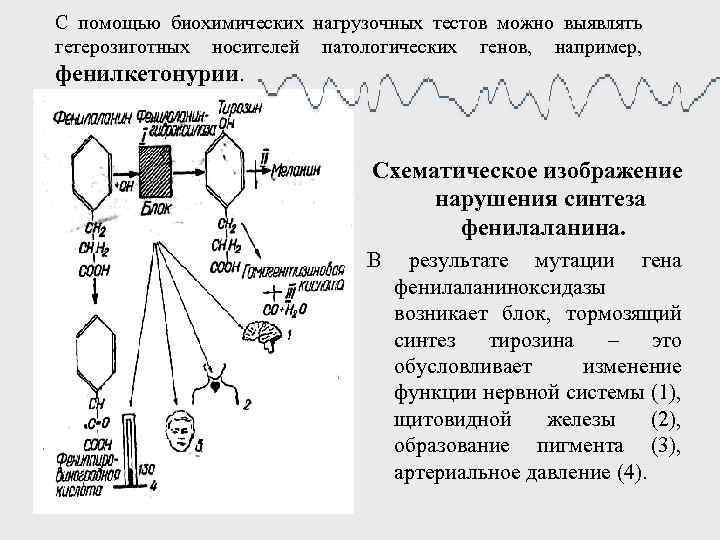 С помощью биохимических нагрузочных тестов можно выявлять гетерозиготных носителей патологических генов, например, фенилкетонурии. Схематическое изображение нарушения синтеза фенилаланина. В результате мутации гена фенилаланиноксидазы возникает блок, тормозящий синтез тирозина – это обусловливает изменение функции нервной системы (1), щитовидной железы (2), образование пигмента (3), артериальное давление (4).
С помощью биохимических нагрузочных тестов можно выявлять гетерозиготных носителей патологических генов, например, фенилкетонурии. Схематическое изображение нарушения синтеза фенилаланина. В результате мутации гена фенилаланиноксидазы возникает блок, тормозящий синтез тирозина – это обусловливает изменение функции нервной системы (1), щитовидной железы (2), образование пигмента (3), артериальное давление (4).
 ПОПУЛЯЦИОННОСТАТИСТИЧЕСКИЙ МЕТОД • Предметом популяционно-статистического метода является изучение частоты генов и генотипов в популяции. • Данным методом изучают наследственные признаки в больших группах населения, в одном или нескольких поколениях. • Сравнительные данные о наследственной патологии в изолятах и крупных городах или странах позволяют получить представление о распространении мутантного гена. • Существенным моментом при использовании этого метода является статистические обработка получаемых данных.
ПОПУЛЯЦИОННОСТАТИСТИЧЕСКИЙ МЕТОД • Предметом популяционно-статистического метода является изучение частоты генов и генотипов в популяции. • Данным методом изучают наследственные признаки в больших группах населения, в одном или нескольких поколениях. • Сравнительные данные о наследственной патологии в изолятах и крупных городах или странах позволяют получить представление о распространении мутантного гена. • Существенным моментом при использовании этого метода является статистические обработка получаемых данных.
 В основе популяционно-статистического метода лежит закон генетического равновесия Харди-Вейнберга, сформулированный в 1908 г. Он отражает закономерность в соответствии с которой при определённых условиях соотношение частоты доминантного гена, его рецессивного аллеля и генотипов в генофонде популяции сохраняется неизменным в ряду поколений этой популяции.
В основе популяционно-статистического метода лежит закон генетического равновесия Харди-Вейнберга, сформулированный в 1908 г. Он отражает закономерность в соответствии с которой при определённых условиях соотношение частоты доминантного гена, его рецессивного аллеля и генотипов в генофонде популяции сохраняется неизменным в ряду поколений этой популяции.
 На основании этого закона, имея данные о частоте встречаемости в популяции рецессивного фенотипа, обусловленного гомозиготным генотипом, можно определить: • Частоту встречаемости указанного рецессивного аллеля в генофонде данного поколения. • Распространив эти сведения на ближайшие поколения, - частоту появления индивидов с рецессивным признаком, а также распространения гетерозиготных носителей рецессивного гена.
На основании этого закона, имея данные о частоте встречаемости в популяции рецессивного фенотипа, обусловленного гомозиготным генотипом, можно определить: • Частоту встречаемости указанного рецессивного аллеля в генофонде данного поколения. • Распространив эти сведения на ближайшие поколения, - частоту появления индивидов с рецессивным признаком, а также распространения гетерозиготных носителей рецессивного гена.
 • Формула Харди Вейнберга полностью применима к идеальной панмиксической (со свободным скрещиванием) популяции, где сохраняется определённое соотношение частот генов в поколениях. • Совместно применение популяционностатистического, клинико-генеалогического и близнецового методов – оптимальный вариант изучения наследственной предрасположенности к какой-либо болезни. Такой подход называется генетикоэпидемиологическим.
• Формула Харди Вейнберга полностью применима к идеальной панмиксической (со свободным скрещиванием) популяции, где сохраняется определённое соотношение частот генов в поколениях. • Совместно применение популяционностатистического, клинико-генеалогического и близнецового методов – оптимальный вариант изучения наследственной предрасположенности к какой-либо болезни. Такой подход называется генетикоэпидемиологическим.
 БЛИЗНЕЦОВЫЙ МЕТОД • Близнецовый метод изучения генетики человека позволяет определить соотносительную роль наследственности и среды в развитии признака, а также даёт возможность оценивать действия на организм некоторых внешних факторов (лечебных препаратов, воспитания, обучения и т. д. ).
БЛИЗНЕЦОВЫЙ МЕТОД • Близнецовый метод изучения генетики человека позволяет определить соотносительную роль наследственности и среды в развитии признака, а также даёт возможность оценивать действия на организм некоторых внешних факторов (лечебных препаратов, воспитания, обучения и т. д. ).
 Фенотипическое сходство между однояйцевыми близнецами
Фенотипическое сходство между однояйцевыми близнецами
 Однако имеется ряд трудностей, связанных со следующими причинами: • Относительно низкой частотой рождения близнецов в популяции (1, 1 – 1, 2% всех рождений, из них 1/3 приходится на монозиготных близнецов, а 2/3 на дизиготных). • Сложностью распознавания монозиготных близнецов, которое проводится на основании сходства генетически детерминированных признаков. Наиболее достоверный критерий монозиготности представляет трансплантационный тест с применением перекрёстной пересадки кожи близнецов.
Однако имеется ряд трудностей, связанных со следующими причинами: • Относительно низкой частотой рождения близнецов в популяции (1, 1 – 1, 2% всех рождений, из них 1/3 приходится на монозиготных близнецов, а 2/3 на дизиготных). • Сложностью распознавания монозиготных близнецов, которое проводится на основании сходства генетически детерминированных признаков. Наиболее достоверный критерий монозиготности представляет трансплантационный тест с применением перекрёстной пересадки кожи близнецов.
 • Процент сходства близнецов по изучаемому признаку называется конкордантностью, а процент различия – дискордантностью. • Для оценки роли наследственности и среды в развитии того или иного признака используют формулу Хольцингера: КМБ% - КДБ% 100% - КДБ%
• Процент сходства близнецов по изучаемому признаку называется конкордантностью, а процент различия – дискордантностью. • Для оценки роли наследственности и среды в развитии того или иного признака используют формулу Хольцингера: КМБ% - КДБ% 100% - КДБ%
 • При значениях Н, приближающихся к нулю, считают, что признак развивается исключительно под действием факторов внешней среды. • При значениях 1 > Н> 0, 7 – признак развивается под действием генетических факторов. • Среднее значение Н (0, 4 > Н> 0, 7 ) свидетельствует о том, что признак развивается под действием факторов внешней среды на фоне генетической предрасположенности.
• При значениях Н, приближающихся к нулю, считают, что признак развивается исключительно под действием факторов внешней среды. • При значениях 1 > Н> 0, 7 – признак развивается под действием генетических факторов. • Среднее значение Н (0, 4 > Н> 0, 7 ) свидетельствует о том, что признак развивается под действием факторов внешней среды на фоне генетической предрасположенности.
 Таблица конкордантности признаков у монозиготных и дизиготных близнецов
Таблица конкордантности признаков у монозиготных и дизиготных близнецов
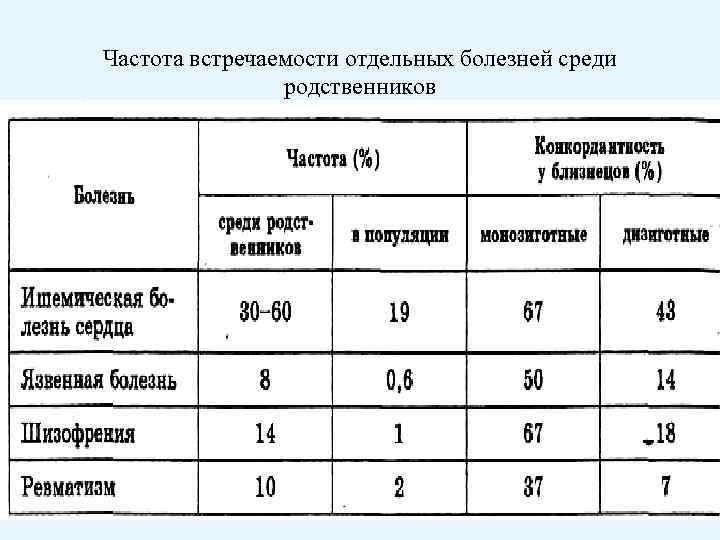 Частота встречаемости отдельных болезней среди родственников
Частота встречаемости отдельных болезней среди родственников
 БИОЛОГИЧЕСКОЕ МОДЕЛИРОВАНИЕ • Биологическое моделирование определенных наследственных аномалий человека можно проводить на мутантных линиях животных, имеющих сходные нарушения. Например, у собак встречается гемофилия, обусловленная рецессивным сцепленным с полом геном, у мышей – незаращение губы и нёба, сходное с аналогичными аномалиями человека, у хомяков и крыс – сахарный диабет, ахондроплазия, мышечная дистрофия и другие.
БИОЛОГИЧЕСКОЕ МОДЕЛИРОВАНИЕ • Биологическое моделирование определенных наследственных аномалий человека можно проводить на мутантных линиях животных, имеющих сходные нарушения. Например, у собак встречается гемофилия, обусловленная рецессивным сцепленным с полом геном, у мышей – незаращение губы и нёба, сходное с аналогичными аномалиями человека, у хомяков и крыс – сахарный диабет, ахондроплазия, мышечная дистрофия и другие.
 Теоретическую основу биологического моделирования в генетике человека даёт закон гомологичных рядов наследственной изменчивости Н. И. Вавилова, согласно которому генетически близкие виды и роды характеризуются сходными рядами наследственной изменчивости.
Теоретическую основу биологического моделирования в генетике человека даёт закон гомологичных рядов наследственной изменчивости Н. И. Вавилова, согласно которому генетически близкие виды и роды характеризуются сходными рядами наследственной изменчивости.
 В настоящее время метод биологического моделирования применяется в основном для изучения мутагенного и тератогенного действия новых лекарственных препаратов перед их клиническими испытаниями и для решения вопросов генной инженерии.
В настоящее время метод биологического моделирования применяется в основном для изучения мутагенного и тератогенного действия новых лекарственных препаратов перед их клиническими испытаниями и для решения вопросов генной инженерии.
 МАТЕМАТИЧЕСКОЕ МОДЕЛИРОВАНИЕ Математическое моделирование – это метод создания и изучения математических моделей. Его применяют для расчета частот генов в популяциях при различных воздействиях и изменениях окружающей среды. Математические методы широко применяются в тех случаях, когда невозможно использование экспериментальных методов (например, анализ большого количества сцепленных генов у человека).
МАТЕМАТИЧЕСКОЕ МОДЕЛИРОВАНИЕ Математическое моделирование – это метод создания и изучения математических моделей. Его применяют для расчета частот генов в популяциях при различных воздействиях и изменениях окружающей среды. Математические методы широко применяются в тех случаях, когда невозможно использование экспериментальных методов (например, анализ большого количества сцепленных генов у человека).
 МЕТОДЫ ГЕНЕТИКИ СОМАТИЧЕСКИХ КЛЕТОК • Методы генетики соматических клеток дают возможность изучать многие вопросы генетики человека в эксперименте. • Для культивирования чаще используют клетки соединительной ткани (фибробласты) и лимфоциты крови. • На искусственных питательных средах можно осуществлять клонирование, т. е. получать потомство одной клетки. Все потомки будут иметь одинаковый генотип (как монозиготные близнецы), что позволяет на клеточном уровне изучать роль генотипа и среды в проявлении признаков. • Можно проводить также селекцию (отбор) клеток с заранее заданными свойствами. Для этого используют селективные питательные среды.
МЕТОДЫ ГЕНЕТИКИ СОМАТИЧЕСКИХ КЛЕТОК • Методы генетики соматических клеток дают возможность изучать многие вопросы генетики человека в эксперименте. • Для культивирования чаще используют клетки соединительной ткани (фибробласты) и лимфоциты крови. • На искусственных питательных средах можно осуществлять клонирование, т. е. получать потомство одной клетки. Все потомки будут иметь одинаковый генотип (как монозиготные близнецы), что позволяет на клеточном уровне изучать роль генотипа и среды в проявлении признаков. • Можно проводить также селекцию (отбор) клеток с заранее заданными свойствами. Для этого используют селективные питательные среды.
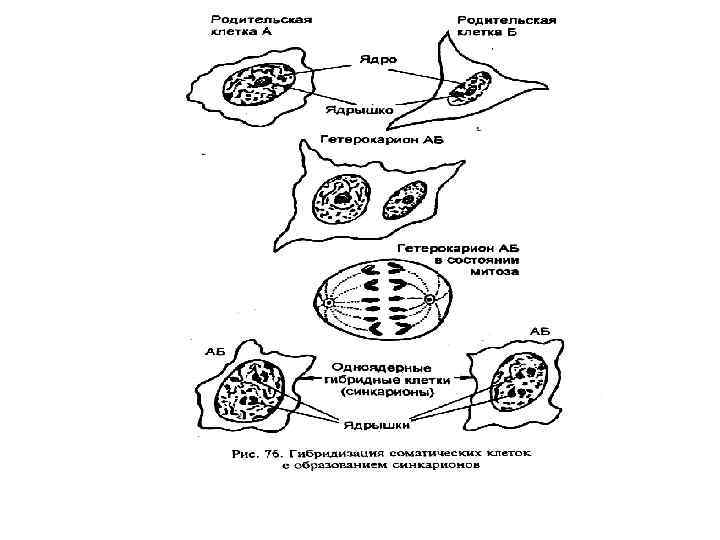
 • Наибольший интерес для генетики человека представляет метод гибридизации клеток. • В смешанной культуре разных типов клеток образуются гетерокарионы – клетки, содержащие два ядра разных клеток в одной цитоплазме. • После митоза из двуядерного гетерокариона образуется две одноядерные клетки, каждая из которых представляет собой синкарион – настоящую гибридную клетку, содержащую хромосомы обоих родительских клеток, т. е. происходит объединение двух геномов.
• Наибольший интерес для генетики человека представляет метод гибридизации клеток. • В смешанной культуре разных типов клеток образуются гетерокарионы – клетки, содержащие два ядра разных клеток в одной цитоплазме. • После митоза из двуядерного гетерокариона образуется две одноядерные клетки, каждая из которых представляет собой синкарион – настоящую гибридную клетку, содержащую хромосомы обоих родительских клеток, т. е. происходит объединение двух геномов.
 • Например, гибридные клетки человека и мыши имеют 43 пары хромосом: 23 от человека и 20 - от мыши. • В дальнейшее происходит постепенное удаление хромосом того организма, клетки которого имеют более медленный темп размножения. У гибридных клеток человека-мыши удаляются хромосомы человека. • В гибридных клетках функционируют хромосомы как человека, так и мыши, гены которых детерминируют синтез соответствующих белков. • Морфологически можно отличить каждую из хромосом ( «дифференциальное окрашивание» ). • Если в гибридной клетке отсутствует какая-либо хромосома и не происходит синтез каких-то белков, то можно предположить, что гены, детерминирующие синтез этих белков, локализованы в ней.
• Например, гибридные клетки человека и мыши имеют 43 пары хромосом: 23 от человека и 20 - от мыши. • В дальнейшее происходит постепенное удаление хромосом того организма, клетки которого имеют более медленный темп размножения. У гибридных клеток человека-мыши удаляются хромосомы человека. • В гибридных клетках функционируют хромосомы как человека, так и мыши, гены которых детерминируют синтез соответствующих белков. • Морфологически можно отличить каждую из хромосом ( «дифференциальное окрашивание» ). • Если в гибридной клетке отсутствует какая-либо хромосома и не происходит синтез каких-то белков, то можно предположить, что гены, детерминирующие синтез этих белков, локализованы в ней.
 Таким образом, этот метод позволяет установить группы сцепления у человека, а используя нехватки и транслокации – выяснять и последовательность расположения генов, т. е. строить генетические карты хромосом человека.
Таким образом, этот метод позволяет установить группы сцепления у человека, а используя нехватки и транслокации – выяснять и последовательность расположения генов, т. е. строить генетические карты хромосом человека.
 ДЕРМАТОГЛИФИЧЕСКИЙ АНАЛИЗ Дерматоглифический анализ это изучение папиллярных узоров пальцев, ладоней и стоп. На этих участках кожи имеются крупные дермальные сосочки, а покрывающий их эпидермис образует гребни и борозды. Дерматоглифические узоры обладают высокой степенью индивидуальности и остаются неизменными в течение всей жизни, поэтому их используют для определения зиготности близнецов, для идентификации личности в криминалистике (дактилоскопия) и другие.
ДЕРМАТОГЛИФИЧЕСКИЙ АНАЛИЗ Дерматоглифический анализ это изучение папиллярных узоров пальцев, ладоней и стоп. На этих участках кожи имеются крупные дермальные сосочки, а покрывающий их эпидермис образует гребни и борозды. Дерматоглифические узоры обладают высокой степенью индивидуальности и остаются неизменными в течение всей жизни, поэтому их используют для определения зиготности близнецов, для идентификации личности в криминалистике (дактилоскопия) и другие.
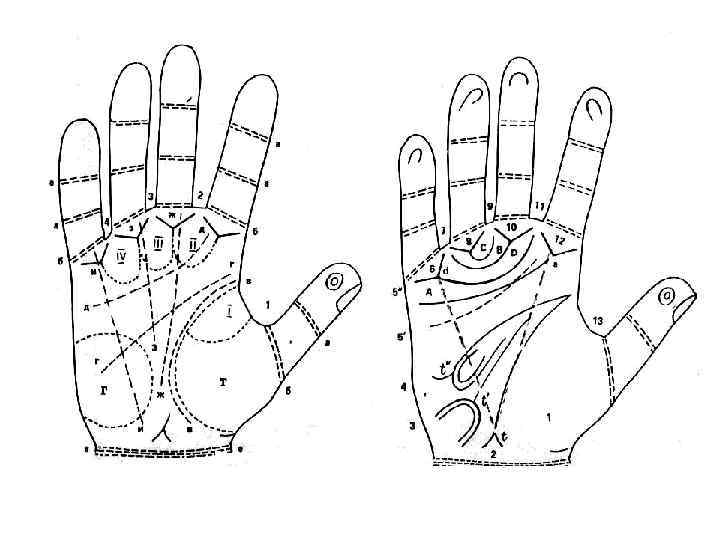
 • На пальцевых подушечках имеются узоры трёх типов: дуги, петли, завитки. • Для большинства узоров характерна дельта (трирадиус) – место схождения трех разнонаправленных папиллярных линий. 1 - дуга, 2 - петля, 3 -завиток, 4 -центр узора, 5 -дельта
• На пальцевых подушечках имеются узоры трёх типов: дуги, петли, завитки. • Для большинства узоров характерна дельта (трирадиус) – место схождения трех разнонаправленных папиллярных линий. 1 - дуга, 2 - петля, 3 -завиток, 4 -центр узора, 5 -дельта
 • В межпальцевых промежутках имеются трирадиусы (a, b, c, d), а вблизи браслетной складки расположен главный ладонный трирадиус t. • Если соединить трирадиусы a, d и t, то получим главный ладонный угол atd, который в норме не превышает 570. • На ладони различают три главные флексорные (сгибательные) борозды: борозда большого пальца, косая и поперечная. Иногда косая борозда сливается с поперечной в одну четырёхпальцевую борозду (ЧПБ). Частота её встречаемости в норме не превышает 5%.
• В межпальцевых промежутках имеются трирадиусы (a, b, c, d), а вблизи браслетной складки расположен главный ладонный трирадиус t. • Если соединить трирадиусы a, d и t, то получим главный ладонный угол atd, который в норме не превышает 570. • На ладони различают три главные флексорные (сгибательные) борозды: борозда большого пальца, косая и поперечная. Иногда косая борозда сливается с поперечной в одну четырёхпальцевую борозду (ЧПБ). Частота её встречаемости в норме не превышает 5%.
 • Сочетание радиальные петель на 4 и 5 пальцах, ЧПБ и главного ладонного угла 600 -860 даёт основание подозревать наследственное происхождение заболевания. • Трудности использования дерматоглифического анализа в медицине заключаются в отсутствии специфических изменений дерматоглифики для подавляющего большинства наследственных заболеваний.
• Сочетание радиальные петель на 4 и 5 пальцах, ЧПБ и главного ладонного угла 600 -860 даёт основание подозревать наследственное происхождение заболевания. • Трудности использования дерматоглифического анализа в медицине заключаются в отсутствии специфических изменений дерматоглифики для подавляющего большинства наследственных заболеваний.
 МЕТОДЫ ПРЕНАТАЛЬНОЙ ДИАГНОСТИКИ НАСЛЕДСТВЕННОЙ БОЛЕЗНИ • Пренатальная диагностика связана с решением ряда биологических и этических проблем до рождения ребёнка, так как при этом речь идёт не об излечении болезни, а о предупреждении рождения ребёнка с патологией, не поддающейся лечению (обычно путём прерывания беременности с согласия женщины). • На современном уровне развития пренатальной диагностики можно установить диагноз всех хромосомных болезней, большинства врождённых пороков развития, энзимопатий, при которых известен биохимический дефект.
МЕТОДЫ ПРЕНАТАЛЬНОЙ ДИАГНОСТИКИ НАСЛЕДСТВЕННОЙ БОЛЕЗНИ • Пренатальная диагностика связана с решением ряда биологических и этических проблем до рождения ребёнка, так как при этом речь идёт не об излечении болезни, а о предупреждении рождения ребёнка с патологией, не поддающейся лечению (обычно путём прерывания беременности с согласия женщины). • На современном уровне развития пренатальной диагностики можно установить диагноз всех хромосомных болезней, большинства врождённых пороков развития, энзимопатий, при которых известен биохимический дефект.
 Показания для пренатальной диагностики: • наличие в семье точно установленного наследственного заболевания • возраст матери старше 37 лет • носительство матерью гена Х-сцепленного рецессивного заболевания • наличие в анамнезе у беременных спонтанных абортов в ранние сроки беременности, мертворождений неясного генеза, детей с множественными пороками развития и с хромосомной патологией • наличие структурных перестроек хромосом (особенно транслокаций и инверсий) у одного из родителей • гетерозиготность обоих родителей по одной паре аллелей при патологии с аутосомно-рецессивным типом наследования • беременные из зоны повышенного радиационного фона
Показания для пренатальной диагностики: • наличие в семье точно установленного наследственного заболевания • возраст матери старше 37 лет • носительство матерью гена Х-сцепленного рецессивного заболевания • наличие в анамнезе у беременных спонтанных абортов в ранние сроки беременности, мертворождений неясного генеза, детей с множественными пороками развития и с хромосомной патологией • наличие структурных перестроек хромосом (особенно транслокаций и инверсий) у одного из родителей • гетерозиготность обоих родителей по одной паре аллелей при патологии с аутосомно-рецессивным типом наследования • беременные из зоны повышенного радиационного фона
 • • В настоящее время применяют непрямые и прямые методы пренатальной диагностики. При непрямых методах исследуют беременную (акушерско-гинекологические методы). При прямых методах исследуют плод. К прямым неинвазивным методам (без хирургического вмешательства) относится ультрасонография. К прямым инвазивным (с нарушением целостности ткани) – хорионбиопсия, амницентез и фетоскопия.
• • В настоящее время применяют непрямые и прямые методы пренатальной диагностики. При непрямых методах исследуют беременную (акушерско-гинекологические методы). При прямых методах исследуют плод. К прямым неинвазивным методам (без хирургического вмешательства) относится ультрасонография. К прямым инвазивным (с нарушением целостности ткани) – хорионбиопсия, амницентез и фетоскопия.
 Ультрасонография (эхография) • Это использование ультразвука для получения изображения плода и его оболочек. • На 12 -20 неделе беременности уже возможна диагностика близнецовой беременности, локализации плаценты, анэнцефалии, дефектов костной системы, закрытие невральной трубки, атрезии желудочно-кишечного тракта.
Ультрасонография (эхография) • Это использование ультразвука для получения изображения плода и его оболочек. • На 12 -20 неделе беременности уже возможна диагностика близнецовой беременности, локализации плаценты, анэнцефалии, дефектов костной системы, закрытие невральной трубки, атрезии желудочно-кишечного тракта.
 Хорионбиопсия • Это - взятие эпителия ворсинок хориона для исследования – проводится трансцервикально (через канал шейки матки) под контролем ультрасонографии между 8 и 10 неделями беременности. • Полученную ткань используют для цитогенетических и биохимических исследований и анализа ДНК. • С помощью этого метода можно выявлять все виды мутаций (генные, хромосомные и геномные).
Хорионбиопсия • Это - взятие эпителия ворсинок хориона для исследования – проводится трансцервикально (через канал шейки матки) под контролем ультрасонографии между 8 и 10 неделями беременности. • Полученную ткань используют для цитогенетических и биохимических исследований и анализа ДНК. • С помощью этого метода можно выявлять все виды мутаций (генные, хромосомные и геномные).
 Амниоцентез • Это - получение амниотической жидкости и клеток плода для последующего анализа. • Пункцию проводят в начале второго триместра беременности (15 -17 недель) через брюшину в амбулаторных условиях под контролем ультразвукового обследования. • Жидкость используют для биохимических исследований (выявляют генные мутации), а клетки – для анализа ДНК (выявляют генные мутации), цитогенетического анализа и выявления Х и Ухроматина (диагностируют геномные и хромосомные мутации). • Осложнения при этом методе исследования не превышают 1%.
Амниоцентез • Это - получение амниотической жидкости и клеток плода для последующего анализа. • Пункцию проводят в начале второго триместра беременности (15 -17 недель) через брюшину в амбулаторных условиях под контролем ультразвукового обследования. • Жидкость используют для биохимических исследований (выявляют генные мутации), а клетки – для анализа ДНК (выявляют генные мутации), цитогенетического анализа и выявления Х и Ухроматина (диагностируют геномные и хромосомные мутации). • Осложнения при этом методе исследования не превышают 1%.
 Фетоскопия • Это – осмотр плода фиброоптическим эндоскопом, введенным в амниотическую полость через брюшную стенку матки. • Метод позволяет смотреть плод, пуповину, плаценту и произвести биопсию. • Фетоскопия сопровождается высоким риском прерывания беременности и технически сложна и поэтому имеет ограниченное применение.
Фетоскопия • Это – осмотр плода фиброоптическим эндоскопом, введенным в амниотическую полость через брюшную стенку матки. • Метод позволяет смотреть плод, пуповину, плаценту и произвести биопсию. • Фетоскопия сопровождается высоким риском прерывания беременности и технически сложна и поэтому имеет ограниченное применение.
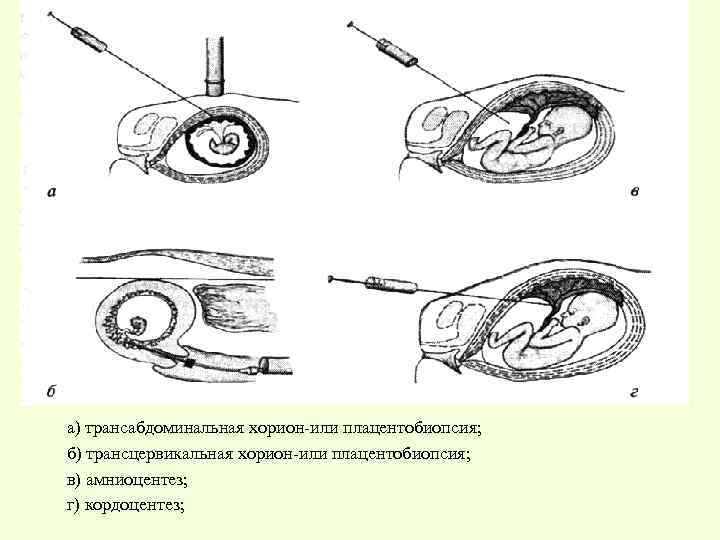 а) трансабдоминальная хорион-или плацентобиопсия; б) трансцервикальная хорион-или плацентобиопсия; в) амниоцентез; г) кордоцентез;
а) трансабдоминальная хорион-или плацентобиопсия; б) трансцервикальная хорион-или плацентобиопсия; в) амниоцентез; г) кордоцентез;
 Вопросы лекционного рейтинга 1. Каково значение медицинской генетики для врача? 2. Каковы особенности человеке как объекта генетических исследований? 3. Перечислите основные методы генетики человека. 4. Перечислите методы пренатальной диагностики наследственных болезней.
Вопросы лекционного рейтинга 1. Каково значение медицинской генетики для врача? 2. Каковы особенности человеке как объекта генетических исследований? 3. Перечислите основные методы генетики человека. 4. Перечислите методы пренатальной диагностики наследственных болезней.


