
Медь Сидорова Алина Климачева Вика 11 б класс

История открытия Эпоха открытия и применения меди — это примерно VI– IV тысячелетие до нашей эры, обширный период, который археологи и историки считают промежуточным звеном между «каменным веком» и «бронзовым» . Латинское название меди Cuprum (древн. Aes cuprium, Aes cyprium) произошло от названия острова Кипр, где уже в III в. до н. э. существовали медные рудники и производилась выплавка меди.

Нахождение в природе Малахит (Cu. OH)2 CO 3 Куприт Cu 2 O, Халькозин Cu 2 s Халькопирит Fe. Cu. S 2 Ковеллин Cu. S
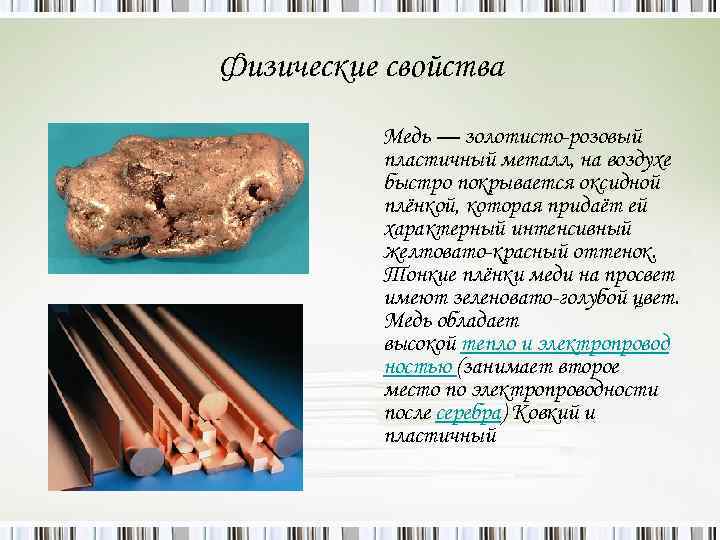
Физические свойства Медь — золотисто-розовый пластичный металл, на воздухе быстро покрывается оксидной плёнкой, которая придаёт ей характерный интенсивный желтовато-красный оттенок. Тонкие плёнки меди на просвет имеют зеленовато-голубой цвет. Медь обладает высокой тепло и электропровод ностью (занимает второе место по электропроводности после серебра) Ковкий и пластичный

Строение Атомные орбитали: 1 s 2; 2 p 6; 3 s 2; 3 p 6; 3 d 10; 4 s 1 у атома меди на 3 d-подуровне 10 электронов, а на 4 sподуровне только один

Химические свойства Ш В сухом воздухе медь практически не окисляется. Медь не реагирует с водородом, азотом, углеродом и кремнием, водой и является довольно инертным металлом. Ш Взаимодействие с неметаллами ь ь ь С кислородом в зависимости от температуры взаимодействия медь образует два оксида: при 400– 500°С образуется оксид двухвалентной меди: 2 Cu + O 2 = 2 Cu. O; при температуре выше 1000°С получается оксид меди (I): 4 Cu + O 2 = 2 Cu 2 O. Аналогично реагирует с серой: при 400°С образуется сульфид меди (II): Cu + S = Cu. S; при температуры выше 400°С получается сульфид меди (I): 2 Cu + S = Cu 2 S.

Ш При нагревании с фтором, хлором, бромом образуются галогениды меди (II): ь Cu + Br 2 = Cu. Br 2; с йодом – образуется йодид меди (I): ь 2 Cu + I 2 = 2 Cu. I. Ш Взаимодействие с кислотами ь В электрохимическом ряду напряжений металлов медь расположена после водорода, поэтому она не взаимодействует с растворами разбавленной соляной и серной кислот и щелочей. ь Растворяется в разбавленной азотной кислоте с образованием нитрата меди (II) и оксида азота (II): 3 Cu + 8 HNO 3 = 3 Cu(NO 3)2 + 2 NO + 4 H 2 O. ь Реагирует с концентрированными растворами серной и азотной кислот с образованием солей меди (II) и продуктов восстановления кислот: Cu + 2 H 2 SO 4 = Cu. SO 4 + SO 2 + 2 H 2 O; Cu + 4 HNO 3 = Cu(NO 3)2 + 2 NO 2 + 2 H 2 O.

ь С концентрированной соляной кислотой медь реагирует с образованием трихлорокупрата (II) водорода: Cu + 3 HCl = H[Cu. Cl 3] + H 2. Ш Взаимодействие с аммиаком Медь растворяется в водном растворе аммиака в присутствии кислорода воздуха с образованием гидроксида тетраамминмеди (II): 2 Cu + 8 NH 3 + 2 H 2 O + O 2 = 2[Cu(NH 3)4](OH)2. Ш Восстановительные свойства Медь окисляется оксидом азота (IV) и хлоридом железа (III): 2 Cu + NO 2 = Cu 2 O + NO; Cu + 2 Fe. Cl 3 = Cu. Cl 2 + 2 Fe. Cl 2. Ш Вытесняет металлы, стоящие правее в ряду напряжений, из растворов их солей Cu+Hg(NO 3)2=Cu(NO 3)2=Hg

Соединения Ш Cu 2 O. В лаборатории этот оксид удобно получать восстановлением щелочного раствора соли меди(II) глюкозой, гидразином или гидроксиламином: 2 Cu. SO 4 + 2 NH 2 OH + 4 Na. OH = Cu 2 O + N 2 + 2 Na 2 SO 4 + 5 H 2 O Ш Оксид Cu 2 O заметно взаимодействует со щелочами. При этом образуется комплекс: Cu 2 O + 2 Na. OH + H 2 O=2 Na[Cu(OH)2] Ш С кислотами: Cu 2 O+H 2 SO 4=Cu. So 4+Cu+H 2 O Ш Для получения оксида меди(II) Cu. O лучше всего использовать разложение нитрата или основного карбоната меди(II): 2 Cu(NO 3)2 = 2 Cu. O + 4 NO 2 + O 2 (Cu. OH)2 CO 3 = 2 Cu. O + CO 2 + H 2 O

ШОксид меди(II) реагирует с кислотами с образованием соответствующих солей меди(II) и воды: Cu. O + 2 HNO 3 → Cu(NO 3)2 + H 2 O. Ш При сплавлении Cu. O со щелочами образуются купраты: Cu. O + 2 KOH → K 2 Cu. O 2 + H 2 O. ШПри нагревании до 1100 °C разлагается: 4 Cu. O → 2 Cu 2 O + O 2↑. Аналитическая химия меди Ионы меди окрашивают пламя в зелёный цвет Медь можно обнаружить в растворе по зелёно-голубой окраске пламени.

Применение