Медь, серебро.ppt
- Количество слайдов: 48

Медь, серебро и их соединения
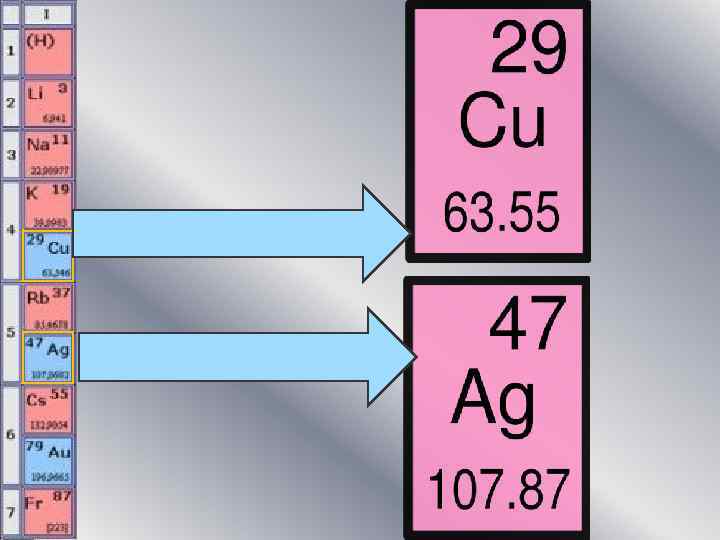
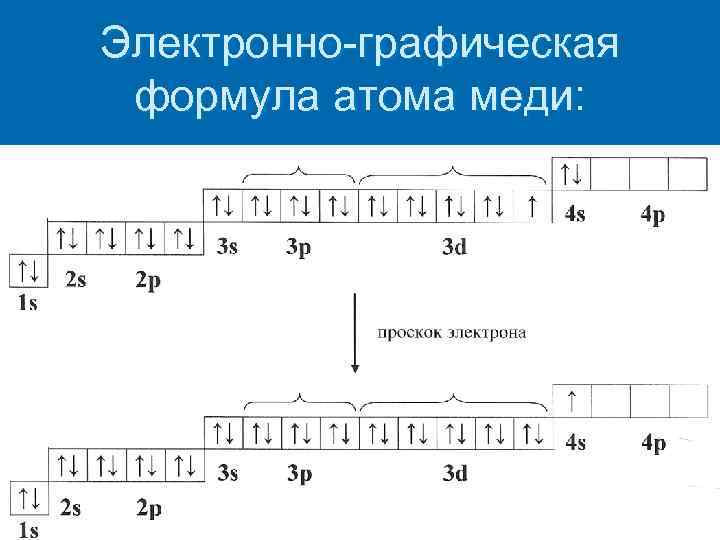
Электронно-графическая формула атома меди:
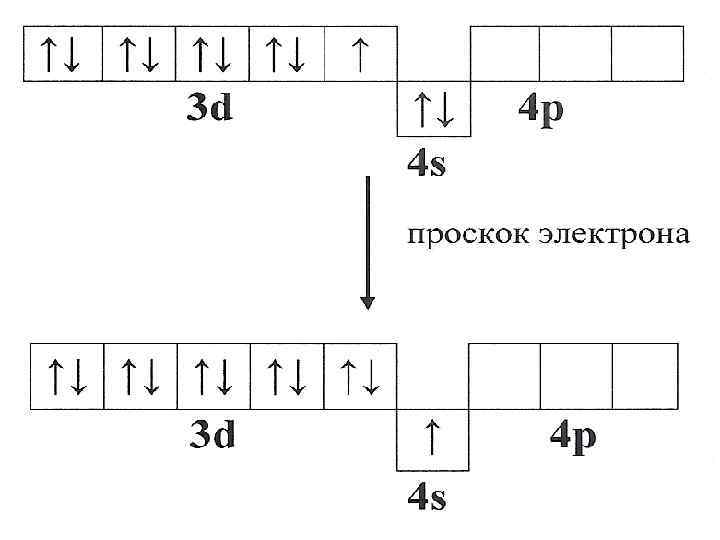

Электронно-графическая формула атома серебра: Элементы d-семейства

Cu 0 – 1 e → Cu+ Cu 0 – 2 e → Cu 2+ Степени окисления 0, +1, +2. Валентность I, II Ag 0 – 1 e → Ag+ Степени окисления 0, +1. Валентность I

Физические свойства


Металл красного цвета, очень ковкий и пластичный. Обладает высокой тепло- и электропроводностью (второе место после серебра)


Блестящий, серебристо-белый, мягкий и пластичный металл. Самый электропроводный среди всех металлов.

Нахождение в природе.

Ковеллин (Cu. S)

Халькозин (медный блеск) Cu 2 S

Халькопирит (Fe. Cu. S 2)

Малахит (Cu. OH)2 CO 3

Аргентит (серебряный блеск) Ag 2 S

Способы получения: 2 Cu. S + 3 O 2 → 2 Cu. O + 2 SO 2 Cu. O + C → Cu + CO Ag 2 S + O 2 → Ag + SO 2
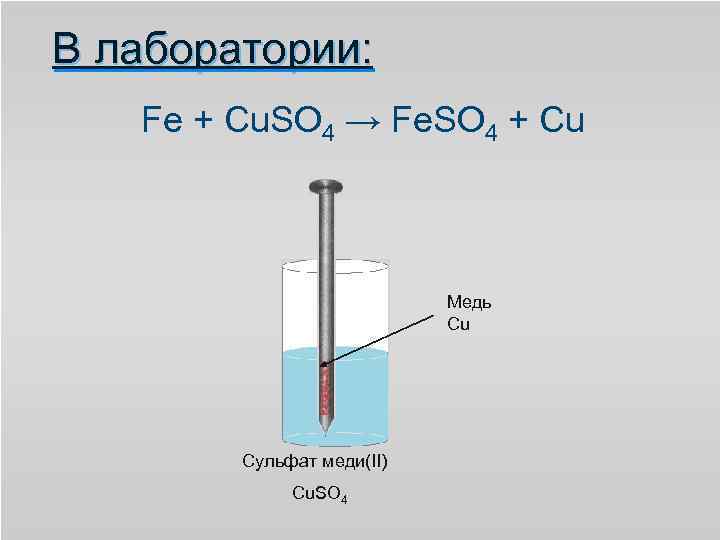
В лаборатории: Fe + Cu. SO 4 → Fe. SO 4 + Cu Медь Cu Сульфат меди(II) Cu. SO 4

Химические свойства

Взаимодействие с простыми веществами: Cu + Cl 2 → Cu. Cl 2 Cu + S → Cu. S 2 Cu + S → Cu 2 S 2 Cu + O 2 → 2 Cu. O 4 Cu + O 2 → 2 Cu 2 O (при 400°С) (при t > 400°С) (t=400 - 500°C) (t >1000°C)

Взаимодействие с кислотами: Cu + HCl ≠ Cu + H 2 SO 4(разб. ) ≠ Cu + 2 H 2 SO 4(конц. ) → Сu. SO 4 + SO 2↑ + 2 H 2 O

Взаимодействие с кислотами: 3 Cu + 8 HNO 3(разб. ) → 3 Сu(NO 3)2 + 2 NO↑ + 4 H 2 O Cu + 4 HNO 3(конц. ) → Сu(NO 3)2 + 2 NO 2↑ + 2 H 2 O

Взаимодействие меди с концентрированной азотной кислотой.

Закончите уравнения реакций: Ag + Cl 2 → Ag + S → Ag + HCl → Ag + H 2 SO 4(разб. ) → Ag + H 2 SO 4(конц. ) → Ag + HNO 3(разб. ) → Ag + HNO 3(конц. ) →

2 Cu + H 2 O + CO 2 + O 2 → (Cu. OH)2 CO 3

4 Ag + 2 H 2 S + O 2 → 2 Ag 2 S + 2 H 2 O

Соединения меди

Оксид меди (I) Сu 2 O – твердое вещество оранжево-красного цвета Проявляет основные свойства. Гидроксид меди (I) Cu. OH неустойчив.

Оксид меди (II) Сu. O – твердое вещество черного цвета

Получение оксида меди (II): Cu(OH)2 → Cu. O + H 2 O 2 Сu(NO 3)2 → 2 Cu. O + 4 NO 2↑ + O 2↑ (Cu. OH)2 CO 3 → 2 Cu. O + CO 2↑ + H 2 O

Оксид меди (II) проявляет основные свойства: Cu. O + 2 HNO 3 → → Cu(NO 3)2 + H 2 O

Гидроксид меди (II). Cu. O + H 2 O ≠ Cu. SO 4 + 2 Na. OH → → Cu(OH)2↓ + Na 2 SO 4 Cu(OH)2 + 2 HNO 3 → → Cu(NO 3)2 + 2 H 2 O

Окислительные свойства оксида и гидроксида меди (II): Cu. O + H 2 → Cu + H 2 O 2 Cu(OH)2 + CH 3 COH → → Cu 2 O↓ + CH 3 COOH + 2 H 2 O

Ø Кристаллогидрат Сu. SO 4· 5 H 2 O Ø Безводный Сu. SO 4

Гидролиз солей меди (II): Cu. SO 4 + 2 H 2 O ↔ H 2 SO 4 + Cu(OH)2↓ Cu 2+ + SO 42 - + 2 H 2 O ↔ 2 H+ + SO 42 - + Cu(OH)2↓ Cu 2+ + 2 H 2 O ↔ 2 H+ + Cu(OH)2↓ среда кислая

Качественные реакции на катионы Cu 2+: Cu. SO 4 + 4 NH 4 OH → [Cu(NH 3)4]SO 4 + 4 H 2 O синий раствор сульфат тетраамминмеди (II) 2 Cu. SO 4 + K 4[Fe(CN)6] → Cu 2[Fe(CN)6]↓ + 2 K 2 SO 4 красно-бурый осадок гексацианоферрат меди (II)

Соединения серебра

Оксид серебра (I) Ag 2 O – темно-коричневый порошок. Обладает основными свойствами. 2 Ag. NO 3 + 2 Na. OH → → Ag 2 O + 2 Na. NO 3 + H 2 O

Растворяется в гидроксиде аммония: Ag 2 O + 4 NH 4 OH → → 2[Ag(NH 3)2]OH + 3 H 2 O Используется для реакции «серебряного зеркала» .

Качественные реакции на катион Ag+: Ag. NO 3 + HCl → Ag. Cl↓ + HNO 3 белый творожистый осадок Растворяется в избытке аммиака: Ag. Cl + 2 NH 4 OH → → [Ag(NH 3)2]Cl + 2 H 2 O хлорид диамминсеребра (I)

Качественные реакции на катион Ag+: Ag. NO 3 + KI → Ag. I↓ + KNO 3 светло-желтый осадок

Качественные реакции на катион Ag+: 2 Ag. NO 3 + Na 2 S 2 O 3 → Ag 2 S 2 O 3↓ + 2 Na. NO 3 белый осадок Ag 2 S 2 O 3 + H 2 O → Ag 2 S↓ + H 2 SO 4 черный осадок

Качественные реакции на катион Ag+: 2 Ag. NO 3 + K 2 Cr. O 4 → Ag 2 Cr. O 4↓ + 2 KNO 3 кирпично-красный осадок 2 Ag. NO 3 + 2 KOH → Ag 2 O↓ + H 2 O + 2 KNO 3 грязно-коричневый осадок

Роль меди в организме: Содержание в организме – 150 мг. Входит в состав: Ø Дыхательных ферментов; Ø Белков, участвующих в переносе кислорода кровью. Недостаток – болезнь Менкеса; Избыток – болезнь Вильсона-Коновалова.

Применение в медицине и фармации: Сульфат меди (II) Cu. SO 4 : Ø Антисептическое, вяжущее средство. Ø Используется при коньюнктивитах и заболеваниях органов мочеполовой системы.

Применение в медицине и фармации: Нитрат серебра (ляпис) Ag. NO 3 : Ø Вяжущее и противовоспалительное действие; Ø Прижигающее действие; Протаргол – коллоидный раствор протеината серебра: Ø Антисептическое и противовоспалительное средство; Ø Орошают слизистые оболочки глаз, органов дыхательной и мочеполовой системы.

Медь, серебро.ppt